|
Масса 1 мл, г
|
Поправка
|
|
0,60-1,03
|
|
1,04-1,72
|
0,0010
|
|
1,73-2,00
|
0,0009
|
Плотность жидкости может быть приближенно
(с точностью до 0,01) определена с помощью ареометра, который представляет собой
стеклянный тонкостенный цилиндрический сосуд, расширяющийся внизу и имеющий на
конце стеклянный резервуар, заполненный дробью, реже ртутью. В верхней части
ареометра имеется шкала с делениями, соответствующими относительной плотности
жидкости, и указанием температуры, при которой следует производить определение.
Имеются ареометры для жидкостей легче и тяжелее воды, для серной кислоты, едких
щелочей, а также ряд специальных ареометров для измерения плотности спирта
(спиртометр), молока (лактометр) и др. Для повышения точности измерения
промышленность выпускает наборы ареометров, шкалы которых охватывают
определенный диапазон плотностей.
Практическая часть
. Определение плотности жидкости
при помощи пикнометра
Чистый сухой пикнометр взвесить на
аналитических весах с точностью до 0,0002 г. Затем заполнить его
дистиллированной водой немного выше метки, закрыть пробкой и поместить в
термостат. После 20-минутной выдержки в термостате при температуре (20±0,1)0С
уровень воды в пикнометре быстро довести до метки, отбирая излишек воды
пипеткой, капилляром или свернутой полоской чистой неволокнистой фильтровальной
бумаги. Пикнометр снова закрыть пробкой, термостатировать еще 10 мин, проверить
соответствие уровня жидкости метке, протереть снаружи досуха чистой мягкой тканью
или фильтровальной бумагой и снова взвесить. После этого пикнометр освободить
от воды, споласнуть последовательно спиртом и эфиром, удалить остатки эфира
продуванием воздуха, заполнить пикнометр испытуемой жидкостью и провести те же
операции, что и с дистиллированной водой.
. Определение плотности жидкости
ареометром
Испытуемую жидкость поместить в цилиндр
ёмкостью не менее 0,5 л и при температуре жидкости 200С осторожно
опустить в неё чистый сухой ареометр. Погружать ареометр в жидкость осторожно,
не выпуская его из рук до тех пор, пока не станет очевидным, что он плавает.
При этом ареометр должен находиться в центре цилиндра и ни в коем случае не
касаться стенок и дна сосуда. Отсчет производят по делениям шкалы ареометра
через 3-4 мин после погружения по нижнему мениску жидкости. После определения
ареометр вымыть, вытереть и убрать в специальный футляр.
Результаты
Показания ареометра: 0,998
Значения, полученные при помощи
пикнометров:
m = 17,923 г.1 = 48,127 г.
m² = 48,927 г.
Расчёт:
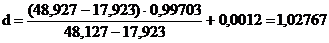
С учётом поправки: 1,02767 + 0,0010 = 1,02867 г./мл.
РН-метрия
Теоретическая часть
Концентрацию водородных ионов принято выражать при помощи
водородного показателя pH, представляющего собой десятичный логарифм [H+], взятый с обратным
знаком:
pH = − lg[H+]
pH нейтральных растворов равен 7, кислых −
меньше 7 и щелочных − больше 7. Большинство природных вод почти
нейтрально (pH = 6,8-7,3).
Сохранение рН воды близким к нейтральному необходимо для
нормального протекания некоторых процессов ее очистки и для использования ее в
быту и промышленности.
Изменение рН воды свидетельствует о загрязнении ее продуктам
распада органических соединений, стоками химических заводов и другими
веществами.
Определяется эта величина потенциометрическим методом с
использованием pH-метра со стеклянным электродом.
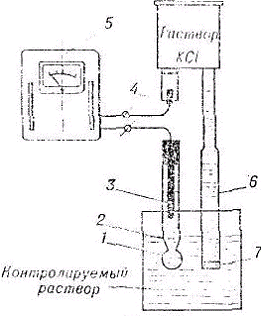
Рис. 1. Электродная схема pH-метра.
Практическая часть
Перед началом измерений прибор включить в сеть при помощи
тумблера и дать нагреться в течение 20 мин. При этом зажигается сигнальная
лампа.
Электроды перед погружением в раствор тщательно промыть
дистиллированной водой и просушить фильтровальной бумагой. Прежде чем
приступить к определению рН исследуемого раствора, проверить правильность
настройки рН-метра по раствору с известным рН. (Для этой цели используют
буферные растворы или 0,1 н. раствор соляной кислоты с рН == 1,1 при t = 20−30°С).
Вначале измерение провести по шкале от 2 до 14, затем
переключить с помощью потенциометра ручной температурной компенсации на более
узкий интервал рН и определить рН с точностью 0,05.
Результат: pH = 7,55
Определение
кислотности воды
Теоретическая часть
Кислотностью воды называется содержание в воде веществ,
вступающих в реакцию с сильными щелочами (едким натром, едким кали). Объем 0,1
н. раствора щелочи, израсходованный на титрование таких веществ, соответствует
общей кислотности воды.
В природных водах кислотность в большинстве случаев зависит
только от содержания свободной растворенной углекислоты.
Часть кислотности, обусловленная присутствием гуминовых и
других слабых органических кислот, растворенных в воде, называется естественной
кислотностью воды; рН такой воды обычно не бывает ниже 4,5. Промышленные
сточные воды могут содержать сильные кислоты или соли сильных кислот и слабых
оснований (чаще всего железа и алюминия), подвергающиеся гидролизу в результате
чего кислотность увеличивается. рН воды обычно в этих случаях снижается
значительно ниже 4,5.
Та часть общей кислотности, при которой снижается рН воды до
4,5 и ниже, называется свободной кислотностью воды.
Кислотность воды определяют титрованием раствором сильного
основания. Количество 0,1 н. раствора сильного основания, при израсходовании
которого рН раствора достигает значения 4,5, соответствует свободной
кислотности, а при израсходовании которого рН раствора достигает значения 8,3 -
соответствует общей кислотности. Если рН исследуемой воды больше 8,3,
то ее кислотность равна нулю.
Практическая часть
Предварительно определяют свободную кислоту, измеряя рН. Если
предварительное определение показало наличие свободной кислоты, то проводят
количественное определение свободной и общей кислотности.
Определение свободной кислотности
К 100 мл исследуемой воды добавить 2 капли раствора
метилового оранжевого и титровать 0,1 н. раствором едкого натра до появления
желтой окраски.
Вычисления проводить по формуле (1).
Определение общей кислотности
К 100 мл исследуемой воды прибавить 3 капли раствора
фенолфталеина и титровать 0,1 н раствором едкого натра до появления розовой
окраски.
Результаты:
Ксвоб.= 0,3
Кобщ. = 0,3
Определение
щелочности воды
Под щелочностью природной воды понимается ее способность
связывать кислоты. Щелочность обуславливается присутствием в воде бикарбонатов,
карбонатов и гидроокисей. Отчасти влияют на величины щелочности такие вещества,
как фосфаты, силикаты, бораты. Большие величины дают сточные воды, содержащие
известь и гипохлорит кальция.
Общая щелочность воды (Що, мг-экв/л) - характеризует
суммарную концентрацию растворенных гидроксидов и анионов слабых кислот НСО3-
и СО32 - за вычетом концентрации ионов водорода.
Результаты титрования по фенолфталеину и метилоранжу позволяют рассчитать
показатель щелочности воды, который численно равен количеству эквивалентов
кислоты, израсходованной на титрование пробы объемом 1 л. При этом потребление
кислоты при титровании по фенолфталеину характеризует свободную щелочность, а
по метилоранжу - общую щелочность, которая измеряется в ммоль/л.
Карбонаты и гидрокарбонаты представляют собой компоненты,
определяющие природную щелочность воды. Их содержание в воде обусловлено
процессами растворения атмосферной СО2, взаимодействия воды с
находящимися в прилегающих грунтах известняками и, конечно, протекающими в воде
жизненными процессами дыхания всех водных организмов.
Определение карбонат- и гидрокарбонат-анионов является
титриметрическим и основано на их реакции с водородными ионами в присутствии
фенолфталеина (при определении карбонат-анионов) или метилового оранжевого (при
определении гидрокарбонат-анионов) в качестве индикаторов.
Практическая часть
100 мл исследуемой воды помещаем в коническую колбу,
прибавляем 3-4 капли метилоранжа и титруем 0,1 н раствором соляной кислоты на
белом фоне до перехода окраски из желтого в слабо-розовый (от одной капли
соляной кислоты). Для того, чтобы точно уловить переход окраски, ставим рядом
контрольную колбу с той же водой и 3-4 каплями метилоранжа. Но изменение
окраски происходит несколько раньше полного перехода всех бикарбонатов в
хлористые соли за счет свободной углекислоты, которая влияет на метиловый
оранжевый индикатор. Влияние это будет тем больше, чем выше щелочность воды.
мл исследуемой воды помещают в коническую колбу, прибавляют
3-4 капли фенолфталеина и титруют 0,1 н раствором соляной кислоты на белом фоне
до полного обесцвечивания.
Свободную и общую щелочность определяют по формулам:
Що=Vмо*k*0.1*1000/V
Щс=Vф*k*0,1*1000/V
где Vмо и Vф - объем 0,1н. раствора соляной кислоты,
израсходованный на титрование по метиловому оранжевому или по фенолфталеину,
мл;
k - поправочный коэффициент для приведения концентрации
соляной кислоты точно к 0,1 н.;
V - объем пробы, взятой на титрование, мл.
Результаты:
Що=0,8*1*0.1*1000/100 = 0,8
Щс=0*k*0,1*1000/V = 0.
Определение
жёсткости
Теоретическая часть
Большое влияние на качество воды оказывают содержащиеся в ней
соли кальция, магния и железа(II), которые и обусловливают жесткость воды,
которая бывает двух видов: временная и постоянная.
Временная или карбонатная жесткость воды (ЖК) обусловлена
содержанием в воде гидрокарбонатов кальция, магния и железа.
Постоянная или некарбонатная жесткость воды (ЖНК) обусловлена
присутствием в воде сульфатов, хлоридов, нитратов и других растворимых солей
кальция и магния.
Общая жесткость воды (ЖО) равна сумме карбонатной и
некарбо-натной жесткостей:
По величине жесткости природную воду делят на:
o очень мягкую - до 1,5
ммоль/л,
o мягкую - от 1,5 до 4
ммоль/л,
o средней жесткости - от 4
до 8 ммоль/л,
o жесткую - от 8 до 12
ммоль/л,
o очень жесткую - свыше 12
ммоль/л.
Общую жесткость воды (ЖО) определяют комплексонометрическим
методом.
Для определения общей жесткости воду титруют раствором
трилона Б в присутствии индикатора (кислотный хромтемносиний или эриохромчерный
Т). В точке эквивалентности при титровании индикатор изменяет окраску розовую
(в присутствии ионов жесткости - Са2+ и Mg2+) на синюю (в отсутствии этих
ионов).
Комплексообразование ионов кальция и магния с трилоном Б
происходит в щелочной среде (рН ≈ 10), поэтому при выполнении работы
используют буферный раствор.
Буферными называют растворы, содержащие слабую кислоту и ее
соль
(CH3COOH + NaCH3COO) или слабое
основание и его соль (NH4OH + NH4Cl). Такие растворы сохраняют постоянную
концентрацию ионов водорода, или рН раствора, как при разбавлении, так и при
добавлении небольших количеств сильных кислот и или щелочей, т.е. оказывают
буферное действие.
Карбонатную жесткость(ЖК) определяют титрованием исследуемой
воды раствором соляной кислоты. При этом растворенные в воде гидрокарбонаты
количественно реагируют с соляной кислотой по уравнению:
Ме(НСО3)2 + 2НС1 = МеС12 +
2СО2 + 2Н2О
Анион НСО3¯ в воде гидролизуется:
НСО3¯ + Н2О <=>
Н2СО3 + ОН¯
Поэтому вода, содержащая гидрокарбонаты кальция и магния,
имеет щелочную реакцию среды. Добавленный к воде метиловый оранжевый окрашивает
ее в желтый цвет. При титровании исследуемой воды раствором соляной кислоты
протекает реакция нейтрализации:
ОН¯ + Н+ = Н2О
Количество ионов ОН¯ эквивалентно концентрации
ионов НСО3¯, следовательно, и концентрации
гидрокарбонатов кальция и магния.
В зависимости от конкретных условий на различных
производствах допускаемая жесткость воды может быть различной. Жесткость воды
хозяйственно-питьевых водопроводов не должна превышать 7 ммоль/л.
Для умягчения воды в промышленности и в быту используют
следующие методы: термический, реагентный и ионообменный методы.
Практическая часть
Определение общей жесткости воды
В две конические колбы влить по 100 мл воды.
Добавить к исследуемой воде 5 мл аммиачного буферного
раствора, поддерживающего рН ≈ 10 и 3-5 капель индикатора кислотного
хромтемносинего или несколько кристалликов эриохромчерного и перемешать.
Бюретку заполнить трилоном Б, предварительно промыв её этим
же раствором. Оттитровать воду раствором трилона Б до перехода розовой или
винно-красной окраски раствора в сине-сиреневый цвет.
Измерив объем трилона Б, пошедший на титрование данной порции
воды, записать результат и провести титрование во второй раз. Если результаты
совпадают (ΔV ≤ 0,1 мл), то рассчитать общую
жесткость воды. В противном случае оттитруйте еще одну пробу воды. Найти
среднее значение объема раствора трилона Б и по закону эквивалентов рассчитать
общую жесткость воды (ммоль/л):
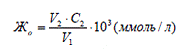
где V1 - объем анализируемой воды, мл;2
- объем раствора трилона Б, мл;
С2 - молярная концентрация эквивалента раствора
трилона Б, моль/л;
3 - коэффициент перевода моль/л в ммоль/л.
Определение карбонатной и некарбонатной жесткости воды
В две конические колбы влить по 100 мл исследуемой воды.
Добавить к 2-3 капли раствора индикатора метилового оранжевого. Оттитровать
подготовленную пробу раствором соляной кислоты известной концентрации при
постоянном перемешивании до тех пор, пока раствор не приобретет оранжевую
окраску. Записать результат. Оттитровать исследуемую воду во второй колбе. Если
результаты совпадут (ΔV ≤ 0,1 мл), то
вычислить карбонатную жесткость воды. В противном случае оттитровать еще одну
или две пробы.
Рассчитать карбонатную жесткость, используя закон
эквивалентов:
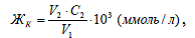
где V1 - объем анализируемой воды, мл;2
- объем раствора соляной кислоты, мл;
С2 - молярная концентрация эквивалента или
молярная
концентрация раствора, моль/л;
3 - коэффициент перевода моль/л в ммоль/л.
Некарбонатную жесткость определить по разности:
ЖНК = ЖО - ЖК
Умягчение воды методом катионирования
Из трубки с катионитом слить избыток воды. При этом следить
за тем, чтобы уровень воды в трубке был выше слоя катионита во избежание
появления воздушных пузырьков внутри катионита. Залить катионит исследуемой
водой. Медленно пропускать воду через слой катионита.
Первые 20-30 мл фильтрата отбросить. Затем отмерить 100 мл
фильтрата, перенести в коническую колбу для титрования и определить общую
жёсткость. Сравнить жёсткость воды до ее умягчения и жёсткость воды после
умягчения.
Результаты
Общая жёсткость: 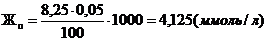
Карбонатная жёсткость: 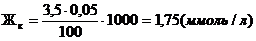
Некарбонатная жёсткость: Жн = 4,125 - 1,75 = 2,375 (ммоль/л)
Общая жёсткость после умягчения: 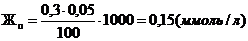
Определение
солёности
. Определение некарбонатной солености
Сущность определения сводится к замещению катионов
водородными ионами при пропускании пробы через слой катионита в Н+-форме,
устранению двуокиси углерода из пробы, пропущенной через катионит, аэроции и
титрованию известного количества пробы раствором едкого натрия.
мл пробы фильтровать со скоростью 0,1 мл/счерез слой
катионита. Первые 80 мл фильтрата отбросить, затем фильтрат собрать в сухую
колбу.
Закончив фильтрование, аэрировать полученный раствор
интенсивной струей воздуха в течение 10 мин. В колбу для титрования перенести
100 мл обработанной таким образом пробы и титровать 0,1н. раствором NaOHпо
метиловому оранжевому.
Некарбонатную соленость (х) в мг-экв/л вычислить по формуле:
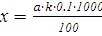 =
=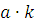 ,
,
где а - объем 0,1 н. NaOH, израсходованного на титрование,
мл;
k - поправочный коэффициент для приведения концентрации NaOH к
0,1н.
Результат: х = 8,15*1 = 8,15 (мг-экв/л)
. Определение общей солености
Общая солёность равна сумме величин некарбонатной солености и
общей щелочности (m). Этот расчет применим для вол, щёлочность которых зависит
исключительно от гидрокарбонат-, карбонат- и гидроксил- ионов. Для вод,
щелочность которых обуславливается еще и другими веществами, например фосфатами
в повышенных концентрациях и анионами слабых кислот, нахождение солёности
расчетным путем приводит к ошибке, пропорциональной концентрации этих веществ.
Вычисляем общую соленость (хо) в мг-экв/л по формуле:
хо = х+m,
где m - общая щелочность, мг-экв/л.
Результат: хо = 8,15+0,8 = 9,05 (мг-экв/л)
Определение
сульфатов в воде
Теоретическаячасть
Сульфаты встречаются во всех природных водах, чаще всего в виде
кальциевых, магниевых и натриевых солей (CaSO4, MgSO4, Na2SO4). Содержание сульфатов в
природных водах колеблется в широких пределах от единиц до десятков тысяч мг/л.
Существует несколько методов определения сульфатов в воде:
весовой, комплексонометрический (трилонометрический), колориметрический.
Комплексонометрический метод дает наиболее надежные
результаты. Сущность этого метода состоит в том, в исследуемую воду вводят ионы
Ba2+(раствор BaCl2), которые связывают ионы
SO42- в трудно растворимые
соединения, выпадающие в осадок:
Ba2+ + SO42- = BaSO4↓
Количество сульфат-ионов оценивают по разности расхода
трилона Б на взаимодействие с ионами Ba2+ до осаждения ионов SO42- и после их осаждения.
Практическая часть
Расчет проводим по формуле:
X =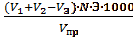 мг/л,
мг/л,
где Vпр - объем исследуемой воды (25 мл)
N - нормальностьтрилона Б
Э - миллиграмм-эквивалент иона SO42 - (48)
V1 = 2,3 мл
V2 = 0,5 мл
V3 = 1,1 мл
Результат: X = 326,4 мг/л.
Определение
химического потребления кислорода
кислотность вода
жесткость примесь
Теоретическая часть
Окисляемость воды (химическое потребление кислорода) - это
условная величина, характеризующая загрязнение воды различными легко
окисляемыми веществами, главным образом органического происхождения, а также
легко окисляющимися неорганическими примесями (H2S, Fe2+, сульфитов, нитритов и
др.).
Различают бихроматную, перманганатную и биохимическую
окисляемости.
Так как степень окисления органических веществ бихроматом в
серной кислоте близка к 100%, то величина бихроматной окисляемости (БО) служит
показателем суммарного содержания органического вещества (ОВ)
ΣОВ = 2•С = БО•12/32
Химическое потребление кислорода (ХПК) - общая концентрация
кислорода, равная количеству бихромата, потребленному растворенным и взвешенным
веществом при обработке пробы воды.
Величина ПО тоже служит для оценки содержания легкоокисляемой
органики. Перманганатный индекс воды - общая концентрация кислорода,
соответствующая количеству иона перманганата, потребляемому при обработке
данным окислителем в данных условиях конкретной пробы воды.
Сущность метода определения перманганатной окисляемости воды
заключается в использовании перманганата калия в качестве сильного окислителя
для разложения органических загрязнителей в исследуемой воде. Проба воды
кипятится с заданным, заведомо избыточным объемом KMnO4, после чего его избыток
оттитровывается щавелевой кислотой.
Реакция окисления примесей перманганатом калия проводится в
кислой среде и протекает следующим образом:
MnO4- + 8H+ +5eàMn2+ + 4H2O
В щелочной или нейтральной среде ион Mn2+ переходит в Mn4+ образуя окись марганца -
бурый осадок:
MnO4- + 2H2O +3e
à MnO2 + 4OH-
Избыток перманганата калия реагирует с вводимой в раствор
щавелевой кислотой:
2KMnO4 + 5H2C2O4
+ H2SO4à MnSO4 +
K2SO4 + 10CO2 + 8H2O
Практическая часть
В колбу поместить чистые кипелки, внести 100 мл пробы, 5 мл
разбавленной серной кислоты и 20 мл 0,01 н раствора перманганата калия. Смесь
нагревать так, чтобы она закипела через 5 мин и кипятить точно 10 мин. К
горячему раствору прибавить 20 мл 0,01 раствора щавелевой кислоты.
Обесцвеченную смесь титровать горячей (лучше при 80-90°C) 0,01 н раствором
перманганата калия до розового окрашивания. Температура смеси при титровании не
должна падать ниже 80°C. Израсходованное количество перманганата отсчитать с
точностью до 0,05 мл. Одновременно провести холостой опыт с водой для
разбавления. Если раствор при кипячении обесцветится или побуреет, определение
повторить с разбавленной пробой. Определение повторять и тогда, когда
перманганат расходуется более 60% добавленного количества, т.е. при расходе
более 12 мл. При титровании разбавленных проб не должно быть израсходовано
меньше 20% добавленного количества (4 мл).
Для холостой пробы отмерить 100 мл дистиллята и обработать ее
аналогично анализируемой пробе. Расход перманганата не должен превышать 0,2 мл.
Расчет перманганатной окисляемости провести по формуле:
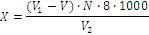
где V1 - объем 0,01 н раствора перманганата калия,
пошедший на титрование анализируемой пробы, мл;
V - объем 0,01 н раствора перманганата калия, пошедший на
титрование холостой пробы, мл.
N - нормальность раствора KMnO4
- миллиграмм-эквивалент кислорода
V2 - объем исследуемой воды, мл
Результат: Х = 3,04 мг/л.
Вывод
Сравнительная таблица показателей исследуемого образца с
нормами СанПиН
|
Показатель
|
Исслед. проба
|
ПДК
|
|
Грубодисперсные примеси, мг
|
415
|
0
|
|
Прозрачность, см
|
30
|
30
|
|
Запах, баллы
|
1
|
0
|
|
Цветность, градусы
|
25
|
20
|
|
Водородный показатель (рН)
|
7,55
|
6,5-8,5
|
|
Щёлочность общая, ммоль/л
|
0,8
|
0,5 - 6,5
|
|
Жёсткость, мг-экв/л
|
4,125
|
1,5-2
|
|
Солёность общая, мг-экв/л
|
9,05
|
7
|
|
Сульфаты, мг/л
|
326,4
|
500
|
|
ХПК, мг/л
|
3,04
|
5,0-7,0
|
Используемая
литература
1. СанПиН
2.1.4.1074-01 (с изменениями от 7 апреля 2009 г., 25 февраля 2010 г.).
3. Курс
лекций дисциплины «Химия воды» СПБГТИ(ТУ).