Расчет параметров растворов
1. Определить объем аммиака (условия нормальные), который
необходимо растворить в 249 г. воды для получения 25%-ного раствора гидроксида
аммония
Дано:
m1(Н2О) = 249 г.
w(NH4OH) = 25%
Найти:
V(NH3) - ?
Решение:
Масса
полученного раствора
mр-ра = m1(Н2О) + m(NH3)
Образование
гидроксида аммония протекает по реакции
NH3 + H2O = NH4OH
Масса
гидроксида аммония m(NH4OH) = m2(H2O) + m(NH3), где m2(H2O) - вода связанная с аммиаком.
Массовая
доля гидроксида аммония равна
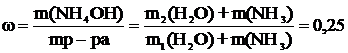
отсюда
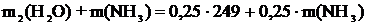
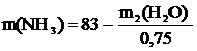
Из уравнения реакции масса воды связанной с аммиаком равна
NH3 + H2O = NH4OH
г./моль 18 г./моль
m(NH3) m2(H2O)2(H2O)
= m(NH3) ×18/17 = 1,06× m(NH3)
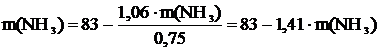
отсюда m(NH3) = 34,4 г
Поскольку при н.у. 1 моль любого газа занимает 22,4 л рассчитаем
объем газа по формуле
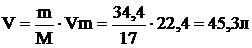
Ответ: 45,3 л
2. В 0,6 л насыщенного раствора PbSO4 содержится
0,186 г. ионов свинца (II). Вычислите произведение
растворимости этой соли
Дано:
V = 0,6
л
m(Pb2+) = 0,186 г.
Найти: ПР - ?
Решение:
Диссоциация соли описывается уравнением PbSO4 = Pb2+ + SO42-
Обозначим растворимость через s моль/л. Поскольку каждый моль
растворенного PbSO4 образует 1 моль ионов Pb2+ и 1 моль ионов SO42-,
[Pb2+] = s, а [SO42-] = s.
Для произведения растворимости имеем
ПР = [Pb2+]×[SO42-] = s×s = s2
Зная, что в насыщенном растворе содержится 0,186 г. ионов свинца (II) рассчитываем растворимость соли:
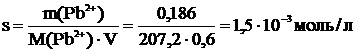
ПР = [Pb2+]×[SO42-] = s×s = s2 = (1,5×10-3)2 = 2,24×10-6
3. В 1 литре воды содержится 38 мг ионов Mg2+ и 108 мг ионов Са2+. Вычислите общую жесткость воды
Дано:
m(Mg2+) = 38 мг
m(Са2+)
= 108 мг
Найти: Ж - ?
Решение:
мг-экв/л жесткости соответствует содержанию 12,16 мг/л магния (Mg2+).
Тогда жесткость воды обусловленная присутствием ионов магния составит:
Ж(Mg2+) = 38/12,16 = 3,1 мг-экв/л
мг-экв/л жесткости соответствует содержанию 20,04 мг/л кальция (Ca2+).
Тогда жесткость воды обусловленная присутствием ионов кальция
составит:
Ж(Ca2+) = 108/20,04 = 5,4 мг-экв/л
Рассчитаем общую жесткость воды:
Жобщ = Ж(Ca2+) + Ж(Mg2+) = 3,1 + 5,4 = 8,5
мг-экв/л
4. Вычислите потенциалы электродов
а) Pt, H2/0,01н HCl; г) Pt, Н2 /раствор с рН = 3;
б) Pt, H2/0,01М HNO3; д) Pt, H2/раствор с рОН=5;
в) Pt, H2/0,01н H2SO4; e) Pt, H2/H2O
Решение:
Потенциал водородного электрода зависит от активности ионов Н+ в
растворе и давления водорода; потенциал стандартного водородного электрода (с
активностью ионов Н+ 1 моль/л и давлением водорода 101.3 кПа) принят
равным нулю.
Для определения электродного потенциала используем уравнение
Нернста.

где φо = 0В - стандартный электродный потенциал; n - число электронов,
принимающих участие в процессе; с - концентрация ионов в растворе, моль/л, R =
8,31кДж/моль - газовая постоянная, Т = 273+25 = 298К, F = 96500Кл/моль -
постоянная Фарадея.
Уравнение Нернста для водородного электрода при t = 25°С имеет вид:
φH2/2H+ = 0,059· lg [c(H+)]
а) Pt, H2/0,01н HCl
Т.к. HCl - одноосновная кислота, то Сн = См = 0,01 моль/л
тогда концентрация ионов водорода, согласно уравнению диссоциации HCl →
H+ + Cl - составит c(H+) = 0,01
моль/л.
φH2/2H+ = 0,059· lg0,01 = -0,118 В
Концентрация ионов водорода, согласно уравнению диссоциации HNO3 → H+ + NO3 - составит c(H+) = 0,01
моль/л
φH2/2H+ = 0,059· lg0,01 = -0,118 В
в) Pt, H2/0,01н H2SO4
Т.к. H2SO4 - двухосновная кислота, то См = Сн/2 = 0,005 моль/л
тогда концентрация ионов водорода, согласно уравнению диссоциации H2SO4 → 2H+ + SO42 - составит c(H+) = 0,01
моль/л.
φH2/2H+ = 0,059· lg0,01 = -0,118 В
г) Pt, Н2 /раствор с рН = 3
φH2/2H+ = 0,059· lg [c(H+)]
учитывая, что рН = - lg [c(H+)]
φH2/2H+ = - 0,059· 3 = -0,177 В
д) Pt, H2/раствор с рОН=5
φH2/2H+ = 0,059· lg [c(H+)]
учитывая, что рН = - lg [c(H+)] и рН = 14 - рОН = 9
φH2/2H+ = - 0,059·9 = -0,531 В
e) Pt, H2/H2O
Для воды рН = 7
φH2/2H+ = - 0,059·7 = -0,413 В
5. Установите термодинамическую вероятность протекания
электрохимической коррозии на поверхности стального изделия с цинковым
протектором в нейтральной водной среде (морская вода) в присутствии
растворенного кислорода. Запишите схему коррозионной гальванопары, уравнения
анодного и катодного процессов. Укажите вид и состав конечного продукта
коррозии. Можно ли использовать в качестве протектора в этом случае олово?
электрохимический аммиак растворимость
термодинамический
Решение:
При
протекторной защите стального изделия цинком в морской воде образуется
гальванопара цинк - железо в воде (среда нейтральная). В воде растворен
кислород.
Схема
гальванопары: Zn / Н2О,
О2 / Fe
Потенциалы:
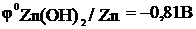 ;
; 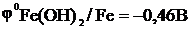
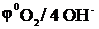 = + 0,814 В.
= + 0,814 В.
Восстановитель - Zn, окислитель - О2.
Zn (-): 2 Zn - 2ē + 2 H2O = Zn(OН)2
+ 2Н+ - процесс окисления
Fe (+): 1 О2 +
4ē + 2 H2O = 4 OH- - процесс восстановления
Zn + О2 + 4H2O = 2 Zn(OН)2
ЕДС = φк - φа = -0,46 - (-0,81) = 0,35 В
ΔG = - z×F×ЕДС = -2×96500×0,35 = -67,55 кДж/моль
F -
постоянная Фарадея (96500 Кл/моль).
ΔG>0, процесс термодинамически возможен.
Рассмотрим
гальванопару Fe-Sn
Потенциалы:
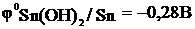 ;
; 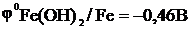
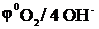 = + 0,814 В.
= + 0,814 В.
Восстановитель - Fe, окислитель - О2.
Схема гальванопары: Fe / Н2О, О2 / Sn
Fe (-): 2 Fe - 2ē + 2 H2O = Fe(OН)2
+ 2Н+ - процесс окисления
Sn (+): 1 О2 +
4ē + 2 H2O = 4 OH- - процесс восстановления
Fe + О2 + 4H2O = 2 Fe(OН)2
Таким образом, видно, что разрушению в данной гальванопаре
подвергается железо, т.е. использовать олово в качестве протекторной защиты
стального изделия невозможно.
. Составьте молекулярные уравнения реакций, которые выражаются
ионно-молекулярными уравнениями:
a) Fe(OH)3 + 3Н+ = Fe3+ + 3Н2О; б) Cd2++ 2ОН- = Cd(OH)2; в) Н+ + NO2- = HNO2.
Решение:
a) Fe(OH)3 + 3Н+ = Fe3+ + 3Н2О
Fe(OH)3 + 3НCl = FeCl3 + 3Н2О(OH)3 + 3Н+ + 3Cl- = Fe3+ + 3Cl- + 3Н2О
Fe(OH)3 + 3Н+ = Fe3+ + 3Н2О
б) Cd2++ 2ОН- = Cd(OH)2;
CdCl2 + 2NaOH = Cd(OH)2 + 2NaCl2+
+ 2Cl- + 2Na+ + 2OH- = Cd(OH)2 +
2Na+ + 2Cl-2++ 2ОН- = Cd(OH)2
в) Н+ + NO2- = HNO2
HCl + NaNO2 = HNO2 + NaCl+ + Cl-
+ Na+ + NO2- = HNO2 + Na+
+ Cl-
Н+
+ NO2- = HNO2
6. Какое значение рН (7<рН<7) имеют растворы солей Na3PO4, K2S, CuSO4? Составьте ионно-молекулярные и
молекулярные уравнения гидролиза этих солей
Решение:3PO4
- соль, образованная сильным основанием и слабой кислотой, подвергается
гидролизу по аниону. Реакция среды щелочная (pH > 7).
Iст. Na3PO4 + H2O  Na2HPO4 + NaOH
Na2HPO4 + NaOH
Na+ + PO43- + НОН  2Na+ + HPO42- +
Na+ + ОН-
2Na+ + HPO42- +
Na+ + ОН-
Na+ + PO43-
+ НОН  2Na+ + HPO42- +
Na+ + ОН-
2Na+ + HPO42- +
Na+ + ОН-
PO43- + НОН  HPO42- + ОН - (избыток
ионов ОН-)
HPO42- + ОН - (избыток
ионов ОН-)
IIст. Na2HPO4 + НОН  NaН2РО4 + NaОН
NaН2РО4 + NaОН
Na+ + HPO42- + НОН  2Na+ + Н2РО4- + ОН-42-
+ H2O
2Na+ + Н2РО4- + ОН-42-
+ H2O  H2PO4- + OH-
H2PO4- + OH-
IIIст. NaH2PO4 + НОН  Н3РО4 + NaОН+ + H2PO4- + НОН
Н3РО4 + NaОН+ + H2PO4- + НОН  Н3РО4 + Na+ + ОН-2PO4-
+ H2O
Н3РО4 + Na+ + ОН-2PO4-
+ H2O  H3PO4 + OH-
H3PO4 + OH-
Гидролиз
протекает преимущественно по первой ступени.2S - соль, образованная
сильным основанием и слабой кислотой, подвергается гидролизу по аниону. Реакция
среды щелочная (рН > 7).
Iст. К2S + HOH  КHS + КOH
КHS + КOH
2К+ + S2- + HOH  К+ + HS- + К+ + OH-
К+ + HS- + К+ + OH-
S2- + HOH  HS- + OH-ст. КHS + HOH
HS- + OH-ст. КHS + HOH  Н2S + КОН
Н2S + КОН
К+ + HS- + HOH  Н2S + К+ + OH-
Н2S + К+ + OH-
HS- + HOH  Н2S + OH-
Н2S + OH-
Гидролиз протекает преимущественно по первой ступени.
Iст. 2CuSO4 + 2HOH  (CuOH)2SO4 + H2SO4
(CuOH)2SO4 + H2SO4
Cu2+ + 2SO42- +
2HOH  2 (CuOH)+ + SO42-
+ 2H+ + SO42-
2 (CuOH)+ + SO42-
+ 2H+ + SO42-
2Cu2+ + 2HOH  2 (CuOH)+ + 2H+
2 (CuOH)+ + 2H+
IIст. (CuOH)2SO4 +
2HOH  2Cu(OH)2 + H2SO4
2Cu(OH)2 + H2SO4
(CuOH)+ + SO42-
+ 2HOH  2Cu(OH)2 + 2H+ + SO42-
2Cu(OH)2 + 2H+ + SO42-
2 (CuOH)+ + 2HOH  2Cu(OH)2 + 2H+
2Cu(OH)2 + 2H+