|
Название
|
Химическая
формула
|
Кристаллическая
сингония
|
Пространственная
группа
|
Параметры
решетки
|
|
|
|
|
Å
|
градус
|
|
1
|
2
|
3
|
4
|
7
|
8
|
|
ДКФД
|
СаНРО4
• 2Н20
|
моноклинная
|
C2
|
а0
= 6.363; b0= 15.19; c0 = 5.815
|
b= 118.48
|
|
ДКФ
|
СаНРО4
|
триклинная
|
Р1
|
а0
= 6.906; Ь0 = 8.577; c0 = 6.634
|
а
= 93.90; b = 91.50; g = 127.63
|
|
a-ТКФ
|
Са3(РО4)2
|
моноклинная
|
Р21/а
|
а0=12.887;
c0 = 27.28; з0 =15.219
|
b = 126.2
|
|
b-ТКФ
|
Са3(РО4)2
|
ромбоэдрическая
|
R3с
|
а0=
10.428; c0 = 37.378
|
|
|
ГА
|
Са5(РО4)3ОН
|
Гексагональная
|
Р63/m
|
а0
= 9.432; c0 = 6.880
|
|
|
Фторапатит
|
Са5(РО4)3F
|
Гексагональная
|
Р63/m
|
а0
= 9.377; c0 = 6.880
|
Са5(РО4)3С1
|
Гексагональная
|
Р63/m
|
а0
= 9.641; c0 = 6.771
|
|
|
Карбонат-апатит
|
Са10(РО4)6CO3
|
Гексагональная
|
Рb
|
a0
= 9.641; с0 = 6.771
|
|
|
ТеКФ
|
Са4(РO4)2O
|
моноклинная
|
Р21
|
а0
= 7.018; b0= 11.98; c0 = 9.469
|
b = 90.88
|
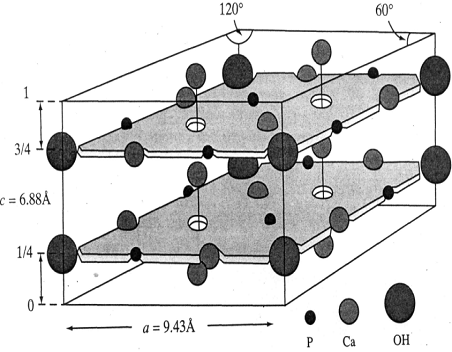
Рис. 1. Упрощенный вид элементарной ячейки
гидроксилапатита
Атом Са что находится в положении 2
окружен шестью атомами кислорода, что относятся группам РО43- и ОН- , в то
время как атом Са, что занимает положение 1, имеет окружение атомами кислорода
близкое к октаэдрическому . Атомы Ca в положении 2 создают треугольник в
плоскости , перпендикулярной к оси С. Треугольники повернуты друг к другу на 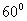 вдоль этой
оси. В структуре фтораапатита атомы
вдоль этой
оси. В структуре фтораапатита атомы 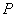 расположены в центре таких
треугольников.
расположены в центре таких
треугольников.
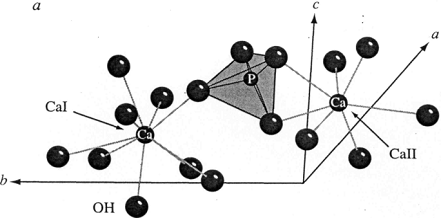
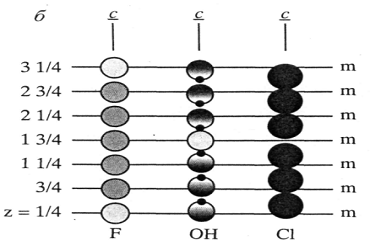
Рис. 2. Фрагмент структуры гидроксилапатита:
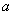 -
координационные полиэдры кальция; б - анионные столбики ионов
-
координационные полиэдры кальция; б - анионные столбики ионов 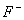 ,
, 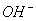 ,
, 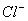 .
.
В случае ГА группы 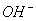 располагаются
немного выше или ниже центра. Атомы
располагаются
немного выше или ниже центра. Атомы 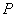 окружены четырьмя атомами
окружены четырьмя атомами 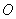 и образуют
тетраэдр практически правильной формы, лишь с небольшим искажением. При
довольно сложной координации атомов
и образуют
тетраэдр практически правильной формы, лишь с небольшим искажением. При
довольно сложной координации атомов 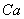 в ячейке ГА образуются 75 связей
в ячейке ГА образуются 75 связей 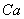 -
-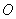 (без учета
связей с кислородом иона гидроксила), 24 связи
(без учета
связей с кислородом иона гидроксила), 24 связи 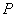 -
- 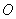 , 6 связей
, 6 связей 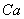 -
- 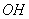 и 2 связи
и 2 связи 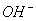 .
.
Стехиометрический ГА может быть
также описан в моноклинной сингонии (пространственная группа Р21/b с
параметрами решетки, а =9.4214(8)Å, b =2a, c= 6.8814(7)Å, b =120°), причем такое
описание не связано с ограничениями, обусловленными зеркальной симметрией.
Снижение симметрии до моноклинной является результатом упорядоченного
расположения ОН- в кальциевых каналах, а также взаимного упорядочения этих
каналов таких образом, который происходит двукратное увеличение параметра b
элементарной ячейки. ГА моноклинной сингонии может быть полученный только
гидротермальным синтезом или термообработкой ГА в атмосфере водной пары.
.2 β-трикальций
фосфат
β-ТКФ (β-трикальций
фосфат) является ортофосфатом кальция со стехиометрическим составом Са3(РО4)2.
Он не может выпадать в осадок из водного раствора, а получается только через
кальцинирование при температуре выше 800°С.
(HPO4)(PO4)5 (OH)® Са3(РО4)2 + Н2О
Выше 1125°С он превращается в a-ТКФ. На температуру
превращения фазы сильно влияют примеси. При комнатной температуре, β-ТКФ имеет
меньшую растворимость, чем a-ТКФ.
В медицине β-ТКФ находит
применение как в чистой фазе, так и в смеси с гидроксилапатитом (так называемый
« бифазный фосфат кальция») в качестве материала для замены кости.
Кристаллографические данные β-ТКФ
следующие (рис.3): ромбоэдрическая система 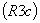 ,
, 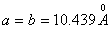 ;
; 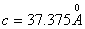 (гексагональная ось); число атомов
в ячейке
(гексагональная ось); число атомов
в ячейке 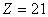 ; плотность
3.067
; плотность
3.067 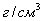 .
.
Рис.3. Структура элементарной ячейки
β-ТКФ.
.3 Получение гидроксилапатита
Существует три основных метода
синтеза фосфатов кальция: осаждением из растворов (мокрый метод), твердофазный
синтез (сухой метод) и гидротермальный синтез. На практике преобладает синтез
фосфатов кальция из водных растворов. Для данного способа характерное множество
факторов, которые изменяются, которые не всегда дают возможность достичь
красивую воспроизводимость, сохранить стехиометрическое соотношение Са/Р в
процессе синтеза, т.е. получить порошок с заданными химическими и физическими
свойствами. Среди множества факторов наиболее критические - рН раствора,
температура реакции и продолжительность процесса [3]. Твердофазный синтез ГА
есть больше продолжительным и энергоемким. Кроме того, этим методом тяжело
достичь гомогенности конечного продукта.
В зависимости от метода синтеза,
может быть получен порошок с разной морфологией, удельной поверхностью,
стехиометрией и степенью кристалличности.
При осаждении ГА из растворов
допускают образование осадка с применением реакции осаждения в результате
смешения водных. растворов соединений, которые содержат ионы Са2+ и РО43-, при
сохранении рН>7 и выдерживании осадка в соответствующих условиях. Как источник
Са2+ изучены СаС12, Ca(NO3)2, Са(ОН)2, СаСО3, CaSO4 • 2Н2О, (СН3СОО)2Са и др.
Как источник фосфатов- ионов могут быть использованы Н3РО4, NH4H2PO4,
(NH4)2HPO4 или К3РО4. Для регулирования рН и введение ОН - групп применяют
водные растворы аммиака или гидроксидов щелочных металлов.
.3.1 Метод осаждения из водных
растворов
Для мокрых методов характерно
образование на начальной стадии осадка, который не отвечает соединению ГА.
Среди множества мокрых методов можно
выделить несколько "классических", которые с теми или иными
изменениями приводятся в литературе. Один из них метод [4], в котором
используют нитрат кальция в качестве источника ионов кальция, основанный на
реакции:
Ca(NO3)2+ 6(NH4)2HPO4+ 8NH4OH =>
Са10(РО4)6(OН)2 + 20NH4NO3 +6H2O
Следует отметить работу, где также в
качестве источник Са использовали Ca(NO3)2:
Ca(NO3)2 + 6KH2PO4 + HNaOH
=>Са10(РО4)б(OН)2 + 6KNO3 + 14NaNO3 + 12Н2О
Рост кристаллов и их выделение из
раствора происходит постепенно; отфильтрованный осадок ГА промывают водой и
спиртом, потом сушат при температуре 40-50°С.
Также был предложен метод, в котором
ГА получают по реакции:
СаС12 + 6(NH4)2HPO4 + 8NH4OH
=>Са10(РО4)6(ОН)2 + 2ONH4C1 + 6H2O
После отстаивания осад промывают
декантацией до рН=7, фильтруют на воронке Бюхнера и сушат на воздухе при
температуре 100°С. Потом осадок отжигают в муфельной печи при температуре
1000°С в течение 2 часов.
Другая группа классических методов
получения ГА кальция мокрым способом основана на реакции [5]:
Са(ОН)2 + 6Н3РО4 Þ
Са10(РО4)6(ОН)2 +18Н2О
Указанную выше базовую реакцию между
Са(ОН)2 и Н3РО4 можно изменить таким образом, чтобы одни реагенты заменить на
другие (иногда частично) того же назначение. Например, описанное получение ГА
на основе реакции:
Са(ОН)2 + 6(NH4)2HPO4 =>
Са10(РО4)6(ОН)2 + 12NH4OH + 6Н2О
В результате смешивания
эквимолекулярных количеств реагентов на протяжении часа и следующего
высушивания осадка при 85°С получали порошки белого цвета, которые отжигали при
1000°С на воздухе в муфельной печи.
Можно получать высококачественный ГА
из смеси Са(ОН)2, Са3(РО4)2, (NH4)3PO4, и Н3РО4, который отвечает соединению
конечного продукта, со следующей ультразвуковой обработкой при частоте 10-30
кГц.
Образование ГА также возможно при
добавлении Са(ОН)2 к водной суспензии Са3(РО4)2 при перемешивании в интервале
температур от 5 до 100°С в атмосфере инертного газа; рН смеси поддерживают
равным 10, регулируя количество подаваемого Са(ОН)2 до тех пор, пока Са/Р не
составит 1.6. Дальше взаимодействие проводят к моменту, когда Са/Р достигает
1.67, поддерживая рН = 7-11.
ГА получают при быстром смешивании
растворов Ca(NO3)2 и К3РО4.. Исходное отношение Са/Р составляет 1.58, а через 6
часов - 1.67. Осаждением из растворов могут быть полученные Mg-, Y-, Zn-, Cd
замещенные апатиты.
.4 Рентгеноструктурный анализ
Рентгеновские лучи генерируются в
специальных устройствах - рентгеновских трубках. Они возникают в результате
взаимодействия быстролетящих электронов с веществом анода, встречающимся на их
пути. Электроны приобретают большую скорость за счет высокой разности
потенциалов между анодом и катодом. Источником электронов является вольфрамовая
нить, через которую пропускается электрический ток. Эти электроны выбивают из
вещества анода g-кванты,
т.е. образуют рентгеновское излучение. При попадании рентгеновского излучения
на поверхность образца, часть рентгеновских лучей рассеивается с образованием
максимумов, удовлетворяющих условию Вульфа-Брэгга [7]:
dhklsinӨ=nλ,
где dhkl - межплоскостное расстояние
для плоскостей с индексами (hkl),
Ө - угол скольжения (половина
угла рассеяния), λ
- длина
волны рентгеновского излучения, n - целое число (порядок отражения).
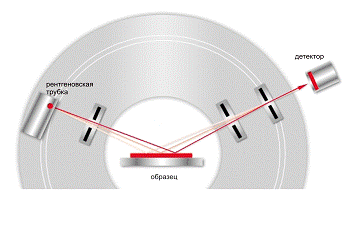
Рис. 4. Схема получения
рентгенограммы
Рассеянное излучение попадает в
детектор, который вращается с заданной скоростью (рис. 4). В результате
полученная рентгенограмма представляет собой зависимость интенсивности
излучения от угла рассеяния. По полученной рентгенограмме получают значения
межплоскостных расстояний, затем проводят индицирование, т. е. сопоставление каждому
межплоскостному расстоянию определенных индексов Миллера h,k,l. Так, например,
для гексагональной системы существует следующая квадратичная форма:
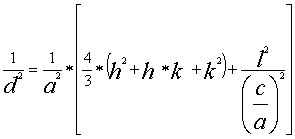
Таким образом, можно определить параметры
кристаллической решетки, используя массив значений индексов Миллера плоскостей,
принадлежащих данной кристаллографической системе, а также ряд межплоскостных
расстояний исследуемого образца.
2. Экспериментальная часть
.1 Материалы и методика эксперимента
Синтез ГА проводили на основе
реакции осаждения из водных растворов. Компоненты реакции выбирали из расчета,
чтобы получить ГА. Делали расчет с помощью программы Chemical Equation Expert
v2.00. (Ca(NO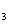 )
)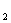 ) = 30
г;(NH4OH)=33.9 мл;(H3 PO
) = 30
г;(NH4OH)=33.9 мл;(H3 PO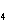 )=7.5 мл.
)=7.5 мл.
pH раствора поддерживали на уровне
10-12. Синтез проводили при комнатной температуре t=20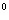 С и
влажности воздуха 58%. Процесс синтеза заключался в том, что в раствор нитрата
Ca(NO
С и
влажности воздуха 58%. Процесс синтеза заключался в том, что в раствор нитрата
Ca(NO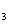 )
)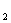 вводили
аммиак NH
вводили
аммиак NH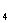 O
O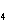 Н.
Н.
Прокапывание раствора NH OН проводили
в течение 40 минут. После прокапывания полученный раствор непрерывно
перемешивался в течение суток.
OН проводили
в течение 40 минут. После прокапывания полученный раствор непрерывно
перемешивался в течение суток.
Полученный в результате синтеза
осадок сушили при комнатной температуре, затем растирали в порошок. От
полученных образцов снимали рентгенограммы с использованием рентгеновского
диффрактометра ДРОН 2.0 в медном излучении (U=30 kB, I=30 mA).
Из порошков было изготовлено два
цилиндрических образца
=
7,2 мм, h1 = 2,7 мм;= 7,25 мм, h2 = 2,5 мм;
Результаты
На
рис. 5 приведены рентгенограммы исходного образца. В качестве исходного образца
выбран первый цилиндрический образец.
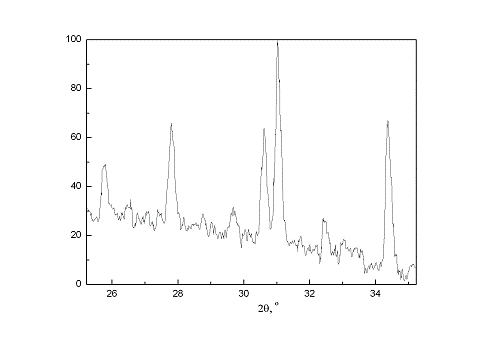
Рис.
5. Рентгеограмма образца
Проверим
фазовый состав образца. Он представлен на рис.6.
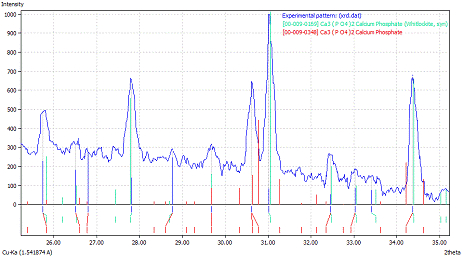
Рис.6.
Фазовый состав образца
Из
этого графика видно что в данном образце отсутствует ГА. Но при этом есть β-ТКФ (β-трикальций
фосфат) является ортофосфатом кальция со стехиометрическим составом Са3(РО4)2 и
α-ТКФ (α -трикальций
фосфат).
Выводы
В
результате эксперимента я освоила метод осаждения водных растворов. Но место ГА
получила β-ТКФ и α-ТКФ. Это
могло произойти из-за разных причин. Например, могли неправильно свесить
компоненты реакции или не правильно провести синтез.
Список
литературы
С.
М. Баринов, В. С. Комлев, Биокерамика на основе фосфатов кальция. М.: Наука,
2005.. I. Kay, R. A. Young, A. S. Posner, Crystal structure of hydroxyapatite,
Nature, 1964, 204, 1050..D. Eanes, I.H. Gillesen, A.S. Posner. Nature, 1965,
208, 365-367.
Ю.Третьяков,
Химия твердого тела, М., МГУ, 1990.
Л.
В. Вилков, Ю. А. Пентин, Физические методы исследования в химии., М., Высшая
школа, 1989.