Физические, физико-химические и химические методы оценки качества продовольственных товаров
КУРСОВАЯ РАБОТА
По дисциплине
«Теоретические основы товароведения»
Тема: Физические, физико-химические и химические
методы оценки качества продовольственных товаров.
Оглавление
Введение
. Аналитический
обзор литературы
.1 Физические
методы
.1.1 Определение
относительной плотности
.1.1.1
Пикнометрический метод
.1.1.2
Ареометрический метод
.1.2 Определение
температур плавления и застывания
.2
Физико-химические методы
.2.1 Поляриметрия
.2.2 Рефрактометрия
.2.3
Фотоколориметрический метод
.2.4 Спектральный
метод
.2.5 Хроматография
.2.6
Потенциометрический метод
.2.7
Кондуктометрический метод
.2.8 Реологические
методы
.2.9
Микроскопирование
.3 Химические
методы
. Материалы и
методы исследования
. Результаты
собственных исследований
Выводы
Библиографический
список
Приложение А
Введение
Измерительные методы - методы
определения (измерения) действительных значений показателей качества с помощью
технических устройств. Они широко применяются для установления химического
состава, физико-химических показателей, доброкачественности, физических и
других свойств пищевых продуктов. В отличие от органолептических показателей
физико-химические показатели специфичны и характерны для товаров однородных
групп. Поэтому эти показатели более многочисленны, что требует применения
разнообразных измерительных методов для их определения. В зависимости от
способов получения результатов эти методы подразделяют на физические,
физико-химические и химические, биохимические, микробиологические,
физиологические, товароведно-технические. При исследовании качества пищевых
продуктов редко используют все методы анализа; чаще ограничиваются теми,
которые соответствуют целям исследования.
Осуществляют их с помощью
приборов и химических реактивов, поэтому полученные результаты выражают
конкретными величинами, отличающимися большой точностью. Однако о качестве
пищевых продуктов нельзя судить только по результатам лабораторных
исследований, объективная оценка будет получена только тогда, когда они будут
дополнены органолептическим анализом.
Измерительные методы
взаимосвязаны с органолептическими методами, дополняют, но не заменяют их. Это
обусловлено тем, что достоинства измерительных методов - объективность оценки,
выражение результатов в общепринятых единицах измерения, сопоставимость и воспроизводимость
результатов - устраняют недостатки органолептических методов. В связи с этим
сочетание методов этих двух групп позволяет провести наиболее полную экспертную
оценку товаров.
Недостатками измерительных
методов являются: высокие затраты на проведение испытаний, для которых
требуются оборудование лаборатории, лабораторное и вспомогательное
оборудование, порой очень дорогостоящее, а также высококвалифицированный
персонал.
Указанные недостатки носят
объективный характер, поэтому трудно или совсем неустранимы. В связи с этим
применение измерительных методов при товарной экспертизе ограничено и
рекомендуется только в тех случаях, когда без данных, получаемых с помощью этих
методов, невозможно сделать объективные и достоверные выводы.
I.
Аналитический обзор литературы
.1 Физические методы
С помощью этих методов
определяют относительную плотность продукта, температуру плавления и
застывания, оптические показатели, структурно-механические свойства и др.
.1.1 Определение относительной
плотности
Плотностью 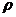 называется
количество массы m данного вещества в единице объема v. В
соответствии с Международной системой единиц (СИ) ее измеряют в кг/м3. при
анализе пищевых продуктов обычно определяют относительную плотность, выражаемую
в виде отношения плотности продукта к плотности стандартного вещества при
определенной температуре. Для жидких продуктов таким стандартным веществом
является вода 40С. При этой температуре вода имеет наибольшую плотность, равную
единице.
называется
количество массы m данного вещества в единице объема v. В
соответствии с Международной системой единиц (СИ) ее измеряют в кг/м3. при
анализе пищевых продуктов обычно определяют относительную плотность, выражаемую
в виде отношения плотности продукта к плотности стандартного вещества при
определенной температуре. Для жидких продуктов таким стандартным веществом
является вода 40С. При этой температуре вода имеет наибольшую плотность, равную
единице.
Относительную плотность исследуемого
продукта определяют по формуле
d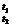 =
= 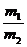 .
.
Где m1
- масса продукта, кг;
m2
- масса воды, кг.
Обычно относительную плотность
определяют при температуре продукта 200С и обозначают символами d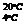 или d
или d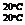 . Для
пересчета значений плотности d
. Для
пересчета значений плотности d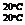 в d
в d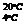 или
наоборот пользуются температурными коэффициентами расширения
или
наоборот пользуются температурными коэффициентами расширения
d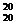 = 1,00177 d
= 1,00177 d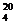 и d
и d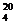 = 0,99823d
= 0,99823d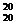 .
.
Относительная плотность жидких
продуктов зависит не только от их температуры, но и от концентрации сухих
веществ.
Показатели плотности важны при
оценке качества молока, определении содержания сухих веществ в плодовых и
ягодных экстрактах, содержания соли в рассолах, проверки крепости спирта и
водки. При этом пользуются для каждого продукта таблицей, в которой приводится
содержание вещества в растворе в зависимости от плотности и температуры его.
Для определения относительной
плотности чаще всего применяют пикнометрический и ареометрический методы.
Пикнометрический метод. Метод
основан на определении массы равных объемов исследуемого продукта и воды при
температуре 20°С.
Приборы и оборудование. Пикнометры
на 10, 25 или 50 мл; аналитические весы; эксикатор; водяной термостат или
ультратермостат; капиллярная пипетка.
Порядок проведения анализа.
Предварительно подготовленный чистый и сухой пикнометр взвешивают на
аналитических весах с точностью до 0,0001 г. Затем его наполняют исследуемой
жидкостью, уровень которой должен быть немного выше метки, и помещают на 20-30
мин в термостат или водяную баню при 20°С. После этого объем жидкости доводят
точно до метки. При излишке жидкости ее удаляют жгутиком из фильтровальной
бумаги, а при недостатке добавляют из капиллярной пипетки. Внутреннюю
поверхность шейки пикнометра, не заполненную жидкостью, тщательно обсушивают полоской
фильтровальной бумаги.
После термостатирования и доведения
объема исследуемой жидкости до метки пикнометр закрывают пробкой, обтирают
фильтровальной бумагой или полотенцем досуха и оставляют на 30 мин около весов,
после чего взвешивают с точностью до ± 0,0001 г.
Таким же образом определяют массу
дистиллированной воды.
Плотность исследуемой жидкости
вычисляют по формуле
d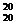 =
= 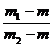 ,
,
где m - масса
пустого пикнометра, г;
m1 - масса
пикнометра с исследуемой жидкостью, г;
m2 - масса
пикнометра с дистиллированной водой, г.
Плотность рассчитывают с точностью
до десятичного знака.
Ареометрический метод. В исследуемый
жидкий продукт погружают ареометр до тех пор, пока масса жидкого продукта,
вытесненного им, не станет равной массе ареометра. Плотность жидкости продукта
определяют по градуированной шкале ареометра в зависимости от уровня его
погружения. Внутри некоторых ареометров имеется термометр, которым можно
измерять температуру исследуемого жидкого продукта. Шкала ареометра рассчитана
на 20°С.
Приборы. Ареометр со шкалой,
показывающей плотность d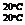 (с ценой деления, равной 0,001);
стеклянный цилиндр; термометр.
(с ценой деления, равной 0,001);
стеклянный цилиндр; термометр.
Порядок проведения анализа. В
стеклянный цилиндр наливают исследуемый жидкий продукт определенной
температуры. Жидкого продукта в цилиндре должно быть достаточно для свободного
погружения ареометра (около 3/4 объема цилиндра). Затем в жидкий продукт
осторожно опускают чистый и сухой ареометр. При этом ареометр не должен
касаться стенок цилиндра. При исследовании прозрачных жидких продуктов деления
отсчитывают по нижнему мениску, а при исследовании непрозрачных - по верхнему.
Если температура исследуемого жидкого продукта отличается от установленной
(20°С), то в результаты определений вносят соответствующую поправку, которую
берут из специальных таблиц.
За конечный результат принимают
среднее арифметическое двух определений, разность между которыми не должна
превышать 0,002 г.
1.1.2 Определение температур
плавления и застывания
Определение температурных
констант проводят при исследовании качества жиров, установлении их природы,
чистоты, отсутствия примесей.
.2 Физико-химические методы
Физико-химические методы
применяются при определении оптических показателей пищевых продуктов. Эти
показатели определяют с помощью поляриметрии, рефрактометрии, фотометрии,
спектроскопии, хроматографии и др.
.2.1 Поляриметрия
Поляриметрический метод основан
на свойстве некоторых веществ изменять направление световых колебании.
Вещества, обладающие свойством
изменять направление колебаний при прохождении через них поляризованного света,
наминаются оптически анизотропными или оптически активными и отличие от
оптически изотропных, или неактивных, которые этих изменений не вызывают.
К веществам последней группы
относятся главным образом такие органические вещества, как сахароза, фруктоза,
глюкоза, винная кислота. Поляриметрический метод разработан для количественного
определения веществ именно этой группы.
У поляризованного луча,
пропущенного через слой раствора оптически активного вещества, меняется направление
колебаний, л плоскость поляризации оказывается повернутой на некоторый угол,
называемый углом поворота плоскости поляризации.
Угол поворота плоскости
поляризации зависит от природы вещества, концентрации его в растворе, толщины
слоя раствора, через который проходит поляризованный луч, а также от длины
полны поляризованного луча и температуры.
Оптическая активность веществ
характеризуется удельным вращением. Под удельным вращением понимают угол, на
который повернется плоскость поляризации при прохождении поляризованного луча
через раствор, в 1 мл которого содержится 1 г растворенного вещества при
толщине слоя раствора (длине поляризационной трубки), равной 1 дм.
Удельное вращение зависит не только
от природы вещества но и от температуры, длины волны поляризованного света и
растворителя, поэтому его принято относить к температуре 20°С и желтой линии
натрия и обозначать 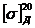 с указанием
растворителя.
с указанием
растворителя.
Угол вращения плоскости поляризации 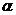 определяют
по формуле
определяют
по формуле
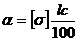 ,
,
где l
- длина трубки, дм;
с - концентрация вещества,
г/100 мл.
Пользуясь этой формулой, легко
вычислить количество вещества в граммах, содержащееся в 100 мл раствора, т. е.
концентрацию с,
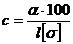 .
.
Основные рабочие части
поляриметра: устройство для поляризации света (поляризатор); устройство для
определения угла поворота плоскости поляризации после прохождения
поляризованных лучей через исследуемый раствор (анализатор); поляризационная
трубка, наполняемая исследуемым раствором и помещаемая между поляризатором и
анализатором.
В качестве поляризаторов
применяют кристаллы исландского шпата или других минералов, обладающих
свойством двойного лучепреломления.
Анализатор в отличие от
поляризатора может поворачиваться вокруг оси прибора. Когда главные линии призм
анализатора и поляризатора расположены параллельно, свет, проходящий через
поляризатор, пройдет и через анализатор (при отсутствии между ними раствора).
Если же главные сечения
анализатора и поляризатора взаимно перпендикулярны, лучи через анализатор не
пройдут.
При всех промежуточных
положениях через анализатор пройдет только часть лучей от призмы поляризатора.
Если поместить между
поляризатором и анализатором оптически активное вещество, количество проходящих
через анализатор лучей изменится в результате того, что плоскость
поляризованных лучей окажется повернутой.
Вращая анализатор, добиваются
исходного (до помещения раствора) положения и по углу поворота прибора,
соединенного со шкалой, судят о степени вращения плоскости поляризации
исследуемым раствором, что позволяет рассчитать количество вещества в растворе.
Различают поляриметры с
установкой на полную темноту, полутеневые с двойным и тройным полем зрения.
Наиболее широкое применение
получили полутеневые поляриметры.
У поляриметров этого типа с
двойным полем зрения поляризатор состоит из двух николей, а у поляриметров с
тройным полем зрения - из трех.
Разновидностью поляриметра
является сахариметр, предназначенный для определения содержания сахарозы в
растворах. В отличие от поляриметров других видов сахариметр имеет линейную
шкалу, градуированную по сахарозе. 100° этой шкалы соответствуют 34, 62
кругового градуса шкалы поляриметра.
Сахариметр показывает 100°,
если в трубке длиной 200 мм поляризуют раствор, в 100 мл которого при 20°С
содержится точно 26 г химически чистой, абсолютно сухой сахарозы.
Особенность оптической системы
сахариметра состоит в том, что анализатор в нем поставлен на полутень по
отношению к потру и укреплен неподвижно. Изменение угла поворота плоскости
поляризации, вызванное исследуемым раствором, устанавливают клиновым кварцевым
компенсатором.
Кварц - оптически активное
вещество, обладающее вращательной способностью, близкой к вращательной
способности сахарозы, но обратной по направлению. Меняя толщину слоя кварца,
можно полностью компенсировать вращение, вызываемое сахарозой.
Существует несколько типов
компенсаторов, отличающихся один от другого количеством кварцевых клиньев и
пластинок. Но принцип действия их одинаков и основан на том, что относительным
перемещением клиньев можно менять толщину кварцевого слоя.
Подвижный клин (или клинья)
смещается шестеренкой, соединенной с подвижной горизонтальной шкалой, что
позволяет отсчитывать непосредственно концентрацию раствора сахарозы.
Приготовление раствора. На
аналитических весах отвешивают точно 26 г сахара-песка или предварительно
измельченного в ступке сахара-рафинада. Навеску переносят в химический стакан,
куда небольшими порциями добавляют теплую дистиллированную воду. Полученный
раствор с помощью воронки и стеклянной палочки без потерь переливают в мерную
колбу вместимостью 100 мл. Стакан и воронку тщательно ополаскивают и промывные
воды также сливают в мерную колбу. Раствор доливают до метки только после того,
как температура его и дистиллированной воды достигнет 20°С. После тщательного
взбалтывания содержимого колбы раствор фильтруют через бумажный фильтр. В
процессе фильтрования во избежание испарения воды и нарушения концентрации
раствора воронку необходимо покрыть часовым стеклом. Сразу по окончании
фильтрования раствор следует подвергнуть поляриметрии.
Порядок проведения анализа.
Трубку сахариметра, только что бывшую в употреблении (не сухую), сначала
ополаскивают в дистиллированной воде, а затем двумя-тремя небольшими порциями
испытуемого раствора. Торцовые (покрывные) стекла промывают дистиллированной
водой и досуха протирают.
При исследовании чистого
сахара-песка или рафинада пользуются трубкой длинной 200 мм, для сметок - 100
мм.
Трубку, закрытую с одной
стороны, наполняют так, чтобы верхний мениск раствора выступал над ее краями,
после чего трубку накрывают стеклышком, а затем уже навинчивают металлическую
головку. Далее проверяют, нет ли в трубке пузырьков воздуха. При наличии их
головку со стеклом снимают и в трубку добавляют несколько капель раствора. С
наружной стороны торцовые стекла должны быть абсолютно сухими, иначе поле
зрения окажется затемненным.
Перед тем, как поместить трубку
в камеру, окуляр зрительной трубы и лупу шкалы вращением их оправ устанавливают
на максимальную резкость изображения так, чтобы были четко видны вертикальная
линия, разделяющая поле зрения на две половины, а в поле зрения лупы - щтрихи и
цифры шкалы и нониуса.
Перед началом измерений прибор
необходимо установить на нуль. Для этого (при отсутствии в камере
поляриметрической кюветы) вращением рукоятки кремальерной передачи добиваются
полной однородности обеих половин поля зрения, при этом нулевые деления шкалы и
нониуса должны совпадать. В противоположном случае посредством ключа перемещают
нониус до совмещения его нулевого деления с нулевым делением шкалы, после чего
приступают к измерениям.
В камеру прибора вкладывают
поляриметрическую кювету с испытуемым раствором, в результате чего изменится
однородность обеих половин поля зрения. Вращением рукоятки кремальерной
передачи уравнивают их освещенность. После этого, пользуясь нониусом,
отсчитывают показания с точностью до 0,50S.
Затем проверяют уравнивание освещенностей обеих половин поля зрения и снова
отсчитывают показания.
Отсчет производят не менее трех
раз; при этом каждый отсчет начинают с возвращения рукоятки в нулевое
положение. Записав все три показания (Р1, Р2, Р3), рассчитывают среднее из них
(Рср) по формуле
 ,
,
где Рср - содержание сахарозы в
исследуемом продукте, % (при использовании трубки длиной 100 мм результат
умножают на 2).
Содержание сахарозы в сахаре принято
выражать в пересчете на сухое вещество, поэтому определяют также влажность
сахара b.
Зная влажность сахара, содержание
сахарозы Х в процентах в пересчете на сухое вещество вычисляют по формуле
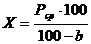 .
.
Сахариметром можно определить содержание
сахарозы в растворе неизвестной концентрации без предварительного взятия
навески. При этом сначала определяют плотность исследуемого вещества
(раствора), а затем вычисляют содержание сахарозы в процентах по формуле
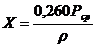 .
.
1.2.2 Рефрактометрия
Рефрактометрический анализ
основан на измерении показателя преломления (рефракции) веществ, по которому
судят о природе веществ, их чистоте или содержании в растворах.
Его широко применяют при исследовании
таких пищевых продуктов, как жиры, томатные продукты, варенье, джем. Этим
методом пользуются также для количественного определения жиров в пищевых
продуктах, влажности, содержания спирта в растворе (в сочетании с
пикнометрическим методом), для пофазного контроля в процессе производства
пищевых продуктов - кондитерских, напитков, некоторых видов консервов и т. д.
Показатель преломления зависит
от температуры, поэтому рефрактометрические измерения принято выполнять при
20°С. При отклонении температуры от 20°С вводят соответствующие температурные
поправки.
Давление также отражается на
результатах рефрактометрических измерений. С повышением его показатели
преломления увеличиваются.
При работе с раствором следует
учитывать, что между показателем преломления и процентным содержанием вещества
в растворе не всегда существует прямая зависимость. Поэтому судить о
концентрации вещества в растворе по показателю преломления можно только при
наличии кривых, выражающих зависимость между этими двумя величинами. В некоторых
случаях по показателю преломления невозможно определить содержание вещества в
растворе, так как даже при значительных колебаниях концентрации вещества
показатель преломления изменяется очень мало (например, для растворов
метилового спирта). При наличии в растворе двух веществ только по показателю
преломления нельзя судить о состоянии системы. В этом случае требуется знать
какие-либо другие физико-химические величины, например температуру кипения или
плавления, плотность вещества.
Для измерения показателя
преломления жидких веществ и растворов применяют приборы, называемые
рефрактометрами.
Большинство рефрактометров
устроено так, что исследуемое вещество помещается между двумя призмами (двумя
половинами призмы). Свет, пропущенный через призму, преломляясь или отражаясь
от границы раздела сред (призма - вещество), освещает только часть шкалы,
образуя достаточно резкую границу света и тени. Положение этой границы на шкале
зависит от угла полного внутреннего отражения исследуемого вещества. На шкале
указаны показатели преломления, соответствующие различным значениям угла
полного внутреннего отражения.
В качестве источника света
пользуются монохроматическим светом натриевой горелки или обычным белым светом,
направляемым специальным зеркалом. Поскольку белый свет состоит из лучей
различной длины волн, при прохождении его через призму возникает явление
светорассеяния (дисперсии), в результате чего на границе света и тени
образуется радужная полоска, затрудняющая отсчет по шкале рефрактометра.
Поэтому во всех современных конструкциях рефрактометров предусматриваются так
называемые компенсаторы, позволяющие устранить дисперсию света.
Компенсаторы - это оптические
системы, представляющие собой совокупность двух или трех призм или линз,
изготовленных из стекла разных видов и установленных так, что различные цвета
спектра налагаются один на другой, благодаря чему граница света и тени
становится отчетливой.
Поскольку световые лучи исходят
из всех точек поверхности призмы и в различных направлениях, на пути между
призмой и шкалой помещают линзу, собирающую все параллельные лучи в фокус.
Таким образом, каждому пучку световых лучей, прошедших через линзу,
соответствует световая точка.
Температуру призмы и
исследуемого вещества контролируют термометрами, вмонтированными в оправу
призм. Для регулирования и поддержания постоянной температуры в полые
металлические оправы призм по специальным устройствам подают воду требуемой
температуры. При отсутствии этих устройств пользуются таблицами температурных
поправок.
Правильность показаний
рефрактометров проверяют с помощью нормальной жидкости или дистиллированной
воды, показатель преломления которой при 20°С равен 1,333, либо пользуются
юстировочной пластинкой, на которой указан показатель преломления. При
наложении пластинки на призму рефрактометра показание шкалы должно совпадать с
показателем, указанным на пластинке.
Рефрактометр ИРФ-22. Этот
прибор применяют для измерения показателей преломления в интервале 1,3-1,7 как
жидких, так и твердых продуктов.
Основные рабочие части прибора:
две призмы, сложенные гипотенузными сторонами и составляющие вместе с оправами
полушаровидной формы измерительную головку, зрительная труба с отсчетным
устройством.
В оправах призм имеются камеры,
через которые пропускают воду и таким образом регулируют температуру призм и
заключенного между ними вещества. Температуру контролируют термометром,
ввинченным в оправу призм. Для устранения радужной полоски на границе раздела
темной и светлой частей поля зрения предназначен компенсатор. Шкала отсчетного
устройства жестко соединена с измерительной головкой и помещена в корпусе
прибора.
Рефрактометр снабжен двумя
зеркалами: одно служит для тления света через исследуемое вещество и призмы,
другое - для освещения шкалы показателей преломления.
Принцип действия рефрактометра.
Лучи света, отражаясь от зеркала, проходят через призму, гипотенузная сторона
которой матовая, благодаря чему происходит рассеивание света. В исследуемое
вещество попадают лучи различных направлений, в том числе и скользящие. Эта
призма является осветительной. Пройдя слой жидкости и преломившись на границе
жидкость - стекло, лучи войдут во вторую призму (измерительную). Максимальным
углом выхода лучей из призмы будет предельный угол, соответствующий скользящим
лучам. Таким образом поле зрительной трубы, поставленной на пути лучей,
окажется раздельным на две части - темную и светлую. При этом положение границы
раздела будет определяться предельным углом, зависящим от природы вещества.
Порядок проведения анализа. С
помощью нормальной жидкости или дистиллированной воды проверяют правильность
показаний рефрактометра. Затем, протерев досуха призмы, оплавленной стеклянной
палочкой на нижнюю призму помещают несколько капель исследуемой жидкости, из
которой предварительным фильтрованием через вату или марлю удаляют взвешенные
частицы. Нижнюю призму накрывают верхней.
Смотря в окуляр, зеркалом
направляют отраженный свет в верхнюю часть окошка оправы призмы, если жидкости
мутные. Затем рычагом перемещают окуляр до совмещения визира с границей раздела
темной и светлой частей поля зрения. Головку окуляра необходимо установить по
глазу так, чтобы деления и цифры шкалы были отчетливо видны. Если граница
окажется расплывчатой, радужной, то, вращая рукоятку компенсатора, добиваются
четкости и записывают показания шкалы. Таким образом производят не менее трех
отсчетов. Окончательным результатом является среднее арифметическое из всех
отсчетов. В процессе определения необходимо следить за показаниями термометра.
Если температура окажется выше или ниже 200С, то необходимо пользоваться
температурными поправками либо произвести предварительное темперирование призм.
Простейшим устройством для
темперирования призм является тубусная склянка вместимостью 3-5 л, соединяемая
резиновыми трубками с оправами призм и установленная несколько выше
рефрактометра. Вода, имеющая температуру на 2-30 выше 200С (в зависимости от
температуры помещения), сначала поступает в оправы, а затем через трубку,
надетую на нижний отросток оправы, в раковину или ведро. Скорость поступления и
вытекания воды в оправы регулируют винтовными зажимами.
После того как граница раздела
света и тени совместится с перекрестием трубы, делают отсчет по шкале. Индексом
для отсчета служит неподвижный горизонтальный штрих. Целые, десятые, сотые и
тысячные доли значения показателя преломления отсчитывают по шкале, десятичные
доли оценивают на глаз.
Рефрактометр РПЛ-3. Этот
рефрактометр предназначен для определения показателя преломления жидкости и
содержания сухих веществ по сахарозе в кондитерских изделиях, консервах, крахмале,
патоке и т. д.
Перед началом измерений
проверяют нуль-пункт прибора, для чего на полированную плоскость измерительной
призмы наносят 1-2 капли дистиллированной воды и устанавливают окуляр на
резкость по шкале и визирной линии сетки. После этого окуляр перемещают по
шкале до тех пор, пока визирная линия сетки не совместится с границей
светотеней. При правильной установки прибора на нуль-пункт граница светотени
при 200С должна совместится с нулевым делением шкалы сухих веществ и делением nD=1.33299
шкалы показателей преломления. В случае отклонения от этих значений прибор
необходимо установить ключом на нуль, для чего следует освободить пробу на
корпусе, через отверстие в корпусе на квадрат винта вставить ключ и вращением
его в ту или другую сторону совместить линию границы светотени с делением nD=1.33299,
нулевым делением шкалы сухих веществ и визирной линией сетки.
Установив прибор на нуль-пункт,
поднимают верхнюю камеру, вытирают соприкасающиеся плоскости призм досуха,
сначала фильтровальной бумагой, а затем неворсистой салфеткой. После этого на
поверхность измерительной призмы наносят 1-2 капли исследуемого раствора и
плавно опускают верхнюю камеру.
В одно из окон осветителем
направляют свет, при этом другое окно должно быть закрыто ширмой. Перемещая
окуляр, вводят в поле зрения прибора границу светотени, устанавливают ее на
резкость, одновременно поворачивают сектор компенсатора. Перемещают рукоятку с
окуляром до совмещения визирной линии сетки с границей светотени и по шкале
производят отсчет показаний. Измерения следует производить при 200С. Анализ
можно проводить при температуре в интервале 10 - 300С. При этом необходимо
вводить поправку на температуру, выраженную в процентах сухих веществ.
Нуль-пункт прибора во всех случаях устанавливают при 200С.
.2.3 Фотоколориметрия
Задача фотоколориметрии -
определение содержания вещества в растворе. Фотоколориметрический метод основан
на избирательном поглощении исследуемым веществом монохроматического света.
Окраска исследуемого растворенного вещества может быть естественной или
полученной при взаимодействии его со специфическими реактивами.
Изменение интенсивности
светового потока при прохождении его через окрашенное вещество измеряют с
помощью фотоэлементов. Каждое окрашенное вещество характеризуется своим
спектром поглощения.
Содержание исследуемого
вещества определяют непосредственно в испытуемом растворе или после
предварительного отделения его от тех примесей, которые также могут
образовывать окрашенные соединения с добавленным реактивом. Интенсивность
окраски исследуемого раствора выражают соотношением между величинами падающего
светового потока до и после прохождения его через этот раствор.
Законы, устанавливающие
зависимость поглощения света веществом от количества поглощающих центров,
открыты Бугером, Ламбертом и Беером.
Бугер установил, что при прочих
равных условиях слои вещества одинаковой толщины поглощают одну и ту же часть
дающего на них светового потока. При этом поглощение светового потока не
зависит от абсолютной интенсивности падающего света. Зависимость между
интенсивностью монохроматического светового потока после прохождения его через
раствор и интенсивностью падающего монохроматического светового потока
выражается убывающей показательной функцией
Ф=Ф0е-k’l,
где Ф0 - интенсивность
падающего монохроматического светового потока;
Ф - интенсивность
монохроматического светового потока после прохождения его через раствор;
е - основание натуральных
логарифмов;
l
- толщина слоя;
k’
- коэффициент поглощения лучей, зависящий от природы вещества и длины волны
светового потока.
При расчетах удобнее
пользоваться десятичными логарифма. Для перехода логарифмов от натуральных к
десятичным применяют формулу
Ф=Ф0 . 10-kl,
где k
- коэффициент погашения лучей (& = 2,3026k').
При одной и той же длине волны
светового потока коэффициенты поглощения и погашения зависят только от природы
вещества. Коэффициент погашения равен обратной величине толщины слоя вещества,
ослабляющего интенсивность проходящего через него светового потока в 10 раз, т.
е. k = 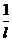 .
.
Беер установил, что между
концентрацией растворенного окрашенного вещества и поглощающей способностью
раствора имеется прямая пропорциональная зависимость
k=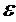 c,
c,
где 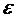 - постоянная величина, зависящая от
природы растворенного вещества и длины волны светового потока, но не зависящая
от его концентрации;
- постоянная величина, зависящая от
природы растворенного вещества и длины волны светового потока, но не зависящая
от его концентрации;
с - концентрация вещества в
растворе.
Закон Бугера - Ламберта
рассматривает изменения поглощения светового потока средой, пропускающей свет,
при изменении толщины этой среды. Закон Беера устанавливает изменения
поглощения светового потока одинаковой толщины при изменении концентрации
вещества.
В отличие от закона Бугера -
Ламберта закон Беера имеет много исключений, которые следует учитывать при
фотоколориметрировании. В практике фотоколориметрии меняются не только
концентрации, но и толщина слоя растворов.
Объединяя приведенные уравнения,
получим выражение основного закона фотоколориметрии Бугера - Ламберта - Беера
для растворов
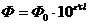
Выразив концентрацию растворенного
вещества в грамм-молях на 1 л, а толщину слоя в сантиметрах, получим
коэффициент молярного погашения (коэффициент 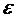 ').
').
При постоянной длине волны
'поглощаемого светового потока и одной и той же температуре коэффициент
молярного погашения - величина постоянная для каждого вещества. В зависимости
от строения вещества коэффициент молярного погашения меняется в очень широких
пределах: так, для хромата калия 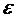 ’ = 500, а для роданида железа
’ = 500, а для роданида железа 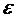 ’ = 100.
Пользоваться уравнением сложно, так как величины концентрации и толщины слоя
находятся в показателе степени. Для приведения его к виду, удобному для
расчета, и выведения некоторых фотометрических величин его преобразовывают в
следующее уравнение:
’ = 100.
Пользоваться уравнением сложно, так как величины концентрации и толщины слоя
находятся в показателе степени. Для приведения его к виду, удобному для
расчета, и выведения некоторых фотометрических величин его преобразовывают в
следующее уравнение:
 lg
lg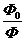 =
= 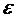 cl.
cl.
пищевой продукт
свойство доброкачественность
Левую часть этого уравнения,
показывающую отношение интенсивности падающего светового потока к интенсивности
светового потока, прошедшего через раствор, называют экстинкцией или погашением
и обозначают Е:
Е=lg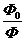 =
=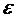 cl.
cl.
Натуральный логарифм отношения
интенсивности падающего светового потока к интенсивности прошедшего через
раствор светового потока называют оптической плотностью или поглощением и
обозначают D:
D=ln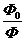 =kcl.
=kcl.
Из сопоставления последних двух
уравнений следует, что между оптической плотностью и экстинкцией имеется
соотношение
Е= 2,3026D.
Экстинкция и оптическая
плотность пропорциональны концентрации вещества в растворе. Отношение
интенсивности светового потока, прошедшего через раствор, к интенсивности
падающего светового потока называют прозрачностью (пропусканием) вещества и обозначают
Т:
Т=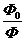 =
=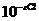 .
.
Величина Т, отнесенная к
толщине слоя 1 см, называется коэффициентом светопропускания, который
показывает, какая часть световой энергии проходит через испытуемый раствор.
Коэффициент пропускания меняется от 1 до 0 или от 100% до 0.
Практика показывает, что
особенно часто нарушается основной закон фотоколориметрии при высоких
концентрациях растворов. Причиной этого является взаимодействие молекул
растворенного вещества друг с другом и с молекулами растворителя. Основной
закон фотоколориметрии нарушается не только при исследовании концентрированных
растворов. Причины, вызывающие подобные нарушения, разнообразны: влияние
электролитов, диссоциация веществ, изменение рН и др.
У одних окрашенных соединений
окраска возникает постепенно и через некоторое время как бы «созревает», у
других - образовавшаяся максимально интенсивная окраска постепенно бледнеет.
Поэтому перед фотоколориметрированием устанавливают интервал времени, в котором
окраска достигает максимальной величины и устойчива и течение времени,
достаточного для колориметрирования. Например, для определения по Гриссу
нитритов в мясных продуктах рекомендуется проводить колориметрирование через 15
мин после внесения реактивов в испытуемую вытяжку.
Образование окрашенного
соединения, его интенсивность зависят и от других факторов: количества и
концентрации применяемых реактивов, порядка их внесения, нестойкости окраски и
ее изменения во времени, вызванного изменением химического состава
растворенного вещества, образования даже небольшого количества других веществ,
имеющих собственную окраску и меняющих оттенок исследуемого раствора.
При проведении
фотоэлектроколориметрии не требуются стандартные растворы для сравнения с
исследуемым образцом. Достаточно приготовить одну серию растворов с известной и
различной концентрацией определяемого вещества, установить зависимость силы
фототока от концентрации стандартных растворов и построить график этой зависимости.
Пользуясь графиком зависимости силы тока от концентрации, определяют
концентрацию испытуемого раствора.
.2.4 Спектральный метод
Спектральный метод - метод,
основанный на измерении пропускания или поглощения света определенной длины
волны различными веществами. В основу спектроскопии положены общие законы,
устанавливающие соотношение между величиной поглощения или пропускания и
количеством поглощающего или пропускающего вещества.
Спектроскопию условно можно
подразделить на эмиссионную и абсорбционную. Эмиссионная спектроскопия
исследует излучательную способность вещества, абсорбционная спектроскопия -
поглотительную способность.
Разновидности спектрального
метода: абсорбционная, инфракрасная и атомно-абсорбционная спектроскопия.
Спектральный анализ используется для определения разнообразных органических
соединений, окрашенных и бесцветных растворов, а также минеральных элементов с
концентрацией 10-2 - 10-6 моля. Точность метода высокая [±(0,1 - 0,5) отн.%].
При спектральных методах используются сложные приборы (СФ-4, СФ-10 и др.).
С помощью абсорбционной
спектроскопии можно определить степень окисленности жира в различных
жиросодержащих продуктах (молоке, сливочном масле и т. п.), наличие пектиновых
и красящих веществ, фенольные соединения (в вине, чае, кофе, плодах и овощах),
кофеин, теобромин в чае и кофе, миоглобин в мясе, микроэлементы во всех
товарах; можно определять состав и количество макро- и микроэлементов,
содержание в пище витаминов А, К, В1, В2, В6, никотиновой кислоты, токоферолов,
каротина и др.
Внедрение спектрального анализа
в практику работы испытательных лабораторий открывает принципиально новые
возможности для определения веществ в многокомпонентных смесях, какими являются
многие потребительские товары.
.2.5 Хроматография
Хроматография - один из
наиболее эффективных методов разделения и анализа сложных смесей веществ. Этот
метод был открыт русским ученым М.С.Цветом в 1903 г. В основу метода положен
принцип различной сорбируемости компонентов смеси на выбранном сорбенте, т. е.
на распределении веществ между двумя не смешивающимися фазами. В настоящее
время он широко используется в различных областях химии и биологии.
Назначение хроматографического
метода - количественное и качественное определение веществ в пробах товаров,
специальным образом отобранных и отобранных. С помощью хроматографии изучают
химический состав пищевых продуктов, его динамику при хранении, природу и
содержание ароматических и красящих веществ, аминокислотный состав и др.
Хроматография - динамическое разделение смеси веществ с помощью сорбционных
методов. Способ хроматографии охватывает множество методов разделения, но общим
для всех них является то, что они основаны на распределении отдельных
соединений между двумя несмешивающимися фазами, одна из которых неподвижна и
омывается другой - подвижной. В роли подвижной фазы может выступать жидкость
или газ, а в качестве неподвижной - твердые тела или жидкость.
Достоинством метода является
высокая чувствительность, что позволяет обнаруживать качественно и определять
количественно вещества, содержащиеся в ничтожно малых количествах (иногда доли
мг%). Существует несколько классификаций хроматографических методов.
В зависимости от механизма
разделения веществ различают следующие виды хроматографии: адсорбционная -
основана на различной способности отдельных веществ адсорбироваться на тех или
иных сорбентах; распределительная - основана на различной растворимости
отдельных компонентов смеси в двух несмешивающихся жидкостях; ионообменная -
основана на различной способности разделяемых веществ к ионному обмену с тем
или иным ионитом; диффузионная - основана на разделении веществ по скорости
диффузии внутри сорбента.
В зависимости от выбранного
типа подвижной и неподвижной фаз различают хроматографию газовую, в которой
подвижной фазой является газ, и жидкостную - подвижная фаза жидкость.
По технике выполнения и по
видам вспомогательных средств различают хроматографию бумажную, колоночную,
тонкослойную, газовую и др.
Перечень физико-химических
показателей качества, которые можно определить с помощью хроматоргафического
метода, достаточно широкий: содержание свободных и связанных аминокислот,
органических кислот, углеводов, ароматических, красящих веществ, жирнокислотный
состав липидов, пестицидов, витаминов и др.
.2.6 Потенциометрический метод
Потенциометрический метод
основан на определении потенциала между электродом, насыщенным водородом, и
жидкостью, имеющей водородные ионы. Этот метод широко используется для
измерения рН, а по величине рН можно судить о свежести мяса и некоторых других
продуктов. В лабораторной практике часто применяется потенциометр ЛПУ-01 для
определения активности водородных ионов в водной среде в пределах рН от 2 до
14.
.2.7 Кондуктометрический метод
Кондуктометрический метод
основан на измерении электропроводности материалов. С помощью этого метода
определяют титруемую кислотность темноокрашенных продуктов (виноградных вин,
плодово-ягодных соков), так как в момент нейтрализации электропроводность
растворов резко снижается или полностью отсутствует. Кондуктометрический метод
измерения влажности сыпучих продуктов основан на зависимости между влажностью
продукта и его электрическим сопротивлением. Определение влажности
кондуктометрическим методом проводится специальными приборами -
электровлагомерами и сводится к измерению сопротивления сыпучего материала.
Этот метод измерения влажности применяется для таких пищевых продуктов, как
зерно, мука, сахар-песок, кофе и др.
.2.8 Реологические методы
Реологические методы - методы,
основанные на измерении различных веществ и материалов. Предназначены для
определения структурно-механических свойств товаров (вязкость, упругость,
эластичность и прочность), многие из которых характеризуют консистенцию.
Применяют в товароведных исследованиях для изучения структурно-механических
свойств пищевых продуктов. С их помощью определяют упруго-вязкие характеристики
теста, вязкость мясного фарша, твердость плодов и овощей, прочность
крахмального клейстера, консистенцию маргарина.
.2.9 Микроскопирование
Микроскопирование - метод,
основанный на использовании микроскопа в качестве измерительного прибора.
Применяются обычные биологические и электронные микроскопы, различающиеся
кратностью увеличения. Метод предназначен для определения строения тканей,
клеток и их органелл, а также видового и количественного составов
микроорганизмов. Наиболее широко микроскопирование применяется при определении
вида крахмальных зерен, наличия в продуктах примесей и микроорганизмов,
микроструктуры различных продовольственных и непродовольственных товаров. При
микробиологических исследованиях микроскопирование сочетается с регистрационным
методом (подсчет количества микроорганизмов).
.3 Химический метод
Этим методом устанавливают
химический состав пищевых продуктов, определяют показатели, характеризующие
качество сырья. С помощью химических методов можно судить об изменениях,
происходящих в пищевых продуктах при транспортировании, хранении и реализации.
Такие методы, как правило,
основаны на химических реакциях исследуемого вещества с определенными
реактивами с использованием приемов весового и объемного анализов.
Химическими методами определяют
содержание в пищевых продуктах минеральных веществ, воды, сахаров, жиров, а
также витаминов и других компонентов.
В товароведной практике эти
методы широко используют для установления соответствия химического состава
пищевых продуктов требованиям стандартов. Например, содержание влаги в пищевых
продуктах может быть установлено высушиванием, электрометрическим и другими
методами. Определение содержания Сахаров основано на их способности окисляться
в щелочной среде солями тяжелых металлов. Содержание минеральных веществ
определяют сжиганием и прокаливанием органической части продукта в муфельных
печах. Наиболее распространенным методом определения поваренной соли в продукте
является метод Мора, основанный на титровании иона хлора раствором
азотно-кислого серебра. Кислотность продуктов устанавливают титрованием
раствором едкой щелочи в присутствии индикатора, а в окрашенных растворах с
помощью рН-метра. Определение содержания витамина С основано на его способности
окисляться 2,6-дихлорфенолиндофенолом.
2. Материалы и методы исследования
Для написания экспериментальной части курсовой
работы использовались продукты:
· Молоко питьевое коровье стерилизованное
классическое Домик в деревне» (3,2%);
· Молоко питьевое УВТ-обработанное
стерилизованное жирное «Простоквашино» (6%);
· Томатная паста «Гастрономъ»;
· Натуральный растворимый
сублимированный кофе «Tchbo».
При определении качества продуктов использовались
физические и физико-химические методы оценки качества продовольственных
товаров.
Определение плотности молока ареометрическим
методом.
Плотность молока определяют лактоденсиметром при
температуре от +10 0С до +25 0С с приведением показаний прибора к стандартной
температуре +20 0С. На средней части прибора имеется шкала с ценой деления
0,001, обозначающая плотность, в верхней части прибора находится шкала
термометра.
мл молока нагревают на водяной бане до +40 0С и
выдерживают при этой температуре 5 минут, чтобы перевести жир в жидкое
состояние, после чего охлаждают до +20 ±2 0С. Лактоденсиметр градуирован при
+20 0С, поэтому при температуре молока, близкой к 20 0С, определение плотности
наиболее точно.
Во избежание образования пены тщательно перемешанную
пробу молока осторожно приливают по стенке в цилиндр, который в тот момент
следует держать в слегка наклоненном положении.
Цилиндр с молоком устанавливают на ровной
горизонтальной поверхности, и в него медленно погружают сухой и чистый
лактоденсиметр, после чего его оставляют в свободно плавающем состоянии.
Лактоденсиметр не должен касаться стенок цилиндра, расстояние между его
поверхностью и стенками цилиндра должно быть не менее 5 мм. Через 1 мин после
установления лактоденсиметра в неподвижном положении отсчитывают показания
температуры и плотности по шкалам прибора. Во время отсчета плотности глаз
должен находиться на уровне верхнего мениска молока.
Определение содержания экстрактивных веществ в
кофе рефрактометрическим методом.
Вкусовые достоинства кофе зависят от содержания
экстрактивных (растворимых в воде) веществ. Количество экстрактивных веществ в
кофе определяют рефрактометром в пересчете на сухое вещество.
Приборы и оборудование. Технические весы,
электрическая плитка, водяная баня, стеклянный стакан на 250 мл, пипетка,
коническая колба объемом 250 мл, мерная колба вместимостью 200 мл, термометр,
бумажный фильтр.
Порядок проведения анализа. Для приготовления
экстракта 10 г кофе помещают в стеклянный стакан на 250 мл и заливают 150 мл
дистиллированной воды. Кофе, залитый водой, доводят до кипения и кипятят в
течение 10 мин.
После кипячения содержимое стакана сливают через
воронку в мерную колбу на 200 мл. частички кофе, приставшие к стенкам стакана,
смывают в колбу дистиллированной водой. Мерную колбу вместе с содержимым
охлаждают проточной водой до 20 0С и доливают дистиллированной водой до метки.
Содержимое колбы взбалтывают и отстаивают в течение 2-3 мин. После этого часть
жидкости (75-100 мл) фильтруют через складчатый фильтр в сухую колбу или
стакан.
Перед началом измерений проверяют нуль-пункт
прибора, для чего на полированную плоскость измерительной призмы наносят 1-2
капли дистиллированной воды и устанавливают окуляр на резкость по шкале и
визирной линии сетки. После этого окуляр перемещают по шкале до тех пор, пока
визирная линия сетки не совместится с границей светотеней. При правильной
установки прибора на нуль-пункт граница светотени при 200С должна совместится с
нулевым делением шкалы сухих веществ и делением nD=1.33299
шкалы показателей преломления. В случае отклонения от этих значений прибор
необходимо установить ключом на нуль, для чего следует освободить пробу на
корпусе, через отверстие в корпусе на квадрат винта вставить ключ и вращением
его в ту или другую сторону совместить линию границы светотени с делением nD=1.33299,
нулевым делением шкалы сухих веществ и визирной линией сетки.
Установив прибор на нуль-пункт, поднимают
верхнюю камеру, вытирают соприкасающиеся плоскости призм досуха, сначала
фильтровальной бумагой, а затем неворсистой салфеткой. После этого на
поверхность измерительной призмы наносят 1-2 капли исследуемого раствора и
плавно опускают верхнюю камеру.
Количество экстрактивных веществ Х в процентах
вычисляют по формуле
Х = Б(А - В)104,
где Б - коэффициент, найденный экспериментальным
путем на основании параллельных определений экстрактивных веществ
рефрактометром (Б = 1,15);
В - показатель преломления воды;
А - показатель преломления исследуемого
раствора;
- коэффициент для получения результата
вычисления в целых единицах.
Определение сухих веществ рефрактометрическим
методом в томатной пасте.
Приборы и оборудование. Технические весы,
пипетка, воронка, бумажный фильтр, ложка, марля, фарфоровая чашка, колба 100
мл.
Порядок проведения анализа. Среднюю пробу
томатной пасты тщательно перемешивают, отбирают ложкой около 100 г продукта,
помещают на марлю или другую ткань, отжимают сок в фарфоровую чашку и фильтруют
его в колбочку через бумагу.
Установив прибор на нуль-пункт, поднимают
верхнюю камеру, вытирают соприкасающиеся плоскости призм досуха, сначала
фильтровальной бумагой, а затем неворсистой салфеткой. После этого на
поверхность измерительной призмы наносят 1-2 капли исследуемого раствора и
плавно опускают верхнюю камеру.
3. Результаты собственных исследований
Исследование плотности молока проводились в
соответствии с ГОСТ Р 52090-2003 «Молоко питьевое. Технические условия».
В результате исследования было установлено, что
плотность молока питьевого УВТ-обработанного стерилизованного жирного
«Простоквашино» и молока питьевого коровьего стерилизованного классического
«Домик в деревне» соответствует плотности молока, регламентированного ГОСТ Р
52090-2003 (Таблица 1).
Таблица 1 - Анализ плотности молока.
|
Наименование
молока
|
Плотность
молока, кг/м3
|
|
фактическое
|
По
ГОСТ Р 52090-2003
|
|
Молоко
питьевое УВТ-обработанное стерилизованное жирное «Простоквашино»
|
1024
|
Не менее 1024
|
|
Молоко
питьевое коровье стерилизованное классическое «Домик в деревне»
|
1028
|
Не менее 1027
|
Исследование экстрактивных веществ в кофе «Tchibo»
проводились в соответствие с ГОСТ 29148-97 «Кофе натуральный растворимый.
Технические условия».
Общее количество влаги и сухих веществ в кофе
берется за 100%. Исходя из таблицы (ПРИЛОЖЕНИЕ А), массовая доля сухих веществ
в кофе должна составлять не более 94%.
В результате расчетов и исследования было
установлено, что количество экстрактивных веществ в кофе натуральном
растворимом «Tchibo» составляет
93%, а следовательно соответствует нормам ГОСТ 29148-97 «Кофе натуральный
растворимый. Технические условия».
Исследование сухих веществ в томатной пасте
проводились в соответствии с ГОСТ 3343-89 «Продукты томатные концентрированные.
Общие технические условия» (Таблица 2).
Таблица 2 - Анализ сухих веществ в томатной
пасте.
|
Наименование
томатной пасты
|
Массовая
доля сухих веществ, %
|
|
Фактическая
|
По
ГОСТ 3343-89
|
По
маркировке
|
|
«Помидорка»
|
21
|
23-27
|
18-22
|
|
«Гастрономъ»
|
25
|
|
25
|
В результате исследования было установлено, что
томатная паста «Гастрономъ» соответствует нормам ГОСТ 3343-89 «Продукты
томатные концентрированные. Общие технические условия» и маркировке продукта, а
томатная паста «Помидорка» не соответствует нормам ГОСТ 3343-89 «Продукты
томатные концентрированные. Общие технические условия» и маркировке.
Выводы
В результате исследования было установлено:
. плотность молока питьевого УВТ-обработанного
стерилизованного жирного «Простоквашино» и молока питьевого коровьего
стерилизованного классического «Домик в деревне» соответствует плотности
молока, регламентированного ГОСТ Р 52090-2003.
. количество экстрактивных веществ в кофе
натуральном растворимом «Tchibo»
соответствует нормам ГОСТ 29148-97 «Кофе натуральный растворимый. Технические
условия».
. массовая доля сухих веществ в томатной пасте
«Помидорка» не соответствует ГОСТ 3343-89 «Продукты томатные концентрированные.
Общие технические условия» и маркировке. Массовая доля сухих веществ в томатной
пасте должна составлять 23-27%, а при измерениях получился меньший результат -
21%. Также маркировка по количеству сухих веществ на томатной пасте «Помидорка»
не соответствует ГОСТ 3343-89 «Продукты томатные концентрированные. Общие
технические условия».
Библиографический список
1. ГОСТ
3343-89 «Продукты томатные концентрированные. Общие технические условия». -
Введ. 01.01.91- М.: Изд-во стандартов,1991. - 9с.
2. ГОСТ
29148-97 «Кофе натуральный растворимый. Технические условия». - Введ. 01.01.99
- Минск: Изд-во стандартов, 1999. - 12с.
. ГОСТ
Р 52090-2003 «Молоко питьевое. Технические условия». - Введ. 30.06.03 - М.:
Изд-во стандартов, 2003. - 8с.
. Драмшева
С.Т. Теоретические основы товароведения продовольственных товаров: Учебник/
С.Т. Драмшева. - М.: Экономика, 1996.- 143 с.
. Исследование
продовольственных товаров: Учебное пособие для товаровед. фак. торг. вузов/
Боровикова Л.А., Гримм А.И., Дорофеев А.Л. и др. - М.: Экономика, 1980. - 336
с.
. Колесник
А.А., Елизарова Л.Г. Введение в товароведение продовольственных товаров. - М.:
Экономика, 1980.- 288 с.
. Колесник
А.Г., Елизарова Л.Г. Теоретические основы товароведения продовольственных
товаров: Учебник для вузов/ А.Г. Колесник, Л.Г. Елизарова. - М.: Экономика,
1990.
9. Елизарова
Л.Г., Стародубцева Т.В. Товароведение с основами стандартизации/ Л.Г.
Елизарова, Т.В. Стародубцева. - М.: Агропромиздат, 1990. - 130 с.
10. Жиряева
Е.В. Товароведение: Маркетинг для профессионалов/ Е.В. Жиряева. - СПб: Питер,
2002. - 416 с.