|
Наименование
показателей
|
Норма
|
|
Контактная
|
Олеум
|
|
Улучшенная
|
1 сорт
техническая
|
|
|
1 Массовая доля
моногидрата (H2SO4),%
|
92,5 - 94,0
|
Не менее 92,5
|
Не нормируется
|
|
2 Массовая доля
свободного серного ангидрида (SO3),%, не более
|
-
|
-
|
24
|
|
3 Массовая доля
железа (Fe),%, не более
|
0,006
|
0,02
|
0,006
|
|
4 Массовая доля
остатка после прокаливания,%, не более
|
0,02
|
0,05
|
0,02
|
|
5 Массовая доля
окислов азота (N2O3),%,
не более
|
0,00005
|
Не нормируется
|
0,0002
|
|
7 Массовая доля
мышьяка (As),%, не более
|
0,00008
|
Не нормируется
|
0,00008
|
|
8 Массовая доля
хлористых соединений (Cl),%, не
более
|
0,0001
|
Не нормируется
|
-
|
|
9 Массовая доля
свинца (Pb),%, не более
|
0,001
|
Не нормируется
|
0,0001
|
|
11 Цвет в см3
раствора сравнения, не более
|
1
|
6
|
Не нормируется
|
2. Физико-химические основы производства
Сгорание жидкой серы происходит по реакции:
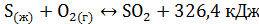 (2.1)
(2.1)
инкубационный период;
период интенсивного горения;
период догорания.
Капли серы в результате прогрева начинают испаряться, а пары
серы активно взаимодействовать с кислородом воздуха. Происходит процесс
диффузионного горения серы с образованием двуокиси серы (SO2).
Константу скорости реакции окисления серы до SO2 можно найти из уравнения
(1):
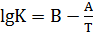 (2.2)
(2.2)
Значения коэффициентов для температур 850-1100˚С:
А=1875, В=2,92.
При высоких температурах скорость окисления серы больше, чем
скорость физических процессов испарения и диффузии. Поэтому общая скорость
реакции определяется процессами массо- и теплоотдачи (протекает в диффузионном
режиме).
Таким образом, необходимым условием полного и быстрого
сгорания серы является оптимальная подача воздуха к устью факела, мелкое и
равномерное распыление серы, турбулентность поток, высокая температура.
На практике получение высококонцентрированного сернистого
ангидрида ограничивается тем, что при температуре более 1300 ˚С быстро
разрушается футеровка печи и газоходов. Кроме того, в этих условиях образуются
окислы азота, которые являются нежелательной примесью. Поэтому сжигание серы
ведут при температуре 950 - 1120 ˚С.
Для обеспечения полного сгорания серы, процесс горения
необходимо вести с избыточной подачей воздуха в печь, чтоы обеспечить объемную
долю сернистого ангидрида (SO2) на выходе из печи в пределах 9,0 - 11,0%.
В производстве серной кислоты контактным методом окисление
сернистого ангидрида в серный идёт по реакции:
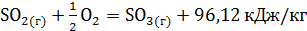 (2.3)
(2.3)
Происходит в присутствии катализатора. Для этого газ
пропускают через слой катализатора, находящегося в стационарном или
псевдоожиженном состоянии.
Реакция окисления обратима и степень окисления газа любого
состава строго определяется температурой и парциальными давлениями компонентов
реакции (1):
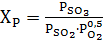 (2.4)
(2.4)
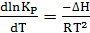 (2.5)
(2.5)
Под степенью превращения понимают отношение количества
окисленного SO2 к количеству его в исходной газовой смеси. Максимальная степень
превращения при заданных условиях достигается в условиях равновесия.
В производственных условиях весьма существенное значение
имеет скорость реакции окисления сернистого ангидрида в серный. От скорости
реакции зависит масса сернистого ангидрида, окисляющегося в единицу времени на
единицу массы катализатора, а, следовательно, расход катализатора, размеры
контактного аппарата и другие показатели процесса контактирования. Скорость
процесса контактного аппарата и другие показатели процесса контактирования.
Скорость процесса контактирования характеризуется константой скорости:
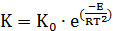 (2.6)
(2.6)
Где К0 - коэффициент, Е - энергия активации, R - универсальная газовая
постоянная, Т - абсолютная температура. Откуда следует, что с увеличением
температуры скорость реакции возрастает, а с уменьшением - уменьшается. Энергия
активации Е окисления сернистого ангидрида в серный в газовой фазе очень
велика, поэтому без катализатора реакция гомогенного окисления практически не
идет даже при высокой температуре. Однако в печи обжига очень небольшое
количество SO2 всё же окисляется до SO3. Катализатор же снижает энергию активации
реакции окисления SO2 и делает её возможной при приемлемых температурах.
В данной системе производства применяется ванадиевая
контактная масса. Активным компонентом ванадиевых контактных масс является
пятиокись ванадия (V2O5), которая в чистом виде слабоактивная в отношении реакции
окисления SO2. Активность её резко увеличивается при добавлении активаторов -
щелочных металлов, особенно калия.
Каталитическая активность, в случае добавки калия, связана с
образованием активного комплекса V2O5 ·K2O·2SO3, который при температуре процесса более 380 ˚С
находится в виде расплава, равномерно распределяется по всей поверхности носителя,
смачивая её. Из-за этой особенности возникает специфический механизм действия
катализатора. Катализаторы работают как абсорбционные, и процесс окисления
протекает внутри слоя активного компонента.
С течением времени активность ванадиевой контактной массы
уменьшается из-за различных причин. Это происходит вследствие засорения пор,
взаимодействия ванадия с компонентами газовой смеси - так называемыми ядами
(мышьяком, соединениями фтора), измельчения гранул катализатора из-за
температурных шоков при пусках-остановках и т.д. Поэтому для сохранения
приемлемой степени контактирования приходится постепенно, по ходу снижения
активности катализатора, повышать рабочую температуру газа на входе во все слои
контактного аппарата.
С уменьшением температуры и увеличением давления газа
значение равновесной степени превращения возрастает. Это обусловлено тем, что
реакция окисления SO2 протекает с выделением тепла и уменьшением общего числа молекул.
Следовательно, увеличение давления газов способствует прохождению данной реакции,
так как при увеличении давления объём газов уменьшается. Принцип Ле-Шателье
работает и в отношении выделяющегося тепла и температуры. Так как тепло
выделяется, то с повышением температуры реакция замедляется, и наоборот.
С увеличением степени превращения уменьшается содержание SO2 в отходящих газах. Такие
газы можно выводить в атмосферу без предварительной очистки. Целесообразно
обеспечивать степень превращения порядка 99,5.
Для повышения степени контактирования используется приём
«Двойное контактирование - двойная абсорбция».
Сущность двойного контактирования состоит в том, что
окисление SO2 (контактирование) ведут в две стадии. На первой стадии
обеспечивается степень превращения не менее 92%. Затем из реакционной смеси
выделяют SO3 с целью увеличения скорости процесса, после чего проводят вторую
стадию контактирования, в которой достигается степень превращения 95% от
оставшегося SO2. Общая степень превращения составляет не менее 99,5%. Улучшение
контактирования на второй ступени объясняется тем, что при удалении SO3 равновесие реакции
смещается вправо, т.е. если продукты реакции удалить, то реакция идёт лучше.
Также реакция идёт лучше, если увеличить концентрацию действующих веществ.
Последней стадией процесса производства серной кислоты
контактным методом является абсорбция серного ангидрида.
Газообразный триоксид серы наиболее полно абсорбируется
,3%-ной кислотой, при меньшей или большей концентрации H2SO4 способность её поглощать
SO3 ухудшается. Над
кислотой, содержащей менее 98,3% H2SO4, в газовой фазе находятся пары воды, над
кислотой содержащей более 98,3% H2SO4 - триоксид серы. Полная абсорбция SO3 в значительной степени
зависит от температуры серной кислоты: чем ниже температура, тем выше степень
абсорбции.
При обработке полученной газовой смеси, содержащей SO3, кислотой концентрацией
менее 98,3% H2SO4 часть триоксида серы соединяется с парами воды, образуя туман
серной кислоты, который плохо улавливается в обычной абсорбционной аппаратуре,
и в основном уносится отходящими газами в атмосферу. При этом на выходе из
выхлопной трубы виден туман. Чем ниже концентрация серной кислоты и выше её
температура, тем больше выделяется из неё паров воды, образуется больше тумана
и выше потери менее SO3. При обработке контактного газа кислотой, концентрация которой
более 98,3% H2SO4, триоксид серы поглощается не полностью, так как из этой кислоты
выделяется SO3. В этом случае отходящие газы также уносят в атмосферу часть
триоксида серы, который с влагой воздуха образует туман серной кислоты.
Если концентрация серной кислоты выше 98,3%, то при
соприкосновении её с серным ангидридом протекает обычный процесс абсорбции. В
этом случае справедлива формула:
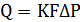 (2.7)
(2.7)
Где Q-количество абсорбируемого SO3, кг/ч; К - коэффициент
абсорбции кг/(м2· ч · Па); F - поверхность насадки; ∆P - движущая сила
абсорбции.
Движущая сила абсорбции выражается формулой:
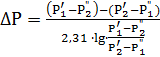 (2.8)
(2.8)
Где 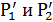 - парциальное давление абсорбируемого газа в начале
и конце процесса, Па;
- парциальное давление абсорбируемого газа в начале
и конце процесса, Па; 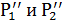 - равновесное давление абсорбируемого газа над
жидкостью при входе и выходе жидкости, Па.
- равновесное давление абсорбируемого газа над
жидкостью при входе и выходе жидкости, Па.
Коэффициент абсорбции при поглощении SO3 серной кислотой
рассчитывают по уравнению:
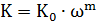 (2.9)
(2.9)
где K0 - константа, численно равная коэффициенту
абсорбции при скорости газа 1м/с; ω - фиктивная скорость газа в
башне, м/с; m
- коэффициент, равный 0,5 при ламинарном потоке и 0,8 при турбулентном потоке.
При извлечении газообразного SO3 из газовой смеси
одновременно с физическим процессом растворения газа в жидкости протекает
химическая реакция - взаимодействие поглощенного серного ангидрида SO3 с водой, содержащейся в
кислоте:
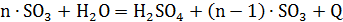 (2.10)
(2.10)
В зависимости от количественного соотношения воды и SO3 получают серную кислоту
с различной долей моногидрата. При n > 1 образуется олеум, при n = 1 моногидрат (массовая
доля H2SO4 100%), а при
n < 1 - водный раствор серной кислоты.
После абсорбции газовая смесь вместе с непоглощенным серным
ангидридом удаляется в атмосферу. Для уменьшения потерь SO3 с отходящими газами его
поглощение в абсорбционном отделении должно быть более полным.
Так как в процессе поглощения SO3 выделяется тепло, то
кислоту, которая используется для абсорбции серного ангидрида необходимо
охлаждать. Поглощение серного ангидрида производится в башнях (абсорберах).
Полнота абсорбции зависит от массовой доли моногидрата в серной кислоте и
температуры поглощающей кислоты, от плотности орошения абсорберов. Теоретически
серный ангидрид наиболее полно абсорбируется серной кислотой с массовой долей
98,3%. При массовой доле моногидрата в серной кислоте меньше или больше 98,3%
способность её поглощать серный ангидрид ухудшается. Это объясняется тем, что
над кислотой с массовой долей H2SO4 меньше 98,3% находятся, главным образом, пары
воды и незначительная часть паров серной кислоты, а над кислотой с массовой
долей H2SO4 более 98,3% увеличивается содержание серного ангидрида. При
обработке газовой смеси кислотой с массовой долей моногидрата H2SO4 менее 98,3% часть
серного ангидрида соединяется с парами воды, образуя туман серной кислоты,
который практически не улавливается в процессе поглощения и уносится с
выхлопными газами из абсорберов. А при обработке газа кислотой с массовой долей
моногидрата H2SO4 более 98,3% серный ангидрид поглощается не полностью и уносится с
выхлопными газами из абсорберов, образуя туман серной кислоты на выходе из
абсорбера.
Степень абсорбции триоксида серы в моногидратном абсорбере
зависит от концентрации и температуры орошающей кислоты. Эта зависимость имеет
вид кривой с максимумом в точке, соответствующей концентрации кислоты примерно
98,3%. Максимальная степень абсорбции достигается при наименьшей температуре
кислоты.
3. Описание технологической схемы
производства
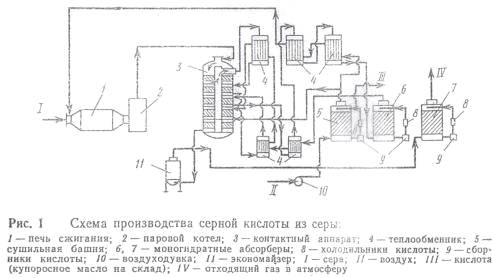
На рис.1 представлена схема производства серной кислоты по
способу двойного контактирования (ДК) из природной или газовой серы, не
содержащей контактных ядов (соединений мышьяка, селена и др.)
Расплавленная и отфильтрованная от минеральных примесей сера
сжигается в потоке предварительно высушенного воздуха. Полученный сернистый газ
с массовой долей около 10% SO2 с температурой свыше 1000 ˚С охлаждается в
паровом котле до 420 ˚С и поступает в пятислойный контактный аппарат. В
трёх верхних слоях катализатора происходит окисление диоксида серы примерно на
60% в каждом и адиабатическое повышение температуры по уравнениям 2.1 (рис. 2).
Охлаждением газа в теплообменниках между полками ступенчатое приближение к
оптимальной кривой. На выходе из третьего слоя достигается степень превращения SO2 в SO3 на 93-95%, при этом
адиабата приближается к равновесной кривой и скорость реакции сильно
уменьшается. Поэтому в способе двойного контактирования (ДК) газ после третьего
слоя поступает на абсорбцию, триоксид серы поглощается практически полностью;
равновесие не лимитирует процесс; соотношение О2: SO2 достигает 10: 1 и в
четвертом слое содержащийся в газе диоксид серы (около 0,5%) окисляется на
90-95%. На некоторых заводах ограничивались четырьмя слоями.
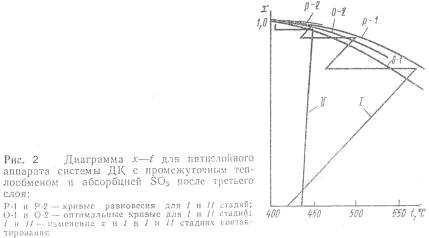
По схеме же, представленной на рис. 2, газ после четвертого
слоя охлаждается добавкой холодного воздуха, происходит еще пятый слой, после
которого общая степень превращения составляет 99,5% или выше. Одного и такая
степень превращения не полностью удовлетворяет современным требованиям по
охране природы.
Абсорбция триоксида серы проводится в башнях с насадкой,
орошаемых раствором кислоты, которая содержит 98,3 - 98,6% H2SO4. Такая кислота в технике
называется моногидратом. Она, являясь азеотропной смесью, обладает наилучшей
поглотительной способностью. Степень абсорбции свыше 99%. При небольшом
разбавлении кислоты над нею появляются водяные пары, образующие с SO3 мельчайшие капельки
сернокислотного тумана, которые плохо улавливаются в башнях с насадкой. Степень
абсорбции резко снижается. Для улучшения абсорбции кислоту, поступающую в
абсорберы, охлаждают в трубчатых холодильниках воздухом или водой до 60-70 ˚С.
В абсорберах и сушильной башне количество циркулирующей орошающей кислоты во
много раз больше, чем необходимо для поглощения SO3, и определяется тепловым
балансом.
4. Материальный баланс печного отделения
Рассчитаем газовую производительность по серной кислоте.
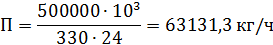
Где 330 - число рабочих дней в году;
- часов в сутках.
Составим балансовое уравнение печного отделения.
X1 63131,3
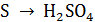
32 98
И рассчитаем теоретическое количество серы для получения
этого количества серной кислоты.
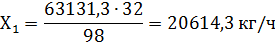
Где 32 - молярная масса серы, кг/кмоль
- мольная масса серной кислоты, кг/кмоль.
С учетом содержания серы CS=99,5%, степени окисления
SO2 в SO3 99,85% и степени
абсорбции 99,9% требуется технической серы.
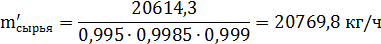
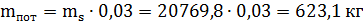 .
.
Где 0,03 - потери серы в печном отделении с учетом
содержания серы в сырье 99,5%, в печи ожигается.
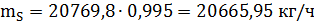
С учетом потерь серы в печном отделении требуется сырья
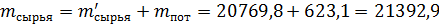
Количество воздуха, необходимого для окисления серы:
20665,95 X1 X2
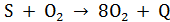 (4.1)
(4.1)
22,4 22,4
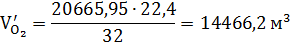
Где 22,4 - мольный объем газа, кг/м.
С учётом избытка воздуха α =
1,4, в печь
поступает:
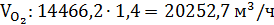
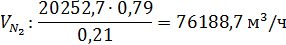
Где 0,21и 0,79 - содержание кислорода и азота в воздухе
(об. доли).
Всего поступает воздуха:
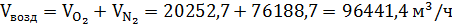
По реакции (4.1) расходуется кислорода:
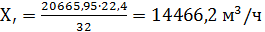 или
или
По стехиометрии образуется такое же количество SO2:
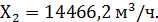
В газовой смеси остаётся непрореагировавшего кислорода:
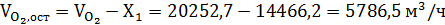
Данные расчетов сводим в табл. 2.
Таблица 2. Материальный баланс печного отделения
|
Приход
|
Расход
|
|
Статья
|
кг/ч
|
м3/ч
|
%, об.
|
Статья
|
кг/ч
|
м3/ч
|
%, об.
|
|
1.Сера, в т.ч. · Сера · As · H2O · Зола 2.Воздух, в т.ч. · Кислород · Азот
|
21392,9 21285,9 32,1 53,5 21,4 124168,3 28932,4
95235,9
|
96441,4
20252,7 76188,7
|
21 79
|
1.Сернистый
газ, в т.ч. · SO2
· O2
· N2
· As
· H2O
2.Потери 3.Зола
|
144917,3 41332,0 8266,4 95235,9 31,1 51,9 623,1
20,8
|
96516,7 14466,2 5786,5 76188,7 10,7 64,6
|
15,0 6,0 78,9
0,01 0,09
|
|
Итого
|
145561,2
|
96441,4
|
100
|
Итого
|
145561,2
|
96516,7
|
100
|
5. Тепловой баланс печного отделения
Тепловой баланс печи для сжигания серы
Реакция сгорания серы с образовавшимся оксидом серы (II) является
экзотермической.
Sг+O2(г) = SO2 + 348 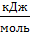 (5.1)
(5.1)
Так как при адиабатическом сжигании серы тепло расходуется на
испарение серы (теплота испарения Qисп=288 кДж/кг) и нагревания печного газа,
рассчитаем температуру печного газа на выходе из печи на входе в котёл-утилизатор
t1. Рассчитываем статьи
прихода и расхода, приняв Qпот=5%Qприх.
Температура серы на входе в печь - 130 ˚С, воздуха - 50 ˚С.
Приход:
. Тепло, вносимое серой
Q1=mS · CS ·
t = 20769,8 · 0,80 · 130 = 2160 · 103 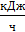
Где CS = 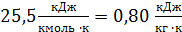 - теплоёмкость серы при t = 130 ˚C
- теплоёмкость серы при t = 130 ˚C
. Тепло, вносимое воздухом
Q2 = mB · CB · t
= 124168,3 · 1,01 · 50 = 6270 · 103 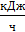
Где CB = 1,01 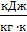 - теплоёмкость воздуха
при t
= 50 ˚C.
- теплоёмкость воздуха
при t
= 50 ˚C.
. Тепло реакции окисления серы
Q3 = mS · qx.p.
= 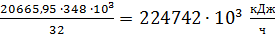
Находим Qприх = Q1 + Q2 + Q3 = 2160 · 103 + 6270 · 103
+ 224742 · 103 = 233172 · 103 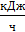
Расход тепла:
. Тепло, расходуемое на нагрев и испарение серы
Где СS = 0,93 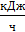 - теплоёмкость серы при tcp = 287,5 ˚C
- теплоёмкость серы при tcp = 287,5 ˚C
. Тепло, уносимое диоксидом серы
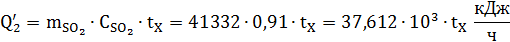
Где 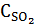 = 58,2
= 58,2 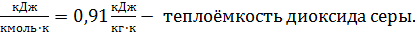
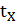 - температура отходящих газов.
- температура отходящих газов.
. Тепло, уносимое кислородом
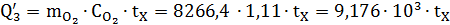
Где 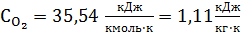 - теплоёмкость кислорода.
- теплоёмкость кислорода.
. Тепло, уносимое азотом
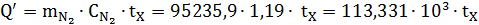
Где 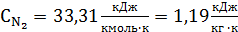 - теплоёмкость азота.
- теплоёмкость азота.
. Теплопотери принимаем равными 5% от Qприх:
Qпот = 0,05 · Qприх = 0,05 · 233172 · 103
= 6659 · 103 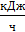
Находим
Qрасх=37,612 · 103 · tx + 9,176 · 103
· tx + 113,331 · 103 +
12006 · 103 ++ 6659 ·103 = 160, 119 · 103 · tx + 18665 · 103,
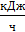
Температуру печного газа находим из уравнения теплового
баланса:
Qприх = Qрасх
· 103 = 160,119 · 103 · tx + 18665 · 103
Находим tx = 1339,7 ˚C
Данные расчетов сводим в табл. 3.
Таблица 3. Тепловой баланс серной печи
|
Приход
|
Расход
|
|
Статья
|
МДж/ч
|
%
|
Статья
|
МДж/ч
|
%
|
|
1.Тепло,
вносимое ·
Серой Q1 · Воздухом Q2 2.Тепло экзотермической реакции Q3
|
2160
6270 224742
|
0,93
2,69 96,38
|
1.Тепло, на
нагрев и Q1 испарения серы. 2.Тепло, уносимое · SO2 · O2 · N2 3.Теплопотери
|
12006 214512
50389 12293 151830 6659
|
5,15 21,61
5,27 65,11 2,86
|
|
Итого
|
233172
|
100
|
Итого
|
233177
|
100
|
Тепловой баланс котла-утилизатора
В котле-утилизаторе печные газы охлаждаются от t = 1339,7 ˚C
до 400 ˚С. В котёл подаётся с t =30 ˚C и образуется перегретый пар
с
t =350 ˚C (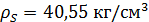 ).
).
Приход:
тепло, вносимое печным газом
Q1 = 214512 · 103 кДж/ч
тепло, вносимое водой
Q2 = m · Cв · tн = m · 4,19 · 30 = 125 ,7 · m 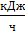
Qприх = Q1 + Q2 = 214512 · 103 + 125,7· m
Расход:
. Тепло, уносимое печными газом при t = 400 ˚С.
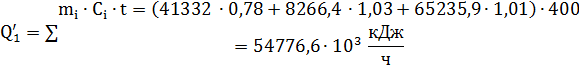
Где 0,78; 1,03; 1,01 - теплоёмкости оксида серы, кислорода,
азота при
t = 400 ˚C, 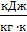 .
.
. Тепло, затрачиваемое на нагрев воды
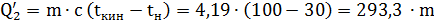 , кДж/ч
, кДж/ч
Где С = 4,19 кДж/кг - теплоёмкость воды.
. Тепло, затрачиваемое на испарение воды
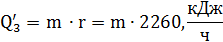
Где r = 2260 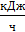 - теплота парообразования
- теплота парообразования
. Тепло, уносимое перегретым паром при t = 250 ˚C.
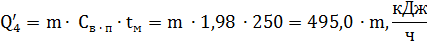
Где 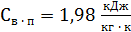 - теплоёмкость взятого пара при t = 250 ◦C.
- теплоёмкость взятого пара при t = 250 ◦C.
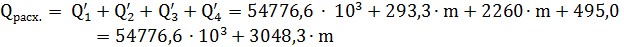
Составляем уравнение теплового баланса котла-утилизатора
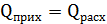
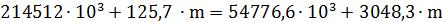
Находим 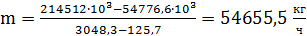
Данные расчетов сводим в табл. 4
|
Приход
|
Расход
|
|
Статья
|
МДж/ч
|
%
|
Статья
|
МДж/ч
|
%
|
|
1.Тепло,
вносимое печным газом Q1 2. Тепло, вносимое водой
|
214512 6870
|
96,9 3,1
|
1.Тепло, уносимое
печным газом 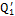 2. Тепло, затраченное на нагрев воды 2. Тепло, затраченное на нагрев воды 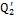 3. Тепло затраченное на испарение воды
4. Тепло, уносимое перегретым паром 3. Тепло затраченное на испарение воды
4. Тепло, уносимое перегретым паром
|
54776,6
16030,5 123521,4 27054,4
|
24,7 7,2
55,8 12,3
|
|
Итого
|
221382
|
100
|
Итого
|
221382,9
|
100
|
Заключение
В курсовой работе приведены характеристики сырья для
производства серной кислоты, физико-химические свойства серы и серной кислоты,
требования к готовому продукту.
Рассмотрены закономерности окисления серы, каталитического
окисления диоксида серы, абсорбции триоксида серы и влияние технологических
параметров на протекание химических реакций.
Рассчитан материальный баланс печи для сжигания серы;
рассчитано количество воздуха, необходимого для окисления серы; рассчитан
состав печного газа. Концентрация диоксида серы в печном газе - 15% (об.)
На основе тепловых расчётов печи для сжигания серы рассчитаны
температура печных газов и расход охлаждающей воды в котле-утилизаторе для
охлаждения печных газов до температуры 400 ˚С.
Литература
1. Б.Т.
Васильев, М.И. Отвачина. Технология серной кислоты. - М.: Химия, 2014. - 384 с.
2. Основы
химической технологии. /И.П. Мухлёнов, А.Е. Торштейн, Е.С. Тумаркина. - М.:
Высш. Шк., 2011 - 463 с.
. Расчеты
по технологии неорганических веществ. /Под ред. М.Е. Позина - Л.: Химия, 2008 - 496 с.
. Краткий
справочник физико-химических величин. /Под ред. К.П. Мищенко и А.А Равдена. -
Л.: Химия, 2012. - 200 с.