Розробка технології виплавки жароміцної сталі в дуговій печі
Розробка
технології виплавки жароміцної сталі в дуговій печі
Зміст
Реферат
Вступ
. Вплив окремих елементів на властивості сталі
2. Вибір футерівки для плавильного агрегату
. Фізико-хімічні основи виплавки сталі в електропечах
3.1 Окислення вуглецю
3.2 Окислення і відновлення мангану
3.3 Окиснення і відновлення силіцію
.4 Окислення і відновлення хрому
.5 Окислення вольфраму
3.6 Окиснення ванадію
3.7 Розкислення сталі
4. Підготовка шихти до завалки
5. Шихтові матеріали та їх підготовка
. Розрахунок шихти
. Завалка шихти і окислювальний період плавки
. Відновлювальний період
. Уведення легуючих додатків і модифікаторів
. Технологічна інструкція
. Техніка безпеки
Список використаних джерел
Вступ
В електрометалургії для виробництва
сталі використовують дугові, вакуумно-дугові, плазмово-дугові та індукційні
печі, печі опору й електрошлакового переплаву, електронно-променеві установки.
Основа роботи електроплавильних печей - теплова дія електричного струму.
У електоропечі можна отримувати
леговану сталь з низьким вмістом сірки і фосфору, неметалевих включень, при
цьому втрати легуючих елементів значно менше. У процесі електроплавки можна
точно регулювати температуру металу та його склад, виплавляти сплави майже
будь-якого складу.
Електросталь, призначена для
подальшого переділу, виплавляється головним чином в дугових печах з основною
футеровкою. Важливі переваги цих печей перед іншими сталеплавильними агрегатами
(можливість нагріву металу до високих температур за рахунок електричної дуги, відновна
атмосфера в печі, менший чад легуючих елементів, високоосновні шлаки, що
забезпечують істотне зниження вмісту сірки) зумовили їх використання для
виробництва легованих високоякісних сталей - корозійностійких, інструментальних
(в тому числі швидкорізальних), конструкційних, електротехнічних, жароміцних
тощо, а також сплавів на нікелевій основі. Світова тенденція розвитку плавки
електродуги - збільшення ємкості одиничного агрегату до 200-400 т, питомої
потужності трансформатора до 500-600 і більше КВА/т, спеціалізація агрегатів (у
одних - тільки розплавлення, в інших -рафінування і легування), високий рівень
автоматизації.
Недоліками електропечей в порівнянні
з кисневими конвертерами є менша продуктивність при однаковій місткості і
труднощі переробки великих кількостей рідкого чавуну.
.
Вплив окремих елементів на властивості сталі
Силіцій - гарний розкислювач, тому
його сплави використовують при виробництві сталей багатьох марок. Витрати
феросиліцію досягають ≈ 0,65 % від випуску сталі. Звичайно в сталях
міститься 0,12 - 0,35 % Si, в високолегованих сталях його вміст доходить до 2 -
3 % і більше. В трансформаторній сталі силіцій знижує втрати на гістерезис.
Сумісно с іншими елементами, особливо хромом, силіцій додають у
інструментальні, корозійно- і жаростійкі, ресорно-пружинні та інші сталі.
Введення в конструкційну сталь до 2% Si підвищує її твердість, міцнісь, межі
пружності і плинності. В ливарному виробництві використовується 30 - 40 %
феросиліцію.
Манган активно з’єднується із киснем
і сіркою, тому він є розкислювачем і десульфуратором рідкої сталі. Як легуючий
додаток манган подрібнює структуру сталі і збільшує прогартованість. При
збільшенні вмісту мангану до 7 % збільшуються межа плинності і межа міцності.
При вмісту мангану більше 10 % дуже зростає опір сталі атмосферній корозії.
Інструментальні сталі містять до 0,4 % Mn, конструкційні - до 0,5% Mn, леговані
манганом - від 0,8 до 28 % Mn. Широко відома зносостійка високоманганова сталь
110Г13 (12 - 14% Mn, 1,1 - 1,3 % С), яка використовується для виготовлення
рабочих органів землеройних машин, помельно- подрібнюючого обладнання. При
виробництві нержавкої сталі манган замінює дефіцитний нікель.
Нікель підвищує прогартованість,
пластичні властивості, жароміцність, корозійну стійкість сталі.
.
Вибір футерівки для плавильного агрегату
Існують два види футерівок для
електричних печей: основна і кисла. Кисла футерівка має значно більшу
стійкість, ніж основна. Не всі марки сталі можна виплавляти в печі з кислою
футерівкою, в склад якої входить велика кількість оксиду силіцію. В кислій
електропечі не треба виплавляти сталі, в склад яких входять елементи,
спорідненість яких до кисню вища за силіцій, а також велика кількість мангану.
Основну футерівку печі слід
застосувати для виплавки сталей з високим вмістом хрому, марганцю, титану,
цирконію, алюмінію, які в кислій печі інтенсивно згорають і руйнують футеровку.
Виплавляючи високоякісні вуглецеві і
леговані сталі ми використовуємо основну футерівку в дуговій печі.
.
Фізико-хімічні основи виплавки сталі в електропечах
3.1 Окислення вуглецю
жароміцна сталь дугова піч
Залізна руда, що завантажується в
піч, розчиняється в шлаку і, таким чином, збільшує вміст окислу заліза в шлаку.
Окис заліза в шлаку може також утворитися в результаті взаємодії окису заліза
шлаку з киснем газової фази. При взаємодії шлаку з корольками металу, а також
на поверхні зіткнення металу з шлаком окис заліза перетворюється на закис
заліза по реакції:
(Fe2О3) + [Fе]
= 3(FеO) (3.1)
Закис заліза, що утворюється,
частково розчиняється в сталі, підвищуючи в ній вміст кисню. Частина
розчиненого кисню може взаємодіяти в об'ємі рідкого металу і у вигляді окислу
вуглецю переходити в спливаючі бульбашки і разом з бульбашками в газову фазу.
Проте у такий спосіб може віддалитися з металу лише невелика кількість вуглецю
і кисню, оскільки тільки ті атоми кисню і вуглецю, які приходять у безпосереднє
зіткнення із спливаючими бульбашками або знаходяться на дуже близькій відстані
від них, можуть переходити в бульбашки. Атоми кисню і вуглецю, що не
знаходяться в безпосередній близькості до бульбашок, практично не можуть
переходити в бульбашки, оскільки дифузія елементів і оксидів відбувається
повільно, а бульбашки спливають з великою швидкістю. Тому основна маса кисню,
що поступила з шлаку в метал, переноситься потоками металу, що перемішується, в
нижні шари. Таким чином, в усьому об'ємі металу вміст кисню виявляється вище за
значення, що відповідають рівновазі з вуглецем і бульбашками окиси вуглецю.
Утворення бульбашок оксиду вуглецю
відбувається на поверхні розділу метал - подина. Із-за шорсткості і пористості
подини, а також поганої змочуваності його металом в ньому утворюються
поглиблення незаповнені металом. У ці поглиблення виділяється з рідкого металу
оксид вуглецю, де і утворюються бульбашки. На поверхні розділу рідкого металу з
бульбашками відбувається утворення нових молекул оксиду вуглецю і виділення їх
в бульбашки. При цьому розміри бульбашок збільшуються. Потім вони відриваються
від подини і спливають на поверхню металу. В процесі вспли-вання об'єм
бульбашок збільшується. Це відбувається як внаслідок зменшення тиску, під яким
знаходиться бульбашка, так і внаслідок того, що в бульбашку переходить деяка
додаткова кількість оксиду вуглецю з об'єму рідкого металу.
При додаванні у ванну великих шматків
залізної руди останні занурюються в шлак і частково в метал. При зіткненні
твердих шматків залізної руди з рідким металом бульбашки оксиду вуглецю можуть
утворюватися на шорсткій поверхні шматків руди.
Схема протікання процесу окислення
зображена на рис.3.1.
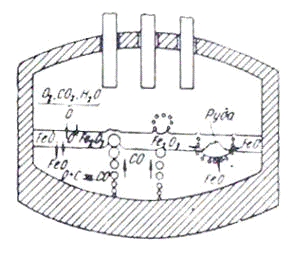
Рисунок 3.1 - Схема протікання
процесу окислення вуглецю в електропечі
Взаємодія між вуглецем і киснем і
виділення оксиду вуглецю, що утворився, хоча і не досягає стану рівноваги,
протікає з великою швидкістю і не лімітує процесу окислення вуглецю.
Іншою причиною, що впливає на
пониження швидкості окислення вуглецю при низьких концентраціях, є зменшення
пористості поверхні подини. При низьких концентраціях вуглецю і відповідно
високих концентраціях кисню активність кисню в металі і закисі заліза в шлаку
сильно зростає. Це викликає перехід великих кількостей закису заліза з металу у
футерівку подини. Поверхня подини покривається глазур'ю, пори в ній зникають,
що перешкоджає виникненню бульбашок на поверхні розділу метал - подина.
.2 Окислення і відновлення
мангану
Реакція [Fe] + (MnО) = (FeO) + [Mn]
може протікати також між металом і основним шлаком. У основному шлаку
активність закису заліза і закису марганцю залежить не лише від концентрації
цих оксидів, але і від основності шлаку. Умови рівноваги реакції окислення
марганцю основним шлаком визначаються наступними рівняннями:
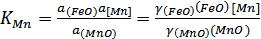
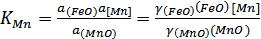 (3.2)
(3.2)
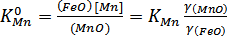
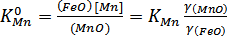 (3.3)
(3.3)
Для практичних
розрахунків зручніше користуватися рівнянням (3.3), оскільки воно безпосередньо
виражає залежність між концентраціями реагуючих речовин. Проте 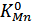
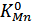 не є однією і тією ж
величиною для різних шлаків. Величини
не є однією і тією ж
величиною для різних шлаків. Величини 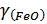
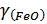 та
та 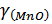
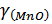 залежать від складу
шлаку, тому
залежать від складу
шлаку, тому 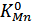
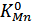 також залежить від
складу шлаку. Якщо шлакова фаза складається тільки із закису заліза і закису
марганцю, то залежність від температури визначається з наступного рівняння:
також залежить від
складу шлаку. Якщо шлакова фаза складається тільки із закису заліза і закису
марганцю, то залежність від температури визначається з наступного рівняння:
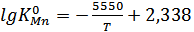
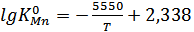 (3.4)
(3.4)
У шлаках, що містять
разом із закисом заліза і закисом марганцю також кремнезем і окис кальцію, 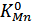
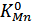 залежить від основності
шлаку. Ця залежність для температури близько 1600° З була встановлена Маурером
і Бішофом (рис.3.2).
залежить від основності
шлаку. Ця залежність для температури близько 1600° З була встановлена Маурером
і Бішофом (рис.3.2).
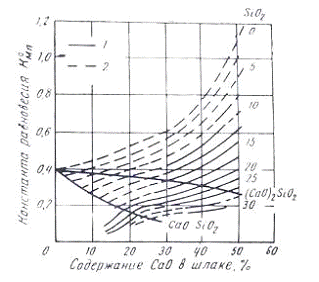
Рисунок 3.2 - Залежність
константи рівноваги реакції окиснення мангану (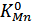
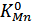 ) від вмісту кремнезему
та окису кальцію у шлаку
) від вмісту кремнезему
та окису кальцію у шлаку
Рівняння (3.4) показує,
що при температурі близько 1600° С пониження температури на 50° С викликає
зменшення 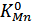
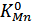 в 1,2 рази, а
збільшення температури викликає таке ж збільшення
в 1,2 рази, а
збільшення температури викликає таке ж збільшення 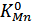
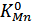 . Користуючись цим
коефіцієнтом і кривими рис.3.2, можна приблизно визначати величину
. Користуючись цим
коефіцієнтом і кривими рис.3.2, можна приблизно визначати величину 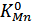
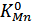 для основних шлаків при
різних температурах.
для основних шлаків при
різних температурах.
Окиснення мрганцю в
основній печі протікає менш повно, ніж в кислій.
3.3
Окиснення і відновлення силіцію
Основні шлаки містять в три-чотири
рази менше кремнезему, ніж кислі. Крім того, кремнезем в основних шлаках
пов'язаний з вапном в міцні силікати. Тому активність кремнезему в основних
шлаках у багато разів менше, ніж в кислих.
Активність закису заліза в основних
шлаках більша, ніж в кислих.
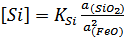
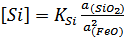 (3.5)
(3.5)
Внаслідок низької
активності кремнезему і високої активності закису заліза рівновага між металом
і шлаком встановлюється при дуже низькому вмісті кремнію в металі. Практично
можна вважати, що увесь кремній, що міститься в шихті, окислюється вже в період
плавлення. Кремній в окислювальний період плавки не відновлюється. У відновний
період плавки, коли зміст закису заліза в шлаку знижується до 0,5%менш, кремній
іноді відновлюється до 0,1-0,15%.
3.4 Окислення і відновлення хрому
Хром з киснем утворює наступні
оксиди: СrО, Сr2О3 і СrО3.
Найбільш стійким з'єднанням є Сr2О3.
У твердих шлаках хром знаходиться у вигляді окислу(Сr2О3).
На підставі результатів досліджень, що відносяться до рівноваги реакції
окислення хрому, можна вважати, що в розплавлених кислих шлаках хром
знаходиться у вигляді закису хрому, а в основних шлаках разом з СrО існує
значна кількість Сr2О3. Хром окислюється по наступній
реакції:
[Сr] + (FeО) = (СrО) + [Fе] (3.6)
У основних шлаках активності закису
заліза і закису хрому не пропорційні концентраціям цих окислів. Тому в рівняння
константи рівноваги повинні входити коефіцієнти активності:
де 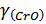
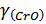 та
та 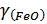
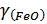 - коефіцієнти
активності відповідних речовин, розчинених у шлаку.
- коефіцієнти
активності відповідних речовин, розчинених у шлаку.
У високоосновних шлаках
значна частина заліза знаходиться у вигляді окислу заліза, хімічно пов'язаного
з окислом кальцію. Таким чином, не все залізо в шлаку знаходиться у вигляді
закису. Частина оксидів заліза в шлаку знаходиться в неактивній формі. Тому
коефіцієнт активності закису заліза змінюється зі зміною основності шлаку.
Аналогічної зміни можна чекати також для оксидів хрому. У основних шлаках
частина хрому знаходиться, ймовірно, у вигляді окислу хрому, пов'язаного з
окислом кальцію, що впливає на коефіцієнт активності закису хрому.
Дані, що характеризують
розподіл хрому між шлаком і металом в основній мартенівській печі у кінці
періоду кипіння зображені на рис.3.3.
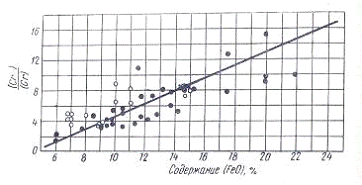
Рисунок 3.3 - Залежність
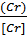
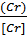 від вмісту (FeO) в
шлаку
від вмісту (FeO) в
шлаку
Досвідчені дані рис.3.3
відповідають приблизно такому рівнянню:
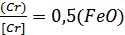
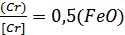 (3.8) (11,41)
(3.8) (11,41)
Умови для окислення
хрому в основній електричній печі приблизно такі ж, як і в мартенівській печі,
тому рівнянням(3.8) можна користуватися для визначення співвідношення між 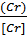
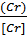 та (FеО), що має місце
у кінці окислювального періоду плавки сталі в основній електричній печі, коли
температура металу дорівнює 1600-1640°С.
та (FеО), що має місце
у кінці окислювального періоду плавки сталі в основній електричній печі, коли
температура металу дорівнює 1600-1640°С.
Температура робить
істотний вплив на процес окислення хрому. Пониження температури на 100°С
підвищує коефіцієнт розподілу хрому в 2-3 рази.
3.5 Окислення вольфраму
Вольфрам і кисень утворюють оксиди
WO2 і WO3. Вольфрам окислюється закисом заліза по
наступній реакції:
[W] + 3(FeO) = (WO3) +
3[Fe], (3.9)
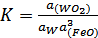
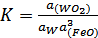 (3.10)
(3.10)
Окис вольфраму не є
міцним з'єднанням і легко відновлюється залізом. При плавці вольфрамової сталі
під кислим шлаком рівновага реакції (3.9) встановлюється при дуже низькій концентрації
окислу вольфраму в шлаку. При плавці вольфрамової сталі під основним шлаком
окис вольфраму, що утворюється, взаємодіє з окислом кальцію:
(WO3) + (CaO)
= (CaO · WO3) (3.11)
Завдяки утворенню
вольфрамовокислого кальцію коефіцієнт активності окислу вольфраму в шлаку
значно зменшується. Коефіцієнт активності окислу вольфраму, так само як і
коефіцієнт активності закису заліза, є функцією основності шлаку.
Найбільший вплив на
повноту окислення вольфраму роблять основність шлаку і вміст закису заліза в
ньому.
Криві рис.3.4 показують
дуже сильне зростання коефіцієнта розподілу вольфраму при збільшенні основності
шлаку.
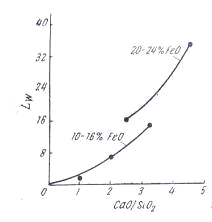
Рисунок 3.4 - Залежність
коефіцієнта розподілу вольфраму від основності шлаку
3.6 Окиснення ванадію
Ванадій може знаходитися в шлаку у
вигляді оксидів VO і V2O3.
Окислення ванадію до закису можна
виразити наступним рівнянням:
[V] + (FеО) = (VО) + [Fе] (3.12)
При плавці сталі під основним шлаком
коефіцієнт розподілу ванадію можна приблизно виразити наступним рівнянням:
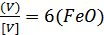
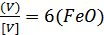 (3.13)
(3.13)
Графічно ця залежність
зображена на рис.3.5.
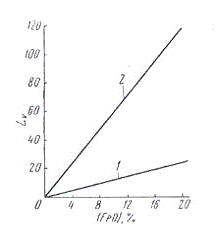
Рисунок 3.5 - Залежність
коефіцієнта розподілу ванадію від вмісту закису заліза у шлаку:
- кислі шлаки; 2 -
основні шлаки
У основному процесі
ванадій окислюється значно повніше, ніж в кислому процесі. Це вказує на те, що
активність оксидів ванадію в основному шлаку у декілька разів менше, ніж в
кислому. Разом із закисом ванадію в шлаку утворюється також окис ванадію V2O3.
У основному шлаку окис ванадію, будучи кислотним оксидом, утворює міцні зв'язки
з основними оксидами, головним чином з окислом кальцію. Це і є причиною низької
активності оксидів ванадію. У кислому шлаку окис ванадію не пов'язаний в міцні
з'єднання і тому ванадій в кислому процесі окислюється менш повно, чим в
основному.
3.7 Розкислення сталі
У кінці окислювального періоду сталь
містить разом з іншими елементами деяку кількість кисню і вуглецю. Якщо таку
сталь розлити по виливницях без попереднього введення в неї розкислювачів, то у
виливницях ці елементи взаємодіятимуть між собою. Окис вуглецю, що утворюється
при цьому, частково піде в атмосферу, частково залишиться в сталі у вигляді
бульбашок.
Навіть у тому випадку, якщо вміст
кисню і вуглецю в рідкій сталі в печі перед випуском дорівнює рівноважним
значенням, після розливання сталі по виливницях можливе утворення бульбашок в
зливках. Внаслідок виборчої кристалізації вміст вуглецю і кисню в матковому
розчині зростає. Тому пружність виділення окислу вуглецю збільшується і може
досягати 2 ат (1,96•105 н/м2) і більше. Окис вуглецю
виділяється з рідкої сталі і утворює бульбашки, які заплутуються серед гілок
зростаючого дендриту.
Для відвертання утворення бульбашок
в зливках необхідно ввести такі елементи в сталь, які в умовах її кристалізації
мали б більшу спорідненість до кисню, ніж вуглець. Найбільш поширеними
розкислюючими елементами є кремній і алюміній. Введення в сталь кремнію в
кількості не менше 0,18-0,23% запобігає утворення і виділення із сталі вуглецю
у вигляді бульбашок. При введенні з кремнієм також і алюмінію відвертання
утворення бульбашок можливе при нижчому вмісті кремнію. Тому усі марки
спокійної сталі, що виплавляються в електричних печах, містять не менше 0,17%
Si.
Разом з цим для повнішого
розкислювання сталі в неї вводять перед випуском з печі також невелику
кількість алюмінію. В деяких випадках для цієї ж мети вводять титан, цирконій і
інші розкислюючі елементи. Якщо в сталі є присутніми розкислюючі елементи в
достатній кількості, то бульбашки окислу вуглецю не утворюються. Кисень, що
міститься в рідкій сталі в розчиненому виді, взаємодіє з розкислюючими
елементами, що призводить до утворення різних оксидів: MnO, SiO2, Al2O3,
TiO2 та інші.
Ці оксиди частково виділяються з
розчину в печі, частково в ковші і у виливницях під час кристалізації. Оксиди,
що утворюються в рідкій сталі в печі і в ковші, частково спливають на поверхню,
частково поступають разом з рідкою сталлю у виливниці. Оксиди, що поступають
разом з рідкою сталлю у виливниці або що утворюються в процесі кристалізації
сталі у виливницях, переважно залишаються в зливках у вигляді неметалічних
включення.
Неметалічні включення погіршують
властивості сталі. Міра погіршення властивостей сталі визначається як кількістю
неметалічних включення, так і їх розміром, характером розподілу і фізичними
властивостями включень. Розкислювання сталі слід проводити так, щоб зменшити
вміст в ній неметалічних включення і знизити їх шкідливий вплив.
.
Підготовка шихти до завалки
Після чергової плавки футерівка
електропечі має деякі пошкодження. В процесі виплавки сталі відкоси поду печі
роз’їдаються металом і шлаком, а стіни оплавляються. Їх треба усунути. Процес
усунення дрібних пошкоджень футерівки називається заправкою. Заправка
виконується після кожної плавки. Заправка повинна виконуватися в мінімально
можливий час, щоб уникнути значного охолодження футерівки печі. В цьому розділі
треба розглянути матеріали, які використовують для заправки і особливості
проведення цього процесу. Для заправки поду і відкосів при основній футерівці
використовують суміш магнезит, доломіт, або їх суміш; при кислій футерівці -
кварцевий пісок або молотий кварцит.
Порошки магнезитові спечені
одержують шляхом високотемпературного відпалення природного магнезита. Вони
призначені для наварки, ремонту і заправки подин тп інших елементів футерівки
електросталеплавильних печей.
Для заправки подин і відкосів
основних електропечей використовують порошок ПМЕ - 87 дрібнозернистий (до 4 мм)
або ПМЕК - 87 з підвищеним вмістом СаО (до 8%) дрібнозернистий (до 4 мм). Вміст
MgO - 87%.
Для заправки основних електропечей
можна використовувати також доломіт. Доломіт - мінерал, що уявляє подвійну соль
кальція і магнія вугільної кислоти (CaCO3 ∙ MgCO3).
Він використовується в сирому і відпаленому вигляді. Марки: ДОМ-32,5 і ДОМ-29
(цифри в позначенні марки відповідають вмісту MgO, %).
. Шихтові матеріали та їх
підготовка
В якості шихтових матеріалів
використовують відходи ковальсько-штампувальних цехів, цехів механічної
обробки, відходи ливарних цехів, низьковуглецеву сталь для шихти, чисті метали
і феросплави.
Сталевий брухт частіше відповідає
хімічному складу сталі. Він має бути не дуже окисленим, не містити кольорових
металів. Брухт повинен бути ваговим, для завантаження шихти за один раз.
Для утворення шлаку використовують
вапняк і вапно (CaCO3 та CaO відповідно). Для розрідження основного
шлаку використовують плавиковий шпат (CaF2), боксит (Al2O3)
і SiO2. Як окисні матеріали використовують кисень (99,05 % О2),
залізну руду, офлюсований агломерат. Для розкислення і легування сталі
використовують FeMn, FeSi, FeCr, технічно чистий алюміній.
Низьковуглецеві сталі, які містять
невеликі кількості домішок, можна використовувати в якості шихти для виплавки
будь-якої марки сталі. Брухт сталевий вуглецевий використовується при виплавці
середнє- і високовуглецевих сталей з необхідною підшихтовкою.
Вороття власного виробництва є
повноцінним шихтовим матеріалом. Використання для плавки лише чистого вороття є
недоцільним тому, що при багаторазовому переплаві підвищується вміст газів і
окислів. Для отримання стабільних результатів треба здійснювати постійне
оновлення оборотного металу. Кількість вороття не повинна перевищувати 75%.
Ливарне вороття треба зберігати
суворо за марками сталей на шихтовому дворі в спеціальній замаркірованій тарі.
Перед використанням вороття треба
відчистити від залишків ливарних форм і стрижнів і подрібнити.
Усі шихтові матеріали повинні бути
очищені від іржі, мастила, піску.
Шихтові матеріали обов’язково
повинен оглянути піротехнік для запобігання попадання у піч вибухонебезпечних
предметів.
.
Розрахунок шихти
Треба розрахувати шихту для виплавки
сталі 60С2Н2А. Піч основна дугова. Маса плавки 5 т.
Розрахунок шихти зручно вести у
вигляді таблиці 6.1.
Розраховуємо кількість елементів
марочного складу на 100 кг. Основні компоненти шихти: Сталь низьковуглецева
шихтова 03пс 25% (25кг), вороття власного виробництва 60С2Н2А 75% (75кг)
Сталь 03 пс вносить:
С 0,0003 • 25 = 0,0075 кг;
Мn 0,0003 • 25 = 0,0075 кг;0,0003 •
25 = 0,0075 кг.
Вороття власного виробництва
вносить:0,006 • 75 = 0,45 кг0,016 • 75 = 1,2 кг0,0055 • 75 = 0,4125 кг0,0155 •
75 = 1,1625 кг
Результати розрахунку заносимо у
таблицю 1.
Підраховуємо кількість елементів на
100 кг металозавалки, що вносяться для розплавлення:
С 0,0075+ 0,45=0,4575
кг0,0075+1,2=1,2075 кг0,0075+0,4125=0,42 кг1,1625 кг
Визначаємо вигар елементів шихти і
заносимо у таблицю 1.
Розрахуємо коефіцієнт засвоєння
елементів КЗ за формулою:
КЗ = (100 - В %)/100,
(6.1)
де В - вигар елементів,%
Розрахуємо кількість елементів,
засвоєну металом:0,4575 • 0,82 = 0,375 кг1,2075 • 0,5 = 0,604 кг0,42 • 0,57 =
0,239 кг1,1625 • 0,98 = 1,139 кг
Таблиця 6.1 - Розрахунок хімічного
складу металу після розплавлення Марка сталі 60С2Н2А
Масова доля елемента в шихтовому матеріалі, %
|
Кількість на 100 кг метало завалки
|
|
C
|
Si
|
Mn
|
Ni
|
C
|
Si
|
Mn
|
Ni
|
|
Сталь низько- вуглецева 03пс
|
0,03
|
0,03
|
0,03
|
|
0,0075
|
0,0075
|
0,0075
|
|
|
Вороття власного виробництва
|
0,006
|
0,016
|
0,0055
|
0,0155
|
0,45
|
1,2
|
0,4125
|
1,1625
|
|
Внесено для розплавлення
|
0,4575
|
1,2075
|
0,42
|
1,1625
|
|
Вигар, %
|
18
|
50
|
43
|
2
|
|
Коефіцієнт засвоєння елементів 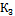 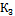 0,820,50,570,98 0,820,50,570,98
|
|
|
|
|
|
Засвоєно металом
|
0,375
|
0,604
|
0,239
|
1,139
|
|
Хімічний склад після розплавлення шихти
|
0,378
|
0,609
|
0,241
|
1,15
|
Визначимо хімічний склад металу
після розплавлення шихти. Для цього розрахуємо загальний вигар елементів за
формулою:
ВЗАГ = ΣЕР - Σ ЕЗМ (6.2)
де ВЗАГ - загальний вигар
елементів;
ΣЕР
- сума маси елементів, внесених для розплавлення;
ΣЕЗМ
- сума маси елементів, засвоєних металом
ВЗАГ =
(0,4575+0,42+1,2075+1,1625) - (0,375+0,239+0,604+1,139) = 0,8905 кг
Маса розплаву сталі МРС =
100 - 0,8905 = 99,1095 кг
Вміст елементів після розплавлення:
С = 0,375•100/99,1095 = 0,378%=
0,604 •100/99,1095 = 0,609%= 0,239•100/99,1095 = 0,241%= 1,139•100/99,1095 =
1,15%
Розрахуємо масу легуючих додатків.
Розрахунок зручно вести також у вигляді таблиці 6.2.
Таблиця 6.2. Розрахунок легуючих
додатків для виплавки сталі 60С2Н2А
|
№ п/п
|
Елемент
|
Аі (%)
|
Ві (%)
|
Сі (%)
|
Аі/Сі
|
Ві/Сі
|
КЗ
|
Рі, кг
|
|
1
|
Si
|
0,609
|
75
|
0,0081
|
0,0213
|
0,5
|
4,1
|
|
2
|
Mn
|
0,241
|
0,55
|
70
|
0,0034
|
0,0079
|
0,57
|
1,17
|
|
4
|
Ni
|
1,15
|
1,55
|
99,8
|
0,0115
|
0,0155
|
0,98
|
0,86
|
Σ Аі/Сі
= 0,023 ΣВі/Сі
= 0,0447
Розрахунки ведуться за спрощеним
методом.
Розрахуємо масу елементів після
розплавлення:
Si = 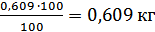
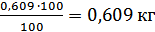 =
= 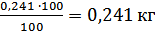
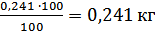 =
= 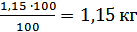
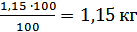
Маса елементів у
готовому металі:= 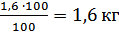
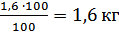 =
= 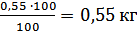
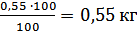 =
= 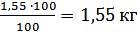
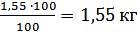
Розраховуємо різницю:=
1,6 - 0,609 = 0,991 кг= 0,55 - 0,241 = 0,309 кг= 1,55 - 1,15 = 0,4 кг
Розраховуємо кількість
легуючих додатків:= 0,991/0,75 = 1,32 кг= 0,309/0,70 = 0,44 кг= 0,4/0,998 = 0,4
кг
Визначимо кінцевий
розрахунковий вміст елементів:= 1,32 + 0,609 =1,929%= 0,44 + 0,241 = 0,681%=
0,4 + 1,15 = 1,55%
Порівняємо результати розрахунку
шихти з хімічним складом сталі, передбаченим стандартом (таблиця 6.3).
Таблиця 6.3. Розрахунковий і
стандартний хімічний склад сталі 60С2Н2А
|
Хімічний склад сталі
|
Вміст елементів, %
|
|
С
|
Si
|
Mn
|
Ni
|
|
Розрахунковий
|
0,378
|
1,929
|
0,681
|
1,55
|
|
Згідно ГОСТ 26-07-402-83
|
0,56-0,64
|
1,4-1,8
|
0,40-0,70
|
1,4-1,7
|
.
Завалка шихти і окислювальний період плавки
Завалку шихти в плавильні агрегати
треба виконувати у певній послідовності.
В дугових електропечах шихта розташовується
горкою до центру печі, укладається по можливості щільніше.
На подину укладається 50 % дрібної
шихти або стружки, потім великі шматки в зоні дії електричних дуг, потім
середні шматки, чушки чавуну, зверху залишок дрібної шихти.
На верх металевої частини шихти при
плавці в основній печі завалюють вапно в кількості 1 - 1,5 % від маси завалки.
За 30 - 60 хвилин до розплавлення шихти на 1 т завалки присаджують: залізну
руду 5 - 9 кг; вапно до 10 кг; плавиковий шпат до 10 кг. Після розплавлення і
підігрівання в піч додають 8 - 10 кг залізної руди і 5 - 10 кг вапна. 2/3
шлака, який утворився, вилучають із печі і до кінця окислювального періоду
працюють з видаленням шлаку. При цьому вміст фосфору зменшується з 0,08 до 0,03
- 0,015. Після розплавлення шихти додають вапно в кількості 1,5 - 2 % від маси
плавки.
Окислення вуглецю і інших домішок
шихти відбувається за рахунок їх взаємодії з окисом заліза, який розчинений у
рідкому металі.
Якщо змінювати концентрацію окису
заліза в шлаку, можна змінювати його концентрацію в металі і регулювати процес
вигоряння вуглецю, фосфору і інших домішок. Висока активність окислювального
шлаку забезпечується підвищенням вмісту залізної руди, зниженням в’язкості
шлаку додаванням плавикового шпату і підвищенням температури, перемішуванням
металу.
В окислювальний період для дугових
електропечей в залежності від місткості існують раціональні значення середньої
потужності, які наведені у таблиці 7.1.
При одержанні до початку розкислення
пониженого вмісту вуглецю навуглецювання металу здійснюється додаванням у піч
електродного бою, коксу або антрациту. Ступінь засвоєння вуглецю залежить також
від температури (таблиця 7.2).
Таблиця 7.1. Раціональні значення
середньої потужності при плавці в дугових електропечах в окислювальний період
|
Номінальна місткість печі, т
|
Потужність, кВт
|
|
0,5
|
150 - 200
|
|
1,5
|
400 - 500
|
|
3,0
|
700 - 900
|
|
5,0
|
900 - 1200
|
|
10,0
|
Таблиця 7.2. Ступінь засвоєння
вуглецю металом в залежності від навуглецювателів і температури металу
|
НавуглецювателіЗасвоєння, %
|
|
|
Електродний бій
|
70 - 80
|
|
Кокс
|
До 60
|
|
Антрацит
|
До 70
|
Примітка: поправка в залежності від
температури металу: холодний метал (1420 - 1440ОС) -10 %; гарячий
метал (1530 - 1580ОС) + 10 %.
.
Відновлювальний період
В цьому періоді плавки вирішуються
наступні задачі:
) максимальне вилучення із металу
кисню;
) десульфурація сталі;
) доведення металу до кінцевого
складу готової сталі;
) нагрівання сталі до температури,
необхідної для нормального розливання.
Після викачування окислювального
шлаку починається відновний період плавки. На початку відновного періоду метал
покривається шаром шлаку. Для цього в піч досаджують шлакотворні суміші на
основі вапна з добавками плавикового шпату, шамотного бою, кварциту. Як
розкислювачів звичайно використовують феромарганець, феросиліцій, алюміній. При
введенні розкислювачів відбуваються наступні реакції:
[Mn]+[O]=(MnO) (8.1)
[Si]+2 [О] = (SiO2) (8.2)
[Al]+ 3[O] = (Al2O3)
(8.3)
В результаті процесів розкислювання
велика частина розчиненого кисню зв'язується в оксиди і віддаляється з ванни у
вигляді нерозчинних в металі неметалічних включень. Процес цей протікає
достатньо швидко і тривалість відновного періоду в основному визначається
часом, необхідним для утворення жвавого шлаку. В малих і середніх печах при
виплавці відповідальних марок сталей продовжують застосовувати метод
дифузійного розкислювання сталі через шлак, коли розкислювачі у вигляді
меленого електродного бою, порошку феросиліцію досаджують на шлак. Вміст кисню
в шлаку знижується і відповідно до закону розподілу кисень з металу переходить
в шлак. Метод цей, хоча і не залишає в металі оксидних неметалічних включень,
вимагає значно більшої витрати часу. У відновний період плавки, а також при
випуску сталі під шаром шлаку, коли відбувається добре перемішування металу з
шлаком, активно відбувається десульфурація металу. Цьому сприяє добре
розкислювання сталі і шлаку, високий вміст вапна в шлаку і висока температура.
В ході відновного періоду вводять легуючі - феротитан, феррохром і ін., а
деякі, наприклад нікель, досаджують разом з шихтою. Нікель не окислюється і не
втрачається при плавці. Добавки тугоплавких феровольфрама, фероніобія
виробляють на початку рафінування, оскільки потрібен значний час для їх
розплавлення. В даний час більшість операцій відновного періоду переносять з
печі в ківш. Наприклад, в кіш вводять порції легуючих або дають їх на струмінь
сталі, витікаючої з печі при її нахилі. Досаджують по ходу випуску
розкислювачі. Ціллю відновного періоду являється забезпечення нагріву сталі до
заданої температури і створення шлаку, десульфуруюча здатність якого
використовується при сумісному випуску з печі разом із сталлю.
.
Уведення легуючих додатків і модифікаторів
Легуючі додатки можуть бути такими,
що не окислюються, (нікель, мідь, молібден), або окислюються (манган, хром,
силіцій, ванадій, титан, алюміній, вольфрам).
Основна частина нікелю уводиться в
завалку, або при плавленні шихти; заданий вміст його доводиться в процесі
кипіння металу. Така присадка нікелю сприяє видаленню водню.
Мідь можна уводити в піч з шихтою.
Електролітична мідь містить водень, тому таке введення сприяє видаленню водню.
Молібден вводиться в ванну після
скачування шлаку.
Ферохром нагрівається до червоного
кольору уводиться в сталь після розкислення її феросиліцієм. Витримка сталі
після додавання ферохрому 25 - 45 хвилин. Для запобігання підкипіння ванни в
цей період на шлак додається вугілля або кокс.
Феросиліцій уводиться шматками
розміром до 50 мм, алюміній - шматками вагою 2 - 3 кг. Під час випускання
металу у ківш треба запобігти перемішуванню його зі шлаком.
Модифікатори (феробор, РЗМ та ін.)
уводяться у ківш, або на жолоб при випусканні металу з печі.
. 10. Технологічна
інструкція
Технологічна інструкція по виплавці
корозійностійкої сталі складається з наступних пунктів:
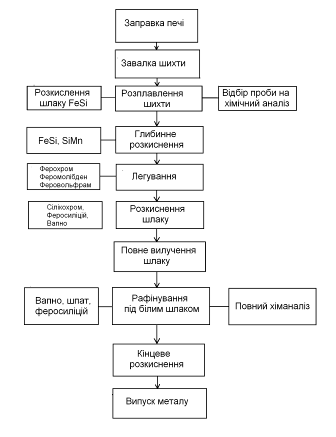
.
Техніка безпеки
Необхідно ретельно спостерігати за
належною роботою механічного і електричного обладнання електропечі і перевіряти
їх перед початком роботи і після ремонту. Особливо важливо знати, яким чином
можна зупинити механізм при аварії або при нещасному випадку. Відповідні кнопки
керування повинні бути чітко позначені, пофарбовані у яскраво-червоний колір і
розташовані якмога ближче і зручніше. Доступ до цих кнопок керування повинен
бути завжди відкритим і порядок користування їми повинен бути відомим не тільки
мастеру або сталевару, але і усім робітникам цеху.
При плавці сталі з окисленням треба
знати правила поводження з киснем. Недбале використання кисню може викликати
вибух, якщо кисень зіткнеться зі мастилом. Тому при роботі з киснем потрібно
користуватися тільки спеціальними редукторами. Трубопроводи, призначені для
кисню, не можна підключати до мережі стисненого повітря, або користуватися
стисненим повітрям для продувки тому, що в мережі стисненого повітря неминуче
присутні масло і волога, які занесені із компресора.
Для підігріву шихти і феросплавів
використовують пальники, які працюють на природному газі. При цьому утворюються
токсичні і вибухонебезпечні газові суміші.
Для запобігання утворення вибухової
суміші в трубопроводах не можна допускати засмоктування повітря в трубопроводи
природного газу. Ці трубопроводи повинні працювати при деякому надлишковому
тиску. Для запобігання отруєнню особливу увагу слід приділяти щільності
трубопроводів.
Корпуси електричних печей повинні
бути заземлені. Опір заземлення не повинен перевищувати 4 Ом.
При роботі на електричних печах під
час перемішування металу, завантаження шихтових матеріалів, або відбирання проб
необхідно вимикати піч або піднімати електроди. Під час плавки треба
користуватися захисними окулярами з темним склом.
Сталевар повинен бути одягнутим у
захисний вовняний костюм. В якості взуття використовують валянки. На голові
повинна бути захисна каска.
При плавці сталі в індукційній
електропечі рукоятки інструменту для осаджування шихти повинні бути ізольовані.
Біля печі повинен бути гумовий килимок.
Біля робочого місця повинна бути
інструкція по техніці безпеки.
Металевий брухт, який
використовується у якості шихти, повинен ретельно оглянути піротехнік для запобігання
попаданню в піч вибухонебезпечних предметів.
Список використаних джерел
1. Марочник сталей и сплавов /В.Г.Сорокин, А.В. Волосникова,
С.А.Вяткин и др.; Под общ.ред. В.Г.Сорокина. - М.:Машиностроение, 1989. - 640
с.
2. Крамаров А.Д. Производство стали в электропечах. Изд. 3-
е, испр. и дополн. Изд-во «Металлургия», 1969 - с 348.
. Методичні вказівки до курсової роботи з дисципліни
«Металургія ливарних сплавів» для студентів спеціальності 8.090403 «Ливарне
виробництво чорних та кольорових металів» денної форми навчання /Укл.Бялік
Г.А., Гонтаренко В.І. - Запоріжжя: ЗНТУ, 2004 - 31 с.