Огневое (окислительное) рафинирование черновой меди
Введение
Огневое
(окислительное) рафинирование черновой меди основано на различиях в сродстве к
кислороду меди и ее примесей, которое можно выразить величинами энергии Гиббса
образования или упругости диссоциации соответствующих оксидов. В ряду элементов,
входящих в состав черновой меди, сродство к кислороду при температурах процесса
убывает в направлении от алюминия к золоту.
Огневое
рафинирование проводят с целью удаления части примесей, обладающих по сравнению
с медью повышенным сродством к кислороду. Такие примеси в отличие от
благородных металлов, которые в этой стадии рафинирования практически не
удаляются, часто называют неблагородными. Огневому рафинированию подвергают
расплавленную медь.
Процесс огневого
рафинирования меди состоит из следующих основных операций: загрузки,
расплавления твердой меди и разогрева расплава, окисления примесей, съема
шлака, раскисления (дразнения) меди и разливки меди в анодные слитки.
Продолжительность процесса рафинирования зависит от многих факторов (состава
черновой меди, вместимости печи, тепловой нагрузки, производительности
загрузочных и разливочных устройств) и колеблется от 12 до 32 ч.
Процессы окисления меди ведут при
1150-1170°С. Увеличение температуры хотя и ускоряет процесс, но одновременно
ведет к повышенному насыщению расплавленной ванны Сu2О, что удлиняет
стадию раскисления и увеличивает расход дорогостоящих восстановителей. В
конечном итоге никакого выигрыша в сокращении времени и стоимости операции не
получается.
1. Теоретические основы
процесса
Цель операции огневого рафинирования
- подготовить черновую медь к электролитическому рафинированию:
удалить вредные примеси (кислород,
серу, железо, никель, цинк, свинец, мышьяк, сурьму, растворенные газы);
получить отливки меди в форме
плотных ровных пластин постоянной массы.
В результате огневого рафинирования
содержание меди в анодах повышается до 99,4-99,6%.
Стадия окисления начинается с
продувания ванны расплава воздухом или воздухом, обогащенным кислородом. При
этом медь постепенно насыщается кислородом и происходит окисление примесей.
С учетом сродства к кислороду при
окислительном рафинировании черновой меди первыми должны были бы окисляться
неблагородные примеси. Однако вследствие их низкой концентрации в расплаве
происходит прежде всего окисление меди по реакции:
Cuж + О2 = 2Cu2Отв
За счет растворения Cu2O
расплавленная медь постепенно насыщается кислородом.
Остаточное содержание примесей
определяется равновесием реакции:
2O + Me = МеО + 2Сu
Сродство к кислороду, а
следовательно, и упругость диссоциации оксидов зависят от их активности. Для
обеспечения максимально полного удаления примесей необходимо, чтобы упругость
диссоциации Cu2O была наибольшей, а упругость диссоциации оксида
примеси минимальной.
Упругость диссоциации Cu2O
возрастает с увеличением концентрации (активности) кислорода в медной ванне.
Ответ на вопрос о том, до какого предела следует насыщать медь кислородом, дает
диаграмма состояния системы Сu - Cu2O (рис. 1).
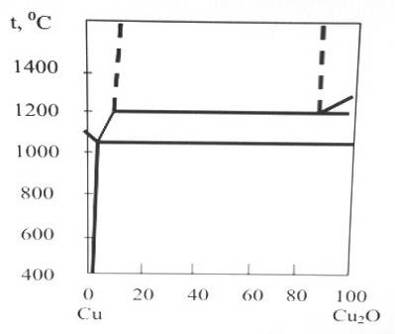
Рис. 1. Диаграмма состояния Сu-O
(участок Сu-Cu2O)
Из диаграммы видно, что
растворимость Сu2O в металлической меди составляет 8,3% (1,04% O2)
при 1150°С; 12,4% (1,56% O2) при 1 200°С.
При температуре рафинирования (1 150-1
170°С) предел растворимости Cu2O составляет около 8,0-8,5%.
Избыточный Cu2O в меди не растворяется и образует самостоятельную
твердую или жидкую (выше 1 200°С) фазу на поверхности расплава. Давление
кислорода в системе при этом остается постоянным, т.е. увеличение концентрации
растворенного в меди кислорода выше 1,04% не ведет к увеличению упругости
диссоциации Cu2O и, следовательно, лишено смысла.
Остаточное содержание примесей в
меди пропорционально активности его оксида в шлаке, следовательно, для максимально
полного удаления примесей при окислительном рафинировании необходимо постоянно
удалять рафинировочные шлаки, чтобы к завершению стадии окисления оставшийся
шлак имел минимальное содержание оксида примеси. Все примеси, находящиеся в
меди, можно разделить на четыре группы:
1. Примеси, образующие твёрдые
растворы с медью (никель и др.).
2. Примеси, образующие
химические соединения с медью, растворимые в ней. Эти примеси практически ничем
не отличаются от первой группы (кислород, селен, теллур и др.).
. Примеси, образующие
химические соединения с медью и нерастворимые в ней. Они обнаруживаются в виде
самостоятельной фазы в виде эвтектики.
. Примеси, не образующие
твердых растворов с медью и не образующие химических соединений в ней (газовые
и шлаковые включения).
Наибольшие трудности при огневом
рафинировании меди вызывает удаление примесей, образующих с медью химические
соединения. К их числу относятся, например, мышьяк, сурьма, селен, теллур и
другие. В этом отношении все примеси можно разбить на три группы:
1) сравнительно легко удаляемые
(железо, сера и др.);
2) удаляемые только частично
(никель);
) практически не удаляемые
(золото, серебро, металлы платиновой группы и др.).
Растворимость в черновой меди
примесей зависит от температуры черновой меди, содержания в ней кислорода,
серы, вида примеси, возможности образования между медью и примесями химических
соединений, твердых растворов и т.д. Её можно определить с помощью диаграмм
состояния медь - примесь.
Железо. Медь и железо в жидком виде при отсутствии кислорода имеют
ограниченную растворимость, при температуре 1083-1094°С они образуют твердый
раствор, содержащий около 4% железа. С понижением температуры растворимость
железа снижается до тысячных долей процента.
Никель. Медь и никель в жидком виде имеют неограниченную взаимную
растворимость, в твердом состоянии образуют твердые растворы.
Сера. В меди присутствует в виде полусернистой меди. Её растворимость
при 1100°С равна 1,8%, она несколько увеличивается с повышением температуры. В
твердой меди сера растворяется незначительно, что приводит к выделению
полусернистой меди в отдельную фазу.
Кислород в меди находится, в основном, в виде оксида меди (I). Некоторое
количество кислорода связано с примесями и присутствует в виде твердого
раствора с медью. Растворимость кислород в жидкой меди при температуре 1200°С
равна 1,5%, растворимость в твердой меди не превышает 0,01%. При охлаждении
черновой меди растворенный в ней оксид меди выделяется в виде самостоятельной
фазы в составе эвтектики.
Селен и теллур. Присутствуют в меди в виде химических соединений - с ленида и
теллурида меди. В жидкой меди эти соединения имеют ограниченную растворимость:
при температуре 1100°С растворимость селена равна около 5%, теллура - около 2%.
В твердой меди они не растворяются и находятся в ней в виде эвтектики.
Серебро, золото, металлы
платиновой группы. В жидкой меди имеют полную растворимость. С твердой медью
образуют твердые растворы или эвтектики.
Для огневого рафинирования меди
используют стационарные отражательные печи.
Печь покоится на
столбчатом фундаменте, что обеспечивает повышенную стойкость подины. На одной
из продольных стен печи имеются рабочие окна с опускающимися заслонками,
предназначенные для загрузки в печь твердых материалов и обслуживания печи во
время работы. Рафинировочные печи отапливаются только высококачественным
топливом (природный газ или мазут). Топочная сторона печи имеет форкамеру, в
которой начинается горение топлива. Окна для съема шлака расположены в одной из
боковых или в задней торцовой стенке печи. Рабочие и шлаковые окна можно
использовать для окислительной и восстановительной обработки расплавленной
меди.
На противоположной
длинной стороне печи имеется щелевая летка, которую перед началом загрузки
закладывают огнеупорным кирпичом или заделывают глиной. Во время разливки меди
в конце операции щель постепенно разбирают сверху, что обеспечивает почти
постоянный напор струи жидкой меди.
Стационарные
отражательные печи применяют для огневого рафинирования как жидкой, так и
твердой черновой меди, а также для переплавки и дополнительного рафинирования
катодной меди при изготовлении из нее вайербарсов - слитков особой формы,
используемых в дальнейшем для проката и волочения проволоки.
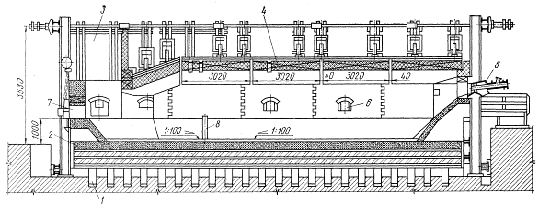
Отражательная печь для рафинирования
меди
2. Металлургический
расчет
Расчет материального
баланса:
Выполнение расчета огневого
рафинирования черной меди следующего химического состава, %:= 99,35; S = 0,386;
Ni = 0,02; Pb = 0,078;= 0,075; As = 0,0163; Bi = 0,017; Sb = 0,03;
Годовая производительность передела
340 тыс. т. анодной меди в год.
Составление материального баланса
плавки.
В печь поступает шихта
состава, %:
- черновая медь - 83,2
анодные остатки - 14,4
брак плавок - 1,1
скрап - 0,53
изложницы - 0,67
выломки - 0,06
заправочный материал - 0,04
Выход продуктов плавки,
%:
- годные аноды - 97,2
брак - 1,1
скрап - 0,53
шлак - 0,39
выломки - 0,06
изложницы - 0,67
потери - 0,05
Годные аноды имеют состав, %:= 99,6;
Ni = 0,043; Fe = 0,0045; Pb = 0,068; S = 0,011;= 0,048; Sb = 0.086; Bi =
0,0014; Se = 0,0085; Te = 0,014.
Состав шлаков, %:= 39; Fe = 11,05;
Al2O3 = 6,8; SiO2 = 42,5;= 0.265; Sb = 0,095;
As = 0,0026; Pb = 0,289;
Годовая производительность отделения
- 340000 т. анодов.
Суточная производительность отделения
340000: 342 = 994 т.
При емкости печи 500 т
выход продуктов плавки:
брака 500. 0,011 = 5,5 т;
скрапа 500. 0,053 = 2,65
т;
выломки 500. 0,0006 = 0,30 т;
шлака 500. 0,0039 = 1,95
т;
изложницы 500. 0,0067 = 3,35;
потери 500. 0,0005 = 0,25 т.
Вес меди в продуктах
плавки:
годных анодах 486. 0,996 = 484,056
т;
браке 5,5. 0,996 = 5,478 т;
скрапе 2,65. 0,996 = 2,640 т;
шлаке 1,95. 0,39 = 0,760
т;
выломках 0,3. 0,996 = 0,298 т;
изложницах 3,35. 0,996 = 3,336 т;
потерях 0,25. 0,070 = 0,017 т.
Приход
Количество черновой меди,
загружаемой в печь:
. 0,832 = 416 т.
В нем меди: 416. 0,9935 = 413,296 т
Количество анодных остатков:
. 0,144 = 72 т В нем меди: 72.
0,9935 = 71,537 т.
Количество загружаемого брака
плавок:
. 0,011 = 5,5
В нем меди: 5,5. 0,996 = 5,478 т.
Количество загружаемого скрапа:
. 0,053 = 2,65 т.
В нем меди: 2,65. 0,996 = 2,640 т.
Количество загружаемых изложниц:
. 0,0067 = 3,35 т.
В них меди: 3,53. 0,996 = 3,336 т.
Количество загруженных выломок:
. 0,0006 = 0,3 т.
В них меди: 0,3. 0,996 = 0,298 т.
Количество заправочного материала:
. 0,0004 = 0,2 т.
Таблица №1. Материальный
баланс плавки
|
Загруженно
|
%
|
Т
|
Содержание меди
|
|
|
|
%
|
т
|
|
Черновая медь
|
83,2
|
416
|
99,35
|
413,296
|
|
Анодные остатки
|
14,4
|
72
|
99,35
|
71,537
|
|
Брак плавок
|
1,1
|
5,5
|
99,6
|
5,478
|
|
Скрап
|
0,53
|
2,65
|
99,6
|
2,640
|
|
Изложницы
|
0,67
|
3,53
|
99,6
|
3,336
|
|
Выломки
|
0,06
|
0,30
|
99,6
|
|
Заправочный материал
|
0,04
|
0,2
|
-
|
-
|
|
ИТОГО:
|
100
|
500
|
-
|
496,585
|
|
Получено
|
|
|
Годных анодов
|
97,2
|
486
|
99,6
|
484,056
|
|
Брак
|
1,1
|
5,5
|
99,6
|
5,478
|
|
Скрап
|
0,53
|
2,65
|
99,6
|
2,640
|
|
Шлак
|
0,39
|
1,95
|
39
|
0,760
|
|
Выломки
|
0,06
|
0,3
|
99,6
|
0,298
|
|
Изложницы
|
0,67
|
3,35
|
99,6
|
3,336
|
|
Потери
|
0,05
|
0,25
|
0,07
|
0,017
|
|
ИТОГО:
|
100
|
500
|
-
|
496,585
|
|
|
|
|
|
|
Расчет горения
природного газа.
Химический состав природного газа,
%:4 = 95,5; C2H3 = 1,2; CO2 = 0,3;
N2 = 3,0.
Расчет на 100м3
природного газа.
На реакцию горения газа требуется
кислорода и образуется при этом СO2 и H2O.
) CH4 + 2O2
= CO2 + 2H2O
2 1 2
,5 x y z= 191 м3 y = 95,5
м3 z = 191 м3
) C2H6
+ 3,5O2 = 2CO2 + 3H2O
3,5 2 3
,2 x y z= 4,2 м3 y = 2,4
м3 z = 3,6 м3
Теоритически требуется
кислорода:
+ 4,2 = 195,2 м3
С учетом избытка воздуха б = 1,1
требуется кислорода:
,2. 1,1 = 214,72 м3
Избыток кислорода составляет:
,72 - 195,2 = 19,52 м3
С кислородом поступает азота:
,72 / 21. 79 = 807,38 м3
Необходимо воздуха:
Таблица №2 Состав продуктов горения
газа
|
Газы
|
кг
|
м3
|
% (обь)
|
|
CO2
|
193,44
|
98,2
|
8,74
|
|
H2O
|
157,37
|
194,6
|
17,33
|
|
N2
|
1013,97
|
810,38
|
72,18
|
|
O2(изб)
|
27,88
|
19,52
|
1,75
|
|
ВСЕГО:
|
1392,66
|
1122,7
|
100
|
Таблица №3 Пересчет природного газа
на массу
|
газы
|
% (обь)
|
м3
|
пересчет
|
кг
|
|
CH4
|
95,5
|
95,5
|
95,5. 16: 22,4
|
68,21
|
|
C2Н6
|
1,2
|
1,2
|
1,2. 30: 22,4
|
1,6
|
|
CO2
|
0,3
|
0,3
|
0,3. 44: 22,4
|
0,6
|
|
N2
|
3,0
|
3,0
|
3. 28: 22,4
|
3,75
|
|
ВСЕГО:
|
100
|
100
|
-
|
74,16
|
Расчет количества
воздуха на окисления черной меди:
Количество закиси меди к концу
операции окисление черновой меди 8% от веса шихты, т.е. 500. 0,08 = 40 т.
Количество O2 в закиси
меди (Cu2О)
Cu - О 144 - 16
- x= 4,44 т. или 4440 кг;
В черновой меди имеется 0,4% O2
или 500. 0,004 = 2 т
или 2000 кг.
Следовательно, необходимо ввести в
ванну печи кислорода:
- 2000 = 2440 кг или 1708 м3
С этим кислородам поступит азота:
. 79 / 21 = 6422,08 м3.
Теоретически воздуха на окисление
требуется:
,08 + 1708 = 8130,08 м3.
В среднем при плавке б = 0,9.
,08: 0,9 = 9033,42 м3 или
9033,42. 1,29 = 11653,11 кг.
Расчет восстановления
меди:
В печи имеется 40т Сu2O В
шлаке меди 0,76 т. (табл. 1), что в пересчете на закись меди составит:
,76. 144 / 128 = 0,85 т или 850 кг
Необходимо восстановить закиси меди:
- 850 = 39150 кг.
Cu2О + С = 4Cu + СО2
- 12
-х
х = 1620 кг.
Восстановление производится мазутом
с содержанием углерода 90%. Тогда потребность мазута составит:
: 0,9 = 1800 кг.
Таблица №4. Суточный материальный
баланс плавки
|
ПРИХОД
|
т
|
РАСХОД
|
т
|
|
1. Черновая медь
|
416
|
1. Годные аноды
|
486
|
|
2. Анодные остатки
|
72
|
2. Брак
|
5,5
|
|
3. Брак плавки
|
5,5
|
3. Скрап
|
2,65
|
|
4. Скрап
|
2,65
|
4. Шлак
|
1,95
|
|
5. Изложницы
|
3,35
|
5. Выломки
|
0,3
|
|
6. Выломки
|
0,3
|
6. Изложницы
|
3,35
|
|
7. Заправочный материал
|
0,2
|
7. Дымовые газы
|
1046,3
|
|
8. Природный газ
|
55
|
8. Потери
|
0,25
|
|
9. Воздух на горение топлива
|
977,85
|
|
|
|
|
10. Воздух на окисление меди
|
11,65
|
|
|
|
|
11. Мазут
|
1,8
|
|
|
|
|
ВСЕГО:
|
1546,3
|
ВСЕГО:
|
1546,3
|
Расчет теплового баланса
отражательной печи:
Приход тепла.
1) Горение топлива:
т = m. Qрн = 55000. 35000 = 1925000000 кДж.
) Физическое тепло топлива:
фт = m. c. t = 55000. 1.54. 1,54. 20 = 1701260 кДж.
) Тепло реакции
восстановления:
2Cu2O + C =
4Cu + CO2 + 226100 кДж
- 226100
-х
х = 30500000 кДж.
а) 4Cu + O2 = 2Cu2O
+ 333062 кДж.
- 333062
-х
х = 25400000 кДж.
б) Cu2O + Fe = 2Cu + FeO
+ 10000 кДж В черновой меди Fe: 416. 0,075 / 100 = 0,312 т
- 10000
-х
х = 55700 кДж.
в) Cu2O + Ni = 2Cu + NiO
+ 80000 кДж В черновой меди Ni: 416. 0,02 / 100 = 0,08 т.
- 80000
-х
х = 108000 кДж.
г) 3Cu2O + Sb = 6Сu + Sb2О3
+ 207000 кДж В черновой меди Sb: 416. 0,03 / 100 = 0,12 т 144 - 207000
-х
х = 171800 кДж.
д) 3Cu2O + As = 6Cu + As2O3
+ 130000 кДж В черновой меди As:
. 0,075 / 100 = 0,312 т 207 - 52000
-х
х = 78000 кДж.
ж) 3Cu2O + 2Bi = 6Cu + Bi
2O3 + 87000 кДж В черновой меди Bi: 416. 0.017 / 100 =
0.07 т 418 - 87000
-х
х = 13920 кДж.
з) S + O2 = SO2
+ 296900 кДж В черновой меди S: 416. 0,386 / 100 = 1,6 т
- 296900
-х
х = 14845000 кДж.
Всего тепла окисления примесей =
40719620 кДж.
) Физическое тепло мазута:
м = m. c. t = 1800. 1,61. 20 = 57600 кДж.
Расход тепла
1. Физическое тепло шлака:
ш = mшл. лшл = 1950. 1254 = 2470000 кДж.
. Физическое тепло меди:
ан = mан. лан = 497800. 727 =
361000000 кДж.
Физическое тепло газов:г
= 871916. 1,4. 1200 = 1470000000 кДж.
. Потери тепла во внешнюю
среду.
а) окна во время загрузки.1
= 1,1. 1,7 = 1,87 м3
1 = 4,96. (Т / 100)4 F. и. t = 4,96 (1200 / 100)4
1,87. 0,9. 3. 4,18 = 6386000 кДж.
б) окна, открытые в период окисления
и восстановления:2 = 0,5. 0,5 = 0,25 м2 на два окна 0,5 м2;3
= 0,7. 0,6 = 0,42 (шлаковые);2 + F3 = 0,5 + 0,42 + 0,92 м2;2
= 4,96 (1200 / 100)4 0,92. 0,78. 3. 4,18 = 2722000 кДж.
в) через окна закрытые:= 1,87 на 3
окна 1,87. 3 = 5,61 м2;
= л. (tкл - tв
/ (S / л + 0,06)) F. t = 0,8. (1300 - 40 / (0,19 / 0,8
+ 0.06)) 5,61. 20. 4,18 = 1730000 кДж.
г) через кладку печи:
свод Q1 = л ((t1
- t2) / S) F. t
1 = 1,39 ((1200 - 50) / 0,38) 118. 24. 4,18 = 49808000 кДж
Q2 = 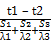
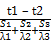 F. t
F. t
Q2 = 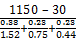
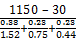 60. 24. 4,18 = 6825000
кДж.
60. 24. 4,18 = 6825000
кДж.
стенки ванны печи
3
= 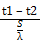
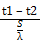 F. t
F. t
3
= 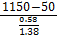
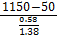 25,7. 24. 4,18 =
6638000 кДж.
25,7. 24. 4,18 =
6638000 кДж.
Всего во внешнюю среду:
74109000 кДж.
Таблица №5 Тепловой
баланс отражательной печи
|
ПРИХОД кДж
|
%
|
РАСХОД
|
кДж
|
%
|
|
1. Горение газа 1925000000
|
96,34
|
1. Тепло шлака
|
2470000
|
0,12
|
|
2. Типло топлива 1701260
|
0,08
|
2. Тепло меди
|
361000000
|
18,06
|
|
3. Реакция востан. 30500000
|
1,52
|
3. Тепло газов
|
1470000000
|
|
4. Реакция окислен. 18469620
|
2,03
|
4. Во внешнюю среду
|
74109000
|
3,70
|
|
5. Тепло мазута 57600
|
0,03
|
5. Неучтеное тепло
|
68149480
|
4,55
|
|
ВСЕГО: 1975728480
|
100
|
ВСЕГО:
|
1975728480
|
100
|
3. Расчет и выбор
оборудования
огневой рафинирование медь
Рассмотрим стационарную
медерафинировочную отражательную печь с суточной производительностью 300 т/сутки.
Емкость печи составляет 300 т, ее размеры: длинна по кладке 18050 мм, высота по
кладке 4600 мм, глубина ванны 760 мм. Характеристика и назначение основных
частей печи: рабочая ванна, футерована периклазохромировым кирпичом;
загрузочные окна - расположены на передней стенки рабочего пространство печи и
предназначены для загрузки шихты; футерованные заслонки закрывают загрузочные
окна, подъем и опускание осуществляется механическим приводом; в них
оборудованы окна для подачи воздуха на окисление и подачи мазута на
восстановление; шлаковое окно расположено на боковой стене печи,
противоположной форкамере и предназначено для съема шлака через него; летка
расположена на задней стенке печи. Предназначена для выпуска расплавленного
металла из печи в разливочные ковши; нагнетательный вентилятор высокого
давления нужен для нагнетания воздуха и сжигание топлива; система сжигания
топлива состоит из двух горелочных устройств, вмонтированных в боковую стену
печи, противоположной понурой части печи; шибер предназначен для создания
внутри печного давления.
Определим количество печей П, шт.,
для выполнения годового задания:
П = G: (£. 342),
где G - годовая производительность
анодного отделения, т;
£
- суточная производительность печи, сутки;
П = 350 000: (300. 342) = 3,41.
Следовательно, принимаем четыре
печи. Длительность разливки при емкости печи 300 тонн, составляет в среднем 5,5
часов, следовательно, нужная производительность машины около 54 т/час. На
каждую печь принимаем одну разливочную машину карусельного типа
производительностью 60 т/час, количество изложниц 25. Для снятия анодов с
изложниц разливочной машины используем две пневматические анодосъемные машины с
механическим приводом, производительность 30 т/час. Для загрузки шихты
используем кран грузоподъемностью 3,3 тонны. Вес годных анодов 486 тонн,
количество анодов укладываемых на одну вагонетку 34, масса анода 0,31 тонн.
Значит на одну вагонетку грузится 34. 0,31 = 10,54 т, следовательно, количество
вагонеток будет равно 486: 10,54 = 46,1 шт. На четыре печи принимаем 188
вагонеток, грузоподъемностью 10 тонн. На предприятии принимаются шлаковые
коробки объемом 0,66 м3. Масса получаемого шлака 1,47 тонн.
Следовательно, получаем на четыре печи 1,47: 2,8: 0,66. 4 = 3,18 шт., Значит
принимаем четыре шлаковые коробки. Вагонетки для подачи меди имеют
грузоподъемность 5 тонн, емкость печи 300 тонн, так как вагонетки используются
не одновременно у всех печей, то опытным путем установлено, что их количество
можно уменьшить в два раза, следовательно, на четыре печи понадобится 300: 5.
4: 2 = 120 шт.
4. Расчет аппаратов
системы пылеулавливание
Большинство пирометаллургических
процессов осуществляется при значительны затратах топлива или электроэнергии.
Затраты на топливо достигают 70% общих производительных затрат, в то же время
до 50 - 70% тепла теряется с газами, шлаками и другими отходами производства,
поэтому рациональное использование вторичных энергоресурсов имеет большое
хозяйственное значение.
Тепло отходящих газов используют для
нагрева котлов-утилизаторов в случаях: когда дымовые газы на выходе из печи
имеют высокую температуру, когда дымовые газы содержат значительное количество
пыли, которая быстро засоряет подогревательные устройства (рекуператоры,
регенераторы). Принципиальная схема газо-пылеулавливания для отражательной печи
содержит в себе котел-утилизатор.
Известны водотрубные и газотрубные
типы котлов-утилизаторов. В котлах первого типа вода циркулирует внутри труб,
омываемых водой. При плавильных печах, когда температура отходящих газов выше
700оС, устанавливают водотрубные котлы, которые менее чувствительны
к работе на дымовых газах содержащих пыль.
Наибольшее распространение в цветной
металлургии получили котлы туннельного типа. За отражательными печами
устанавливают аппараты серии ТОП. Камера котла представляют собой прямоугольный
газоход; грани которого экранированы радиационными поверхностями (боковые стены
- испарительными ширмами, потолок - трубами пароперегревателя), в нижней части
установлены водоохлаждемые бункеры. За испарительными ширмами установлен
рекуператор из труб. Поверхности нагрева котла подвешены на потолочном
перекрытии. Для котлов-утилизаторов предусмотрена система ударной очистки.
Теплоутилизационные аппараты типа
ТОП обеспечивают подогрев дутья до 400оС и регенеративный возврат в
печь до 30% тепла сжигаемого топлива. Низкое гидравлическое сопративление
котлов этого типа снижает подсосы воздуха и обеспечивает высокий КПД
пылеулавливания. Последнее позволяет, минуя циклоны грубой очистки,
устанавливать электрофильтры сразу за котлом.
Производим расчет котла-утилизатора.
Для того, чтобы определить тип котла-утилизатора, необходимо рассчитать
паропроизводительность. Расчет ведем на основании уравнения теплового баланса
работы котла. Найдем количество тепла передаваемое газами Qкот,
кДж:0
кот = Vг. (Свх. tвх - Cвых.
tвых) = Д. (iпара - iводы), где Vг
- секундный объем газов, м3/сек;
Свх - теплоемкость газов
на входе в котел, кДж/м3;вх - температура газов на входе
в котел, оС;вых - теплоемкость газов на выходе из котла,
кДж/м3;вых - температура газов на выходе из котла, оС;
Д - паропроизводительность котла,
кг/ч;пара - теплосодержание полученного пара, кДж/кг;воды
- теплосодержание питающей воды, кДж/кг.
Сначала определим объем газов: 6,75.
Далее находим удельную теплоемкость
газов на входе в котел Свх при температуре газов tвх =
1400оС, при этой температуре удельные теплоемкости газовых
составляющих, кДж/м3. оС:
Свх =%ССО2 +%СН2О
+%СN2 +%CO2изб,
Свх = 8,74. 2,3405+17,33.
1,8151+72,18. 1,4371+1,75. 1,522 = 1,58
Аналогично рассчитываем удельную
теплоемкость газовых составляющих на выходе из котла при температуре tвых
= 300оС, кДж/м3. оС:вых = 8,74.
1,8808+17,33. 1,5379+72,18. 1,308+1,75. 1,3583 =1,4
Рассчитываем количество
передаваемого от газов тепла по формуле, подставив в левую часть числовые
значения:кот = 6,75.(1,58. 1400 - 1,40. 300) = 12096.
Исходим из того, что в котле
получаем насыщенный пар при давлении 10 атм, при этом: iпара =
2769,59 кДж/кг, tпара = 180оС, температуру питающей котел
воды принимаем равной 15оС, теплосодержание воды при температуре iводы
= 62,85 кДж/кг.
Находим паропроизводительность
котла, преобразовав формулу:
Д = Qкот (iпара
- iводы),
Д = 12096 (2769,59 - 62,85) = 4,469
кг/сек или 16т/час.
По данной паропроизводительности
16т/ч выбираем тип котла по справочнику, тип котла ТОП-40.
. Технический контроль и
автоматизация процесса
Автоматизация производственного
процесса представляет собой сложный комплекс мероприятий, цель которых
освободить человека от функций непосредственного управления процессом, передав
их специальным устройствам. При этом программирование, задание режимов,
наблюдение за работой средств автоматизации, наладку и обслуживание их
осуществляет человек.
Контроль за автоматическим процессом
осуществляется централизованно из операторского помещения. На каждой печи
контролируются следующие технологические параметры: расход топлива на горелки;
расход вентиляторного воздуха; температура свода; давление вентиляторного
воздуха; давление под сводом печи; температура металла; температура изложниц.
Регулирование давление под сводом
печи осуществляется изменением производительности дымососов (воздействием на
направляющие аппараты), установленными за котлами-утилизаторами, или
перемещением шибера.
Регулирование температуры в рабочем
пространстве отражательной печи осуществляется изменением подачи топлива.
Температура измеряется радиационным пирометром, визированным на карбофраксовый
стакан, установленный в своде. Количество природного газа, подаваемое к
горелкам, регулируется поворотом регулирующих заслонок или крана. Система
соотношения «топливо-воздух» выполняется с коррекцией по экстремуму температуры
факела. Системой регулирования «топливо-воздуха» подсчитывается теоритическое
количество воздуха, подаваемого в печь. Коэффициент избытка воздуха
устанавливается вручную задатчиком и корректируется экстремальным регулятором
до достижения наивысшей температуры факела. Работа экстремального регулятора
основана на принципе поиска максимума температуры.
Поддержание оптимального значения
коэффициента избытка воздуха при изменении расхода топливо возможно только с
использованием автоматических устройств: общий расход топлива, расход
вторичного воздуха и расход воздуха на окисление контролируют приборы КСД - 3С
ДМ, давление под сводом контролируют приборы КСД - 3С ДК, температуру под
сводом контролируют приборы КСП 3С ТЕРА - 50, в качестве регулятора соотношения
«топливо - воздуха» выступают приборы Р-2511 СДМ и КРП - 3С ДМ, температуру
отходящих газов и вторичного воздуха показывают приборы МПЩПРС ТХН.
Технический контроль за процессом
плави проводиться совместно с отделом технического контроля. Для определения
глубины окисления, а так же окончания процесса восстановления, отбирается
ложечная проба. Измерение температуры расплава металла во время доводки его
перед разливом и во время разлива проводиться работником цеха. Во время разлива
представители ОТК осуществляют контроль за качеством отлитых анодов.
Список используемых
источников
1. Лякишев Н.П, Плинер
Ю.Л, Игнатенко Г.Ф, Алюмотермия - М металлургия, 1718.
. Гордон Г.М, Пейсахов
И.Л., Пылеулавливание и очистка газов - М металлургия 1968.
. Страк Е.Б.
Газоочистные аппараты и установки в металлургии - М: Металлургия, 1973.
. Злобинский Б.М. Охрана
труда в металлургии - М: Металлургия. 1968.
. Ильинский Б.Д, Техника
безопасности в черной металлургии - М: Металлургия, 1967.
. Уткин Н.И. Металлургия
цветных металлов - М: Металлургия, 1985.
. Деомидовский Д.А.
Металлургические печи цветной металлургии - М: Металлургия, 1970.