|
Характерные
точки цикла
|
Значения
P бар
|
Параметров
Т К
|
Состояния
V м3/кг
|
|
1
|
1,4
|
370
|
0,7651
|
|
2
|
9,98
|
520
|
0,1509
|
|
3
|
610
|
0,1509
|
|
4
|
11,7
|
813
|
0,2012
|
|
5
|
4,8
|
1269
|
0,7651
|
Показатели политропы: процесса 1-2 и 4-5
n1-2=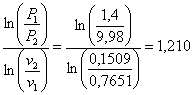 n4-5=
n4-5=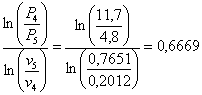
. Определение процессных теплоемкостей газовой
смеси и показателя адиабаты:
Сv=åCvi×g
Cp=åCpi×gi
где Сvi
и Cpi
-
теплоемкости каждого компонента в составе смеси находим с учетом количества
атомов и молекулярной массы по формулам:
Сvi=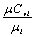 Cpi=
Cpi=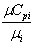
Cv=
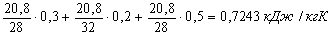
Cp=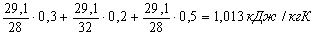
Показатель адиабаты
k=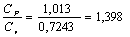
7. Процессные теплоемкости по формулам для:
процесса 1-2
С1-2=Сv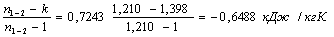
процесс 2-3:
С2-3=Сv
процесс 3-4:
С3-4=С Р
процесс 4-5:
С4-5=Cv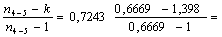 1,5906кДж/кгК
1,5906кДж/кгК
процесс 5-1:
С5-1=Сv
. Изменение внутренней энергии Du,
энтальпии Dh , и энтропии Ds
в процессах, составляющих цикл:
Изменение внутренней энергии в любом процессе: Du=Cv(Tj-Ti)
Du1-2=0,7243(520-370)=108,65
кДж/кг
Du2-3=0,7243(610-520)=65,19кДж/кг
Du3-4=0,7243(813-610)=147,03кДж/кг
Du4-5=0,7243
(1269-813)=330,29 кДж/кг
Du5-1=0,7243
(370-1269)=-651,15 кДж/кг
Изменение энтальпии в любом процессе: Dh=Cp(Tj-Ti)
Dh1-2=1,013(520-370)=151,95кДж/кг
Dh2-3=1,013
(610-520)=91,17кДж/кг
Dh3-4=1,013(813-610)=205,64кДж/кг
Dh4-5=1,013
(1269-813)=461,93кДж/кг
Dh5-1=
1,013 (370-1269)=-910,69 кДж/кг
Изменение энтропии в любом процессе: DS=Ci-jln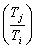
Ds1-2=-0,6488ln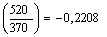 кДж/кгК
кДж/кгК
Ds2-3=0,7243ln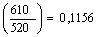 кДж/кгК
кДж/кгК
Ds3-4=1,013
ln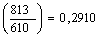 кДж/кгК
кДж/кгК
D s4-5=1,5906ln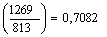 кДж/кгК
кДж/кгК
Ds5-1=0,7243ln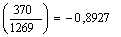 кДж/кгК
кДж/кгК
9. Количество работы изменения объема l,
совершаемой в каждом из процессов, и тепла q
подводимого (отводимого) в каждом из процессов составляющих цикл:
для процесса 1-2
l1-2=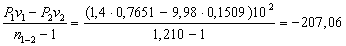 кДж/кг
кДж/кг
q1-2=C1-2(T2-T1)=-0,6488(520-370)=-97,32кДж/кг
для процесса 2-3
l2-3=0
q2-3=C2-3(T3-T2)=0,7243(610-520)=65,19
кДж/кг
для процесса 3-4
l3-4=P(v4-v3)=(0,2012-0,1509)11,7×102=58,85кДж/кг
q3-4=C3-4(T4-T3)=1,013(813-610)=205,64кДж/кг
для процесса 4-5
l4-5=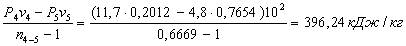 4-5=C4-5(T5-T4)=1,5906(1269-813)=725,31кДж/кг
4-5=C4-5(T5-T4)=1,5906(1269-813)=725,31кДж/кг
для процесса 5-1
l5-1=0
q5-1=C5-1(T1-T5)=0,7243(370-1269)=-651,15кДж/кг
10. Количество тепла q1,
подводимое в цикле:
q1=65,19+205,64+725,31=996,14кДж/кг
. Количество тепла q2,
отводимое в цикле: q2=-97,32-651,15=-748,47кДж/кг
. Полезная работа lц=-207,06+58,85+395,24=247,03кДж/кг
. Термический КПД цикла
ht=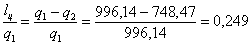
. Термический КПД цикла Карно
Таблица 2
|
Наименование
процесса
|
n кДж/кг
|
Du кДж/кг
|
Dh кДж/кг
|
Ds кДж/кг 0К
|
l кДж/кг
|
q кДж/кг
|
|
1-2
|
1,210
|
108,65
|
151,95
|
-0,2208
|
-207,06
|
-97,32
|
|
2-3
|
¥
|
65,19
|
91,17
|
0,1156
|
0
|
65,19
|
|
3-4
|
1
|
147,03
|
205,64
|
0,2910
|
58,85
|
205,64
|
|
4-5
|
0,6669
|
330,29
|
461,63
|
0,7082
|
395,24
|
725,31
|
|
5-1
|
¥
|
-651,15
|
-910,69
|
-0,8927
|
0
|
-651,15
|
Таблица 3
|
Наименование
расчетных величин
|
Значения
|
|
Подведенное
тепло, q1, кДж/кг
|
996,14
|
|
Отведенное
тепло q2, кДж/кг
|
-748,47
|
|
Работа
цикла lц, кДж/кг
|
247,03
|
|
КПД
цикла ht
|
0,249
|
|
КПД
цикла Карно htk
|
0,71
|
Первый закон термодинамики.
Вся подведенная к рабочему телу теплота идет на
изменение его внутренней энергии и на совершение работы.
q=Du+l
Для процессов: 1-2 q=Du+l;
3-4 q=Du+l;
4-5 q=Du+l;
5-1 q=Du
Второй закон термодинамики.
Теплота не может быть полностью превращена в
работу, поэтому КПД теплового двигателя никогда не может быть равен единице.
газовый теплоемкость энтропия цикл
Литература
1. В.Л. Ерофеев, П.Д. Семенов, А.С.
Пряхин «Теплотехника» изд. Академия, 2008
. М.М. Лавриков «Теплотехника», М.
Стойиздат, 1985г.
. «Общая теплотехника» М.-Л, 1963
. В.П. Исаченко, В.А. Осипова, А.С.
Сухомел «Теплопередача», 3 изд., М.,1975
. М.М. Хазен, Ф.П. Казакевич, М.Е.
Грицевский «Общая теплотехника», М. 1966
. В.А. Кириллин, В.В. Сычев, А.Е.
Шейндлин «Техническая термодинамика» 2 изд., М.,1974