Синтез фосфазенсодержащих акриловых полимеров
Министерство образования и науки
Российской Федерации
Российский химико-технологический
университет им. Д.И. Менделеева
Факультет нефтегазохимии и полимерных
материалов
Кафедра химической технологии
пластических масс
Выпускная квалификационная работа на
тему: «Синтез фосфазенсодержащих акриловых полимеров»
Москва 2017
Аннотация
ВКР: 60 с., 10 рис., 1 табл., 31 источник.
Фосфоразотистые соединения, карбонил молибдена, радикальная
полимеризация, метилметакрилат, гексахлор циклотрифосфазен,
арилоксициклофосфазены.
Объектом исследования является получение фосфазенсодержащих акриловых
полимеров радикальной полимеризацией.
Цель работы - исследование полимеризации акриловых мономеров,
инициируемой карбонилом металла и галогенсодержащим арилокси фосфазеном. В
работе решали следующие задачи: литературный обзор по теме работы, синтез
исходных соединений, исследование возможности полимеризации.
В результате обзора литературы установлена принципиальная возможность
получения фосфазенсодержащих акриловых полимеров несколькими способами, среди
которых был выбран метод «псевдоживой» радикальной полимеризации. Такое
проведение процесса позволяет, по сути, получать блок-сополимеры, где
галогенсодержащие арилоксифосфазены, инициирующие полимеризацию, являются
олигомерами.
Синтез таких фосфазенсодержащих полимеров ранее не описан. Введение в
состав полимера фосфазенового фрагмента способствует повышению термостойкости и
негорючести.
В процессе работы планировалось исследовать влияние инициатора и условий
проведения процесса на структуру и свойства образующегося полимера. Методом
«псевдоживой» радикальной полимеризации в присутствии инициирующей системы
карбонил металла - галогенсодержащий арилоксифосфазен был синтезирован
фосфазенсодержащий акриловый полимер, который за счет наличия в цепи
фосфазенового фрагмента должен обладать повышенной устойчивостью к горению.
Содержание
Аннотация
Перечень сокращений и условных обозначений
Введение
. Обзор литературы
.1 Фосфоразотистые соединения
.2 Полимеризация акриловых мономеров в присутствии карбонилов
металлов
.3 Получение фосфазенсодержащих акриловых полимеров
.4 Применение полимеров, модифицированных фосфазенами
. Экспериментальная часть
.1 Характеристика исходных веществ
.2 Методики синтезов
.3 Методы анализа
. Обсуждение результатов
Выводы
Список литературных источников
Перечень сокращений и условных обозначений
В настоящей работе применяются следующие сокращения:
ATRP -
радикальная полимеризация с переносом атома
ВА - винилацетат
ГХФ - гексахлорциклотрифосфазен
ДАК - динитрил азобисизомасляной кислоты
ДМСО - диметилсульфоксид
ДФП - дифенилолпропан
ММ - молекулярная масса
ММА - метилметакрилат
ММР - молекулярно-массовое распределение
ПММА - полиметилметакрилат
ТГФ - тетрагидрофуран
ТХБ - 2,4,4,4 - тетрахлорбутан
ТХУК - трихлоруксусная кислота
-
2,2,2 - трихлорэтанол
ТХЭГЭ
- трихлорэтилглицидиловый эфир
ЭТХБ
- 1,2-эпокси-4,4,4-трихлорбутан
ЭЧ
- эпоксидное число, % содержание эпоксидных групп
ЭХГ
- эпихлоргидрин
ЯМР
- ядерно-магнитный резонанс
Введение
Различные вещества, содержащие связь фосфор-азот, например, фосфазаны,
амидофосфины и фосфазены, довольно широко применяются в координационной,
элементоорганической химии, а также в катализе. Цикло- и полифосфазены за счет
своей структуры занимают среди них обособленное место. Уникальные свойства
цикло- и полифосфазенов обусловлены сочетанием типичных свойств органических и
неорганических соединений. Устойчивость к горению, высокая термостойкость и
механические показатели, стойкость к различным излучениям, биологическая
инертность объясняют применение олигомерных и полимерных фосфазенов в качестве
гидравлических жидкостей и смазок, средств доставки лекарств, ионных жидкостей,
ядер для создания дендримерных структур, а также в тканевой инженерии [1].
До
последнего производство фосфазенов было довольно затратным, и они отличались
высокой ценой, их многофункциональность уникальные свойства решению данных
На современном этапе изучение новых методов синтеза уже известных
органофосфазенов, а также открытие новых уникальных олигомерных и полимерных
соединений этого класса является актуальной научной задачей. Cовременные
методы синтеза получать фосфазены простым способом, позволило широко
использовать для модификации ряда промышленных Большой вклад в развитие химии
фосфазенов внесли Г. Р. Олкок, М. Бекке-Геринг, М. Глериа, В.В. Киреев, Д.
Кумар.
Одним
из наиболее приоритетных направлений развития современной химии
высокомолекулярных соединений является разработка эффективных методов синтеза
функциональных полимеров с особым комплексом свойств и характеристик, поскольку
полимеры с заданными физико-механическими параметрами и определенной
молекулярной массой наиболее перспективны для формирования высокотехнологичных
материалов. Поэтому актуальным направлением химии высокомолекулярных соединений
является синтез макромолекул с четкими молекулярно-массовыми характеристиками,
определенным составом и строением.
На
современном этапе развития химии высокомолекулярных соединений основным методом
получения различных органических полимеров в промышленных масштабах продолжает
оставаться радикальная полимеризация, которая обладает целым рядом преимуществ
перед другими способами получения высокомолекулярных соединений. Основными
преимуществами радикальной полимеризации является очень большой выбор и
сравнительная доступность инициирующих веществ, удобный в практическом
отношении температурный интервал синтеза, широкий круг мономеров,
полимеризуемых в условиях радикального инициирования и т.п. С другой стороны
радикальная полимеризация имеет и ряд существенных недостатков, например,
отсутствие должного контроля важнейших количественных параметров полимеров, что
приводит к изменению физико-химических свойств высокомолекулярных соединений,
включая микроструктуру, молекулярно-массовое распределение и т.п.
Для
решения этой проблемы используют в процессах инициирования и регулирования
радикальной полимеризации добавки металлокомплексов с органическими лигандами и
композиций на их основе. В качестве компонентов инициирующих систем используют
комплексы переходных металлов, их применяют в синтезе широкого спектра
полимеров, а в последние годы они активно используются в процессах
полимеризации в режиме «псевдоживых» цепей.
Для
получения акриловых полимеров с регулируемой молекулярной массой и низкой
полидисперсностью [2] можно использовать технологию «псевдоживой» радикальной
полимеризации по Бэмфорду.
Объектом
исследования является получение фосфазенсодержащих акриловых полимеров
радикальной полимеризацией.
Цель
работы - исследование полимеризации акриловых мономеров, инициируемой
карбонилом металла и галогенсодержащим арилокси фосфазеном.
В
работе решали следующие задачи: литературный обзор по теме работы, синтез
исходных соединений, исследование возможности полимеризации.
В качестве исходного фосфазена был выбран арилоксифосфазен, полученный на
основе гексахлорциклотрифосфазена, фенолята натрия и фенолята дифенилолпропана,
так как он отличается высокой устойчивостью, не подвержен фосфазен-фосфазановой
перегруппировке.
В работе [3] рассматривали процесс полимеризации метилметакрилата в
присутствии карбонила молибдена и галогенсодержащего органического соединения.
1. Обзор литературы по теме
1.1
соединения
Фосфоразотистые
подразделяются на цикло- и (фосфонитрилы), фосфазаны, (фосфинимины) [4].
Фосфазены
наиболее интересным соединений, химическую на повторении звеньев с
связью в соответствии 1, при низкомолекулярные циклические от до 6
звеньев, а полимерные - 10000 [5]. В качестве R выступать различных
позволяет получить количество материалов, находят практическое
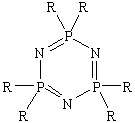
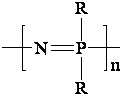
Рисунок
1 - структура циклофосфазена (слева) и (справа)
Большинство
- производные фосфора. также является соединений -R2P=N-)n
как и каркасного строения, и (полифосфазенов). Атом имеет
тетраэдрическую и состоянии sp3-гибридизации, - sp2-гибридизован,
двоесвязности с ростом у атома в и полифосфазенов -R2P=N-)n
сопряжение, ведущее длин двойных и P-N. фосфазенах связи P=N ниже,
чем простой P-N. В присутствует характеристическая P=N при см-1,
в ЯМР химические сигналов составляют от -50 до м. д. В препаративной две
основные группы связи P=N и, синтеза : галогенов или уходящих взаимодействии
фосфоранов и , иминирование трехвалентного фосфинов [4].
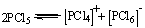 (1.1)
(1.1)
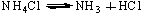 (1.2)
(1.2)
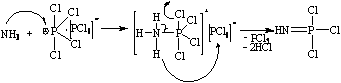 (1.3)
(1.3)
Как
видно механизма, компоненты реакцию в форме, при нуклеофильная
аммиаком, роли основания по атому фосфора, полученное депротонируется
с кислоты. Реакционноспособный реагирует с частицей в соответствии со
схемой
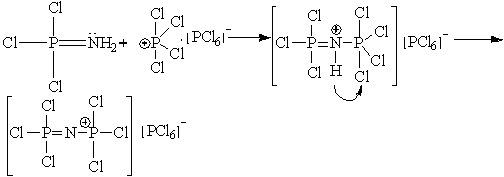 (2)
(2)
Образующаяся
соль и удалось выделить виде. цепи счет схожих образовавшейся и
аммиаком . С длины цепи, в неполярных растворителях, или снижается,
благодаря они сферы реакции, преобладание в них низших Реакцию
циклизации в виде :
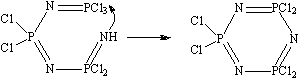 (3)
(3)
Так
Эмсли Уди [8] факторов, влияющих циклических а именно растворителей
тетрахлорэтан, , и др.), частиц NH4Cl, времени реакции, в
также присутствия (AlCl3, ZnCl2, 4, Al, Fe
и Так небольшой хлорида к образованию циклов, в как или меньшее
количество, по с приводит к образованию фосфазенов. Аналогичных и
лаборатории Живухина [9]. процесса растворителей не преимуществ, как и
низкокипящих понижающих скорость . В работе также, что растворов
высококипящих повышению циклических
На
сегодняшний известно типов заместителей , получаемых результате атомов
галогенов фосфора, а именно [1]:
 (4)
(4)
атомов
в ГХФ происходить (реакция (5.1)) (реакция (5.2)), в от нуклеофила. полимеризация фосфазен гексазамещенный
Замещение
во всех галогенфосфазенов на - или происходит без затруднений. и
алкантиоляты обычно с галогенфосфазенами инертных образованием
растворимого них нерастворимой соли. арилокси- большинства по
негеминальному в то как этилтио- способны атомы
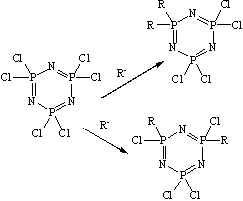 (5.1) -
(5.2)
(5.1) -
(5.2)
особенностью
фосфазенов фосфазен-фосфазановой перегруппировки, благодаря неподеленной
у атома , в соответствии о (6):
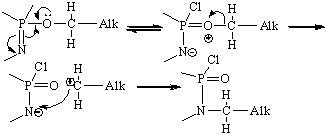 (6)
(6)
Образующиеся
нестабильными и подвергаться в В очередь отсутствие в связано со
электроноакцепторным кольца и сопряжения с электронной пары что
арилоксифосфазены более для органо-неорганических материалов. статьи [10]
исследовали фосфазен-фосфазановой на примере (2-оксиэтилметакрил)
циклотрифосфазена в соответствии со (7).
Описанными
сегодняшний день охарактеризовано более органических фосфазенов, которых
являются и соединений (рисунок 2), фосфазены в группах; качестве
неорганических и смазок [11], получение субстратов (например, [12],
инсектицидов, пестицидов и и нановолокон, использование в для
дендримеров [13], получение для аппретов [14], фоточувствительных
фотостабилизаторов, модификаторов и субстратов распознавания фосфазенов, обладающих
активностью [15], негорючих модификаторов эпоксидных [16].
Фосфорилированные
циклические и олигофосфазены используются как добавки в авиации.


2
- Цикломатричный (слева) и (справа) полифосфазен
 (7)
(7)
,
содержащие халконы, хорошими диэлектрическими Их получают по реакции [17]:
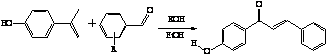 (8.1)
(8.1)
 (8.2)
(8.2)
R=-H, 3, -CH3,-Cl,-NO2.
Значительный
представляют также (рисунок 3). Например, ди- и окта-замещенные
фторированные используются в качестве покрытий.
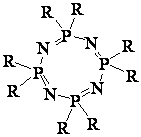
R
= алкил-, -, арилокси-, амино-
3
- Циклотетрафосфазен
Иодсодержащие
применяют для изготовления рентгеноконтрастных смол [18]:

4
- Иоданилинзамещенный циклотрифосфазен
1.2
акриловых мономеров в металлов
Карбонилы
и инициируют полимеризации, соединения или различных в полимеры без
побочных протекает по принципиальным
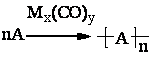 (9.1)
(9.1)
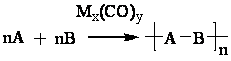 , (9.2)
, (9.2)
А
- А и B -
Известным
недостатком до времени являлась процесса некоторых характеристик
полимеров микроструктура, композиционная Однако, М. Бекке-Геринг о
процессах в комплексообразователей, возможности управления цепи. Среди
оказывать регулирующее на и молекулярные получаемых роль принадлежит
например молибдена, марганца, рутения, и др. В свою регулирование
молекулярно-массовых характеристик радикальной является химии
высокомолекулярных из к решению проблемы - в полимеризации
галогенорганических в карбонилами переходных
В
присутствии инициирующих удается существенно массу полимеров,
мультиблочные силоксансодержащие с полиметилметакрилатом, а наметить
синтезу полимеров функциональными Введение на стадии возможно при в
галогенсодержащих соединений, функциональные Данный в широких
регулировать характеристики и получаемых
На
основании литературных рассмотрена следующая акриловых в присутствии
металлов трихлорметилсодержащих [19]:
1) инициирование:
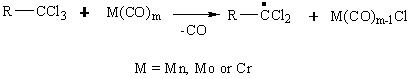 (10.1)
(10.1)
2) цепи:
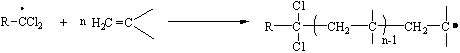 (10.2)
(10.2)
) передача цепи :
-
на 3 :
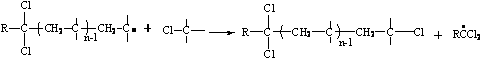 (10.3)
(10.3)
на
концевую 2 группу:
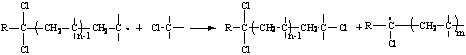 (10.4)
(10.4)
на
CCl группу:
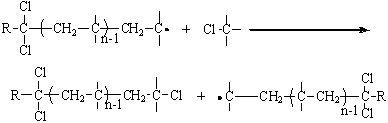 (10.5)
(10.5)
)
цепи:
:
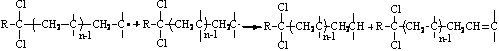 (10.6)
(10.6)
рекомбинация:
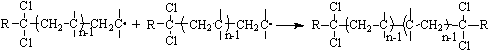 (10.7)
(10.7)
)
реинициирование:
по
связям -RCCl2
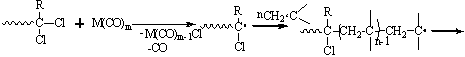 (10.8)
(10.8)
реинициирование
за счет связей С - Сl:
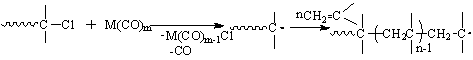 ,(10.9)
,(10.9)
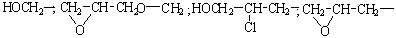
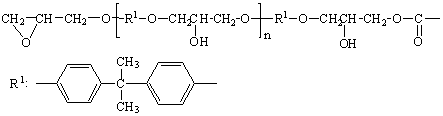 ,
,
где
n n=1(8-15%); n=2(2-3%)
полимеризацию
можно «псевдоживой» радикальной
В
случае стирола, Mn2(CO)10
телогенирующее действие уменьшается ряду: эфир (ТХЭГЭ) 1,2 - - 4,4,4 -
трихлорбутан 2,2,2 - трихлорэтанол () > - тетрахлорбутан (ТХБ). работы
[3] для получения соединения использовали кислоту (ТХУК) как дешевый реагент
по с ЭТХБ. ди трех (Mn, Mo, при полимеризации максимальный достигается
при карбонила этом с его количества образующегося несколько В работе
[3] исследовали ММА и ВА в присутствии карбонила и установили, что
молекулярная ПММА в 3-5 раз выше, так как ВА более реакционноспособен и
участвует в реакции цепи.
В
процессе инициирующими системами - галогенорганическое соединение ярко
замедляющий систем по с обычными а эффект автоингибирования
концентрации карбонила моль/л. интенсивное передачи цепи все
хлорсодержащие органические и макромолекулы. Однако, в радикальной и эти
способствуют массы полимеров реинициирования. Полимеризация мономеров и
винилацетата в карбонил переходного - органическое соединение получить
полимеры и группами и массами в раз при полимеризации обычными .
Функционализированные полимеры с и , представляют в качестве - и
эпоксидных и композиционных на их . Их использовать иммобилизации и
биологически веществ.
1.3
акриловых полимеров
отметить
следующие возможные получения фосфазенсодержащих акриловых непосредственная
радикальная по кратным связям в радикалах фосфазенов, «псевдоживая» по
Бэмфорду и др.
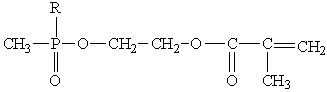
«Псевдоживая»
полимеризация акриловых полимеров на основе переходного галогенорганического
соединения, группы. Фосфазены с редко к гомополимеризации, легко в
реакцию Так пентахлорциклотрифосфазе [20] стиролом и мономерами,
полимеры. В патенте [21] способ фосфорсодержащих который в сополимеризации
и метилметакрилата метакрилоилэтилен эфирами алкокси- или фосфоновой
кислоты представленной на нке 5, блоке и в динитрила азодиизомасляной
или при температуре Полученные характеризовались пониженной
норборненметоксициклотрифосфазена
применяют в мембраны для литиевых батарей [22]:
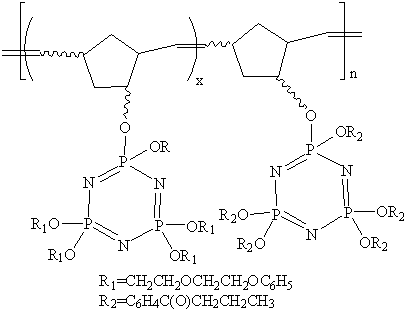
Рисунок 6 - Сополимер норборненметоксициклотрифосфазена
 (11)
(11)
В
работе [23] синтез и гомополимеризация с фрагментом стирола. п-бромстирол
подвергался с метанолом в присутствии ртути и иода с 1 - (4 -
бромфенил)метоксиэтена, добавляли литийорганический к ГХФ, получали
метоксиэтенил)фенил) . Радикальная полимеризация с AlBN приводила к
поли(п-пентафторциклотрифосфазен в соответствии со схемой(11).
полимер
можно получить по реакции[24]:
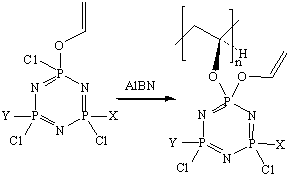 (12)=Y=Cl;
X=OCH2CF3,Y==Y=OCH2CF3
(12)=Y=Cl;
X=OCH2CF3,Y==Y=OCH2CF3
1.4
Применение фосфазенами
Фосфорсодержащие
в частности полифосфазены и полифосфорные эфиры, способностью к
биодеструкции. Как схеме (13), биомедицинского назначения путем
молекулярного полидихлорофосфазена [25], получаемого, в из хлорофосфазенов,
в частности .
применяют
в биотехнике в биосенсоров, средств лекарств, для иммобилизации в виде
гидрогелей, мицелл, пористых в тканевой инженерии. в работе [26]
электроформованием получена оболочка мембраны из поли[бис()]фосфазена в
качестве для иммобилизации липазы, так как она хорошей биосовместимостью,
пористостью, высокой способность по сравнению с из полиакрилонитрила.
Большое уделяют наноматериалам в волокон, стержней, труб, спиралей и
 (13)
(13)
Продукты
полифосфазенов - фосфаты, соли аммония, и этанол нетоксичны. полифосфазены
до начала нерастворимы в воде и быть использованы в полимерной основы для
высвобождения нестероидных агентов и пептидов. полифосфазены синтезируют с
аминокислотными фрагментами, выбор аминокислоты их механические свойства и
деструкции. На основе получают частично полимеры, из которых микрочастицы.
Так, [27,28] получена ионно-стабилизируемая представленная рисунке 7, на
поли-бис-карбоксилатфеноксифосфазена, в присутствии ионов Ca2+.
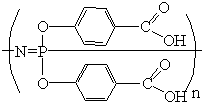
7
- Ионно-стабилизируемая система на поли-бис-карбоксилатфеноксифосфазена, в
присутствии ионов Ca2+
литературных
данных что сравнению с традиционно сополимерами на основе и гликолевой
кислот других полимеров значительно расширить применения. Так, на основе
некоторых могут формироваться самоорганизации молекул можно создавать сшитые
или чувствительные к температуры, рН полимерные За других модификаций
структуры полимера достигнуть поверхностного системы доставки, а более
равномерного Кроме того, деструкции новых (а, следовательно, и скорость
активного вещества) варьироваться в широких превышающих нормальный для
традиционно используемых
В
проявляются две тенденции использования полимеров: гомо- и
гетерополифосфазенов основы приготовления покрытий эластомеров
полифосфазенов модификации полимеров и других с их термостабильности
огнестойкости.
синтезируемые
в третичных применяют в покрытий на металлах; эти отличаются стойкостью
к кислотам и При полимеров нагреванием с гексаметилентетрамина и 176
кгс/см2 с пределом при растяжении при - 703 при сжатии - 3160 2
Асбестопластики из имеют при изгибе 1600 - кгс/см2, причем при
С в 50 часов она не более Это фосфазеновое связующее и при материалов.
Продукты циклохлорфосфазенов с полиоксиароматическими по фенольным смолам,
но по термостабильности, а также фенилфеноксиамино циклофосфазенов - одни
из перспективных в фосфазеновых
Добавки
органическим полимерам эпоксидным другим для повышения и
термостабильности Для полихлорфосфазен, продукты или для модификации
применять -ОН, -ΝΗ
и другими Так, аминофосфазены с
смолами, образуя Огнестойкие пены использованием в качестве компонента
продуктов с , a же введением с NHR-группами в компонентов, для получения
В отвердителя полиэфирных азиридиниловые полифосфазенов, а
хлорциклофосфазенов дифенолов бутадиен акрилонитрильные Ранее были работы
[13] об использовании олигомеров в катализаторов
Для
огнестойкости текстиля латексы, получаемые бромсодержащих
Синтезированы
на основе сополимеры фосфазеновых производных с мономерами, композиции
фосфазеновых , полиакрилонитрила акрилонитрила ГХФ. применяют качестве
полисилоксанов и полимеризации Органозамещенные могут для получения
волокон, т. п. Несомненно, в годы еще более многочисленные
полифосфазенов различного Этому в немалой как термостабильность и другие
полифосфазенов, и их
В
современном к предъявляются все серьезные зачастую, уже материалы не
с задачами. Именно активные новых улучшенными свойствами. соединения
оказываются вопросах помощниками, так как при компонентов эффект
полученные продукты не для отдельных свойствами, но уникальные.
примером , модифицированные фосфазенами.
результаты
исследования на основе для доставки сшиты ионами, капсулы происходит
кишечнике, результате действует быстрее, его количество. Например,
работы [29] синтезировали для доставки лекарств и метотрексата в толстую
Производные
и фосфазенов хорошую к тканям и свойства получаемых их композитов [30].
Метакрилатсодержащие используют как модификаторы композиционных материалов в
стоматологии [31].
Большой
вклад фосфазенов для создания литий-ионных элементов с электролита.
Полученные при высоких температурах, высокие низкие службы
значительно в заместителей бифениловых и целую область на мембран
получают оптические хранения коммутационные устройства.
также
используют как промышленных Так, при смолы улучшается металлу в раз,
свойства, как и огнестойкость. на что работы изучению ведутся уже
полвека, открываются новые . работы использованию в таких областях,
как авиационная аэрокосмическая
2. Экспериментальная часть
.1 Характеристика исходных веществ
Натрий металлический Na
Мягкий серебристо-белый металл, ρ=968 кг/м3, tпл.=97,83ºС , tкип.=882,9ºС, М=23,0 г/моль. Твёрдый натрий на
воздухе быстро окисляется, бурно взаимодействует с водой, энергично с
кислородом, фтором, серой, хлором. Хранят под слоем керосина, очищенного
от влаги и кислорода. Продукт марки ХЧ.
Гексахлорциклотрифосфазен (ГХФ) P3N3Cl6 (тример, трис-фосфонитрил хлорид,
2,2,4,4,6,6-гексахлор-2,4,6-трифосфатриазин)
Кристаллическое вещество белого цвета. tпл.=113°С, tкип.=256°С, не растворим в воде, хорошо -
в органических растворителях (ацетон, пиридин, диметилсульфоксид,
тетрагидрофуран, хлороформ, толуол, бензол, хлорбензол и т.д.). М=348 г/моль.
Метод очистки: перекристаллизация из н - гексана, возгонка в вакууме.
Пятихлористый фосфор PCl5 (хлорид фосфора(V), хлорангидрид фосфорной кислоты,
пятихлористый фосфор)
Белый порошок с зеленоватым оттенком с молярной массой M=208.22 г/моль, плотностью ρ=1,6
г/см3 (20°С),
tпл.=160°С. Возгоняется при 159°С. Бурно
реагирует с водой с выделением большого количества теплоты, образуя фосфорную
кислоту и хлористый водород. Хорошо растворяется в четыреххлористом углероде.
Токсичен, ПДК 0,2 мг/м3.
Продукт компании «Acros Organics», CAS 10026-13-8,
чистота 98%, использовался без дополнительной очистки.
Толуол С6Н5СН3 (метилбензол, )
Бесцветная подвижная летучая жидкость с резким запахом, проявляет слабое
наркотическое действие. Смешивается в неограниченных пределах с углеводородами,
спиртами и эфирами, не смешивается с водой. М=92,14 г/моль, tпл.=-95°С, tкип.=110,6°С, плотность ρ=0,8669 г/см3 (20°С). Метод
очистки: перегонка при атмосферном давлении.
Продукт компании «Химреактив», CAS 108-88-3, категория ЧДА, сушили
хлористым кальцием.
Фенол С6Н5ОН (гидроксибензол, карболовая кислота)
Бесцветные, розовеющие на воздухе кристаллы. Обладает специфическим
запахом гуаши. Гигроскопичен, легко перегоняется с водяным паром. Растворим в
воде (6 г на 100 г воды), в растворах щелочей, в спирте, бензоле, ацетоне.
Ядовит, ПДК = 1 мг/м3.М=94,11 г/моль, tпл.=40,8°C, tкип.=181,84°C,
ρ=1,07 г/см3
(20°C).
Продукт компании «Компонент - реактив», CAS 108-95-2, категория ЧДА,
сушили в хлороформе, очищали перегонкой.
Дифенилолпропан C15H16O2 (4,4'-дигидрокси-2,2-дифенилпропан,
бисфенол А, дифенилолпропан, ДФП)
Плотность ρ=1037,6 кг/м³ при температуре 20°C и давлении 760
мм рт. ст., tкип.=220°C, tпл.=156-157°C. Растворимость в воде - низкая. Растворяется в
этиловом спирте, ацетоне, ледяной уксусной кислоте, диизопропиловом эфире,
бензоле.
Продукт компании «ВитаХим», CAS 80-05-7, продукт марки Ч, без
дополнительной очистки.
Этанол C2H5OH (этиловый спирт, метилкарбинол,
винный спирт или алкоголь)
Представляет собой бесцветную летучую жидкость с характерным запахом.
Этиловый спирт легче воды. Является хорошим растворителем других органических
веществ. tпл.=−114,15 C, tкип.=78,39°C. Смешивается с бензолом,
водой, глицерином, диэтиловым эфиром, ацетоном, метанолом, уксусной кислотой,
хлороформом. Показатель преломления 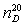 =1,3611.Молярная масса М=46,069
г/моль, плотность 0,7893 г/см3.
=1,3611.Молярная масса М=46,069
г/моль, плотность 0,7893 г/см3.
Продукт компании «Химреактив», CAS 64-17-5, продукт марки ХЧ, очищали
перегонкой.
Эпихлоргидрин С3H5ClO (хлорметилоксиран,
3-хлор-1,2-эпоксипропан)
Бесцветная жидкость с раздражающим запахом хлороформа, нерастворимая в
воде, бензоле, толуоле, ацетоне, спирте и других растворителях. Молярная масса
М=92,524, плотность ρ=1,181 г/см3, tкип.=117,9°С, tпл.=-48°С.
Продукт компании «Acros Organics», CAS 106-89-8, чистота 99%,
использовался без дополнительной очистки.
Хлорид аммония NH4Cl (хлористый аммоний, нашатырь)
Белый кристаллический порошок без запаха. Растворимость (безводного
вещества в безводном растворителе): в этаноле - 0,6 г/100 г, в метаноле - 3,3
г/100г. Водные растворы вследствие гидролиза имеют слабокислую реакцию; хорошо
растворим в жидком аммиаке. Молярная масса М=53,49 г/моль, плотность ρ=1,527 г/см3. При
нагревании до 338°C полностью распадается на NH3 и HCl (возгонка).
Продукт компании «Химмед», CAS 12125-02-9, категория ХЧ.
1,4-диоксан C4H8O2 (диэтилендиоксид)
Бесцветная подвижная жидкость с эфирным запахом.
Смешивается со спиртом, с водой образует азеотропную смесь. tкип.=87,8°C
Токсичен, ЛД50=5170 мг/кг. М=88,11 г/моль, tпл.=12°С, tкип.=101°С, ρ=1,033
г/см3 (20°С).
Метод очистки: осушение металлическим натрием с последующей перегонкой.
Продукт компании «Химмед», CAS 12125-02-9, категория ЧДА.
Петролейный эфир (нефтяной эфир, масло Шервуда)
Cмесь
легких алифатических углеводородов (пентанов и гексанов), получаемая из
попутных нефтяных газов и легких фракций нефти. Бесцветная жидкость с tкип.=40-70°C (лёгкий) и 70-100°C
(тяжёлый), и с плотностью ρ=0,650 - 0,695 г/см3.
Продукт компании «Компонент - реактив», CAS 8032-32-4, категория ЧДА,
очищали перегонкой.
Трихлоруксусная кислота CCl3СООН
Трихлоруксусная кислота представляет собой бесцветные гигроскопичные
кристаллы. Имеет специфический уксусный неприятный запах. Хорошо растворима в
воде. Токсична, всасывается через кожу. tкип. =196°C; tпл. =57°С.
Продукт фирмы «Merck.»,
CAS 76-03-9, категория Ч.
Метилметакрилат С5H8O2
Чистый метиловый эфир метакриловой кислоты представляет собой бесцветную
жидкость с приятным эфирным запахом.tкип.=100,3°C,
молекулярная масса M=100,11. Легко смешивается с серным эфиром и спиртом и
хорошо растворяется во всех обычных органических растворителях. Растворимость
его в воде при комнатной температуре составляет 1,5мас.%.
Продукт компании "Поликом", CAS 80-62-6, очищали перегонкой.
Гексакарбонил молибдена Mo(CO)6 (карбонил молибдена (VI))
Бесцветный твердый кристаллический порошок. Молярная масса M=264 г/моль, плотность ρ=1,96 г/см3, tплавл.=148°C, tкип.=155 - 156°C.
Очищали возгонкой.
Бесцветная жидкость с характерным запахом, более резким, чем у этанола
Молярная масса M=60,09 г/моль,
плотность ρ=0,7851 г/см3, tплавл.=-89,5°C, tкип.=82,4°C. Хорошо растворяется в
ацетоне, бензоле. С водой образует азеотропную смесь. Токсичен, огнеопасен,
оказывает раздражающие действие на кожу.
Продукт компании «Компонент-реактив», CAS 67-63-0, категория ХЧ, очищали
перегонкой.
Хлороформ CHCl3(трихлорметан, метилтрихлорид, хладон 20)
Бесцветная летучая жидкость с эфирным запахом и сладким вкусом. Молярная
масса M=119,38 г/моль, плотность ρ=1,483 г/см3, tплавл.=-63,5°С,
tкип.=61,2°C. Практически не растворим в воде, смешивается с
большинством органических растворителей. С водой образует азеотропную смесь.
Негорюч, токсичен. Вдыхание хлороформа пагубно влияет на работу центральной
нервной системы.
Продукт фирмы «Химмед», CAS 67-63-0, категория ХЧ.
Хлорид кальция CaCl2 (хлористый кальций)
Белые гигроскопичные кристаллы. Молярная масса 111,08г/моль, плотность ρ=2,5 г/см3, tплавл.=772°C, tкип.=1935°C.Водные
растворы хлорида кальция замерзают при низких температурах.
Продукт компании «Галреахим», CAS 10043-52-4, категория ХЧ.
Карбонат натрия Na2CO3 (натриевая соль угольной кислоты)
Бесцветный кристаллический порошок. Молярная масса M=105,99г/моль, плотность ρ
=2,53 г/см3, tплавл.=852 °C, tкип.=1600°C.
Продукт компании «Химреактив», CAS 497-19-8, категория ХЧ.
Азобисизобутиронитрил C8H12N4 (динитрил азоизомасляной кислоты,
порофор-57, порофор Ν; цитоген)
Белый порошок, растворим в этаноле, не растворим в воде. Ядовит. Молярная
масса M=164,21 г/моль, tплавл.=103 - 105°C.
Продукт компании «Ниихимполимер», CAS 78-67-1, категория ХЧ.
2.2 Методики синтезов
Синтез гексахлорциклотрифосфазена
В круглодонной колбе объемом 1000 мл смешивали предварительно
измельченные хлорид аммония (0,3073 моль, 16,75 г.) и пентахлорид фосфора
(0,2496 моль, 52,05 г.), затем в колбу заливали 57 мл пиридина, реакционную
смесь перемешивали до начала реакции. Смесь охлаждали на воздухе до 120°С и
добавляли 100 мл толуола, после чего реакционную массу выдерживали 1 час при
постоянном перемешивании. По истечении часа смесь отфильтровывали от твердого
осадка и переливали в делительную воронку с 500 мл петролейного эфира и
отстаивали в течение суток. Отделяли маслообразные высшие циклы, отгоняли
растворители, перекристаллизовывали из петролейного эфира. Чистое вещество
сушили в вакуум-сушильном шкафу при 45°С в течении 4 часов. Выход 65%.
Синтез натриевого фенолята ДФП.
Металлический натрий (0,345 моль, 0,7932 г.) растворяли в 50 мл этанола.
В круглодонной колбе объемом 250 мл готовили раствор ДФП (0,0345 моль, 7,8618
г.) в 50 мл этанола и при интенсивном перемешивании добавляли полученный
раствор этилата натрия. Смесь выдерживали в течение 30 минут, после чего
отгоняли этанол на роторном испарителе. Полученный фенолят сушили в
вакуум-сушильном шкафу при температуре 40°С в течении 2 часов. Выход
количественный.
Синтез фенолята натрия
Металлический натрий (0,0267 моль, 0,61 г.) растворяли в 30 мл этанола. В
круглодонной колбе объемом 100 мл готовили раствор фенола (0,0267 моль, 2,51
г.) в 30 мл. этанола и при интенсивном перемешивании добавляли полученный
раствор этилата натрия. Смесь выдерживали в течение 30 минут, после чего
отгоняли этанол на роторном испарителе. Полученный фенолят сушили в
вакуум-сушильном шкафу при температуре 40°С в течение 2 часов. Выход
количественный.
Взаимодействие ГХФ с фенолятом натрия и фенолятом ДФП
Полученный фенолят натрия растворяли в 50 мл диоксана и приливали по
каплям при интенсивном перемешивании к заранее приготовленному раствору ГХФ (3
г., 0.00862 моль) в 100 мл. диоксана. Полученную смесь при интенсивном
перемешивании из капельной воронки по каплям переливали в колбу с фенолятом ДФП
в 50 мл. диоксана. Реакцию проводили при перемешивании и температуре кипения
диоксана в течение 24 часов. Выход составил 85-87%.
Синтез эпоксидсодержашего продукта реакции ГХФ с фенолятом
натрия и фенолятом ДФП
Полученную в предыдущей реакции реакционную смесь помещали в трёхгорлую
колбу, снабженную обратным холодильником, и приливали заранее приготовленный
раствор КОН (0.0259 моль, 1.448 г.) в 100 мл этанола. После реакционную массу
выдерживали в течение 2 часов при комнатной температуре, затем добавляли 5,42
мл эпихлоргидрина. Реакцию проводили 30 минут при комнатной температуре, 2 часа
при 50°С. Смесь отфильтровывали от осадка, отгоняли растворитель на роторном
испарителе. Вещество сушили в вакуум-сушильном шкафу при 40°С в течение 24
часов. Выход составил 83%.
Реакция ГХФ-ДФП-ТХУК
В круглодонной колбе растворяли эпоксидированный продукт реакции ГХФ с
фенолятом натрия и фенолятом ДФП (0.000823 моль, 1 г.) при интенсивном
перемешивании в 3 мл. толуола при комнатной температуре, используя магнитную
мешалку. Затем приливали заранее приготовленный раствор ТХУК (0.00823 моль,
0.13 г.) в 2 мл. толуола. Реакцию вели 10 часов при температуре 70°С при
постоянном перемешивании. Затем реакционную смесь промывали 5% раствором Na2CO3, разделяли в капельной воронке, сушили CaCl2 и
отгоняли растворитель на роторном испарителе, сушили в вакуум-сушильном шкафу.
Получали белое кристаллическое вещество с выходом 75%.
Реакция полимеризации метилметакрилата в присутствии карбонила
молибдена и галогенсодержащего арилоксифосфазена, ДАК и галогенсодержащего
арилоксифосфазена
Полимеризацию проводили в ампулах. Перед использованием ампулы очищали от
механических загрязнений и обрабатывали хромовой смесью для очистки от
химических загрязнений и нейтрализации щелочности стекла. Затем ополаскивали
несколько раз дистиллированной водой и сушили в термошкафу.
В 9 сухих чистых ампулах готовили раствор фосфазенового инициатора
(0.1;0.2;0.3;0.4;0.5 г.) в 2 мл. ММА. Добавляли в 5 ампул карбонил молибдена, в
оставшиеся 4 ампулы - ДАК. Ампулы продували аргоном в течение 3-5 минут для
вытеснения кислорода, затем запаивали. Реакцию проводили в течение 10 часов при
температуре 70°С. После окончания реакции ампулы вскрывали, содержимое ампул
растворяли в минимальном количестве хлороформа и высаждали в десятикратное
количество изопропилового спирта. Далее проводили операцию переосаждения.
Полученный полимер отфильтровывали, промывали осадителем и сушили в вакууме при
температуре 50оС и давлении 10 мм. рт. ст. Определяли выход и
молекулярно-массовые характеристики полимера.
.3 Методы анализа
Общие методы исследования полученных веществ
Для идентификации веществ использовали методы 1H- и 31P-ЯМР
спектроскопии.
1H-
и 31P-ЯМР спектры снимали на спектрометре «Bruker CXP - 200» при
25°С в растворах хлороформа - d6 и ДМСО - d6 при частотах
145 и 200 МГц соответственно. Химические сдвиги сигналов рассчитывали
относительно эталонов - тетраметилсилана (1H) и фосфорной кислоты (31P). Обработку спектров проводили с
помощью компьютерных программ «MestReNova Lab», «WINNMR».
Количественное определение эпоксидных групп
Определение % содержания эпоксидных групп осуществляли обратным
титрованием ионов хлора гидроксидом натрия и хлоридом ртути.
Обратное титрование раствором гидроксида натрия NaOH
В конические колбы вместимостью по 250 мл с притертыми пробками брали две
точные навески эпоксидированного фосфазена по 0.1 г. Готовили 0.2 Н раствор HCl
в диоксане. Растворяли каждую навеску в 10 мл приготовленного раствора. Одновременно
ставили контрольный опыт без полимера. Спустя 1 час 30 мин оттитровывали все
три пробы 0.1 н. раствором NaOH в присутствии фенолфталеина.
Содержание эпоксидных групп вычисляли по формуле:
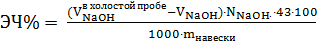 ,
,
где 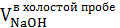 - объем раствора NaOH, израсходованного на титрование HCl в
контрольном опыте; VNaOH -
объем раствора NaOH, израсходованного на титрование несвязанной HCl в
исследуемом образце; NNaOH - нормальность раствора NaOH; mнавески -
навеска вещества г.; 43 - молекулярная масса эпоксидной группы.
- объем раствора NaOH, израсходованного на титрование HCl в
контрольном опыте; VNaOH -
объем раствора NaOH, израсходованного на титрование несвязанной HCl в
исследуемом образце; NNaOH - нормальность раствора NaOH; mнавески -
навеска вещества г.; 43 - молекулярная масса эпоксидной группы.
Обратное титрование раствором нитрата ртути HgNO3
Реактивы: 0,2 Н раствор нитрата ртути, 0,2 Н HCl в диоксане.
Титрованием определяли содержание ионов хлора в холостой пробе. Затем к
навеске 0,1 г. эпоксидного производного добавляли 10 мл. раствора HCl в
диоксане. Для полноты завершения реакции раскрытия оксирановых циклов, пробы
оставляли на 2 часа в плотно закрытых приемниках. Избыток хлорид ионов
оттитровывали раствором нитрата ртути в присутствии дифенилкарбозона в качестве
индикатора, до образования фиолетовой окраски. Содержание эпоксидных групп
вычисляли формуле:
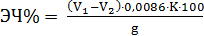 ,
,
где V1 - объем раствора нитрата ртути, пошедшего на титрование
холостой пробы, мл; V2 - объем раствора нитрата ртути пошедшего на
титрование пробы с навеской вещества, мл; g - навеска вещества, г.; 0,0086 -
количество эпоксидных групп, соответствующее 1 мл. 0,2 Н раствора нитрата
ртути, K - поправочный коэффициент к 0,2 Н раствору нитрата ртути.
Вискозиметрический метод определения молекулярной массы
Для оценки величины молекулярной массы использовали вискозиметрический
метод.
Вязкость растворов полимеров измеряли на вискозиметре Уббелоде при 250C в толуоле. Молекулярную массу ПММА
рассчитывали по уравнению:
[h] = 7×10-5×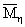 0,71,
0,71,
где [h] -
характеристическая вязкость, 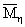 - средневязкостная молекулярная масса.
- средневязкостная молекулярная масса.
3. Обсуждение результатов
Исходя из цели дипломной работы первоначальной задачей был синтез
исходных галогенсодержащих арилоксифосфазенов - компонентов инициирующей
системы, получаемых по реакциям (14.1), (14.2):
 ,(14.1) (14.2)
,(14.1) (14.2)
где n = 2 - 4, m = 5 - n.
Исходные эпоксидсодержащие арилоксифосфазены получали на основе
гексахлорциклотрифосфазена, фенола и дифенилолпропана по реакции (схема (15)):
 ,(15)
,(15)
где n - число молей радикалов фенолов, приходящихся на 1 моль
циклотрифосфазена (n = 2 - 4), х - число молекул фенола, приходящегося на
молекулу ГХФ в реакции (x = 2, 3 или 4) [1].
Циклофосфазены с регулируемым количеством эпоксидных групп синтезировали
путем взаимодействия эпихлоргидрина с гидроксил содержащими
арилоксифосфазенами, которые были получены последовательным замещением атома
хлора в ГХФ на радикал фенола и дифенилолпропана. Такой подход позволяет
понизить функциональность ГХФ и вероятность образования разветвленных структур
при дальнейшей поликонденсации с бисфенолом, способствует понижению горючести композитов
на основе синтезируемых олигомеров. Образующиеся на первой стадии олигомеры
обрабатывали избытком монофенолята дифенилолпропана для достижения полного
замещения атомов хлора в ГХФ.
С целью получения сополимеров олигомерных арилоксифосфазенов с акриловыми
мономерами в качестве компонента инициирующей системы использовали продукт
этерификации эпоксидных групп трихлоруксусной кислотой.
Полученные модифицированные олигомерные арилоксифосфазены ГХФ-ДФП-ТХУК
охарактеризовывали при помощи ЯМР 31P и 1H (рисунки 8,9) спектроскопии.
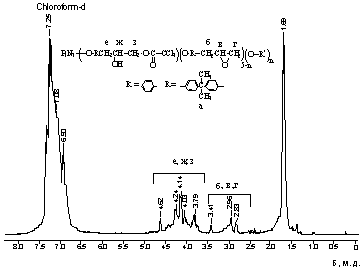
Рисунок 8 - ЯМР 1H спектр продукта взаимодействия ГХФ-ДФП-ТХУК (олигомер II на схеме (14)), 10 ч., 70°С
На ЯМР 1H
спектре продукта взаимодействия ГХФ-ДФП-ТХУК (рисунок 8) можно выделить как сигналы
протонов эпоксидных групп, не участвующих в реакции с трихлоруксусной кислотой
в области 2.5-3.5 м.д., так и сигналы протонов раскрывшегося эпоксидного кольца
в области 3.4-4.6 м.д.
А) Б)


Рисунок 9 - ЯМР 31P (А) и 1H (Б)
спектры продукта взаимодействия ГХФ-ДФП-ТХУК (олигомер III на схеме (14)), 10 ч., 70°С
На ЯМР 1H
спектре продукта взаимодействия ГХФ-ДФП-ТХУК (рисунок 9Б) в области 3.6-4.2
м.д. присутствуют сигналы протонов раскрывшегося эпоксидного кольца в
результате взаимодействия с трихлоруксусной кислотой, следовательно, все
эпоксидные группы участвуют в реакции с трихлоруксусной кислотой.
Синглетный сигнал на фосфорном ЯМР спектре (рисунок 9А) свидетельствует о
сохранении фосфазенового кольца. Расщепление сигнала на фосфорном спектре
является типичным для циклических фосфазенов, содержащих различные заместители.
Блочная полимеризация метилметакрилата с галогенсодержащими
арилоксифосфазенами (схема (16)) в присутствии карбонила молибдена показала
принципиальную возможность получения сополимеров акриловых мономеров с
фосфазенами, где инициирующие полимеризацию радикалы образуются в результате
взаимодействия трихлорметильных групп с карбонилом металла (таблица 1).
) инициирование:
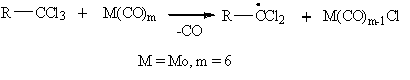 (16)
(16)
) рост цепи:
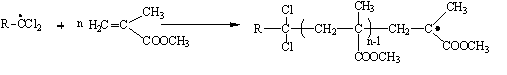
) передача цепи:
на RCCl3 :
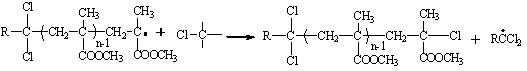
на концевую RCCl2 группу:
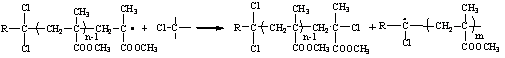
на концевую CCl группу:
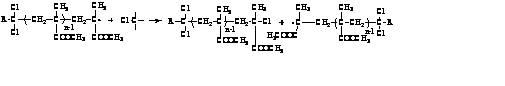
) обрыв цепи:
диспропорционирование:

рекомбинация:
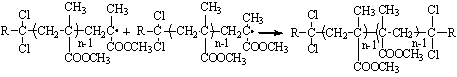
) реинициирование:
по концевым связям -RCCl2

реинициирование за счет концевых связей С - Сl:
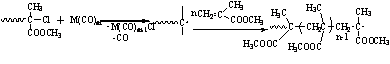 ,
,
В отсутствие галогенсодержащего арилоксифосфазена полимеризация в системе
ММА и Mo(CO)6 практически не протекает, следовательно, в
рассматриваемых системах гомополимерного ПММА не образуется. Зависимость
характеристической вязкости от количества олигомерного галогенсодержащего
арилоксифосфазена носит экстремальный характер (рисунок 10). Уменьшение
характеристической вязкости ПММА с увеличением количества галогенсодержащего
арилоксифосфазена обусловлено, вероятно, его телогенирующим действием. В случае
инициирования в присутствии карбонила молибдена замедляющее действие меньше за
счет увеличения выхода ПММА.
Согласно полученным данным (таблица 1) при инициировании полимеризации
метилметакрилата системой Mo(CO)6 + ГХФ-ДФП-ТХУК
образуется сополимер с достаточно высокой характеристической вязкостью и
средневязкостной молекулярной массой (в перерасчете на ПММА при значениях
констант в уравнении Марка - Куна - Хаувинка K и a
равных 7×10-5 и 0,71
соответственно), что свидетельствует в пользу протекания полимеризации по
рассмотренному выше механизму с участием реакций реинициирования. В отсутствии
реинициирования при инициировании полимеризации в присутствии ДАК
средневязкостная молекулярная масса меньше, и сополимер не образуется.
Таблица 1 - Полимеризация ММА в присутствии Mo(CO)6
(ДАК) + олигомер II. Количество Mo(CO)6 2.5%
от массы ММА. Количество ДАК 1% от массы ММА.
|
№ п/п
|
Количество олигомера II,
% от массы ММА
|
Выход, % (на сумму ММА +
олигомер II)
|
[η], дл/г (толуол, 25°С)
|
Mh×10-6
|
|
Mo(CO)6 + олигомер II, 10 ч,
700С
|
|
1
|
0
|
нет
|
-
|
-
|
|
2
|
10,0
|
78
|
1,08
|
0,8
|
|
3
|
13,5
|
69
|
1,51
|
1,3
|
|
4
|
20,0
|
65
|
1,69
|
1,5
|
|
5
|
25,0
|
70
|
1,00
|
0,7
|
|
ДАК + олигомер II,
10 ч, 700С
|
|
1
|
5,0
|
47
|
0.098
|
0.027
|
|
2
|
10,0
|
25
|
0.144
|
0.046
|
|
3
|
15,0
|
0.190
|
0.068
|
|
4
|
20,0
|
60
|
0.130
|
0.040
|
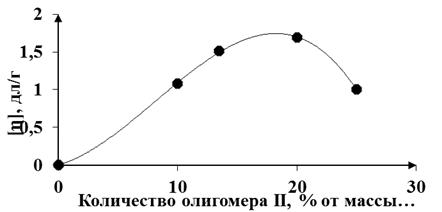
Рисунок 10 - Зависимость характеристической вязкости ПММА при
инициировании полимеризации системами Mo(CO)6 + олигомер II от
количества олигомера II, 10 ч, 700С. Мольное соотношение
ТХУК: фосфазен = 1:1
В дальнейшем планируется подобрать оптимальные условия полимеризации.
Выводы
В ходе работы:
) проведен литературный обзор в области получения
фосфазенсодержащих акриловых полимеров, согласно которому установлена
принципиальная возможность полимеризации метилметакрилата, инициируемой
карбонилом металла и галогенсодержащим арилоксифосфазеном. Для синтеза выбран
арилоксифосфазен на основе гексахлор циклотрифосфазена, фенолята натрия и
фенолята дифенилолпропана, так как он устойчив, не подвергается фосфазен -
фосфазановой перегруппировке;
2) на основе гексахлорциклотрифосфазена, фенола, дифенилолпропана и
трихлоруксусной кислоты синтезирован и охарактеризован при помощи ЯМР 1Н
и 31P спектроскопии галогенсодержащий арилоксифосфазен, инициирующий
в присутствии карбонила молибдена полимеризацию метилметакрилата;
3) методом «псевдоживой» радикальной полимеризации метилметакрилата
в присутствии инициирующей системы карбонил молибдена - галогенсодержащий
арилоксифосфазен синтезирован фосфазен содержащий полиметилметакрилат со
средневязкостной молекулярной массой Mh = 1×106.
Список литературных источников
1. Терехов И. В. Функциональные олигомерные
арилоксициклотрифос фазены и полимерные композиты на их основе. Дис. канд. хим.
наук. М.: РХТУ им. Д.И. Менделеева, 2014. 113 c.
2. Bamford C., Hargreaves K. Studies in
polymerization. XVII. The initiation of vinyl polymerization by tetrakis
(triphenyl phosphate) nickel (0) // Proc. R. Soc. Lond. A. 1967. V. 297. P. 425
- 439.
. Molybdenum carbonyl - initiated
copolymerization of trichloromethyl containing epoxy oligomer with methyl
methacrylate / Kireev V.V. [et al.]. Polymer Science. Series A. 2007. V. 49. P.
802 - 808.
4. Олкок Г. Фосфоразотистые соединения. М.:Мир. 1976 г.
563 c.
5. Gleria
M., Jaeger R. of phosphazene // J. Organomet. Polym. V. 11 P. 43 - 45.
. Allcock
H. Recent advances phosphazene (phosphonitrilic) // Chem. Rev. 1972. 72 (4). 356.
7. Schenck R., G.
Über phosphornitrilchloride
und umsetzungen (I.) Berich.
chemi. 1924. V. (8). P.
. Emsly
J., P.B. Elucidation the reaction phosphorus pentachloride ammonium
chloride phosphorus-31 nuclear resonance spectroscopy J. Chem. A. 1970. P.
3028.
9. Способ получения
пат. 1211317 AC; 15.1. 68; опубл. 25.05. 69.
. Robert F.
Hayes and Christopher W. Allen . The Mechanism of a Phosphazene - Phosphazane
Rearrangement // Dalton Transactions. 2015. V. 18. P. 1 - 18.
. Relationship
between molecular structures and tribological properties of phosphazene
lubricants / Weimin Liu [et al.]. 2002. P. 394 - 400.
. Allcock
H.R., R.W., O’Brien Phosphorus-nitrogen compounds. Synthesis of derivatives
of and cyclic // J. Chem. Soc. V. 99 P. 3987.
. Mitjaville
J., A.M., Majoral Facile syntheses phosphorus containing receptors //
Lett. 1994. 35. 6865.
. Surface
Functionalization with Phosphazenes: Part 6. Modification of
Polyethylene-Co-Polyvinylalcohol Copolymer Surface Plates with Fluorinated
Alcohols and Azobenzene Derivatives Using Chlorinated Phosphazenes as Coupling
Agents / Milani R. [et al.] // Journal of Inorganic and Organometallic Polymers
and Materials. 2008. V. 18(3). P. 344 - 351.
. Phosphorus-nitrogen
compounds part 22. Syntheses, structural investigations, biological activities
and DNA interactions of new mono and bis (4-fluorobenzyl)
spirocyclophosphazenes / Selen Bilge Kocak [et al.] // Polyhedron. 2011. V. 30. P. 2896 - 2907.
. Halogenated
hydroxy-aryloxy phosphazenes and epoxy oligomers based on them. / I. V.
Terekhov [et al.]. 2013. V. 86(10). P. 1648 - 1652.
. Synthesis,
сharacterization and dielectric properties of
phosphazenes containing chalcones / Kenan Koran [et al.] // Polyhedron. 2014.
V. 10. P. 1016.
. Synthesis
of iodine-containing cyclophosphazenes for using as radiopacifiers in dental
composite resin / Yuchen Zhao [et al.]. 2014. V. 43. P. 432 - 438.
. Polymerization
of methyl methacrylate and vinyl acetate initiated by the manganese
carbonyl-1,2-epoxy-4,4,4-trichlorobutane system / Kireev V.V. [et al.] //
Polymer Science.Series B. 2006. V. 48. P. 138 - 141.
. Selvaraj
I., Chandrasekhar V. of 2-(4′-vinyl-4-biphenylyloxy)pentachlorocyclotriphosphazene
acrylate and monomers // 1997. V. (14). P.
21. Способ получения
фосфорсодержащих полимеров: пат. 2206163 AC; заявл. 02.07.76; опубл. 27.06.2006.
22. Gabino A.Carriedo.
Phosphazenes. 2008. V. 37. P.262 - 322.
23. Jonathan
C. Shaw, Christopher W. Allen. Organophosphazenes 27:the synthesis and
polymerization of (4-ethenylphenyl) pentafluoro cyclotriphosphazene //
Phosphorus, sulfur, and silicon. 2014. V. 189. P. 1156 - 1164.
24. Kenneth R.
Carter, Christopher W. Allen. Mixed
substituent poly[(vinyloxy)cyclotriphosphazenes // Polymer Chemistry. 2013. V.
51. P. 2288-2293.
. Substituent
exchange reactions of trimeric and tetrameric aryloxycyclophosphazenes with
sodium 2,2,2 - trifluoroethoxide / Xlao Liu [et al.] // Dalton Transactions.
2012. V. 41. P. 2100 - 2109.
. Preparation
of coaxial-electrospun poly[bis(p-methylphenoxy)] phosphazene nanofiber
membrane for enzyme immobilization / Shu-Gen Wang [et al.] // Molecular
Sciences. 2012. V. 13. P. 14136 - 14148.
. Lu S.Y.,
I. Recent in the of halogen-free retardant polymers Prog. Polym. Sci. V.
27. 1661.
. Inoue
K., S., Tanigaki Polymerisation of 2-(4 methacryloxy)
pentachlorotriphosphazene // Polym. Sci. Part 1992. V. P. 145 - 148.
. Design,
synthesis and ex-vivo release studies of colon - specific polyphosphazene -
anticamer drug conjugates. / Rajiv Sharma [et al.]. 2014. P. 1104 - 1114.
. Epoxy
oligomers based on eugenol cyclotriphosphazene derivates / Kireev V.V. [et al.]
// Polymer Science. Serias A. 2008. V. 50. P. 609 - 615.
31. Метакрилатсодержащие
олигофосфазены как перспективные модификаторы полимерных композиционных
материалов для стоматологии / В.П.Чуев [и др.] // Институт стоматологии. 2010.
С. 94 - 96.