Исследование эмульсионной полимеризации некоторых акриловых мономеров с использованием диоксида титана в качестве неорганического носителя, анализ его влияния на свойства получаемых дисперсий
Реферат
с.87, табл.8, рис. 34, источников 37
АКРИЛОВЫЕ МОНОМЕРЫ, ДИОКСИД ТИТАНА, ЭМУЛЬСИОННАЯ
ПОЛИМЕРИЗАЦИЯ, ЯДРО, ОБОЛОЧКА, КОМПОЗИТНЫЕ ЧАСТИЦЫ, КАПСУЛЯЦИЯ,
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ, ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ, ДИСПЕРСИОННЫЙ АНАЛИЗ,
АГРЕГАТИВНАЯ УСТОЙЧИВОСТЬ, РЕОЛОГИЧЕСКИЕ СВОЙСТВА, ОХРАНА ТРУДА
Объектами исследования являются метилметакрилат,
бутилметакрилат, бутилакрилат, нонилакрилат. В качестве неорганического
носителя использовался диоксид титана различных марок (Light
Stabilizer 210, Hombikat
UV100, АК).
Инициатором является персульфат аммония, эмульгатором - натрий
алкилбензолсульфонат (сульфонол).
Целью данной работы является исследование
эмульсионной полимеризации некоторых акриловых мономеров с использованием
диоксида титана в качестве неорганического носителя, анализ его влияния на
свойства получаемых дисперсий.
В процессе работы были синтезированы дисперсии
полиметилметакрилата с использованием диоксида титана в качестве
неорганического носителя, так и без него. В аналогичных условиях были синтезированы
дисперсии полибутилметакрилата, сополимера метилметакрилата с нонилакрилатом и
сополимера метилметакрилата с бутилакрилатом.
У полученных дисперсий определяли поверхностное
натяжение, содержание нелетучих веществ, долю диоксида титана в твердой фазе
дисперсии, рН. Оценивали агрегативную устойчивость и исследовали реологические
свойства синтезированных дисперсий.
В результате исследования было определено
влияние диоксида титана на стабильность и свойства дисперсий полиакрилатов.
Определено, что дисперсии, содержащие композитные частицы «полимер-носитель»
способны структурироваться с течением времени и обладают тиксотропными
свойствами.
Содержание
Введение
. Литературный обзор
.1 Эмульсионная полимеризация
.2 Капсуляция
. Объекты и методы исследования
.1 Объекты исследования
.1.1 Мономеры
.1.2 Неорганический наполнитель
.1.3 Вспомогательные вещества
.2 Методы исследования
.2.1 Определение кислотно-основных
свойств поверхности (метод потенциометрического титрования в неводной среде)
.2.2 Дисперсионный анализ диоксида
титана и полученных дисперсий методом динамического светорассеяния
.2.3 Определение поверхностного
натяжения жидкостей
.2.4 Определение массовой доли
нелетучих веществ
.2.5 Определение содержания диоксида
титана в дисперсии
.2.6 Исследование реологических
свойств дисперсий
.2.7 Определение рН дисперсий
. Результаты и их обсуждение
.1 Выбор неорганического носителя
для акриловых дисперсий
.2 Синтез дисперсий акриловых
полимеров
.3 Влияние неорганического носителя
на стабильность и свойства акриловых дисперсий
.4 Влияние свойств полимера на
свойства акриловых дисперсий, синтезируемых с использованием неорганического
носителя
. Охрана труда и защита окружающей
среды
.1 Свойства применяемых в работе
материалов
.2 Меры пожарной профилактики
.2.1 Определения категории помещения
по взрывопожароопасности по НПБ 105-03 и класса помещения по ПУЭ
.2.2 Средства пожаротушения
.2.3 Нормы хранения ЛВЖ и ГЖ в
лаборатории
.2.4 Правила работы с ЛВЖ и ГЖ
.3 Метеорологические и
санитарно-гигиенические условия в лаборатории
.4 Вентиляция лабораторного
помещения
.5 Освещение помещения лаборатории
.6 Электробезопасность на рабочем
месте
.7 Водоснабжение и канализация,
удаление сливов и отходов
.8 Условия безопасного проведения
исследований
Заключение
Список использованной литературы
Введение
Водные дисперсии полимеров, получаемые методом
эмульсионной полимеризации, известны достаточно давно и широко используются в
различных областях науки и техники. В зависимости от условий синтеза получают
дисперсии с различными свойствами и размером частиц. Варьируя мономеры, можно
гибко регулировать пленкообразующие свойства таких систем и синтезировать
материалы различного назначения.
Дисперсии полимеров широко применяют при
производстве водно-дисперсионных лакокрасочных материалов. Технология
производства таких материалов включает в себя стадии приготовления водного
полуфабриката, диспергирования пигментов и наполнителей в нем, и стадию
составления, на которой в дисперсию полимера вводится пигментная паста.
Диспергирование пигментов непосредственно в дисперсии не проводят, т.к. из-за
возникающих сильных сдвиговых усилий происходит разрушение дисперсии. Основной
технологической задачей при этом является проблема стабилизации таких суспензий
и предотвращение оседания частиц пигментов, а также проблема равномерного
распределения частиц дисперсной фазы по объему материала. В результате
неравномерного распределения частиц пигментов и наполнителей, могут ухудшаться
декоративные и эксплуатационные свойства воднодисперсионных ЛКМ, в частности
укрывистость, белизна, расход и т.п.
Для решения проблемы равномерного распределения
наполнителя по объему полимерной фазы в 70-х годах 20-го века было предложено
проводить полимеризацию непредельных соединения непосредственно в присутствии
наполнителя. Как правило, полимеризацию при этом проводили или в среде жидкого
мономера, или в растворе. Изучение полимеризации на носителях позволило
определить основные закономерности этого процесса. Например, воздействуя на
поверхность частиц носителя можно получить активные частицы и проводить
полимеризацию непосредственно на них. При этом могут образовываться композитные
частицы типа «ядро-оболочка», где ядром является частица носителя, а оболочка
состоит из полимера.
В то же время вызывает интерес свойства водных
дисперсий полимеров, синтезированных с использованием неорганического носителя
с размером частиц, соизмеримых с размером частиц самой дисперсии и обладающего
различной поверхностной активностью. Наличие такого наполнителя может приводить
как к увеличению стабильности дисперсии за счет дополнительного
структурирования, так и наоборот, ускоряя разрушение дисперсии за счет
появления центров коагуляции. Кроме того, предварительная обработка поверхности
частиц наполнителя может позволить получить дисперсии, содержащие композитные
частицы типа «полимер-наполнитель». Благодаря своему строению, такие
композитные частицы обладают рядом уникальных свойств и могут использоваться в
медицине, микроэлектронике, в оптике и т.п.
Таким образом, можно предложить решение проблемы
равномерного распределения частиц пигмента в водной дисперсии полимеров,
проводя эмульсионную полимеризацию некоторых акриловых мономеров с
использованием неорганического носителя, в частности, диоксида титана. При этом
можно добиться более равномерного распределения частиц пигмента, получить уже
наполненный ЛКМ с улучшенными оптическими свойствами.
Соответственно, получение дисперсий с
композитными частицами «полимер-наполнитель» является актуальной задачей,
которая позволяет решить проблему равномерного распределения частиц пигмента в
водной дисперсии полимеров, избегая процесса диспергирования.
1. Литературный обзор
.1 Эмульсионная полимеризация
Радикальная полимеризация непредельных
соединений в зависимости от способа проведения подразделяется на полимеризацию
в массе, растворе, суспензионную и эмульсионную. Эмульсионная полимеризация
получила наибольшее распространение для получения устойчивых дисперсий
полимеров. Она выделяется ярко выраженными особенностями механизма, благодаря
чему для нее характерны большие скорости и степени полимеризации [1].
Эмульсионная полимеризация протекает в сложной
многокомпонентной системе, в которой одновременно имеют место несколько
физических и химических процессов. Это диспергирование мономера, перераспределение
эмульгатора между мономерной и водной фазами согласно растворимости, распад
инициатора на радикалы, микроэмульгирование мономера, инициирование
полимеризации.
Все эти процессы влияют на механизм образования
полимерно-мономерных частиц (ПМЧ), их диаметр, распределение частиц по размерам
(РЧР) и на молекулярную массу (ММ) и молекулярно-массовое распределение (ММР).
Реакционная система в эмульсионной полимеризации
представляет собой 30-60%-ую эмульсию мономера в воде, стабилизированную
поверхностно-активным веществом (ПАВ). В эмульсионной полимеризации обычно
используются анионно-активные ПАВ, содержащие в качестве полярной группы анион
органической или неорганической кислоты, в качестве неполярной - достаточно
длинный углеводородный радикал, например С17H35COO-.
Молекулы ПАВ уже при очень небольших концентрациях, порядка 1%, образуют
ассоциаты, называемые мицеллами. Концентрации ПАВ, используемые в
эмульсионной полимеризации (до 5%), как правило, превышают критические
концентрации мицеллообразования (ККМ). Поэтому реакционная система в
эмульсионной полимеризации содержит два типа частиц: капли размером 103-
104 нм и мицеллы размером 5-10 нм [1].
Для проведения эмульсионной (латексной)
полимеризации мономер предварительно диспергируется в жидкости, практически не
растворяющей ни мономер, ни полимер, обычно в воде, и в виде эмульсии
подвергается полимеризации. Конечный продукт реакции представляет собой
коллоидный раствор полимера, легко коагулируемый обычными методами. Подобные
коллоидные растворы благодаря известному сходству с латексом натурального
каучука получили название синтетических латексов. Для облегчения
эмульгирования мономера и повышения агрегатной устойчивости синтезированных
латексов в систему вводятся специальные эмульгаторы (соли высших жирных кислот,
мыла, соли органических сульфокислот, синтетические моющие средства или другие
поверхностно-активные вещества), действие которых заключается в понижении
поверхностного натяжения на границе фаз мономер - вода [2].
В отсутствие эмульгатора дисперсия капель
мономера в воде, полученная перемешиванием, сразу же после остановки мешалки
снова разделяется на два слоя; вследствие высокого натяжения на границе двух
фаз, стремящегося уменьшить поверхность раздела, капли сливаются в сплошную
массу (коалесценция). Эмульгатор, адсорбируясь на поверхности капель, образует
прочный защитный слой и препятствует их коалесценции. При этом углеводородная
цепь молекул ПАВ, обладающая гидрофобным характером, обращена к мономерной
фазе, а гидрофильная солеподобная группа - к воде. Устойчивость такого слоя ПАВ
обусловлена двойственным характером молекул мыла, тем, что они обладают
сродством как к диспергированным частицам мономера, так и к дисперсионной фазе
[2].
Скорость полимеризации в эмульсии значительно
выше, чем в гомогенных системах, и молекулярная масса полимера больше. Исходя
из уравнения
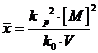
можно ожидать, что увеличение
скорости полимеризации приведет к соответствующему снижению степени
полимеризации. Однако, как показали экспериментальные данные, это уравнение
неприменимо к латексной полимеризации, так как один и тот же фактор (изменение
условий инициирования, рН среды, природа эмульгатора, его концентрация и т.д.)
может по-разному влиять на скорость и степень полимеризации [2]. Например, при
эмульсионной полимеризации стирола в присутствии гидроперекиси третичного
бутила добавление восстановителя (железистосинеродистого калия) вызывает
ускорение полимеризации в 50 раз, т.е. на 5000%, в то время как средняя
молекулярная масса снижается всего на 20% и остается очень высокой. А.И.
Юрженко и Н.С. Цветков, изучая аналогичный процесс в присутствии
водорастворимых инициаторов, установили, что степень полимеризации в отличие от
ее скорости мало зависит от природы эмульгатора.
Другие исследователи показали, что с
повышением концентрации эмульгатора скорость полимеризации непрерывно
возрастает, тогда как степень полимеризации, достигнув определенного значения,
в дальнейшем не меняется[2].
Отличия в скорости полимеризации и
размерах ПМЧ можно объяснить разным механизмом их образования из-за увеличения
содержания в исходной эмульсии микрокапель мономера при получении эмульсии при
добавлении эмульгатора в мономер. В этом случае микрокапли становятся основным
источником образования ПМЧ.
Образование микрокапель мономера при
массопереносе ПАВ из одной фазы в другую происходит в условиях повышенной
концентрации ПАВ в межфазном слое и предопределяет формирование на их
поверхности насыщенного адсорбционного слоя из молекул эмульгатора. Флуктуация
концентраций ПАВ в приповерхностном слое может привести к изменению локальной
концентрации ПАВ и к образованию структур типа жидкокристаллической тонкой
пленки, формирующей оболочку на поверхности микрокапель мономера, либо других
упорядоченных структур из молекул ПАВ [3]. Как правило, диаметр капель
составляет не менее 1 мкм.
На кинетику эмульсионной
полимеризации, резко отличающуюся по своим закономерностям от других способов
полимеризации, влияют не только температура, количество и природа инициатора,
но также количество и характер эмульгатора, соотношение фаз (т.е. концентрация
мономера в системе), рН среды, скорость и способ перемешивания. Число и
величина диспергированных частиц зависят от соотношения фаз и некоторых других
факторов и резко меняются в ходе реакции. При этом изменения тем значительнее,
чем более грубодисперсная исходная эмульсия (рис. 1.1) [2].
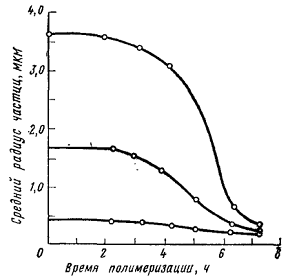
Рисунок 1.1 - Уменьшение среднего
размера частиц при полимеризации
Столь большое сокращение размера
частиц (в несколько раз) не может быть объяснено одной усадкой, величина
которой при полимеризации около 20%. Этот факт, а также и то, что число частиц
иногда возрастает в 1000 раз и больше, опровергают мнение, что латексная
полимеризация протекает внутри частиц эмульсии.
Особенности эмульсионной
полимеризации объясняются прежде всего свойствами растворов мыл, являющихся
средой для реакции полимеризации.
Молекулярная растворимость мыл очень
мала, и основная масса их в растворе находится в виде мицелл, содержащих 50-
100 молекул эмульгатора.
В зависимости от концентрации
раствора могут образоваться круглые или пластинчатые мицеллы. В том и другом
случае гидрофобные углеводородные цепи направлены, друг другу навстречу (рис.
1.2).
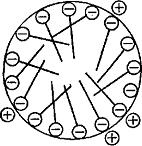
Рисунок 1.2 - Строение круглой
(ионной) мицеллы
Нерастворимые в воде углеводороды и
мономеры обладают сравнительно большой растворимостью в растворах мыл,
достигающей 6,8% у стирола и 9% у изопрена (коллоидное растворение). При
коллоидном растворении изменяются размеры мицелл; в частности, линейный размер
(d) растет
пропорционально проценту растворенного мономера (w), т. е. Δd=Kw, но
расстояние между полярными группам молекул ПАВ (h) остается
практически постоянным. Эти данные подтверждают мнение, что во время
перемешивания раствора мыла с мономером его молекулы диффундируют из капель
эмульсии через воду внутрь мицелл [2].
Процесс коллоидного растворения
в отличие от процесса образования самой эмульсии протекает самопроизвольно с
уменьшением свободной энергии (ΔF<0), а
вычисленная теплота растворения близка к значению, наблюдаемому при образовании
истинных растворов. Другими словами, мономер образует истинный раствор с
углеводородными цепями мыла.
Эмульсионная или латексная полимеризация
нерастворимых в воде мономеров (стирол, винилацетат, винилхлорид, бутадиен,
изопрен и др.) под действием персульфатов, перекиси водорода и аналогичных им
водорастворимых соединений начинается в мицеллах мыла, содержащих
растворенный мономер. Это подтверждается практически полным отсутствием
полимера в капельках мономера (по результатам анализа в них
находится меньше 0,1% полимера), выделенных на промежуточных этапах реакции.
Хотя не исключена возможность полимеризации в водном растворе, вклад ее
должен быть очень небольшим вследствие незначительной концентрации мономера;
кроме того, при этом можно было бы ожидать образования сравнительно
низкомолекулярных полимеров, что противоречит экспериментальным данным[2].
Образующиеся продукты реакции обладают высокой
молекулярной массой. Этот факт и большая скорость ее указывают на то, что
полимеризация происходит главным образом в мицеллах, в которых содержание
мономера гораздо выше и где отношение поверхности к объему значительно больше,
чем в каплях. Свободные радикалы, инициирующие реакцию, возникают в водной
фазе, где находится персульфат пли перекись, при этом обычно
образуются приблизительно 1018 радикалов в 1 мл в минуту.
По мере полимеризации мономера свежие порции
его, поступающие по-прежнему из капель эмульсии, растворяются в полимере с
образованием полимерно-мономерных частиц, в которых и происходит дальнейшая
реакция (эмульсионная полимеризация, при которой цепи растут только в одной
фазе, является, по существу, гомофазным процессом; этим она и отличается от
гетерофазных полимеризации, где рост цепи происходит в нескольких фазах). Капли
при этом играют роль резервуара, откуда мономер поступает в зону реакции;
величина их не оказывает существенного влияния на ход полимеризации. Таким
образом, становится понятной большая разница в величине диспергированных частиц
до и после реакции (см. рис. 1.1).
Другим подтверждением этого механизма латексной
полимеризации является то, что до известного предела с увеличением концентрации
эмульгатора (она обычно равна 1-5% от массы мономера) одновременно растет и
скорость полимеризации и коллоидная растворимость мономера.
Так как полимер в отличие от мономера не
образует истинного раствора с углеводородными цепями молекул мыла, последние
постепенно вытесняются; вследствие нарушения равновесия усиливается приток
мономера из капель эмульсии в мономерно-полимерную частицу. При степени
превращения мономера в полимер, равной 10-20% (фактический процент зависит от
соотношения фаз и концентрации эмульгатора), мицеллярное мыло полностью
расходуется на образование защитных слоев вокруг полимеризующихся частиц.
В конце полимеризации система представляет собой
синтетический латекс, в котором твердые коллоидные частицы стабилизированы
адсорбированным на их поверхности электролитом (молекулы мыла) [2].
Образующиеся коллоидные частицы значительно меньше по размерам, чем капли
эмульсии. При добавлении электролитов (кислоты, соли и т. д.) к
синтезированному латексу и нагревании его происходит коагуляция с выпадением
полимера в виде порошка. На рисунке 1.3 приведена схема эмульсионной
полимеризации.
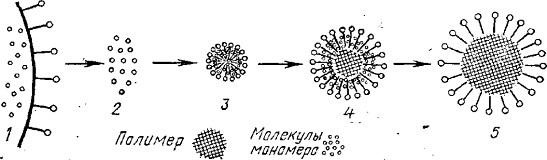
Рисунок 1.3 - Схематическое изображение
эмульсионной полимеризации:
- капля эмульсии; 2-диффузия молекул
мономера из капель эмульсии; 3 - раствор мономера в мицелле; 4 -
полимерно-мономерная частица; 5 - коллоидная частица латекса
Изучение кинетики полимеризации под влиянием
окислительно-восстановительных систем (гидроперекись изопропилбензола +
+соединения Fe2+)
С. С. Медведевым, а. также работы Г. Марка, В. Гогенштейна и ряда других исследователей
показали, что суммарная энергия активации Е латексной полимеризации и значение
предэкспоненциального члена А в уравнении Аррениуса обычно значительно меньше,
чем при проведении процесса в гомогенных условиях. Это уменьшение обусловлено
прежде всего повышением энергии активации и падением значения А для реакции
обрыва цепи, что приводит к замедлению этого процесса. В результате общая
скорость полимеризации на 2-3 порядка выше и средняя молекулярная масса на один
порядок больше, чем в случае гомогенных систем при тех же инициаторах[2].
По мнению С. С. Медведева, эти факты объясняются
малой скоростью диффузии макрорадикалов внутри полимерно-мономерных частиц, где
вязкость велика и где в основном протекает полимеризация. Благодаря этому
снижается вероятность обрыва, что находит свое выражение в малой величине
предэкспоненциального члена уравнения Аррениуса [2].
Другое толкование было дано У. Смитом и Р.
Юэртом для латексной полимеризации стирола в присутствии персульфата калия. Как
показали расчеты этих исследователей, если все свободные радикалы, полученные
при распаде инициатора, попадают в полимерно-мономерную частицу, то в среднем в
нее проникает один радикал каждые 10-100 с. Обрыв инициированной этим радикалом
полимерной цепи может произойти только через еще 10- 100 с. Так как скорость
присоединения молекул мономера к растущему радикалу составляет величину порядка
1000 молекул в секунду, за это время цепь успевает «вырасти» до очень больших
размеров. Таким образом, в результате того что свободные радикалы проникают в
полимерно-мономерную частицу «с опозданием», уменьшается скорость обрыва и
возрастает молекулярная масса полимера. Хотя такое объяснение пригодно для
латексной полимеризации нерастворимых в воде мономеров в присутствии
водорастворимых инициаторов, когда первоначальные свободные радикалы возникают
в водной фазе, оно неприемлемо в случае малорастворимых инициаторов, когда
инициирование происходит в мицеллах [11].
Несмотря на то, что теория У. Смита и Р. Юэрта
дает возможность понять ряд особенностей эмульсионной полимеризации, в
количественном аспекте она плохо согласуется с поведением многих применяемых на
практике систем, особенно таких, у которых полимер нерастворим в собственном
мономере (например, нерастворимость поливинилхлорида в винилхлориде). Некоторые
наблюдающиеся при этом аномалии лучше объясняются теорией С.С. Медведева, где
основную роль играет поверхность мономерно-полимерной частицы. Теория У. Смита
и Р. Юэрта, по-видимому, лучше описывает процессы, при которых полимер растворим
в собственном мономере (например, полистирол), когда реакция протекает во всем
объеме частицы [2].
При применении мономеров, обладающих
сравнительно хорошей растворимостью в воде (например, акрилонитрил), и
водорастворимых инициаторов полимеризация протекает сначала в молекулярном
(истинном) растворе, а затем в выпадающих из раствора агрегатах макромолекул.
Если растворимость мономера в воде составляет 1-3% (виниловые эфиры,
метилметакрилат и др.) и инициатор водорастворим, происходят, по-видимому, одновременно
процессы, характерные для мономеров как с хорошей, так и с плохой
растворимостью. Когда применяются нерастворимые в воде инициаторы,
инициирование и полимеризация, независимо от растворимости мономера, протекают
в мицеллах мыла, содержащих растворенные мономер и инициатор (а также в каплях
эмульсии).
Во всех случаях основная масса полимера
образуется в полимерно-мономерных частицах небольших размеров.
С точки зрения природы основных процессов,
протекающих в реакционной системе, эмульсионная полимеризация может быть
разбита на три этапа. Первый этап является коллоидно-химическим, поскольку его
главным результатом является возникновение агрегатов - устойчивых
полимер-мономерных частиц (ПМЧ). Существуют три пути их формирования:
. При эмульсионной полимеризации практически не
растворимых в воде мономеров стирола (0,1 г/л) и бутадиена (0,8 г/л) первичные
радикалы, образовавшиеся при распаде инициатора в водной фазе, диффундируют в
мицеллы, где инициируют полимеризацию находящегося там мономера. В капли радикалы
практически не попадают, т.к. суммарная поверхность мицелл примерно на два
порядка превышает суммарную поверхность капель.
. Мономеры, заметно растворимые в воде -
винилхлорид (4- 15 г/л), винилацетат (25 г/л), полимеризуются достаточно
интенсивно в водной фазе. Поскольку соответствующие полимеры в воде не
растворимы, в результате образуются ПМЧ, стабилизированные ПАВ, которые
находятся в водной фазе.
. Параллельно с образованием первичных частиц по
тому или другому механизму происходит их слипание (коагуляция). В результате
удельная поверхность частиц, а с ней и свободная поверхностная энергия
уменьшаются, и система становится более устойчивой [1].
К концу первого этапа число частиц уменьшается
на 2-3 порядка и далее не изменяется [1].
Второй этап эмульсионной полимеризации протекает
в псевдостационарных условиях, которые характеризуются относительным
постоянством числа частиц, концентрации мономера в них и постоянной
концентрацией радикалов роста [1].
Скорость полимеризации при проведении реакции в
эмульсиях можно увеличить применением активных окислительно-восстановительных
систем для инициирования, которые дают возможность осуществлять процесс при
низких температурах. Благодаря тому, что энергия активации очень мала и
значительно ниже энергии активации разветвления цепи, получаемые полимеры
содержат меньше разветвлений, чем при других методах полимеризации. Применение
окислительно-восстановительных систем (чаще всего Fe2+
- персульфат и Fe2+
- гидроперекись кумола) позволяет синтезировать латексные полимеры и сополимеры
бутадиена при 10 °С и более низких температурах, причем присоединение идет
преимущественно в положение 1,4 [2].
В присутствии растворимых солей переходных
металлов (RhСl3·3Н2O,
IгС1з, CoSiF6)
можно осуществить стереоспецифическую эмульсионную полимеризацию бутадиена,
что, вероятно, связано с образованием устойчивых к воде комплексов, являющихся
активными центрами полимеризации; микроструктура полимера определяется
характером металла и его лигандов. Например, синдиотактический кристаллический
полиметилметакрилат можно получить, проводя полимеризацию при 20°С в
присутствии перекиси бензоила и катионного эмульгатора (цетилпиридинийхлорид),
который одновременно выступает как компонент инициирующий системы с
образованием ион-радикалов [2].
Эти исследования указывают на принципиальную
возможность сочетания очень выгодного в технологическом отношении метода
эмульсионной полимеризации с получением высококачественных стереорегулярных
полимеров.
Кроме инициаторов (можно возбудить эмульсионную
полимеризацию радиохимическими методами, при этом наиболее вероятными
инициаторами реакции являются радикалы ОН·, возникающие в результате
радиолиза воды) и эмульгаторов при эмульсионной полимеризации часто добавляют
регуляторы рН (буферы), регуляторы поверхностного натяжения (одноатомные
алифатические спирты), позволяющие изменять величину капель эмульсии в желаемых
пределах, регуляторы полимеризации, стабилизаторы и пластификаторы [2].
В качестве эмульгаторов при проведении
эмульсионной полимеризации могут использоваться неионогенные ПАВ
(полиэтоксиэтилированные высшие жирные спирты, полипропиленгликоли и др.).
Полимеризация в присутствии таких ПАВ имеет свои закономерности, несколько
отличающиеся от тех, которые имеют место при применении ионных эмульгаторов.
Кроме того, соответствующими исследованиями и практикой установлено, что
наилучшая стабильность латексов обеспечивается применением смеси ионогенных и
неионогенных эмульгаторов [3].
В последнее время одним из направлений
исследований в эмульсионной полимеризации является получение дисперсий,
содержащих частицы субмикронных размеров, причем с монодисперсным по размеру
частиц составом. Используя в качестве дисперсионной среды алифатические
углеводороды и стабилизируя эмульсию метилметакрилата полидиметилсилоксаном,
были получены микросферы из полиметилметакрилата размером не более 400 нм. При
этом отклонение по размеру частиц составляло не более 5% [4]. Применяя в
качестве исходных мономеров стирол, дивинилбензол и хлорметилстирол, в
присутствии монодисперсного полистирола были синтезированы монодисперсные по
составу дисперсии, частицы полимера в которых содержали на поверхности
хлорметильные группы [5]. Обрабатывая частицы такого полимера аминами,
например, этилендиамином, можно предотвратить агрегацию частиц и дополнительно
стабилизировать данную дисперсию.
Еще одним перспективным применением эмульсионной
полимеризации может служить возможность получения микросфер полимера с
полостями внутри. Такие микросферы можно использовать как сорбенты,
транспортные контейнеры или как молекулярные сита. Подобные микросферы
синтезируют с использованием эмульсий типа «вода в масле в воде». В мономере
диспергируют водные растворы солей, стабилизируя эмульсию органорастворимыми
ПАВ. Полученную эмульсию воды в мономере диспергируют в воде, применяя в
качестве эмульгатора водорастворимые ПАВ. В процессе синтеза вода,
диспергированная в мономере переходит в водную дисперсионную среду, при этом
образуются полимерные частицы с пустотами внутри [6].
Эмульсионная полимеризация используется и для
получения частиц типа «ядро-оболочка». Ядром и оболочкой такой частицы является
полимер. Например, получая методом эмульсионной полимеризации полистирол и
диспергируя его в метилметакрилате, можно получить полимерную частицу с более
высокой температурой стеклования [7]. Используя в качестве сомономера
хлорметилстирол, были получены частицы полимера, содержащие на поверхности
реакционноспособные группы [8].
Большой интерес вызывает возможность
использовать в качестве ядра таких композитных частиц неорганического носителя.
При этом можно решить несколько задач. Например, можно получить частицы, с
бесконечно большой температурой стеклования, для термостойких конструкционных
материалов. Сорбируя на поверхности неорганического пигмента мономер и проводя
эмульсионную полимеризацию, можно модифицировать поверхности носителя
полимером, т.е. получить закапсулированную частицу пигмента.
.2 Капсуляция
Одним из приоритетных направлений в химии и
технологии полимерных материалов является создание композитов на основе
полимеров и неорганических частиц. При этом преследуются различные цели:
получение антисептических препаратов, токопроводящих и светоотражающих пленок,
фотоматериалов и др. [9].
Традиционные способы модификации полимерных
материалов неорганическими наночастицами имеют ряд существенных недостатков,
обусловленных сложностью обеспечения агрегативной устойчивости частиц,
нежелательным увеличение вязкости смесей при высоких концентрациях и
отсутствием равномерного распределения наполнителя. Одновременно возникают
проблемы совмещения полимеров с различными наполнителями, обеспечивающего
получение материалов с равномерно распределенными в объеме полимерной матрицы
наночастицами. Одним из перспективных технологических способов получения таких
композиционных материалов является полимеризация в высокодисперсных эмульсиях,
дисперсная фаза которых содержит наночастицы различных материалов [9], [10].
Такие композиты могут найти применение в
катализе, в практике создания газовых сенсоров, оптически прозрачных светофильтров,
УФ-фильтров, жидкокристаллических экранов [11], получения материалов с
антибактериальными свойствами для последующего их использования в
биомедицинской технологии [12].
В настоящее время разработаны различные методы
получения наноразмерных частиц неорганической природы [13]. Однако, в
большинстве случаев получаемые наночастицы полидисперсны, а также неоднородны
по составу и форме. Одним из способов получения представительных рядов
нанонаполнителей, различающихся между собой лишь по одному параметру (размер,
форма, структура, химия поверхности и т.д.), является их целенаправленный
синтез. [14].
Приоритетным направлением является создание
композитных частиц на основе полимеров и неорганических частиц, в которых
полимер принимает участие в стабилизации наночастиц, предотвращая из
агломерацию. Наночастицы могут быть помещены не только в объем материала и
тонкие пленки, но и на поверхность микросфер [10].
По типу морфологий полимерные композиционные
сферы делятся на структуры «ядро-оболочка», «частично локализованные
полусферы», «матрицы» и частицы, в которых эти домены локализованы в
поверхностном слое частицы-матрицы (структура типа «конфетти»).
При иммобилизации в полимерные микросферы
неорганических наночастиц разрешается несколько проблем:
) защита неорганического материала полимерной
оболочкой (магнетит, кремнезем);
) возможность создания маркеров, в качестве
которых может выступать неорганический материал, содержащийся на поверхности
или в объеме частицы-носителя (магнетит);
) возможность создания при определенных условиях
новых материалов, например, фотоинициатора;
) повышение агрегативной устойчивости дисперсий
(например, пигменты, сажа и т.д.);
) повышение механических свойств материалов
(кремнезем);
) снижение газопроницаемости материала за счет
упрочненных полимерных пленок (глина).
Различные методы синтеза полимерных микросфер,
содержащих неорганические наночастицы, можно объединить в три группы:
комбинирование раздельно полученных
неорганических наночастиц и полимера;
получение неорганических наночастиц в полимерных
микросферах или в присутствии готовых макромолекул полимера;
полимеризация мономеров в присутствии
неорганических наночастиц.
Первое направление основано на получении
неорганических наночастиц и полимерного материала независимыми друг от друга
способами. В рамках этого направления синтеза можно выделить два метода
инкапсулирования неорганического материала в полимер [10]:
неорганические наночастицы вводятся в
затравочные полимерные микросферы;
полимерные ПАВ адсорбируются на поверхности
неорганического материала.
Например, первые магнитнаполненные полимерные
микросферы для медицины пытались получить из биосовместимых и биоразлагаемых
полимеров, таких как альбумин, поливиниловый спирт и др. [15].
Другой метод получения полимерных микросфер,
содержащих неорганические наночастицы, состоит в механическом захвате
неорганических частиц полимером [16].
Существует метод, который позволяет вводить
неорганический материал в уже сшитую полимерную матрицу [17]. Такие микросферы
состоят из сефарозного геля, в который неорганические наночастицы включены
путем адсорбции или осаждения в гель. Полученный по такому методу материал
используют в качестве аффинной среды для хроматографии. Однако, из-за слабой
фиксации неорганических наночастиц внутри микрогеля промывка любым буферным
раствором может привести к десорбции и высвобождению неорганических наночастиц,
что является главным их недостатком при использовании.
Способ получения полимерных микросфер с
иммобилизированными неорганическими наночастицами, заключающийся в адсорбции
полимера на поверхность неорганического материала, был изучен на примере
использования магнитных наночастиц двух диаметров: около 10 нм и 200 - 400нм,
при этом на поверхность магнитных наночастиц формировался тонкий полимерный слой
путем физической или химической адсорбции полимера. При химической адсорбции
имеет место взаимодействие между функциональными группами полимеров (-СООН, -РО3Н2,
-NH2)
и функциональными группами магнитных наночастиц, наличие которых возможно после
активации поверхности последних. Обычно использую гидрофильные полимеры, такие
как полиакриловая кислота, полиметилметакрилат, полипропиленгликоль или
производные полисилоксана. Следует отметить, что тонкий слой полимера,
адсорбированного на неорганические магнитные наночастицы, не изменяет ценные
суперпарамагнитные свойства этих неорганических нанообъектов.
Композиционные частицы могут быть получены из
функциональных полимерных микросфер, заранее синтезированных одним из методов
гетерофазной полимеризации. Полимерные дисперсии синтезируются в растворе солей
различных металлов. Включение неорганического материала в полимер
осуществляется либо осаждением, либо окислительно-восстановительной реакцией
между ионами металла [10].
Восстановление солей металла на поверхности
полимерных частиц является еще одним способом получения композитных микросфер.
Такие полимерные микросферы используются в качестве проводящих полимерных
материалов или в качестве каталитических систем [10].
Многослойные композитные частицы представляют
собой органическое ядро, неорганический слой (вокруг ядра), образованный
оксидами металла, и полимерную оболочку.
Для получения полимерных микросфер, содержащих
неорганические наночастицы, используют различные методы проведения гетерофазной
полимеризации в присутствии неорганического материала, такие как эмульсионная,
суспензионная и дисперсионная полимеризация.
Наиболее распространенным процессом получения
композиционных микросфер является затравочная полимеризация мономеров в
присутствии затравочных неорганических наночастиц [18]. В этом случае
неорганический материал должен отвечать ряду требований:
. Поверхность материала должна быть гидрофобной,
что достигается за счет адсорбции ПАВ или ее химической модификации. На
поверхности должны содержаться реакционноспособные группы для взаимодействия с
функциональными группами полимера, либо вещества, способствующие гидрофобному
взаимодействию с поверхностью полимера. В качестве таких модифицирующих агентов
могут быть использованы, например, силаны, титанаты, двухосновные кислоты и др.
. Неорганические частицы должны сохранять
коллоидную стабильность. Наночастицы стабилизируются путем адсорбции ПАВ,
которые обычно используются при эмульсионной полимеризации.
Для инкапсулирования неорганических наночастиц в
полимер, концентрация ПАВ должна быть ниже величины критической концентрации
мицеллообразования (ККМ), чтобы предотвратить образование мицелл в исходной
системе и исключить образование полимерных микросфер, не содержащих
неорганический материал [10]. Кроме того, для полимеризации необходимо
использовать нерастворимые в воде инициатор и мономер, для исключения
образования олигомерных водорастворимых ПАВ [19].
В последнее время для получения наполненных
неорганическим материалом полимерных микросфер используют так называемую
миниэмульсионную полимеризацию [20], которую проводят в две стадии. На первой
стадии в присутствии ПАВ получают стабильную дисперсию неорганических частиц в
стироле. Затем ее переводят в воду, добавляя новые ПАВ. Для предотвращения
процесса созревания по Оствальду в мономерную фазу (в качестве гидрофобной
добавки) добавляют гександекан. Содержание неорганического материала в
полимерных микросферах, полученных таким способом, составляет 20% масс.
Для увеличения содержания неорганического
материала в полимерных частицах была предложена другая методика их синтеза
[21]. Мономер и неорганические наночастицы независимо диспергируют в воде в
присутствии додецилсульфата (ДСН) в качестве ПАВ и последовательно смешивают
при различных соотношениях мономер/неорганический материал с целью получения
полимерных микросфер с различной концентрацией неорганических наночастиц. Затем
смесь подвергают ультразвуковой обработке для создания необходимой дисперсности
системы и инициируют процесс полимеризации [10].
Применение подобной технологии позволяет
синтезировать полимерные микросферы с различным строением поверхности, с узким
распределением частиц по размерам, имеющие структуру «ядро-оболочка». Подобные
полимерные микросферы могут вводиться в защитные слои эмульсионных
фотографических материалов, в качестве антистатических компонентов [22].
Современные светочувствительные материалы,
представляющие собой полимерную основу с нанесенными на нее эмульсионными и
вспомогательными слоями, обладают способностью накапливать статическое
электричество в процессе эксплуатации. Защита фильмовых материалов от
возникновения зарядов статического электричества всегда была актуальной и
важной проблемой. Статическое электричество на светочувствительных слоях может
возникать по целому ряду причин, таких как, пониженная влажность воздуха;
большие скорости перемотки пленки в съемочной и проекционной аппаратуре;
технологические параметры изготовления фотографического материала;
неоптимальные условия хранения и эксплуатации. Задача устранения
электризуемости пленок на весь период их изготовления и эксплуатации с
сохранением оптических и физико-механических свойств материала до сих пор
остается весьма актуальной [22].
Защита полимерных материалов от статического
электричества осуществляется различными как физическими, так и химическими
способами.
К физическим способам относятся ионизация
воздуха, уменьшение коэффициента трения, заземление оборудования, создание
соответствующего температурно-влажностного режима в помещении, где проводится
работа с пленкой. К химическим способам относится использование различных
электропроводящих покрытий или антистатическая обработка поверхности изделий. В
качестве антистатиков могут быть использованы различные органические или
неорганические вещества, обладающие ионной или электронной проводимостью.
В последние десятилетия в практике производства
фотоматериалов достаточно широко используется способ создания
микрошероховатости на поверхности защитных слоев фотоматериалов путем введения
полимерных частиц малых размеров, благодаря которым предотвращается тесный
контакт между витками пленки, находящейся в рулоне, например, применяя при
производстве пленок высокодисперсную полимерную суспензию полиметилметакрилата
(ПММА) [23].
Перед введением суспензии требуется тщательное
диспергирование системы во избежание образования агрегатов в растворах
защитного (или вспомогательного) слоя и тщательная фильтрация перед поливом.
Недостатком этого метода являлась определенная мутность среды и, как следствие
этого, снижение разрешающей способности.
Применение частиц типа «ядро-оболочка» с
различным строением поверхности позволило снизить напряженность электрического
поля, без ухудшения фотографических свойств светочувствительного материала
[22].
В качестве перспективного наполнителя внимание
привлекают наночастицы оксида цинка. Особый интерес к ним вызван их оптическими
свойствами, то есть проявлением фотолюминесценции, возникающей за счет природы
связи между атомами и параметров кристаллической решетки. В настоящее время
существует несколько способов получения наночастиц оксида цинка. Наиболее
известными и изученными являются: гидротермальный метод, химическая
конденсация, термическое разложение и гидролиз солей цинка в спиртовом
растворе[10]. К недостаткам такого наполнителя можно отнести нестойкость к
действию кислот и щелочей, при этом развитая поверхность лишь способствует
ускорению этих процессов.
Избежать подобных явлений позволяет капсуляция
частиц оксида цинка в полимере.
Формирование полимерных микросфер с
иммобилизированными на их поверхности наночастицами оксида цинка может
происходить в несколько этапов. Первый состоит в получении устойчивой дисперсии
наночастиц оксида цинка в углеводороде, поверхность которых характеризуется
определенным гидрофильно-липофильным балансом, обеспечивающим им
поверхностно-активные свойства. Второй этап предполагает обеспечение
устойчивости микрокапель мономера, содержащих наночастицы оксида цинка в
поверхностном слое полимерных частиц. Для этого в систему добавляют цетиловый
спирт и додецилсульфат натрия, способные образовывать в межфазном слое
жидкокристаллические пленки - структурно-механический фактор стабилизации. При
этом межфазное натяжение существенно снижается. На третьем этапе проводят
полимеризацию с инициированием на границе раздела фаз персульфатом калия, и
образующийся полимер осаждается в поверхностном слое, поскольку вода является
осадителем полимера [10].
Применяя в качестве носителя частицы магнетита,
возможно получение магнитных жидкостей, которые широко используются в качестве
термосенсоров [24]. При этом эксплуатационные показатели таких сенсоров
превосходят свойства уже применяемых.
Перспективной областью применения частиц типа
«ядро-оболочка» является получение нанокомпозитных гелей. Подобный гель может
использоваться в качестве молекулярного сита в фармацевтической промышленности,
в медицине, в качестве агента при анализе наркотических веществ. Вводя в состав
таких гелей капсулированные частицы магнетита, возможно получение материала,
свойства которого изменяются под действием электромагнитного поля [25], [26].
Таким образом, используя различные методы
гетерофазной полимеризации, можно синтезировать полимерные микросферы,
содержащие неорганические наночастицы с различной морфологией, с разными
диаметрами и различным содержанием неорганического материала в полимере,
имеющие широкий спектр применения - от использования их в магнитной сепарации
различных технических средств до полимерных суспензий биомедицинского
назначения.
2. Объекты и методы исследования
.1 Объекты исследования
.1.1 Мономеры
· Метилметакрилат (ММА) -
· Бутилметакрилат (БМА) -
· Бутилакрилат (БА) -
· Нонилакрилат (НА) -
Характеристики мономеров приведены в таблице
2.1.1:
Таблица 2.1.1 - Характеристики мономеров
|
Мономеры
|
Внешний
вид
|
Молярная
масса, г/моль
|
Ткип,
°С
|
Плотность,
ρ
кг/м3
|
|
Метилметакрилат
|
бесцветная
жидкость
|
100,12
|
100
|
936
|
|
Бутилметакрилат
|
бесцветная
жидкость
|
142,20
|
169
|
895
|
|
Бутилакрилат
|
бесцветная
жидкость
|
128,17
|
147,4
|
911
|
|
Нонилакрилат
|
бесцветная
жидкость
|
198,31
|
190
|
1431
|
Все мономеры перед проведением полимеризации
подвергали очистке от ингибитора промывкой 5% водным раствором щелочи 3 раза.
Затем мономеры промывали от щелочи дистиллированной водой до нейтральной
реакции по универсальной индикаторной бумаге и осушали их хлористым кальцием. Очищенные
мономеры хранили в холодильнике. Непосредственно перед полимеризацией мономеры
подвергали вакуумной перегонке в среде азота.
Чистые мономеры хранятся в прохладном месте, так
как при комнатной температуре они склонны к полимеризации (как в присутствии
инициатора, так и без него).
.1.2 Неорганический наполнитель
В качестве неорганического наполнителя
использовали диоксид титана различных марок.
) диоксид титана Light
Stabilizer 210 (фирма DuPont)
|
кристаллическая
модификация
|
рутил
|
|
плотность,
кг/м3
|
4200
|
|
показатель
преломления
|
2,75
|
) диоксид титан Hombikat
UV100 (фирма Sachtleben)
|
кристаллическая
модификация
|
анатаз
|
|
содержание
диоксида титана, %
|
более
90
|
|
показатель
преломления
|
2,5
|
|
средний
размер частиц, мкм
|
1
|
|
удельная
поверхность (БЭТ), м2/г
|
250
|
) диоксид титана марки АК (фирма «Промхимпермь»)
|
кристаллическая
модификацияанатаз
|
|
|
содержание
диоксида титана, %
|
не
менее 99
|
|
показатель
преломления
|
2,5
|
|
средний
размер частиц, мкм
|
23,3*
|
|
удельная
поверхность (БЭТ), м2/г
|
61,2
|
Средний размер частиц определялся исходя из
величины удельной поверхности
.1.3 Вспомогательные вещества
Инициатор - персульфат аммония
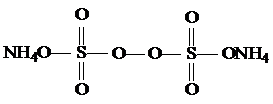
Молярная масса = 228 г/моль;
Эмульгатор - натрий
алкилбензолсульфонат (сульфонол)
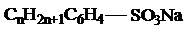
Массовая доля нелетучих веществ =
29%, ККМ= 0,67 г/л, σККМ = 30 мН/м;
2.2 Методы исследования
.2.1 Определение кислотно-основных
свойств поверхности (метод потенциометрического титрования в неводной среде)
Для определения содержания кислотно-основных
центров с одновременным установлением их силы, использовался метод неводного
титрования этих центров раствором паратолуолсульфокислоты и едкого натра.
В качестве растворителя использовался ацетон,
являющийся индеферентным растворителем с большой дифференцирующей силой. В
отличие от воды, имеющей ионное произведение, равное 14, логарифм константы
сольволиза ацетона равен 26, т.е. шкала рН или рС для органического
растворителя растягивается с 14 до 26. Причем для ацетона имеет место удачная
величина разбега ЭДС при переходе от сильных кислот к сильным основаниям,
равной ≈1400, то есть имеется возможность прямой корреляции значения ЭДС
полунейтрализации кислоты и основания со значением рК или функции Гаммета при
условном переносе ее значений для водной среды.
В качестве электрода сравнения используется
хлорсеребряный электрод, заполненный насыщенным спиртовым раствором хлористого
калия. В качестве рабочего электрода - стеклянный электрод марки ЭСЛ - 061. В
промежутке между экспериментами стеклянный электрод регенерируется в слабом
водном растворе соляной кислоты.
При потенциометрическом титровании значения рН и
рК связаны уравнением:
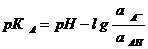 , (1)
, (1)
где а А - активность
диссоциированной кислоты;
а АН - активность
недиссоциированной кислоты.
Аналогичная зависимость и для рКВ.
Обычно рК может быть установлено по величине рН, соответствующей
полунейтрализации, то есть когда 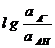 обращается в 0. Однако это
относится к водным растворам и хотя уравнение справедливо и для неводных
систем, но практически, воспользоваться им затруднительно из-за
неопределенности значения pH переходящего в pL
(концентрация ионов лиония (CH3-CO-CH3H+)). Как
видно, pK связано со
значением потенциала в точке полунейтрализации.
обращается в 0. Однако это
относится к водным растворам и хотя уравнение справедливо и для неводных
систем, но практически, воспользоваться им затруднительно из-за
неопределенности значения pH переходящего в pL
(концентрация ионов лиония (CH3-CO-CH3H+)). Как
видно, pK связано со
значением потенциала в точке полунейтрализации.
Приборы и оборудование:
pH-метр
Измерительная система, состоящая из:
хлорсеребряного электрода сравнения, заполненного насыщенным спиртовым
раствором хлорида калия, платинового электрода, термокомпенсатора.
Магнитная мешалка.
Стеклянный стакан вместимостью 50 см3.
Варипипетка.
Материалы и реактивы:
пара-Толуолсульфокислота
- Ацетон (ГОСТ 2603-79)
Едкий натр (ГОСТ 2263-79)
Спирт этиловый (ГОСТ 5964-82)
Ход определения:
,5 г исследуемого пигмента, взвешенного с
точностью до 0,01г, вносили в стакан вместимостью 50 см3. Добавляли
30 мл ацетона и помещали стакан на магнитную мешалку. Электродную систему
погружали в стакан с суспензией и включали перемешивание.
После установления значения потенциала снимали
начальное показание милливольтметра. Затем порциями добавляли титрант в
суспензию исследуемого пигмента. После добавления каждой порции титранта
необходимо регистрировать значения потенциала. Титрование заканчивали, когда
добавление нескольких порций титранта к суспензии не приводило к изменению
потенциала.
По результатам была построена кривая зависимости
потенциала от объема добавленного титранта. Силу основных центров находили по
кривой титрования пара-толуолсульфокислотой. Для этого определяли
потенциалы полунейтрализации основных центров, и рассчитывали для них функцию
Гаммета по уравнению:
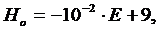 (2)
(2)
где E - ЭДС,
соответствующая полунейтрализации данного основного центра, мВ.
Для расчета силы кислотных центров
предварительно проводилось титрование раствора пара-толуолсульфокислоты
в ацетоне раствором едкого натра в этиловом спирте. По полученной в результате
титрования кривой находили значение потенциала полунейтрализации. Значение
функции Гаммета при этом потенциале принимают равным 7. Используя линейность
зависимости функции Гаммета от потенциала, значение функции Гаммета вычисляется
по формуле:
Но/dЕ = 0,01,
(3)
Концентрация кислотных (основных)
центров на поверхности вычисляли на основании (дифференциальной) кривой
титрования по следующей формуле:
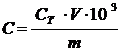 , (4)
, (4)
где С - концентрация кислотных
(основных) центров, мкмоль/г;
Cт -
концентрация титранта, моль/дм3;
V - объем
титранта, соответствующий точке эквивалентности, см3;
m - масса
пигмента, г.
.2.2 Дисперсионный анализ диоксида
титана и полученных дисперсий методом динамического светорассеяния
Определение размера частиц и
распределения по размерам полученных дисперсий и диоксида титана, производилось
с помощью прибора Nanotrack Ultra 151.
Суть данного метода определения размеров частиц
заключается в регистрации рассеяния света частицами (дифракционная картинка),
при этом угол рассеяния света универсально пропорционален размеру частиц.
Рассеянное частицами излучение регистрируется
под разными углами с помощью высокочувствительного многоэлементного кремниевого
детектора - фотодиодной матрицы. Излучение полупроводниковых лазеров с помощью
линзы фокусируются в плоскость детектора, проходя при этом через измерительную
кювету в которой осуществляется проток анализируемой суспензии, эмульсии или
сухого порошкообразного материала.
При наличии в кювете частиц наблюдается
рассеяние света. Индикатриса рассеяния определяется размером частиц и длиной
волны лазера, которая постоянна. Измерение индикатрисы и последующая
программная обработка результатов позволяет определить характер распределения
частиц по размерам данной системы. Фотодиодные матрицы одновременно
обеспечивают измерение интенсивности рассеянного излучения.
2.2.3 Определение поверхностного натяжения
жидкостей
Определение поверхностного натяжения жидкостей
производили по методу Дю Нуи.
Оценка поверхностного натяжения этим методом
заключалась в измерении силы F,
необходимой для отрыва кольца, погруженного в жидкость, от поверхности
жидкости.
Для отрыва кольца от поверхности жидкости
необходимо приложить усилие, которое равно произведению поверхностного
натяжения жидкости на полный периметр смачивания тела.
Кольцо имеет внутренний радиус R1
и
внешний - R1+2R2
(R2
-
радиус проволоки, из которой изготовлено кольцо). В момент отрыва кольца от
поверхности жидкости сила равна:
F
= σ2πR1
+ σ (R1
+ 2R2)
2π = 4πRσ,
(5)
где R
= R1+2R2
Сила F,
необходимая для отрыва кольца, определяется с помощью торсионных весов.
Исследуемую жидкость помещают в стаканчик и
устанавливают на столик торсионных весов. Поднимая столик с помощью винта,
платиновое кольцо погружают в исследуемую жидкость. Рычаг весов из положения
«Арретир» устанавливают на нулевую отметку шкалы. Поворотом винта, поднимая или
опуская столик, уравновешивают платиновое кольцо в жидкости по индикатору путем
совмещения его стрелки с вертикальной риской. Плавно поворачивают рычаг весов
до момента отрыва кольца от поверхности жидкости. Отмечают показания весов в
момент отрыва.
По окончании измерений рычаг весов устанавливают
в положение «Арретир», кольцо снимают и промывают ацетоном, после чего
просушивают на фильтровальной бумаге.
Определение усилия отрыва проводят несколько
раз, усредняют показания весов и рассчитывают поверхностное натяжение жидкости
на границе с воздухом по формуле:
σ = К∙ (m
+ n), мН/м (6)
где К - постоянная платинового кольца, равная
0,03959;
m - масса чашки,
равная 334,45 мг;
n - показания весов,
мг.
.2.4 Определение массовой доли нелетучих веществ
Определение массовой доли нелетучих веществ
производилось в соответствии с ГОСТ Р 52487-2005 (ИСО 3251:2003).
Чистую сухую чашку m0
взвешивали с точностью 0,0002 г на аналитических весах. Пробу помещали в чашку
и равномерно распределяли её по дну. Чашку с навеской взвешивали на
аналитических весах (m1).
После взвешивания помещали чашку в сушильный шкаф, предварительно нагретый до
температуры (105±2) °С и выдерживали в шкафу до постоянной массы.
Перед взвешиванием чашку охлаждали до комнатной
температуры в эксикаторе.
Массовую долю нелетучих веществ (NV,%)
рассчитывали по формуле:
NV = ((m2
- m0)
/ (m1
- m0))
∙ 100,
где m2
- масса чашки с остатком, г;
m0
- масса пустой чашки, г;
m1
- масса чашки с пробой для испытаний, г.
.2.5 Определение содержания диоксида титана в
дисперсии
Содержание диоксида титана определяли гравиметрическим
методом по величине потери массы при прокаливании.
Образец дисперсии коагулировали насыщенным
водным раствором квасцов. Образовавшийся осадок отделяли от жидкости
центрифугированием. Осадок многократно промывали от эмульгатора горячей
дистиллированной водой. После каждой промывки осадок отделяли
центрифугированием. Промытый осадок высушивали при температуре (105 ± 2) ºС.
В прокаленный до постоянной массы и взвешенный с
точностью до 0,0002 г фарфоровый тигель помещали высушенный до постоянной массы
осадок и взвешивали на аналитических весах с точностью до 0,0002 г. Осадок
прокаливали в муфельной печи при температуре 600°С в течение 1 часа. Затем
тигель охлаждали в эксикаторе и взвешивали. Прокаливание проводили до
достижения постоянной массы образца.
Содержание диоксида титана в твердой фазе
дисперсии Х (в %) вычисляли по формуле:
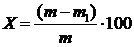
где m - масса
навески до прокаливания, г;
m1 - масса
навески после прокаливания, г.
Содержание диоксида титана в
дисперсии Y (в %) рассчитывали
по формуле:
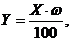
где X -
содержание диоксида титана в твердой фазе дисперсии, %
w
- массовая доля нелетучих веществ в дисперсии, %
.2.6 Исследование реологических
свойств дисперсий
Реологические свойства дисперсий
исследовали на ротационном вискозиметре Mettler RM 180 Rheomat.
Принцип изучения реологических
свойств на ротационном вискозиметре заключается в том, что измеряется
напряжение сдвига, возникающее в материале, помещенном в узкий зазор между
вращающимся и неподвижным коаксиальными цилиндрами. Вращающийся внутренний
цилиндр связан осью с пружиной, которая передает момент вращения от внутреннего
цилиндра на потенциометр. Показания потенциометра пропорциональны моменту
вращения, который линейно зависит от напряжения сдвига. В зависимости от
пределов измерения вязкости вискозиметр снабжен набором внутренних и внешних
измерительных цилиндров.
Внешний цилиндр измерительной
системы наполняли исследуемым образцом и присоединяли к прибору. Измерения
проводились при постоянной температуре, начиная с самых низких частот вращения.
Напряжение сдвига τ (в Па)
рассчитывали по формуле:
τ = Кα
где К - константа измерительного
цилиндра;
α - показания прибора.
Динамическую вязкость η (в Па∙с)
рассчитывали по следующей формуле:
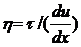
Используя полученные данные, строили
зависимости вязкости и напряжения сдвига от градиента скорости сдвига.
.2.7 Определение рН дисперсий
рН дисперсий определяли с помощью
рН-метра марки рН-121.
В качестве измерительного электрода
использовался хлорсеребряный электрод. В качестве электрода сравнения -
стеклянный.
3. Результаты и их обсуждение
В последнее время большой интерес
вызывают композитные дисперсии полимеров и неорганических пигментов. Частицы
полимерной дисперсии, сорбируясь на поверхности частиц пигмента, препятствуют
их агрегации и позволяют более равномерно распределиться частицам пигмента в
водной фазе, что в свою очередь приводит к изменению оптических свойств таких
систем [14]. Например, при применении диоксида титана в качестве носителя
повышается укрывистость воднодисперсионного материала, изменяются реологические
свойства и снижается расход самого диоксида титана.
С другой стороны, наличие
неорганического носителя, приводит к изменению физико-механических свойств
полимеров [29].
Одним из способов получения подобных
композитных систем является совмещение водной суспензии неорганического
наполнителя и дисперсий полимеров, содержащих полимер, способный
адсорбироваться на поверхности частиц пигмента [30].
Другим подходом к получению таких
композитных систем может быть непосредственный синтез полимера из мономеров с
использованием неорганического наполнителя [26]. В этом случае возможно
образование композитных частиц типа «ядро-оболочка», ядром которых служит
частица наполнителя; частиц полимера, наполненных неорганическими частицами или
композитных частиц, состоящих из частицы наполнителя с адсорбированными на нем
частицами полимера. В любом варианте, конечным результатом является уже
наполненный водно-дисперсионный лакокрасочный материал.
Целью данной работы было
исследование эмульсионной полимеризации некоторых акриловых мономеров c
использованием диоксида титана в качестве неорганического носителя, а также
влияние его на свойства получаемых дисперсий.
Для достижения поставленной цели
было необходимо решить следующие задачи:
выбрать неорганический носитель для
акриловых дисперсий;
синтезировать методом эмульсионной
полимеризации дисперсии акриловых полимеров с использованием диоксида титана в
качестве неорганического носителя;
оценить влияние неорганического
носителя на стабильность и свойства полученных дисперсий;
На начальном этапе работы методом
дисперсионного анализа было определено распределение по размеру частиц
некоторых марок диоксида титана и кислотно-основные свойства их поверхности. По
результатам исследования был выбран один из образцов диоксида титана и получены
дисперсии полиметилметакрилата, как с использованием неорганического носителя,
так и без него. У синтезированных дисперсий определялась агрегативная устойчивость,
содержание диоксида титана в твердой фазе, оценивались реологические свойства.
На основании полученных данных были
выбраны условия синтеза получаемых дисперсий.
.1 Выбор неорганического носителя
для акриловых дисперсий
полимеризация дисперсия
акриловый диоксид титан
С целью выбора наиболее
высокодисперсного неорганического носителя, подходящего для синтеза композитных
дисперсий, были изучены несколько образцов диоксида титана.
Образцы диоксида титана
диспергировали в воде с добавлением небольшого количества ПАВ на ультразвуковом
диспергаторе УЗДН в течение 15 секунд. Поскольку диоксид титана марки АК для
сохранения своих свойств был обработан органическими соединениями
производителем, то пигмент предварительно прокаливали при температуре 600 °С в течении 5 часов.
На рисунке 3.1 представлены
результаты дисперсионного анализа для выбранных образцов диоксида титана.
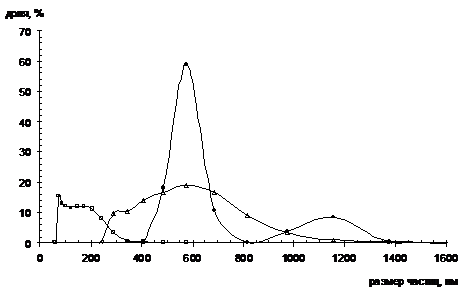

Рисунок 3.1 - Кривые численного распределения по
размеру частиц образцов диоксида титана:
1 - Light Stabilazer 210, 2 -
Hombikat UV100, 3 - АК
Из рисунка 3.1 видно, что наименьшим средним
размером частиц обладает образец диоксида титана Light
Stabilazer. Его водные
суспензии более устойчивы к седиментации и, кроме того, не требуют
дополнительной стабилизации. Суспензии диоксида титана марок Hombikat
и АК неустойчивы во времени, в течение 1 часа происходит почти полное осаждение
частиц пигмента.
Частицы диоксида титана могут оказывать влияние
как на сам процесс полимеризации, так и на стабильность образующейся дисперсии,
например за счет адсорбции на своей поверхности мономера, инициатора или
эмульгатора.
Для определения возможности сорбции компонентов
системы на поверхности частиц диоксида титана, методом неводного титрования
были определены концентрация и сила кислотно-основных центров. На рисунках
3.2-3.4 представлены гистограммы распределения кислотных и основных центров
исследованных образцов диоксида титана.

Рисунок 3.2 - Гистограмма распределения
кислотных и основных центров диоксида титана марки Hombikat UV100

Рисунок 3.3 - Гистограмма распределения
кислотных и основных центров диоксида титана марки АК

Рисунок 3.4 - Гистограмма распределения
кислотных и основных центров диоксида титана Light
Stabilazer
Таблица 3.1 - Суммарное содержание кислотных и
основных центров образцов диоксида титана
|
Марка
диоксида титана
|
Суммарное
содержание кислотных центров, мкмоль/г
|
Суммарное
содержание основных центров, мкмоль/г
|
|
Hombikat
UV100
|
63,0
|
162,7
|
|
АК
|
192,0
|
121,7
|
|
Light Stabilazer
|
203,8
|
101,2
|
Можно заметить, что на поверхности диоксида
титана марки Hombikat
преобладают основные центры. В тоже время на поверхности частиц диоксида титана
Light Stabilazer
и АК в основном преобладают кислотные центры.
С точки зрения кислотно-основного баланса
поверхности диоксида титана при инициировании процесса эмульсионной
полимеризации персульфатом аммония наиболее подходящим для использования в
качестве носителя при получении дисперсий является Hombikat UV100,
имеющего максимальное содержание основных центров.
Однако, для получения дисперсий, устойчивых во
времени, необходимо, чтобы размер частиц неорганического носителя был соизмерим
с размером частиц получаемой дисперсии. Поэтому для синтеза дисперсий методом
эмульсионной полимеризации выбран диоксид титана Light
Stabilazer.
Поскольку персульфат аммония является
инициатором при проведении эмульсионной полимеризации акриловых мономеров,
необходимо определить величину его адсорбции на поверхности неорганического наполнителя.
Так как при диссоциации персульфата аммония в воде образуется персульфат-анион,
весьма вероятно, что заметной адсорбции инициатора на преобладающих кислотных
центрах поверхности диоксида титана Light
Stabilazer не будет.
Для определения адсорбции персульфата аммония в
водную суспензию диоксида титана вводили инициатор в том же самом количестве,
что используется для инициирования полимеризации. Суспензию перемешивали с
помощью механической мешалки в течение 1 часа при температуре 20-22°С.
Содержание персульфата аммония в водной фазе
определяли методом йодометрического титрования. Результаты приведены в таблице
3.2.
Таблица 3.2 - Содержание персульфата аммония в
исходном растворе и в водной фазе после адсорбции на диоксиде титана
|
Содержание
персульфата аммония, г/л
|
|
в
исходном растворе
|
после
адсорбции
|
|
4,80
|
4,58
|
Установлено, что содержание персульфата в водной
фазе до проведения адсорбции и после нее практически не изменяется, при этом
величина его адсорбции на поверхности диоксида титана незначительна и
составляет 0,04 мМоль/г. Кроме того, диоксид титана не вызывает распада
инициатора.
При механическом воздействии на пигмент в водной
суспензии в присутствии эмульгатора и при нагревании, может происходить
«разбивка» агрегатов диоксида титана и уменьшение размеров частиц. Для оценки
влияния механического воздействия, присутствия ПАВ и температуры на размер
частиц образующейся суспензии диоксида титана был проведен дисперсионный анализ
с помощью лазерного анализатора размеров частиц NanoTrack
на разных стадиях приготовления суспензии: после механического перемешивания в
течение 1 часа, введения сульфонола и перемешивания в течение 1 часа, а также
при нагревании до температуры 60-65 °С и выдержки при
перемешивании в течение 6 часов.
На рисунке 3.5 представлены результаты
дисперсионного анализа суспензии диоксида титана в зависимости от условий.
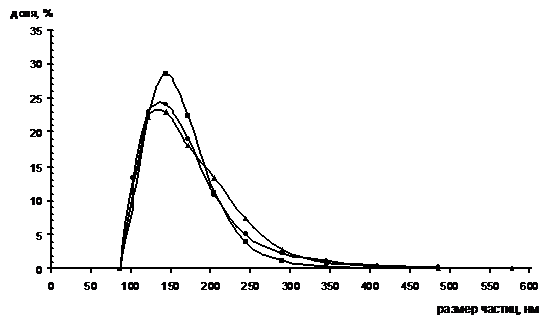

Рисунок 3.5 - Кривые численного распределения по
размеру частиц диоксида титана в зависимости от условий:
- исходная суспензия; 2 - суспензия с добавкой
ПАВ; 3 - суспензия с добавкой ПАВ, выдержанная при температуре 60-70°C.
Из рисунка 3.5 можно заметить, что введенный
эмульгатор вызывает незначительное укрупнение частиц суспензии, за счет их
частичной коагуляции (кривая 2). Температура и механическое воздействие
приводят к сужению кривой распределения (кривая 3), т.е. происходит частичное
разрушение ранее образовавшихся агрегатов.
На основании дисперсионного анализа суспензий,
полученных при вышеназванных условиях, можно сделать вывод, что использование
эмульгатора при повышении температуры обработки приводит к снижению полидисперсности
суспензии диоксида титана, практически не изменяя наивероятнейшего размера
частиц.
3.2 Синтез дисперсий акриловых полимеров
Из литературных данных известно, что в качестве
инициатора для эмульсионной полимеризации используют водорастворимые перекисные
соединения - персульфаты калия или аммония, пероксид водорода. Обычно
концентрация инициатора не превышает 3% от массы мономера [31].
В данной работе, в качестве инициатора
использовался персульфат аммония, в количестве 1 и 2% от массы мономера.
В качестве эмульгаторов в эмульсионной
полимеризации используются натриевые и калиевые соли жирных кислот, сульфаты с
алкильными заместителями, алкил- и алкилбензолсульфонаты. Поскольку
полимеризация протекает преимущественно в мицеллах, то эмульгатор вводят в
количествах, превышающих критическую концентрацию мицеллообразования (ККМ)
[31].
В качестве эмульгатора в данной работе
использовалась натриевая соль алкилбензолсульфоновой кислоты - сульфонол.
Для определения концентрации сульфонола как
эмульгатора была определена его критическая концентрация мицеллообразования
(ККМ) по изотерме поверхностного натяжения (Рис. 3.6). Поверхностное натяжение
растворов ПАВ различной концентрации определяли методом отрыва кольца (метод Дю
Нуи).
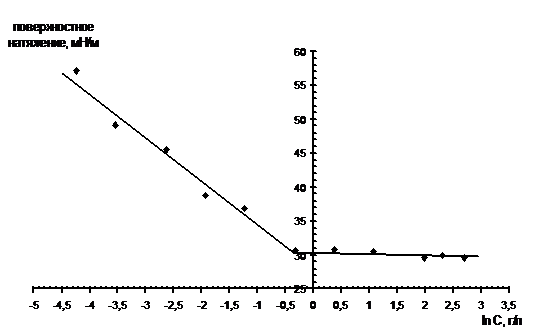
Рисунок 3.6 - Изотерма поверхностного натяжения
натрий алкилбензолсульфоната (сульфонола)
Из приведенных данных следует, что критическая
концентрация мицеллообразования составляет 0,67 г/л.
Известно, размер частиц дисперсий при
эмульсионной полимеризации зависит от количества эмульгатора [31].
В данной работе для получения устойчивых
дисперсий с малым размером частиц была выбрана концентрация эмульгатора
заведомо больше ККМ в связи с тем, что часть эмульгатора будет расходоваться на
сорбцию на поверхности частиц диоксида титана.
При получении водных дисперсий полимеров
концентрация мономера в исходной системе обычно составляет от 15 до 40% [31].
В качестве мономера в данной работе
использовался метилметакрилат, как наиболее дешевый и доступный из акриловых
мономеров.
Концентрация метилметакрилата составляла 15% от
массы водной фазы, концентрация инициатора 1% от массы мономера. Синтез
полимерных дисперсий проводили при интенсивном перемешивании при температуре
65-70 °С
в течение 6-7 часов.
У синтезированной дисперсии определяли размер
частиц. Результаты дисперсионного анализа представлены на рисунке 3.7 (кривая
1).
В аналогичных условиях (температура,
концентрация эмульгатора и инициатора) была синтезирована дисперсия с
увеличенной до 30% концентрацией мономера. Данные ее дисперсионного анализа
представлены на рисунке 3.7 (кривая 2)
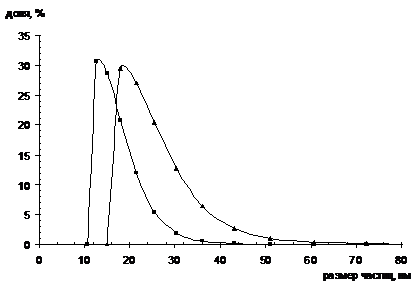

Рисунок 3.7 - Кривые численного распределения по
размеру частиц синтезированных дисперсий:
- исходная концентрация метилметакрилата 15%; 2
- исходная концентрация метилметакрилата 30%.
Как можно заметить, при концентрации мономера
15% средний размер частиц дисперсии полиметилметакрилата составляет 20 нм, при
концентрации 30% - средний размер частиц 15 нм.
При этом увеличение концентрации мономера в
системе приводит к заметному изменению в характере распределения, заметно
снижая полидисперсность. В том и другом случае максимальный размер частиц не
превышает 75 нм и условия синтеза позволяют получать полимерные дисперсий с
наноразмерными частицами.
У синтезированных дисперсий полиметилметакрилата
были определены некоторые показатели, которые представлены в таблице 3.3
Таблица 3.3 - Характеристика дисперсий
|
Наименование
показателя
|
Дисперсия
ПММА
|
Дисперсия
ПММА с использованием диоксида титана в качестве неорганического носителя
|
|
[ММА]= 15%
|
[ММА]= 30%
|
[ММА]= 15%
|
[ММА]= 30%
|
|
Массовая
доля нелетучих веществ, %
|
12,4
|
22,8
|
15,7
|
24,6
|
|
рН
|
2,9
|
2,75
|
3,9
|
4,5
|
|
Поверхностное
натяжение мН/м
|
27,9
|
33,9
|
31,2
|
31,2
|
|
Содержание
диоксида титана в твердой фазе дисперсии, %
|
-
|
-
|
7,3
|
7,8
|
|
Конверсия
мономера, %
|
75
|
83
|
75
|
80
|
По результатам исследования синтезированных
дисперсий ПММА можно отметить, что конверсия мономера во всех случаях
достаточно высока и составляет 75-83%. Хотя раствор сульфонола исходной
концентрации имеет уровень рН равный 8,0, уровень рН синтезированных дисперсий
заметно ниже. Низкое значение рН дисперсий можно объяснить гидролизом
эмульгатора до алкилбензолсульфоновой кислоты в процессе синтеза.
Поверхностное натяжение дисперсий при увеличении
концентрации мономера незначительно увеличивается, т.е. происходит уменьшение
концентрации ПАВ в дисперсии, за счет сорбции его на большем количестве частиц
полимера.
Также были синтезированы дисперсии ПММА,
содержащие диоксид титана. Доля диоксида титана составляла 10% от массы
мономера. Диоксид титана предварительно перемешивали в растворе инициатора в
течение 1 часа при температуре 20-25 °С. Затем, в систему
вводили эмульгатор, перемешивали в течение 10 минут и постепенно вводили
мономер. Синтез проводили при температуре 65-70 °С в течение
6-7 часов.
Концентрация инициатора была увеличена до 2% от
массы мономера, для компенсации его возможного разложения при получении
суспензии диоксида титана.
У полученных дисперсий определяли массовую долю
нелетучих веществ, рН среды, поверхностное натяжение. Результаты анализа также
представлены в таблице 3.3.
Можно отметить, что наличие диоксида титана не
влияет на конверсию мономера. Конверсия мономера составляет 75-80%.
Незначительно увеличивается рН дисперсий, что можно объяснить уменьшением
количества эмульгатора в растворе и, соответственно, уменьшением количества
алкилбензолсульфоновой кислоты, образующейся в результате гидролиза сульфонола.
Об уменьшении количества эмульгатора в растворе также свидетельствует
увеличение поверхностного натяжения дисперсии. Уменьшение количества ПАВ можно
объяснить его сорбцией на поверхности частиц диоксида титана или на поверхности
образующихся композитных частиц «полимер - пигмент».
Для определения количества диоксида титана,
вошедшего в состав твердой фазы, образец дисперсии коагулировали
концентрированным раствором квасцов, полученный осадок многократно промывали
дистиллированной водой для удаления электролита и эмульгатора. Осадок отделяли
центрифугированием от водной фазы и высушивали до постоянной массы при
температуре Т=105 °С.
Содержание диоксида титана в твердой фазе
дисперсии определяли гравиметрическим методом, по потере массы при прокаливании
при температуре 600 °С. Результаты эксперимента
представлены в таблице 3.3.
Как следует из экспериментальных данных,
содержание диоксида титана в твердой фазе дисперсий ПММА, полученных с
использованием его в качестве неорганического носителя, составило около 8%, вне
зависимости концентрации мономера. Т.е. почти 80% введенного при полимеризации
диоксида титана вошло в состав композитных частиц.
На рисунке 3.8 представлены микрофотографии
синтезированных дисперсий. На рисунке 3.9 приведена микрофотография исходной
суспензии диоксида титана.
Рисунок 3.8 - Микрофотографии синтезированных
дисперсии при концентрации метилметакрилата 15% (а, б) и 30% (в, г):
а) и в) - дисперсия ПММА; б) и г) - дисперсия
ПММА с использованием диоксида титана в качестве неорганического носителя (размер
ячейки сетки на всех рисунках 30х30 мкм)

Рисунок 3.9 - Микрофотография суспензии диоксида
титана (размер ячейки сетки 30х30 мкм)
Из рисунков 3.8-3.9 видно, что крупных агрегатов
частиц диоксида титана нет и частицы равномерно распределены по объему.
У полученных акриловых дисперсий с
использованием диоксида титана в качестве неорганического носителя также
определяли дисперсионный состав. На рисунке 3.10 приведены кривые распределения
по размерам частиц композитных дисперсий.


Рисунок 3.10 - Кривые численного распределения
по размеру частиц дисперсий, синтезированных с использованием диоксида титана в
качестве неорганического носителя:
- исходная концентрация метилметакрилата 15%; 2
- исходная концентрация метилметакрилата 30%.
По кривым распределения можно заметить, что
средний размер частиц в дисперсиях, полученных с использованием диоксида титана
в качестве неорганического носителя, увеличился и составил 50 нм при исходной
концентрации мономера 30% (рис. 3.10, кривая 2). Кривая распределения для
дисперсии с концентрацией мономера 15% обладает бимодальностью, с двумя
максимумами на 120 нм и 450 нм (рис. 3.10, кривая 1). Частицы с размером около
120 нм могут соответствовать частицам диоксида титана, частицам
полиметилметакрилата и композитным частицам «полимер - пигмент». Частицы с
размером около 450 нм вероятно соответствуют крупным агрегатам частиц диоксида
титана и полимера.
Более низкие значения размера частиц при более
высокой концентрации мономера (рис. 3.10, кривая 2) вероятнее всего связаны с
тем, что при малом содержании мономера образующегося полимера недостаточно для
полной «капсуляции» частиц пигмента. Соответственно, в случае большей
концентрации мономера, полиметилметакрилата образуется больше и происходит
более полная капсуляция частиц пигмента полимером.
.3 Влияние неорганического носителя на
стабильность и свойства акриловых дисперсий
Одним из важных показателей дисперсионных систем
является их агрегативная устойчивость, т.е. характер изменения размера частиц
дисперсии в течение времени. Для оценки агрегативной устойчивости
синтезированных дисперсий определяли их дисперсионный состав в зависимости от
времени хранения.
На рисунках 3.11-3.15 приведены результаты
дисперсионного анализа синтезированных дисперсий в течение времени.
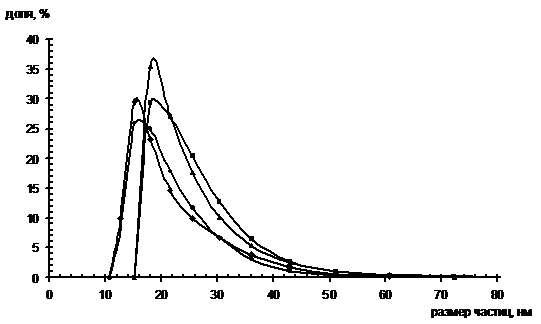

Рисунок 3.11 - Кривые численного распределения
по размеру частиц дисперсий ПММА, в зависимости от времени. 1 - через 1 час; 2
- через 1 сутки; 3 - через 30 суток; 4 - 56 суток. Исходная концентрация
метилметакрилата 15%
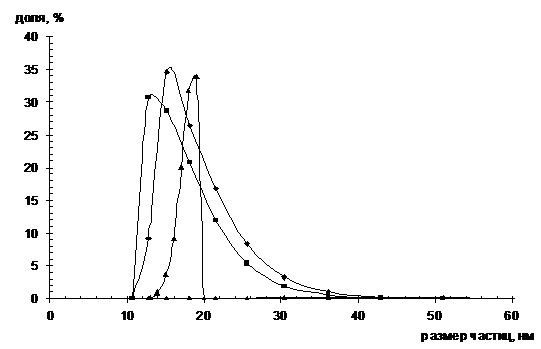

Рисунок 3.12 - Кривые численного распределения
по размеру частиц дисперсий ПММА, в зависимости от времени. 1 - через 1 час; 2
- через 6 суток; 3 - через 17 суток. Исходная концентрация метилметакрилата 30%
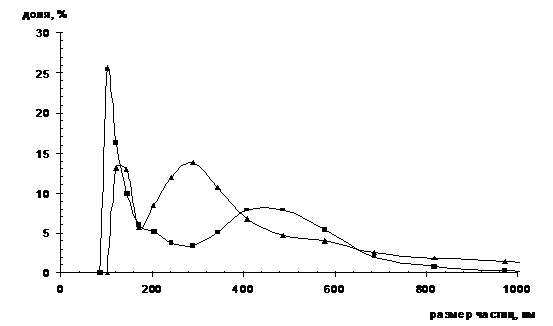

Рисунок 3.13 - Кривые численного распределения
по размеру частиц дисперсий ПММА, синтезированных с использованием диоксида
титана в качестве неорганического носителя, в зависимости от времени. 1 - через
1 час; 2 - через 7 суток. Исходная концентрация метилметакрилата 15%


Рисунок 3.14 - Кривые численного распределения
по размеру частиц дисперсий ПММА, синтезированных с использованием диоксида
титана в качестве неорганического носителя, в зависимости от времени. 1 - через
14 суток; 2 - через 59 суток. Исходная концентрация метилметакрилата 15%


Рисунок 3.15 - Кривые численного распределения
по размеру частиц дисперсий ПММА, синтезированных с использованием диоксида
титана в качестве неорганического носителя, в зависимости от времени. 1 - через
2 суток; 2 - через 14 суток. Исходная концентрация метилметакрилата 30%
Из рисунка 3.11 видно, что синтезированная
дисперсия ПММА устойчива во времени. Заметного изменения размера частиц не
происходит, лишь по истечении 30 суток происходит смещение кривой распределения
в сторону меньших размеров частиц. Вероятно, это связано с пептизацией крупных
полимерных агломератов. Увеличение концентрации мономера не приводит к
ухудшению стабильности полимерной дисперсии (рис 3.12), лишь с течением времени
наблюдается незначительная коагуляция частиц (рис. 3.12, кривые 1 и 3).
В случае использования диоксида титана в
качестве неорганического носителя наблюдаются несколько иные явления (рис.
3.13-3.15). Например, у дисперсии ПММА, полученной при исходной концентрации
мономера 15%, в течение 7 суток наблюдаются два противоположных процесса -
пептизация крупных и агрегация мелких частиц, о чем свидетельствует сближение
максимумов на кривой распределения (рис. 3.12, кривая 1). С одной стороны,
размер частиц уменьшается с 400-500 нм до 200-250 нм, с другой стороны,
уменьшается доля тонкодисперсной фракции (рис 3.13, кривые 1 и 2). В целом
полидисперсность системы увеличивается.
При более длительном хранении процесс коагуляции
начинает превалировать и средний размер частиц возрастает до 250-300 нм (рис.
3.14, кривая 1), и через 60 суток дисперсия разрушается - средний размер частиц
составляет 850-1000 нм.
При увеличении исходной концентрации
метилметакрилата, средний размер частиц композитной дисперсии ПММА - диоксид
титана, составляет 80-90 нм (рис. 3.15, кривая 1). Но сама система обладает
большей агрегативной устойчивостью. Через 14 суток средний размер частиц
увеличивается всего лишь до 120-150 нм (рис 3.15, кривая 2). Более высокую
стабильность таких дисперсий, вероятнее всего, можно объяснить более высокой
адсорбцией эмульгатора на поверхности дисперсной фазы. В результате этого
меньшее количество ПАВ подвергается гидролизу. Хотя, константа диссоциации
алкилбензолсульфоновой кислоты соизмерима с константой диссоциации натриевой
соли той же кислоты, величина гидрофильно-липофильного баланса для сульфонола
меньше, чем для алкилбензолсульфоновой кислоты.
Таким образом, вероятно, в системе присутствуют
ПАВ двух типов: алкилбензолсульфоновая кислота и сульфонол (анионактивный) с
разной поверхностной активностью. В данном случае количество анионактивного ПАВ
больше, и стабильность дисперсий оказывается выше. Кроме того, на поверхности
диоксида титана модификации рутил всегда находятся атомы алюминия. Алкилбензолсульфоновая
кислота может взаимодействовать с алюминием, образуя нерастворимые соли, что
может вызывать коагуляцию частиц. Т.к. в данных дисперсиях количество
алкилбензолсульфоновой кислоты меньше, стабильность их оказывается выше.
Одним из важных показателей полимерных
материалов являются их реологические свойства. Наличие в дисперсной фазе
неорганического носителя может оказывать значительное влияние на характер
течения таких дисперсий.
Для оценки реологических свойств синтезированных
с использованием диоксида титана в качестве неорганического носителя в
сравнении с дисперсий ПММА, с помощью ротационного вискозиметра получали кривые
течения данных дисперсий.
На рисунке 3.16 представлены кривые течения
дисперсий ПММА, полученных при различных исходных концентрациях мономера. На
рисунке 3.17 представлены кривые зависимости динамической вязкости от скорости
сдвига для тех же образцов.


Рисунок 3.16 - Кривые течения дисперсий ПММА,
при различной исходной концентрации мономера. 1 - концентрация метилметакрилата
15%; 2 - концентрация метилметакрилата 30%.


Рисунок 3.17 - Зависимость динамической вязкости
дисперсий ПММА от скорости сдвига при различной исходной концентрации мономера:
1 - концентрация метилметакрилата 15%; 2 - концентрация метилметакрилата 30%
Как следует из рисунков 3.16 и 3.17 дисперсии
ПММА по характеру течения являются ньютоновскими жидкостями. Вязкость дисперсии
с большей концентрацией мономера несколько выше, чем у дисперсии с меньшим
количеством метилметакрилата, что объясняется большим содержанием дисперсной
фазы.
Реологические свойства дисперсий, содержащих
диоксид титана, отличаются от поведения дисперсий, содержащих только полимер.
На рисунках 3.18 и 3.19 представлены
соответственно кривая течения и зависимость динамической вязкости от скорости
сдвига для дисперсии ПММА, содержащей диоксид титана. Исходная концентрация
мономера составляла 15%.

Рисунок 3.18 - Кривая течения дисперсии ПММА,
содержащей диоксид титана. Исходная концентрация мономера 15%.
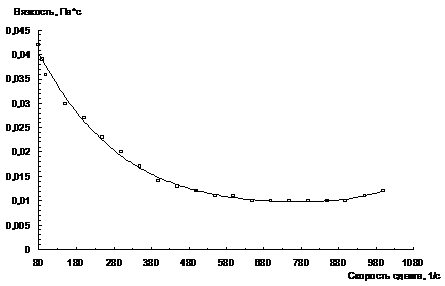
Рисунок 3.19 - Зависимость динамической вязкости
дисперсии ПММА, содержащей диоксид титана, от скорости сдвига. Исходная
концентрация мономера 15%.
Согласно рисункам 3.18 и 3.19 дисперсия, содержащая
композитную дисперсную фазу, по характеру течения не является «ньютоновской»
жидкостью в отличие от дисперсии, полученной без использования неорганического
носителя. Характер изменения динамической вязкости при увеличении скорости
сдвига свидетельствует о значительной тиксотропии, т.е. достаточно сильном
структурировании дисперсии, синтезированной с использованием неорганического
носителя. Однако, при достаточно высоких скоростях сдвига (более 800 см-1)
система приобретает слабую дилатансию.
С целью оценки тиксотропии дисперсий, полученных
с использованием неорганического носителя, с помощью ротационного вискозиметра
у композитной дисперсии определяли реологические свойства сначала с увеличением
скорости сдвига до максимума, а затем с уменьшением от максимального значения
до минимального. Кроме того, после достижения минимальной скорости сдвига,
систему выдерживали в течение определенных промежутков времени, необходимых для
восстановления разрушенной структуры.
На рисунках 3.20-3.24 приведены кривые течения
анализируемой дисперсии в зависимости от времени структурного восстановления.
Верхняя ветвь кривой соответствует «прямому» ходу, нижняя - «обратному».
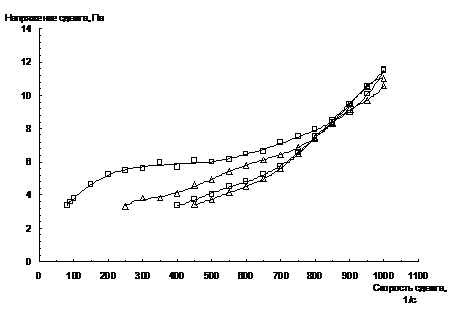

Рисунок 3.20 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным
испытанием. Исходная концентрация мономера 15%. 1 - исходная дисперсия; 2 - 30
минут.
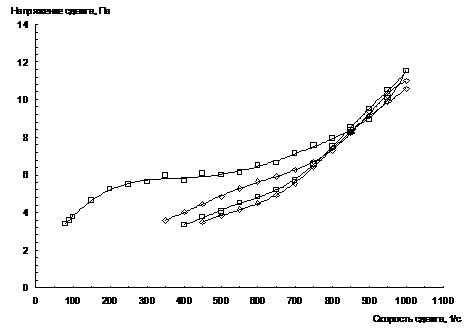

Рисунок 3.21 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным
испытанием. Исходная концентрация мономера 15%. 1 - исходная дисперсия; 2 - 60
минут.
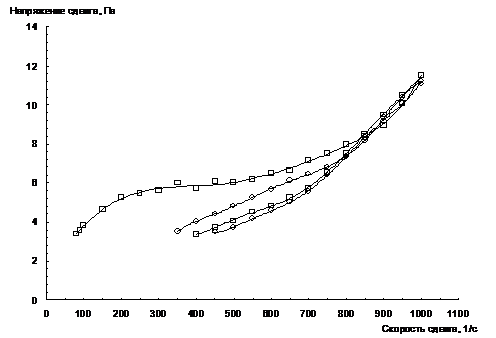
Рисунок 3.22 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным
испытанием. Исходная концентрация мономера 15%. 1 - исходная дисперсия; 2 - 90
минут.
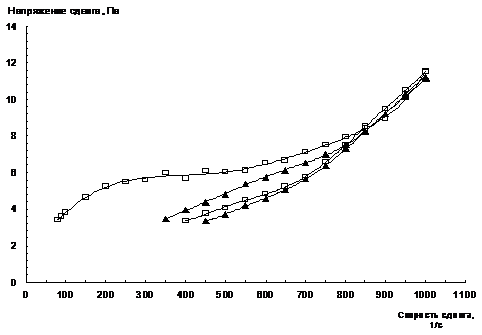

Рисунок 3.23 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным
испытанием. Исходная концентрация мономера 15%. 1 - исходная дисперсия; 2 - 120
минут.


Рисунок 3.24 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным испытанием.
Исходная концентрация мономера 15%. 1 - исходная дисперсия; 2 - 1 сутки.
О времени восстановления системой своей
структуры можно судить по степени приближения кривой течения через определенный
промежуток времени к кривой течения исходной композитной дисперсии.
Из рисунков 3.20 - 3.25 можно заметить, что
структурирование системы не восстанавливается даже через 1 сутки, о чем
свидетельствуют более низкие значения динамической вязкости при всех скоростях
сдвига.


Рисунок 3.25 - Зависимость динамической вязкости
дисперсии ПММА, содержащей диоксид титана, от скорости сдвига, при различном
времени выдержки перед повторным испытанием. Исходная концентрация мономера
15%. 1 - исходная дисперсия; 2 - 1 сутки.
При увеличении исходной концентрации мономера до
30% наблюдаемое явление структурирования сохраняется, причем процесс протекает
быстрее - уже через 30 минут вязкость дисперсии достигает практически
начального значения (рис. 3.27) и характер течения восстанавливается до
исходного (кривые 1 и 2, рис. 3.26).
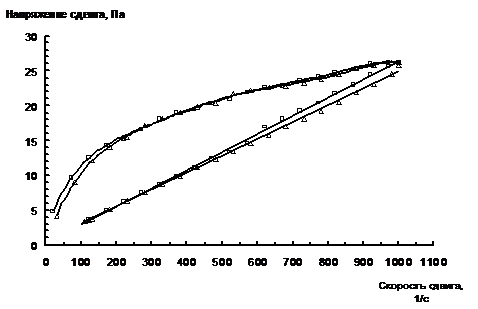

Рисунок 3.26 - Кривая течения дисперсии ПММА,
содержащей диоксид титана, при различном времени выдержки перед повторным
испытанием. Исходная концентрация мономера 30%. 1 - исходная дисперсия; 2 - 30
минут.


Рисунок 3.27 - Зависимость динамической вязкости
дисперсии ПММА, содержащей диоксид титана, от скорости сдвига при различном
времени выдержки перед повторным испытанием. Исходная концентрация мономера
30%. 1 - исходная дисперсия; 2 - через 30 минут.
Структурирование дисперсий, содержащих диоксид
титана, вероятно можно объяснить тем, что в процессе синтеза образуются
композитные частицы «полиметилметакрилат-диоксид титана». Строение таких частиц
может быть различным - «ядро-оболочка», наполненная частица и т.п. Но в любом
случае, вне зависимости от строения таких частиц, диоксид титана может
приводить к изменению в структуре макромолекул полиметилметакрилата. Например,
макромолекула может принимать такую конформацию, что сложноэфирные связи
элементарных звеньев полимера будут ориентированы в сторону дисперсионной
среды. Т.к. сложноэфирная группа обладает небольшим дипольным моментом, можно
ожидать появления ориентационных взаимодействий между ними, и, как следствие,
появление определенных структур.
3.4 Влияние свойств полимера на свойства
акриловых дисперсий, синтезируемых с использованием неорганического носителя
Поскольку полиметилметакрилат является
достаточно жестким полимером с высокой температурой стеклования, для
модификации полимера композитной дисперсии в состав исходной мономерной смеси
вводили другие акриловые мономеры, способствующие снижению температуры
стеклования. В качестве таких мономеров были выбраны бутилакрилат и
нонилакрилат. Их содержание в мономерной смеси составляло 30%.
На основе таких мономерных смесей были
синтезированы дисперсии, как с использованием диоксида титана в качестве
неорганического носителя, так и без него. Также, для сравнения были получены
дисперсии на основе гомополимера бутилметакрилата.
Синтез дисперсий проводили в тех же самых
условиях, что и при синтезе дисперсии полиметилметакрилата.
У синтезированных дисперсий определяли массовую
долю нелетучих веществ, содержание диоксида титана в твердой фазе дисперсии,
поверхностное натяжение и рН. Результаты испытаний представлены в таблице 3.4.
Таблица 3.4 - Результаты испытаний
синтезированных дисперсий
|
Дисперсия
|
Массовая
доля нелетучих веществ, %
|
Поверхностное
натяжение, мН/м
|
рН
|
Содержание
диоксида титана в твердой фазе, %
|
|
дисперсия
сополимера метилметакрилата с нонилакрилатом (70:30)
|
12,9
|
31,0
|
2,85
|
-
|
|
дисперсия
сополимера метилметакрилата с нонилакрилатом (70:30) с диоксидом титана
|
13,2
|
30,2
|
4,6
|
4,1
|
|
дисперсия
сополимера метилметакрилата с бутилакрилатом (70:30)
|
13,5
|
29,1
|
2,8
|
-
|
|
дисперсия
сополимера метилметакрилата с бутилакрилатом (70:30) с диоксидом титана
|
12,7
|
30,6
|
3,65
|
0,7
|
|
дисперсия
полибутилметакрилата
|
12,0
|
42,0
|
2,65
|
-
|
|
дисперсия
полибутилметакрилата с диоксидом титана
|
13,4
|
36,9
|
3,2
|
0,2
|
По данным таблицы 3.4 можно заметить, что
содержание диоксида титана в твердой фазе дисперсий на основе
полибутилметакрилата и на основе сополимера метилметакрилата и бутилакрилата не
превышает 1%. В дисперсиях на основе сополимера метилметакрилата и
нонилакрилата доля диоксида титана в твердой фазе выше и достигает 4%.
Столь низкое содержание диоксида титана в
дисперсии можно объяснить с точки зрения физических свойств полимера.
Полибутилметакрилат имеет температуру стеклования около 30 °С,
в то время как у полиметилметакрилата температура стеклования достигает 105 °С.
Поскольку температура синтеза достигала 70 °С, то при таких
условиях полиметилметакрилат находился в стеклообразном состоянии, а
полибутилметакрилат - в высокоэластическом. Если учитывать, что в процессе
эмульсионной полимеризации в системе находятся полимер-мономерные частицы, то,
очевидно, что температура размягчения их будет еще ниже. Подобные частицы
прилипают к частицам диоксида титана и «склеивают» частицы пигмента между
собой. Т.е. в данных условиях образование стабильной дисперсии не происходит,
но происходит преждевременная коагуляция частиц дисперсной фазы. Аналогичные
явления происходят и для системы метилметакрилат-бутилакрилат (температура
стеклования сополимера около 30 °С). В случае применения метилметакрилата и
нонилакрилата температура стеклования образующегося сополимера несколько выше,
составляет около 35 °С, и доля скоагулировавших частиц оказывается меньше.
Когда в полимеризации участвует только метилметакрилат, температура размягчения
полимер-мономерных частиц оказывается выше или соизмеримой с температурой
синтеза. Соответственно, при интенсивном перемешивании коагуляции таких частиц
не происходит.
На рисунках 3.28-3.31 приведены результаты
реологических исследований полученных дисперсий.
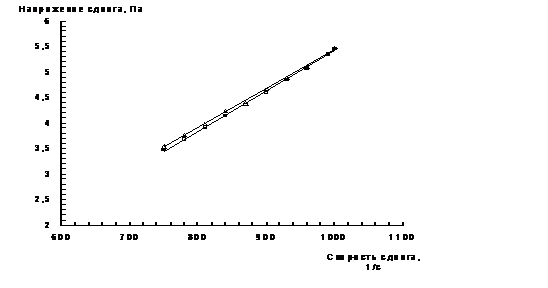

Рисунок 3.28 - Кривые течения дисперсий
сополимеров с ММА: 1 - дисперсия сополимера метилметакрилата с бутилакрилатом;
2 - дисперсия сополимера метилметакрилата с нонилакрилатом.
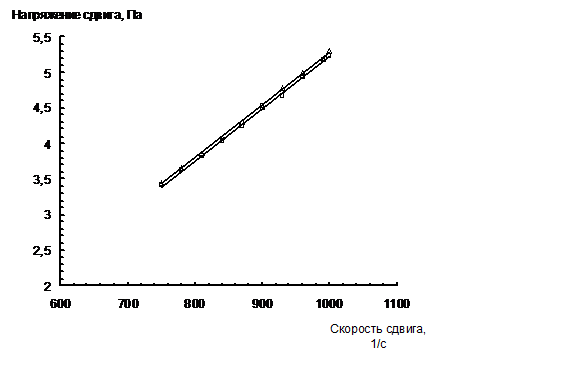

Рисунок 3.29 - Кривые течения дисперсий
сополимеров с ММА, содержащих диоксид титана: 1 - дисперсия сополимера
метилметакрилата с бутилакрилатом; 2 - дисперсия сополимера метилметакрилата с
нонилакрилатом.
|
 а) а)
|
 б) б)
|
Рисунок 3.30 - Зависимость динамической вязкости
дисперсии сополимера метилметакрилата с бутилакрилатом от скорости сдвига: а)
дисперсия, не содержащая диоксида титана; б) дисперсия, полученная с
использованием диоксида титана.
|
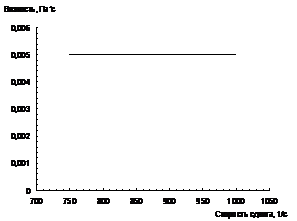 а) а)
|
 б) б)
|
Рисунок 3.31 - Зависимость динамической вязкости
дисперсии сополимера метилметакрилата с нонилакрилатом от скорости сдвига: а)
дисперсия не содержащая диоксида титана; б) дисперсия, полученная с
использованием диоксида титана.
По характеру течения все исследуемые дисперсии
относятся к ньютоновским жидкостям. Поскольку, в составе дисперсной фазы
практически отсутствует пигмент, то его влияние на свойства полимерных частиц
дисперсной фазы незначительно. Соответственно, структурирование не происходит,
что подтверждается кривыми течения и зависимости динамической вязкости от
скорости сдвига.
4. Охрана труда и защита окружающей среды
.1 Свойства применяемых в работе материалов
Токсичные свойства применяемых в работе веществ,
представлены в таблице 4.1
Таблица 4.1 - Токсикологические характеристики
применяемых материалов [32-34]
|
Наименование
вещества, формула
|
Характер
действия на организм человека
|
ПДК
|
Класс
опасности по ГОСТ 12.1.00 7-76
|
Средства
индивидуальной защиты
|
|
|
|
в
воздухе рабочей зоны, мг/м3
|
в
промышленных сточных водах, мг/л
|
|
|
|
|
1
|
2
|
3
|
4
|
5
|
6
|
|
|
Бутилметакрилат
(БМА)
|
Действует
на нервную систему, нарушает функцию печени
|
30
|
0,02
|
3
|
Противогаз
марки «А», спецодежда, очки, перчатки
|
|
|
Бутилакрилат
(БА)
|
Обладает
наркотическим действием, вызывает нарушение липоидно-жирового обмена
|
10
|
0,01
|
3
|
Противогаз
марки «А», очки, перчатки
|
|
|
Нонилакрилат
(НА)
|
Наркотическое
действие, раздражает слизистые оболочки
|
20
|
0,01
|
3
|
Противогаз
марки «А», спецодежда, очки, перчатки
|
|
|
Метилметакрилат
(ММА)
|
Действует
наркотически и общетоксически. Раздражает кожу и слизистые оболочки
|
50
|
-
|
3
|
Противогаз
марки «А», спецодежда, очки, перчатки
|
|
Ацетон
|
Наркотическое
действие
|
200
|
2,2
|
4
|
Противогаз
марки «А», спецодежда
|
|
Натрий
алкилбензолсульфонат (сульфонол)
|
Малотоксичен.
Слабо раздражает кожу и слизистые оболочки органов дыхания и глаз. Вызывает
сухость кожи
|
---
|
---
|
6
|
Средства
защиты кожи (резиновые перчатки и защитные крема)
|
Взрывопожароопасные свойства используемых
веществ приведены в таблице 4.2
Таблица 4.2 - Взрывопожароопасные свойства
применяемых материалов [32-35]
|
Наименование
вещества
|
Агрегатное
состояние
|
Температура
кипения, °С
|
Плотность,
кг/м3
|
Температура,
°С
|
Пределы
воспламенения
|
|
|
|
|
вспышки
|
воспламенения
|
самовоспламенения
|
концентрационные,
%
|
температурные,
°С
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
|
Бутилметакрилат
(БМА)
|
Бесцветная
жидкость
|
169
|
895
|
33,3
|
---
|
---
|
---
|
---
|
|
Бутилакрилат(БА)
|
Бесцветная
жидкость
|
147,4
|
911
|
38
|
---
|
280
|
1,0-7,4
|
30-70
|
|
Нонилакрилат
(НА)
|
Бесцветная
жидкость
|
190
|
1431
|
101,8
|
---
|
334
|
1,7-6,4
|
59-100
|
|
Метилметакрилат
(ММА)
|
Бесцветная
жидкость
|
100
|
936
|
8
|
10
|
460
|
2-43
|
|
Ацетон
|
Бесцветная
жидкость
|
56,24
|
790,8
|
-18
|
---
|
465
|
2,2-13,0
|
-20-6
|
|
Натрий
алкилбензолсульфонат (сульфонол)
|
Вязкая
светло-желтая жидкость
|
---
|
---
|
---
|
---
|
---
|
---
|
---
|
.2 Меры пожарной профилактики
.2.1 Определения категории помещения по
взрывопожароопасности по НПБ 105-03 и класса помещения по ПУЭ
При установлении категории помещения по НПБ
105-03 необходимо знать избыточное давление взрыва. Расчет этого параметра
производится на основе следующих допущений:
в помещении лаборатории произошел розлив ЛВЖ
(легко воспламеняющейся жидкости) в количестве 3 литров. Расчет ведем по самой
легколетучей жидкости (ацетону);
площадь испарения от разлившейся жидкости
принимаем равной 1 м2 на 1 литр ЛВЖ;
максимальное время испарения ЛВЖ принимаем
равным 3600 с;
свободный объем помещения принимаем равным 80%
от геометрического объема помещения.
Для индивидуальных горючих веществ, в состав
которых входят С, Н, N,
О, СI, Br,
I, F,
избыточное давление взрыва (∆P)
рассчитываем по формуле:
ΔP=(Pmax-P0)*(m*z)/(Vсв*ρ)*(100/Сcm)*(1/kн),
где ∆P
- избыточное давление взрыва, кПа;
Рmax
- максимальное давление взрыва стехиометрической газо- или паровоздушной смеси
в замкнутом объеме, кПа (Рmax
для ацетона равен 570 кПа);
Р0 - атмосферное давление в
помещении, принимаем 101 кПа;
m - масса ЛВЖ,
вышедшей в результате расчетной аварии в помещении, кг;
z - коэффициент
участия горючего вещества во взрыве (так как ацетон при комнатной температуре
является нагретым выше температуры вспышки, то z
= 0,3);
Vсв
- свободный объем помещения, м3;
ρ - плотность паров
ЛВЖ, кг/м3;
Сcm
- стехиометрическая концентрация паров ЛВЖ, %(об.);
kн
- коэффициент, учитывающий негерметичность помещения и неадиабатичность
процесса горения (допускается принимать kн
= 3).
Массу ЛВЖ, вышедшей в результате расчетной
аварии в помещении, определяем следующим образом:
m = W*Fn*τ,
где W
- интенсивность испарения, кг/(м2с);
Fn
- площадь испарения от разлившейся ЛВЖ, м2;
τ - длительность
испарения жидкости, 3600с.
Интенсивность испарения ЛВЖ вычисляем по
формуле:
W = 10-6*η*√M*Pн,
где η - коэффициент,
зависящий от скорости и температуры воздушного потока в помещении (при скорости
движения воздуха в помещении лаборатории 0,1 м/с и температуре воздуха 20˚C
принимаем η = 2,40);
Рн - давление насыщенных паров при
расчетной температуре, кПа;
При скорости движения воздуха в тяге 0,1 м/с и
температуре воздуха 20˚C
М - молекулярная масса ЛВЖ (для ацетона М = 58,08 г/моль).
Давление насыщенного пара ацетона при 20˚C
определяем по уравнению Антуана:
lg
Pн
= A-(B/(t+C)),
где A,
B, С - константы
Антуана (для ацетона А = 6,37551, B
= 1281,721, С = 237,088), t
- температура воздуха в помещении,˚C.
Тогда:н =
6,37551-((1281,721)/(20+237,088))=1,390;
Рн = 101,390 =24,547 кПа.
Тогда интенсивность испарения:
W = 10-6*2,40*√58,08*24,547
= 4,49*10-4 кг/(c*м2),
а масса ЛВЖ, вышедшей в результате расчетной
аварии в помещении:
m = 4,49*10-4*3*3600
= 4,849 кг;
Свободный объем помещения определяется по
формуле:
Vсв
= 0,8*V,
где V
- геометрический объем помещения, м3 (в помещении лаборатории V
= 96,08 м3).
Получаем свободный объем помещения:
Vсв
= 0,8*96,08 = 76,864 м3.
Плотность паров ацетона определяем по формуле:
ρ = М/(V0*(1+0,00367*t)),)
где V0
=22,4 м3/кмоль.
Получаем:
ρ = 58,08/(22,4*(1+0,00367*20)) = 2,416 кг/м3.
Стехиометрическую концентрацию паров ацетона
рассчитываем по формуле:
Сcm
= 100/(1+4,84*β),
где β - стехиометрический
коэффициент кислорода в реакции горения;
β = nс+(nн-nx/4)
- (n0/2),
где nc,
nн,
nx, n0
- число атомов углерода, водорода, галогенов и кислорода в молекуле ацетона
соответственно.
β = 3+(6-0)/4 - (1/2) = 4;
Ссm
= 100/(1+4,84*4) = 4,912%(об);
В итоге рассчитываем избыточное давление взрыва:
ΔР=(570-101)*((4,849*0,3)/(76,864*2,416))*(100/4,91)*1/3=24,931
кПа.
В соответствии с НПБ 105-03 лаборатория, в
которой проводились эксперименты, имеет категорию «А» по взрывопожароопасности,
так как избыточное расчетное давление взрыва более 5 кПа. В соответствии с ПУЭ
помещению присваиваем класс B-1б.
.2.2 Средства пожаротушения
Средствами пожаротушения мономеров и
растворителей являются: асбестовое одеяло, песок, огнетушители ОУ-2, ОП-10,
гасительные составы с концентрацией CO2
30%, N2
43%. [36]
Таблица 4.3 - Средства пожаротушения
[36]
|
Наименование
вещества
|
Средства
пожаротушения
|
|
1
|
2
|
|
1
БМА, БА
|
Тонкораспыленная
вода, пена
|
|
2
НА
|
Огнетушитель
углекислотный ОУ-2, песок, асбестовое одеяло
|
|
3
ММА
|
Огнетушитель
углекислотный ОУ-2, песок, асбестовое одеяло, порошковый огнетушитель ОП-2
|
|
4
Ацетон
|
Пена,
тонкораспыленная вода, воздушно-механическая пена на основе пенообразователя
ПО-1, газовые огнегасительные составы
|
|
5
Натрий алкилбензолсульфонат (сульфонол)
|
|
.2.3 Нормы хранения ЛВЖ и ГЖ в лаборатории
Химические реактивы хранятся в закрытых банках,
стеклянных сосудах. На каждом сосуде должна быть этикетка с точным названием
вещества и его подробная характеристика (концентрация, плотность, чистота).
Низкокипящие жидкости, ЛВЖ и ГЖ должны храниться
в толстостенной посуде с плотно закрывающимися пробками, помещенной в
специальный металлический ящик с крышкой, стенки и дон которого должны быть
выложены асбестом. Запрещается хранение в лабораторном помещении ЛВЖ с
температурой кипения ниже -50˚С.
При переносе небольших количеств веществ,
находящихся в стеклянных сосудах, необходимо применять вёдра.
Нормы хранения ЛВЖ и ГЖ в лаборатории
устанавливаются такими, чтобы в случае одновременного розлива всех ЛВЖ и ГЖ
имеющихся в помещении, не создавались взрывоопасные концентрации. Нормы
хранения ЛВЖ: 1 литр на сотрудника, но не более 3 литров на комнату.
.2.4 Правила работы с ЛВЖ и ГЖ
ЛВЖ и ГЖ следует доставлять в лабораторию в
плотно закрытой посуде, помещённой в специальный металлический ящик с ручками.
Все работы с ЛВЖ и ГЖ должны проводиться в вытяжном шкафу при работающей
вентиляции, выключенных газовых и нагревательных приборах.
При случайных розливах ЛВЖ, а также при утечке
горючих газов, необходимо выключить все источники открытого огня,
электронагревательные приборы. Место розлива засыпать песком, затем собрать его
деревянной лопаткой или совком.
Сосуды, в которых проводились работы с ЛВЖ и
горючими веществами, по окончанию работы должны быть промыты.
Запрещается сливать ЛВЖ и ГЖ в канализацию.
Отработанные жидкости следует собирать раздельно, в специальную герметичную
тару.
Спецодежду, загрязненную ЛВЖ и ГЖ, необходимо
заменить во избежание возможного воспламенения.
.3 Метеорологические и санитарно-гигиенические
условия в лаборатории
Исходя из метеорологических условий, в
соответствии с ГОСТ 12.1.005-88 в лаборатории может выполняться легкая
физическая работа (категория I), а также физическая работа средней тяжести
(категория II (а, б)).
Согласно нормам в холодное время года
температура воздуха должна поддерживаться 20-23°С, влажность воздуха 40-60%,
скорость движения воздуха не более 0,2 м/с. В теплое время года - 22-25°С,
60-40%, не более 0,2 м/с соответственно. Метеорологические условия в
лаборатории соответствуют нормам.
Общий объем помещения в лаборатории составляет
96,08 м3, площадь помещения при этом составляет 27,45 м2.
Постоянных работников в помещении лаборатории 2. На одного работающего
приходиться 9,15 м2 от общей площади помещения лаборатории. Высота
помещения 3,5 м. Лаборатория оснащена тремя вытяжными шкафами длиной 1 м. В
вытяжных шкафах работают два человека, следовательно, на одного человека
приходиться 1,5 м длины вытяжного шкафа.
В соответствии с нормами высота лаборатории
должна быть не менее 3 м, на одного человека должно приходиться не менее 4,5 м2
площади помещения и 1-1,5 м длины вытяжного шкафа. Следовательно, помещение
лаборатории соответствует принятым нормам.
.4 Вентиляция лабораторного помещения
Система искусственной вентиляции в лаборатории
приточно-вытяжная. Скорость подсоса воздуха в вытяжном шкафу при высоте
поднятой створки 0,3 м составляет 0,5 м/с. Кратность воздухообмена в вытяжном
шкафу рассчитывается по формуле:
К = W/V,
где К - кратность воздухообмена, ч-1;
W - объем воздуха,
удаляемого из помещения в единицу времени, м3/ч;
V - объем вытяжного
шкафа или лаборатории, м3.
Объем воздуха удаляемого из помещения в единицу
времени, рассчитывается по формуле:
W = ν*S*3600,
где ν - скорость
воздуха в рабочем проеме, м/с;
S - площадь сечения,
м2;
S = 0,3*1 = 0,3 (м2),
W = 0,5*0,3*3600 =
540 (м3/ч).
Кратность воздухообмена для вытяжного шкафа:
К = 540/1,89 = 285,714 (ч-1).
Кратность воздухообмена для лаборатории:
К = 540/96,08 = 5,62 (ч-1).
.5 Освещение помещения лаборатории
В соответствии со СНиП 23-05-95 в лаборатории
предусмотрено естественное боковое освещение. Искусственное освещение
осуществляется люминесцентными лампами ЛД (дневного света - 8 ламп) мощностью
40 Вт. Освещенность не менее 300 лк на одно рабочее место. Освещение вытяжного
шкафа осуществляется светильниками ВЗГ - 300(лампы накаливания мощностью не
более 300 Вт). Коэффициент естественного освещения в вытяжном шкафу 1 - 0,75%,
на поверхности стола 1,5%. Застекленная площадь окон 20%. В лаборатории можно
проводить зрительные работы высокой и средней точности. Разряд зрительной
работы 3 и 4. Группа помещения 1.
.6 Электробезопасность на рабочем месте
Категория помещения по электробезопасности - 1,
с повышенной опасностью. Источниками возгорания могут являться неисправные
электроприборы и электропроводка в электроприборах.
Электронагревательные приборы при ежедневной эксплуатации
должны очищаться от пыли и грязи. При использовании масляной бани необходимо
следить, чтобы масло не попадало на электроплитку и рядом не находились ЛВЖ и
ГЖ. Все приборы должны иметь свое постоянное место с достаточной тепловой
изоляцией. В качестве изолирующего материала используется керамическая плитка,
асбест. В лаборатории имеется заземление и питающая сеть с напряжением 220 В.
.7 Водоснабжение и канализация, удаление сливов
и отходов
Водоснабжение горячей и холодной водой
осуществляется от городской сети, в соответствии со СНиП 2.04.01 - 85. Отходы
химических веществ подлежат сливу в специально оборудованные емкости для слива
органики, кислот, щелочей. Запрещается сливать в канализацию опасные химические
вещества. По мере заполнения тары отходы подлежат утилизации.
.8 Условия безопасного проведения исследований
Все работы проводить в помещениях при постоянно
работающей приточно-вытяжной вентиляции, обеспечивающей чистоту воздуха рабочий
зоны лаборатории. При нормальном режиме работы в лаборатории концентрация
вредных веществ в воздухе не превышает ПДК, все нагревательные приборы
находятся в исправности, работает вентиляция, оборудование отвечает
предъявляемым ему требованиям.
Аварийным режимом работы считается наличие
условий способных вызвать взрыв, пожар, отравление работающих.
Причинами аварийного режима работы могут
служить:
воспламенение ГЖ при нагревании на
электроплитке;
розлив в лаборатории легколетучих жидкостей
образующих ядовитые пары, а так же большого количества азота.
При выделении паров огне-, взрывоопасных веществ
в помещении лаборатории необходимо открыть окна, включить вентиляцию. При
создании опасной концентрации паров огне-, взрывоопасных веществ вблизи от
работающих электроприборов выключить их общим рубильником в коридоре, но не
выключать вилку или рубильник в аварийном помещении.
В случае аварии каждый работник лаборатории
должен принять меры по ликвидации аварии и немедленно известить начальника
лаборатории о случившемся.
Заключение
Методом эмульсионной полимеризации синтезированы
дисперсии полиметилметакрилата с использованием в качестве неорганического
носителя диоксида титана. Показано, что диоксид титана практически полностью
входит в состав композитной дисперсии и позволяет получать устойчивые системы
на основе полиметилметакрилата и диоксида титана.
Установлено, что введение носителя не оказывает
значительного влияния на размер частиц дисперсии.
При исследовании реологических свойств дисперсий
обнаружено, что полимерные дисперсии, синтезированные с использованием в
качестве неорганического носителя диоксид титана, обладают выраженной
тиксотропией.
При синтезе дисперсий с использованием акриловых
мономеров с большей длиной алифатического заместителя установлено, что
содержание диоксида титана в твердой фазе таких дисперсий не превышает 4%.
Полученные дисперсии по характеру течения являются ньютоновскими жидкостями.
Список использованной литературы
1.
Семчиков Ю.Д. Высокомолекулярные соединения: Учебник для вузов / Ю.Д. Семчиков
- Н.Новгород: Издательство Нижегородского государственного университета им.
Н.И. Лобачевского; М.: Издательский центр «Академия», 2003. - 368 с.
.
Шур А.М. Высокомолекулярные соединения: Учебник для ун-тов. - 3-е изд.,
перераб. и доп. - Высшая школа, 1981. - 656 с., ил.
.
Хаддаж М., Жавченков С.В., Грицкова И.А. Влияние на кинетические характеристики
эмульсионной полимеризации стирола способа получения эмульсии // Вестник МИТХТ,
т. 6, №4, 2011. - С. 97 - 101.
4.
Klein S.M., Manoharan V.N., Pine D.J., Lange F.F. Preparation of monodisperse
PMMA microspheres in nonpolar solvents by dispersion polymerization with a
macromonomeric stabilizer // Colloid Polym. Sci. - 2003. - Vol. 282. - P. 7-13.
.
Okubo M., Iwasaki Y., Yamamoto Y. Preparation of micron-size monodisperse
polymer microspheres having cationic groups // Colloid Polym. Sci. - 1992. -
Vol. 270. - P. 733-737.
.
Kim J.-W., Joe Y.-G., Suh K.-D. Poly(methyl methacrylate) hollow particles by
water-in-oil-in-water emulsion polymerization // Colloid Polym. Sci. - 1999. -
Vol. 277. - P. 252-256.
.
Okubo M., Ito A., Hashiba A. Production of submicron-sized multihollow polymer
particles having high transition temperatures by the stepwise alkali/acid
method // Colloid Polym. Sci. - 1996. - Vol. 274. - P. 428-432.
.
Sarobe J., Forcada J. Synthesis of core-shell type polystyrene monodisperse
particles with chloromethyl groups // Colloid Polym. Sci.
- 1996. - Vol. 274. - P.
8-13.
.
Грицкова И.А., Губин С.П., Левачёв С.М., Журавлёва П.Л. Синтез полистирольных
микросфер, содержащих на поверхности наночастицы оксида цинка // Вестник МИТХТ,
т. 6, №5, 2011. - С. 146 - 151.
.
Грицкова И.А., Гервальд А.Ю., Прокопов Н.И., Ширякина Ю.М., Серхачев Н.С.
Синтез полимерных микросфер, содержащих неорганические наночастицы // Вестник
МИТХТ, т. 6, №5, 2011. - С. 9 - 20.
11.
Morkos H., Özgür Ü. Zinc oxide fundamentals. Materials and
devise technology. - Weinheim: Wiley-VCH, 2009. 488 p.
.
Wang H., Wingett D., Engelhard M., Feris K., Reddy K.M., Turner P., Layne J.,
Hanley C., Bell J., Tenne D. Fluorescent dye encapsulated ZnO particles with
cell-specific toxicity for potential use in biomedical applications // J.
Matter Sci.: Matter Med. 2009. V.20. - P.
11-22.
.
Гусев А.И. Наноматериалы, наноструктуры, нанотехнологии. - М.: Физматлит, 2007.
416 с.
.
Серенко О.А., Музафанов А.М. Макромолекулярные наночастицы и полимерные
нанокомпозиты // Вестник МИТХТ, т. 6, №5, 2011. - С. 47 - 52.
15.
Deng Y., Wang L., Yang W., Fu S., Elassari A. Preparation of magnetic polymeric
particles via inverse microemulsion polymerization process // J. Magnetism
& Magnetic Materials. 2003. V. 257. P. 69-78.
.
Hertzog B., Mottl T., Yim D., Mathiowitz E. Scientific and clinical
applications of magnetic carriers. - NY: Plenum Press, 1997. P. 77-92.
.
Safarik I., Safarikova M. Magnetic techniques for the isolation and
purification of proteins and peptides // BioMagnetic Research and Technology.
2004. 2.: 7 http://www.biomagres.com/content/2/1/7
.
Zhang Y., Kohler N., Zhang M. Surface modification of superparamagnetic
magnetite nano-particles and their intracellular uptake // Biomaterials. 2002.
V.23. P. 1553-1561.
.
Hoffmann D., Landfester K., Antonietti M. Encapsulation of magnetite in polymer
particles via the miniemulsion polymerization process // Magnetohydrodynamics.
2001. V. 37. P. 217-222.
.
Zheng W., Gao F., Gu H. Magnetic polymer nanospheres with high and uniform
magnetite content //J. Magnetism & Materials. 2005. V. 288. P. 403-410.
.
Dormann J.L., Fiorani D., Tronc E. Magnetic relaxation in fine-particle systems
// Adw. Chem. Phys.
1997. V. 98. P.
283-494.
.
Чадаев П.Н., Грицкова И.А., Михайлов А.С., Сакварелидзе М.А. Полимерные
микросферы в качестве антистатических компонентов защитного слоя
светочувствительных материалов // Вестник МИТХТ, т. 5, №5, 2010. - С. 36 - 40.
.
Сакварелидзе М.А. Антифрикционные покрытия фильмовых материалов на основе
полистирольных микросфер / М.А. Сакварелидзе, С.М. Левачев // Мир техники кино.
- 2007. - №3. - С. 6-9.
24.
Omer M., Haider S., Park S-Y. A novel route for the preparation of thermally
sensitive core-shell magnetic nanoparticles // Polymer 52. - 2011. - P.91-97.
25.
Булатова Р.Р., Бакеева И.В. Нанокомпозитные гели // Вестник МИТХТ, т. 6, №1,
2011. - С.3 - 101.
26.
Ho K.М.,
Ying Li W., Him Wong C., Li P. Amphiphilic polymeric particles with core -
shell nanostructures: emulsion-based syntheses and potential applications //
Colloid Polym. Sci. - 2010. - Vol.
288. - P. 1503-1523.
.
Карякина М.И. Испытание лакокрасочных материалов и покрытий. - М.: Химия, 1988.
- 272 с.: ил.
.
Горловский И.А., Индейкин Е.А., Толмачев И.А. Лабораторный практикум по
пигментам и пигментированным лакокрасочным материалам: Учеб. пособие для вузов.
- Л.: Химия, 1990. - 240с.
.
Тагер А. А. Физикохимия полимеров: Учеб. пособие для ВУЗов / А. А. Тагер. - 2-е
изд. - М.: АН СССР, 1963. - 372 с.
30.
Hook J., Fitzwater S., Reffner J., Bors D. Paint hiding of TiO2-polymer
composites in latex paints // The Dow Chemical Company, Spring House Technical
Center, 727 Norristown Road, Spring House, Pennsylvania, USA, 19477-0904.
.
Wiley J. & Sons. Principles and applications of emulsion polymerization //
J. Wiley & Sons. / by Chorng -Shyan Chern.2008. 252
p.
.
Вредные вещества в промышленности: Органические вещества: Новые данные с 1974
по 1984 гг.: Справочник / под общ. ред. Э. Н. Лебиной, И. Д. Гадаскиной. - Л.:
Химия, 1985. - 464 с.
.
Беспамятнов, Г. П. Предельно-допустимые концентрации химических веществ в
окружающей среде: Справочник / Г. П. Беспамятнов, Ю. А. Кротов. Л.: Химия,
1985. - 528 с.
.
Токсичные, пожаро- и взрывоопасные свойства веществ, применяющихся в химической
и нефтехимической промышленности: Методические указания / Сост. Е.А. Фролова,
Е.Л. Белороссов. - Ярославль: ЯПИ, 1987. - 36 с.
.
Пожарная опасность веществ и материалов: Справочник / под общ. ред. И. В.
Рябова. - М.: Стройиздат, 1970, т.12.
.
Безопасность жизнедеятельности: Учеб. пособие / под ред. Белороссова Е. Л.
-Ярославль, ЯОУЭЗ, 2001. - 414 с.
37.
Охрана труда и защита окружающей среды в курсовых и дипломных работах студентов
химико-технологических специальностей: Учеб. пособие. - Ярославль.: ЯПИ, 1991