Энтропия
РОССИЙСКАЯ
ФЕДЕРАЦИЯ
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ
ФГБОУ ВПО
«ТЮМЕНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
ИНСТИТУТ
ДИСТАНЦИОННОГО ОБРАЗОВАНИЯ
СПЕЦИАЛЬНОСТЬ/НАПРАВЛЕНИЕ/МАГИСТРАТУРА
«Сервис»
Контрольная
работа
По
дисциплине: Химия
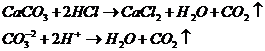
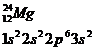
Относится к семейству р-элементов
Вал: II
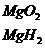
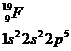
Относится к семейству р-элементов
Вал: I
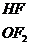
Молекула воды состоит из одного
атома кислорода, связанного ковалентной связью с двумя атомами водорода. Два
неспаренных р-электрона атома кислорода О очень реакционноспособны. Они всегда
готовы образовать химические связи с двумя s-электронами атомов водорода.
Поскольку атомы водорода друг от друга заметно отталкиваются, угол между
химическими связями (линиями, соединяющими ядра атомов) водород - кислород не
прямой (90°), а немного больше - 104,5°. Химические связи эти полярные:
кислород гораздо более электроотрицательный, чем водород, и подтягивает к себе
электронные облака, образующие химические связи. Вблизи атома кислорода
скапливается избыточный отрицательный заряд, а у атомов водорода -
положительный. Поэтому и вся молекула воды тоже попадает в отряд
"химических полярников" - веществ, молекулы которых представляют
собой электрические диполи.
Энтропия - мера хаотичности системы.
Процесс возможен, если идет с увеличением энтропии (один из критериев
возможности процесса).При переходе воды из жидкой в газовую фазу, энтропия
увеличивается, так как газ менее упорядочен, чем жидкость.
Энтропия алмаза больше, чем графита,
так как у алмаза более прочная структура. Следовательно, энтропия перехода
будет отрицательная.

- окислитель- восстановитель
Поверхностное натяжение - это
стремление вещества (жидкости или твердой фазы) уменьшить избыток своей
потенциальной энергии на границе раздела с другой фазой (поверхностную
энергию). Определяется как работа, затрачиваемая на создание единицы площади
поверхности раздела фаз (размерность Дж/м2).
Поверхностное натяжение жидкости
зависит:
) от природы жидкости, т. е. от сил
притяжения между молекулами данной жидкости;
) от температуры (с увеличением
температуры поверхностное натяжение уменьшается).
Запишем стандартные потенциалы
металлов(Fe)=-0,44B(Cr)=-0,74B
Стандартный потенциал хрома более
отрицательный, следовательно, в этой гальванопаре хром будет служить анодом. А
покрытие - анодное.
В кислой среде
(-) Cr | 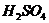 | Fe
(+)(-):
| Fe
(+)(-):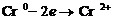 - окисление
- окисление
К(+):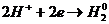 - восстановление
- восстановление
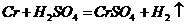
Во влажном воздухе
(-) Cr | 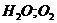 | Fe (+)
| Fe (+)
А: 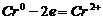 - окисление
- окисление
К: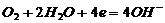 - восстановление
- восстановление
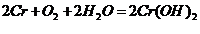
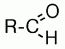
Альдегиды - это органические
вещества, молекулы которых содержат карбонильную группу, которая связана по
крайней мере с одним атомом водорода и углеводородным радикалом.
R-CH=O + H2
t,Ni → R-CH2-OH
первичный спирт
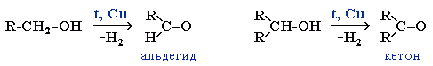
Присоединение воды:
│=O + H2O ↔ H -C - OH
(гидратная форма альдегида - формальдегида)
│
реакция медь гидрооксид
полимеризация
Реакции окисления
. Реакция серебряного зеркала -
качественная реакция на альдегидную группу:
R-CH=O +
Ag2O NH3→ R-COOH + 2 Ag↓
карбоновая кислота
. Окисление гидроксидом меди(II):
R-CH=O + 2Сu(OH)2
t → R-COOH + Cu2O +2H2O
голубой красный
Реакции замещения
С галогенами:
CH3-CH=O + Cl2 → Cl-CH2-CH=O + HCl
хлоруксусный
альдегид
O
│
Реакции полимеризации
CH2=O t,kat → (-CH2-O-)n
полиформальдегид
Реакции поликонденсации
H-CH=O + (n+1) C6H5-OH t,kat→ nH2O +
[-C6H3(OH)-CH2-C6H3(OH)-]n
фенолформальдегидная смола
Титр - масса растворённого вещества (в граммах),
содержащаяся в одном миллилитре (см³) раствора.
Дана молярная концентрация эквивалента (в
нормалях)
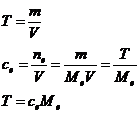 , Т=0,1*36,5=3,65(г/мл)
, Т=0,1*36,5=3,65(г/мл)