Свойства оксида железа
ВВЕДЕНИЕ
Данная работа посвящена изучению свойств оксида железа (III) Fe2O3,
также известного как минералы: гематит (α-Fe2O3),
лимонит (Fe2O3•H2O), входит в состав магнетита (FeO•Fe2O3).
Тема курсовой работы представляет практический и теоретический интерес.
Проект будет полезен предприятиям, синтезирующим вещество Fe2O3
в промышленных масштабах.
Также проект полезен как сборник информации о железе, некоторых его
оксидах, оксиде железа (III) в частности, и минералах, в состав которых он
входит.
Цели, выполнение которых необходимо достичь по окончании работы над
проектом: собрать наиболее полную информацию об оксиде железа (III), изучить
его свойства и способы синтеза.
Задачи проекта:
.Собрать полноценную и актуальную информацию по теме.
.Изучить свойства железа и его оксида (III) Fe2O3,
на основе чего узнать о применении этих веществ.
.Рассмотреть все возможные способы синтеза и выделить наиболее выгодный
из них.
По окончании данного проекта следует сделать заключение по проделанной
работе, указать какие задачи были выполнены, а какие нет.
1. ЖЕЛЕЗО
Железо было известно еще до нашей эры. Люди древнего Египта и Северной
Америки пользовались предметами, сделанными из метеоритного железа. В те
времена железо было самым распространенным материалом после бронзы.
Считается, что народы Кавказа и Туркестана первыми получили железо из
минералов. Позже железо распространилось в Вавилон, Египет, Грецию и Рим.
Железо, полученное примитивным способом (который состоял в нагревании железной
руды с древесным углем в ямах или печах из глины), было загрязнено шлаком и
очищалось долгой ковкой.
На древнем Востоке при выплавке железа использовались печи, оснащенные
мехами для подачи воздуха. В XV в.
за счет увеличения потока подаваемого воздуха была увеличена температура выплавки.
Благодаря этому удалось получить чугун, который был очень хрупок и ломался от
удара молотка. Позже было получено ковкое железо путем нагревания чугуна с
древесным углем в горне в токе воздуха.
Огромным скачком в металлургии железа является замена древесного угля
коксом - восстановителем, источником углерода и одновременно горючим
материалом. Уже в XIX в. были
разработаны технологические процессы получения стали. [26]
1.1 Нахождение в природе
В природе железо практически не встречается в свободном состоянии. Обычно
оно входит в состав минералов в виде различных соединений. Его содержание в
земной коре составляет 4,7 вес. %.
Наиболее типичными минералами железа являются: Сидерит, Лимонит, Гематит,
Магнетит. Также существуют и другие минералы: Вюстит, Пирит, Марказит,
Лёллингит, Миспикель, Мелантерит, Вивианит и пр.
Залежи полезных ископаемых, содержащих минералы железа, находятся в
разных странах: России, Швеции, Норвегии, Франции, Греции, Италии, Кубе, Турции
и пр. [1]
Процентное содержание железа в минералах колеблется от 25 до 70%. Руды,
содержащие менее 45% железа, относятся к бедным и в промышленности не
используются. Обогащают руды магнитным способом. Гематит или лимонит превращают
в магнетит термической обработкой и пропускают через магнитное поле для
отделения от пустой природы.
Железо входит в состав гемоглобина - компонента эритроцитов крови живых
организмов. У некоторых видов вместо железа в молекуле гемоглобина присутствует
медь. [2]
1.2 Получение и применение
Чистое мало окисляемое металлическое железо может быть получено
восстановлением оксида железа (III) Fe2O3 водородом при нагревании:
Fe2O3+3H2=2Fe+3H2O
Восстанавливая Fe2O3 водородом при 278-340°С, получают
пирофорное железо, при 550-650°С - железо, свыше 700°С - спекшуюся массу
губчатого металлического железа.
Чисто железо можно получить путем термического разложения пентакарбонила
железа Fe(CO)5 без доступа кислорода и при температуре свыше
140°С, а также электролизом водного раствора FeCl2·4H2O с добавлением NH4Cl при 30°С. [1]
Загрязненное металлическое железо может быть получено алюмо- или
кремнетермическим восстановлением оксида железа (III) Fe2O3 и оксидов железа (II, III) Fe3O4.
Fe2O3+2Al=2Fe+Al2O3
Fe3O4+8Al=9Fe+4Al2O3 [3]
Для получения различных ферросплавов (феррохрома, ферровольфрама,
ферромолибдена и др.) применяются алюмо- или кремнетермическое восстановление
смеси Fe2O3 с оксидами соответствующих металлов (Cr2O3,
WO3, MoO3 и т.д.). При кремнетермическом восстановлении
используют элементарный кремний или ферросилиций. [4]
Для получения сверхчистого железа (10-6% примесей) используют
метод зонной плавки.
Для получения чугуна или сырого железа (сплавы железа с углеродом)
используются минералы, не содержащие серу, мышьяк и фосфор: гематит, лимонит,
магнетит, сидерит. [5]
Получение чугуна путем восстановления железных руд осуществляется в
доменных печах. Процесс превращения чугуна (сырого железа) в ковкое железо
проходит путем окисления и частичного удаления примесей (S, P, As, Si и пр.), т.е. путем аффинажа по
процессу Пудделя, Бессемера, Томаса или Мартена.
Доменная печь имеет форму двух усеченных конусов, которые соединены
основаниями. Ее высота - 65 м, диаметр 5-11м. Рабочий объем печи - 200-2000 м3,
производительность - около 2000 т чугуна в сутки. Верхний конус печи называется
шахтой. Он сделан из огнеупорных кирпичей и имеет в верхней части так
называемый «колошник» - автоматическое устройство для удаления доменных газов.
Нижний конус сделан из огнеупорного силикатного кирпича. В его нижней части
находится горн, имеющий цилиндрическую форму. Сама печь поддерживается
металлическими конструкциями, так как имеет достаточной большой вес.
Процесс выплавки чугуна проходит так: сверху в доменную печь загружают
измельченную железную руду, которую послойно перемешивают с коксом; снизу под
давлением поступает предварительно нагретый воздух, в котором сгорает кокс.
Образующийся при горении оксид углерода восстанавливает железо из его оксидов:
CO+Fe2O3=2Fe+3CO2↑
Так как реакция обратима, в соответствии с принципом Ле-Шателье,
равновесие смещается влево при повышенной температуре. Поэтому реакция
осуществляется, в основном, в верхней части печи, где температура ниже. Часть Fe2O3 восстанавливается только до FeO:
Fe2O3+CO=2FeO+CO2↑
В нижней части печи, где температура очень высокая, восстановителем
является непосредственно углерод:
FeO+C=Fe+CO
Вследствие очень высокой температуры в нижней части печи железо плавится
и стекается вниз. Пространство, освобожденное в связи с этим, заполняют сверху
новыми слоями руды и кокса. [8]
Железо и его сплавы активно применяются во всех отраслях промышленности в
связи с его возможностью сохранять механические и физико-химические свойства
при температурах до 900 °C.
Сплавы железа бывают нескольких типов: магнитные, немагнитные, кислотостойкие,
твердые, нержавеющие, жаропрочные и др.
Стали используются в производстве электровозов, вагонов, железно-дорожных
рельсов, тракторов, буровых установок, подъемных кранов и применяются во многих
других отраслях. [12]
Помимо стали и чугуна известны сплавы, содержащие 4-6,5% железа, такие
как латунь и бронза. В них железо служит добавкой для модификации прочности,
пластичности, твердости, ковкости, скорости старения и др. свойств.
Железо и его сплавы для современной техники имеют огромное значение.
Расход железа превышает 100 млн. тонн в год во всем мире. [17]
.3 Физические свойства и химические свойства
Чистое железо в компактном состоянии представляет собой серебристо-серый
металл с синеватым отливом, имеющий плотность 7,867 г/см3, твердость
4-5 по шкале Мооса, т. пл. 1536°C и т.
кип. 3250°C. Железа существует в виде четырех
аллотропных модификаций, а именно: α-Fe, устойчивое до 768°C, β-Fe, устойчивое в интервале 768-906°C, γ-Fe,
устойчивое в интервале 906-1401°C, и δ-Fe, устойчивое в интервале 1401-1536°С.
Модификация α, β, δ имеют кубическую
объёмноцентрированную кристаллическую структуру, а модификация γ-гранецентрированную кубическую
структуру решетки. Модификация α и δ - ферромагнитны, а β и γ - диамагнитны. Ферромагнетизм
исчезает, когда железо нагрето до точки Кюри 768°C. [3]
В тонко измельченном состоянии металлическое железо обладает пирофорными
свойствами и образуется в результате перегонки амальгамы железа или
восстановления Fe2O3 водородом примерно при 270°.
Горячее пирофорное железо самопроизвольно загорается на воздухе,
поскольку, будучи тонкоизмельченным и имея водород включения, энергично
взаимодействует с кислородом воздуха. [14]
Известно очень большое число сплавов (чугуны, стали и др.), образуемых
железом с различными металлами (Со, Ni, Мn, Сr, Мо,
W, V, Nb, Zr, Sb, Ti, Sn, Pb, Al, Be, Mg, Zn и Cu), а также с неметаллами -
углеродом, кремнием, азотом, фосфором, серой, водородом.
Было замечено, что железо в легированных сталях образует твердые
растворы, эвтектические твердые сплавы и интерметаллические соединения с
многочисленными элементами. Примеры интерметаллических соединений: Fe3Mo2,
Fe5Nb3, FeCr, FeZn7, Fe5Zn21, Fe2Sn, FeSn, FeSn2, Fe2W, Fe3W2, Fe3Zr2, Fe3Ti, FeAl3, Fe2N, Fe4N, Fe3P, Fe3C, Fe2C, Fe3Si2, FeSi, FeSi2 и Fe2Si.
Основным легирующим элементом железа является углерод. Введенный в
относительно небольших количествах углерод существенно изменяет характер и
свойства железа. Уже говорилось о том, что сплавы железа с другими элементами,
содержащие 0-1,7% углерода, относятся к сталям, а содержащие 1,7-6,7%
углерода,- к чугунам. Углерод может находиться в железе в виде графита
(элементный углерод) или в форме цементита.
Системы железо - углерод с содержанием углерода более 6,67% не
рассматриваются, поскольку в технике используются только сплавы, содержащие
примерно до 5% углерода. Углерод способствует увеличению прочности, твердости,
сопротивления и уменьшению пластичности. [16]
Механические свойства железа зависят от степени его чистоты. В чистом
состоянии железо достаточно мягко, ковко, тягуче, вязко, оно хорошо проводит
тепло и электричество. При загрязнении железа различными неметаллами или
металлами механические свойства его в значительной степени меняются.
В компактном состоянии чистое железо устойчиво в сухом воздухе и ржавеет
во влажном воздухе, превращаясь в Fe2O3 · n Н2O (где
n имеет значение, близкое к единице) -
ржавчину; последняя образует пористую, рыхлую пленку, которая не предохраняет
железо от действия кислорода.

Когда загрязненное железо соприкасается с влагой и двуокисью углерода из
атмосферы, на поверхности металла образуются гальванические пары, в которых
железо, являясь отрицательным элементом, разрушается. Из-за электрохимической
коррозии поверхность загрязненного железа во влажном воздухе за короткое время
покрывается ржавчиной. Ионы Fe2+ с анионами ОН- (из воды)
или СО32- (образовавшимися при растворении СO2 в воде) образуют Fe(OH)2
или FeCO3, которые в водной среде и в присутствии кислорода
превращаются в Fe(OH)3 (или в Fe2O3·3H2O). [19]
Для предохранения железа от действия коррозионных агентов его покрывают
слоем масляной краски, эмали или другого металла: Zn (цинкование), Sn
(лужение), Сr (хромирование), Ni (никелирование), Cd (кадмирование), РЬ (свинцевание) -
либо проводят поверхностное окисление расплавленным NaNO3 или KNO3.
Пары воды разлагаются нагретым докрасна железом выше 700° по обратимому
уравнению:
Fe+4H2O=Fe3O4+4H2↑
При комнатной температуре железо растворяет примерно 0,005% водорода. При
этом образуется гидрид включения FeH,
который способствует увеличению твердости железа:
Fe+4H2O=2FeH
Один грамм железа растворяет при 1530°C 0,272 см3 водорода, при 1550°-0,279 см3
водорода и при 1650°-0,310 см3 водорода.
Насыщенное водородом железо при нагревании на воздухе до 900° теряет
значительную часть этого газа.
При обычной температуре сухой кислород не взаимодействует с железом. При
нагревании полированной железной пластинки в кислороде выше 150° наблюдается
потемнение ее поверхности, а при нагревании до белого каления образуется магнетит:
Fe+2O2=Fe3O4
При 1900° в присутствии кислорода железо полностью превращается в оксиды.
При ≈ 900° растворимость кислорода в α-Fe равна 0,18%, а в β-Fe и γ-Fe она
больше. Железо с небольшим содержанием кислорода образует твердые и хрупкие
сплавы.
При нагревании железо взаимодействует с газообразным хлором, превращаясь
в Fe2Cl6, но не вступает в реакцию с жидким хлором. При действии
паров брома или йода на порошкообразное кристаллическое железо получают Fe3Br8 (или 2FeBr3 · FeBr2) и Fe3I8 (или 2FeI3·FeI2):
Fe+3Cl2=Fe2Cl6
Fe+4Br2=Fe3Br8
Fe+3Br2=Fe2Br6
Тонко измельченное железо взаимодействует при нагревании с серой, образуя
сульфиды FeS, FeS2:
Fe+S (ромбич.) = FeS Fe+2S (ромбич.) = FeS2
Сера плохо растворима в железе, но сульфид железа FeS (из сплавов системы железо - сера)
образует с железом эвтектику, которая содержит 30% серы, плавится при 985°,
обладает ломкостью при красном калении и ухудшает качество железа (чугуна или
стали).
При нагревании железного порошка в токе аммиака образуются нитриды Fe2N, Fe4N:
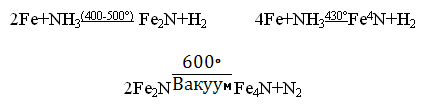
Фосфор, мышьяк и кремний образуют с железом при нагревании
интерметаллические соединения, например Fe3P, Fe2P,FeP, Fe3As2, Fe2As, Fe3As4, Fe3Si2, FeSi, FeSi2, Fe2Si.
Поскольку нормальный потенциал системы Fe/Fe2+ равен -0,44 в, железо относится к
легко окисляемым металлам. Под действием разбавленных неорганических кислот (НСl, H2SO4 и др.) оно превращается в
соответствующие соли железа (II) с
выделением водорода:
Fe+2HCl - FeCl2 +H2 Fe + H2SO4
= FeSO4 + H2
Разбавленная азотная кислота, взятая в избытке, взаимодействует с железом
по уравнению:
4Fe+10HNO3= 4Fe(NO3)2+NH4NO3+3H2O
Концентрированные кислоты, такие, как HNO3 и H2SO4, взаимодействуют с железом при нагревании по
уравнениям:
Fe + 4HNO3 = Fe(NO3)3 + NO +
2H2O
2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O
Нормальный потенциал системы Fe/Fe3+ равен -0,036 в. [11]
Под действием концентрированных кислот HNO3, H2SO4, Н2СгO4 железо становится пассивным благодаря образованию плотной
защитной пленки на поверхности металла, меняющей значение электрохимического
потенциала.
Железо подвергается действию концентрированных растворов щелочей.
Разбавленные растворы щелочей действуют на железо только в присутствии двуокиси
углерода.
Железо вытесняет металлы Bi, Sb, Pb, Sn, Cu, Ag, Hg, и Au из растворов их солей. [12]
С физиологической точки зрения железо имеет особое значение для организма
человека и животных, поскольку является катализатором процесса дыхания. Как уже
упоминалось, железо входит в состав молекулы гемоглобина. Молекула гемоглобина
состоит из интерциклического соединения гема, которое содержит двухвалентное
железо, и белка глобина. В легких человека гемоглобин присоединяет кислород,
превращаясь в оксигемоглобин, который разносится кровью, снабжая кислородом все
клетки организма. [22]
2. МИНЕРАЛЫ
Магнетит, Fe3O4, содержит до 72% железа и
представляет собой черные кубические кристаллы со слабым металлическим блеском,
плотностью 4,9-5,2 г/см3, твердостью 5,6-6 по шкале Мооса и
магнитными свойствами.
Гематит, α-Fe2O3 (от греческого слова
hematikos, что означает «кровавый»), содержит до 65% железа и представляет
собой красно-черные ромбоэдрические кристаллы с плотностью 5-5,3 г/см3,
твердостью 5,5-6 по шкале Мооса. α-Fe2O3 легко
восстанавливается при нагревании под действием Н2, С, СО, А1, Si и
др.
Лимонит (гетит), Fe2O3•H2O или HFeO2, содержит до
60% железа и представляет собой кристаллы, гранулы, оолиты или конкреции
черно-коричневого цвета. Плотность лимонита 3,3-4 г/см3, твердость
1-4 по шкале Мооса. Плотность гетита 4-4,4г/см3, твердость 4,5-5,5
по шкале Мооса. В отличие от других железосодержащих руд лимонит и гетит легче
всех восстанавливаются до металлического железа.
Сидерит, FeCO3, содержит примерно 35% железа, обладает
желтовато-белым (с серым или коричневым оттенком в случае загрязнения) цветом,
плотностью 3,9 г/см3 и твердостью 3,5-4,5 по шкале Мооса.
Пирит, FeS2, содержит 46,6% железа и встречается в виде
кубических кристаллов, желтых, как латунь, с металлическим блеском
(желтовато-коричневым оттенком), плотностью 4,9-5,2 г/см3,
твердостью 6-6,5 по шкале Мооса. Он содержит в небольшом количестве Со, Ni, As,
Sb и иногда Сu, Ag, Аu.
Марказит, FeS2, также содержит 46,6% железа, но встречается в
виде желтых, как латунь, бипирамидальных ромбических кристаллов с плотностью
4,6-4,9 г/см3 и твердостью 5-6 по шкале Мооса. При температуре 450°
он превращается в пирит.
Лёллингит, FeAs2, содержит 27,2% железа и встречается в виде
серебристо-белых бипирамидальных ромбических кристаллов с плотностью 7,0 - 7,40
г/см3 и твердостью 5 - 5,5 по шкале Мооса.
Миспикель, FeAsS, содержит 34,3% железа и встречается в виде белых
моноклинных призм с плотностью 5,6-6,2 г/см3 и твердостью 5,5-6 по
шкале Мооса.
Мелантерит, FeSO4•7H2O, реже встречается в природе
и представляет собой зеленые (или серые из-за примесей) моноклинные кристаллы,
обладающие стеклянным блеском, хрупкие, с плотностью 1,8-1,9 г/см3.
Вивианит, Fe3(PO4)2 •8Н2O, встречается в виде сине-серых или
зелено-серых моноклинных кристаллов с плотностью 2,95 г/см3 и
твердостью 1,5-2 по шкале Мооса.
Помимо описанных, известны и другие минералы, например: ильменит FeTiO3,
магномагнетит (Fe, Mg)[Fe2O4], фиброферрит FeSO4(OH)•4,5Н2O,
ярозит KFe3(SO4)2(OH)6, кокимбит Fe2(SO4)3•9Н2O, рёмерит Fe2+Fe3/2+(SO4)4•14H2O,
графтонит (Fe, Мn)3(РO4)2, скородит Fe3+AsO4•2Н2O,
штренгит FePO4•2H2O, фаялит Fe2SiO4,
альмандит Fe3Al2[SiO4]3, андрадит
Ca3Fe2[SiO4]3, гиперстен (Fe, Mg)2[Si2O6],
геденбергит (Са, Fe)[Si2O6], эгирин (Na, Fe) [Si2O6],
шамозит Fe42+Al[AlSi3O10(OH)6
•nН20, нонтронит (Fe3+, Al)2[Si4O10](OH)2•nH2O.
Кроме этих минералов, многие алюмосиликаты, какими являются глины,
загрязнены соединениями железа. [1, 6]
3. ОКСИДЫ ЖЕЛЕЗА
Оксид железа (II), FeO, получают окислением металлического
железа, термическим разложением FeC2O4·2H2O без доступа воздуха, восстановлением
оксида железа (III) Fe2O3 оксидом углерода при 500° или водородом при 700-800°,
прокаливанием (650-700° в отсутствие воздуха) смеси стехиометрически
необходимых количеств Fe2O3 и порошка металлического железа, нагреванием FeCO3 при 490-581°:
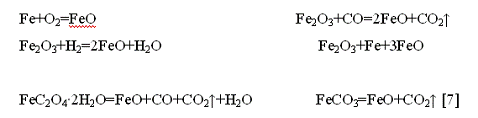
Соединение FeO представляет
собой диамагнитный черный неустойчивый кристаллический порошок (структура типа NaCl). Оно превращается в Fe2O3 при нагревании до 200-250° на воздухе, диспропорционирует на
Fe3O4 и металлическое железо при 570°, плавится примерно при 1360°;
трудно растворимо в воде и щелочах, легко растворяется в кислотах с
образованием солей железа (II);
восстанавливается до металлического железа под действием H2 или CO при
нагревании; разлагает при нагревании воду с образованием Fe2O3 и выделением H2:
FeO+H2O=Fe2O3+H2↑ [11, 13]
Оксид железа (II) образует с
многочисленными оксидами металлов соединения типа шпинелей Fe2+[Me23+O4] или перовскита Fe2+Me4+O3.
Оксид железа (III), Fe2O3, является самым устойчивым природным кислородсодержащим
соединением железа, которое встречается в форме минералов гематита или красного
железняка. [14]
Известны три модификации оксида железа (III), а именно: α-Fe2O3, γ-Fe2O3 и δ-Fe2O3. Модификация α-Fe2O3
(соответствующая
гематиту) парамагнитна и образуется окислением железа на воздухе при
температуре выше 200°, а также нагреванием δ-Fe2O3 в течение 3 часов при 110° или сжиганием пирофорного
железа на воздухе при комнатной температуре и давлении меньше 760 мм рт. ст.
Модификация γ-Fe2O3 ферромагнитна и образуется
окислением железа на воздухе при температуре ниже 200°, а также окислением Fe3O4 или нагреванием α-Fe2O3 при 300°. Модификация δ-Fe2O3 ферромагнитна и образуется окислением растворов солей
железа (II) в щелочах. [15]
Модификации оксида железа(III)
могут также быть получены прокаливанием гидроксида железа (III), Fe(OH)3 при 700°,
нитрата Fe(NO3)3•6Н2O при 600-800°, карбоната FeCO3 при 500° на воздухе, сульфата FeSO4 или пирита FeS2 на воздухе:
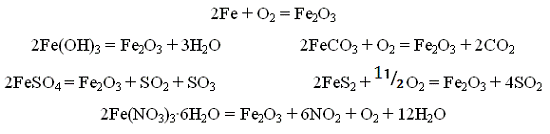
Нагревание порошкообразного железа или трихлорида железа в водном паре
также дает Fe2O3.
Соединение α-Fe2O3 представляет собой красный порошок с плотностью 5,24 г/см3,
который плавится примерно при 1550°,трудно растворим в воде и может быть восстановлен
до Fe3O4, FeO или металлического железа
водородом, углеродом, оксидом углерода, металлическим алюминием или элементным
кремнием. При восстановлении α-, γ-, δ-Fe2O3 водородом (280-340°) образуется пирофорное
металлическое железо, а при алюмо- или кремнетермическом восстановлении
модификаций α-, γ-, δ-Fe2O3 образуется загрязненное металлическое железо.
Растворимость α-, γ-, δ-Fe2O3 модификаций в кислотах зависит от температуры и
продолжительности прокаливания окиси перед растворением. Если оксид железа был
слегка прокален, он растворяется в кислотах.
Окись железа под названием железный сурик, охра, мумия, применяется как
пигмент приготовления для красок. [1]
Оксид железа(II, III), Fe3O4, со структурой шпинели Fe2+[Fe23+O4] встречается в природе в виде минерала магнетита.
Соединение Fe3O4
можно получить
прокаливанием других оксидов железа или восстановлением Fe2O3 (400-500°) водородом, насыщенным парами воды, или
оксидом углерода (800°).3O4
представляет собой ферромагнитные ломкие (твердость 5,6-6,5 по шкале Мооса)
черные кубические кристаллы с металлическим блеском; они трудно растворимы в
воде и кислотах, имеют т. пл. 1538° и разлагаются при 1787°. [18]
Оксид железа(II, III) устойчив
в сухом воздухе и служит для изготовления электродов, поскольку является
хорошим проводником электрического тока и устойчив к действию химических
реагентов. [12]
4. ОКСИД ЖЕЛЕЗА (III)
.1 Применение
Применяется как сырьё при выплавке чугуна в доменном процессе,
катализатор в производстве аммиака, компонент керамики, цветных цементов и
минеральных красок, при термитной сварке стальных конструкций, как носитель
аналоговой и цифровой информации (напр. звука и изображения) на магнитных
лентах (ферромагнитный γ-Fe2O3), как полирующее средство
(красный крокус) для стали и стекла.[1]
В пищевой промышленности используется в качестве пищевого красителя
(E172).
В ракетомоделизме применяется для получения катализированого карамельного
топлива, которое имеет скорость горения на 80% выше, чем обычное топливо.[23]
Является основным компонентом железного сурика (колькотара). [12]
.2 Колькотар
Колькотар - коричневая минеральная краска. Другие названия: парижская или
английская красная краска, caput mortuum vitrioli, крокус, железный сурик; в
алхимии - красный лев. [15]
По составу колькотар представляет более или менее чистую безводную окись
железа. Хотя безводная окись железа и встречается в природе в очень больших
количествах (красный железняк, железный блеск), но ценные сорта этой краски
вырабатываются искусственно или получаются как побочный продукт при добывании
нордгаузенской кислоты из железного купороса, а также при прокаливании основных
серножелезных солей, выделяющихся из раствора при приготовлении железного
купороса из купоросного камня. [27]
4.3 Получение и синтез
. Fe2O3 образуется при прокаливании на воздухе всех гидратов и
кислородных соединений железа, а также Fe(NO3)3 и FeSO4. Так, например, прокаливают в течение 2 час. на
полном пламени бунзеновской горелки Fe(OH)3, полученный по методу Г.
Гюттига и Г. Гарсайда.
Fe(OH)3 = Fe2O3 + 3H2O [1]
. По указанию Д. Н. Финкельштейна 100 г Fe(NO3)3 • 9H2O нагревают в большом фарфоровом тигле на электрической
плитке. Вначале соль спокойно плавится, образуя бурую жидкость, постепенно
испаряющуюся. При 121° жидкость начинает кипеть, выделяя постоянно кипящую
68%-ную HNO3.
Постепенно жидкость начинает загустевать и необходимо частое
перемешивание, чтобы избежать толчков и разбрызгивания. Начиная со 130°,
непрерывно перемешивают жидкость фарфоровым шпателем, причем она загустевает, образуя
пасту (без перемешивания жидкость внезапно затвердевает в сплошную массу). При
132° паста сразу рассыпается в порошок, продолжая выделять пары HNO3.
Не переставая перемешивать, продолжают нагревание до полного высушивания;
весь процесс занимает 20-25 мин. Сухую массу растирают, переносят в тигель и
прокаливают в муфеле при 600-700° в течение 8-10 час. При достаточной чистоте
исходного нитрата железа полученный продукт отвечает квалификации х. ч. Выход
95-98% теоретического, т. е. около 19 г. [9]
. Для приготовления чистого препарата к нагретому до кипения раствору
закисной соли железа прибавляют вычисленное количество горячего раствора
щавелевой кислоты, причем выпадает закисное щавелевокислое железо. Его
отфильтровывают, тщательно промывают водой, высушивают и прокаливают при
доступе воздуха, непрерывно перемешивая. Выход 90-93% теоретического.
Получаемый препарат содержит 99,79-99,96% Fe2O3. [8]
. В фарфоровый котелок емкостью 4 л, снабженный крышкой, помещают раствор
500 г Fe(NO3)3 • 9Н2О в 2 л воды. Через
трубку, проходящую до дна котелка, пропускают не слишком сильный ток NH3,
промытого щелочью и водой. Время от времени перемешивают жидкость газоотводящей
трубкой.
По окончании осаждения жидкости дают отстояться, раствор декантируют и
промывают осадок горячей водой до удаления NO3 в промывных водах.
Отмытый Fe(OH)3 просушивают в фарфоровых чашках, после чего
прокаливают в течение 5-6 час. при 550-600°. Выход 96 г (96-97%
теоретического). [10]
. При получении Fe2O3, служащего сырьем для приготовления Fe высокой
чистоты, исходный нитрат железа должен быть исключительно чист. Путем
многократной перекристаллизации Fe(NO3)3 • 9Н2О
Кливс и Томпсон получили препарат, содержащий всего 0,005% Si и менее 0,001%
других примесей. [14]
. По Брандту целесообразнее всего исходить из химически чистого железа.
Последнее растворяют в НСl,
раствор при нагревании обрабатывают сероводородом, фильтруют и в фильтрате
двухвалентное железо окисляют в трехвалентное кипячением с небольшим
количеством HNO3. Смесь дважды выпаривают с концентрированной HCl и, растворив остаток в избытке
разбавленной НСl, несколько раз
взбалтывают раствор с эфиром в большой делительной воронке.
Если исходный материал содержал Со, то содержимому воронки дают
отстояться, спускают через кран нижний (водный) слой и к оставшейся в воронке
эфирной вытяжке прибавляют часть по объему смеси, полученной встряхиванием НСl (уд. в. 1,104) с эфиром. Сильно
встряхивают, снова сливают нижний слой и операцию повторяют.
Выпаривание целесообразно проводить в плоской фарфоровой чашке.
После выпаривания остается хрупкая соляная масса, легко отделяющаяся от
чашки. Ее истирают в ступке и порциями по 40-50 г умеренно прокаливают в
платиновой чашке. Остаток несколько раз смешивают с сухим углекислым аммонием и
вновь прокаливают при слабом красном калении, часто перемешивая.
Эту операцию повторяют до приблизительно постоянного веса (точно
постоянный вес не может быть достигнут, так как незначительное количество Fe2O3
уносится парами (NH4)2СО3). [11]
железо металл оксид минерал
ЗАКЛЮЧЕНИЕ
Цели, поставленные в начале исследовательской работы, были полностью
выполнены:
) Собрана информация о железе, его оксидах и минералах:
Железо - ковкий, серебристо-белый металл с высокой реакционной
способностью. В соединения проявляет степени окисления +2, +3, +6. Имеет
оксиды: Fe+2O, Fe2+3O3, Fe3O4 (Fe+2O·Fe+32O3). Оксид железа (III) Fe2O3 помимо получения синтетическим путем, можно обнаружить в
залежах природных руд. Он входит в состав некоторых минералов таких как:
гематит, лимонит, магнетит.
) Изучены свойства Fe2O3 и сделаны выводы о его применении:
Вещество Fe2O3 используется для получения чистого мало окисляемого
железа путем восстановления водородом, а так же в электронных носителях
информации (вследствие магнитности), как полирующее средство (красный крокус)
для стали и стекла, в пищевой промышленности и является основным компонентом
колькотара (так как соединение является красящим).
) Изучены несколько способов синтеза вещества. Наибольший выход
продукта равняется 98% от теоретического. Добиться этого результата можно по методу
Д.Н. Финкельштейна, путем нагревания Fe(NO3)3 • 9H2O в
большом фарфоровом тигле на электрической плитке при постоянном помешивании.
СПИСОК ЛИТЕРАТУРЫ
1)Рипан Р. Неорганическая химия: В 2-х т./Р. Рипан, И.
Четяну; Перев. с рум. Д.Г. Батыра, Х.М. Харитона; Под ред. В.И. Спицына, И.Д.
Колли. - М.: Издательство «Мир» 1972. - 2 т.
)Кнунянц И.Л. Краткая химическая энциклопедия: В 5-ти т. /
Ред. кол. И.Л. Кнунянц (отв. ред.) и др. - М.: Издательство «Советская
Энциклопедия», 1967 - 5 т.
)Лидин, Р.А. Химические свойства неорганических веществ:
учеб. пособие для вузов / Р.А. Лидин, Молочко, Л.Л Андреева. Под ред. Р.А.
Лидина.- М.: Химия, 2000 - 480 с.
)Некрасов Б.В. Основы общей химии Т. I. изд. 3-е, испр. и
доп. Издательство «Химия», 1973 - 656 с.
)Реми Г. Курс неорганической химии в 2-х т. / Г. Реми; А.П.
Григорьева, А.Г. Рыков; Под ред. А.В. Новоселовой. - М.: Издательство
«Мир»,1966 - 2 т.
)Паффенгольц К.Н. Геологический словарь: в 2-х т./ Ред. ком.
К.Н. Паффенгольц (отв.ред.), Л.И. Боровиков, А.И. Жамайда, И.И. Краснов и
др.-М.: Издательство «Недра», 1978 - 2 т.
)Эфимов А.И. Свойства неорганических соединений. Справочник /
А.И. Ефимов и др. - Л.: Химия, 1983 - 392 с.
)Брауэр Г. Руководство по неорганическому синтезу: в 6 т.
Пер. с нем./ Под ред. Г Брауэр. - М.: Издательство «Мир», 1985 - 6 т.
)Карякин Ю.В. Чистые химические реактивы / Ю.В. Карякин, И.И.
Ангелов. - М.: Государственная научно-техническое издательство химической
литературы, 1955 - 585 с.
)Ключников Н.Г. Практикум по неорганическому синтезу. - М.:
Издательство «Просвещение» , 1979 - 271 с.
)Терентьева Е.А. Неорганические синтезы: В 2-х т. / Пер. с
англ. Е.А. Терентьевой, под ред. Д.И. Рябчикова, - М.: Издательство иностранной
литературы, 1951 - 2т.
)Глинка Н.Л. Общая химия: Учебное пособие для вузов. - 23-е
изд., испр./ Под ред. В.А. Робиновича. - Л.: Химия 1983-704 с.: ил.
)Захаров Л.Н. Начала техники лабораторных работ. - Л.: Химия,
1981 - 192 с.
)Спицын В.И. Неорганическая химия. Ч. I: Учебник - М.:
Издательство МГУ, 1991 - 480 с.: ил.
)Рабинович В.А. Краткий химический справочник. - Л.: Химия,
1977.
)Ахметов Н.С. Общая и неорганическая химия. - М.: Высшая
школа, 2004.
)Карапетянц М.Х., Дракин С.И. Общая и неорганическая химия. -
М.: Химия, 1981.
)Практикум по общей и неорганической химии / Под ред.
Воробьева А.А., Дракина С.И. - М.: Химия, 1984.
)Жарский И.М., Новиков Г.И. Физические методы исследования в
неорганической химии. - М.: Высшая школа, 1988.
)Краснов К.С. Молекулы и химическая связь. - М.: Высшая
школа, 1974.
)Коттон Ф., Уилкинсон Дж. Основы неорганической химии. - М.:
Издательство «Мир», 1979.
)Исидоров В.А. Экологическая химия. - СПб.: Химиздат, 2001.
)Коттон Ф., Уилкинсон Дж. Современная неорганическая химия.
Ч. 1 M.: Мир, 1969.
)Ливер Э. Электронная спектроскопия неорганических соединений,
М.: Мир, 1987, 2 т.
)Лидин Р.А. и др. Химические свойства неорганических веществ.
- 3-е изд., испр. - М.: Химия, 2000 - 480 с.
)Трифонов Д.Н., Трифонов В.Д. Как были открыты химические
элементы - М.: Просвещение, 1980.
)Химия: Справ. изд. / В. Шретер, К.-Х. Лаутеншлегер, Х.
Бибрак и др.: Пер. с нем. 2-е изд., стереотип. - М.: Химия, 2000.