Контроль качества лекарственных форм
ГБОУ ВПО«Саратовский государственный
медицинский университет им. В.И.Разумовского Минздрава России»
Кафедра фармацевтической химии
Заведующий кафедрой доцент Голиков
А.Г.
ОТЧЕТ (ДНЕВНИК)
производственной практики по
фармацевтической химии
Контроль качества лекарственных форм
Студентки Кузнецовой Лилии Павловны 6 курса группы 2
Место практики Аптека ФГБУ «СарНИИТО»Минздрава России
Г.Саратов, ул. Чернышевского, д. 148
Руководитель от аптеки Дедюкина Н.Г. заведующая-провизор
год
1.Знакомство с рабочим местом провизора аналитика
аптечный лекарственный
контроль
Провизору, назначенному на должность для выполнения контроля качества
лекарственных средств, изготовляемых в аптеках, необходимо владеть всеми видами
внутриаптечного контроля.
Руководителю аптеки и его заместителям следует обеспечить условия
выполнения всех видов контроля в соответствии с требованиями приказа №214
Провизору-аналитику, впервые назначенному на должность, необходимо пройти
курс стажировки в территориальной контрольно-аналитической лаборатории.
Результаты
контроля качества лекарственных средств регистрируются в журналах по
прилагаемым формам (Приложения Б
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100857>,
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100884>,
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100900>,
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100919>,
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100950> к
приказу№ 214). Все журналы должны быть прошнурованы, страницы в них
пронумерованы, заверены подписью руководителя и печатью аптеки. Срок хранения
журналов - один год.
Отчет
о работе по контролю качества лекарственных средств, изготовленных в аптеке,
составляется по итогам за год и направляется в территориальную
контрольно-аналитическую лабораторию (центр контроля качества лекарственных
средств) по прилагаемой форме (Приложение Ж
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100968> к
приказу № 214).
Для
проведения химического контроля качества лекарственных средств, изготовляемых в
аптеках, должно быть оборудовано специальное рабочее место, оснащенное типовым
набором оборудования, приборами и реактивами, а также обеспечено нормативными
документами, справочной литературой (Приложение А
<consultantplus://offline/main?base=LAW;n=16599;fld=134;dst=100148> к
приказу № 214).
Рабочие
места химиков - аналитиков в аптеках должны быть оборудованы в аналитическом
кабинете, размещенном в непосредственной близости от ассистентской, асептической
и помещения для приготовления внутриаптечных заготовок, концентратов и
полуфабрикатов.
В
аналитическом кабинете должны быть типовой аналитический стол (конструкции
ЦАНИИ), который отвечает современным требованиям организации рабочих мест,
удобен в эксплуатации, имеет красивый внешний вид, окрашен в светлые тона, что
способствует повышению работоспособности и снижению утомляемости химика -
аналитика.
На столе под стеклом или на специальной подставке целесообразно
разместить методики анализов концентратов и полуфабрикатов отдельных
лекарственных форм; таблицы расчетов количественных экспресс - анализов,
таблицы качественных анализов и т.д. Некоторые справочные материалы удобно
располагать в виде картотек.
В аналитическом кабинете должны быть: вытяжной шкаф для работы с
ядовитыми, летучими веществами и концентрированными кислотами, водопровод с
холодной и горячей водой; раковина со сливом в канализацию и подводка
технического тока.
Необходимой аппаратурой и инвентарем аналитические кабинеты должны
оснащаться согласно требованиям инструкции по контролю качества лекарств и
нормам технического и хозяйственного оснащения аптек.
Организация рабочих мест химиков - аналитиков должна отвечать следующим
требованиям:
. Стулья должны быть со спинкой, подъемно - поворотной конструкции с тем,
чтобы можно было обеспечить правильное соотношение высоты рабочей поверхности
стола и стула при допустимой разнице высот (дифференции) в 270-300 мм.
. Каждый предмет должен иметь свое строго определенное место.
. На рабочем месте не должно быть предметов, которые не требуются в
данной работе.
. Часто используемые предметы и материалы следует размещать в зоне
досягаемости с учетом удобств выполнения тех или иных операций.
. Рука химика - аналитика при выполнении работы должна совершать наиболее
удобные и менее утомительные движения.
Химик - аналитик должен соблюдать определенную последовательность при
выполнении отдельных видов работ в зависимости от конкретных условий
производственной деятельности данной аптеки.
Вместе с тем для большинства химиков - аналитиков целесообразно начинать
рабочий день с осуществления контроля за фармацевтической деятельностью,
санитарным состоянием аптеки и проверки обеспеченности своего рабочего места
всем необходимым.
Работу непосредственно по контролю удобнее начинать с проверки качества
дистиллированной воды. Затем следует проверить качество дистиллированной воды
на различных рабочих местах.
Химик - аналитик должен проверять качество и сроки хранения
дистиллированной воды, имеющейся в аптеке на различных рабочих местах, поэтому
все сборники и бюретки с дистиллированной водой должны быть пронумерованы.
В целях экономии времени регистрацию результатов анализов
дистиллированной воды следует производить в специальном журнале.
После проверки качества дистиллированной воды целесообразно проверить
качество заполнения бюреточной установки в ассистентской. Для этого
рекомендуется иметь подставку с набором склянок с надписями, соответствующими
числу и порядку различных растворов в бюретках. Растворы из бюреток набираются
в соответствующие склянки, после чего на своем рабочем месте химик - аналитик
проверяет их подлинность.
Регистрацию результатов проверки качества заполнения бюреточной установки
целесообразно также вести в отдельном журнале.
В дальнейшем химику - аналитику необходимо приступить к проведению
качественных анализов медикаментов, поступивших из отдела запасов (или
материальной) в ассистентскую комнату. Для этого все штанглазы следует также
пронумеровать. При этом дублированные штанглазы одного наименования
должны иметь дополнительную нумерацию. Например, штанглазы с глюкозой
нумеруются следующим образом: 101-01, 101-02, 101-03 и т.д.; c сахаром: 226-1,
226-2, 226-3 и т.д.
Для выполнения качественных реакций на различные медикаменты удобно
использовать планшеты с углублениями. Результаты качественных реакций
рекомендуется записывать в Журнал для регистрации результатов проверки
подлинности медикаментов (дефектура)
Затем химику - аналитику целесообразно приступить к проведению
химического анализа концентратов, полуфабрикатов и внутриаптечных заготовок.
Периодически, не реже одного раза в квартал, химик - аналитик проверяет
качество скоропортящихся и нестойких препаратов. В случае несоответствия
качества препарата требованиям фармакопеи химик - аналитик обязан сообщить об
этом заведующему аптекой (или его заместителю) для принятия необходимых мер
Перечень оснащения контрольно-аналитического кабинета (стола) включает:
испытательное оборудование: весы аналитические, ручные, технические,
гири, колориметр-нефелометр, микроскоп, термометры, ареометры, денситометры,
пикнометры и др.;
лабораторная посуда, применяемая для аналитических работ в аптеках
(бюретки, воронки, капельницы, цилиндры, колбы, пипетки, пробирки, тигли и
др.);
вспомогательные материалы, инструменты, приспособления (штативы, зажимы,
трубки, бумага фильтровальная, вата и др.);
титрованные растворы (йода, йодмонохлорида, бромата калия,
хлороводородной кислоты, гидроксида натрия, нитрита натрия, нитрата серебра и
др.);
индикаторы (22 наименования);
бумага индикаторная (РИФАН, универсальная, лакмусовая красная,
нейтральная, синяя и др.);
реактивы (156 наименований), готовятся только в КАнЛ;
растворители (ацетон, глицерин, спирт этиловый, хлороформ, эфир и др.).
) Вытяжной шкаф
) Раковина со сливом в канализацию и подводом холодной воды
) Аналитический стол
) Стол вспомогательный
) Стул
) Стол вспомогательный
) Шкаф для хранения запасов реактивов и посуды
) Реактивы
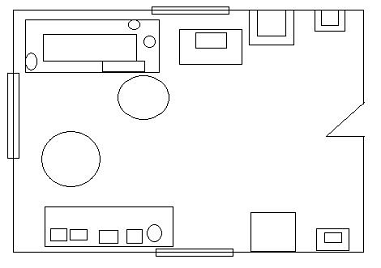
Оснащение аналитического стола
а) реактивы
б) рефрактометр
в) титровальная установка
г) вертушка
д) бюретка для отмеривания дист. Воды
е) фотоэлектроколариметр
ж) РН метр
з) поляриметр
и) аппарат для флуорисцентного анализа растворов
к) микроскоп
л) устройство для контроля растворов
м) весы аналитические
н) переговорное устройство
Обязанности провизора - аналитика. Приказы и инструкции, регламентирующие
работу провизора - аналитика.
В своей деятельности провизор-аналитик руководствуется:
нормативными документами по вопросам выполняемой работы;
методическими материалами, касающимися соответствующих вопросов;
Положением об аптечном учреждении;
правилами санитарного режима аптечных учреждений и трудового распорядка;
приказами и распоряжениями директора предприятия (непосредственного
руководителя);
настоящей должностной инструкцией.
Провизор-аналитик должен знать:
нормативные правовые акты и другие руководящие материалы вышестоящих
органов по вопросам фармации;
принципы оказания лекарственной помощи населению, а также
профессиональной деятельности по занимаемой должности;
организацию и экономику фармации;
- нормативные и методические материалы по анализу и контролю
качества лекарств, фармацевтическому порядку, санитарному режиму аптечных
учреждений (предприятий);
основы трудового законодательства;
правила и нормы охраны труда и пожарной безопасности.
ФУНКЦИИ
На провизора-аналитика возлагаются следующие функции:
Проведение контроля качества поступающих и изготовленных в аптекелекарственных
средств.
Контроль за соблюдением технологических правил и приемов
изготовлениялекарственных средств.
Соблюдение требований санитарного режима, правил и норм охраны труда.
Должностные обязанности
Для выполнения возложенных на него функций провизор-аналитик обязан:
Производить контроль поступающих и изготовленных в аптеке
лекарств,концентрированных растворов, внутриаптечных заготовок.
Применять все виды внутриаптечного контроля, выполняемые в условиях
аптеки, включая приемочный контроль, методы фармацевтического анализа
лекарственных средств и лекарственного растительного сырья.
Контролировать соблюдение технологических правил и приемов изготовления
лекарств.
Обеспечивать контроль за соблюдением фармацевтического порядка и
санитарного режима.
Соблюдать правила и нормы охраны труда и пожарной безопасности.
Взаимодействие аналитической лаборатории, кабинета (стола) с другими
службами учреждения
Территориальная (региональная) контрольно-аналитическая лаборатория или
центр по контролю качества лекарственных средств (далее "контрольно -
аналитическая лаборатория") является составной частью контрольно -
разрешительной системы обеспечения качества лекарственных средств, медицинской
техники и изделий медицинского назначения Министерства здравоохранения и медицинской
промышленности ПМР.
Контрольно - аналитическая лаборатория организуется с целью осуществления
государственного надзора за производственной деятельностью аптечных учреждений
и предприятий, а также государственного контроля за качеством лекарственных
средств:
изготовляемых аптеками всех типов, мелкорозничными аптечными
учреждениями, фармацевтическими фабриками (предприятиями), малыми и совместными
предприятиями территориального подчинения независимо от их организационно -
правового статуса и форм собственности;
качества лекарств, фармацевтическому порядку, санитарному режиму аптечных
учреждений (предприятий);
основы трудового законодательства;
правила и нормы охраны труда и пожарной безопасности.
Санитарные требования к помещениям и оборудованию аптек
Помещения аптек следует оборудовать, отделывать и содержать в
соответствии с правилами санитарного режим в чистоте и надлежащем порядке.
Перед входами в аптеку должны быть приспособления для очистки обуви от грязи.
Очистка самих приспособлений должна проводиться по мере необходимости, но не
реже 1 раза в день. Рабочие места персонала аптеки в зале обслуживания
населения должны быть оснащены устройствами, предохраняющими работников от
прямой капельной инфекции. Оконные фрамуги иди форточки, используемые для проветривания
помещений, защищаются съемными металлическими или пластмассовыми сетками с
размерами ячейки не более 2 х 2 мм. В летний период, при необходимости, окна и
витрины, расположенные на солнечной стороне, должны быть обеспечены
солнцезащитными устройствами, которые располагаются между рамами или с внешней
стороны окон. Материалы, используемые при строительстве аптек, должны
обеспечивать непроницаемость для грызунов, защиту помещений от проникновения
животных и насекомых. Не допускается использование гипсокартонных полых
перегородок. Все строительные материалы должны иметь гигиенические сертификаты.
Поверхности стен и потолков производственных помещений должны быть гладкими,
без нарушения целостности покрытия, допускающими влажную уборку с применением
дезсредств. Места примыкания стен к потолку и полу не должны иметь углублений,
выступов и карнизов. Материалы покрытия помещений должны быть антистатическими
и иметь гигиенические сертификаты (водостойкие краски, эмали или кафельные
глазурованные плитки светлых тонов). Полы покрываются неглазурованными
керамическими плитками, линолиуюм или релином с обязательной сваркой швов.
Помещения аптек должны иметь как естественное, так и искусственное
освещение.Общее искусственное освещение должно быть предусмотрено во всех
помещениях, кроме того, для отдельных рабочих мест устанавливается местное
освещение. Искусственное освещение осуществляется люминисцентными лампами и
лампами накаливания. Системы отопления и вентиляции должны выполняться по
действующим СНиПам. В помещениях хранения должен проводиться контроль за
параметрами микроклимата (температура, влажность, воздухообмен).Технологическое
оборудование, используемое в аптеках, должно быть зарегистрировано в Минздраве
России, разрешено к применению в установленном порядке и иметь сертификат
соответствия.Установка оборудования должна производиться на достаточном
расстоянии от стен, чтобы иметь доступ для очистки, дезинфекции и ремонта (как
правило, путем замены составных частей). Оборудование не должно загораживать естественный
источник света или загромождать проходы. Не допускается размещение в конкретных
производственных помещениях машин, аппаратов и др., не имеющих отношения к
технологическому процессу данного производственного помещения.В
производственных помещениях не допускается вешать занавески, расстилать ковры,
разводить цветы, вывешивать стенгазеты, плакаты и т.п. Для этого могут быть
использованы коридоры, комнаты отдыха персонала аптек, кабинеты.Информационные
стенды и таблицы, необходимые для работы в производственных помещениях, должны
изготовляться из материалов, допускающих влажную уборку и
дезинфекцию.Декоративное оформление непроизводственных помещений, в том числе
озеленение, допускается при условии обеспечения за ними необходимого ухода
(очистка от пыли, мытье и т.д.) по мере необходимости, но не реже 1 раза в
неделю.В моечной комнате должны быть выделены и промаркированы раковины (ванны)
для мытья посуды, предназначенной для приготовления: инъекционных растворов и
глазных капель, внутренних лекарственных форм, наружных лекарственных форм.
Запрещается пользоваться этими раковинами для мытья рук.Для мытья рук персонала
в шлюзах асептического блока и в заготовочной, ассистентской, моечной, туалете
должны быть установлены раковины (рукомойники), которые целесообразно
оборудовать педальными кранами или кранами с локтевыми приводами. Рядом
устанавливают емкости с дезрастворами, воздушные электросушилки. Запрещается
пользоваться раковинами в производственных помещениях лицам, не занятым
изготовлением и фасовкой лекарственных средств.
Санитарные требования к помещениям и оборудованию асептического блока
Помещения асептического блока должны размещаться в изолированном отсеке и
исключать перекрещивание "чистых" и "грязных" потоков.
Асептический блок должен иметь отдельный вход или отделяться от других
помещений производства шлюзами.Перед входом в асептический блок должны лежать
резиновые коврики или коврики из пористого материала, смоченные
дезинфицирующими средствами.В шлюзе должны быть предусмотрены: скамья для
переобувания с ячейками для спецобуви, шкаф для халата и биксов с комплектами
стерильной одежды; раковина (кран с локтевым приводом), воздушная
электросушилка и зеркало; гигиенический набор для обработки рук; инструкции о
порядке переодевания и обработке рук, правила поведения в асептическом блоке
(Приложение 5, 6).В ассистентской-асептической не допускается подводка воды и
канализации. Трубопроводы для воды очищенной следует прокладывать таким
образом, чтобы можно было легко проводить уборку.Для защиты стен от повреждений
при транспортировке материалов или продукции (тележки или др.) необходимо
предусмотреть специальные уголки или другие приспособления.Для исключения
поступления воздуха из коридоров и производственных помещений в асептический
блок в последнем необходимо предусмотреть приточно-вытяжную вентиляцию, при
которой движение воздушных потоков должно быть направлено из асептического
блока в прилегающие к нему помещения, с преобладанием притока воздуха над
вытяжкой.Рекомендуется с помощью специального оборудования создание
горизонтальных или вертикальных ламинарных потоков чистого воздуха во всем
помещении или в отдельных локальных зонах для защиты наиболее ответственных
участков или операций (чистые камеры). Чистые камеры или столы с ламинарным потоком
воздуха должны иметь рабочие поверхности и колпак из гладкого прочного
материала. Скорость ламинарного потока - в пределах 0,3-0,6 мс(-1) при
регулярном контроле стерильности воздуха не реже 1 раза в месяц.Для дезинфекции
воздуха и различных поверхностей в асептических помещениях устанавливают
бактерицидные лампы (стационарные и передвижные облучатели) с открытыми или
экранированными лампами. Количество и мощность бактерицидных ламп должны
подбираться из расчета не менее 2 - 2,5 вт мощности неэкранированного
излучателя на 1 м3 объема помещения. При экранированных бактерицидных лампах 1
Вт на 1 м3. Настенные бактерицидные облучатели ОБН-150 устанавливают из расчета
1 облучатель на 30 м3 помещения; потолочные ОБП-300 - из расчета 1 на 60 м3;
передвижной ОБП-450 с открытыми лампами используют для быстрого обеззараживания
воздуха в помещениях объемом до 100 м3. Оптимальный эффект наблюдается на
расстоянии 5 м от облучаемого объекта.
Санитарно-гигиенические требования к персоналу аптек
Работники аптеки, занимающиеся изготовлением, контролем, расфасовкой
лекарственных средств и обработкой аптечной посуды, а также соприкасающиеся с
готовой продукцией, при поступлении на работу проходят медицинское
обследование, а в дальнейшем профилактический осмотр в соответствии с
действующими приказами МЗ РФ. Результаты осмотров заносятся в санитарную
книжку.Каждый сотрудник должен оповещать руководящий персонал о любых
отклонениях в состоянии здоровья. Сотрудники с инфекционными заболеваниями,
повреждениями кожных покровов к работе не допускаются. Выявленные больные
направляются на лечение и санацию. Допуск к работе проводится только при
наличии справки лечпрофучреждения о выздоровлении. Персонал обязан выполнять
правила личной гигиены и производственной санитарии, носить технологическую
одежду, соответствующую выполняемым операциям.При входе в аптеку персонал
обязан снять верхнюю одежду и обувь в гардеробной, вымыть и продезинфицировать
руки, надеть санитарную одежду и санитарную обувь. Перед посещением туалета
обязательно снимать халат. Запрещается выходить за пределы аптеки в санитарной
одежде и обуви. В периоды распространения острых респираторных заболеваний
сотрудники аптек должны носить на лице марлевые повязки. Санитарная одежда и
санитарная обувь выдается работникам аптеки в соответствии с действующими
нормами с учетом выполняемых производственных операций. Смена санитарной одежды
должна производиться не реже 2 раз в неделю, полотенец для личного пользования
- ежедневно. Комплект специальной одежды для персонала, работающего в
асептических условиях, должен быть стерильным перед началом работы.
Целесообразно предусмотреть в санитарной одежде персонала отличительные знаки,
например, спецодежду или ее детали другого цвета, кроме белого, чтобы легче
распознать нарушения порядка перемещения персонала в асептической зоне, между
помещениями или за пределами асептического блока, в других производственных
зонах. Производственный персонал должен регулярно принимать душ, тщательно
следить за чистотой рук, коротко стричь ногти, не покрывать их лаком.
В помещениях хранения на всех штангласах с лекарственными средствами
должны быть указаны: номер серии организации-изготовителя, номер анализа
контрольно-аналитической лаборатории (центра контроля качества лекарственных
средств), срок годности, дата заполнения и подпись заполнившего штанглас. На
штангласах с лекарственными средствами, содержащими сердечные гликозиды, должно
быть указано количество единиц действия в одном грамме лекарственного
растительного сырья или в одном миллилитре лекарственного средства.
В ассистентских комнатах на всех штангласах с лекарственными веществами
должны быть указаны: дата заполнения, подпись заполнившего штанглас и
проверившего подлинность лекарственного вещества. На штангласах с ядовитыми и
сильнодействующими лекарственными веществами должны быть указаны высшие разовые
и суточные дозы, а на штангласах с лекарственными веществами, предназначенными
для изготовления стерильных лекарственных форм, должна быть предупредительная
надпись "Для стерильных лекарственных форм".
Штангласы с растворами, настойками и жидкими полуфабрикатами должны быть
обеспечены нормальными каплемерами или пипетками. Число капель в определенном
объеме должно быть установлено взвешиванием и обозначено на штангласе.
Заполнение штангласа, бюретки в бюреточной установке, штангласа с
нормальным каплемером или пипеткой должно проводиться только после полного
использования лекарственного средства и соответствующей обработки штангласа.
Номенклатура концентратов, полуфабрикатов и внутриаптечной заготовки
лекарственных средств, изготовляемых в аптеках, должна утверждаться
территориальной контрольно-аналитической лабораторией и доводиться до сведения
всех аптек соответствующей территории. В данный перечень могут включаться
только прописи, содержащие совместимые лекарственные вещества, на которые
имеются методики анализа для химического контроля
.Анализ воды очищенной и воды для инъекций
Согласно приказу № 214 вода очищенная ежедневно из каждого баллона или на
каждом рабочем месте подвергается качественному контролю на отсутствие
хлоридов, сульфатов,кальция.
Вода очищенная для приготовления растворов для инъекций, глазных капель и
лекарственных форм для новорожденных, кроме этих примесей проверяются на
отсутствие восстанавливающих веществ, аммиака и углекислоты.
ВОССТАНАВЛИВАЮЩИЕ ВЕЩЕСТВА. 100 мл. воды доводят до кипения, прибавляют 1
мл. 0,01 Н раствора калия перманганата и 2 мл. разведенной серной кислоты,
кипятят 10 минут, розовая окраска должна сохранится.
ДИОКСИД УГЛЕРОДА. При взбалтывании с равным количеством известковой воды
в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в
течение часа.
АММИАК. К 10 мл. воды прибавляют 0,15 мл. реактива Несслера, перемешивают
и через 5 минут сравнивают с эталоном, состоящим из 0,0002% раствора аммиака и
такого же количества реактива. Окраска используемого образцане должна превышать
эталон.
ХЛОРИДЫ. К 10 мл. воды прибавляют 0,5 мл. раствора азотной кислоты,
прибавляют 0,5 мл. раствора серебра нитрата. В растворе не должно быть
изменений.
СУЛЬФАТЫ. К 10 мл воды прибавляют 0,5 мл. разведенной хлористоводородной
кислоты, прибавляют 1 мл. раствора хлорида бария. В растворе не должно быть
изменений.
СОЛИ КАЛЬЦИЯ. К 10 мл воды прибавляют 1 мл раствора хлорида аммония и 1
мл. раствора аммиака. Раствор делят на две равные части, к одной из них
прибавляют 1 мл раствора оксалата аммония. Между растворами не должно быть
заметных различий
Полный химический анализ воды очищенной и воды для инъекций по ВФС
производятся ежеквартально в центре по контролю качества лекарственных средств.
Кроме химического анализа, вода очищенная и вода для инъекций
подвергается бактериологическому контролю (не реже 2-х раз в квартал) и
контролю на отсутствие пирогенных веществ (ежеквартально).
.Анализ лекарств, изготавливаемых в аптеках по рецептам. Глазные капли
Капли глазные - лекарственная форма, предназначенная для инстилляции в
глаз.
Глазные капли представляют собой водные или масляные растворы или
тончайшие суспензии лекарственных веществ.
К глазным каплям предъявляются следующие требования: стерильность,
стабильность, изотоничность, изогидричность, отсутствие видимых невооруженным
глазом механических загрязнений.
Глазные капли и концентрированные растворы лекарственных веществ для их
приготовления, должны изготавливаться в асептических условиях .
Осмотическое давление глазных капель должно соответствовать осмотическому
давлению раствора натрия хлорида 0.9+0.2%. Для изотонирования можно
использовать хлорид натрия, сульфат натрия, нитрит натрия в необходимом
количестве, с учетом совместимости с лекарственными веществами.
Капли глазные должны быть изотоничны со слезной жидкостью. В отдельных
случаях допускается применение гипертонических или гипотонических растворов, о
чем должно быть указано в частных статьях.
Для приготовления капель глазных применяют растворители и вспомогательные
вещества, разрешенные к медицинскому применению и указанные в частных статьях.
Для приготовления капель глазных используют стерильные растворители: воду
дистиллированную, изотонические буферные растворы, масла и др.
В качестве стабилизаторов, консервантов, пролонгаторов и других
вспомогательных веществ используют: натрия хлорид, натрия сульфат, натрия
нитрат, натрия метабисульфит, натрия тиосульфат, натрия фосфорнокислые соли
одно- и двузамещенные, кислоту борную, кислоту сорбиновую, нипагин, производные
целлюлозы и др.
Капли глазные должны приготавливаться в асептических условиях и быть
стерильными.
Стерилизацию капель глазных осуществляют методами, указанными в частных
статьях в соответствии со статьей "Стерилизация".
Проверку капель глазных на стерильность проводят в соответствии со
статьей "Испытание на стерильность" (с. 187).
Капли глазные должны выдерживать испытания на механические включения.
Испытания на механические включения проводят в соответствии с
инструкцией, утвержденной Министерством здравоохранения СССР. Настоящая
Инструкция устанавливает порядок визуального контроля глазных капель,
изготовленных в аптеках, на отсутствие механических включений. Под
механическими включениями подразумеваются посторонние подвижные нерастворимые
вещества, кроме пузырьков газа, случайно присутствующие в растворах. В процессе
изготовления растворы подвергаются первичному и вторичному контролю.
Первичный контроль осуществляется после фильтрования и фасовки раствора.
При этом просматривается каждая флакон с раствором. При обнаружении
механических включений раствор повторно фильтруют, вновь просматривают,
укупоривают, маркируют и стерилизуют. Растворы, изготовленные асептически,
просматривают один раз после розлива или стерилизующего фильтрования.
Вторичному контролю подлежат также 100% флаконов с растворами, прошедших
стадию стерилизации перед их оформлением и упаковкой.
Контроль растворов на отсутствие механических включений осуществляется
провизором - технологом с соблюдением условий и техники контроля.
Упаковка. Упаковка должна обеспечивать стабильность и стерильность
препарата при хранении и транспортировании и иметь, как правило, устройство для
закапывания.
Хранение. В прохладном, защищенном от света месте, если нет других
указаний в частных статьях.
Отклонения, допустимые в общем объеме жидких лекарственных форм при
изготовлении массо-объемным способом*(2.5.)
. Отклонения, допустимые в массе навески отдельных лекарственных веществ
в жидких лекарственных формах при изготовлении способом по массе или
массо-объемным способом, а также в мазях, определяются не на концентрацию в
процентах, а на массу навески каждого вещества, входящего в эти лекарственные
формы (приложение 2, пп. 2.7 и 2.9.).
Например, при изготовлении 10 мл 2% раствора пилокарпина гидрохлорида
берут массу навески 0,2 г, для которой допускается отклонение +- 10 %. При
анализе достаточно установить, что было взято не менее 0,18 г и не более 0,22 г
пилокарпина гидрохлорида.
Возьми: Раствора пилокарпина гидрохлорида 1% - 10 мл
Выдай. Обозначь.
По 2 капли 3 раза в день в оба глаза.
Rp.: Sol. Pilocarpini hydrochloridi 1% - 10 ml. Signa. По 2 капли З раза в день в оба глаза.
Свойства ингредиентов.hydrochloridum - бесцветные кристаллы или белый
кристаллический порошок без запаха. Гигроскопичен. Очень легко растворим в
воде. Список А.
В прописи выписано одно лекарственное вещество, поэтому заключение о
совместимости ингредиентов нецелесообразно.
Ингредиенты совместимы.
Характеристика лекарственной формы.
Выписана жидкая лекарственная форма - глазные капли, представляющие собой
раствор легкорастворимого вещества
Проверка доз веществ списка А и Б и норм одноразового отпуска.
В глазных каплях проверка доз не проводится.
Паспорт письменного контроля.
Лицевая сторона Оборотная сторона
Выдал: Pilocarpini hydrochloridi 0,1 Пилокарпина гидрохлорида 0,1
Дата. Подпись. Натрия хлорида 0,09 - (0,1 х 0,22)=
Получил: Pilocarpini hydrochloridi 0.1 =0,068, где 0,22 - изотонический
Дата. Подпись. эквивалент пилокарпина гидро-
Дата. № рецепта хлорида по натрия хлориду.
Aquae pro injectionibus 10 ml Воды очищенной 10 млhydrochloridi 0,1chloridi 0,068
Объем
10 мл
Простерилизовано.
Приготовил (подпись)
Проверил (подпись)
Отпустил (подпись)
Рассчитаем осмолярность раствора:.: Solutionis Natrii chloridi 0,9 %
В настоящее время для выражения осмотической активности оф-
тальмологических, инъекционных и инфузионных растворов используют понятия
«осмоляльность» и «осмолярность». Молярная концентрация - количество вещества в
молях, содержащееся в 1 л раствора. Моляльная концентрация - это количество
вещества в молях, содержащееся в 1 кг раствора. Осмоляльность или осмолярность
указывает на содержание в моляльном или молярном растворе активных частиц
(молекул, ионов), создающих определенное осмотическое давление.
Офтальмологические и инъекционные растворы изготавливают в массо-объемной
концентрации, поэтому более удобной в использовании является характеристика
осмолярности.
Если количество осмотически активных частиц в осмолярном растворе таково,
что создаваемое ими давление соответствует физиологическому, такие растворы
называют изоосмолярными. Единицей измерения осмолярности является миллиосмоль
(тысячная доля осмолярной концентрации). Теоретическую осмолярность
рассчитывают по формуле
С= 1000 mn/М,
где С - миллиосмолярность раствора, мосмоль/л;- масса вещества в
растворе, г/л;- число оомотически активных частиц в растворе, образовавшихся в
результате диссоциации при растворении (n = 1, если вещество в растворе не
диссоциирует; n = 2, если вещество при диссоциации образует два иона; n - 3,
если - три и т.д.); М - молекулярная масса вещества, находящегося в растворе. В
нашем примере.
С= 1000 9 2/58,84 = 308 мОсм.
Известно, что 0,9 % раствор натрия хлорида является изотоничным слезной
жидкости и плазме крови, следовательно, концентрация 308 мОсм является
изоосмолярной.
Технология лекарственной формы с теоретическим обоснованием.
Одним из требований, предъявляемых к глазным каплям, является их
изотоничность. Изотонический эквивалент пилокарпина гидрохлорида по натрия
хлориду равен 0,22, т.е. 0,22 г натрия хлорида создают такое же осмотическое
давление, что и 1 г пилокарпина гидрохлорида. Чтобы получить изотонический
раствор в объеме 10 мл, следует взять 0,09 г натрия хлорида. Учитывая,
изотонический эквивалент пилокарпина, рассчитаем какому количеству натрия
хлорида будет эквивалентно 0,1 пилокарпина т.е. (0.1 0,22) = 0,022 г натрия
хлорида, следовательно, натрия хлорида достаточно взять для изотонирования 0,09
- 0,022 0,068 г.
В асептических условиях в стерильную подставку отмеривают 5-6 мл воды
очищенной и растворяют 0,1 г пилокарпина гидрохлорида и 0,07г натрия хлорида. В
паспорте письменного контроля провизор-технолог расписывается в выдаче 0,1 г
пилокарпина гидрохлорида (список А), а ассистент расписывается в получении
указанного количества препарата (Приказ МЗ РФ № 110 от 12.02.07.). Раствор
фильтруют в стерильный отпускной флакон нейтрального стекла через
предварительно промытый стерильный бумажный фильтр (или стерильный стеклянный
фильтр № 3) и через тот же фильтр профильтровывают оставшееся количество
растворителя (во избежание значительных потерь лекарственного вещества на
фильтре). Флакон с раствором укупоривают стерильной резиновой проб-кой,
просматривают его на отсутствие механических включений. При на- личии
механических включений раствор фильтруют повторно и вновь проверяют на
отсутствие загрязнений. Далее флакон обкатывают металлическим колпачком и
проводят стерилизацию. Раствор стерилизуют паром под давлением при температуре
121°С в течение 8 минут. После стерилизации раствор вновь проверяют на
отсутствие механических включений.
Упаковка и оформление.
Флакон оранжевого стекла оформляют этикеткой розового цвета «Глазные
капли», на которой указывают номер аптеки, рецепта, дату изготовления, Ф.И.О.
больного, способ применения. Наклеивают предупредительные этикетки «Хранить в
прохладном и защищенном от света месте», «Обращаться с осторожностью».
Оформление соответствует МУ «Об утверждении единых правил оформления лекарств,
приготовляемых в аптечных учреждениях (предприятиях) различных форм
собственности» от 24.07.97.
Флакон опечатывают и выписывают сигнатуру (Приказ МЗ РФ №
от 12.02.07.).
Оценка качества.
Анализ документации. Номер имеющегося рецепта, паспорта письменного
контроля и номер лекарственной формы идентичны. Расчеты проведены, верно.
Оформление соответствует МУ «Об утверждении единых правил оформления лекарств,
приготовляемых в аптечных учреждениях (предприятиях) различных форм
собственности» от 24.07.97.
Цветность. Приготовленные капли бесцветные. Механические включения
отсутствуют.
Качество укупорки. При переворачивании флакона раствор не под-текает, что
свидетельствует о герметичности упаковки. -
ОСОБЕННОСТИ ХИМИЧЕСКОГО КОНТРОЛЯ
Определение подлинности пилокарпина гидрохлорида проводят по реакции
образования надхромовых кислот, которые образуют с пилокарпином растворимый в
хлороформе комплекс сине-фиолетового цвета.
Количественное определение пилокарпина гидрохлорида проводят методом
алкалиметрии в присутствии органического растворителя. Сумму пилокарпина
гидрохлорида и натрия хлорида титруют серебра нитратом. Объем серебра нитрата,
прореагировавшего с натрия хлоридом, рассчитывают по разности между объёмами
серебра нитрата и натрия гидроксида, учитывая различную молярность натрия гидроксида
и серебра нитрата.
ОРГАНОЛЕПТИЧЕСКИЙ КОНТРОЛЬ
Бесцветная, прозрачная жидкость.
ОПРЕДЕЛЕНИЕ ПОДЛИННОСТИ
Пилокарпина гидрохлорид. К 0,2 мл раствора прибавляют 0,1 мл кислоты
серной разведенной, 1 мл раствора водорода пероксида,
,1 мл раствора калия бихромата, 1 мл хлороформа и взбалтывают.
Хлороформный слой окрашивается в сине-фиолетовый цвет.
Хлорид-ион. К 0,2 мл раствора прибавляют по 0,1 мл кислоты азотной
разведённой и раствора серебра нитрата.
Появляется белый творожистый осадок, растворимый в растворе аммиака.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Пилокарпина гидрохлорид. Алкалиметрический метод. К 0,5 мл раствора
прибавляют 23 мл хлороформа и титруют 0,02 моль/л раствором натрия
гидроксида при взбалтывании до розового окрашивания водного слоя (индикатор - фенолфталеин)
(V мл).
мл 0,02 моль/л раствора натрия гидроксида соответствует 0,004894 г,
пилокарпина гидрохлорида.
Пилокарпина гидрохлорид и натрия хлорид. Аргентометрический метод
(Фаянса). К 0,5 мл раствора прибавляют 0,1 мл раствора бромфенолового синего,
по каплям кислоту уксусную разведенную до зеленовато-желтого окрашивания и
титруют 0,1 моль/л раствором серебра нитрата до фиолетового окрашивания (V м
Объем 0,1 моль/л раствора серебра нитрата (V) в миллилитрах, израсходованный на
титрование натрия хлорида, вычисляют по разности: 1 мл 0,1 моль/л раствора
серебра нитрата соответствует 0,005844 г натрия хлорида.
Новокаина 0,2
Сульфацил-натрия 2,0
Раствора фурацилина /1:5000/ - 20,0 мл
ОСОБЕННОСТИ ХИМИЧЕСКОГО КОНТРОЛЯ
Для определения подлинности новокаина и сульфацила-натрия используют
реакцию образования азокрасителя, т.к. оба препарата содержат первичную
ароматическую аминогруппу. Количественное определение сульфацила-натрия
выполняют методом ацидиметрии.
Новокаин определяют в сумме с сульфацил-натрием методом нитритометрии,
т.к. аргентометрическому определению новокаина мешает сулфацил-натрий, который
вступает с серебра нитратом в реакцию комплексообразования.
Объем натрия нитрита, прореагировавшего с новокаина гидрохлоридом,
рассчитывают по разности между объёмами натрия нитрита и кислоты
хлороводородной.
ОРГАНОЛЕПТИЧЕСКИЙ КОНТРОЛЬ
Прозрачная жидкость, желтого цвета.
ОПРЕДЕЛЕНИЕ ПОДЛИННОСТИ
Новокаин и сульфацил-натрий.
. К 0,3 мл раствора прибавляют 0,2 мл кислоты хлороводородной
разведённой, 0,1 мл 0,1 моль/л раствора натрия нитрита и 0,10,3 мл
полученной смеси вливают в 12 мл свежеприготовленного щелочного
раствора бетта-нафтола. Образуется оранжево-красное окрашивание.
. К 0,5 мл лекарственной формы прибавляют 0,1 мл разведенной кислоты
серной и 0,2 мл 0,1 моль/л раствора калия перманганата. Фиолетовая окраска
тотчас исчезает.
Сульфацил-натрий. К 0,1 мл лекарственной формы прибавляют 0,1 мл раствора
меди сульфата. Образуется голубовато- зеленый осадок, который не изменяется при
стоянии.
Хлорид-ион. К 0,2 мл лекарственной формы прибавляют 0,1 мл раствора
серебра нитрата, появляется белый осадок.
Фурацилин. К 12 мл лекарственной формы прибавляют 2 мл раствора
натрия гидроксида. Появляется оранжево-красное окрашивание.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Сульфацил-натрий. Ацидиметрический метод. К 1 мл лекарственной формы
прибавляют 0,2 мл раствора метилового оранжевого, 0,1 мл раствора метиленового
синего и титруют 0,1 моль/л раствором кислоты хлороводородной до исчезновения
зелёного и появления коричневато-фиолетового окрашивания.
мл 0,1 моль/л раствора кислоты хлористоводородной соответствует 0,02542 г
сульфацил-натрия.
Новокаин и сульфацил-натрий. Нитритометрический метод. К 1 мл
лекарственной формы прибавляют 23 мл воды очищенной, 1 мл кислоты
хлороводородной разведённой, 0,2 г калия бромида, 0,2 мл раствора тропеолина
00, 0,1 мл раствора метиленового синего и при 18-20°С титруют по каплям 0,1
моль/л раствором натрия нитрита до перехода красно-фиолетового окрашивания в
голубое. 1 мл 0,1 моль/л раствора натрия нитрита соответствует 0,02728 г
новокаина.
Содержание новокаина (Х) в граммах рассчитывают по формуле.
Фурацилин. Метод фотоэлектроколориметрии. К 0,5 мл лекарственной формы
прибавляют 7,5 мл воды очищенной, 2 мл 0,1 моль/л раствора натрия гидроксида и
перемешивают. Через 20 мин измеряют оптическую плотность окрашенного раствора
(D ) с толщиной поглощающего слоя 10 мм на фотоколориметре (max = 450
нм - синий светофильтр). В качестве контрольного раствора используют воду
очищенную. Параллельно проводят реакцию с 0,02% раствором фурацилина
(стандартный раствор). К 0,5 мл 0,02% раствора фурацилина прибавляют 7,5 мл
воды очищенной, 2 мл 0,1 моль/л раствора натрия гидроксида, перемешивают и
измеряют оптическую плотность (D ) при тех же условиях, что и исследуемый
раствор.
Содержание фурацилина в лекарственной форме (Х) в граммах рассчитывают по
формуле.
Рибофлавина 0,002
Аскорбиновой кислоты 0,02
Натрия хлорида 0,05
Раствора глюкозы 2%-10 мл
ОСОБЕННОСТИ ХИМИЧЕСКОГО КОНТРОЛЯ
В состав лекарственной формы входит сильный восстановитель
кислота аскорбиновая, поэтому все реакции подлинности на глюкозу, основанные на
её восстановительных свойствах в щелочной среде, не применимы. Используется
реакция конденсации с тимолом в среде кислоты серной концентрированной.
Натрия хлорид определяют методом аргентометрии, кислота аскорбиновая при
этом не мешает количественному определению, т.к. будет вступать в реакцию
окисления-восстановления с серебра нитратом только после того, как прореагирует
натрия хлорид.
ОРГАНОЛЕПТИЧЕСКИЙ КОНТРОЛЬ
Жёлто-зелёная прозрачная жидкость.
ОПРЕДЕЛЕНИЕ ПОДЛИННОСТИ
Рибофлавин. Раствор имеет зеленовато-желтый цвет и зеленую флуоресценцию
в ультрафиолетовом свете.
Аскорбиновая кислота и натрия хлорид. К 0,2 мл раствора прибавляют 0,2 мл
воды, 0,2 мл кислоты азотной разведенной и 0,2 мл раствора серебра нитрата.
Образуются белый творожистый осадок, который со временем темнеет за счет
образования металлического серебра.
Глюкоза. Помещают 0,5 мл раствора в фарфоровую чашку и выпаривают на
водяной бане. После охлаждения к сухому остатку прибавляют 0,01 г тимола, 0,3
мл кислоты серной концентрированной и 0,1 мл воды. Появляется красно-фиолетовое
окрашивание.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Рибофлавин. К 0,5 мл раствора прибавляют 9,5 мл воды и измеряют
оптическую плотность (D ) полученного раствора при длине волны около 445 нм в
кювете с толщиной слоя 10 мм. Раствор сравнения вода. Параллельно
измеряют оптическую плотность (D ) раствора, содержащего 2,5 мл 0,004%
стандартного раствора рибофлавина (0,0001 г) и 7,5 мл воды.
Содержание рибофлавина (Х) в граммах рассчитывают по формуле.
Аскорбиновая кислота. Алкалиметрический метод. 2 мл раствора титруют 0,02
моль/л раствором натрия гидроксида до малинового окрашивания (индикатор
фенолфталеин). 1 мл 0,02 моль/л раствора натрия гидроксида соответствует
0,00352 г аскорбиновой кислоты.
Натрия хлорид. Аргентометрия (метод Фаянса). К 1 мл раствора прибавляют
0,1 мл раствора бромфенолового синего, по каплям кислоту уксусную разведенную
до зеленовато-желтого окрашивания и титруют 0,1 моль/л раствором серебра
нитрата до фиолетового окрашивания. 1 мл 0,1 моль/л раствора серебра нитрата
соответствует 0,005844 г натрия хлорида.
Глюкоза. Рефрактометрический метод. Определяют показатель преломления
раствора (n) и воды (n ) при 20°С.
Количество глюкозы (Х) в граммах вычисляют по формуле.
,00160 - фактор показателя преломления раствора аскорбиновой кислоты;
С - концентрация аскорбиновой кислоты в растворе, определенная химическим
методом, в %;
,00179 - фактор прироста показателя преломления раствора натрия хлорида;
С - концентрация натрия хлорида в растворе, определенная химическим
методом, в %; 0,00142 - фактор прироста показателя преломления раствора
безводной глюкозы.
Тиамина бромида 0,002
Кислоты никотиновой 0,001
Раствора натрия хлорида 0,9% - 10,0
ОСОБЕННОСТИ ХИМИЧЕСКОГО КОНТРОЛЯ
Определение суммы тиамина бромида и кислоты никотиновой проводят методом
нейтрализации, основанном на кислотных свойствах кислоты никотиновой и реакции
вытеснения тиамина бромида из его соли.
Суммарное содержание тиамина бромида и кислоты никотиновой рассчитывают
по среднему ориентировочному титру.
Количественное определение натрия хлорида проводят аргентометрическим
методом. Небольшое количество тиамина бромида не мешает количественному
определению натрия хлорида, т.к. на 1 мл, содержащий 0,0002 г тиамина бромида
необходимо 0,009 мл 0,1 моль/л раствора титранта.
ОПРЕДЕЛЕНИЕ ПОДЛИННОСТИ
Тиамина бромид. Реакция окисления и образования тиохрома. К 1 мл
исследуемого раствора прибавляют по 15 капель 5% раствора калия феррицианида и
натрия гидроксида, 3 мл хлороформа или бутилового спирта, хорошо встряхивают и
дают отстояться.
Слой органического растворителя в УФ-свете имеет синюю флуоресценцию
(тиамин).
Бромиды. К 1 мл исследуемого раствора прибавляют 1 мл разведенной кислоты
хлороводородной, 0,5 мл раствора хлорамина и 1 мл хлороформа и взбалтывают;
хлороформный слой окрашивается в желтый цвет.
Кислота никотиновая. К 1 мл исследуемого раствора прибавляют 15 капель
раствора меди (II) ацетата, образуется осадок голубого цвета. Или к 1 мл
исследуемого раствора прибавляют 0,5 мл раствора меди (II) сульфата и 2 мл
раствора тиоцианата аммония. Появляется зеленое окрашивание вследствие
образования тройного комплексного соединения.
Хлориды. К 0,5 мл исследуемого раствора приливают по 0,5 мл разведенной
кислоты азотной и раствора серебра нитрата, при этом выпадает хлопьевидный
осадок, растворимый в 10% растворе аммиака, и фильтруют. К части фильтрата
прибавляют разведенной азотной кислоты до кислой реакции на лакмус, выпадает
белый осадок серебра хлорида.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Тиамина бромид и кислота никотиновая. Метод алкалиметрии. 10 мл
исследуемого раствора титруют 0,01 моль/л раствором натрия гидроксида до
появления розового окрашивания (индикатор - раствор фенолфталеина). 1 мл 0,01
моль/л раствора натрия гидроксида соответствует 0,002360 г суммы тиамина
бромида и кислоты никотиновой.
Натрия хлорид. Аргентометрия (метод Фаянса). К 1 мл раствора прибавляют
0,1 мл раствора бромфенолового синего, по каплям кислоту уксусную разведенную
до зеленовато-желтого окрашивания и титруют 0,1 моль/л раствором серебра
нитрата до фиолетового окрашивания. 1 мл 0,1 моль/л раствора серебра нитрата
соответствует 0,005844 г натрия хлорида.
ЕДИНЫЕ ПРАВИЛА ОФОРМЛЕНИЯ ЛЕКАРСТВ, ПРИГОТОВЛЯЕМЫХ В АПТЕЧНЫХ УЧРЕЖДЕНИЯХ
(ПРЕДПРИЯТИЯХ) РАЗЛИЧНЫХ ФОРМ СОБСТВЕННОСТИ
Настоящие правила распространяются на все лекарства, приготовляемые в
аптечных учреждениях (предприятиях) индивидуально, в порядке внутриаптечной
заготовки, фасовки для населения и лечебно-профилактических учреждений.
Общие положения
. Все лекарства, приготовляемые в аптечных учреждениях (предприятиях),
оформляются соответствующими этикетками.
. Этикетки для оформления лекарств, приготовляемых индивидуально и в
порядке внутриаптечной заготовки и фасовки, в зависимости от способа их
применения, подразделяются на:
этикетки для лекарств внутреннего употребления с надписью
"Внутреннее";
этикетки для лекарств наружного применения с надписью
"Наружное";
этикетки на лекарства для парентерального введения с надписью "Для
инъекций";
этикетки на глазные лекарства с надписью "Глазные капли",
"Глазная мазь".
. Аптечные этикетки имеют на белом фоне следующие сигнальные цвета:
внутренние - зеленый,
наружные - оранжевый,
глазные капли и глазные мази - розовый,
для инъекций - синий.
. На всех этикетках для оформления лекарств, приготовленных индивидуально
и в порядке внутриаптечной заготовки и фасовки, должны быть типографским
способом отпечатаны предупредительные надписи, соответствующие каждой
лекарственной форме:
для микстур "хранить в прохладном и защищенном от света месте",
"перед употреблением взбалтывать",
для мазей, глазных мазей и глазных капель - "хранить в прохладном и
защищенном от света месте",
для капель внутреннего употребления - "хранить в защищенном от света
месте".
Все этикетки обязательно должны содержать предупредительную надпись
"беречь от детей".
. На лекарства, которые прописаны в лекарственных формах, не указанных в
п. 4 и требуют особых условий хранения, обращения и применения, соответствующие
предупредительные надписи наклеиваются.
Размеры этикеток
. Размеры этикеток определены в соответствии с размерами посуды, в
которой отпускаются лекарства. Этикетки должны иметь следующие размеры:
для флаконов емкостью от 10 до 100 мл - 63х30 мм, выше 100 мл - 90х48 мм;
для флаконов емкостью свыше 200 мл - 120х50 мм;
для пакетов - 70х50 мм;
для коробок и пакетов с лекарствами индивидуального приготовления - 70х43
мм;
для коробок с лекарствами внутриаптечной заготовки и фасовки - 70х50мм;
для банок емкостью 10-30 г - 66х20 мм, свыше 30 г - 81х27 мм.
. Анализ инъекционных лекарственных форм
К инъекционным лекарственным формам относятся стерильные водные и
неводные растворы, суспензии, эмульсии и сухие твердые вещества (порошки,
пористые массы, таблетки), которые растворяют в стерильном растворителе
непосредственно перед введением. Это специфические лекарственные формы,
известные под общим названием инъекции (injectiones).
К инъекционным лекарственным формам предъявляются следующие требования:
отсутствие механических примесей, стерильность, стабильность, апирогенностъ, к
отдельным растворам - изотоничностъ, что указывается в соответствующих
нормативных документах или рецептах. Инъекционные растворы могут быть
изогидричными и изотоничными в соответствии с требованиями частных статей.
Для реализации указанных требований необходимо соблюдение особых условий
приготовления инъекционных лекарственных форм, которые предусматривают:
требования к помещению, производственному оборудованию, персоналу, лекарственным
и вспомогательным веществам, растворителям, укупорочным материалам, организации
и проведению технологических процессов (растворение, стабилизация, фильтрация,
стерилизация, упаковка, маркировка).
Важнейшей составной частью технологического процесса всех инъекционных
лекарственных форм является организация работы в асептических условиях и
стерилизация.
Растворы для инъекций готовят в соответствии с требованиями ГФ, приказов
МЗ, инструкций, НД.
Технологический процесс приготовления растворов для инъекций состоит из
следующих стадий:
. Подготовительные работы.
. Приготовление раствора (стабилизация, изотонирование при
необходимости).
.Фильтрование и фасовка раствора.
. Стерилизация раствора.
. Контроль готовой продукции.
. Оформление.
Подготовительные работы (подготовка персонала, подготовка асептического
блока, организация работы в асептических условиях; подготовка посуды и
вспомогательных материалов; подготовка растворителей и препаратов) приведены в
приказе № 309 от 21.10.97. Рассмотрим стадии непосредственного приготовления
растворов для инъекций.
Приготовление раствора. Приготовление растворов для инъекций может
производиться только в аптеках, имеющих на это разрешение - лицензию,
выдаваемую уполномоченным на то органом.
Не разрешается готовить растворы для инъекций при отсутствии методик их
полного химического анализа, режима стерилизации, данных о химической
совместимости входящих ингредиентов и технологии изготовления.
Персональная ответственность за организацию работы асептических блоков и
приготовление растворов для инъекций возлагается на заведующих аптеками. Они
обязаны проводить ежеквартально инструктаж и проверку знаний работников
асептических блоков по правилам приготовления растворов для инъекций, а также
при приеме или переводе их на работу в асептический блок. Лица, не владеющие
технологией изготовления растворов для инъекций, к работе в асептическом блоке
не допускаются. В связи с весьма ответственным способом применения и большой
опасностью ошибок, которые могут быть допущены во время работы, приготовление
инъекционных растворов нуждается в строгой регламентации и неукоснительном
соблюдении технологии. Не допускается одновременное приготовление нескольких
инъекционных растворов, включающих различные ингредиенты или одни и те же, но в
разных концентрациях. На рабочем месте во время приготовления инъекционных
растворов не должны быть штангласы с лекарственными веществами, которые не
имеют отношения к этим ра створам.
Приготовление инъекционных растворов производится массо-объѐмным
методом, при котором лекарственное вещество берется по массе, а растворитель -
до получения определенного объема раствора. Необходимость приготовления
растворов в массо-объѐмной концентрации объясняется тем, что при введении
с помощью шприца лекарственный препарат дозируется по объѐму.
Технологическая стадия «Приготовление раствора» включает три технологические
операции:
подготовка сырья (проведение расчетов, отвешивание веществ и отмеривание
растворителя), непосредственно приготовление раствора (растворение веществ,
если необходимо - добавление стабилизатора, получение нужного объѐма) и
первичный анализ.
Взятое по массе лекарственное вещество помещают в стерильную мерную
колбу, растворяют в небольшом количестве растворителя, а затем доводят до
определенного объѐма. При отсутствии мерной посуды количество
растворителя, необходимое для приготовления раствора, определяют расчетным
способом, пользуясь величиной плотности раствора данной концентрации или
коэффициентом увеличения объѐма.
Объѐм, занимаемый стабилизаторами, входит в общий объем раствора,
поэтому они добавляются одновременно с лекарственными веществами.
При укрупненном приготовлении растворов для инъекций требуются емкости
вместимостью от 10 л и более. В крупных межбольничных и больничных хозрасчетных
аптеках растворение лекарственных препаратов производится в стеклянных 20 -
литровых реакторах оборудованных электроподогревом и электромешалками. В
средних по мощности производства межбольничных аптеках процесс перемешивания
жидкости механизирован с помощью мешалок различного типа.
Немедленно после приготовления раствора проводят опросный контроль. Далее
приготовленный раствор для инъекций подвергают полному первичному химическому
контролю, который заключается в определении подлинности (качественный анализ) и
количественного содержания (количественный анализ) действующих веществ и
стабилизатора. Результаты полного химического контроля растворов для инъекций
регистрируются в журнале по установленной форме. В случае удовлетворительного
результата приступают к фильтрованию и фасовке. Контроль готовой продукции.
После стерилизации проводят, в т о р и ч н ы й контроль на отсутствие
механических включений, качественный и количественный анализ. Для анализа
отбирают один флакон раствора от каждой серии (за одну серию раствора считают
продукцию, полученную в одной емкости от одной за- грузки лекарственного
вещества). Одновременно проводится проверка качества укупорки флаконов
(алюминиевый колпачок не должен прокручиваться при повороте вручную) и объем
наполнения флаконов (±5 %). Контроль растворов для инъекций на стерильность и
пирогенные вещества осуществляется в соответствии с требованиями действующих
инструкций и НД.
Таким образом, контроль качества растворов для инъекций должен охватывать
все стадии их приготовления. Результаты по-стадийного контроля приготовления
растворов для инъекций регистриру ются в специальном журнале по установленной
форме (пр. МЗ РФ№214 от 16.07.97г. прил. 5).
Изготовление и контроль качества стерильных растворов в аптеках
осуществляется в соответствии с требованиями действующих ГФ, «Методических
указаний по изготовлению стерильных растворов в аптеках», действующих
нормативных документов, приказов и инструкций.
Изготовление стерильных растворов запрещается при отсутствии данных о
химической совместимости входящих в них лекарственных веществ, технологии и
режиме стерилизации, а также при отсутствии методик анализа для их полного
химического контроля.
Подготовка вспомогательных, укупорочных материалов, посуды, средств малой
механизации должна осуществляться в соответствии с требованиями действующих
нормативных документов, приказов и инструкций.
Вода очищенная, вода для инъекций, лекарственные вещества и
вспомогательные материалы, используемые при изготовлении стерильных растворов,
должны соответствовать требованиям действующих ГФ и других нормативных
документов.
Категорически запрещается одновременное изготовление на одном рабочем
месте нескольких стерильных растворов, содержащих ЛВ с различными
наименованиями или одного наименования, но в разных концентрациях.
Стерилизацию растворов необходимо проводить не позднее, чем через три
часа от начала изготовления, под контролем фармацевта или провизора.
Микробиологический контроль растворов на стерильность и испытание на
пирогенность растворов для инъекций и инфузий проводится в соответствии с
требованиями действующей ГФ.
Стерильные растворы должны храниться в условиях, учитывающих
физико-химические свойства входящих в них веществ, и не более установленного
срока годности. По истечении сроков годности стерильные растворы подлежат
изъятию. Повторная стерилизация растворов не допускается. Стерильные растворы
считаются забракованными при несоответствии требованиям нормативных документов
по внешнему виду; величине рН; подлинности и количественному содержанию
входящих веществ; присутствию видимых механических включений; при недопустимых
отклонениях от номинального объема раствора; нарушениях фиксированное™
укупорки; нарушениях действующих требований к оформлению ЛС, предназначенных к
отпуску
Растворы глюкозы. Промышленностью выпускаются растворы - глюкозы для
инъекций в концентрации 5%, 10%, 25% и 40%. Вместе с тем, инъекционные растворы
глюкозы в значительных количествах готовятся в аптеках. Растворы глюкозы
сравнительно нестойки при длительном хранении. Основным фактором, определяющим
устойчивость глюкозы в растворе, является рН среды. В щелочной среде происходит
ее окисление, карамелизация и полимеризация. При этом наблюдается пожелтение, а
иногда побурение раствора. ГФ X предписывает стабилизировать растворы глюкозы
смесью натрия хлорида 0,26 г на 1 л раствора и 0,1М раствора кислоты
хлористоводородной до рН = 3,0 - 4,0. В условиях аптеки для удобства работы
этот раствор (известный под названием стабилизатор Вейбеля) приготавливают
заранее по прописи:
Натрия хлорида 5,2 г
Кислоты хлористоводородной разбавленной (8,3 %) 4,4 мл
Воды для инъекций до 1л
При приготовлении растворов глюкозы (независимо от ее концентрации)
стабилизатора Вейбеля добавляют 5 % от объема раствора.
Большое значение для стабильности изготавливаемых растворов имеет
качество самой глюкозы, которая может содержать кристаллизационную воду. В
соответствии с ФС 42-2419 - 86 производится глюкоза безводная, содержащая 0,5%
воды (вместо 10%) Она отличается растворимостью, прозрачностью и цветом
раствора . При использовании глюкозы водной ее берут больше, чем указано в
рецепте.
Растворы натрия гидрокарбоната.
Растворы натрия гидрокарбоната в концентрации 3, 4, 5 и 7 % применяются
для капельного внутривенного введения при гемолизе крови, ацидозах, для
реанимации (при клинической смерти), для регулирования солевого равновесия.
При использовании натрия гидрокарбоната «годен для инъекций» не всегда
удается получить прозрачные и устойчивые растворы, поэтому применяют натрия
гидрокарбонат «х.ч.» или «ч.д.а.». Ввиду потенциальной нестабильности натрия
гидрокарбоната его растворяют при возможно более низкой температуре (15 -
20°С), избегая сильного взбалтывания раствора. Проводят первичный химический
анализ, фильтруют, укупоривают и проверяют на отсутствие механических примесей.
При положительном анализе флакон, укупоренный резиновой пробкой, закрывают
металлическим колпачком и обкатывают. Во избежание разры-
ва флаконов при стерилизации их заполняют раствором не более чем на 80 %
объема. Раствор стерилизуют при 120ºС 8 минут.
Во время стерилизации натрия гидрокарбонат подвергается гидролизу. При
этом выделяется углерода диоксид и образуется натрия карбонат. При охлаждении
идет обратный процесс, углекислота растворяется и образуется натрия
гидрокарбонат. Поэтому для достижения равновесия в системе, простерилизованные
растворы можно использовать только после их полного охлаждения, не ранее чем
через 2 часа, перевернув их несколько раз с целью перемешивания и растворения
углекислоты, находящейся над раствором. После стерилизации проводят вторичный
контроль качества раствора и оформляют к отпуску. Полученный раствор должен
быть бесцветным и прозрачным, рН 8,9 - 9,1. При внутриаптечной заготовке срок
хранения раствора при комнатной температуре 30 суток. Прозрачные растворы с
концентрацией натрия гидрокарбоната 7 - 8,4 % можно получить при стабилизации
трилоном Б с последующей микрофильтрацией через мембранные фильтры «Владипор»
типа МФА-А №1 или № 2 с предфильтром из фильтровальной бумаги.
.Приказ № 305. Анализ дефектуры
ИНСТРУКЦИЯ ПО
ОЦЕНКЕ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ, ИЗГОТОВЛЯЕМЫХ В АПТЕКАХ
1. Качество лекарственных средств (в том числе гомеопатических),
изготовляемых в аптеках, устанавливается по комплексу показателей,
характеризующих их качество.
Уровень качества лекарственных средств оценивается в соответствии с
требованиями, регламентированными действующими Государственной Фармакопеей,
приказами и инструкциями Министерства здравоохранения Российской Федерации.
. Для оценки качества лекарственных средств, изготовленных в аптеках,
применяются два термина: "Удовлетворяет" ("Годная
продукция") или "Не удовлетворяет" ("Брак")
требованиям действующих Государственной Фармакопеи, приказов и инструкций
Министерства здравоохранения Российской Федерации.
. Уровень качества изготовленных лекарственных средств определяется
органолептическим и измерительными методами.
.1. Несоответствие по описанию (внешний вид, цвет, запах).
.2. Несоответствие по прозрачности или цветности.
.3. Несоответствие по распадаемости.
.4. Неоднородность по измельченности или смешиванию порошков, мазей,
суппозиториев, гомеопатических тритураций.
.5. Наличие видимых механических включений.
.6. Несоответствие прописи по подлинности:
.6.1. Ошибочная замена одного лекарственного вещества другим, отсутствие
прописанного или наличие непрописанного вещества.
.6.2. Замена лекарственных средств на аналогичные по фармакологическому
действию без обозначения этой замены на требовании, рецепте (копии рецепта,
этикетке).
.7. Отклонения от прописи по массе или объему.
.7.1. Отклонения по общей массе (объему).
.7.2. Отклонения по массе отдельных доз и их количеству.
.7.3. Отклонения по массе навески (или по концентрации) отдельных
лекарственных веществ.
.8. Несоответствие по величине pH.
.9. Несоответствие по величине плотности.
.10. Несоответствие по стерильности.
.11. Несоответствие по микробиологической чистоте.
.12. Нарушение фиксированности укупорки (для стерильных лекарственных
форм).
.13. Нарушение действующих правил оформления лекарственных средств,
предназначенных к отпуску.
. Изменения в составе лекарственных форм (если необходимо) должны
производиться только с согласия врача, за исключением случаев, установленных действующими
Государственной Фармакопеей, приказами и инструкциями Минздрава России и должны
отмечаться на требовании, рецепте (копии рецепта, этикетке). При отсутствии
указанной отметки на требовании, рецепте (копии рецепта, этикетке) качество
изготовления лекарственной формы оценивается "Неудовлетворительно".
. Изменения в количестве отпущенного лекарственного средства или отпуск
таблеток вместо порошков должны также отмечаться на требовании, рецепте (копии
рецепта, этикетке).
. При определении отклонений в проверяемых лекарственных формах следует
использовать измерительные средства того же типа (с одинаковыми
метрологическими характеристиками), что и при их изготовлении в аптеках.
.Жидкие лекарственные средства индивидуального изготовления и для
стационарных учреждений. Приказ 308
В виде жидких лекарственных форм в аптеке готовят:
.лекарственные формы по индивидуальным рецептам или требованиям ЛПУ;
.концентраты, полуфабрикаты;
.внутриаптечную заготовку и фасовку жидких лекарственных форм.
Основные правила изготовления жидких лекарственных форм
Общие правила изготовления, последовательность растворения и смешивания
лекарственных средств . При изготовлении жидких лекарственных форм с водной
дисперсионной средой в первую очередь отмеривают рассчитанный объем воды
(очищенной, для инъекций или ароматной), в котором последовательно растворяют
твердые лекарственные и вспомогательные вещества с учетом растворимости и
возможного их взаимодействия.
Первыми в отмеренном объеме воды растворяют ядовитые и наркотические
вещества (список А), затем наркотические и сильнодействующие (список Б), а
далее несильнодействующие с учетом их растворимости. Для повышения
растворимости веществ умеренно, мало или медленно растворимых их предварительно
измельчают, а в процессе изготовления их растворы нагревают с учетом
физико-химических свойств и перемешивают. При изготовлении растворов очень мало
растворимых или практически нерастворимых веществ, кроме вышеперечисленных
операций используют получение растворимых производных (комплексообразование,
образование растворимых солей) и солюбилизацию в соответствии с нормативной
документацией. Изготовленный раствор фильтруют через фильтр, материал которого
подбирают с учетом физико-химических свойств веществ и назначения раствора.
Твердые лекарственные вещества в состав лекарственной формы могут быть введены
в виде заранее изготовленных концентрированных растворов, которые добавляются
после растворения твердых веществ и фильтрования раствора .Если в состав
лекарственной формы входят другие жидкие лекарственные средства, их добавляют к
водному раствору в следующей последовательности:
водные нелетучие и непахучие жидкости,
иные нелетучие жидкости, смешивающиеся с водой,
водные летучие жидкости,
жидкости, содержащие спирт, в порядке возрастания его концентрации
летучие и пахучие жидкости.
При добавлении всех жидкостей также следует учитывать их принадлежность к
определенному списку, растворимость и способность смешиваться с водой. При
изготовлении растворов в вязких и летучих растворителях непосредственно в сухой
флакон для отпуска дозируют лекарственное средство или вещество,
вспомогательные вещества, затем взвешивают растворитель (спирт отмеривают).При
использовании вязких растворителей (глицерин, масла) применяют нагревание с
учетом физико-химических свойств лекарственных веществ. При растворении в
спирте или хлороформе -нагревают только в случае необходимости и с соблюдением
мер предосторожности.Растворы, содержащие летучие вещества, нагревают при
температуре не более 40-45 град.С. Жидкости, содержащие эфир и его смеси со
спиртом не нагревают. Растворы фильтруют через сухой фильтрующий материал,
который подбирают с учетом вязкости и летучести растворителя, соблюдая меры
предосторожности для снижения потерь, связанных с испарением.
Они подвергаются всеми видами контроля и это можно представить в виде
схемы.
Жидкие лекарственные формы, изготовленные по индивидуальным рецептам и
требованиям ЛПУ подвергаются всеми видами контроля: обязательным (письменному,
органолептическому и контролю при отпуске), выборочным (физическому, опросному)
и химическому (качественному или полному химическому контролю).
Все виды контроля осуществляются в соответствии с требованиями приказов
МЗ РФ № 214 и № 305
Качественному и количественному анализу (полный химический контроль)
подвергаются выборочно:
Лекарственные формы, изготовленные в аптеке по индивидуальным рецептам
или требованиям лечебных организаций, проверяются в количестве не менее трех
лекарственных форм при работе в одну смену с учетом различных видов
лекарственных форм. Особое внимание обращается на лекарственные формы для
детей; применяемые в глазной практике; содержащие наркотические и ядовитые
вещества; растворы для лечебных клизм.
АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ
.ПИСЬМЕННЫЙ КОНТРОЛЬ. 1.Проверяют соответствие записей в паспорте
письменного контроля прописи в рецепте, правильности произведенных расчетов.
.ОПРОСНЫЙ КОНТРОЛЬ.
. Проводится после изготовления фармацевтом не более 5-ти лекарственных
форм.
.Провизор-технолог называет первый входящий в лекарственную форму
ингредиент, а в сложны лекарственных формах указывает и его количество.
.Фармацевт затем называет все взятые им ингредиенты и их количество. Если
взят концентрат или полуфабрикат, то называет также их состав и количество.
. ОРГАНОЛЕПТИЧЕСКИЙ КОНТРОЛЬ.
.внешний вид лекарственной формы,
.цвет,
.запах,
.отсутствие механических включений
.ФИЗИЧЕСКИЙ КОНТРОЛЬ:
.общий объем лекарственной формы,
.находят отклонения по объему,
.проверяют качество укупорки,
.сравнивают с допустимыми нормами отклонений.
.ХИМИЧЕСКИЙ КОНТРОЛЬ:
.качественный анализ,
.количественный анализ,
.производят необходимые расчеты содержания ингредиентов.
.КОНТРОЛЬ ПРИ ОТПУСКЕ.
Внутриаптечный контроль жидких лекарственных форм также
предусматриваетпроверку специфических показателей качества:
ОТСУТСТВИЕ МЕХАНИЧЕСКИХ ВКЛЮЧЕНИЙ.
Под механическими включениями подразумевают посторонние подвижные
нерастворимые вещества, кроме пузырьков газа, случайно присутствующих в
растворах.
Проверяют их путем легкого встряхивания и перевертывания вверх дном с
последующим наблюдением за раствором в прямом и отраженном свете. Если в
растворе содержатся взвешенные частицы, то они при этом опускаются вниз и
попадают в поле зрения.
Растворы, содержащие частицы, заметные невооруженным глазом должны быть
повторно процежены или профильтрованы.
ГЕРМЕТИЧНОСТЬ УКУПОРКИ.
Осуществляется после переворачивания флакона с жидкой лекарственной
формой вверх дном. При этом жидкость не должна протекать через пробку.
ПРОВЕРКА ОБЩЕГО ОБЪЕМА.
Производится тем же цилиндром и другой измерительной посудой, с помощью
которой готовили растворы.
Натрия салицилата 6,0
Раствора калия иодида 4,0 - 200,0
Подлинность.
. К 1-2 мл лекарственной формы прибавляют 1 мл хлороформа, 2-3
Капли разведенной соляной кислоты, 2-3 капли 0,5% раствора перманганата
калия и энергично встряхивают. Хлороформный слой окрашивается в
фиолетовый цвет (иодид-ион).
. К 2 мл раствора прибавляют 1 мл раствора винной кислоты, 1 мл
ацетата натрия. Раствор охлаждают водопроводной водой и встряхивают. Постепенно
выпадает белый кристаллический осадок, растворимый в
разведенных минеральных кислотах и растворах едких щелочей (ион калия).
. К нескольким каплям добавляют 1-2 капли хлорида железа (III).
Появляется сине-фиолетовое окрашивание (салицилат-ион).
Количественное определение.
Калия иодид
К 5 мл раствора прибавляют 5-10 мл воды, 2 мл разведенной кислоты, 1-2
капли раствора эозината натрия и титруют 0,1 моль/л раствором нитрата серебра
до перехода окраски от желтой к розовой.
Натрия салицилат.
К 1 мл раствора прибавляют 2-3 мл эфира, 1 каплю 0,05% раствора
метилового оранжевого и титруют при встряхивании 0,1 М раствором соляной
кислоты до розового окрашивания водного слоя.
.Твердые лекарственные формы. Порошки
Порошки должны быть однородными при рассмотрении невооруженным глазом и
иметь размер частиц не более 0,160 мм, если нет других указаний в частных
статьях.
Сложные порошки готовят с учетом свойств ингредиентов и их количеств. При
наличии в составе сложного порошка ингредиентов в разных количествах смешение
начинают с веществ, входящих в меньших количествах, постепенно добавляя
остальные ингредиенты.
Ядовитые и сильнодействующие вещества в количествах менее 0,05 г на всю
массу используют в виде тритураций - смеси с молочным сахаром или другими
вспомогательными веществами, разрешенными к медицинскому применению (1:100 или
1:10).
Отклонения, допустимые в массе дозированных порошков:
Хранение. В упаковке, предохраняющей от внешних воздействий и
обеспечивающей стабильность препарата в течение указанного срока годности, в
сухом и, если необходимо, прохладном, защищенном от света месте.
Кислотыаскорбиновой 0,1
Кальцияглюконата 0,25
Подлинность.
. Около 0,5 г порошка растворяют при нагревании в 8-10 каплях разведенной
уксусной кислоты и прибавляют 5-7 капель раствора оксалата аммония. Образуется
белый осадок, растворимый в соляной кислоте (ион кальция).
. Растворяют 0,05 г порошка при нагревании в 8-10 каплях воды, прибавляют
2-3 капли пергидроля и смесь кипятят 2-3 минуты. Затем охлаждают и прибавляют
1-2 капли раствора хлорида железа (III).
Появляется желто-зеленое окрашивание (глюконат-ион).
. К 0,005 г порошка прибавляют по 1-2 капли растворов гексацианоферрата
(III) калия и хлорида железа (III). Появляется синее окрашивание (кислота
аскорбиновая).
. К 0,01 г порошка прибавляют 3-5 капель воды и 2-3 капли раствора
Нитрата серебра . Выделяется осадок серого цвета (кислота аскорбиновая).
Количественное определение.
Кислота аскорбиновая.
0,05 г порошка растворяют в 5 мл воды в колбе с притертой пробкой и
титруют 0,1 н. раствором йода до слабо-желтого окрашивания.
Кальция глюконат.
К 0,05 г порошка добавляют 3-5 мл воды при нагревании. После Охлаждения
прибавляют 3-5 мл аммиачного буферного раствора, 3-4капли индикатора кислотного
хром темно-синего и титруют 0,05 М раствором трилона Б до сине-фиолетового
окрашивания.
.Мягкие лекарственные формы (мази, суппозитории)
Оценка качества мазей
Качество приготовленных мазей оценивают так же, как и других
лекарственных форм, то есть проверяют документацию (рецепт, паспорт), упаковку,
оформление, отсутствие расслаивания и механических включений, отклонение в
массе. Определение подлинности проводят визуально по внешнему виду и
органолептическим признакам (запах, цвет и др.), зависящим от свойств входящих
в мазь лекарственных веществ и от использованных мазевых основ.
Однородность мазей определяют по величине частиц твердой фазы (ГФ XI).
Для этого используют биологический микроскоп, снабженный окулярным микрометром
МОБ-1 при увеличении окуляра 15 объектива 8 .
Цену деления окулярного микрометра выверяют по объекту-микрометру для
проходящего света (ОПМ). Пробу мази отбирают, как указано в статье «Отбор проб
лекарственных средств», и она должна соответствовать не менее 5,0 г. Если
концентрация лекарственных веществ в мазях превышает 10 %, то их разбавляют
соответствующей основой до содержания около 10 % и перемешивают. При отборе
следует избегать измельчения частиц.
Методика определения. Из средней пробы мази берут навеску 0,05 г и
помещают на необработанную сторону предметного стекла. Другая сторона
предметного стекла обработана следующим образом: на середине его алмазом или
каким-либо другим абразивным материалом наносят квадрат со стороной около 15 мм
и диагоналями. Линии окрашивают с помощью карандаша по стеклу. Предметное стекло
помещают на водяную баню до расплавления основы, прибавляют каплю 0,1 % -ного
раствора Судана III для жировых, углеводородных и эмульсионных основ типа В/М
или 0,15 %-ного раствора метиленового синего для гидрофильных и эмульсионных
основ типа М/В и перемешивают. Пробу накрывают покровным стеклом (24 x 24 мм).
Фиксируют его путем слабого надавливания и просматривают в четырех полях зрения
сегментов, образованных диагоналями квадрата. Для анализа одного препарата
проводят 5 определений средней пробы. В поле зрения микроскопа должны
отсутствовать частицы, размер которых превышает нормы, указанные в частных
статьях.
Определение рН мазей необходимо для контроля стабильности лекарственных
веществ и основы во время хранения. Сдвиг рН свидетельствует об изменении
физико-химических свойств последних.
Важным критерием качества мазей являются показатели
структурно-механических (реологических) свойств. Консистенция мазей влияет на
процессы их приготовления и расфасовки, намазываемости мазей и высвобождения из
них лекарственных веществ.
Одним из важных факторов, от которых зависит консистенция, - это
предельное напряжение сдвига, характеризующее способность мази оказывать
некоторое сопротивление при намазывании и экструзии (способности выдавливаться
из туб, дозаторов и т. д.).
Особенность. В состав мази входят тугоплавкие вещества, поэтому их
расплавляют в первую очередь.
г воска желтого помещают в фарфоровую чашку и расплавляют, затем
добавляют 2,5 г парафина, 2,0 ланолина безводного и в самом конце 5 г масла
подсолнечного. Затем сплав переносят в теплую ступку и перемешивают до
охлаждения. Готовую мазь переносят в широкогорлую банку. Оформление к отпуску в
соответствии с требованиями НД. Основная этикетка: “Мазь”, дополнительная
“Хранить в прохладном месте”. Срок годности лекарственной формы 10 суток
(приказ № 214 от 16.07.97).
Оценка качества: анализ документации, правильность упаковки и оформления,
органолептический контроль, отклонение в массе.
Возьми:
Нефти нафталанской рафинированной 7,0
Парафина1,8
Петролатума1,2
Смешай, чтобы получилась мазь.
Дай. Обозначь.
Мазь нафталанская.
Наносить на воспаленные суставы.
1.1.Rp.:Naphtalaniliquidiraffinati7,0,8,2fiat unguentum
Da.Signa: Мазь нафталанная.
Технология лекарственной формы с теоретическим обоснованием
В выпарительной чашке первым на водяной баннера сплавляют 1,2петролатума,
как более тугоплавкий комитент. Добавляют1,8 парафина и, после его
расплавления, жидкий компонент нафталанскую нефть. Гомогенизацию мази проводят
В нагретой ступке при температуре помешивания расплава до полного охлаждения.
.8.Упаковкаиоформление
Мазь помещают в стеклянную баночку на10,0снавинчивающейся крышкой.
Наклеивают номер рецепта. Оформляют этикеткой «Наружное», предупредительные
надписи:«Хранить в прохладном, защищенном от света месте»,«Беречь от
детей»всоответствиисприказомМЗРФ№376от13.11.96г.
Оценка качества
Анализ документации. Рецепт выписан правильно. Ингредиенты совместимы.
Паспорт письменного контроля и номер соответствуют рецепту.
Правильность упаковки и оформления. Емкость банки соответствует
количеству мази. Укупорка правильная. Оформле ние соответствует приказу МЗРФ
№376 от13.11.96г.
Органолептический контроль. Мазь темно-коричневого, почти черного цвета с
запахом нафталанской нефти однородна.
Масса мази 10,0+1,0, что соответствует нормам допустимых отклонений
(±10%)в общей массе мазей.
Контроль качества суппозиторий.
Качество изготовленных суппозиториев оценивают также, как и
Других лекарственных форм, по показателям: однородность, цвет, запах,
отсутствие механических включений; проводят качественный и количественный
анализ; проверяют рецепт, паспорт письменного контроля, сигнатуру, этикетку, их
соответствие изготовленному препарату, упаковку и оформление.
Органолептический контроль.
Внешний вид, цвет и запах суппозиториев должны соответствовать введенным
в их состав лекарственным и вспомогательным веществам Готовые суппозитории на
гидрофильных основах представляют собой студни, сохраняющие первоначальную
форму при комнатной температуре, но растворяющиеся или набухающие при температуре
тела.
Специфичным для качества суппозиториев являются размер и форма, которые
должны соответствовать суппозиториям, выписанным в прописи рецепта. Вагинальные
свечи могут иметь форму шарика, язычка или яйцевидную; ректальные - конуса,
цилиндра с заостренными
Концами или форму сигары. Палочки должны быть одинаковой толщины по всей
длине и с одной стороны заострены. Все суппозитории должны иметь одинаковую
форму, размеры, достаточную твердость или упругость (для вагинальных
суппозиториев), обеспечивающую удобство применения.
Однородность смешивания. Суппозиторная масса должна быть однородной, без
вкраплений масла какао или лекарственных веществ. Для изготовленных
суппозиториев однородность еще раз проверяется на продольном срезе. На срезе
суппозиториев, изготовленных способом выливания в формы, допускается наличие
воздушного стержня или воронкообразною углубления. Пластичность массы при
изготовлении способом ручного формирования проверяют в процессе изготовления по
способности массы отставать от стенок ступки собираться на головке пестика.
Физический контроль.
При дозировании суппозиториев, изготовленных способом ручного
формирования, сформированный параллелепипед (брусок) должен быть равного
сечения по всей его длине. Масса свечей должна находиться в интервале,
указанном в ГФ. Отклонения в массе отдельных свечей не должны превышать ±5 %.
Средняя масса суппозиториев согласно ГФ определяется взвешиванием 20
суппозиториев. Регламентирован максимальный диаметр ректальных суппозиториев -
неболее 1,5 см, палочек - неболее 1 см.
В контрольно-аналитической лаборатории 1 раз в квартал проверяют
температуру плавления, которая должна быть не выше 37°С (метод 2аГФ), и в
специальном приборе время полной деформации суппозиториев, изготовленных на
липофильных и дифильных основах. Согласно ГФ время полной деформации должно
быть не более 15 мин. Суппозитории, растворяющиеся в
Секретах слизистой оболочки, проверяют на растворимость. Они должны
растворяться при 37±1°Свтечение 1 ч.
Письменный контроль.
После изготовления суппозиторной массы (перед операцией дозирования)
заполняют лицевую сторону ППК. Последовательность записи ингредиентов должна
отражать порядок их добавления в состав суппозиториев при изготовлении. В ППК
указывают массы взятых лекарственных и вспомогательных веществ (основы и всех
веществ, введенных дополнительно), общую массу, число суппозиториев, массу
одного суппозитория, все коэффициенты и формулы, используемые при расчетах.
Возьми: Осарсола 0,2
Глюкозы 0,2
Масла какао достаточное количество, чтобы получился шарик.
Дай таких доз № 10. Обозначь. По 1 шарику на ночь во влагалище.
этап. Проверка совместимости компонентов.
Компоненты совместимы.
этап. Проверка доз осарсола (список А). ВРД = 0,25, ВОД = 1,0.
Доза на один шарик составляет 0,2, суточная доза также равна 0,2.
Следовательно, высшие разовая и суточная доза осарсола в шариках не превышена.
этап. Расчеты (оборотная сторона ППК).
1 Осарсола 2,0
2 Глюкозы 2,0
3 Масла какао 4 х 10 - (2,0+2,0) = 36,0
Общая масса 40,0, число шариков № 10
этап. Технология шариков с теоретическим обоснованием.
В рецепте не указана масса масло какао, следовательно в расчетах
принимаем массу шарика за 4,0 (указания ГФ Х1 изд.). Глюкоза хорошо
растворяется в воде, осарсол очень малорастворим, поэтому при смешивании с
жировой основой (масло какао) образуется комбинированный тип дисперсной системы
(водный раствор глюкозы образует тип эмульсии, осарсол - тип суспензии).
В ступке растворяют в нескольких каплях воды 2,0 глюкозы, получают по
требованию у провизора-технолога (материально-ответственного лица) 2,0
осарсола, добавляют в ступку и тщательно растирают. Затем по частям добавляют
предварительно измельченное в стружку масло какао. Смесь уминают до однородной,
пластичной массы, отстающей от стенок ступки. При необходимости добавляют небольшое
количество ланолина безводного. Суппозиторную массу переносят на капсулу и
взвешивают. Массу указывают на обороте рецепта и в паспорте письменного
контроля, чтобы при повторном изготовлении ориентироваться на обозначенную
массу.
С помощью дощечки на стекле пилюльной машинки формируют брусок. Используя
резак, на бруске делают насечки, согласно количеству прописанных доз. Делят на
10 равных частей. Из каждой части с помощью дощечки выкатывают шарик. При
изготовлении шариков тщательно следят за соблюдением санитарных норм.
этап. Упаковка и оформление к отпуску
Каждый шарик заворачивают в парафинированную (вощаную) капсулу и помещают
в пакет или коробку. Оформляют основной этикеткой “Наружное”, дополнительными:
“Хранить в прохладном, защищенном от света месте”, “Обращаться с
осторожностью”. Лекарственная форма опечатывается. Рецепт остается в аптеке.
Больному выписывается сигнатура.
этап. Оценка качества шариков.
. Анализ документации:
сигнатура и паспорт письменного контроля выписаны правильно. Дозы не завышены.
. Упаковка и оформление:
Каждый шарик аккуратно завернут в капсулу , на пакете прикреплены
основная и дополнительная этикетки согласно требованиям НД. Пакет опечатан.
. Внешний вид:
Шарики с глюкозой и осарсолом имеют однородную форму и цвет. На продольном
срезе отсутствуют вкрапления и механические включения.
. Отклонения в массе отдельных шариков не превышают ±5% (4,0±0,2), согласно требованиям ГФ Х1 изд.
этап. Вывод:
Шарики (вагинальные суппозитории) приготовлены удовлетворительно и могут
быть отпущены больному.
.Анализ концентратов, жидких лекарственных форм(бюретка), полуфабрикатов
и фасовки, внутриаптечной заготовки
Качественному и количественному анализу (полный химический контроль)
подвергаются обязательно: Вся внутриаптечная заготовка лекарственных средств
(каждая серия).
Качественному анализу подвергаются обязательно:
Все лекарственные средства, концентраты и полуфабрикаты (в том числе
гомеопатические настойки, тритурации, растворы, разведения), поступающие из
помещений хранения в ассистентскую комнату, а в случае сомнения - лекарственные
средства, поступающие в аптеку со склада.
Концентраты, полуфабрикаты и жидкие лекарственные средства в бюреточной
установке и в штангласах с пипетками в ассистентской комнате при заполнении.
Лекарственные средства промышленного производства, расфасованные в
аптеке, и внутриаптечная заготовка, изготовленная и расфасованная в аптеке
(каждая серия)
Концентрированные растворы (концентраты) - заранее изготовленные растворы
лекарственных веществ более высокой концентрации, чем концентрация, в которой
эти вещества выписываются в рецептах.
Концентраты предназначены для быстрого и качественного изготовления
жидких лекарственных форм.
Рекомендуется изготавливать концентраты из веществ гигроскопичных,
выветривающихся, содержащих значительное количество кристаллизационной воды.
Номенклатура концентрированных растворов определяется спецификой
рецептуры и объемом работы аптеки и утверждается в соответствии с требованиями
действующей Инструкции.
Концентраты изготавливают по мере необходимости с учетом срока их
годности. Перечень концентрированных растворов, рекомендованных для
использования при изготовлении в аптеках жидких лекарственных форм, условия их
хранения и сроки годности приведены в приложении № 4 приказа МЗ РФ № 308 от
21.10.97.
Концентрированные растворы изготавливают массо-объемным методом в мерной
посуде в асептических условиях в соответствии с требованиями действующей
Инструкции, используя свежеполученную воду очищенную.
В случае отсутствия мерной посуды объем воды очищенной рассчитывают,
используя значение плотности концентрата или коэффициент, соответствующий
увеличению его объема при растворении 1 г лекарственного вещества (приложения №
7,9 приказа МЗ РФ № 308).
Изготовленные растворы фильтруют, подвергают полному химическому контролю
и на отсутствие механических включений. При изготовлении концентрированных
растворов следует избегать концентраций, близких к насыщенным, так как при
понижении температуры возможна кристаллизация растворенного вещества.
Отклонение в концентрации растворов допускается в пределах:
до 20% концентрации раствора (включительно) - не более ±2%
более 20% концентрации раствора - не более ±1%.
Например, для 10% от 9,8% до 10,2%
% от 19,6% до 20,4%
% от 49,5% до 50,5%
В случае превышения нормы допустимого отклонения производят исправление
концентрации раствора.
Емкости с концентрированными растворами оформляют этикетками с указанием
наименования и концентрации раствора, номера серии и анализа, даты
изготовления, срока годности.
Концентрированные растворы хранят в соответствии с физико-химическими
свойствами лекарственных веществ, входящих в их состав, в простерилизованных,
плотно укупоренных емкостях (баллонах, штангласах), в защищенном от света
месте, при температуре 3-50С или выше 250С.
Изменение цвета, помутнение, появление хлопьев, налетов ранее
установленного срока годности являются признаками непригодности растворов.
Приготовить 1 л 20% раствора магния сульфата.
Расчеты:
с использованием мерной посуды
Магния сульфата 20,0
Воды очищенной до 1000 мл
с учетом плотности раствора
Плотность 20% раствора магния сульфата 1,093. Для приготовления берут
200,0 магния сульфата и 893 мл (1093-200) воды очищенной. При этом получается
1093,0 раствора, объем которого равен 1000 мл.
с учетом коэффициента увеличения объема
Коэффициент увеличения объема для магния сульфата равен 0,50 мл/г, то
есть 1,0 магния сульфата займет объем 0,5 мл, а 200,0 магния сульфата - 100 мл
(0,5х200). Необходимо взять 900 мл (1000-100) воды очищенной.
Показатели плотности раствора и коэффициента увеличения объема даны в
приказе МЗ РФ № 308.
Технология:
в мерной посуде
В стерильную мерную колбу отвешивают 200,0 магния сульфата, растворяют в
части воды очищенной, затем доводят водой до 1000 мл, фильтруют через фильтр,
полученный раствор анализируют.
при отсутствии мерной посуды
В стерильную подставку отмеривают 900 мл свежеперегнанной воды очищенной,
растворяют в ней 200,0 магния сульфата, затем раствор фильтруют и анализируют.
.2. Оценка качества:
Концентрированные растворы подвергают полному химическому контролю и
проверяют на отсутствие механических включений. Концентрация раствора может
оказаться крепче или слабее требуемой, тогда необходимо довести концентрацию до
необходимой разбавлением или укреплением раствора.
Например, получено 1 л 25% раствора магния сульфата. Следовало
приготовить 20% раствор. Концентрация раствора допускается в пределах от 19,6
до 20,4%. Количество воды, необходимой для разбавления находят по формуле:
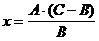
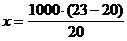
Проверка
расчета: к 1000 мл 23% раствора магния сульфата добавили 150 мл воды очищенной,
общий объем стал 1150 мл, в нем находится 230 г вещества.
Отсюда: 1150 мл - 230 г
- х
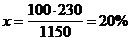
Следовательно, раствор соответствует требуемой концентрации.
Концентрированные растворы повторно проверяют на содержание действующих
веществ после их разбавления или укрепления. После фильтрования склянки с
концентрированными растворами оформляют этикеткой с указанием наименования и
концентрации раствора, даты изготовления, номера серии и номера анализа (приказ
МЗ РФ № 308 от 21.10.97).
Физические и физико-химические методы
К ним относятся: определение температур плавления и затвердевания, а
также температурных пределов перегонки; определение плотности, показателей
преломления (рефрактометрия), оптического вращения (поляриметрия);
спектрофотометрия -- ультрафиолетовая, инфракрасная; фотоколориметрия,
эмиссионная и атомно-абсорбционная спектрометрия, флуориметрия, спектроскопия ядерного
магнитного резонанса, масс-спектрометрия; хроматография -- адсорбционная,
распределительная, ионообменная, газовая, высокоэффективная жидкостная;
электрофорез (фронтальный, зональный, капиллярный); электрометрические методы
(потенциометрическое определение рН, потенциометрическое титрование,
амперометрическое титрование, вольтамперометрия).
Кроме того, возможно применение методов, альтернативных фармакопейным,
которые иногда имеют более совершенные аналитические характеристики (скорость,
точность анализа, автоматизация). В некоторых случаях фармацевтическое
предприятие приобретает прибор, в основе использования которого лежит метод,
еще не включенный в Фармакопею (например, метод романовской спектроскопии --
оптический дихроизм). Иногда целесообразно при определении подлинности или
испытании на чистоту заменить хроматографическую методику на
спектрофотометрическую. Фармакопейный метод определения примесей тяжелых
металлов осаждением их в виде сульфидов или тиоацетамидов обладает рядом
недостатков. Для определения примесей тяжелых металлов многие производители
внедряют такие физико-химические методы анализа, как атомно-абсорбционная
спектрометрия и атомно-эмиссионная спектрометрия с индуктивно связанной
плазмой.
В некоторых частных статьях ГФ X рекомендуется определять температуру
затвердевания или температуру кипения (по ГФ XI -- «температурные пределы
перегонки») для ряда жидких ЛC. Температура кипения должна укладываться в
интервал, приведенный в частной статье. Более широкий интервал свидетельствует о
присутствии примесей.
Во многих частных статьях ГФ X приведены допустимые значения плотности,
реже вязкости, подтверждающие подлинность и доброкачественность ЛC.
Практически все частные статьи ГФ X нормируют такой показатель качества
ЛC, как растворимость в различных растворителях. Присутствие примесей в ЛB
может повлиять на его растворимость, снижая или повышая ее в зависимости от
природы примеси.
Физические
методы анализа
Подлинность лекарственного вещества подтверждают; агрегатное состояние
(твердое вещество, жидкость, газ); окраска, запах; форма кристаллов или вид
аморфного вещества; гигроскопичность или степень выветриваемости на воздухе;
устойчивость к воздействию света, кислорода воздуха; летучесть, подвижность,
воспламеняемость (жидкостей). Окраска лекарственного вещества -- одно из
характерных свойств, позволяющее осуществить его предварительную идентификацию.
Степень белизны (оттенка) твердых лекарственных веществ можно оценить
различными инструментальными методами на основе спектральной характеристики
света, отраженного от образца. Для этого измеряют коэффициенты отражения при
освещении образца белым светом. Коэффициент отражения -- это отношение величины
отраженного светового потока к величине падающего светового потока. Он
позволяет определить наличие или отсутствие у лекарственных веществ цветового
оттенка по степени белизны и степени яркости. Для белых или белых с сероватым
оттенком веществ степени белизны теоретически равна 1. Вещества, у которых она
0,95--1,00, а степени яркости < 0,85, имеют сероватый оттенок.
Более объективным является установление различных физических констант:
температуры плавления (разложения), температуры кипения, плотности, вязкости.
Важный показатель подлинности -- растворимость лекарственного препарата в воде,
растворах кислот, щелочей, органических растворителях (эфире, хлороформе,
ацетоне, бензоле, этиловом и метиловом спирте, маслах и др.).
Константой, характеризующей гомогенность твердых веществ, является
температура плавления. Ее используют в фармацевтическом анализе для
установления подлинности и чистоты большинства твердых лекарственных веществ.
Известно, что это температура, при которой твердое тело находится в равновесии
с жидкой фазой при насыщенной фазе пара. Температура плавления является
постоянной величиной для индивидуального вещества. Присутствие даже небольшого
содержания примесей изменяет (как правило, снижает) температуру плавления
вещества, что позволяет судить о степени его чистоты. Под температурой
плавления подразумевается интервал температур, при котором происходит процесс
плавления испытуемого препарата от появления первых капель жидкости до полного
перехода вещества в жидкое состояние. Некоторые органические соединения при
нагревании разлагаются. Процесс этот происходит при температуре разложения и
зависит от ряда факторов, в частности от скорости нагрева. Приведенные
интервалы температур плавления указывают на то, что между началом и окончанием
плавления лекарственного вещества интервал не должен превышать 2°С. Если
переход вещества из твердого в жидкое состояние нечеткий, то вместо интервала
температуры плавления устанавливают температуру, при которой происходит только
начало или только окончание плавления. Следует учитывать, что на точность
установления температурного интервала, при котором происходит плавление
испытуемого вещества, могут влиять условия подготовки образца, скорость подъема
и точность измерения температуры, опытность аналитика.
Температура кипения -- это интервал между начальной и конечной
температурой кипения при нормальном давлении 760 мм рт.ст. (101,3 кПа).
Температуру, при которой в приемник перегнались первые 5 капель жидкости,
называют начальной температурой кипения, а температуру, при которой перешло в
приемник 95% жидкости, -- конечной температурой кипения. Указанные пределы температур
можно установить макрометодом и микрометодом. Следует учитывать, что
температура кипения зависит от атмосферного давления. Температуру кипения
устанавливают только у сравнительно небольшого числа жидких лекарственных
препаратов: циклопропана, хлорэтила, эфира, фторотана, хлороформа,
трихлорэтилена, этанола.
При установлении плотности берут массу вещества определенного объема.
Плотность устанавливают с помощью пикнометра или ареометра, строго соблюдая
температурный режим, так как плотность зависит от температуры. Обычно это
достигается термостатированием пикнометра при 20°С. Определенные интервалы
значений плотности подтверждают подлинность этилового спирта, глицерина, масла
вазелинового, вазелина, парафина твердого, галогенопроизводных углеводородов
(хлорэтила, фторотана, хлороформа), раствора формальдегида, эфира для наркоза,
амилнитрита и др.
Вязкость (внутреннее трение) -- физическая константа, подтверждающая
подлинность жидких лекарственных веществ. Различают динамическую (абсолютную),
кинематическую, относительную, удельную, приведенную и характеристическую
вязкость. Каждая из них имеет свои единицы измерения.
Для оценки качества жидких препаратов, имеющих вязкую консистенцию,
например глицерина, вазелина, масел, обычно определяют относительную вязкость.
Она представляет собой отношение вязкости исследуемой жидкости к вязкости воды,
принятой за единицу.
Растворимость рассматривают не как физическую константу, а как свойство,
которое может служить ориентировочной характеристикой испытуемого препарата.
Наряду с температурой плавления растворимость вещества при постоянной
температуре и давлении является одним из параметров, по которому устанавливают
подлинность и чистоту практически всех лекарственных веществ.
Методика определения растворимости основана на том, что навеска
предварительно растертого (в необходимых случаях) препарата вносится в
отмеренный объем растворителя и непрерывно перемешивается в течение 10 мин при
(20±2)°С. Растворившимся считают препарат, в растворе которого в проходящем свете
не наблюдается частиц вещества. Если для растворения препарата требуется более
10 мин, то его относят к числу медленно растворимых. Их смесь с растворителем
нагревают на водяной бане до 30° С и наблюдают полноту растворения после
охлаждения до (20±2)°С и энергичного встряхивания в течение 1--2 мин.
Метод фазовой растворимости дает возможность осуществлять количественную
оценку степени чистоты лекарственного вещества путем точных измерений значений
растворимости. Суть установления фазовой растворимости заключается в
последовательном прибавлении увеличивающейся массы препарата к постоянному
объему растворителя. Для достижения состояния равновесия смесь подвергают
длительному встряхиванию при постоянной температуре, а затем с помощью диаграмм
определяют содержание растворенного лекарственного вещества, т.е.
устанавливают, является ли испытуемый препарат индивидуальным веществом или
смесью. Метод фазовой растворимости отличается объективностью, не требует для
выполнения дорогостоящего оборудования, знания природы и структуры примесей.
Это позволяет использовать его для качественного и количественного анализов, а
также для изучения стабильности и получения очищенных образцов препаратов (до
степени чистоты 99,5%), Важное достоинство метода -- возможность отличать оптические
изомеры и полиморфные формы лекарственных веществ. Метод применим ко всем видам
соединений, которые образуют истинные растворы.
Физико-химические методы
Приобретают все большее значение для целей объективной идентификации и
количественного определения лекарственных веществ. Получивший распространение в
различных отраслях недеструктивный анализ (без разрушения анализируемого
объекта) играет важную роль и в фармацевтическом анализе. Для его выполнения
пригодны многие физико-химические методы, в частности оптические, ЯМР-, ПМР-,
УФ- и ИК- спектроскопия и др.
В фармацевтическом анализе наиболее широко используют физико-химические
методы, которые могут быть классифицированы на следующие группы: оптические
методы; методы, основанные на поглощении излучения; методы, основанные на
испускании излучения; методы, основанные на использовании магнитного поля;
электрохимические методы; методы разделения; термические методы.
Большинство перечисленных методов (за исключением оптических,
электрохимических и термических) широко применяют для установления химической
структуры органических соединений.
Физико-химические методы анализа имеют ряд преимуществ перед
классическими химическими методами. Они основаны на использовании как
физических, так и химических свойств веществ и в большинстве случаев отличаются
экспрессностью, избирательностью, высокой чувствительностью, возможностью
унификации и автоматизации.
.Товароведческий анализ лекарственного сырья
Цель товароведческого анализа - определить подлинность, чистоту и доброкачественность
лекарственного сырья. Проводится на складе в контрольно-аналитической
лаборатории.
Первый этап товароведческого анализа (прием и проверка документов партии
сырья) производится в приемном отделении склада. Партия сырья - сырье,
поступившее одновременно от одного поставщика с одними оправдательными
документами о качестве. Партия по весу должна быть не менее 50 кг. Отдельные
ящики или мешки в партии называются местами в партии.
) Прежде всего при поступлении партии сырья на склад от поставщика
проверяется наличие и качество оправдательных документов. Вначале проверяется
накладная, затем сертификат качества (качественное удостоверение) или протокол
анализа завода изготовителя и т.д.
) Внешний осмотр партии сырья: на наличие подмоченных мест и на наличие
мест с нарушенной целостностью упаковки (места с нарушенной целостностью
анализируются отдельно).
) Подсчет количества мест для вскрытия: если на склад поступило от 1 до 5
мест, то вскрывают все; если на склад поступило от 6 до 50 мест, то любые 5
мест; если на склад поступило свыше 50 мест, то вскрывают 10% мест.
) Вскрытие мест. Сырье бракуется без анализа, если:
при вскрытии обнаруживается затхлый запах, не исчезающий при
проветривании в течение суток
если отсутствует естественный запах, или присутствует несвойственный
запах сырья
явно бросаются в глаза механические примеси
при наличии явных вредителей и/или ядовитых растений
В этом случае создается специальная комиссия и составляется акт браковки
сырья, после этого вызывается поставщик.
Второй этап товароведческого анализа (взятие средней пробы и пробы на
поврежденность амбарными вредителями) производится в приемном отделении склада.
) Отбор средней пробы для анализа. Из каждого вскрытого места берут три
точечных пробы (выемки) из разных мест: сверху, снизу и из середины, отступая
от поверхности сырья на 10 см вглубь, чтобы не было заведомо больше сырья с
повышенной влажностью и измельченностью. Выемки берутся вручную, если сырье
крупное; если сырье мелкое и/или сыпучее, то используют зерновой щуп.
Все выемки проверяются на однородность и смешиваются вместе - получается
общая (объединенная) проба. Из этой объединенной пробы методом квартования
берется средняя проба, вес которой указан в ГФ XI, том 2, с. 267.
Для взятия средней пробы методом квартования общая проба раскладывается
на столе в виде квадрата высотой не более 3 см, делится по диагонали на четыре
треугольника. Два противоположных треугольника объединяются и взвешиваются -
вес должен быть равен весу средней пробы. Два оставшихся треугольника в общей
пробе объединяются вместе и из них берется проба на пораженность амбарными
вредителями.
Средняя проба упаковывается в целлофановый пакет и снабжается двумя
этикетками (одна внутрь, одна снаружи). Содержание этикетки: наименование
сырья, поставщик, масса средней пробы, дата отбора средней пробы, подпись лица,
взявшего среднюю пробу.
Проба на поврежденность амбарными вредителями помещается в стеклянную
банку с притертой пробкой и также снабжается двумя этикетками. По весу проба на
поврежденность амбарными вредителями разная: для крупного сырья - 1 кг, для
мелкого - 0,5 кг.
Затем эти пробы отправляются на анализ в лабораторию склада.
Третий этап товароведческого анализа (анализ средней пробы в
контрольно-аналитической лаборатории).
При получении средней пробы она взвешивается, затем методом квартования
берутся три аналитические пробы, вес которых также указан в ГФ XI, том 1. Вес
аналитических проб разный.
|
Первая аналитическая проба
Определяется: - подлинность - измельченность - наличие примесей (чистота)
|
Вторая аналитическая проба
Определяется влажность
|
Третья аналитическая проба
Определяется: - действующие вещества - зольность
|
Аналитические пробы анализируются отдельно:
Анализ первой аналитической пробы:
Раскладывается на столе и производится макроскопический анализ в
соответствии с внешними признаками, затем проба просеивается через сито с
определенным диаметром отверстия, указанным в ГФ XI. То, что отсеялось,
взвешивается и определяется в процентах (масса первой аналитической пробы
берется за 100%) - так находится измельченность в процентах.
Далее в первой аналитической пробе ищут примеси, которые указаны в
фармакопейной статье на данное сырье в параграфе "числовые
показатели". Когда все примеси выделены, их определяют в процентах и
устанавливают соответствие по чистоте требованиям Государственной Фармакопеи.
Анализ второй аналитической пробы:
Из данной пробы берется навеска и помещается в бюкс, котрый затем
помещается в сушильный шкаф и выдерживается при температуре 100°C в течение
часа, и затем охлаждается в эксиккаторе. После этого сырье взвешивают: потеря в
массе в процентах определяет влажность сырья.
Анализ третьей аналитической пробы:
Из данной пробы берется точная навеска и помещается в тигель, затем
сжигается в муфельной печи, прокаливается, охлаждается и взвешивается - таким
образом находят процент общей золы. Оставшуюся золу растворяют в 10% H2SO4. Это
говорит о наличии минеральных примесей.
Четвертый этап товароведческого анализа
По результатам анализа в контрольно-аналитической лаборатории оформляется
документ о качестве - аналитический паспорт, куда заносятся все данные о сырье
при его поступлении и результаты анализа, которые говорят о подлинности и
доброкачественности сырья. Далее делается заключение о возможности применять и
реализовывать данное сырье и на основании какого нормативно-технического
документа проведен анализ. Аналитический паспорт подписывается
провизором-аналитиком, непосредственно проводившим анализ, и заведующим
контрольно-аналитической лаборатории. Обычно на обратной стороне этого же
документа пишется сертификат соответствия, который еще раз подтверждает
качество сырья и дает возможность реализовать его в пределах области или
республики. Например, если анализ проведен в Нижегородском центре контроля
качества лекарственного сырья, то такое сырье можно реализовывать только в
пределах Нижегородской области. В пределах России реализуется сырье только с
российским сертификатом качества.
Эти документы имеют юридическую силу, оформляются только чернилами, без
помарок, подтверждаются подписями и печатями.
11.Изучение приказа № 318 «Об утверждении инструкции по организации
хранения в аптечных учреждениях различных групп лекарственных средств и изделий
медицинского назначения»
ТРЕБОВАНИЯ К ПОМЕЩЕНИЯМ ХРАНЕНИЯ ОГНЕОПАСНЫХ И ВЗРЫВООПАСНЫХ СРЕДСТВ
Вещества огнеопасные, способные к образованию взрывчатых смесей, а также
склонные к самовозгоранию при контакте с воздухом, водой, горючими веществами
или при действии солнечных лучей должны храниться изолированно в условиях,
полностью исключающих возможность такого контакта, а также влияния высоких
температур и механического воздействия.
Складские помещения для хранения огнеопасных и взрывоопасных веществ
должны полностью соответствовать действующим нормативным документам.
Лекарственные средства огнеопасные и взрывоопасные следует хранить по
принципу однородности в соответствии с их физико-химическими, пожароопасными
свойствами и характером упаковки. С этой целью огнестойкие склады разбиваются
на отдельные помещения (отсеки) с пределом огнестойкости строительных
конструкций не менее 1 часа.
При отсутствии отдельных хранилищ для легковоспламеняющихся веществ
допускается хранить их в общем складском здании - в помещениях, соответствующих
требованиям п. 2.3. настоящей инструкции и другим требованиям пожарной
безопасности, согласованными с органами Государственной противопожарной службы.
Данные помещения должны иметь вентиляцию.
Необходимое (на одну рабочую смену)количество огнеопасных веществ для
текущего расхода допускается содержать в фасовочных комнатах складов или аптек,
но при строгом соблюдении мер пожарной безопасности. Оставшееся количество
огнеопасных веществ по окончании работы в конце смены возвращается на место
основного хранения.
Полы складов и разгрузочных площадок должны иметь твердое, ровное
покрытие, исключающее выбоины и другие неровности. Запрещается применять доски
и железные листы для выравнивания полов. Полы должны обеспечивать удобное и
безопасное передвижение людей, грузов и транспортных средств, обладать
достаточной прочностью и выдерживать нагрузки от хранимых материалов,
обеспечивать простоту и легкость уборки складского помещения.
Складские помещения для хранения огнеопасных и взрывоопасных
лекарственных средств должны быть оборудованы несгораемыми и устойчивыми
стеллажами и поддонами, рассчитанными на соответствующую нагрузку. Стеллажи
устанавливаются на расстоянии 0,25 м от пола и стен, ширина стеллажей не должна
превышать 1 м и иметь отбортовки не менее 0,25 м. Продольные проходы между
стеллажами должны быть не менее 1,35 м.
Электроустановки должны монтироваться и эксплуатироваться в соответствии
с действующими нормативными документами.
В аптеках для хранения огнеопасных и взрывоопасных веществ
предусматриваются изолированные помещения.
Помещение хранения огнеопасных и взрывоопасных веществ должно быть
оборудовано средствами автоматической пожарной защиты и сигнализацией в
соответствии с действующими нормативными документами.
В аптеках допускается хранение легковоспламеняющихся и горючих жидкостей
до 10 кг во встроенных несгораемых шкафах с дверьми шириной не менее 0,7 м и
высотой не менее 1,2 м. Место расположения шкафа должно быть удалено от тепло
выводящих поверхностей, проходов и иметь свободный доступ к нему.
В аптеках, встроенных в здание другого назначения, количество хранимых
огнеопасных веществ в не расфасованном виде (легковоспламеняющиеся жидкости) не
должно превышать 100 кг.
Легковоспламеняющиеся жидкости в количестве свыше 100 кг необходимо
хранить в отдельно стоящем здании в стеклянной или металлической таре
изолированно от помещений хранения огнеопасных веществ других групп.
Под особым вниманием и постоянным строгим контролем должны находиться
помещения приема, отпуска и расфасовки лекарственных средств и изделий
медицинского назначения с огнеопасными и взрывоопасными свойствами.
При поступлении товара необходимо срочное его распределение по местам
основного хранения. Во избежание несчастных случаев в помещениях приема и
отпуска категорически запрещается даже кратковременное хранение этих
медицинских товаров. При приеме товара надлежит особое внимание обращать на
состояние укупорки тары индивидуального хранения.
Категорически запрещается одновременная расфасовка нескольких огнеопасных
и взрывоопасных лекарственных веществ в одном помещении. Количество веществ на
рабочем месте фасовщика не должно превышать сменной потребности. В конце
рабочего для остатки веществ возвращаются в помещение основного хранения.
После окончания фасовки каждого наименования лекарственных веществ
помещения тщательно проветриваются.
На складах основного хранения огнеопасных и взрывоопасных средств
снаружи, а также на дверях каждого помещения хранения и работы с названными
средствами и внутри этих помещений должны быть сделаны несмываемые, ясно
видимые надписи: "Огнеопасно", "Взрывоопасно", "Курить
воспрещается", "В случае пожара звонить по телефону...".
Около входа в каждое помещение аптеки или аптечного склада хранения
огнеопасных и взрывоопасных средств и внутри помещения должны быть вывешены
таблички с надписью "Ответственный за обеспечение пожарной безопасности
Ф.И.О.".
Ответственному лицу необходимо производить осмотр помещения ежедневно и
целью уборки оставшихся огнеопасных и взрывоопасных веществ и проведения других
мер в конце рабочего дня.
ОСОБЫЕ ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К УСЛОВИЯМ ХРАНЕНИЯ ОГНЕОПАСНЫХ И
ВЗРЫВООПАСНЫХ ВЕЩЕСТВ
Хранение огнеопасных веществ
К группе огнеопасных веществ, хранящихся в фармацевтических (аптечных)
организациях, относятся легковоспламеняющиеся вещества, представляющие собой в
основном жидкости и легкогорючие вещества (Приложение к данной инструкции).
Хранение легковоспламеняющихся и горючих жидкостей должно осуществляться
отдельно от других материалов.
При необходимости нагревание огнеопасных веществ должно производиться на
водяных банях или электроплитах с закрытой спиралью.
Легковоспламеняющиеся жидкости (коллодий, спирт этиловый, скипидар, эфир
и другие, указанные в приложении к данной инструкции) хранят в плотно
укупоренной прочной, стеклянной или металлической таре, чтобы предупредить
испарение жидкостей из сосудов.
Бутыли, баллоны и другие крупные емкости с легковоспламеняющимися и
горючими жидкостями должны храниться на полках стеллажей в один ряд по высоте,
запрещается их хранение в несколько рядов по высоте с использованием различных
прокладочных материалов. Складирование этих веществ у отопительных приборов не
допускается. Расстояние от стеллажа или штабеля до нагревательного элемента
должно быть не менее 1 м.
Хранение бутылей с легковоспламеняющимися и горючими жидкостями должно
осуществляться в таре, предохраняющей от ударов, или в баллоно-опрокидывателях
в один ряд.
На рабочих местах производственных помещений в фармацевтических
(аптечных) организациях эти средства могут храниться в количествах не
превышающих сменную потребность. При этом емкости, в которых они хранятся,
должны быть плотно закрыты.
Не допускается хранение легковоспламеняющихся и горючих жидких веществ в
полностью заполненной таре. Степень заполнения должна быть не более 90% объема.
Спирты в больших количествах хранятся в металлических емкостях, которые
заполняют не более, чем на 75% объема.
Не допускается совместное хранение легковоспламеняющихся веществ с
минеральными кислотами (особенно серной и азотной кислотами), сжатыми и
сжиженными газами, легкогорючими веществами (растительными маслами, серой,
перевязочным материалом), а также с неорганическими солями, дающими с
органическими веществами взрывоопасные смеси (калия хлорат, калия перманганат,
калия хромат и т.д.).
Эфир медицинский и эфир для наркоза хранят в фабричной упаковке, в темном
прохладном месте (вдали от огня и нагревательных приборов).
Кальция гидрохлорид - не горюч, но при контакте с жидкими маслообразными
органическими продуктами может вызвать их загорание, а с аммиаком и солями
аммония - взрыв, поэтому хранение его должно осуществляться изолированно, с
учетом описанных свойств.
При обращении с легковоспламеняющимися жидкостями (фасовка, переноска,
погрузка и т.д.) необходимо соблюдать особую осторожность, а также постоянно
наблюдать за состоянием тары, ее герметичностью и исправностью. При обнаружении
дефектов и неисправностей тары немедленно должны приниматься меры к их
устранению или содержащиеся в ней вещества перекладываются в другую исправную
тару.
Пробки бочек допускается отвинчивать и завинчивать только инструментами
из мягкого металла, не дающими искр при ударе или деревянным молотком. При
откатке бочек и загрузке их в хранилище необходимо соблюдать осторожность,
чтобы избежать ударов по бочке и образования искр. Пролитая на пол жидкость
должна быть немедленно убрана.
Отдельные легковоспламеняющиеся жидкости (спирт, эфир медицинский и др.)
обладают свойствами образовывать при хранении статическое электричество, искра
которого может вызвать воспламенение жидкости. Поэтому фасовку таких жидкостей
на складе следует производить в отдельных помещениях, оборудованных средствами
пожарной защиты. При их сливе и фасовке металлические сосуды должны иметь
заземление.
Тару, освобожденную от легковоспламеняющихся жидкостей, следует оставить
на некоторое время открытой.
Хранение взрывоопасных веществ
К этой группе веществ относятся взрывчатые вещества и вещества
взрывоопасные, то есть способные к образованию взрывчатых смесей (Приложение к
данной инструкции).
Вещества этой группы должны храниться в отдельно стоящем складском здании,
отвечающим требованиям п. 2.3. настоящей инструкции. Хранение серебра нитрата в
аптеках и на складах в небольших количествах (на складах до 5 кг, в аптеках до
50 г) необходимо осуществлять изолированно в соответствии с правилами хранения
ядовитых веществ.
При хранении взрывоопасных веществ следует принимать меры против
загрязнения их пылью, которая может служить причиной взрыва.
Емкости с взрывоопасными веществами (штангласы, жестяные барабаны,
склянки и т.п.) необходимо плотно закрывать во избежании попадания паров этих
веществ в воздух.
Калия перманганат при взаимодействии с пылью, серой, органическими
маслами, эфирами, спиртом, глицерином, органическими кислотами и другими
органическими веществами - взрывоопасен. Хранить его на складах следует в специальном
отсеке в жестяных барабанах, а в аптеках - в штангласах с притертыми пробками
отдельно от указанных выше средств. Не допускается совместное хранение с
легковоспламеняющимися и горючими веществами. Жестяные барабаны и штангласы с
калия перманганатом своевременно освобождают от пыли осторожно, избегая трения.
Раствор нитроглицерина (относится к взрывчатым веществам) следует хранить
в аптеках или аптечных складах в небольших хорошо укупоренных склянках или
металлических сосудах в прохладном темном месте с соблюдением мер
предосторожности от огня. Передвигать посуду с нитроглицерином и отвешивать
этот препарат следует с особой осторожностью, так как испарение пролитого
нитроглицерина угрожает взрывом. Попадание даже малых количеств на кожу может
вызвать отравление (сильные головные боли).
При работе с диэтиловым эфиром не допускается встряхивание, удары, трения
и т.п.
Категорически запрещается хранение всех взрывоопасных и огнеопасных
веществ с кислотами и щелочами.
Переноска баллонов с огнеопасными и легковоспламеняющимися жидкостями
должна производиться вдвоем в специально приспособленных клетях или корзинах с
исправными ручками захвата. Корзины с большими бутылями, ящики или клети (свыше
20 кг), а также вещества, помещенные в твердую тару, переносить (перемещать)
необходимо только на специальных тележках с мягким ходом колес.
При хранении азотной и серной кислот должны быть приняты меры к
недопущению соприкосновения их с древесиной, соломой и прочими веществами
органического происхождения.
В помещении хранения взрывоопасных и огнеопасных веществ категорически
запрещается входить с керосиновыми лампами и свечами, следует пользоваться
только электрофонарями.
ХРАНЕНИЕ И ОБРАЩЕНИЕ С КИСЛОРОДНЫМИ БАЛЛОНАМИ
Хранение и обращение с кислородными баллонами должно осуществляться в
строгом соответствии с Правилами устройства и безопасной эксплуатации сосудов,
работающих под давлением, утвержденными Госгортехнадзором.
.Определение концентрации этилового спирта. Спиртометром, с
использованием рефрактометрии, с помощью алкоголеметрических таблиц.
Этано́л (эти́ловый
спирт, метилкарбино́л, ви́нный
спирт или алкого́ль, часто в просторечии просто «спирт») - одноатомный
спирт с формулой
<#"818401.files/image005.gif">
В водных растворах этилового спирта линейная зависимость показателя
преломления от концентрации наблюдается до концентрации спирта 60-80%. При этом
показатель преломления увеличивается значительно. В пределах концентрации 80 -
90 % показатель преломления не изменяется, а при концентрации 90-96 %
становится отрицательным. Таким образом, определение содержания спирта в
анализируемых смесях в определяемых смесях в пределах концентрации 80 - 96%
возможно после их разбавления в 3 , 4 раза.
Немаловажное значение имеет температура, при которой проводят
определение. При расчетах следует видеть температурную поправку.
Концентрацию спирта определяют обязательно при 20˚С спиртометром
(АСП 95- 105, АСП-2 96-101, спиртометром с термометром АСПТ 60-100% или
денсиметром N16 0,76-0,82). Фармакопейными способами определения концентрации
водно-спиртовых растворов являются: по плотности и температуре кипения.
Плотность водно-спиртовых растворов находится в интервале от 0,78929
(абсолютный спирт) до 0,99823 (вода). Определяется плотность при стандартной
температуре (200С). Существует прямая зависимость между плотностью
спирто-водного раствора и его концентрацией. Плотность спирто-водного раствора
может быть определена ареометром, пикнометром. Шкала ареометров градуирована
при температуре 200С. Можно измерить плотность и при другой температуре. Но в
этом случае концентрацию спирта определяется по специальным таблицам (№ 1, № 2
комитета стандартов, мер и измерительных приборов - табл. ГОСТ).
Разновидностью ареометров являются спиртомеры. Используются стеклянные
спиртомеры типа А (ГОСТ 3639-61). Определение концентрации спирта в растворах
производят в интервале температур от +400С до -250С. Результат определения
обязательно приводят к температуре +200С. По методике ГФ Х1 (с. 24) проводят
определение плотности с помощью пикнометров. Плотность рассчитывают по формуле:
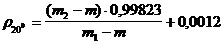
r200 - плотность в г/см2
m -
масса пустого пикнометра, г
m1 -
масса воды очищенной с пикнометром, г
m2 -
масса спирто-водного раствора с пикнометром, г
,0012 - плотность воздуха при 200С и барометрическом давлении (1013 гПа =
760 мм рт.ст.).
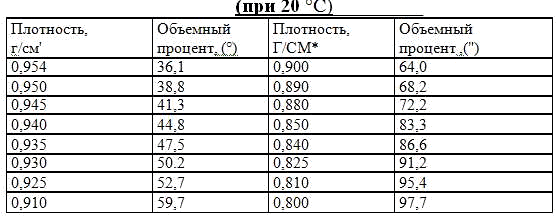
При работе со спиртом в условиях аптеки приходится производить различные
расчеты. Для этих целей используют алкаголеметрические таблицы, которые
приведены в ГФ Х1 (М., 1987, с.303-321). Их в Фармакопее дано 5.
Пользуясь таблицей № 1 можно:
1 Определить крепость водно-спиртового
раствора по массе и объему по известной плотности.
2 Определить количество абсолютного
спирта в граммах в 100 мл спиртового раствора.
3 Определить количество абсолютного
спирта в миллилитрах в 100 г водно-спиртовой смеси.
4 Определить плотность водно-спиртового
раствора по известной крепости спирта.
Пример 1. Определить крепость водно-спиртового раствора по массе и
объему, если плотность раствора равна 0,8880. По табл. 1 (с.309) находим
концентрацию водно-спиртового раствора по массе 61,33% и по объему 69%.
Пример 2. Определить количество абсолютного спирта в граммах в 1000 мл
водно-спиртового раствора крепостью 96,5%. По табл. 1 (с.313) находим:
в 100 мл содержится 73,16 г абсолютного спирта
в 1000 мл 731,6 г абсолютного спирта.
Пример 3. Определить количество абсолютного (безводного) спирта в
миллилитрах в 500 г водно-спиртового раствора крепостью 90,55%. По табл. 1 (с.
312) находим:
в 100 г содержится 109,58 мл абсолютного спирта
в 500 г 547,9 мл абсолютного спирта
Таблица № 2. ГФ Х1, Т.1, С.315.
Применяется таблица для расчета количества спирта определенной крепости и
воды, которое нужно смешать, чтобы получить 1 кг водно-спиртового раствора
нужной концентрации. Исходная концентрация спирта от 96 до 32% , с интервалом в
1%; слабые концентрации ограничены 92-30%, с интервалом 10%.
Пример: Приготовить 1 кг спирто-водного раствора 70% из 90%. Рассчитать
количество крепкого спирта и воды. По табл. 2 находим: 728 г 90% 272 г воды.
Табл. 3. ГФ Х1, Т.1, с.318. Согласно данной таблице находится количество
воды в объемных единицах (мл), которые следует добавить к 1000 объемам (мл)
спирта (от 35% до 95% с интервалом 5%), чтобы получить спирт различной крепости
от 30% до 90% (интервал 5%). Объем получаемого спирта не определяется.
Пример: Сколько нужно добавить воды к 1 л 70%, чтобы получить 40% спирт.
По таблице находим 774 мл воды следует добавить к 1000 мл 70% спирта.
Табл. 4 (ГФ Х1, Т.1, с. 319) Указывает количество спирта в миллилитрах
различной крепости (от 95% до 35%) и воды, которые необходимо смешать, чтобы
получить 1 л спирта крепостью от 35% до 90% с интервалом в 5%. По своему
строению данная таблица аналогична табл. 2.
Табл. 5 (ГФ Х1, Т.1, с.320-321). Указывает количество в миллилитрах
спирта различной крепости (от 95,1% до 96,5%) с интервалом 0,1% и воды, которые
следует смешать, чтобы получить 1 л спирта крепостью от 30% до 95% с интервалом
в 5%. Количество разводимого спирта в таблице даны с точностью до 0,1.
Пример: Сколько миллилитров нужно взять спирта 95,9% и воды, чтобы
получить 1 л 60% спирта. По таблице находим: 625,7 мл спирта 404,4 мл воды.