Расчет ректификационной установки
ВВЕДЕНИЕ
Колонные ректификационные аппараты и установки являются важнейшим
массообменным оборудованием химических, нефтехимических и других смежных
отраслей промышленности. Наибольшее распространение в процессах ректификации
получили тарельчатые и насадочные аппараты.
Ректификацией называется процесс разделения однородных гомогенных смесей
на составляющие вещества или группы составляющих веществ путем взаимодействия
пара и жидкости, не находящихся в термодинамическом равновесии. При
взаимодействии пара и жидкости компоненты перераспределяются между фазами: пар
обогащается легколетучим компонентом или низкокипящим (НК), а жидкость -
высококипящим компонентом (ВК).
В основе любого метода расчета лежит ряд исходных допущений, упрощающих
расчетную процедуру. При расчете ректификационной установки принимаем следующие
допущения:
1. Состав жидкости, стекающий в куб колонны, равен составу пара,
поднимающегося из кипятильника в колонну (xw = yw).
2. Состав пара, поступающего из колонны в дефлегматор, равен составу
жидкости, стекающей из дефлегматора в колонну (yp = xp).
. Скрытые мольные теплоты парообразования компонентов смеси равны,
а это значит, что один кмоль сконденсировавшегося пара испаряет один кмоль
жидкости, вследствие чего, количество пара, поднимающегося по колонне, не
меняется.
. Исходная смесь поступает в колонну при температуре кипения.
Связь между равновесными концентрациями жидкости и пара для идеальных
растворов устанавливается на основании законов Рауля и Дальтона. На основании
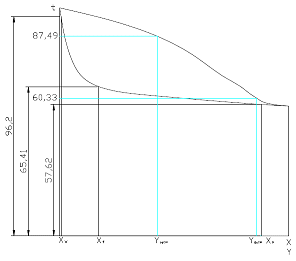
данных по равновесию могут быть построены графики: 1) кривая равновесия у-х; 2)
изобара температур кипения и конденсации t - x, y.
Задание
Производительность по исходной смеси - 4 т/ч;
Концентрация ацетона:
в исходной смеси - aF =
40% (масс.),
в дистилляте - aР =
96% (масс.),
в кубовом остатке - aW =
1,8% (масс.).
Температура:
охлаждающей воды - 12 °С,
дистиллята после холодильника - 24 °С,
кубового остатка после холодильника - 28 °С,
исходной смеси - 20 °С.
Давление насыщенного водяного пара - 6,0 кгс/см2,
Коэффициент избытка флегмы - 1,55.
Колонна работает под атмосферным давлением.
Исходная смесь и флегма вводятся в аппарат при температуре кипения.
Расчет проводится в следующей последовательности.
1. Определение производительности по дистилляту и кубовому остатку
Производительность колонны по дистилляту определяем по формуле:
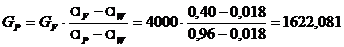 кг/ч =
0,45 кг/с.
кг/ч =
0,45 кг/с.
Производительность
колонны по дистилляту определяем из уравнения:
GW = GF - GP =
4000 - 1622,081 = 2377,919кг/ч = 0.66 кг/с.
Проверка:
.
0,4 = 1622,081. 0,96 + 2377,919. 0,018
=
1557,197 + 42,803
=1600
2. Определение минимального и действительного флегмового числа
Пересчитываем массовые концентрации в мольные по формуле:

где
Х - концентрация низкокипящего компонента А (ацетона) в бинарной смеси, мол.
доли;
а
- содержание низкокипящего компонента А (ацетона) в бинарной смеси, масс. доли;
МА,
МВ - молярная масса компонента А (ацетона) и В (вода) (соответственно).
Молярные
массы: ацетон - 58 кг/кмоль.
вода
- 18 кг/кмоль.
Тогда
концентрация исходной смеси:
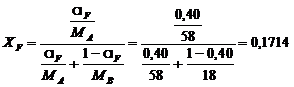 ;
;
дистиллята:
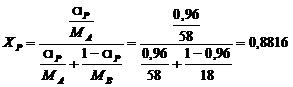 ;
;
кубового
остатка:
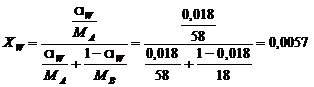 .
.
Минимальное
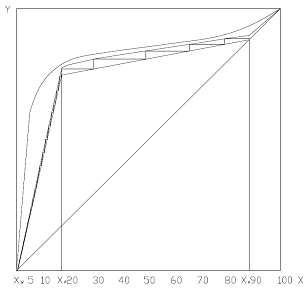
флегмовое число определяем графо-аналитическим способом. Для этого на основании
опытных данных [7, 8], в координатах у-х строим кривую равновесия для смеси
ацетон-вода при атмосферном давлении и кривую температур кипения и конденсации.
На
диаграмме у-х из точки 1 (хр = ур) через точку 2′ (хF, уF*)
проводим прямую линию до пересечения с осью у. Отрезок, отсекаемый на оси у,
обозначим через Вmax = 0,78. По величине этого отрезка находим минимальное
флегмовое число
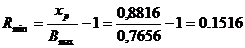 .
.
Равновесные
данные для смеси ацетон-вода
|
Содержание компонента А,
мол. %
|
Температура кипения, t,
°С
|
|
в жидкости (х)
|
в паре (у)
|
|
|
0
|
0,0
|
100
|
|
5
|
60,3
|
77,9
|
|
10
|
72
|
69,6
|
|
20
|
80,3
|
64,5
|
|
30
|
82,7
|
62,6
|
|
40
|
84,2
|
61,6
|
|
50
|
85,5
|
60,7
|
|
60
|
86,9
|
59,8
|
|
70
|
88,2
|
59
|
|
80
|
90,4
|
58,2
|
|
90
|
94,3
|
57,5
|
|
100
|
100,0
|
56,9
|
Действительное флегмовое число определяем, используя уравнение:
R = KR . Rmin = 1,55 . 0.1516= 0.2349
На
диаграмме у-х наносим линии рабочих концентраций (рабочие линии) для
оптимального флегмового числа R = 0,2349: для этого на оси у откладываем отрезок 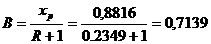 , конец которого соединяем прямой с точкой 1 (хр =
ур); точку пересечения этой прямой с вертикальной линией, проведенной с
абсциссы хF, обозначим точкой 2 (хF, уF) и,
наконец, точку 2 соединяем с точкой 3 (хW = уW).
Линии 1-2 и 2-3 являются рабочими линиями для верхней и нижней частей колонны,
соответственно.
, конец которого соединяем прямой с точкой 1 (хр =
ур); точку пересечения этой прямой с вертикальной линией, проведенной с
абсциссы хF, обозначим точкой 2 (хF, уF) и,
наконец, точку 2 соединяем с точкой 3 (хW = уW).
Линии 1-2 и 2-3 являются рабочими линиями для верхней и нижней частей колонны,
соответственно.
3.
Определение средних значений параметров по колонне, физико-химических и термодинамических
констант фаз
Жидкая фаза.
Средняя мольная концентрация в нижней части колонны:
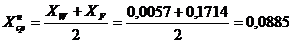 .
.
Средняя
мольная концентрация в верхней части колонны:
 .
.
Средняя
мольная концентрация по колонне:
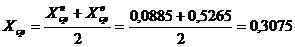 .
.
Средняя
массовая концентрация по колонне:
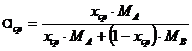
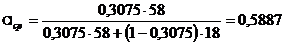 .
.
Средняя
температура в нижней части колонны:
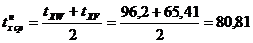 °С.
°С.
Средняя
температура в верхней части колонны:
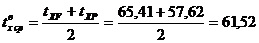 °С.
°С.
Средняя
температура по колонне:
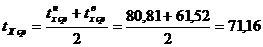 °С.
°С.
Значения
tXW, tXF, tXР взяты из диаграммы t - x, y .
Средняя
мольная масса
Мх
ср = МА . Хср + МВ . (1 - Хср),
Мх ср = 58 . 0,3075 + 18 . (1 - 0,3075) = 30,301 кг/кмоль.
Средняя плотность определяется по формуле:
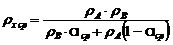
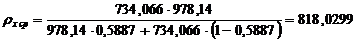 кг/м3.
кг/м3.
где
ρА и ρВ -
плотность компонентов А (ацетона) и В (воды) при температуре tx cp.
ρА = 734,066 кг/м3 при tx cp = 71,16 °С [1, с. 512];
Приложение Б.
ρВ = 978,14 кг/м3.
Среднюю
вязкость рассчитываем по уравнению:
lg μх ср =
Хср . lg μА + (1 - Хср) . lg μB,
где
μА и μВ -
динамические коэффициенты вязкости компонентов А (ацетона) и В (воды), Па.с.
μА = 0,217 МПа . с при tcp = 71,16 °С [1, с. 516]; Приложение Б.
μВ = 0,419 МПа . с.
lg μх ср = 0,3075 . lg 0,217 + (1 -
0,3075) . lg 0,419 = -0,46547
μх ср = 0,342 МПа . с = 0,342 . 10-3 Па . с.
Среднее
поверхностное натяжение определяем по уравнению
σх ср = σА . Хср + σB . (1 -
Хср),
где
σА и σB - поверхностные натяжения компонентов А (ацетон) и В (вода), н/м.
σА = 17,54 . 10-3 н/м при tх cp =
71,16 °С [1, с. 526]:
σВ = 64,61 . 10-3 н/м.
σх ср = 17,54 . 10-3 . 0,3075 + 64,61 . 10-3 (1 -
0,3075) = 50,13 . 10-3 н/м.
Коэффициент
диффузии при средней температуре определяем [1]:
Dx (t) = Dx
(20) [1 + b . (t - 20)],
где
Dx (20) - коэффициент диффузии при t =
20 °С, м2/с;
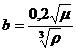
здесь
μ
[мПа . с] и ρ [кг/м3] - вязкость и плотность растворителя (воды) при t =
20 °С; t = tх cp.
Коэффициент
диффузии при 20 °С рассчитываем по эмпирическому уравнению [1]:
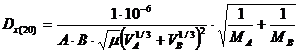
где
VA и VB - мольные объемы компонентов А (ацетона) и В (воды),
см3/моль;
А,
В - коэффициенты, зависящие от свойств компонентов, А= 1,0; В = 4,7 [1, с.
269]:
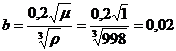 .
.
Мольные
объемы компонентов [1, с. 288]:
VA = 14,8∙3+6∙3,7+7,4
= 74 см3/моль;
VB = 18,9
см3/моль.
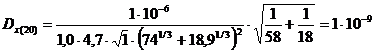 м2/с.
м2/с.
Dx (t) =
1 . 10-9 [1 + 0,02 (71,16 - 20)] = 2 . 10-9 м2/с.
Паровая
фаза.
Средняя
мольная концентрация в нижней части колонны:
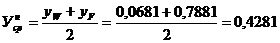 .
.
Средняя
мольная концентрация в верхней части колонны:
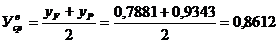 .
.
Средняя
мольная концентрация по колонне:
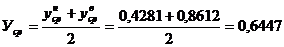 .
.
Средняя
температура в нижней части колонны: 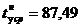 °С.
°С.
Средняя
температура в верхней части колонны: 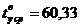 °С.
°С.
Температуры
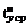 ,
,  найдены
из диаграммы t - x, y .
найдены
из диаграммы t - x, y .
Средняя
температура по колонне:
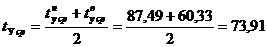 °С.
°С.
Средняя
мольная масса
Му
ср = МА . уср + МВ . (1 - уср) = 58 . 0,6447 + 18 . (1 - 0,6447) =
=
43,786 кг/кмоль.
Средняя
плотность:
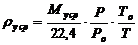
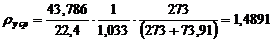 кг/м3.
кг/м3.
здесь
Т = 273 + tу ср, °С; Р = 1 кгс/см2 (давление в колонне
атмосферное).
Средняя
вязкость [1]:
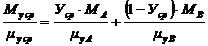
где
μуА и μуВ -
динамический коэффициент вязкости паров компонента А (ацетон) и В (вода).
μуА = 0,95 . 10-5 Па.с при tу cp = 73,91 °С [9, с. 8, 9]:
μуВ = 1,23 . 10-5 Па.с.
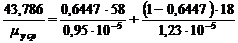 ,
,
μу ср = 0,982 . 10-5 Па . с.
Коэффициент
диффузии для паровой фазы определяем по уравнению [1]:
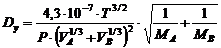
где
Р - давление кгс/см2 (давление в колонне атмосферное);
Т
= 273 + tу ср, °С. 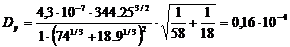 м2/с.
м2/с.
4. Определение диаметра колонны
Диаметр колонны определяем по уравнению [1]:
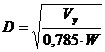
Расход, проходящего по колонне пара, может быть определен:
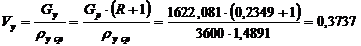 м3/с.
м3/с.
Скорость
пара в колонне определяем по уравнению (2.9). Предварительно принимаем
расстояние между тарелками h = 300 мм. Используем ранее найденные ρх cp = 818,0299 кг/м3 и ρу cp = 1,4891 кг/м3. Для колпачковых тарелок С = 0,032.
Тогда скорость пара в колонне:
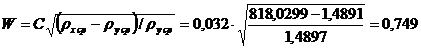 м/с.
м/с.
Тогда
диаметр колонны
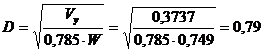 м.
м.
Принимаем
стандартное значение диаметра колонны D = 0,8 м (см. Приложение В) и
уточняем скорость пара в колонне:
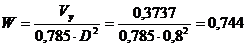 м/с.
м/с.
5. Определение высоты колонны
По уравнению находим коэффициент массоотдачи в жидкой фазе:
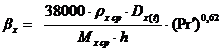 .
.
где
ρх ср - средняя плотность жидкой фазы, кг/м3;
Dх(t) -
коэффициент диффузии при средней температуре жидкости, м2/с;
Мх
ср - средняя молекулярная масса жидкости, кг/кмоль;
h - линейный
размер, h = 1 м;
 -
диффузионный критерий Прандтля, равный
-
диффузионный критерий Прандтля, равный
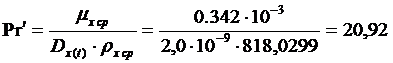 ;
;
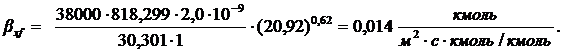
Коэффициент
массоотдачи в паровой фазе находим по уравнению (2.19):
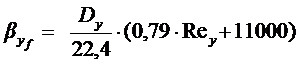
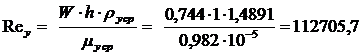 .
.
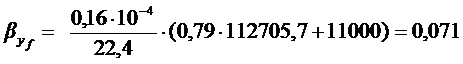
Общий
коэффициент массопередачи Kyf находим из уравнения (2.17):
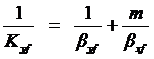 ,
,
где
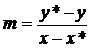 - тангенс угла наклона линии равновесия;
- тангенс угла наклона линии равновесия;
у*,
х* - равновесные концентрации.
Так
как величина m является переменной по высоте колонны, находим ее
значение для различных концентраций, используя диаграмму (рис. 1)
В
пределах от Хw до Хр выбираем ряд значений Х, для каждого значения Х
определяем по диаграмме (рис. 1) величины у* - у, х - х* как разность между
равновесной и рабочей линией, а затем по этим значением определяем величину m.
Результаты сводим в таблицу 3.2.
Определение
коэффициента массопередачи
|
х
|
0,0057
|
0,1
|
0,2
|
0,3
|
0,4
|
0,5
|
0,6
|
0,7
|
0,8
|
0,8816
|
|
у*- у
|
0,0631
|
0,2942
|
0,0509
|
0,0561
|
0,052
|
0,046
|
0,041
|
0,035
|
0,0379
|
0,0527
|
|
х -х*
|
0,0141
|
0,0659
|
0,2676
|
0,2972
|
0,2736
|
0,2419
|
0,2156
|
0,1825
|
0,1068
|
0,0527
|
|
m
|
4,4752
|
4,4634
|
0,1902
|
0,1888
|
0,1901
|
0,1902
|
0,1902
|
0,1919
|
0,3549
|
1,000
|
|
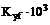 2,993,0036,1436,2736,1536,1436,1435,9925,3611,69 2,993,0036,1436,2736,1536,1436,1435,9925,3611,69
|
|
|
|
|
|
|
|
|
|
|
Для построения кинетической кривой воспользуемся формулой:
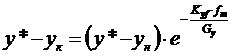 .
.
Значения
разности (у* - ун) это значения АС = (у* - у) для каждого выбранного значения х
в пределах от хw до хр.
Рабочая
площадь тарелки может быть найдена из Приложения В, таблица В.1: Fp =
0,395 м2.
Мольный
расход пара по колонне:
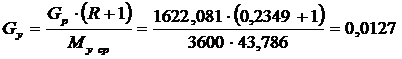 кмоль/с.
кмоль/с.
По
данным таблицы 3.3 строим кинетическую кривую. Точки А1, А2, А3, …, А10 лежат
на рабочих линиях, точки С1, С2, С3, …, С10 - на равновесной кривой.
Вычисленные отрезки В1С1, В2С2, В3С3, …, В10С10 откладываются от
соответствующих точек С вниз. Кинетическая кривая начинается в начале
координат, проходит через точки В1, В2, В3,…, В10 и заканчивается в правом
верхнем углу диаграммы у-х (рис. 3.3).
Число
действительных тарелок, которое обеспечивает заданную четкость разделения,
определяется путем построения "ступенек" между рабочими и
кинетической линиями. Число ступеней в пределах концентраций XW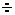 XP равно числу действительных тарелок.
XP равно числу действительных тарелок.
К
построению кинетической кривой
|
х
|
0,0057
|
0,1
|
0,2
|
0,3
|
0,4
|
0,5
|
0,6
|
0,7
|
0,8
|
0,8816
|
|
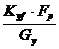 0,09 0,09
|
0,09
|
1,12
|
1,13
|
1,12
|
1,12
|
1,12
|
1,12
|
0,79
|
0,36
|
|
|
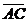 , мм6,31 , мм6,31
|
29,42
|
5,09
|
5,61
|
5,20
|
4,60
|
4,10
|
3,50
|
3,79
|
5,27
|
|
|
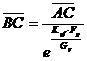 , мм5,74 , мм5,74
|
26,78
|
1,66
|
1,82
|
1,69
|
1,50
|
1,33
|
1,14
|
1,72
|
3,66
|
|
В результате построения (рис. 3.3) получаем число действительных тарелок n= 50, тарелка питания 46-я снизу.
Высоту колонны определяем по уравнению (2.10)
H = (n - 1) . h + Hсеп +
Hкуб = (50 - 1) . 0,3 + 0,8 + 2,0 =
17,5 м.
6. Определение гидравлического сопротивлении
колонны с колпачковыми тарелками
Полное гидравлическое сопротивление колонны определяем по уравнению
(2.20), а гидравлическое сопротивление тарелки - по уравнению (2.22).
По таблице В.2 Приложения выбираем тарелку типа ТСК-1 для колонны
диаметром D = 800 мм. Эта тарелка имеет следующие параметры:
рабочая площадь тарелки Fp = 0,395 м2;
площадь прохода паров Fо = 0,049 м2;
площадь слива Fсл = 0,021 м2;
периметр слива П = 0,57 м;
длина пути слива lx = 0,52 м;
количество колпачков на тарелке m = 24;
диаметр колпачка 80 мм.
Сопротивление сухой тарелки:
 Па;
Па;
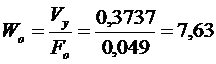 м/с,
м/с,
где
Fo - площадь прохода паров, м2.
Глубина
барботажа, согласно уравнению (2.29):
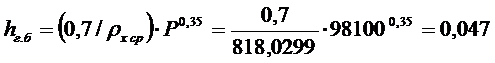 м.
м.
Высота
подпора жидкости над сливным порогом по уравнению (2.33):
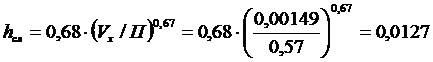 м,
м,
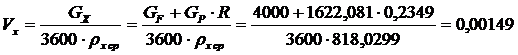 м3/с;
м3/с;
П
= 0,578 м (из характеристики тарелки).
Для
дальнейших расчетов примем колпачок капсульный с прямоугольными прорезями
шириной b = 4 мм; количество прорезей в одном колпачке z = 20 (см. Приложение,
таблицы В.4, В.5). Высоту открытия прорези рассчитываем по уравнению (2.30):
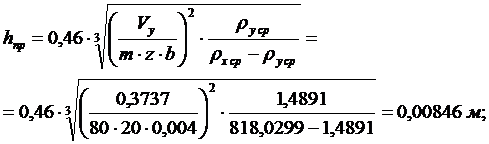
принимаем
по таблице В.4 высоту прорези hпр = 20 мм.
Высоту
установки колпачка примем hу = 10 мм.
Высоту
сливного порога найдем по уравнению (2.31)
hпор
= hг.б - hсл + hпр + hу = 0,047 - 0,0127 + 0,020 + 0,01 = 0,064 м.
Тогда
величина перепада уровня жидкости на тарелке (по уравнению 2.28)
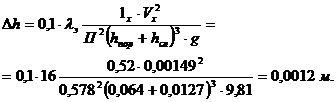
Сопротивление
слоя жидкости на тарелке, согласно уравнению (2.27):
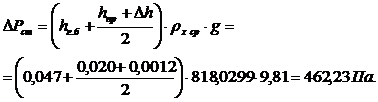
Тогда
гидравлическое сопротивление тарелки (пренебрегая ΔРσ)
ΔРт = ΔРсух + ΔРст = 195,05 + 462,23 = 657,28 Па,
а
гидравлическое сопротивление колонны
ΔРк = n ∙
ΔРт = 50 ∙ 657,28 = 32864 Па.
Проверим
ранее принятое расстояние между тарелками h = 0,3 м. Для этого необходимо
рассчитать величину относительного уноса жидкости.
Высота
пены, образующейся на тарелке, согласно уравнению (2.35):
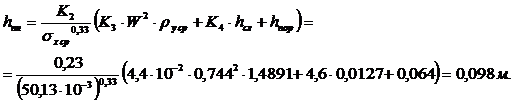
Тогда
величина относительного уноса жидкости (уравнение 2.34)

,0245
< 0,1, следовательно, расстояние между тарелками выбрано верно.
Значение
коэффициентов К1, К2, К3, К4 и показателя степени n взяты из таблицы В.6
Приложения.
7. Определение диаметра штуцеров
Диаметр штуцера определяем по уравнению:
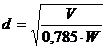
Штуцер
подачи флегмы:
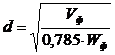 ,
,
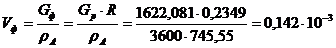 м3/с.
м3/с.
Принимаем
Wф = 0,5 м/с, тогда
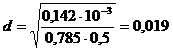 м.
м.
Стандартный
размер трубы для изготовления штуцера Ø20х4 мм, [6, с. 16].
Штуцер
подачи исходной смеси:
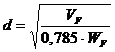 ,
,
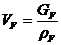 ;
; 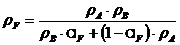 ,
,
при
tXF = 65,41 °С
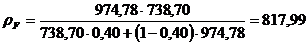 кг/м3,
кг/м3,
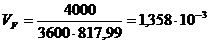 м3/с.
м3/с.
Принимаем
WF = 0,8 м/с, тогда
ректификационный колонна
термодинамический
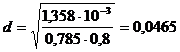 м.
м.
Стандартный
размер трубы для изготовления штуцера Ø48х4 мм, [6, с. 17].
Штуцер
выхода кубового остатка:
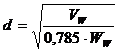 ,
,
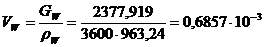 м3/с.
м3/с.
ρВ = 963,24 кг/м3 - плотность воды при 87,49°С.
Принимаем
WW = 0,3 м/с, тогда
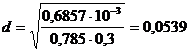 м.
м.
Стандартный
размер трубы для изготовления штуцера Ø56х3,5 мм, [6, с. 16].
Штуцер
выхода кубовой жидкости (подается на кипятильник):
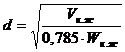 ,
,
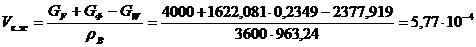 м3/с.
м3/с.
Принимаем
Wк.ж = 0,3 м/с, тогда
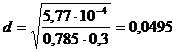 м.
м.
Стандартный
размер трубы для изготовления штуцера Ø56х3,5 мм, [6, с. 17].
Штуцер
выхода паров из колонны:
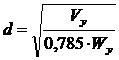 ,
,
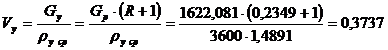 м3/с.
м3/с.
Принимаем
Wу = 15 м/с, тогда
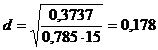 м.
м.
Стандартный
размер трубы для изготовления штуцера Ø194х6 мм, [6, с. 17].
8. Тепловые расчеты
Подогреватель
исходной смеси
Уравнение теплового баланса для подогревателя:
Q = 1,05 . GF . 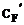 . (tXF - tнач) = Gг.п . r,
. (tXF - tнач) = Gг.п . r,
здесь тепловые потери приняты в размере 5% от полезно затрачиваемой
теплоты;
tXF -
температура кипения исходной смеси;
tнач -
начальная температура (задана).
Удельная теплоемкость исходной смеси
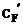 = аF .
СА + (1 - аF) . СВ,
= аF .
СА + (1 - аF) . СВ,
где
СА, СВ - удельные теплоемкости ацетона и воды при средней температуре
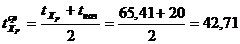 °С;
°С;
СА
= 0,5369 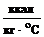 ; СВ = 0,9983
; СВ = 0,9983 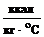 , [1, с.
562]; таблица Б.7 Приложения.
, [1, с.
562]; таблица Б.7 Приложения.
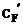 = 0,40 .
0,5369 + (1 - 0,40) . 0,9983 = 0,809
= 0,40 .
0,5369 + (1 - 0,40) . 0,9983 = 0,809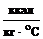 =
3390,238
=
3390,238 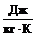 .
.
Q = 1,05 . GF . 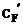 (tXF - tнач) = 1,05 .
(tXF - tнач) = 1,05 .  .
3390,238 (71,16 - 20) =
.
3390,238 (71,16 - 20) =
=202352
Вт.
Расход греющего пара:
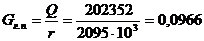 кг/с,
кг/с,
r = 2095 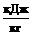 при Р = 6,0 кгс/см2 [1, c. 550]:
при Р = 6,0 кгс/см2 [1, c. 550]:
Температура
насыщенного водяного пара при Р = 5,8 кгс/см2 составляет 156,7°С [1, c.
550]:
Большая
разность температур:
Δtб = 158,1 - 20
= 138,1 °С;
меньшая
разность температур:
Δtм = 158,1 - 65,41 = 92,69°С.
Так
как 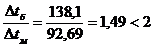 , тогда среднюю разность температур определяем по
уравнению:
, тогда среднюю разность температур определяем по
уравнению:
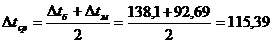 °С.
°С.
Коэффициент
теплопередачи принимаем ориентировочно равным 300Вт/м2.К [6, с. 47].
Поверхность
теплообмена подогревателя исходной смеси
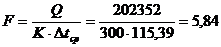 м2.
м2.
Принимаем
одноходовой кожухотрубчатый теплообменник со следующими характеристиками [6, с.
51]:
- диаметр кожуха 325 мм;
- труба 20х2 мм;
количество труб в теплообменнике 100 шт;
длина труб 1,5 м;
поверхность теплообмена 9,5 м2.
Дефлегматор
(конденсатор)
Расход теплоты, отдаваемый охлаждающей воде при конденсации паров в
дефлегматоре, определяется из уравнения теплового баланса дефлегматора:
QД = GР . (R + 1) . rР = GВ . CВ . (tк - tн),
rР =
аР . rА + (1 - аР) . rВ.
Удельные теплоты парообразования ацетона rА и воды rВ при
tХр=57,62 °С:
rА = 521,275 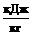 ; rВ = 2363,395
; rВ = 2363,395 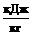 , [1, с.
541-542]:
, [1, с.
541-542]:
rР = 0,96 .
521,275 + (1 - 0,96) . 2363,395 = 594,95 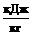 .
.
QД = 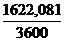 . (0,2349+ 1) . 594,95 .103 = 331041,39 Вт.
. (0,2349+ 1) . 594,95 .103 = 331041,39 Вт.
Принимаем
температуру охлаждающей воды на выходе из дефлегматора 25°С, тогда расход
охлаждающей воды
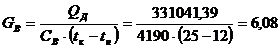 кг/с.
кг/с.
Большая
разность температур:
Δtб = 57,62 - 25
= 32,62°С;
меньшая
разность температур:
Δtм = 23 - 12 = 11 °С.
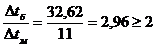 , то
, то
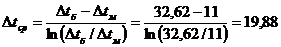 °С.
°С.
Принимаем
ориентировочно коэффициент теплопередачи К = 500 Вт/м2 . К [6, с. 47].
Поверхность
теплообмена дефлегматора:
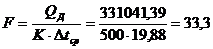 м2.
м2.
Принимаем
четырехходовой кожухотрубчатый теплообменник со следующими характеристиками [6,
с. 51]:
- диаметр кожуха 400 мм;
- труба 20х2 мм;
количество труб в теплообменнике 181 шт;
длина труб 3 м;
поверхность теплообмена 34 м2.
Холодильники
дистиллята и кубового остатка
Расход теплоты, отдаваемый охлаждающей воде в водяном холодильнике
дистиллята, определяется из уравнения теплового баланса:
Q = GР . 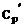 . (tХр - tр кон) = GВ . CВ . (tк - tн),
. (tХр - tр кон) = GВ . CВ . (tк - tн),
где
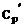 - теплоемкость дистиллята при его средней температуре
(tХр + tр кон)/2;
- теплоемкость дистиллята при его средней температуре
(tХр + tр кон)/2;
tр кон -
конечная температура дистиллята после холодильника, °С (по условию задания).
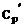 = аР .
СА + (1 - аР) . СВ,
= аР .
СА + (1 - аР) . СВ,
СА
= 0,5388 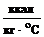 ; СВ = 0,9985
; СВ = 0,9985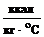 , при
средней температуре
, при
средней температуре 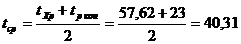 °С; [1, с. 562]:
°С; [1, с. 562]:
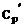 = 0,96 .
0,5388 + (1 - 0,96) . 0,9985 = 0,56638
= 0,96 .
0,5388 + (1 - 0,96) . 0,9985 = 0,56638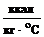 =
2373,141
=
2373,141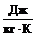 .
.
Q = GР . 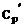 . (tXр - tр кон) =
. (tXр - tр кон) = 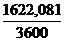 .
2373,141 (57,62 - 23) = 37018,66 Вт.
.
2373,141 (57,62 - 23) = 37018,66 Вт.
Расход охлаждающей воды при нагревании ее на 15 °С в холодильнике
товарного дистиллята:
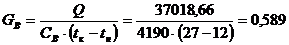 кг/с.
кг/с.
Большая
разность температур:
Δtб = 57,32 - 27
= 30,32 °С;
меньшая
разность температур:
Δtм = 23 - 12 = 11 °С.
Так
как 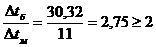 , то среднюю разность температур определяем
, то среднюю разность температур определяем
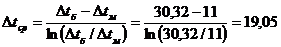 °С.
°С.
При
ориентировочном значении К = 400 Вт/м2 . К поверхность теплообмена холодильника
товарного дистиллята составит
 м2.
м2.
Принимаем
одноходовой кожухотрубчатый теплообменник со следующими характеристиками [6, с.
51]:
- диаметр кожуха 273
мм;
- труба 25х2
мм;
количество труб в теплообменнике 37 шт;
длина труб 2 м;
поверхность теплообмена 6 м2.
Расход теплоты, отдаваемый охлаждающей воде в водяном холодильнике
кубового остатка, определяется из уравнения теплового баланса:
Q = Gw . 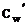 . (tХw - tw кон) = GВ . CВ . (tк - tн),
. (tХw - tw кон) = GВ . CВ . (tк - tн),
где
СW - теплоемкость кубового остатка при его средней
температуре (tХw + tW кон)/2;
tW кон -
конечная температура кубового остатка после холодильника, °С (по условию
задания).
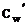 = аw .
СА + (1 - аw) . СВ,
= аw .
СА + (1 - аw) . СВ,
СА
= 0,5532 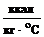 ; СВ = 1,0
; СВ = 1,0 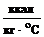 , при
средней температуре
, при
средней температуре 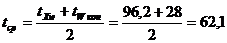 °С; [1, с. 562]:
°С; [1, с. 562]:
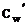 = 0,01 .
0,5532 + (1 - 0,01) . 1,0 = 0,996
= 0,01 .
0,5532 + (1 - 0,01) . 1,0 = 0,996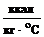 =
4171,279
=
4171,279 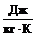 .
.
Q = Gw . 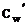 . (tXw - tW кон) =
. (tXw - tW кон) = 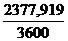 .
4171,279 (96,2- 28) =
.
4171,279 (96,2- 28) =
=187909,25
Вт.
Расход охлаждающей воды при нагревании ее на 15 °С в холодильнике
кубового остатка:
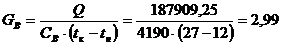 кг/с.
кг/с.
Большая
разность температур:
Δtб = 96,2 - 27 =
69,2 °С;
меньшая
разность температур:
Δtм = 28 - 12 = 16 °С.
Так
как 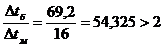 , то среднюю разность температур определяем
, то среднюю разность температур определяем
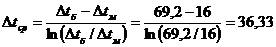 °С.
°С.
При
ориентировочном значении К = 400 Вт/м2 . К [6, с. 47], поверхность теплообмена
холодильника кубового остатка составит
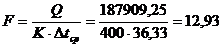 м2.
м2.
Принимаем
одноходовой кожухотрубчатый теплообменник со следующими характеристиками [6, с.
51]:
- диаметр кожуха 325
мм;
- труба 20х2
мм;
количество труб в теплообменнике 100 шт;
длина труб 4 м;
поверхность теплообмена 25 м2.
Кипятильник
(испаритель)
Количество теплоты QК,
которое надо подать в куб колонны, определяется из уравнения теплового баланса
колонны:
QК = QД + GР . СР . tХр + GW . СW . tХw - GF . СF . tХF + Qпот.
Тепловые потери принимаем 3% от полезно затрачиваемой теплоты; удельные
теплоемкости взяты соответственно при tXp = 57,62 °С, tXF = 65,41 °С, tXw = 96,2°С.
СР = аР . СА + (1 - аР) . СВ = 0,96 . 0,5485 + (1 - 0,96) . 0,9998 =
=
0,5756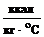 = 2276,990
= 2276,990  .
.
СF = аF .
СА + (1 - аF) . СВ = 0,40 . 0,554 + (1 - 0,40) . 1,0 =
=
0,8171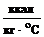 = 3423,817
= 3423,817  .
.
СW = аW .
СА + (1 - аW) . СВ = 0,018 . 0,581 + (1 - 0,018) . 1,009 =
=
0,8341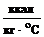 = 3494,87
= 3494,87  .
.
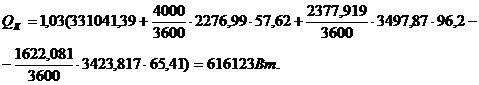
Расход греющего пара при Р = 6,0 кгс/см2:
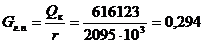 кг/с.
кг/с.
Средняя
разность температур равна разности между температурой насыщенного пара при Р =
6,0 кгс/см2 и температурой кипения кубового остатка:
Δtср = 158,1 - 96,2 = 61,9°С.
При
ориентировочно принятом коэффициенте теплопередачи К = 2000 Вт/м2.К, [6, с. 47]
поверхность кипятильника составит:
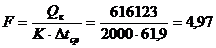 м2.
м2.
Принимаем
одноходовой кожухотрубчатый теплообменник со следующими характеристиками [6, с.
51]:
- диаметр кожуха 273
мм;
- труба 20х2 мм;
количество труб в теплообменнике 61 шт;
длина труб 1,5 м;
поверхность теплообмена 6,0м2.
Примечание:
При расчете поверхности кипятильника температура кипения кубовой жидкости
tXw = 96,2 °С взята при атмосферном
давлении. Не учтено увеличение температуры кипения кубовой жидкости в связи с
увеличением давления в кубе колонны на величину ΔРк = 0,1-0,15 кгс/см2.
СПИСОК
ЛИТЕРАТУРЫ
1. Павлов
К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и
аппаратов химической технологии. - Л.: Химия, 1987. - 576с.
2. Справочник
химика, т. 5. - М.: Химия, 1968. - 975 с.
. Отраслевой
стандарт (Ост 26-01-1488-83).
. Доманский
И.В., Исаков В.П. и др. Под общей редакцией Соколова В.Н. Машины и аппараты
химических производств: Примеры и задачи. - Л.: Машиностроение, 1982. - 384 с.
. Расчеты
основных процессов и аппаратов нефтепереработки. Справочник/Под редакцией
Судакова Е.Н., 3-е изд., перераб. и доп. - М.: Химия, 1979. - 568 с.
. Борисов
Г.С., Брыков В.П., Дытнерский Ю.И. и др. Под ред. Дытнерского Ю.И. Основные
процессы и аппараты химической технологии, 2-е изд., перераб. и дополн. - М.:
Химия, 1991. - 496 с.
. Коган
В.Б., Фридман В.М, Кафаров В.В. Равновесие между жидкостью и паром. Справочное
пособие, книга 1-я и 2-я. - М.-Л.: Наука, 1966. - 640 с. + 786 с.
. Плановский
А.Н., Рамм В.М., Каган С.З. Процессы и аппараты химической технологии, 4-е изд.
- М.: Химия, 1967. - 848 с.
. Романков
П.Г., Курочкина М.И. Расчетные диаграммы и номограммы по курсу "Процессы и
аппараты химической промышленности". - Л.: Химия, 1985. - 54 с.
. Чернышев
А.К., Коптелов В.Г., Листов В.В., Заичко Н.Д. Основные теплофизические свойства
газов и жидкостей. Номографический справочник. - Кемеровское изд-во, 1971. -
225 с.
. Плановский
А.Н., Николаев П.И. Процессы и аппараты химической и нефтехимической
технологии, 3-е изд. - М.: Химия, 1987. - 496 с.