|
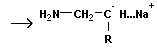 инициирование инициирование
|
|
|
|
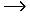
|
|
|
|
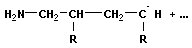 рост цепи рост цепи
|
|
|
|
|
обрыв цепи
|
Полимеризация может осуществляться между разными мономерами. Такие
соединения называют сополимерами. В табл. 1 приведены примеры полимеров и
сополимеров, получаемых реакцией полимеризации[5].
Таблица 1 Важнейшие полимеры и сополимеры
|
Мономер
|
Мономерное
звено
|
Полимер
|
|
этилен
|
|
полиэтилен
|
|
винилхлорид
|
|
поливинилхлорид
|
|
Стирол
|
|
полистирол
|
|
бутадиен-1,3
|
|
полибутадиен
|
|
стирол +
бутадиен-1,3 Ошибка! Недопустимый объект гиперссылки. <>
полистиролбутадиен
|
|
|
1.2 Реакции сополимеризации
Рассмотрим особенности процесса радикальной сополимеризации. В
случае сополимеризации молекул А и В с образованием радикалов, центрированных
на молекулах А или В растущей цепи, должны иметь место 4 стадии роста цепи[6]:
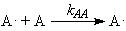
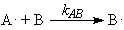
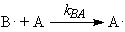
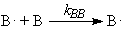
Итак, в случае радикальной полимеризации мы имеем дело с распределением
продуктов по молекулярным массам и многомаршрутный процесс с бесконечно большим
числом маршрутов. Продукты реакции Pi образуются в стадиях роста при
передаче цепи на мономер.

Второй путь образования продуктов (полимерных молекул) -
стадии обрыва цепи на Xi и Xj.
1.3 Реакции поликонденсации
В общем виде схема основной реакции поликонденсации-роста
цепи - может быть представлена следующим, образом.:
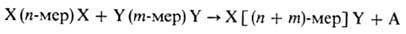
(n и m-любое целое число, включая единицу, X и Y-исходные
функциональные группы, А - низкомолекулярный продукт поликонденсации). При этом
взаимодействие мономеров друг с другом или с образовавшимися олигомерами и
последних между собой подчиняется практически одним и тем же законам[7].
Поскольку при поликонденсации мономеры исчерпываются уже при
невысоких степенях завершенности реакции, рост цепи высокомолекулярного
полимера происходит преим. в результате многократного соединения между собой
олигомерных или полимерных молекул по концевым функциональным группам (принцип
многократного удвоения), при этом число молекул в системе уменьшается (в этом
ступенчатый характер поликонденсации). Уменьшается в ходе поликонденсации и
количество исходных функциональных групп - реакционных (активных) центров, хотя
в ряде случаев образующиеся при поликонденсации связи реагируют как между
собой, так и с исходными реакционными центрами. Росту полимерной цепи при
равновесной поликонденсации сопутствует обратная реакция полимера с
выделяющимся низкомолекулярным продуктом, что ограничивает молекулярную массу
полимера.
Типичная реакция поликонденсации лежит в основе получения
фенолформальдегидных смол[9]
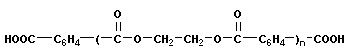 +
+
1.4 Термопластичные полимеры
Термопластичные полимеры способны многократно размягчаться при
нагревании и отвердевать при охлаждении. Эти и многие другие свойства
термопластичных полимеров объясняются линейным строением их макромолекул. При
нагревании взаимодействие между молекулами ослабевает и они могут сдвигаться
одна относительно другой, полимер размягчается, превращаясь при дальнейшем
нагревании в вязкую жидкость. На этом свойстве базируются различные способы
формования изделий из термопластов, а также соединение их сваркой[10].
Однако на практике не все термопласты так просто можно перевести в
вязко-текучее состояние, так как температура начала термического разложения
некоторых полимеров ниже температуры их текучести (поливинилхлорид, фторопласты
и др.). В таком случае используют различные технологические приемы, снижающие
температуру текучести (например, вводя пластификаторы) или задерживающие
термодеструкцию (введением стабилизаторов, переработкой в среде инертного
газа).
Линейным строением молекул объясняется также способность
термопластов не только набухать, но и хорошо растворяться в правильно
подобранных растворителях. Тип растворителя зависит от химической природы
полимера. Растворы полимеров даже очень небольшой концентрации (2...5 %)
отличаются довольно высокой вязкостью. Причиной этого являются большие размеры
полимерных молекул по сравнению с молекулами обычных низкомолекулярных веществ.
После испарения растворителя полимер вновь переходит в твердое состояние. На
этом основано использование растворов термопластов в качестве лаков, красок,
клеев и вяжущего компонента в мастиках и полимеррастворах.
К недостаткам термопластов относятся; низкая теплостойкость
(обычно не выше 80... 120 °С), низкая поверхностная твердость, хрупкость при
пониженных температурах и текучесть при высоких, склонность к старению под
действием солнечных лучей и кислорода воздуха.
1.5 Термореактивные полимеры
Молекулы термореактивных полимеров до их отверждения имеют
линейное строение, такое же, как молекулы термопластичных полимеров, но размер
молекул реактопластов намного меньше.
В отличие от термопластов, у которых молекулы химически
инертны и не способны соединяться друг с другом, молекулы термореактивных
олигомеров химически активны. Они содержат либо двойные (ненасыщенные) связи,
либо химически активные группы. Поэтому при определенных условиях (нагревании,
облучении или добавлении веществ-отвердителей) молекулы термореактивных
олигомеров соединяются друг с другом, образуя сплошную пространственную сетку,
как бы одну гигантскую макромолекулу.
После отверждения свойства полимеров изменяются: они перестают
размягчаться при нагревании, не растворяются, а только набухают в
растворителях, становятся более прочными, твердыми и термостойкими.
К термореактивным полимерам, используемым в строительстве,
относятся фенолоальдегидные, карбамидные, полиэфирные, эпоксидные и
полиуретановые.
Фенолоальдегидные полимеры - первые синтетические полимеры,
которые в начале XX в. начали получать методом поликонденсации фенолов с
альдегидами. В качестве фенольного сырья применяют фенол, крезол, ксиленол и
резорцин, а альдегидного - формальдегид, фурфурол, уротропин и лигнин.
Фенолоформальдегидные полимеры ~ наиболее распространенные
полимеры этого класса. Их получают поликонденсацией фенола с формальдегидом.
Фенол представляет собой бесцветные кристаллы с характерным сильным запахом;
токсичен. Вдыхание его приводит к отравлению, а попадание на кожу вызывает
ожоги. Формальдегид - газ, тоже с резким удушливым запахом. Следует помнить,
что отрицательные свойства, присущие исходным компонентам, в значительной
степени передаются и полимеру. В зависимости от соотношения исходных продуктов
поликонденсации и характера катализаторов получают различные виды
фенолоформальдегидных полимеров[11].
2. Электротехническая медь
Медь (лат. Cuprum) - один из семи металлов, известных с глубокой
древности. Значительные запасы медных руд находятся в США, Чили, России (Урал),
Казахстане (Джезказган), Канаде, Замбии и Заире[12].
Медь входит в состав более 150 минералов, промышленное применение
нашли 17 из них, в том числе: борнит (Cu5FeS4), халькопирит
(медный колчедан - CuFeS2), халькозин (медный блеск - Cu2S),
ковеллин (CuS), малахит (Cu2(OH)2[CO3]).
Переработка сульфидных руд дает около 80% от всей добываемой меди.
У меди уникальное сочетание свойств, обеспечившее ей широкое
применение, - высокие электро- и теплопроводность, хорошая коррозионная
стойкость, высокая пластичность и привлекательный естественный цвет. Более 70%
всей потребляемой меди идет на электротехнические изделия, 15% - на элементы
строительных конструкций, 5% - на детали машин и механизмов, 4% - на
транспортные конструкции и 4% - на другие виды изделий, в том числе на
изготовление артиллерийского оружия. Строительная промышленность потребляет
около 40% всей производимой меди, электротехника и электроника около 26%, общее
машиностроение - около 14%, транспортное машиностроение - около 11%,
промышленность товаров широкого потребления - остальные 9%. Кабели,
электротехнические шины, трансформаторные обмотки и другие электротехнические
изделия изготавливаются из разных сортов меди. В тех случаях, когда требуется
максимальная электропроводность, применяется "бескислородная медь с
высокой электропроводностью", в других же случаях пригодна
"технически чистая" медь, содержащая 0,02-0,04% кислорода. Небольшая
добавка мышьяка повышает прочность красной меди (продукта огневого
рафинирования), но такая медь, содержащая кислород, с трудом поддается сварке.
Медь с пониженным содержанием кислорода обладает хорошими литьевыми свойствами
и применяется для изготовления химико-технологического оборудования, медных
труб, автомобильных радиаторов, судовых конденсаторов, бытовых водопроводных
труб, кровельного материала и других технических изделий[13].
В природе встречается и самородная медь.
Чистая медь - ковкий и мягкий металл в изломе розоватого цвета,
достаточно тяжелый, отличный проводник тепла и электричества, легко
подвергается обработке давлением. Именно эти качества позволяют применять
изделия из меди в электротехнике - в настоящее время более 70% всей
производимой меди идет на выпуск электротехнических изделия. Для изделий с
максимальной электропроводностью, используют так называемую «безкислородную»
медь. В иных случаях годна и технически чистая медь, содержащая 0,02-0,04%
кислорода.
Основные характеристики меди: удельный вес - 8,93 г/cм3, температура
плавления - 1083°С, удельное электрическое сопротивление меди при 20°С 0,0167
Ом*мм2/м. Чистая медь обладает высокой электрической проводимостью
(на втором месте после серебра). Именно это качество меди используют в
промышленности для изготовления электротехнических шин из меди.
Медные шины изготавливаются по ГОСТ 434-78. Состояния в котором
поставляются медные шины потребителю: не отожженная (маркировка - Т-твердое),
отожженным (М-мягкое) и ТВ-твердые шины, изготовленные из бескислородной меди.
В деформированном состоянии прочность меди выше, чем у отожженного
металла, а значения электропроводности понижены.
Сплавы, повышающие прочность и улучшающие другие свойства меди,
получают введением в нее добавок, таких, как цинк, олово, кремний, свинец,
алюминий, марганец, никель. На сплавы идет более 30% меди.
Латуни - сплавы меди с цинком (меди от 60 до 90% и цинка от 40 до
10%) - прочнее меди и менее подвержены окислению. При присадке к латуни кремния
и свинца повышаются ее антифрикционные качества, при присадке олова, алюминия,
марганца и никеля возрастает антикоррозийная стойкость. Листы, литые изделия
используются в машиностроении, особенно в химическом, в оптике и
приборостроении, в производстве сеток для целлюлознобумажной промышленности.
Бронзы. Раньше бронзами называли сплавы меди (80-94%) и олова
(20-6%). В настоящее время производят безоловянные бронзы, именуемые по
главному вслед за медью компоненту.
Алюминиевые бронзы содержат 5-11% алюминия, обладают высокими
механическими свойствами в сочетании с антикоррозийной стойкостью.
Свинцовые бронзы, содержащие 25-33% свинца, используют главным
образом для изготовления подшипников, работающих при высоких давлениях и
больших скоростях скольжения.
Кремниевые бронзы, содержащие 4-5% кремния, применяют как дешевые
заменители оловянных бронз.
Бериллиевые бронзы, содержащие 1,8-2,3% бериллия, отличаются
твердостью после закалки и высокой упругостью. Их применяют для изготовления
пружин и пружинящих изделий.
Кадмиевые бронзы - сплавы меди с небольшим количества кадмия
(до1%) - используют при производстве троллейных проводов, для изготовления
арматуры водопроводных и газовых линий и в машиностроении.
Припои - сплавы цветных металлов, применяемые при пайке для
получения монолитного паяного шва. Среди твердых припоев известен
медносеребряный сплав (44,5-45,5% Ag; 29-31% Cu; остальное - цинк)[14].
В России медные шины изготавливают нескольких заводов:
Каменск-Уральский ОЦМ, Кольчугинский ОЦМ, Кировский ОЦМ.
Мировое производство меди в 2007 году выросло на 2,5% по сравнению
с 2006 г. и составило 17,76 млн. тонн. Потребление меди в 2007 году выросло на
4%, при этом медное потребление Китая взлетело на 25% за год, в то время как
медное потребление в США резко упало на 20%[15].
Заключение
Полимеризация- процесс образования высокомолекулярного
вещества (полимера) путём многократного присоединения молекул
низкомолекулярного вещества (мономера, олигомера) к активным центрам в растущей
молекуле полимера. Молекула мономера, входящая в состав полимера, образует т.наз.
мономерное (структурное) звено. Элементный состав (молекулярные формулы)
мономера и полимера приблизительно одинаков.
Обычно мономерами являются соединения, содержащие кратные
связи, которые способны, раскрываясь, образовывать новые связи с другими молекулами,
обеспечивая рост цепей.
Механизм полимеризации обычно включает в себя ряд связанных
стадий:
- инициирование - зарождение активных
центров полимеризации;
- рост (продолжение) цепи - процесс
последовательного присоединения молекул мономеров к центрам;
- передача цепи - переход активного центра
на другую молекулу;
- разветвление цепи - образование нескольких
активных центров из одного;
- обрыв цепи - гибель активных центров.
У меди уникальное сочетание свойств, обеспечившее ей широкое
применение, - высокие электро- и теплопроводность, хорошая коррозионная
стойкость, высокая пластичность и привлекательный естественный цвет. Сплавы,
повышающие прочность и улучшающие другие свойства меди, получают введением в
нее добавок, таких, как цинк, олово, кремний, свинец, алюминий, марганец,
никель. На сплавы идет более 30% меди.
Cписок используемой литературы
1. А.Г.
Стомберг, Д.П. Семченко. Физическая химия. М.: «Высшая школа»- 2003. 527с.
2. В.А.
Киреев. Курс физической химии. М.: Химия- 1995. 776с.
. А.Б
Лукьянов. Физическая и коллоидная химия. М.:Химия-2000. 224с.
. Сангалов
Ю.А. Полимеры и сополимеры изобутилена, 2001, 384 с.
. Сангалов
Ю.А. Полимеры и сополимеры бутилена, Фундаментальные проблемы и прикладные
аспекты, 2001, 264 с.
. Шур
А.М. Высокомолекулярные соединения, 2001, 656 с.
. Феттес
Е.N. Химические реакции полимеров том 2, 2007, 536 с.
. Кабанов
В.А. Энциклопедия полимеров Том 3, 2007, 576 с.
. Каргин
В.А. Энциклопедия полимеров Том 3, 2007, 755 с.
. Коршак
В.В. Итоги науки химические науки химия и технология синтетических
высокомолекулярных соединений том 6, 2001, 54 с.
. Коршак
В.В. Химия и технология синтетических высокомолекулярных соединений Том 9,
2007, 136 с.
. Л.Ф.
Попова. От лития до цезия. М., “Просвещение”, 2002, 266 с.
. В.Е.
Лунев. Познакомьтесь с медью. М.,”Металлургия”, 2005, 158 с.
. Отв.
за ред. Л.К. Иугалин. Химия минералов меди. Новосибирск, “Наука”, 2000, 196 с.
. Л.Ф.
Попова. Медь. М., “Просвещение”, 2009, 47 с.