Техническая термодинамика
Федеральное
агентство по образованию
Государственное
образовательное учреждение
высшего
профессионального образования
«Сибирская
государственная автомобильно-дорожная академия (СибАДИ)»
Конспект лекций по технической
термодинамике
для студентов специальности 270109
«Теплогазоснабжение и вентиляция»
Омск 2013г.
Лекция 1
Термодинамика (ТД) - это наука о силах, связанных с теплотой. Состоит из
двух греческих слов termo- «тепло» и dynamos - «сила».
ТД, как наука возникла с появлением тепловых машин в 18 в.
ТД - один из основных разделов теплотехники.
Теплотехника - наука и отрасль техники, изучающая методы получения и
использования теплоты, а также способы преобразования теплоты в другие виды
энергии.
Теплотехника состоит из трех основных разделов:
1. Термодинамика.
- Физическая ТД - изучает основы и способы преобразования энергии в
физические явления.
- Химическая ТД - изучает химический состав топлива.
- Техническая ТД
2. Теория тепломассообмена. Изучает различные виды теплообмена и способы
передачи теплоты, принципы действия и устройство теплообменных аппаратов.
Позволяет выполнять расчеты теплообменного аппарата и тепловой изоляции.
3. Промышленная теплотехника. Изучает использование теплоты в
различных областях. Исследует различные виды топлива, изучает принцип действия
и устройство теплоэнергетический установок (котельных, паровых и газовых
турбин, паровых машин).
Знание теплотехники позволяет:
· изучать процессы, связанные с использованием теплоты,
· увеличивать эффективность использования топлива,
· минимизировать отрицательные факторы деятельности человека,
связанные с получением теплоты при использовании углеродсодержащего топлива.
Направления использования теплоты:
. Технологическое
При технологическом использовании теплота служит для :
- изменения физических свойств материалов (плавление металлов,
термообработка металлов),
- протекания большинства химических процессов.
2. Энергетическое
При энергетическом использовании теплота преобразуется в механическую
работу с помощью тепловых машин.
Тепловая машина - это устройство, в котором тепловая энергия (от сгорания
топлива) преобразуется в механическую работу (вращение вала).
Тепловые машины делятся на:
1. Поршневые двигатели
2. Роторные двигатели
. Газотурбинные двигатели
. Реактивные двигатели
По способу подвода теплоты :
· С внешним подводом теплоты. Двигатель Стирлинга КПД в 1,5 раза больше
солнечных батарей.
· С внутренним подводом теплоты. Двигатель, в котором
происходит выделение теплоты, от сгорания топлива, непосредственно внутри двигателя.
Теплота в тепловой машине расходуется на нагрев рабочего тела, в
результате чего рабочее тело совершает механическую работу (перемещение поршня
или вращение вала)
Проблемы,
связанные с получением теплоты.
1. Экологическая. Для получения теплоты в 90% случаев используется
углеродсодержащее топливо (нефть, нефтепродукты, газ, уголь). В 10% случаев
теплота вырабатывается на АЭС. До 3% случаев при помощи возобновляемых
энергетических ресурсов (ветер, солнце, приливы-отливы).
При сжигании углеродсодержащего топлива, в атмосферу выбрасывается
огромное количество продуктов сгорания (CO2 (углекислый газ), CO (угарный газ)), что приводит к обострению парникового эффекта, так как
углекислый газ пропускает солнечные лучи на Землю, но препятствует охлаждению Земли
в космос.
Так же происходит выделение оксида серы, что приводит к кислотным дождям.
Выбрасывается огромное количество золы и сажи.
2. Экономическая. Коэффициент полезного использования топлива как
правило не превышает 40%. (η бенз. = 30÷40 %, η диз. = 35÷50 %). Очевидно, что гораздо
рациональнее разработать более эффективные технологические процессы
использования теплоты, позволяющие уменьшить расходы достаточно дорогостоящего
топлива, чем увеличивать добычу топлива.
Главными путем решения этих проблем является активное увеличение
эффективности использования топливно-энергетических ресурсов и всестороннее
принятии энергосберегающих технологий.
Лекция 2.
Техническая термодинамика
Техническая термодинамика - это наука, изучающая процессы взаимного преобразования
теплоты и работы, свойства рабочих тел и особенности термодинамических
процессов и циклов.
ТД основана на трех экспериментально установленных законах (началах ТД):
Нулевой закон
термодинамики.
Закон теплового равновесия между телами. Согласно этому закону все тела
стремятся к состоянию теплового равновесия и после его достижения не могут
самопроизвольно выйти из данного состояния (холодное тело принимает температуру
окружающей среды).
Первый закон
термодинамики.
Является по существу законом сохранения энергии применительно к
термодинамическим процессам. Согласно ему невозможен процесс возникновения
энергии из неоткуда или её исчезновение.
Второй закон
термодинамики.
Определяет направление протекания термодинамических процессов.
Устанавливает, что невозможен самопроизвольный процесс передачи теплоты от
холодного тела к более нагретому. Согласно этого же закона невозможно полное
преобразование теплоты в работу посредствам тепловых машин.
Объектом исследования ТД является термодинамическая система или в
простейшем случае рабочее тело.

Термодинамическая система (ТДС) - это совокупность макроскопических тел,
являющихся объектом изучения и, как правило, обменивающихся энергией друг с
другом и с окружающей средой.
Макроскопические тела - это тела имеющие массу и размеры соизмеримые с
окружающими нас предметами.
Тела не входящие в изучаемую систему называются окружающей (внешней)
средой.
Границу между ТДС и окружающей средой называют контрольной поверхностью,
через которую происходит обмен энергией.
Рабочее тело - это, как правило, газ, посредствам которого осуществляется
преобразование теплоты в механическую работу.
Термодинамический метод исследований.
Данный метод основан на законах термодинамики и представляет собой их
логическое и математическое развитие. Базируется на таких науках как физика и
математика.
При термодинамическом методе исследования изучается состояние ТДС. Причем
состояние ТДС характеризуется с помощью термодинамических параметров
(макропараметров). Основными макропараметрами являются давление, объем и
температура.
ТД - наука феноменологическая, она рассматривает вещества (тела) как
сплошную целостную среду и использует для его исследования макропараметры.
Макропараметры определяются путем прямого измерения или рассчитываются с
использованием термодинамических законов.
Кроме термодинамического метода исследования существуют и другие,
например статистический метод, которым является молекулярно-кинетическая теория
(МКТ)

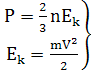
Преимущества термодинамического метода:
1. Достаточно просты способы определения термодинамических
параметров, и соответственно исследования ТДС, в том числе прогнозирования
поведения её состояния при некотором внешнем воздействии.
2. Относительно простой математический аппарат и доступность
практического исследования.
. Не использует гипотез о структуре вещества и его микросостоянии.
Основная задача ТД - поиск наиболее рациональных способов преобразования
теплоты в работу (в тепловых машинах) или наоборот работы в теплоту (в
холодильных машинах или тепловых насосах).
Равновесное
состояние термодинамической системы. Термодинамический процесс.
Если любую систему изолировать от окружающей среды, то с течением времени
система придет в равновесное состояние.
Равновесное состояние - это состояние ТДС, при котором значения
параметров, характеризующих состояние ТДС, одинаковы во всех точках ТДС и не
изменяются со временем. В такой ТДС отсутствуют потоки энергии или вещества.
Перейдя в равновесное состояние, при отсутствии внешних воздействий,
система остается в нем неограниченно долгое время.
При внешнем воздействии значения параметров системы начинают меняться,
система переходит в новое состояние - происходит термодинамический процесс.
Термодинамический процесс (ТДП) - это переход ТДС из одного равновесного
состояния в другое, при котором изменяется хотя бы один из её параметров.
При термодинамическом исследовании для повышения наглядности и упрощения
расчетов, ТДП принято изображать графически в P-V, T-S и других координатах.
Изотермический Изобарный Изохорный
 T = const
T = const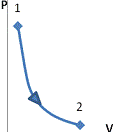 P = const
P = const V = const
V = const
Адиабатный
 Q = 0
Q = 0
Равновесное состояние рабочего тела (ТДС) изображается точкой с
соответствующими координатами.
ТДП изображается линией, соединяющей два равновесных состояния.
Лекция 3.
Основные параметры термодинамической системы
Основой термодинамического исследования является определение параметров,
характеризующих состояние ТДС.
Параметры состояния - физическая величина, количественно характеризующая
ТДС (рабочее тело).
Основными макропараметрами являются давление, объем или удельный объем,
температура.
Давление - физическая величина, равная отношению силы равномерно
распределенной по поверхности тела, к площади поверхности расположенной
перпендикулярно данной силе.
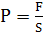 Р, Па
Р, Па 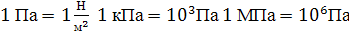
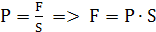

Кроме того в технике часто используются внесистемные единицы давления
бар = 105Па = 100 кПа = 0,1 МПа
Техническая атмосфера
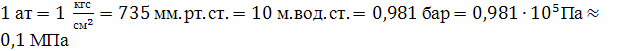
Физическая атмосфера
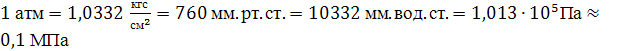
Объем. V, м3. Удельный объем v, м3/кг - объем 1 кг вещества; величина обратная
плотности
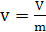 ;
; 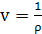 .
.
Температура - есть мера интенсивности теплового движения молекул (в
молекулярной физике), характеризует тепловое состояние тела или степень нагрева
тела.
Качественной мерой температуры является наше ощущение тепла, а
количественной мерой являются показания термометра.
Понятие «температура» вводиться нулевым законом ТД, который вводит понятие
теплового равновесия между телами, а величиной характеризующей данное
равновесное состояние является температура.
Разность температуры тел между собой определяет меру их отклонения от
теплового равновесия. Из этого следует, что если тела имеют одинаковую
температуру, то между ними не происходит теплообмена, и соответственно если
между телами не происходит теплообмен, то у них одинаковая температура.
Температурой называется параметр, характеризующий внутреннее движение
равновесной системы, т.е. величину её внутренней энергии (в ТД).
В системе СИ используются две температурные шкалы.
. Международная практическая температурная шкала (Цельсия). (t)
За 0°C принята температура кристаллизации
или температура плавления льда. За 100°С принята температура кипения дистиллированной
воды (при нормальных атмосферных условиях)

2. Термодинамическая температурная шкала, абсолютная температурная
шкала (Кельвина), основанная на втором законе ТД. (T)
За 0К принята температура абсолютного нуля (это температура при которой
прекращается всякое тепловое движение молекул). В качестве второй, реперной
(базовой) точки, принята температура «тройной точки воды». Эта точка
соответствует определенным значениям температуры и давления, при которых вода
может существовать одновременно в твердом, жидком и газообразном состояниях,
находящихся в равновесии между собой.
Температура тройной точки воды: 279,16 К при Р = 609 Па.
Т, К = 273,15 + t,°C; 1К = 1°C
Менее используемая, но не менее известная температурная шкала Фарингейта.
(t,°F)
t, °C = 5/9(t,°F - 32°); 1°F ≠ 1°C
Лекция 4.
Уравнение состояния идеального газа
Если система предоставлена самой себе (т.е. отсутствуют внешние
воздействия), то через некоторое время (время релаксации) в системе
устанавливается равновесие, т.е. значение параметров выравнивается в разных
точках системы. При этом все параметры системы будут однозначно связаны
определенным соотношением, которое называется уравнением состояния данной
системы.
Уравнение состояния, связывающее между собой значения давления,
температуры и объема, называется уравнением состояния ТДС.
Общий вид этого уравнения следующий:
f (P; V; T) = 0
где f - функция зависящая от свойств
данной системы. Число независимых параметров равно двум, т.е. любой из трех
параметров может быть определен по двум другим.
P = f (V; T) ; V = f (P; T) ; T = f (P; V)
Вопрос о получении уравнения состояния достаточно сложен и полностью не
решен даже для газа. Получено уравнение состояния идеального газа.
Идеальный
газ.
При изучении свойств газов в ТД и физике прибегают к упрощению и вводиться
понятие идеальный газ.
Идеальным называется газ, в котором :
· Отсутствуют силы взаимодействия между молекулами (притяжение,
отталкивание);
· Пренебрегают объемом молекул;
· Столкновения молекул между собой и со стенками системы
являются абсолютно упругими.
Для решения теплотехнических задач с некоторым приближением принимают,
что свойства реальных газов соответствуют свойствам идеальных газов при
плотности газа (при его температуре и давлении) близкой к нормальным условиям.
Уравнение
Клапейрона.
Данное уравнение получено расчетным путем на основании МКТ (с
использованием постоянной Больцмана и числа Авогадро).
Задолго до того, как уравнение состояния было получено в молекулярной
физике, закономерности поведения газов были изучены экспериментально и получены
уравнения состояний.
В 1834 г. французским физиком Клапейроном путем обобщения известных
газовых законов (закон Бойля-Мариотта T=const, PV=const; закон
Гей-Люссака Р=const, V/Т=const;
закон Шарля V = const, P/Т = const), было получено уравнение состояния
для газов близких по своим свойствам к идеальному. При m=const. Уравнение
Клапейрона в исходной форме
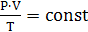
Константа имеет свое значение для каждого газа
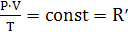
R’, 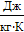 - удельная газовая постоянная, её
значения для каждого идеального газа приводятся в справочниках.
- удельная газовая постоянная, её
значения для каждого идеального газа приводятся в справочниках.
Уравнение Клапейрона для 1кг идеального газа:
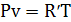
Уравнение Клапейрона для произвольной массы идеального газа
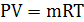

Физический смысл удельной газовой постоянной - удельная газовая
постоянная численно равна работе расширения 1кг идеального газа при нагревании
его на 1К при постоянном давлении.
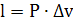
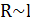
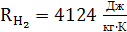
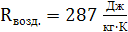
Уравнение
Менделеева - Клапейрона.
В 1874 г Дмитрий Иванович Менделеев на основании уравнения Клапейрона и
закона Авогадро вывел уравнение состояния, которое не содержит индивидуальной
для каждого газа константы.
Согласно закону Авогадро равное количество молей различных газов при
одинаковых условиях (при равных давлениях и температурах) занимают одинаковый объем.
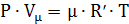
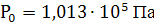
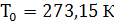
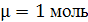

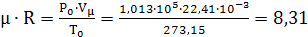
R, 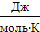 - универсальная газовая постоянная
(для 1 моля любого газа)
- универсальная газовая постоянная
(для 1 моля любого газа)
Уравнение Менделеева - Клапейрона для произвольного количества моль газа:
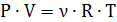
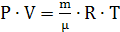
Физический смысл универсальной газовой постоянной - универсальная газовая
постоянная численно равна работе расширения 1 моля идеального одноатомного газа
при нагревании его на 1К при постоянном давлении.
Лекция 5.
Способы передачи и изменения энергии. Внутренняя энергия
Любое тело в любом состоянии обладает внутренней энергией. Параметр,
который характеризует значение внутренней энергии, называется температурой.
Внутренняя энергия зависит от:
· Кинетической энергии молекул (т.е. от скорости движения
молекул);
· Потенциальной энергии молекул (т.е. от расстояния между
молекулами).
И определяется значениями:
· Давления;
· Объема.
Таким образом, значение внутренней энергии можно охарактеризовать с
помощью параметров состояния ТДС: давление, объем, температура.
Являясь функцией параметров состояния, внутренняя энергия и сама является
параметром состояния ТДС.
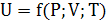 U, Дж - внутренняя
энергия
U, Дж - внутренняя
энергия
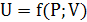 u, Дж/кг -
внутренняя энергия 1 кг вещества.
u, Дж/кг -
внутренняя энергия 1 кг вещества.
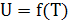

Являясь параметром состояния, внутренняя энергия при изменении не зависит
от характера процесса.
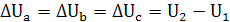
Для ν моль вещества: Для m кг газа
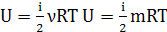
универсальная газовая постоянная: удельная газовая постоянная:
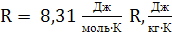
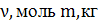
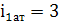
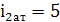 (H2, O2, N2, воздух)
(H2, O2, N2, воздух)
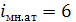 (СO2)
(СO2)
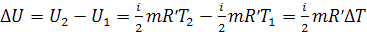
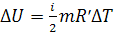
Таким образом, при изменении внутренней энергии обязательно измениться
температура.
Передача энергии может осуществляться различными способами, для ТД
наиболее важны два способа:
· Передача энергии в виде теплоты
· Совершение механической работы
Передача
энергии в виде теплоты.
Происходит между телами, имеющими разные температуры, при этом передача
энергии происходит от тел с большей температурой к телам с меньшей
температурой. Количество энергии, переданное таким образом, называется
количеством теплоты.
Q, Дж
- количество теплоты
q,
Дж/кг - удельное количество теплоты (количество теплоты 1кг вещества)
Подведенная к системе теплота называется положительной (Q(+)), отведенная - отрицательной (Q(-))
Передача
энергии в форме работы.
Количество энергии, переданное таким образом, называется работой.
L, Дж
- работа
l,
Дж/кг - удельная работа (работа 1кг вещества)

При передаче энергии таким способом происходит либо перемещение рабочего
тела (техническая работа). Например, в газовой турбине: перемещение рабочего
тела заставляет вращаться турбинное колесо;
либо изменение объема рабочего тела. Например, в поршневых двигателях:
увеличение объема рабочего тела совершает работу по перемещению поршня, при
этом, работа совершается системой и является положительной, работа, совершенная
над системой, будет являться отрицательной.
Теплота и работа являются различными формами передачи энергии.
Теплота является формой передачи энергии на молекулярном уровне без
видимого движения тела.
Работа - форма передачи энергии за счет макропроцесса, при этом
происходит изменение объема, давления и температуры или перемещение.
Работа
изменения объема.

Пусть в цилиндре под поршнем находиться 1кг рабочего тела, производящего
на поршень площадью S давление P, действующего с силой F.
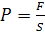

Δh-перемещение поршня.
При подведении теплоты q,
возрастают температура, кинетическая энергия молекул, давление рабочего тела и
сила, действующая на поршень. В момент, когда значение этой силы превысит
значение сил внешних воздействий, начинает изменяться объем и совершается
работа.
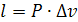
при Р = const и m = 1кг.

Работа изменения объема является функцией процесса, поэтому зависит от
промежуточных состояний.
Работа изображается в P-V координатах, в определенном масштабе
и имеет следующий геометрический смысл: работа численно равна площади фигуры
под линией графика процесса.


Для некоторых процессов работа изменения объема будет равна интегралу
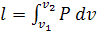
Лекция 6.
Термодинамические циклы
ТД циклы - это совокупность процессов, начинающихся в некоторой точке и,
после совершения всех процессов, заканчивающихся в этой же точке (система
возвращается в первоначальное состояние).
Все тепловые машины работают по прямому ТД циклу - по часовой стрелке.
Холодильные машины работают по обратному ТД циклу - против часовой стрелки.
Термодинамический
цикл тепловой машины.

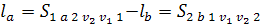
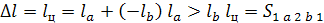
Работа, полученная в цикле равна сумме работ всех процессов полученных в
цикле.
Работа цикла положительна, если цикл выполняется по часовой стрелке и
отрицательна, если цикл выполняется против часовой стрелки.
Термодинамический
цикл холодильной установки.

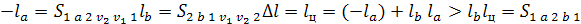
Первый закон
термодинамики.
Первый закон ТД, это частный случай общего закона сохранения энергии,
выраженный применительно в механической работе и теплоте. Он устанавливает, что
теплота и работа могут взаимно преобразовываться при постоянном количественном
соотношении между собой.
В 1839 г. Юлиус Роберт Майер впервые предположил, что работа и теплота
могут взаимно преобразовываться.
В период с 1840 по 1843 гг. Джеймс Джоуль экспериментально установил
соотношение между работой и теплотой.
В опыте Джоуля механическая энергия (потенциальная) грузов, которые
опускались с некоторой высоты, преобразовывалась во внутреннюю энергию воды в
изолированном сосуде (происходит нагревание воды).

Джоуль проводил опыты с грузами различной массы, различным диаметром
шкива и продолжительностью вращения лопаток.
В опыте Джоуля силы трения совершают положительную работу, поэтому
внутренняя энергия воды возрастает, а механическая энергия груза убывает.
Джоуль установил, что внутренняя энергия системы в конечном состоянии
была равна сумме внутренней энергии в начальном состоянии и работы.

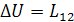
Давление и объем рабочего тела остаются практически постоянными и
значение температуры полностью определяет значение внутренней энергии.
Таким образом Джоуль установил тепловой эквивалент работы.
Работа в 4,19 Дж позволяла получить 1 калорию теплоты.
Данный процесс происходит адиабатически, т.е. Q=const.
Соотношение постоянно при любой массе груза, таким образом, Джоуль
сформулировал первый закон ТД для адиабатического процесса:
Изменение внутренней энергии ΔU теплоизолированной системы равно
работе, совершенной внешними силами.
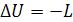
В общем случае внутренняя энергия системы может изменяться одновременно
как за счет теплообмена с окружающими телами, так и за счет совершения работы
внешними силами.
Первый закон ТД является обобщением огромного количества опытных фактов и
является, по сути, законом природы. В зависимости от области применения первый
закон ТД имеет две формулировки:
. Изменение внутренней энергии системы (ΔU), при её переходе из одного
состояния во второе, равняется сумме количества теплоты (Q), подведенной извне, и работе
внешних сил Lвнеш, действующих на неё.

. Количество теплоты (Q), подведенное к системе, расходуется на изменение её внутренней энергии
(ΔU) и на совершение системной работы
портив действия внешних сил.
вода цикл газотурбинный
энергия
Лекция 7.
Первый закон термодинамики для изопроцессов
Первый закон
ТД для изохорного процесса.
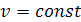
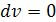
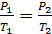
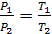

При подводе теплоты q1 пропорционально увеличению давления
от Р1 до Р2 увеличивается температура.
При изохорном процессе работа равна нулю, так как
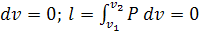
Первый закон ТД для изохорного процесса
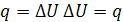
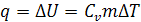
Так как
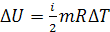
и 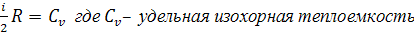
Первый закон
ТД для изобарного процесса.

Из уравнения Менделеева - Клапейрона
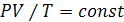 для изобарного процесса следует
для изобарного процесса следует
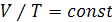
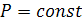

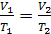
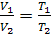
При подводе теплоты в изобарном процессе пропорционально увеличению
объема происходит возрастание температуры и наоборот.
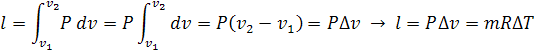
Изменение внутренней энергии зависит от температуры и соответственно так
же изменяется в соответствии с уравнением 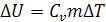
Первый закон ТД для изобарного процесса
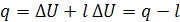
Первый закон
ТД для изотермического процесса.
Осуществить изотермический процесс можно только при наличии достаточно
большого источника теплоты данной температуры, который обеспечивает непрерывный
подвод теплоты в течение процесса при постоянной температуре. Согласно
уравнения Клапейрона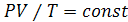 для изотермического процесса следует
для изотермического процесса следует 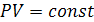 .
.

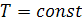
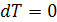
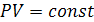
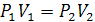
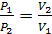
В изотермическом процессе с подводом теплоты одновременно с увеличением
объема происходит обратное уменьшение давления.
График процесса в P-V координатах изображается равнобокой гиперболой.
Первый закон ТД для изотермического процесса
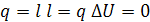
Из уравнения Клапейрона следует, что 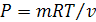 , тогда для 1кг
, тогда для 1кг
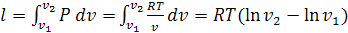
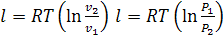
Первый закон
ТД для адиабатного процесса.
Адиабатный процесс совершается в системе, которая не обменивается
теплотой с окружающей средой.
Адиабатный процесс является наиболее эффективным для преобразования
внутренней энергии ΔU в работу L, так как отсутствует тепловые потери. Для
этого систему необходимо теплоизолировать.
Реальные процессы не могут быть адиабатными, поскольку некоторые потери
теплоты всегда существуют. Но при быстром протекании процесса, теплообмен между
системой и внешней средой можно считать незначительным в инженерных расчетах.
С некоторыми допущениями быстро протекающие процессы можно считать
адиабатными. Первый закон ТД для адиабатного процесса
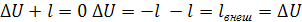
Увеличение температуры при адиабатном сжатии приводит к тому, что
давление возрастает более резко, чем при изотермическом процессе.
Резкое нагревание воздуха при адиабатном сжатии используется в дизельных
двигателях. Воздух при этом нагревается от 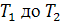 .
.
Уравнение для адиабатного процесса
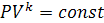 ,
,
де k - показатель адиабаты (коэффициент
Пуассона)
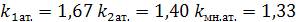
Работа газа в адиабатном процессе вычисляется через температуры
начального и конечного состояния следующим образом
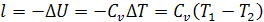
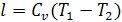 , для 1 кг газа
, для 1 кг газа
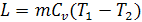 , для m кг
газа
, для m кг
газа

Уравнение работы газа в адиабатном процессе в случае, если неизвестны
температуры начального и конечного состояния (Т1, Т2), но
известны давления (Р1, Р2) и удельные объемы (v1, v2) в начале и в конце процесса.
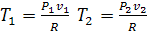
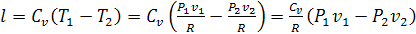
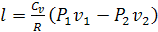
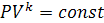 - уравнение адиабаты, отсюда можно получить соотношения
между параметрами:
- уравнение адиабаты, отсюда можно получить соотношения
между параметрами:
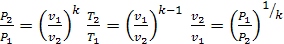
Лекция 8.
Теплоемкость. Уравнение Майера
Теплоемкость - это количество теплоты, которое нужно подвести или отнять
от тела для изменения его температуры на один градус.
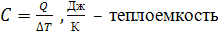
Удельная теплоемкость - это количество теплоты, которое нужно подвести
или отнять от одного килограмма вещества для изменения его температуры на один
градус.
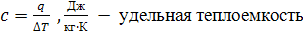
Зная теплоемкость, можно определить количество теплоты q, которое нужно подвести к телу для
изменения его температуры на величину ΔT.
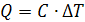
Теплоемкости различных веществ различны, их значения определены
экспериментально и приводятся в справочниках.
В зависимости от способа задания количества вещества (рабочего тела)
используют следующие теплоемкости:
. Удельная теплоемкость
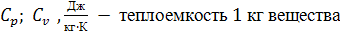
. Объемная теплоемкость

. Молярная теплоемкость

Факторы,
влияющие на теплоемкость.
Основными факторами, влияющими на теплоемкость, являются характер
протекания процесса и температура тела.
. Теплоемкость зависит от характера протекания процесса, при котором
подводится или отводится теплота. При экспериментальном определении
теплоемкость рассматриваются два процесса:
Протекание при v=const Cv (изохорная теплоемкость)
Протекание при P=const CP (изобарная теплоемкость)
Связь между изохорной теплоемкостью и изобарной теплоемкостью установил
немецкий ученый Юлиус Майер.
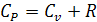
Рассмотрим процесс подвода теплоты к 1 кг рабочего тела для изменения его
температуры на 1 К.
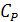
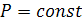
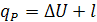
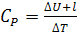
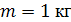

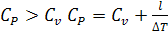
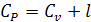
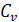
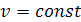
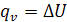
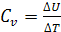
В изобарном процессе подводимая к системе теплота расходуется не только
на изменение внутренней энергии, как в случае изохорного процесса, но и на
совершение работы (расширения) против действия внешних сил. Поэтому для
изменения температуры тела на 1°C (К)
расходуется больше теплоты.
Из уравнения Майера 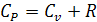 следует, что газовая постоянная R имеет следующий физический смысл: она численно равна работе,
совершенной газом при расширении его в результате нагревания на 1°C (К), при условии сохранения постоянного
давления.
следует, что газовая постоянная R имеет следующий физический смысл: она численно равна работе,
совершенной газом при расширении его в результате нагревания на 1°C (К), при условии сохранения постоянного
давления.

. Теплоемкость зависит от температуры тела.
С увеличением температуры значение теплоемкости возрастает.
Иногда в приближенных и в предварительных расчетах данной зависимостью
пренебрегают, либо значение теплоемкости принимают равным среднему значению в
данном диапазоне температур.
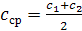
Но в большинстве случаев зависимость теплоемкости от температуры
учитывают, так как при большой разности температур погрешность может достигать
10%.
Так как 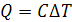 , то площадь под линией процесса численно равна количеству
теплоты, которую необходимо подвести для изменения температуры тела на величину
ΔT.
, то площадь под линией процесса численно равна количеству
теплоты, которую необходимо подвести для изменения температуры тела на величину
ΔT.
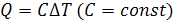
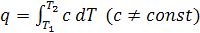
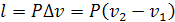
Согласно первому закону ТД
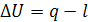
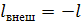
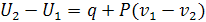
Отсюда количество теплоты, подводимое в процессе равно
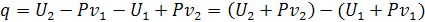
С целью упрощения расчетов ТД процессов удобно ввести функцию:
I, Дж
- энтальпия
i,
Дж/кг - удельная энтальпия (энтальпия 1кг вещества)
Энтальпия представляет собой энергию, связанную с данным состоянием
рабочего тела. А так как она определяется исключительно параметрами состояния
(внутренняя энергия, давление и объем), то и сама является функцией состояния.
Энтальпия имеет очень большое значение в теплотехнике, в том числе в
случае расчета потоков рабочего тела (например, в газовых турбинах). С её
помощью значительно упрощается выполнение расчетов и графическое представление
процессов.
Политропный
процесс.
Политропный процесс - это ТД процесс, совершаемый при постоянной
теплоемкости системы. Включает в себя все изопроцессы:
- Изобарный; Р=const; С=СP,
- Изохорный; V=const; С=СV,
- Изотермический; Т=const; С=Q/ΔT= ± ∞,
- Адиабатный; Q=const; С=0.
Уравнение политропы имеет вид: 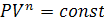 , где n - показатель политропы.
, где n - показатель политропы.
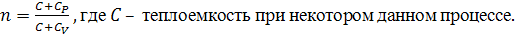
Показатели
политропы для изопроцессов следующие

Изобарный процесс. 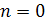 , так как.
, так как. 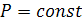 и уравнение политропы вынуждено выглядеть так:
и уравнение политропы вынуждено выглядеть так: 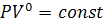
Изохорный процесс. Изохорный процесс: 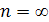 , так как
, так как 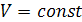 , и в процессе
, и в процессе 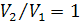 , а из уравнения политропы следует, что
, а из уравнения политропы следует, что 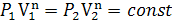 , то есть, что
, то есть, что
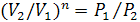 , то есть
, то есть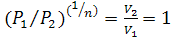 ,
,
а это возможно, только если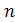 является бесконечным. Тогда
уравнение политропы:
является бесконечным. Тогда
уравнение политропы: 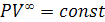
Изотермический
процесс. 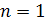 , так как
, так как 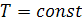 , значит, по -закону Бойля Мариотта
<#"706135.files/image089.gif">, и уравнение политропы вынуждено выглядеть так:
, значит, по -закону Бойля Мариотта
<#"706135.files/image089.gif">, и уравнение политропы вынуждено выглядеть так: 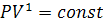 .
.
Адиабатный
процесс.
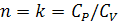
(где
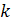 - показатель адиабаты
<#"706135.files/image138.gif"> представляют собой гиперболы,
крутизна которых возрастает с увеличением показателя n. Самая крутая из них
изохора (n=∞), а самая пологая - изобара (n=0).
- показатель адиабаты
<#"706135.files/image138.gif"> представляют собой гиперболы,
крутизна которых возрастает с увеличением показателя n. Самая крутая из них
изохора (n=∞), а самая пологая - изобара (n=0).
Лекция 10.
Второй закон термодинамики
Согласно первому закону ТД энергия может преобразовываться из одного вида
в другой с сохранением общего количества энергии. Однако он имеет два
допущения.
Во-первых, он не накладывает ограничения на возможность превращения
энергии из одного вида в другой.
Согласно первому закону ТД работу всегда можно превратить в теплоту, а
теплоту в работу на 100%. Однако существует ограничение при преобразовании
теплоты в работу. Тело всегда можно нагреть, совершая работу трения. Подобным
образом электрическая энергия может быть преобразована в теплоту, внутриядерная
энергия может быть преобразована в теплоту. Теплота является «низшей» формой
энергии, в которую преобразуется любой другой вид энергии. И если бы в природе
не существовало ограничений на преобразование теплоты (например, в работу), то
была бы возможность создания вечного двигателя второго рода, который путем
охлаждения окружающих тел (например, воды в мировом океане) превращал взятую от
них теплоту в работу (например, корабль, движущийся по океану забирает воду и
превращает ее в работу).
· Например, при охлаждении вод мирового океана массой 1021
кг всего на 1К выделяется теплота 1024 Дж, что эквивалентно
сжиганию угля массой 1017 кг. Протяженность состава с такой массой
угля равна расстоянию от солнца до границы солнечной системы. Ежегодно на Земле
вырабатывается в 10 тыс. раз меньше энергии, поэтому вечный двигатель второго
рода был бы не менее привлекателен, чем первого.
Английский физик Кельвин в 1851 г дал следующую формулировку второго
закона ТД: Невозможен процесс, единственным конечным результатом которого будет
превращение всей теплоты извлеченной из теплового источника, или иначе: из всей
теплоты подведенной от нагревателя (горячего источника). Только часть её может
быть преобразована в работу, остальная часть должна быть отведена в холодный
источник (охладитель).
Во-вторых, первый закон ТД не устанавливает направление тепловых
процессов. Так же он не может отличить обратимые процессы от необратимых.
Однако, как показывает опыт, тепловые процессы могут протекать только в
одном направлении, данные процессы называются необратимыми.
· Например, при тепловом контакте двух тел с разными
температурами теплота передается всегда от тела с высокой температурой к телу с
более низкой.
Исходя из этого, немецкий физик Клаузиус дал вторую формулировку второго
закона ТД: теплота не может самопроизвольно, без некоторого данного процесса,
переходить от тела с низкой температурой к телу с высокой температурой.
Энтропия.
Передачу энергии в форме работы легко наблюдать по изменению объема или
перемещению рабочего тела.
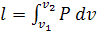
· Например, работа зависит от изменения объема dv и давления P.
Как мы знаем, обмен энергией может так же происходить в форме обмена
теплотой. Температура является одним из признаков передачи энергии в виде
теплоты. Однако, измеряя температуру не всегда можно определить количество
переданной теплоты.
· Например, при подводе теплоты к кипящей воде температура
остается постоянной.
Параметр, который изменяется только от количества теплоты, был предложен
в 1852 г. Рудольфом Клаузиусом и впоследствии назван энтропией (S).
Энтропия не может быть измерена (так же как и потенциальная энергия тела)
и определяется только расчетным путем. По аналогии с интегралом вычисления
работы количество теплоты зависит от изменения энтропии.
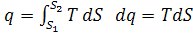
Отсюда следует, что при подведении к системе теплоты (dq>0) энтропия системы возрастает (dS>0). И наоборот, при уменьшении
энтропии (dS<0) следует, что теплота от
системы отводиться.
Для расчета количества теплоты необходима функция зависимости T от S аналогично случаю, когда для определения количества работы
необходима функция зависимости Р от V. Поэтому в ТД используются не только Р - V координаты, но и координаты T - S,
характеризующие теплообмен между телами.
Тепловая
диаграмма.

Диаграмма в T-S координатах.
Графическая зависимость между температурой и энтропией называется
тепловой диаграммой.
Тепловая диаграмма очень широко используется при ТД исследованиях, а так
же значительно сокращает расчеты.
Площадь под графиком численно характеризует количество теплоты
подведенной в процессе.
Физический смысл имеет не абсолютное значение энтропии, а разность
энтропий ΔS в
двух состояниях системы.
Лекция 11.
Аналитическое выражение второго закона термодинамики
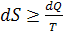
S,
Дж/К- бесконечно малое приращение энтропии системы;- бесконечно малое
количество теплоты, полученное системой от источника тепла;- абсолютная
температура источника теплоты;
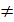 - соответствует необратимым процессам;
- соответствует необратимым процессам;
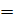 - соответствует обратимым процессам.
- соответствует обратимым процессам.
Необратимый процесс - процесс, который может самопроизвольно протекать
только в одном определённом направлении.
Обратимый процесс (то есть равновесный) - термодинамический процесс,
который может проходить как в прямом, так и в обратном направлении, проходя
через одинаковые промежуточные состояния.
Все реальные процессы, как правило, необратимы.
Для бесконечно малого обратимого процесса 2-й закон термодинамики имеет
вид:
dQ=TdS
Утверждение по существованию энтропии является основой 2-го закона
термодинамики.
Причём энтропия системы при совершении реальных процессов - возрастает.
Круговые
процессы и циклы.
Условие
работы тепловой машины.
Тепловой машиной называется устройство, позволяющее производить работу
при циклическом процессе теплообмена между рабочим телом и источником теплоты.
Такая машина может быть обратимой (только теоретически) и необратимой.
Необратимая машина совершает необратимый цикл.
Как показывают наблюдения - все виды энергии, в конечном счете,
превращаются в теплоту, которая затем рассеивается в окружающую среду.
Мера этого рассеивания характеризуется энтропией. Чем больше рассеивается
(обесценивается) энергия, тем больше увеличивается энтропия.
Термодинамический цикл - это совокупность термодинамических процессов,
после совершения которых, система возвращается в исходное состояние.
Для того, чтобы от тепловой машины можно было получить полезную работу,
необходимо выполнить следующие условия:
1. Необходимо наличие рабочего тела, т.е. тела, посредством
которого, осуществляется взаимное преобразование теплоты и работы;
2. Необходимо наличие двух источников теплоты с различными
температурами (нагреватель и охладитель);
. Работа тепловой машины должна быть цикличной, т.е. рабочее тело,
совершая ряд процессов, должно возвращаться в исходное положение.
Рассмотрим
простейший цикл тепловой машины

l1=S1a2v2v11
Tн
> Т0
В исходном состоянии рабочее тело имеет давление и объем - p1 и
v1
При подводе к рабочему телу теплоты q1 система переходит во
второе состояние, совершая при этом положительную работу l1,
численно равную площади.
В процессе сжатия (возвращение системы в исходное состояние) от рабочего
тела необходимо отводить теплоту q2 к охладителю, с температурой T0.
В этом процессе затрачивается работа l2 (работа системы -
отрицательная) l2=S2b1v1v22.
Таким образом, работа цикла (lц=l1+(-l2)) равна сумме работ всех процессов цикла (lц=S1a2b1)
Первый закон ТД для процессов данного цикла будет иметь вид
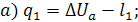
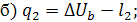
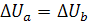
Сложим уравнения для ТД процессов a и b с учетом того, что изменение
внутренней энергии за цикл равно 0, получим
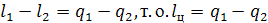

Работа цикла тепловой машины равна разности подведенной и отведенной
теплоты. Чтобы получить большую работу цикла, необходимо, чтобы эта разность
была больше.
Чтобы этого достичь, необходимо одновременно со сжатием охлаждать рабочее
тело. При этом потребляется меньшее значение работы, затрачиваемое на сжатие.
Если при сжатии не охлаждать рабочее тело, то работа сжатия будет равна
работе расширения. И работа цикла будет равна нулю (lц=0)
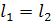
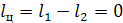
КПД тепловой
машины.
Степень совершенства работы тепловой машины оценивается коэффициентом
полезного действия
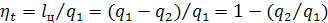
КПД тепловой машины всегда меньше 1 или 100%, т.к. часть теплоты,
подведенной к рабочему телу, необходимо отводить в окружающую среду.
Таким образом, доказана формулировка второго закона ТД (формулировка
Карно). Полное превращение теплоты в работу с помощью тепловой машины -
невозможно.
Лекция 12.
Вычисление энтропии
Уравнение первого закона ТД (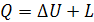 ) в дифференциальной форме имеет вид:
) в дифференциальной форме имеет вид:
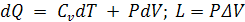
Выразим давление из уравнения Клапейрона: 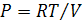 .
.
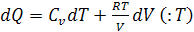
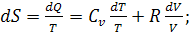
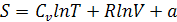
Поскольку в термодинамике используется не абсолютное значение энтропии, а
ее изменение, то отсчет значения энтропии можно вести от любого состояния, т.е.
const a из уравнения исключим.
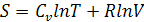
Изменение энтропии между двумя состояниями системы, при постоянной
теплоемкости, можно вычислить по формулам:
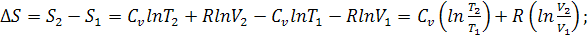
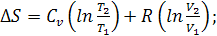
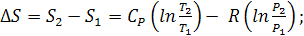
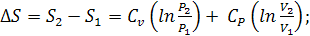
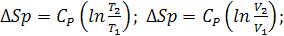
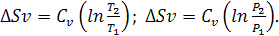
Изображения
процессов в T-S координатах

Адиабатный
процесс.
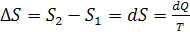
(в T-S координатах адиабата изображается вертикальной прямой)

Изотермический
процесс.
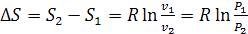
(в T-S координатах изотерма изображается горизонтальной прямой)

Изохорный и
изобарный процессы.
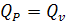 - невозможно при
- невозможно при 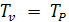
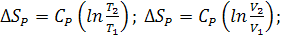
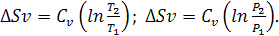
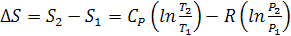
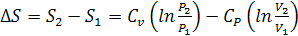
Цикл Карно.
Наиболее выгодный теоретический цикл теплового двигателя, преобразующий
максимальное количество теплоты в максимальное количество работы, предложил в
1824 году французский ученый Сади Карно.
Как видно из полученной ранее формулы
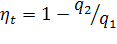
КПД возрастает при уменьшении 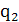 или при увеличении
или при увеличении 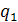 .
.
Отсюда можно заключить, что выбирая процесс расширения и сжатия,
протекающий с отводом и подводом теплоты, можно изменить величину КПД. Карно
предложил цикл, состоящий из двух обратимых адиабатных процессов. Обратимые
процессы это те, в которых отсутствуют потери (механические, рабочего тела,
теплоты и т.д.). Эти допущения Карно применил к своей машине. Изотермический
процесс был выбран, т.к. вся теплота, подводимая к рабочему телу, полностью
превращается в работу. Адиабатный процесс протекает без потери теплоты. Т.о.
изотермические и адиабатные процессы являются самыми выгодными процессами, для
получения максимальной работы. Рассмотрим все процессы данного цикла

1-2 - Изотермическое расширение с подводом теплоты 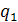 от нагревателя с температурой
от нагревателя с температурой 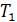 .
.
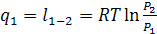
-3 -
Адиабатное расширение
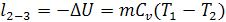
-4 - Изотермическое сжатие с отводом теплоты 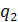 в охладитель с температурой
в охладитель с температурой 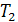 .
.
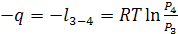
-1 - Адиабатное сжатие, в результате которого, рабочее тело нагревается
до температуры 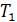 .
.
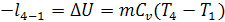
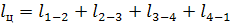
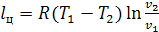
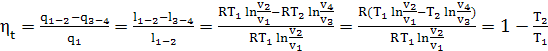

Из уравнения КПД цикла Карно следует, что при отсутствии разницы между
нагревателем и охладителем, КПД тепловой машины равно нулю.
Это означает, что невозможно превращение теплоты в работу в случае
отсутствия охладителя 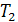 , либо нагревателя
, либо нагревателя 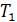 , т.е. теплота может быть
преобразована в работу только тогда, когда есть перепад температур.
, т.е. теплота может быть
преобразована в работу только тогда, когда есть перепад температур.
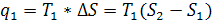


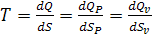
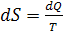
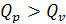
т.к. в изобарном процессе подводимая к системе теплота расходуется не
только на изменение внутренней энергии, как в случае изохорного процесса (v=const), но и на совершение работы против действия внешних
сил, поэтому для изменения температуры тела на 1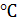 расходуется больше теплоты.
расходуется больше теплоты.
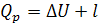
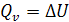
Лекция 13
Аналитическое выражение второго закона ТД
Из анализа цикла Карно можно записать следующую зависимость. Термический
КПД:
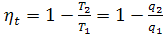
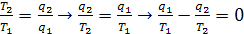
Для обратимого цикла Карно сумма приведенной теплоты 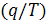 в процессах 1-2 и 3- 4 равна нулю.
в процессах 1-2 и 3- 4 равна нулю.
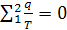
Если взять необратимый процесс, протекающий с теми же температурами
нагревателя и охладителя, то в связи с потерями давления, потерями теплоты,
вихревыми потерями и т.д., получим:
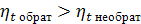
Термический КПД обратимого процесса будет больше, чем необратимого.
Из условия, что для обратимого цикла
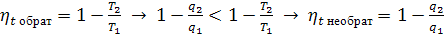

Т.о. для необратимого цикла получим:
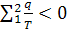
Перейдя к произвольному циклу получим
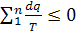
«=» - для обратимых процессов;
«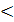 » - для необратимых процессов.
» - для необратимых процессов.
Параметр, характеризующий в данном выражении количество приведенной
теплоты 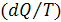 называется - энтропией.
называется - энтропией.
На основании вышеизложенного можно записать: 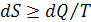 - аналитическое выражение второго
закона ТД для обратимых «=» и необратимых «
- аналитическое выражение второго
закона ТД для обратимых «=» и необратимых «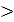 » процессов (циклов). dS - бесконечно малое приращение
энтропии, в результате получения системой бесконечно малого количества теплоты
dq от источника с температурой Т.
» процессов (циклов). dS - бесконечно малое приращение
энтропии, в результате получения системой бесконечно малого количества теплоты
dq от источника с температурой Т.
Для изолированной ТДС можно записать 
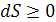
Энтропия изолированной системы при обратимых процессах не изменяется, а
при необратимых (реальных) процессах она возрастает.
Уравнение первого закона ТД с учетом второго закона ТД имеет вид:
· для обратимых процессов
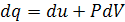 ;
;
· для необратимых процессов
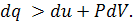
Тепловые двигатели, работа которых осуществляется за счет энергии
топлива, сжигаемого в цилиндре самого двигателя (в камере сгорания над
поршнем), называются поршневыми ДВС.
ДВС подразделяются на:
а) двигатели с принудительным воспламенением горючей смеси (от
электрической искры), работающей с подводом теплоты при постоянном объеме -
цикл Отто (характерен для бензиновых двигателей).
б) двигатели с самовоспламенением горючей смеси (от сжатия),
работающей с подводом теплоты при постоянном давлении - цикл Дизеля.
в) двигатели с самовоспламенением горючей смеси, со смешанным
подводом теплоты сначала при постоянном объеме, а затем при постоянном давлении
- цикл Тринклера (по данному циклу работают все современные «дизельные двигатели»).
Рабочие процессы реального двигателя нельзя исследовать ТД методом, т.к.
реальные процессы необходимо рассматривать с учетом газовой динамики, а также
экспериментальных специфических методов.
Но, с помощью ТД метода анализируются циклы тепловых двигателей на
начальном этапе (базовом) расчета двигателя.
Для этого используют следующие допущения:
. процесс сгорания топлива заменен на процесс подвода теплоты через
стенки цилиндра;
2. процесс выпуска отработавших газов заменен процессом отвода
теплоты (у ДВС) через стенки цилиндра; рабочее тело реального двигателя через
выпускной клапан выталкивается в атмосферу.
. процессы расширения и сжатия принимаются адиабатными;
. принимается, что рабочее тело не заменяется в цикле, т.е.
остается постоянным.
Лекция 14.
Индикаторная диаграмма идеального двигателя
В идеальном двигателе рабочим телом является идеальный газ (воздух),
процессы протекают без потерь теплоты и работы.

Индикаторная диаграмма - это график, изменения давления внутри цилиндра
двигателя при перемещении поршня.
Подобная диаграмма у реальных двигателей снимается специальными
приборами, которые называются индикаторами (это быстродействующие датчики
давления).
График строится в зависимости от объема занимаемого рабочего тела, либо
угла поворота коленчатого вала (в 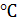 ).
).
В.М.Т. - верхняя мертвая точка
Н.М.Т. - нижняя мертвая точка
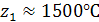 ;
; 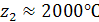 ;
;
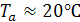 ;
; 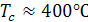
В точке с температура воздуха может превысить температуру
самовоспламенения топлива (это используется в дизельных двигателях).
В точке с происходит впрыск топлива форсункой, смешиваясь с раскаленным
воздухом горючая смесь воспламеняется, соответственно выделяется некоторое
количество теплоты, сначала при постоянном объеме (процесс с-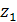 ) и затем продолжается при постоянном
давлении (
) и затем продолжается при постоянном
давлении (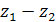 - изобарный подвод теплоты).
- изобарный подвод теплоты).
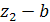 - адиабатное расширение (рабочий ход поршня);
- адиабатное расширение (рабочий ход поршня);
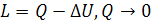 ,
, 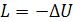 .
.
Температура понижается 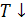 ;
; 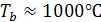 .
.
b-O - выпуск рабочего тела в окружающую
среду;a - впуск «нового» рабочего тела (с температурой окружающей среды).
Процессы выпуска и впуска достаточно сложны в расчетах. Необходимо
использовать знание законов динамики. Поэтому в ТД эти процессы заменяются
одним изохорным отводом теплоты 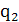 , процессом b-a.
, процессом b-a.
Основными параметрами цикла являются: термический КПД и работа цикла
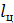 - влияет на экономичность,
- влияет на экономичность,
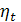 - влияет на мощность,
- влияет на мощность,
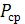 - влияет на крутящийся момент двигателей
- влияет на крутящийся момент двигателей
Выходные параметры
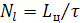 ,
, 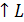 либо
либо 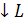
Входные параметры:  ,
, 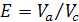
Цикл Отто.
Цикл быстрого сгорания (цикл с изохорным подводом теплоты, цикл
бензинового двигателя). Состоит из 4-х процессов:
1. адиабатное сжатие (процесс а-с);
2. изохорного подвода теплоты (с-z);
. адиабатного расширения (z-b);
4. изохорного отвода теплоты (b-a).

Температура в конце сжатия в точке с в цикле Отто (в цикле бензинового
двигателя) должна быть меньше температуры самовоспламенения топлива 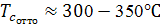 , поэтому степень сжатия не может
быть высокой
, поэтому степень сжатия не может
быть высокой


(т.е. объем в точке с у дизеля меньше, чем у бензина)
В точку с подается искра свечей зажигания (цикл с принудительным воспламенением
топлива, электрической искрой).
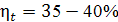
Лекция 15.
Цикл с изобарным проводом теплоты. Цикл с воспламенением от сжатия
Инженером Дизелем был предложен цикл работы ДВС, в котором отсутствует
ограничение степени сжатия (и следовательно КПД) температурой самовоспламенения
(возможностью детонации, как в цикле Отто). В цикле Дизеле сжимается воздух (а
не топливно-воздушная смесь, как в цикле Отто). Степень сжатия в цикле Дизеля
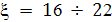

Цикл состоит из 4-х процессов
) а - с -адиабатное сжатие;
Тс 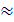 400 °С -
500 °С, что выше температуры
самовоспламенения топлива, поэтому при подачи в данную точку топлива,
происходит самовоспламенение.
400 °С -
500 °С, что выше температуры
самовоспламенения топлива, поэтому при подачи в данную точку топлива,
происходит самовоспламенение.
Точка а соответствует параметрам окружающей среды.
В цикле Дизеля процесс подвода теплоты (сгорания топлива) происходит
изобарно ( Р = const).
) c -z - изобарный подвод теплоты;
Топливо распыляется сжатым воздухом (от компрессора) одновременно с
перемещением поршня, поэтому давления не возрастает.
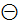 НЕДОСТАТОК: значительная часть мощности двигателя (до 10 %)
теряется на привод компрессора для сжатия воздуха.
НЕДОСТАТОК: значительная часть мощности двигателя (до 10 %)
теряется на привод компрессора для сжатия воздуха.
3) z - в -адиабатное расширение; Тz = 2000 °С
) в - а -изохорный отвод теплоты; Тв =1000 °С
Характеристиками цикла Дизеля являются те же параметры, что и в цикле
Отто, и добавляется r -
степень предварительного расширения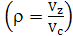
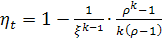
Цикл
Тринклера.

При высоких степенях сжатия (в цикле Дизеля). Выгода от высокого
термического КПД уменьшается, т.к. возрастает расход работы на преодоление сил
трения, т.е. уменьшается механический КПД (ηm).
Оптимальной является степень сжатия, при которой суммарный КПД будет
максимальным.
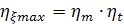
(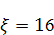 - оптимально)
- оптимально)
Также недостатком высокой степени сжатия является необходимость повышения
прочности деталей двигателя из-за возрастания сил, действующих на них, и
соответственно, увеличения массы деталей и двигателя в целом.
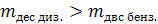 (в 1,5-2 раза)
(в 1,5-2 раза)
Стремление упростить конструкцию, повысить надежность двигателя,
отказаться от воздушного компрессора привело к созданию двигателя со смешанным
подводом теплоты.
Данный цикл был предложен и воплощен в реальном двигателе русским ученым
Густафом Васильевичем Тринклером.
В точке с происходит впрыск топлива под давлением больше 100 атмосфер,
создаваемого топливным насосом высокого давления (ТНВД), причем затраты
мощности двигателя на привод насоса ТНВД значительно меньше, чем на привод
воздушного компрессора.
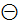 НЕДОСТАТОК: высокая шумность работы ТНВД.
НЕДОСТАТОК: высокая шумность работы ТНВД.
В точке с начинают сгорать легкие фракции топлива, происходит изохорный
подвод теплоты 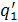 (c-z1 -быстрое сгорание). Затем сгорают более тяжелые
фракции, происходит изобарный подвод теплоты (z1- z2).
(c-z1 -быстрое сгорание). Затем сгорают более тяжелые
фракции, происходит изобарный подвод теплоты (z1- z2).
Характеристиками цикла являются те же параметры, что и в циклах Отто и
Дизеля, и добавляется λ - степень повышения давления
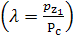
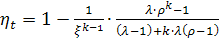
Термический КПД данного цикла возрастает с увеличением степени сжатия и
степени повышения давления, и уменьшается с увеличением степени
предварительного расширения.
Изображение
циклов Отто, Дизеля и Тринклера в T-S координатах. Сравнение циклов между
собой.

Цикл Отто.
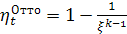
При увеличении степени сжатия (для повышения КПД) положение точки с
изменится, т.к. изменится температура сжатия.
Площадь, соответствующая работе цикла увеличится, т.о. КПД цикла 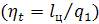 повысится.
повысится.

Цикл Дизеля.
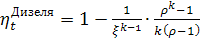
Термический КПД данного цикла является функцией степени сжатия ξ и степени предварительного
расширения ρ, при увеличении ξ и уменьшении ρ термический КПД возрастает

Цикл
Тринклера.
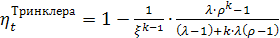
Термический КПД увеличивается с увеличением степени сжатия и уменьшается
с увеличением ρ.
Это объясняется следующим.
Чем больше степень сжатия ξ, тем больше степень полезного
рабочего расширения, следовательно, больше полезная результирующая работа
цикла.
Сравнение
циклов между собой по Т-S диаграмме.

Представим циклы с различным подводом теплоты на Т-S диаграмме.
Для того, чтобы было возможно сравнить циклы между собой, сравнения
необходимо проводить в подобных (равных) условиях:
· одинаковая начальная температура, и другие параметры (точка a)
· одинаковое количество отводимой теплоты q2 (процесс b-a)
· значение внутренней энергии в точке z одинаково (одинаковая температура)
lотто
< lтрин. < l диз , т.к. q1отто
< q1трин. < q1 диз

Т.о. мы графическим способом сравнили между собой циклы. Самый высокий
термический КПД - в цикле Дизеля.
Цикл
газотурбинных установок (ГТУ).
ГТУ является одним из видов теплового двигателя и имеет следующее
преимущество перед ДВС:
 Достоинства:
Достоинства:
а) имеет меньшую массу, при той же мощности (высокую удельную
мощность);
б) более высокий КПД, чем у поршневых ДВС.
 НЕДОСТАТКИ:
НЕДОСТАТКИ:
а) высокая частота вращения (более 10 000 об/мин), что ограничивает
их использование на наземных транспортных средствах;
б) оптимальным является только один режим работы (при определенной
частоте вращения).
ГТУ широко используется:
1. В качестве энергоустановок (для
привода генераторов электрического тока);
2. В качестве привода компрессоров (на
магистралях газо- и нефтепроводах);
3. В авиации;
4. На морских судах;
5. На ж/д локомотивах

Схема ГТУ.
Компрессор К нагнетает воздух в камеру сгорания КС. В камеру сгорания
подается топливо топливным насосом ТН, в КС происходит сгорание топлива при P=const. Из КС газы поступают в сопло С, где приводят в
движение колесо турбины Т, воздействуя на лопатки Л. Отработавшие газы ОГ
выпускаются в атмосферу.
Колесо турбины Т приводит в движение ТН и К (вспомогательные механизмы),
а также электрогенератор ЭГ, преобразующий кинетическую энергию в
электрическую.
Лекция 16.
Уравнение состояния реальных газов
Для решения
практических задач необходима наглядность физических свойств газов и рабочих
тел.
Уравнение состояния нельзя найти термодинамическим методом. Его получают
экспериментально, либо путем введения поправочных коэффициентов уравнения
состояния идеального газа.
Основные отличия реальных газов от идеального объясняются:
1. Наличием сил притяжения и
отталкивания между молекулами;
2. Молекулы реальных газов занимают
некоторый объем.
Данные факторы имеют все большее значение с повышением плотности газов.
Первая поправка учитывает силы притяжения, действующие в направлении
действия внешнего давления. Увеличиваем его на добавочное давление Δp, называемое внутренним.
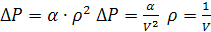
Вторая поправка учитывает объем, недоступный для движения молекул.

В - объем газа, учитывающий «недоступный объем», т.к. в связи с наличием
сил отталкивания молекул не могут быть доведены до соприкосновения.
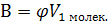
Эти поправки учитываются в уравнении Ван-дер-Ваальса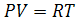
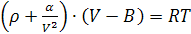
α, В- зависят от природы газа.
Погрешность данного уравнения возрастает с увеличением плотности (ρ)
Уравнение
Майера - Боголюбова.
В 1937 году ученый Майер и русский ученый Боголюбов получили уравнение,
которое более точно описывало уравнение идеального газа.
Уравнение Майера - Боголюбова
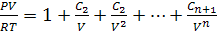
Сn - вириальные коэффициенты, которые
являются функцией температуры.
Уравнение позволяет более точно описать состояние газов при высоких
температурах или при очень низких температурах.
Фазовые
равновесия. Фазовые температуры.
Переход вещества из одной фазы в другую называется фазовым переходом.
Если однофазовая система пришла в равновесие, то температура и давление во всех
частях системы одинаковы.
Для многофазной системы верно: если одна фаза (и более) находится в
равновесии, то температура, давление и химические потенциалы равны во всех
частях системы.
В зависимости от давления и температуры вещество может находиться в
различных агрегатных состояниях (твердое, жидкое, газ, плазма).
Правило фаз
Гиббса.
Оно устанавливается для термодинамической системы, находящейся в
равновесии и имеющей несколько компонентов и несколько фаз:
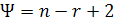
Ψ - число степеней свободы;
n -
число компонентов;
r -
число фаз в системе.
Для однокомпонентной системы, находящейся в одном фазовом состоянии:
Ψ=2, т.е. число независимых параметров
равно двум.
PV=RT
ПРИМЕР:
· Для двухфазной системы (кипящая вода с паром) число степеней свободы
равно единице (Ψ=1, при n=1, r=2).
· Для трехфазной системы (тройная точка воды), когда в
равновесии находится жидкая, твердая и газообразная фаза воды (Ψ=0, при n=1, r=3).
Отсюда следует, что вещества могут находиться в равновесии только при
постоянных и конкретных значениях температуры и давления, причем индивидуально
для каждого вещества.
Лекция 17.
Фазовая диаграмма воды

В P - T координатах.
· О - тройная точка воды;
· В равновесии существует три фазы в этой точке.
· К - критическая точка;
· Максимальное значение параметров Р и Т для сосуществования
2-х фаз.
· О - В - линия сублимации;
· О - А - линия плавления;
· О - К - линия кипения.
По Фазовой Р-Т диаграмме можно установить в каком агрегатном состоянии
будет находиться конкретное вещество, при заданных значениях давления и
температуры.
Фазовая диаграмма индивидуальна для каждого вещества.
Термин «газ» используют применительно к веществам, находящихся в
нормальных условиях в газообразном состоянии.
Термин «пар» применяют для обозначения газообразной фазы вещества,
находящихся при нормальных условиях в состоянии жидкости.
Насыщенный
пар. Перегретый пар. Водяной пар.
1. Водяной
пар - имеет широкое применение в энергетике и промышленности. Он используется в
качестве рабочего тела в паросиловых установках, тепловых и атомных станций, а
так же как теплоноситель в теплообменных аппаратах.
Парообразование - процесс превращения жидкости в пар.
Испарение - парообразование, происходящее только на свободной поверхности
тела (жидкости) при любой температуре.
Интенсивность парообразования индивидуальна для каждой жидкости.
При испарении температура жидкости понижается, т.к. из нее уходят
наиболее быстрые молекулы. И средняя кинетическая энергия оставшихся молекул
уменьшается.
Кипение. При повышении температуры жидкости, интенсивность испарения
возрастает, и при некоторой температуре насыщения (кипения), зависящей от
природы жидкости и давления окружающей среды, наступит парообразование во всем
объеме жидкости. Это явление называется кипение.
В качестве центра образования паровых пузырьков служат нерастворимые в
жидкости газы, мелкие частицы твердых тел, царапины на стенках сосудов, т.е.
конденсаты.
Затем пузырек увеличивается в объеме, за счет испаряющейся в нем
жидкости, вследствие чего растет подъемная (архимедова) сила. Пузырек
отрывается от стенок и проходит через объем жидкости в паровое пространство.
Температура кипения зависит от давления в паровом пространстве.
Давление температур кипения называют - давлением и температурой
насыщения.
Давление и температура остаются постоянными. Но температура зависит от
давления. Чем больше давление, тем выше конденсация.
Насыщенный пар.
При испарении жидкости одновременно происходит ее конденсация, т.е.
молекулы пара возвращаются обратно в жидкость. Причем по мере заполнения паром
пространства над жидкостью интенсивность парообразования снижается и ускоряется
процесс конденсации.
В некоторый момент скорость парообразования и конденсации сравняются, и в
системе наступит динамическое равновесие, т.е. число вылетевших молекул будет
равно числу возвратившихся.
Пар в этом случае имеет максимальную плотность и называется насыщенным.
Сухой
насыщенный пар.
Если вся жидкость при кипении перейдет в пар (при постоянном давлении и
температуре), то такой пар называется сухим насыщенным.
Перегретый
пар.
Если сухой пар нагревать при постоянном давлении, то его температура
будет возрастать и, получаемый при таком процессе пар, будет называться
перегретым.
Влажный
насыщенный пар.
Влажный насыщенный пар получается при неполном испарении жидкости и
является смесью сухого пара с мельчайшими капельками жидкости. Массовая доля
сухого пара во влажном, называется степенью сухости пара.
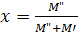
M"
- масса сухого насыщения пара (кг);
M' -
масса насыщенной жидкости во влажном паре (кг).
для сухого пара х = 1
для жидкости х = 0
В процессе парообразования х изменяется от 0 до 1.
Парообразование
при постоянном давлении.
Производство
водяного пара для промышленных нужд осуществляют при постоянном давлении.
Процесс
образования перегретого пара состоит из 3х частей:

Точка а соответствует температуре 0 °С
) a - b - подогрев
жидкости до температуры кипения;
Точка в - вода при температуре кипения 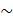 100°С
100°С
2) b - с - процесс парообразования при постоянной температуре;
Точка с - сухой насыщенный пар
) с - d - пароперегрев до высокой (требуемой) температуры пара.
Точка d - перегретый пар.
Лекция 18.
P-V диаграмма для пара (парообразование)

а-аn -изотерма, характеризующая состояние
жидкости при 00С;
в-вn - линия насыщения жидкости,
характеризующая состояние жидкости при температуре кипения (нижняя пограничная
кривая);
с-сn - линия сухого насыщенного пара (верхняя
пограничная кривая).
При некотором, вполне определенном для каждой жидкости, давлении
пограничные кривые сходятся в точке К, называемой критической. Эта точка
соответствует некоторому критическому состоянию вещества, при котором
отсутствуют различия между жидкостью и паром.
Пограничные кривые делят диаграмму на 3 области:
1. Левее нижней пограничной кривой находится область жидкости
2. Между верхней и нижней пограничными кривыми - область влажного
насыщенного пара.
3. Правее и выше верхней пограничной кривой - область перегретого пара.
Области сухого пара нет. Имеется только кривая сухого пара.
По P-V диаграмме можно определить агрегатное состояние вещества при
известном давлении. Например для давления Р = 22,064 МПа: Ткр = 373,95 0С; V = 0,0031038 м3/кг