Дослідження шкідливих речовин у тютюновому димі
ВСТУП
Сьогодні смертність населення
України визначається передусім неінфекційними захворюваннями, тісно пов’язаними
з широким розповсюдженням факторів ризику, які характерні для поведінки людини.
Серед них тютюнокуріння - основна причина передчасної смерті, якій можна
запобігти. Тютюн - фактор ризику більш ніж 25 хвороб.
Існують цифри та факти щодо куріння:
· за оцінками
Всесвітньої організаації охорони здоров’я (ВООЗ) близько третини дорослого
населення світу (серед яких 200 мільйонів - жінки) курять;
· кожного року в
світі тютюн викликає 3,5 мільйонів смертей, або 1000 - щодня;
· за прогнозами,
глобальна тютюнова «епідемія» забере життя 250 мільйонів сучасних дітей та
підлітків;
· за даним ВООЗ
Україна займає 17 місце серед країн, які споживають цигарки.
При тютюнопалінні
відбувається суха дистиляція і неповне згоряння висушених тютюнових листків в
незалежності від того, використовуються вони в натуральному вигляді (скручена в
трубочку), в цигарці чи в сигарі. При повільному згорянні виділяється дим, що є
неоднорідною (гетерогенною) сумішшю, що складається в середньому з 60 % різних
газів і 40 % мікроскопічних дьогтевих крапель (аерозолі). В газовій фракції
тютюнового диму міститься, крім азоту (59 %), кисню (13,4 %), ще й оксид
вуглецю (IV) (13,6 %), оксид вуглецю (II) (4 %), водяна пара (1,2 %), ціаністий
водень (0,1 %), оксиди Нітрогену, акролеїн та інші речовини.
В Україні з 16 грудня 2012 року
заборонено куріння в усіх громадських місцях - згідно з ухваленим у травні
законом «Про внесення змін до деяких законів щодо вдосконалення окремих
положень про обмеження місць куріння тютюнових виробів».
В різних країнах діють різні
обмеження тютюнопаління і штрафи
<#"699550.files/image001.jpg">, або ізонітрильну 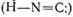 форму.
Дослідження ціанідної кислоти фізичними методами показали, що рівновага зміщена
виключно в напрямку нітрильної форми:
форму.
Дослідження ціанідної кислоти фізичними методами показали, що рівновага зміщена
виключно в напрямку нітрильної форми:
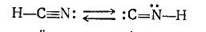
Вміст ізонітрильної форми в
ціанідній кислоті був доведений хроматографічним методом, припускають, що вміст
її становить близько 0,5-1,0%. Можливо, що висока токсичність ціанідної кислоти
обумовлена присутністю ізонітрильної форми.
Електронна структура ціанідної
кислоти
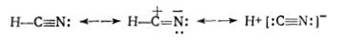
Ціанідна кислота гідролізує за
достатньо високої температури, процес проходить швидко лише при температурі
близько 1200оС
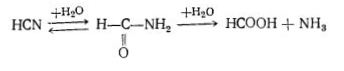
При взаємодії з лугами
<#"699550.files/image006.jpg">
Із сірковмісними
<#"699550.files/image008.jpg">
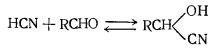
При високих температурах
ціанідна кислота взаємодіє з вуглеводнями, утворюючи нітрили
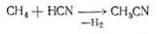
Галогени взаємодіють з
ціанідною кислотою з утворенням галогенціанідів
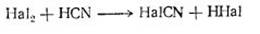
Взаємодія з хлором
<#"699550.files/image001.jpg">,
або ізонітрильну 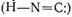 форму. Рівновага
зміщена виключно в напрямку нітрильної форми. А висока токсичність ціанідної
кислоти обумовлена присутністю ізонітрильної форми
форму. Рівновага
зміщена виключно в напрямку нітрильної форми. А висока токсичність ціанідної
кислоти обумовлена присутністю ізонітрильної форми
Ціанідна кислота гідролізує за
достатньо високої температури.
Ціанідна кислота взаємодіє з
лугами
<#"699550.files/image012.jpg">
На основі цієї реакції готують
індикаторний папір. Інтенсивність синього забарвлення паперу залежить від
концентрації ціанідної кислоти у повітрі. Подібним же чином можна приготувати
індикаторну трубку з силікагелем.
· Утворення гваякової
сині - реакція основана на окиснені компонентів своякової смоли до своякової
сині сіллю купруму(ІІ) в присутності ціанід-аніонів та води. Чутливість реакції
становить 0,001мг HCN в 1дм3 повітря. Така реакція не є специфічною(таке ж
забарвлення визивають окисники), а також аміак, формальдегід і сірчаний газ
заважають виявленню.
· Фенолфталінова
реакція - основана на окиснені фенолфталіна до фенолфталеїна при взаємодії з ціанідною
кислотою і сульфатом купруму у воді. Фенолфталеїн у лужному середовищі дає
характерне фіолетово-червоне забарвлення:
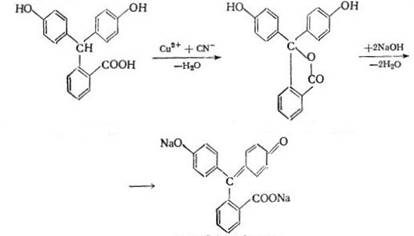
Мінімальна концентрація для
виявлення становить 0,01мг/дм3. Така реакція не є специфічною (таке ж
забарвлення проявляється в присутності інших окисників), а також аміак і
сірчаний газ заважають виявленню.
· Проба з
метилоранжем і хлоридом меркурію - основана на зміні кольору метилоранжа від
помаранчевого до рожевого під дією соляної кислоти, утвореною при взаємодії
ціанідної кислоти з хлоридом меркурію:
+ 2HCN → Hg(CN)2 + 2HCl
Мінімальна концентрація для
виявлення становить 0,01-0,03мг HCN в 1дм3 повітря. Реакція не специфічна, гази
кислотного характеру дають таку ж реакцію.
· Пікратна реакція -
при взаємодії пірата натрія з ціанідною кислотою в слабко лужному розчині,
колір розчину змінюється із жовтого до червоно-коричневого. Зміна забарвлення
пов’язана з утворенням ізопурпуру натрію
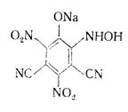
Мінімальна концентрація для
виявлення становить 0,12мг/дм3. Реакція специфічна, але для виявлення заважають
диціан та ацетон.
· Утворення
берлінської лазурі - при нагріванні розчину ціаніда калія з декількома краплями
розчину сульфату феруму(ІІ) ціанід перетворюється в гексаціаноферат калію
(фероціанід калію):
KCN + FeSO4 → K2SO4 +
Fe(CN)2(CN)2 + 4KCN → K4[Fe(CN)6]
При додаванні до розчину з
фероціанідом розбавленого розчину хлориду феруму(ІІІ) утворюється синій осад
берлінської лазурі (гексаціаноферат феруму (ІІІ)) (феро-фероціаніду):
K4[Fe(CN)6] + 4FeCl3 →
Fe4[Fe(CN)6]3 + 12KCl
Ця проба являється одною з найбільш
специфічних для виявлення ціанідної кислоти. При малому вмісті ціанідів в пробі
осад берлінської лазурі не утворюється, але розчин забарвлюється в синій або
синьо-зелений колір. Мінімальна концентрація для виявлення ціанідної кислоти
становить близько 0,001мг в 1дм3 повітря.
· Методи, основані на
реакціях глутаконового альдегіду - ціанід при дії хлораміна Т чи іншого
розчинного у воді хлораміна можна перетворити у хлорціан, який розриває
піридинове кільце з утворенням глутаконового альдегіда. Глутаконовий альдегід з
речовинами, які мають подвижний атом гідрогену, дає забарвлені сполуки.
Мінімальна концентрація для виявлення ціанідної кислоти становить 0,0001 -
0,0003 мг/дм3.
3.2
Загальна характеристика та опис методу дослідження ціанідів
Грунтуючись на наведених методиках,
ми провели декілька досліджень. Спроби з утворенням берлінської лазурі,
пікратна та бензидинова реації не дозволяли визначити ціанідну кислоту ні в
тютюновому димі, ні в розчині. Тому ми дійшли висновку, що основною причиною
невдалих дослідів, є те, що тютюновий дим, як багатокомпонентна система, має у
своєму складі альдегіди. Вони взаємодіють з синильною кислотою та ціанідами, що
призводить до суттєвого зниження концентрації ціанідної кислоти, яку ми
намагались визначити в тютюновому димі.
Оскільки наведені вище методики
визначення синильної кислоти виявились непридатними для нашого дослідження, ми
вирішили оптимізувати ту з них, яка, на нашу думку, була найбільш придатною. За
фундамент дослідження ми взяли методику бензидинової реації визначення
ціанідної кислоти. В наведеній методиці потрібно було приготувати індикаторний
папір. Інтенсивність синього забарвлення індикаторного паперу залежить від концентрації
ціанідної кислоти у повітрі. Детальний опис методики, яку ми взяли за основу,
наведений у додатку Д.
Спираючись на дану методику, ми
вирішили перевірити можливість застосування такого способу проведення досліду,
який ґрунтується на безпосередньому зв’язуванні ціанід-йонів з йонами
купруму(2+) одразу після переведення їх у розчин з цигаркового диму. Для цього
ацетат купруму (Cu(CH3COO)2∙H2O) розчинили у воді, приготувавши розчин з
приблизною концентрацією 1,5 г/дм3. Важливим було також і те, щоб розчин купрум
ацетату був достатньої концентрації для кількісного зв’язування ціанідів у
сполуку купрум(І) ціанід.
З пропусканням тютюнового диму через
розчин купрум(ІІ) ацетату одразу почав утворюватись осад, згідно рівнянь таких
реакцій:
+ + 2HCN → Cu(CN)2↓+ 2H+
Cu(CN)2→ 2CuCN↓ + (CN)2
Утворений ціан ((CN)2) (див. Додаток
Е) реагуючи з водою в розчині знову утворює ціанідну і ціанатну кислоти, які в
свою чергу реагують з Cu2+:
(CN)2 + H2O →HCN + HCNO+ +
2HCN → Cu(CN)2↓+ 2H++ + 2HCNO→ Cu(CNO)2↓+ 2H+
Після прокурювання через
поглинальний розчин диму цигарок, розчин з осадом закорковується і
відставляється для дозрівання на декілька годин. Отриманий осад фільтрується та
промивається достатньою кількістю промивної рідини до повного видалення йонів
Купруму(2+), адсорбованих на поверхні прихованокристалічного осаду. Повноту
видалення йонів Купруму(2+) контролюють відсутністю аналітичного ефекту у
фільтраті з K4[Fe(CN)6] - йони Cu2+ утворюють цегляно-червоний осад Cu[Fe(CN)6]
. Таке промивання потрібно для того, щоб отримані результати не були
завищеними. Причиною завищених результатів можуть слугувати всі наявні в осаді,
чи абсорбовані на його поверхні, йони або сполуки купруму, крім ціанідів
купруму. Тому з осаду вимивається весь «зайвий» купрум.
Після промивання, осад висушується,
фільтрувальний папір з осадом спочатку озолюється на пальнику, а потім
прожарюється у печі за температури 650°-700°С:
↓ + О2 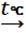 CuО
+ CО2 + N2
CuО
+ CО2 + N2
Після прожарювання осаду за такої
температури протягом 1-1,5 годин можна бути впевненими в тому, що всі органічні
речовини та інші сполуки тютюнового диму відсутні, так як і часточки
фільтрувального паперу.
Після цього осад розчиняється у
H2SO4 з додаванням декількох крапель HNO3:
CuО + 2H+ 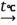
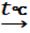 Cu2+ + H2O
Cu2+ + H2O
Отриманий розчин переносимо у
мірну колбу об’ємом 25см3 і доводимо дистильованою водою до мітки. З одержаного
розчину відбираються аліквоти об’ємом 2 см3 і титруються розчином ЕДТА в
присутності аміачного буферу з індикатором мурексидом за встановленою методикою
прямого титрування купруму з мурексидом. (див. Додаток Ж)
Після титрування батареї
розчинів з 6 мікроколб, ми проаналізували отримані результати. За нашими
розрахунками в кожній цигарці міститься близько 0,2623 - 0,3660 ∙ 10-3 г
ціанідної кислоти. Розрахунки наведено у додатку З.
Висновки до
розділу 3
Якісне визначення ціанідної кислоти
можна проводити різними хімічними методами. Які засновані як на її здатності
утворювати комплексні сполуки з солями металів, так і на реакціях, при яких
утворюються кольорові сполуки.
Найбільш поширеними є:
· Бензидинова реація
· Утворення гвоякової
сині
· Пікратна реакція
· Утворення
берлінської лазурі
Спроби з утворенням берлінської
лазурі, пікратна та бензидинова реація не дозволяли визначити ціанідну кислоту
ні в тютюновому димі, ні в розчині.
Можливою причиною невдалих спроб
визначення синильної кислоти в тютюновому димі, є те, що тютюновий дим, як
багатокомпонентна система, має у своєму складі альдегіди та інші компоненти,
які взаємодіють з синильною кислотою та ціанідами, що призводить до суттєвого
зниження їх концентрації і відсутності або спотворенні аналітичних ефектів.
Спираючись на методику, ми обрали
спосіб проведення досліду, оснований на безпосередньому зв’язуванні ціанідів з
йонами купруму одразу після переведення їх у розчин з цигаркового диму.
Перевагою створенної методики є
можливість переведення ціанідної кислоти у важкорозчинну сполуку, що запобігає
витраті ціанідної кислоти на побічні реакції.
Результати одержані з використанням
нашої методики вказують на присутність в тютюновому димі ціанідної кислоти в
середньому 0,2623 - 0,3660 ∙ 10-3 г на 1 цигарку. Це достатньо добре
узгоджується з теоретично передбаченими результатами 0,2400 ∙ 10-3 г на 1
цигарку.
Дана методика передбачає подальше
дослідження з метою удосконалення та підвищення точності й ефективності.
Можливі втрати при проведенні досліду можна пояснити так: установка, яка
використовувалась для прокурювання цигарок, не достатньо ефективна. Під час
проведення досліду було установка декілька разів зламувалась, що перешкоджало
кількісному переведенню ціанідної кислоти в розчин.
ВИСНОВКИ
Тютюнопаління - основна причина
передчасної смерті. В різних країнах діють різні обмеження тютюнопаління. Від
хвороб, розвиток яких є наслідком тютюнопаління, щорічно помирає 5,4 млн осіб.
Тобто 1 з 10 смертей у світі спричинена саме вживанням тютюнових виробів.
Основним для тютюнових виробів
елементом, через який їх вживають, є нікотин. Непрямим свідченням цього є
кількаразові спроби випуску сигарет без нікотину, які повсюдно потерпіли фіаско
на ринку.
Тютюновий дим є неоднорідною
(гетерогенною) сумішшю, яка складається в середньому з 60% різних газів і 40%
мікроскопічних дьогтьових крапель (аерозолів). При тютюнопалінні відбувається
суха дистиляція і неповне згоряння висушених тютюнових листків.
Складові тютюнового диму можна
поділити на такі групи: органічні речовини (нікотин, акролеїн, нітроза міни та
ін.); неорганічні речовини(чадний газ, оксиди Нітрогену, ціанідна кислота,
сполуки важких металів); вільні радикали. Тютюновий дим містить у своєму складі
канцерогени, які мають різну хімічну природу. Вони складаються з 44 окремих
речовин, 12 груп або сумішей хімічних речовин. Речовини, які містяться в тютюновому
димі, викликають рак, захворювання легенів та інші хвороби.
Серед складових, які присутні
в тютюновому димі, для нашого дослідження ми обрали ціанідну кислоту. Синильна
кислота синтезована вперше в 1782 році шведським хіміком Карлом Шеєле. Під час
Першої світової війни ціанідна кислота вперше була рекомендована як ОР.У мирний
час ціанідна кислота та її солі широко використовуються в промисловості , у
сільському господарстві. Ціанідна кислота має або нітрильну 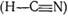 , або ізонітрильну
, або ізонітрильну
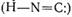 форму.
Ціанідна кислота взаємодіє з лугами
<http://uk.wikipedia.org/wiki/%D0%9B%D1%83%D0%B3%D0%B8_(%D1%85%D1%96%D0%BC%D1%96%D1%8F)>
, продукатами є ціаніди
<http://uk.wikipedia.org/wiki/%D0%A6%D1%96%D0%B0%D0%BD%D1%96%D0%B4%D0%B8>.
Важливою є реакція ціанідної кислоти з речовинами, які мають карбонільну групу
(ціангідрування). При отруєнні через ротову порожнину смертельними дозами для
синильної кислоти є 1 мг/кг маси тіла.
форму.
Ціанідна кислота взаємодіє з лугами
<http://uk.wikipedia.org/wiki/%D0%9B%D1%83%D0%B3%D0%B8_(%D1%85%D1%96%D0%BC%D1%96%D1%8F)>
, продукатами є ціаніди
<http://uk.wikipedia.org/wiki/%D0%A6%D1%96%D0%B0%D0%BD%D1%96%D0%B4%D0%B8>.
Важливою є реакція ціанідної кислоти з речовинами, які мають карбонільну групу
(ціангідрування). При отруєнні через ротову порожнину смертельними дозами для
синильної кислоти є 1 мг/кг маси тіла.
Якісне визначення ціанідної
кислоти можна проводити різними хімічними методами. Найбільш поширеними є:
бензидинова реація, утворення гвоякової сині, пікратна реакція, утворення
берлінської лазурі. Спроби з утворенням берлінської лазурі, пікратна та
бензидинова реація не дозволяли визначити ціанідну кислоту ні в тютюновому
димі, ні в розчині.
Тютюновий дим - багатокомпонентна
система, має у своєму складі альдегіди та інші компоненти, які взаємодіють з
синильною кислотою та ціанідами, що призводить до суттєвого зниження їх
концентрації і відсутності або спотворенні аналітичних ефектів.
Створена методика визначення
ціанідної кислоти в тютюновому димі не може вважатись точною, оскільки не
проведено було досліди щодо селективності та стехіометрії реакції осадження
CuCN, а також можливість перебігу побічних реакцій за участю Cu2+. Але
результати одержані з використанням нашої методики вказують на присутність в
тютюновому димі ціанідної кислоти у такому обсязі, що достатньо добре
узгоджується з теоретично передбаченими результатами.
Перевагою створенної методики є
можливість переведення ціанідної кислоти у важкорозчинну сполуку, що запобігає
витраті ціанідної кислоти на побічні реакції.
Список
використаної літератури
1. Андреева
Т.И. Табак и здоровье/ Андреева Т.И., Красовский К.С. - К., 2004. - 224с.
. Байєр
Б. Історія людства / Байєр Б., Бірштайн У. та ін. - К.: Промінь, - 2002. -
с.56-68.
. Бобков
С.С. Синильна кислота / Бобков С.С., Смірнов С.К. - М.: Химия. - 1970. - 172с.
4. Бражников В. В. Дифференциальные
детекторы для газовой хроматографии <http://www.xumuk.ru/encyklopedia/869.html>
- М.: 1974 .- с.172.
. Гапоненко В. Основні фонди тютюнової
промисловості УРСР та їх використання - К.: 1970, ч. 9. - 251с.
. Генкова Л. Л. Почему это опасно / Л. Л.
Генкова, Н. Б. Славков; пер. з болг. Ф. М. Калинко. - М.:Просвещение, 1989. -
с.2-9.
. Енциклопедія українознавства
<http://uk.wikipedia.org/wiki/%D0%95%D0%BD%D1%86%D0%B8%D0%BA%D0%BB%D0%BE%D0%BF%D0%B5%D0%B4%D1%96%D1%8F_%D1%83%D0%BA%D1%80%D0%B0%D1%97%D0%BD%D0%BE%D0%B7%D0%BD%D0%B0%D0%B2%D1%81%D1%82%D0%B2%D0%B0>:
в 10 т. [під ред. В. Кубійович
<http://uk.wikipedia.org/wiki/%D0%9A%D1%83%D0%B1%D1%96%D0%B9%D0%BE%D0%B2%D0%B8%D1%87_%D0%92%D0%BE%D0%BB%D0%BE%D0%B4%D0%B8%D0%BC%D0%B8%D1%80_%D0%9C%D0%B8%D1%85%D0%B0%D0%B9%D0%BB%D0%BE%D0%B2%D0%B8%D1%87>.
] - Париж; Нью-Йорк:Молоде життя
<http://uk.wikipedia.org/wiki/%D0%9C%D0%BE%D0%BB%D0%BE%D0%B4%D0%B5_%D0%B6%D0%B8%D1%82%D1%82%D1%8F>-1954-1989.
Т. ІІІ - с.36-48.
. Иванова Галина Михайловна.
Теплотехнические измерения и приборы : учеб. для студентов вузов, обучающихся
по направлению подгот."Теплоэнергетика" Г. М. Иванова, Н. Д.
Кузнецов, В. С.Чистяков. - 2-е изд., перераб. и доп. - Москва : Изд-во МЭИ,
2005 (Красноармейск (Моск.обл.) : Типография-Н). - 458с.
. Камразе Александр Наумович.
Контрольно-измерительные приборы и автоматика : [Учеб. для сред. ПТУ] / А. Н.
Камразе, М. Я. Фитерман. - 2-е изд., перераб. и доп. - Л. : Химия : Ленингр.
отд-ние, 1988. - с.12-18.
. Карапетьянц Михаил Христофорович. Общая
и неорганическая химия : [Учеб. для вузов] / М. Х. Карапетьянц, С. И. Дракин. -
3-е изд., - М. : Химия, 1994. - 588с.
. Краткая химическая энциклопедия [под
ред. И.Л. Кнунянц ]: в 5 т. - М.:1967. -Т. 4. - 639с.
. Кулаков, Михаил Васильевич.
Технологические измерения и приборы для химических производств: учебник для
студентов вузов, обучающихся по специальности "Автоматизация и комплексная
механизация химико - технологических процессов" / М. В. Кулаков. - Изд.
4-е, перепеч. с третьего изд. 1983 г. - Москва : АльянС, 2008. - 423с.
. Мала гірнича енциклопедія
<http://uk.wikipedia.org/wiki/%D0%9C%D0%B0%D0%BB%D0%B0_%D0%B3%D1%96%D1%80%D0%BD%D0%B8%D1%87%D0%B0_%D0%B5%D0%BD%D1%86%D0%B8%D0%BA%D0%BB%D0%BE%D0%BF%D0%B5%D0%B4%D1%96%D1%8F>:
3 т. [ За ред. В. С. Білецького
<http://uk.wikipedia.org/wiki/%D0%91%D1%96%D0%BB%D0%B5%D1%86%D1%8C%D0%BA%D0%B8%D0%B9_%D0%92%D0%BE%D0%BB%D0%BE%D0%B4%D0%B8%D0%BC%D0%B8%D1%80_%D0%A1%D1%82%D0%B5%D1%84%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%87>]
- Донецьк: Донбас, 2004.- Т. І. - 478c.
. Павленко В. А. Газоанализаторы / В. А.
Павленко /жур. Аналитическая химия, - М., 1965 - с.12-23.
. Пархотик И. И. Как сохранить здоровье.-
К.: Наукова думка, 1981.- с.45-49.
. Подчайнова В.Н. Медь / Подчянова В.Н.,
Сімонова Л.Н. - М: Наука - 1990. - 279с. - (Аналитическая химия елементов).
. Пришибил Р. Аналитическое применение
этилендиамин-тетрауксусной кислоты и родственных соединений - М: Мир - 1975 -
524с.
. Производственная и пожарная автоматика:
[Учеб. Для вузов МВД СССР] / Высш. инж. Пожар. - техн. шк. МВД СССР. - М.:
ВИПТШ, 1985 - Ч. 1: Производственная автоматика для предупреждения пожаров и
взрывов / А.А. Навацкий; Под общ. ред. Н. Ф. Шатрова. - М. : ВИПТШ, 1985. -195
с.
. Сігал А. Тютюни України / А. Сігал, -
К., 2002. -246 с.
. Сорты табака [Електронний ресурс] /
Игорь Константинов // Сайт о табаке и курении <http://www.tabacum.ru/>,
2006 - Режим доступу : www.tabacum.ru
. Справочник химика: 3 т. [под ред.
Никольский Б.П. и др.] - Л.: Химия, 1971. - Т. 2. - 1968 - Ленинград ; Москва :
Госхимиздат, 1951-1952. - 3 т.).
. Типи нарізання тютюну [Електронний
ресурс] / Роман Старчинский / Сайт о табаке и курении
<http://www.tabacum.ru/>, 2007 - Режим доступу : Tabakerka.dk
<http://www.tabakerka.dk/>
. Топольский Н. Г. Основы
автоматизированных систем пожаро- взрывоопасности объектов. - М.: МИПБ МВД
России, 1997. - 164 с.
. Тютюновий дим [Електронний ресурс] / За
матеріалами електронної енцеклопедії - вікіпедія - Режим доступу :
<http://uk.wikipedia.org>
. Федоров Л. А. Ни дня без химии :
(Календарь-справ. по хим. безопасности) / Центр экол. политики России, Союз «За
хим. Безопасность». - М., 1999. - 95с.
. Шварценбах Г. Комплексонометрическое
титрование / Шварценбах Г., Флашка Г. - М: Химия - 1970 - 360с.
. Brotherton Т. К., Lynn JW, The
synthesis and chemistry of cyanogen, "Chemical reviews", 1959. - р.
841