Биоэнергетика: преобразование энергии в биологических системах и роль нарушений энергетики клетки в патологических процессах
Биоэнергетика:
преобразование энергии в биологических системах и роль нарушений энергетики
клетки в патологических процессах
1. Биоэнергетика клетки
клетка митохондрия энергетика энергия
Молекулярные механизмы потребления энергии живой клеткой,
механизмы преобразования энергии в клетке в форму, которая может быть
использована для совершения различных видов полезной работы (биосинтез,
транспорт веществ, мышечное сокращение и т.д.) изучает Биоэнергетика - наука о
«судьбе» энергии в клетке. Энергетика биологических мембран (биоэнергетика)
представляет одну из точек роста современной биохимии, биофизики,
физико-химической биологии.
Источником энергии для большинства биологических процессов
является Солнце. Фотосинтезирующие организмы используют энергию света,
излучаемого Солнцем, для синтеза органических соединений, которые, в свою
очередь, служат строительным материалом и источником энергии для животных и
других организмов, неспособных самостоятельно усваивать энергию солнечного
света. Энергия света, поглощаемого фотосинтезирующими организмами, в ходе
многочисленных световых и темновых стадий фотосинтеза преобразуется в
химическую энергию макроэргических (богатых энергией) соединений, которые и
являются непосредственным источником энергии для процессов биосинтеза. К числу
наиболее важных макроэргических соединений, которые служат универсальным
источником химической энергии для всех организмов, относится молекула
аденозинтрифосфорной кислоты (ATP). Молекула АТР впервые выделена в 1929 году
Фиске и Суббароу из кислых экстрактов мышц. Вскоре после этого было
установлено, что АТР является участником большинства процессов энергетического
обмена в живой клетке. В 1931 году академик В.А. Энгельгардт обнаружил связь
между синтезом АТР и клеточным дыханием (явление окислительного
фосфорилирования). Позднее он установил, что АТР участвует в мышечном
сокращении. В 1941 году Липман сформулировал основной закон биоэнергетики,
согласно которому энергия внешнего источника сначала запасается в форме
химической энергии молекул АТР и лишь затем используется для совершения
полезной работы. Представление об АТР как универсальной «энергетической валюте»
нашло многочисленные подтверждения и стало краеугольным камнем всей
биоэнергетики. Подавляющее большинство энергоемких биологических процессов,
таких, как реакции биосинтеза, перенос ионов и различных веществ внутри клетки,
мышечное сокращение, сопряжено с энергодонорной реакцией гидролиза АТР, в ходе
которой происходит выделение энергии:
+ Н2О => ADP (аденозиндифосфорная кислота) + Pi
(неорганический фосфат) + энергия.
Наряду с этими процессами в клетке происходят
энергоакцепторные реакции синтеза АТР, которые компенсируют убыль АТР:
+ Pi + энергия => АТР + H2O.
2. Митохондриальная мембрана. ЭТЦ Митохондрий
2.1
Структурно-функциональная организация митохондрий
Митохондрия имеет две мембраны: внутреннюю и наружную,
и, соответственно, две камеры (внутреннюю и наружную), отделенные
друг от друга внутренней мембраной. Инвагинации внутренней мембраны в полость
внутренней камеры образуют кристы. Пространство между кристами и наружной
мембраной непрерывно и формирует единственную камеру межмембранного
пространства. Соответственно, матрикс, окруженный складками
внутренней мембраны, образует внутреннюю камеру (Рис. 2). Внешняя митохондриальная
мембрана проницаема для малых молекул и ионов, которые перемещаются
через трансмембранные каналы, сформированные семейством интегральных мембранных
белков, названных поринами. Имеются также потенциал-зависимые анионные каналы,
образованные чувствительными к мембранному потенциалу наружной мембраны
поринами, которые позволяют обмениваться метаболитами между митохондрией и
цитоплазмой.
Внутренняя мембрана непроницаема для Н+, и это
чрезвычайно важное свойство мембраны является ключевым для митохондриальной
трансдукции энергии. У химических веществ, таких как ионы и малые
молекулы, которые пересекают внутреннюю мембрану, есть специфические
транспортеры. Внутренняя мембрана содержит как интегральные белки - ключевые
катализаторы окислительнго фосфорилирования - дыхательные комплексы
электронтранспортной цепи переноса электронов, так и АТФ - синтазный комплекс.
2.2
Компоненты митохондриальной дыхательной цепи и дыхательные комплексы
Митохондриальная дыхательная цепь состоит из ряда
переносчиков электронов, которые функционируют как
окислительно-восстановительного пары (Рис. 1). В качестве таких пар выступают,
главным образом, простетические группы интегральных белков. Выделяют
четыре транспортера электронов, или дыхательных комплекса (I-IV), каждый из
которых способен катализировать процесс переноса электронов по ЭТЦ. Помимо
комплексов дыхательной цепи перенос электронов обеспечивают ряд
низкомолекулярных переносчиков - челноков: убихинон, цитохром c. Как отмечалось, перенос
электронов по ЭТЦ вдоль мембраны формирует перенос протонов через мембрану.
Комплекс I
(НАДН-убихиноноксидоредуктаза; НАДН-дегидрогеназа) состоит из 42-43
различных полипептидов, включая FMN-содержащий флавопротеид и 6 железо-серных
центров. Комплекс I по своей структуре имеет L-форму с двумя «руками»:
длинной «рукой», состоящей из гидрофобного мембранного белка, находящегося в
липидном слое внутренней митохондриальной мембраны, и короткой «рукой», имеющей
гидрофильную часть, выступающую в матрикс и содержащую FMN и активный центр
связывания НАДH.
Эти две важные функциональные части комплекса I имеют независимое
генетическое происхождение.
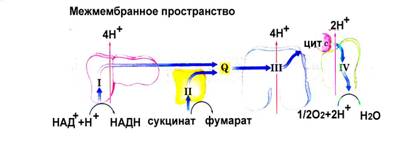
Рисунок 1. Организация электронтранспортной цепи митохондрий
Комплекс I - НАДН-убихиноноксидоредуктаза; НАДН-дегидрогеназа, Комплекс
II - сукцинатдегидрогеназа;
сукцинат-убихинон оксидоредуктаза, Комплекс III - комплекс цитохромов bc1; убихинон-цитохром c оксидоредуктаза, Комплекс
IV - цитохром c оксидаза;
цитохромоксидаза (цитохром c-O2 оксидоредуктаза).
Комплекс I, выделяют путем мембранной солюбилизации по методу,
предложенному У. Хатефи (Hatefi Y., 1985). Для исследования функциональной
активности комплекса I используют тест на чувствительность к ротенону -
специфическому стехиометрическому ингибитору комплекса I в митохондриях.
Убихинон - растворимый в липидной фазе бензохинон с длинной
боковой изопреноидной цепью, который способен перемещаться
путем диффузии в каждом из двух слоев бислоя фосфолипидов внутренней
мембраны и обеспечивать челночный перенос электронов между мембранными белками.
Комплекс II (сукцинатдегидрогеназа;
сукцинат-убихинон оксидоредуктаза) - мембраносвязанный компонент цикла лимонной
кислоты (цикла Кребса), который функционирует и как фрагмент
митохондриальной дыхательной цепи. В составе комплекса II - интегрального белка
имеются ковалентно связанный FAD и железо-серные центры,
локализованные в мембранном внешнем домене, которые катализируют перенос
электронов от сукцината к убихинону и гему цитохрома b, находящемуся в
гидрофобном мембранном домене.
Комплекс III (комплекс цитохромов bc1; убихинон-цитохром c оксидоредуктаза) состоит
из 9-10 полипептидов, 3 из которых участвуют в
окислительно-восстановительных реакциях. Кроме того, с двумя
отдельными доменами комплекса III связаны две молекулы убисемихинона.
Комплекс IV (цитохром c оксидаза;
цитохромоксидаза; цитохром c-O2 оксидоредуктаза) - финальный катализатор
дыхательной цепи митохондрий. Функция комплекса IV заключается в
восстановлении O2 до H2O за счет передачи четырех электронов от восстановленного
цитохрома c
в процессе, который использует 4 Н+ из матрикса. Стоит отметить, что
дисфункция комплекса IV наблюдается при многих патологических
состояниях, в процессе старения.
Стехиометрия комплексов дыхательной цепи -
интересный предмет исследований. Ранние спектрофотометрические исследования
переносчиков электронов в изолированных митохондриях и определение содержания
дыхательных комплексов в митохондриальных фрагментах,
препарированных акустическими или химическими воздействиями на митохондрии,
показали, что они находятся в простых мольных соотношениях. Электронные
переносчики и комплексы образуют функциональные ансамбли («сборки») с
характерными белок-белковыми взаимодействиями, которые эффективны
для быстрого переноса электронов. Кроме того, расположение митохондриальных
комплексов характеризуются малыми межмолекулярными расстояниями, что
препятствует их медленному дрейфу и существенным перемещениям в мембране,
способным привести к потере своей специфической функции. Отдельная митохондрия
печени содержит  10000 полных дыхательных сообществ (комплексов),
их количество увеличено в митохондриях почки и в 2 раза больше в митохондриях
сердца по сравнению с митохондриями печени.
10000 полных дыхательных сообществ (комплексов),
их количество увеличено в митохондриях почки и в 2 раза больше в митохондриях
сердца по сравнению с митохондриями печени.
Комплексы I, III и IV взаимодействуют между собой с образованием суперкомплексов,
характеризующихся определенным стехиометрическим составом, начиная от дрожжей и
заканчивая более высокими уровнями организации у растений и
млекопитающих. Недавно сообщалось о наличии суперкомплексов I1III2 и I1III2IV1 в митохондрии сердца
быка.
Окисление и электрохимические потенциалы в митохондриальной
дыхательной цепи. Электроны, последовательно восстанавливая компоненты
электронтранспортной цепи, поступают от доноров электронов - НАДН или сукцината
к акцептору - O2. Cогласно уравнению Нернста, электроны движутся по ЭТЦ в направлении
компонентов с более положительными окислительными потенциалами (стандартными
окислительно-восстановительными потенциалами, определяемыми отношением концентраций
окисленных и восстановленных форм). Различия в окислительно-восстановительном
потенциале электронных переносчиков определяют экзэргонические
реакции перекачки Н+ в межмембранное пространство.
Комплексы I, III и IV функционируют как протонные (Н+) насосы, действуя
последовательно относительно электронного потока и параллельно
относительно потока Н+. Протонные насосы питаются свободной энергией
сопряженных окислительно-восстановительных реакций, протекающих в
митохондрии, при этом катализируемое окисление и выброс Н+ являются
и векторными (строго направленными) и сопряженными реакциями.
Движение Н+ осуществляется в направлении от матрикса к
межмембранному пространству, благодаря чему матрикс заряжается отрицательно (N-сторона), а
межмембранное пространство - положительно (P-сторона). Например, комплекс
I катализирует два
одновременных и обязательных процесса: экзергоническую передачу
одного протона и одного электрона от НАДН и перенос второго Н+ из
матрикса к убихинону, сопряженных с эндергоническим переносом 4 Н+
из матрикса в межмембранное пространство.
Химическая свободная энергия падения
окислительно-восстановительного потенциала электронов, проходящих
через дыхательные комплексы, используется для создания Н+
электрохимического градиента (потенциала 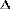 µH), выражаемого
в единицах электрического потенциала как протон - движущая сила -
µH), выражаемого
в единицах электрического потенциала как протон - движущая сила - 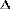 p, рассчитываемая по
уравнению:
p, рассчитываемая по
уравнению:
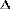 p (мВ) =
p (мВ) = 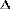
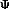 m - (2.3 RT/F)
m - (2.3 RT/F) 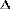 pH,
pH,
где: 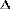
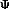 m - трансмембранный электрический
потенциал внутренней митохондриальной мембраны,
m - трансмембранный электрический
потенциал внутренней митохондриальной мембраны, 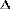 pH - градиент pH на внутренней мембране; R, T, и F - газовая постоянная,
абсолютная температура и константа Фарадея, соответственно. При
температуре 37 °C
pH - градиент pH на внутренней мембране; R, T, и F - газовая постоянная,
абсолютная температура и константа Фарадея, соответственно. При
температуре 37 °C 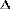 p =
p = 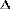
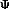 m - 60
m - 60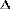 pH. Основной вклад в
создание
pH. Основной вклад в
создание 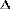 p в большинстве случаев
вносит
p в большинстве случаев
вносит 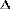
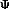 m, который количественно составляет примерно
150-180 мВ,
m, который количественно составляет примерно
150-180 мВ, 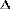 p равна 200-220 мВ.
p равна 200-220 мВ. 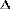 p - движущая сила процесса
фосфорилирования АДP и торможения потока электронов в контролируемом
метаболическом состоянии (в отсутствие АДP). Протонный потенциал
p - движущая сила процесса
фосфорилирования АДP и торможения потока электронов в контролируемом
метаболическом состоянии (в отсутствие АДP). Протонный потенциал 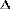 µH состоит из двух
компонентов: 1) электрического (
µH состоит из двух
компонентов: 1) электрического ( 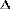
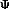 m) и 2) химического или осмотического (
m) и 2) химического или осмотического (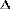 pH). Биофизическая основа
дыхательного контроля заключается в том, что
pH). Биофизическая основа
дыхательного контроля заключается в том, что 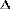 p в состоянии остановить
экзергоническое окисление субстратов вследствие установления равновесия между
свободной энергией электронного потока между
окислительно-восстановительными парами ЭТЦ и потоком Н+ между камерами
митохондрии. Кроме того, мембранный потенциал обеспечивает движущую силу для
переноса катионов, таких как K + и Ca2 +, активно поглощаемых митохондрией.
p в состоянии остановить
экзергоническое окисление субстратов вследствие установления равновесия между
свободной энергией электронного потока между
окислительно-восстановительными парами ЭТЦ и потоком Н+ между камерами
митохондрии. Кроме того, мембранный потенциал обеспечивает движущую силу для
переноса катионов, таких как K + и Ca2 +, активно поглощаемых митохондрией.
Роль электрохимического потенциала и F1-АТP-азного молекулярного
ротора в фосфорилировании АДP. В целом процесс окислительного фосфорилирования критически
зависит от целостности и непроницаемости внутренней митохондриальной
мембраны. Первая часть процесса заключается в преобразовании химического потенциала
НАДН и энергии окисления янтарной кислоты (сукцината) в Н+
электрохимический градиент, вторая часть процесса заключается в
катализируемом АТP-синтазой эндергоническом синтезе АТP за счет использования
энергии протонного градиента. Этот процесс термодинамически возможен, поскольку
освобождаемая энергия при переносе электронов по ЭТЦ и движущая протонная сила
сохраняют достаточно свободной энергии, приблизительно равной 34 кДж на моль
электронной пары, чтобы привести к ресинтезу одного моля АТP, требующему  32 кДж.
32 кДж.
Митохондриальная АТP-синтаза (комплекс V) является АТP-азой F-типа, имеющей два
различных компонента: F1 - периферический мембранный белок, и F0 - интегральный белок,
являющийся неотъемлемой частью внутренней митохондриальной мембраны.
Каталитический домен F1 - шаровидное сообщество 5 белков - α, β, γ, δ, и ε со стехиометрией 3:3:1:1:1. γ-, δ-, и ε-субъединицы формируют
основу белкового ансамбля. Движение субъединиц АТФ-синтазы
чрезвычайно важно для выполнения ее функции, частота - 50-100 тактов
в секунду. Вращение, которое использует энергию Н+
потока, осуществляется в F0 субъединице. Скорость митохондриального дыхания
зависит от доступности АДP для осуществления функции комплекса F1-АТP. Градиенты АДP и АТP через внутреннюю
мембрану уравновешиваются активностью транслоказы адениннуклеотидов,
функция которой состоит в обеспечении поступления АДP в матрикс и АТP в цитозоль для
осуществления энергозависимых процессов.
Экспериментально установлено, что для синтеза одной
молекулы АТP
требуется перемещение  3-4 Н+. Эффективность
фосфорилирования в изолированной митохондрии определена как отношение
ADP/O с экспериментальными
значениями 2.6-2.7 для NAD-зависимых субстратов и 1.6-1.7 для окисления
сукцината. Эти значения близки к отношениям ADP/O - 2.5 и 1.5,
соответственно, которые были получены теоретически, полагая, что количество
перекачиваемых Н+ при переносе пары электронов равняется
10 для НАДН и 6 для сукцината.
3-4 Н+. Эффективность
фосфорилирования в изолированной митохондрии определена как отношение
ADP/O с экспериментальными
значениями 2.6-2.7 для NAD-зависимых субстратов и 1.6-1.7 для окисления
сукцината. Эти значения близки к отношениям ADP/O - 2.5 и 1.5,
соответственно, которые были получены теоретически, полагая, что количество
перекачиваемых Н+ при переносе пары электронов равняется
10 для НАДН и 6 для сукцината.
Митохондриальная секвестрация Ca2 +. Добавление ионов Ca2+ к изолированным
митохондриям даже в присутствии АДP приводит к их захвату
(секвестрации) в энергозависимом процессе. Митохондрия поглощает
Ca2+ в обмен на Н+ в процессе, приводимом в действие АТP или мембранным
потенциалом, которые управляют Ca2+/H+ - насосом со
стехиометрией 1:1. Митохондрии накапливают большое количество Ca2+ с одновременным
поглощением Pi и осаждением Ca2+ в матриксе в виде нерастворимой соли, подобной
гидроксилапатиту, в связи с чем концентрация Ca2 + в матриксе изменяется
умеренно. Другой путь поступления Ca2+ в митохондрию функционально связан с открытием Ca2+-опосредованных пор
высокой проницаемости. Внезапное увеличение проницаемости внутренней
митохондриальной мембраны под влиянием ряда факторов вызывает
истечение и втекание больших молекул и ионов, которые нарушают мембранный
потенциал. Внутримитохондриальный Ca2+ признан аллостерическим активатором
некоторых матриксных дегидрогеназ, таких как NADН+-изоцитратдегидрогеназа,
пируватдегидрогеназа, α-кетоглутаратдегидрогеназа
кофактором митохондриальной NO-синтазы (mtNOS).
3.
Молекулярные преобразователи энергии
Энергопреобразующие мембраны способны к трансформации
химической энергии окисляемых субстратов, АТP, либо энергии светового
излучения в электрическую энергию, а именно в трансмембранную разность
электрических потенциалов 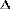
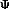 m или в энергию разности концентраций веществ в
растворах, разделенных мембраной (осмотическую энергию). Среди
энергопреобразующих мембран можно выделить такие структуры как внутренняя
мембрана митохондрий, внутренняя (цитоплазматическая) мембрана бактериальных
клеток, мембраны тилакоидов хлоропластов и цианобактерий, вакуолярная мембрана
(тоноласт) растений и грибов. Ряд мембран не несут энергетических функций.
Энергетические превращения в живой клетке могут быть разделены на две группы,
локализованные в мембранах и использующие энергию сопрягающих ионов, и
локализованные в цитоплазме клетки и использующие энергию АТP и других
высокоэнергетических веществ. АТP образуется из АДP и неорганического фосфата системами
фотосинтетического, дыхательного и субстратного фосфорилирования.
m или в энергию разности концентраций веществ в
растворах, разделенных мембраной (осмотическую энергию). Среди
энергопреобразующих мембран можно выделить такие структуры как внутренняя
мембрана митохондрий, внутренняя (цитоплазматическая) мембрана бактериальных
клеток, мембраны тилакоидов хлоропластов и цианобактерий, вакуолярная мембрана
(тоноласт) растений и грибов. Ряд мембран не несут энергетических функций.
Энергетические превращения в живой клетке могут быть разделены на две группы,
локализованные в мембранах и использующие энергию сопрягающих ионов, и
локализованные в цитоплазме клетки и использующие энергию АТP и других
высокоэнергетических веществ. АТP образуется из АДP и неорганического фосфата системами
фотосинтетического, дыхательного и субстратного фосфорилирования.
В большинстве случаев преобразование энергии в биологических
мембранах можно описать схемой:
энергетические ресурсы => ∆µI => полезная работа,
где ∆µI есть трансмембранная
разность электрохимических потенциалов иона I. Энергетические ресурсы,
потребляемые мембранной системой, сначала используются для транспорта иона I через мембрану против
сил электрического поля и в направлении большей концентрации I (энергизация мембраны).
Затем энергия, накопленная в электрической и осмотической форме, используется в
качестве движущей силы, чтобы совершать ту или иную полезную работу. Таким
образом, процессы утилизации внешней энергии и совершения за ее счет работы
оказываются сопряжены через образование и использование ∆µI. Поэтому ион I может быть назван
сопрягающим ионом.
Существует классификация биологических мембран, основанная на
том, какой ион используется мембраной как сопрягающий.
) Энергопреобразующие мембраны, использующие H+ как сопрягающий ион:
· внутренняя мембрана митохондрий;
· мембрана тилакоидов хлоропластов;
· мембрана бактериальных хроматофоров;
· внешняя мембрана клеток растений и грибов;
· мембрана вакуолей (тонопласт) растений и грибов.
2) Энергопреобразующие мембраны, использующие Na+ как сопрягающий ион:
· внешняя мембрана животной клетки;
· внутренняя (цитоплазматическая) мембрана
некоторых морских аэробных бактерий и морских анаэробных бактерий.
3) Энергопреобразующие мембраны, роль которых
ограничивается созданием ионного градиента:
· мембраны лизосом;
· внешняя мембрана некоторых животных клеток
(например, слизистой желудка);
· саркоплазматический ретикулум и другие
мембранные структуры, накапливающие Ca2+.
4) Мембраны, не способные к превращению энергии:
· внешняя мембрана митохондрий;
· внешняя мембрана оболочки хлоропласта;
· внешняя мембрана бактерий;
· мембрана пероксисом.
5) Мембраны, энергетические функции которых не
доказаны, но и не исключены:
· эндоплазматический ретикулум;
· кариолемма.
4. Роль митохондриальных нарушений в развитии
патологии
Среди наиболее распространенных болезней цивилизации,
принимающих масштаб эпидемий, можно выделить: диабет, нейро-дегенеративные
расстройства, остеохондроз, метаболический синдром. В основе проявлений
метаболического синдрома (и ряда других болезней цивилизации) лежит первичная
инсулинорезистентность и сопутствующая гиперинсулинемия. Дисфункция
митохондрий, гиперпродукция оксида азота и реактивных форм кислорода играют
важную роль в развитии диабетического и токсического поражения печени. Мягкое
разобщение митохондрий, использование внутримитохондриальных антиоксидантов и
биоэнергетических субстратов для коррекции дисфункции митохондрий представляет
перспективный терапевтический подход в коррекции многих патологических
состояний.
диабет - клинический симптомокомплекс, обусловленный
первичной или вторичной инсулиновой недостаточностью, сложное
полифункциональное заболевание, характеризующееся многообразными
метаболическими нарушениями, гипергликемией, глюкозурией, развитием ранней
микро- и макроангионатии. По различным источникам в мире насчитывается от 120
до 180 млн. больных диабетом, что составляет 2-3% от всего населения планеты;
дисбактериоз - нарушение состава микрофлоры кишечника, что создает
фон для развития многих хронических заболеваний;
аллергии;
атеросклероз - на сегодняшний день сердечно-сосудистые
заболевания являются главной медико-социальной проблемой, причиной
преждевременных летальных исходов (около 55% эпизодов), инвалидности (примерно
в 43% случаев) и временной нетрудоспособности (около 9%) среди населения
экономически развитых стран;
Следует отметить, что наиболее распространенные хронические
неинфекционные заболевания, такие, как рак, сахарный диабет,
сердечно-сосудистые и нейродегенеративные заболевания, - это возрастные,
многофакторные, полигенные заболевания, часто имеющие значительный
неферментативный, неметаболический, химический компонент.
Заключение
Дыхание - основной процесс превращения энергии в
эукариотических клетках, который осуществляется в митохондриях.
Нарушения структуры и функции митохондрий представляют
ключевой этап развития многих патологических состояний.
Супероксианион-радикалы, генерируемые миохондриальной респираторной цепью,
представляют основной источник окислительных повреждений в клетке, которые
могут явиться в свою очередь важнейшей причиной нейродегенеративных
расстройств, диабетических осложнений, старения. Образование свободных
радикалов митохондриями зависит от величины митохондриальной протон-движущей
силы. Мягкое разобщение, использование внутримитохондриальных антиоксидантов
представляет перспективный терапевтический подход коррекции многих
патологических состояний.
) Важнейшая биологическая функция преобразования энергии
локализована во внутренней митохондриальной мембране. Перенос электронов через
комплексы электрон транспортной цепи приводит к синтезу АТФ в реакции
окислительного фосфорилирования.
) Согласно современным представлениям комплексы ЭТЦ
организованы в виде суперкомплексов, что позволяет осуществлять перенос
электронов без диффузии промежуточных продуктов в окружающую среду.
) Нарушения структурной организации и функциональной
активности митохондрий связано с развитием разнообразных состояний.
Библиографический список
1.
Скулачев В.П. Законы биоэнергетики // Соросовский Образовательный Журнал. 1997.
№1. С. 9-14.
.
Романовский Ю.М., Тихонов А.Н. Молекулярные преобразователи энергии живой
клетки. Протонная АТФ-синтаза - вращающийся молекулярный мотор // Успехи
Физических Наук. 2010. Т. 180. С. 931-956.
.
Скулачев В.П. Энергетика биологических мембран. - М.: Наука. 1989. 564 с.
. Mitchell P. Coupling of phosphorylation to electron and hydrogen
transfer by chemiosmotic type of mechanism. // Nature. 1961. V. 191. Р. 144-148
. Green D.E. On the enzymic mechanism of oxidative phosphorylation
/ D.E. Green, Z.H. Vande // Proc. Natl. Acad. Sci. USA. - 1982. - Vol. 79. - P
1064-1068.
. Pullman M.E. A soluble protein fraction required for coupling
phosphorylation to oxidation in submitochondrial fragments of beef heart
mitochondria / M.E. Pullman, H. Penefsky, E. Racker // Arch. Biochem. Biophys.
- 1958. - Vol. 76. P. 227-230.
. Boyer P.D. ATP synthase-past and future / P.D. Boyer // Biochim.
Biophys. Acta. - 1998. - Vol. 1365. - P. 3-9.
. Mitchell P. Stoichiometry of proton translocation through the
respiratory chain and adenosine triphosphatase systems of rat liver
mitochondria / P. Mitchell, J. Moyle // Nature. - 1965. - Vol. 208. P. 147-151.
. Mitchell P. Estimation of membrane potential and pH difference
across the cristae membrane of rat liver mitochondria / P. Mitchell, J. Moyle
// Eur. J. Biochem. - 1969. - Vol. 7. - P. 471-484.