Гидролиз солей
Введение
Гидролиз солей - это химическое взаимодействие ионов соли с ионами воды,
приводящее к образованию слабого электролита.
Если рассматривать соль как продукт нейтрализации основания кислотой, то
можно разделить соли на четыре группы, для каждой из которых гидролиз будет
протекать по-своему.
Соль, образованная сильным основанием и сильной кислотой (KBr, NaCl, NaNO3),
гидролизу подвергаться не будет, так как в этом случае слабый электролит не
образуется. Реакция среды остается нейтральной.
1. Гидролиз
солей
Гидролиз
солей - разновидность реакций гидролиза, обусловленного протеканием реакций
ионного обмена в растворах (преимущественно, водных) растворимых
солей-электролитов. Движущей силой процесса является взаимодействие ионов
<https://ru.wikipedia.org/wiki/%D0%98%D0%BE%D0%BD> с водой, приводящее к
образованию слабого электролита
<https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D1%82>
в ионном или (реже) молекулярном виде («связывание ионов»).
Различают
обратимый и необратимый гидролиз солей:
.
Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону):
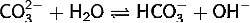 (1)
(1)
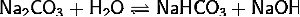 (2)
(2)
(раствор
имеет слабощелочную среду, реакция протекает обратимо <https://ru.wikipedia.org/wiki/%D0%9E%D0%B1%D1%80%D0%B0%D1%82%D0%B8%D0%BC%D1%8B%D0%B5_%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B8>,
гидролиз по второй ступени протекает в ничтожной степени)
.
Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону):
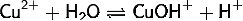 (3)
(3)
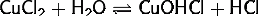 (4)
(4)
(раствор
имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени
протекает в ничтожной степени)
.
Гидролиз соли слабой кислоты и слабого основания:
 (5)
(5)
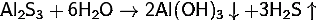 (6)
(6)
(равновесие
смещено в сторону продуктов, гидролиз протекает практически полностью, так как
оба продукта реакции уходят из зоны реакции в виде осадка или газа).
.
Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор
нейтрален.
.1
Количественные характеристики гидролиза
Количественно гидролиз соли характеризуется степенью гидролиза h и
константой гидролиза К.
Степень гидролиза. Показателем глубины протекания гидролиза является
степень гидролиза. Доля вещества, подвергшегося гидролизу, называется степенью
гидролиза:
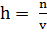 (7)
(7)
где h - степень гидролиза;
п - количество прогидролизованных частиц;- общее число молекул вещества.
Степень гидролиза зависит от температуры, концентрации соли, константы
гидролиза.
Константа гидролиза. Если представить уравнение гидролиза в общем виде:
МА + Н2О «HА + МОН, где МА - соль;
НА - кислота;
МОН - основание,
то константа равновесия этой реакции будет следующая:
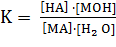 (8)
(8)
Концентрация воды в разбавленном растворе и константа равновесия этого
процесса - величины постоянные. Произведение двух постоянных величин будет
также величиной постоянной: К[Н2О]=Кг - это и будет константа гидролиза.
Константа гидролиза для данной реакции равна:
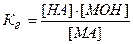 (9)
(9)
Физический смысл константы гидролиза заключается в том, что она
характеризует способность данной соли подвергаться гидролизу. Чем больше Кг,,
тем в большей степени протекает гидролиз.
Кг зависит от природы соли и температуры.
.2 Константа
гидролиза
Константа
гидролиза - константа равновесия
<https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%81%D1%82%D0%B0%D0%BD%D1%82%D0%B0_%D1%80%D0%B0%D0%B2%D0%BD%D0%BE%D0%B2%D0%B5%D1%81%D0%B8%D1%8F>
гидролитической реакции. Так константа гидролиза соли равна отношению
произведения равновесных концентраций продуктов реакции гидролиза к равновесной
концентрации соли с учетом стехиометрических коэффициентов.
В
качестве примера ниже приводится вывод уравнения константы гидролиза соли,
образованной слабой кислотой и сильным основанием:
 (10)
(10)
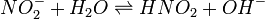 (11)
(11)
Уравнение
константы равновесия для данной реакции имеет вид:
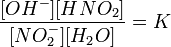 или
или 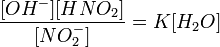 (12)
(12)
Так
как концентрация молекул воды в растворе постоянна, то произведение двух
постоянных 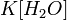 можно заменить одной новой - константой гидролиза:
можно заменить одной новой - константой гидролиза:
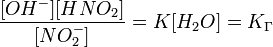 (13)
(13)
Численное
значение константы гидролиза получим, используя ионное произведение воды
<https://ru.wikipedia.org/wiki/%D0%98%D0%BE%D0%BD%D0%BD%D0%BE%D0%B5_%D0%BF%D1%80%D0%BE%D0%B8%D0%B7%D0%B2%D0%B5%D0%B4%D0%B5%D0%BD%D0%B8%D0%B5_%D0%B2%D0%BE%D0%B4%D1%8B>
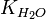 и константу диссоциации
<https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%81%D1%82%D0%B0%D0%BD%D1%82%D0%B0_%D0%B4%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86%D0%B8%D0%B8>
азотистой кислоты
<https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>
и константу диссоциации
<https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%81%D1%82%D0%B0%D0%BD%D1%82%D0%B0_%D0%B4%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86%D0%B8%D0%B8>
азотистой кислоты
<https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>
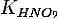 :
:
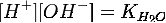 (14)
(14)
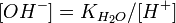 (15)
(15)
подставим
в уравнение константы гидролиза:
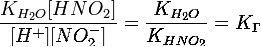 (16)
(16)
В
общем случае для соли, образованной слабой кислотой и сильным основанием:
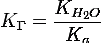 (17)
(17)
где
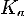 - константа диссоциации слабой кислоты, образующейся
при гидролизе
- константа диссоциации слабой кислоты, образующейся
при гидролизе
Для
соли, образованной сильной кислотой и слабым основанием:
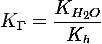 (18)
(18)
где
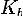 - константа диссоциации слабого основания,
образующегося при гидролизе
- константа диссоциации слабого основания,
образующегося при гидролизе
Для
соли, образованной слабой кислотой и слабым основанием:
гидролиз соль кислота основание
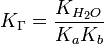 (19)
(19)
2. Подавление
и усиление гидролиза солей
Гидролиз соли часто следует усиливать или ослаблять, в зависимости от
технологических или аналитических целей. Например, получение многих кислых
солей, таких как гидрокарбонат натрия, осуществляется практическим путем
гидролиза средних солей, и степень гидролиза при этом следует повышать.
Смещение равновесия гидролиза соли можно производить тремя способами:
повышение температуры раствора соли;
повышение концентрации раствора соли;
добавлением к раствору соли кислоты или щелочи, или другой
гидролизующейся соли.
Повышение температуры усиливает гидролиз, что видно из выражения КГ, при
нагревании КВ возрастает значительно в большей степени, чем Кдисс. Слабых
кислот и оснований. Разбавление раствора повышает степень гидролиза во всех
случаях, кроме солей, образованных двумя слабыми компонентами.
Разбавление раствора NН4СН3СОО в равной степени изменит все концентрации,
т.е. не изменит величину дроби и не повлияет на смещение равновесия. Для
усиления гидролиза солей слабых оснований следует добавлять щелочь, связывающую
образующиеся ионы водорода. При добавлении щелочи происходит нейтрализация
кислоты, т.е. гидролиз усиливается. Связать ионы Н+ можно также, солью сильного
основания и слабой кислоты, например, Na2СО3, К3РО4. При этом ионы Н+
связываются в сложные анионы НСО3 - , НРО4 2 - или в молекулы слабых кислот. Для усиления гидролиза солей слабых кислот
и сильных оснований следует добавлять кислоту для нейтрализации образующихся
при гидролизе ионов ОН - ,
эти ионы можно также связать в комплексные ионы [Со (ОН)] + , [AI (ОН)2] + или
в нейтральные молекулы слабых оснований, действием на растворы гидролизующихся
солей солями слабых оснований и сильных кислот. Ослабление гидролиза солей,
дающих щелочную среду в растворе, производится добавлением щелочи.
2.1 Факторы,
влияющие на степень гидролиза
Степень гидролиза зависит от:
¾ температуры,
¾ концентрации раствора,
¾ природы растворяемого вещества
Гидролиз эндотермическая реакция, поэтому повышение температуры
усиливает гидролиз.
Повышение концентрации ионов водорода ослабляет гидролиз, в
случае гидролиза по катиону. Аналогично, повышение концентрации гидроксид-ионов
ослабляет гидролиз, в случае гидролиза по аниону.
При разбавлении водой равновесие смещается в сторону протекания
реакции, т.е. вправо, степень гидролиза возрастает.
Добавки посторонних веществ могут влиять на положение равновесия
в том случае, когда эти вещества реагируют с одним из участников реакции. Так,
при добавлении к раствору сульфата меди
раствора гидроксида натрия, содержащиеся в нем гидроксид-ионы будут
взаимодействовать с ионами водорода. В результате их концентрация уменьшится,
и, по принципу Ле Шателье, равновесие в системе сместится вправо, степень
гидролиза возрастет. А если к тому же раствору добавить раствор сульфида
натрия, то равновесие сместится не вправо, как можно было бы ожидать (взаимное
усиление гидролиза) а наоборот, влево, из-за связывания ионов меди в
практически нерастворимый сульфид меди.
5). Концентрация соли. Рассмотрение этого фактора приводит к
парадоксальному выводу: равновесие в системе смещается вправо, в соответствии с
принципом Ле Шателье, но степень гидролиза уменьшается.
Пример,(NO3)3
Соль гидролизуется по катиону. Усилить гидролиз этой соли можно, если:
нагреть или разбавить раствор водой;
добавит раствор щёлочи (NaOH);
добавить раствор соли, гидролизующейся по аниону Nа2СО3;
Ослабить гидролиз этой соли можно, если:
растворение вести на холоде;
готовить как можно более концентрированный раствор Al(NO3)3;
добавить к раствору кислоту, например, HCl
2.2 Гидролиз солей многокислотных оснований и многоосновных кислот
проходит ступенчато
Ранее мы рассмотрели гидролиз солей, образованных одноосновными кислотами
и однокислотными основаниями. Продуктами гидролиза таких солей являются кислоты
и основания.
Если соль образована слабой многоосновной кислотой или слабым
многокислотным основанием, то гидролиз данной соли может протекать ступенчато.
Число ступеней гидролиза зависит от основной слабой кислоты и кислотности
слабого основания.
Рассмотрим гидролиз соли, образованной слабой многоосновной кислотой и
сильным основанием. В водном растворе этих солей на первой ступени гидролиза
образуется кислая соль вместо кислоты и сильное основание. Ступенчато
гидролизуются соли K2SiO3, Na2SO3,
Na2S, Na3PO4 и др., например, гидролиз Na2CO3
может быть изображен в виде уравнений.
Первая ступень:
Na2CO3 + Н2О ↔ NaHCO3
+ NaOH;32- + H2O ↔ НCO-3 + OH-.
Продуктами первой ступени гидролиза является кислая соль гидрокарбонат
натрия NaHCO3 и гидроксид натрия NaOH.
Вторая ступень:
3
+ Н2О ↔ Н2СО3 + NaOH;-3
+ Н2О ↔ Н2СО3 + ОН-.
Продуктами второй ступени гидролиза карбоната натрия Na2CO3
являются гидроксид натрия и слабая угольная кислота Н2СО3.
Гидролиз по второй ступени протекает в значительно меньшей степени, чем по
первой ступени. Среда раствора соли карбоната натрия Na2CO3
- щелочная (рН > 7), так как в растворе увеличивается концентрация
гидроксид-ионов ОН.
Гидролиз солей трехосновных слабых кислот протекает по трем ступеням. В
качестве примера приведем уравнения гидролиза фосфата натрия.
Первая ступень:
3РО4
+ Н2О ↔ Na2НРО4 + NaOH;
РО43- + Н2О ↔ НРО42-
+ NaOH.
Вторая ступень:
2НРО4
+ Н2О ↔ NaH2PO4 + NaOH;
НРО42- + Н2О ↔ H2PO-4
+ ОН-.
Третья ступень:
2PO4
+ Н2О ↔ Н3РО4 + NaOH;
Н2РО-4 + Н2О ↔ Н3РО4
+ ОН-.
Гидролиз по первой ступени происходит в значительно большей степени, чем
по второй. По третьей ступени гидролиз фосфата натрия практически не идет.
Рассмотрим гидролиз соли, образованной слабым многокислотным основанием и
сильной кислотой. В водных растворах таких солей на первой ступени образуется
основная соль вместо основания и сильная кислота. Ступенчатому гидролизу
подвергаются соли: MgSO4, FeCl3, FeCl2, ZnCl2
и др., например, гидролиз хлорида цинка ZnCl2 протекает по двум
ступеням.
Первая ступень:
2+
H2О ↔ ZnOHCl + HC1;2+ + Н2О ↔
(ZnOH)+ + Н+.
Вторая ступень:
+ H2O ↔ Zn(OH) 2 + HC1;
(ZnOH)+ + Н2О ↔ Zn(OH)2 + H+.
Гидролиз соли идет по катиону, так как соль образована слабым основанием
Zn(OH)2 и сильной кислотой НСl. Катионы цинка Zn2+
связывают гидроксид-ионы ОН- воды. На первой ступени образуется
основная соль ZnOHCl и сильная кислота НСl. На второй ступени образуется слабое
основание Zn(OH)2 и тоже сильная хлороводородная кислота. Гидролиз
по первой ступени протекает значительно больше, чем по второй. В растворе
увеличивается концентрация ионов водорода Н+ и реакция среды будет
кислая (рН <7).
Заключение
Гидролиз - один из методов деструкции белков, в результате которого
происходит разрыв пептидных связей белковой молекулы. Процесс идет с
присоединением воды и образованием азотистых соединений. Гидролиз может быть
полным или частичным в зависимости от способа расщепления.
Полный гидролиз белка может осуществиться только путем нагревания его при
температуре более 100 градусов с разбавлением минеральными кислотами и
щелочами. В этом случае получается смесь конечных продуктов гидролиза, включая
свободные аминокислоты, полипептиды, аммиак, побочные продукты, образующиеся в
результате разрушения аминокислот и их взаимопревращения, а также
карамелизованные углеводы и др.
Список
использованных источников
1. Глинка,
Н.Л. Общая химия./ Н.Л. Глинка. - Л: Химия, 2000. - с. 249-255. 2. Глинка, Н.Л.
Задачи и упражнения по общей химии./
. Н.Л.
Глинка, - Л.: Химия, 1987. - с. 146-156. 3.
. Задачи
и упражнения по общей химии./ Б.И. Адамсон [и др.]. - М.: Высшая школа, 2004. -
с. 255. 17 4.
. Некрасов,
Б.В. Основы общей химии./ Б.В. Некрасов. в 2-х то- мах - СПб.: ЛАНЬ 2003. 5.
Фролов, В.В. Химия/ В.В.
. Фролов.
- М.: Высшая школа, 1986. - с. 204-208