Аналитическая химия
МОСКОВСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
имени М.В.
Ломоносова
Химический
факультет
Зачетная
задача
студента 2 курса 210 группы
Сулимова Никиты Алексеевича
Преподаватель:
к. х. н., доцент Пасекова Нина Александровна
Москва -
2015
Содержание
Введение
Раздел 1
.1 Описание объекта
.2 Качественный анализ
.3 Вывод
Раздел 2. Обоснование выбора
методики для проведения количественного анализа образца
Раздел 3
.1 Расчет массы навески
.2 Схема определения
.3 Растворение образца
3.4 Приготовление стандартного
раствора дихромата калия
3.5 Количественное определение
железа
.6 Вывод
Список литературы
Введение
Целью данной работы является проведение
качественного и количественного анализа выданного образца, представляющего
собой природный или промышленный объект, а именно, определение его состава и
нахождение процентного содержания одного из составляющих элементов исследуемого
образца по выбранной методике.
Раздел 1
.1 Описание объекта
Объект представляет собой мелкодисперсный
порошок бордово-коричневого цвета. Предположительно это измельченная руда или
минерал.
.2 Качественный анализ
По результатам предварительных испытаний не было
выявлено ни одного катиона, входящих в состав данного образца. Для определения
качественного состава был использован систематический анализ (кислотно-щелочной
метод). Ход анализа представлен в приведенной ниже таблице 1.
Таблица 1. Качественный анализ образца
|
№
|
Исследуемый
объект
|
Реагент
|
Наблюдения
|
Вывод
|
|
1
|
Образец
|
Царская
водка
|
Вещество
почти полностью растворилось, раствор желто-оранжевого цвета
|
Возможное
присутствие Fe3+, остается нерастворимый осадок SiO2
|
|
2
|
Образец
|
H2SO4
(1M)
|
Осадок
не образуется
|
Отсутствуют
катионы I и II группы
|
|
3
|
Образец
|
H2SO4
(конц.)
|
Осадок
не образуется
|
Отсутствуют
катионы I и II группы
|
|
4
|
Раствор
1
|
NaOH
(2M) + H2O2(3%)
|
Образуется
осадок бурого цвета и бесцветный раствор.
|
Предположительно
присутствует Fe3+
|
|
5
|
Раствор
2
|
NH4Cl
тв. (to); дитизон
|
Осадок
не образуется; в опыте с дитизоном нет красного окрашивания
|
Отсутствуют
Al3+ и Sn4+, нет также Cr6+ (раствор бесцветен); в опыте с дитизоном Zn2+ не
обнаружен
|
|
6
|
Осадок
2
|
Промыть
NaOH (2M), HNO3 (2M) + H2O2 (3%)
|
Осадок
полностью растворился, образовался бледно-желтый раствор
|
В
осадке не было HSbO3
|
|
7
|
Раствор
3
|
NH3
(конц.) до щелочной реакции NH4Cl + H2O2 (3%) (to)
|
Предположительно
присутствуют Fe2O3 xH2O и MnO(OH)2, нет Cu2+, Ni2+, Co2+ (раствор б/ц)
|
|
8
|
Осадок
3
|
HNO3
(2M)
|
Весь
осадок растворился
|
MnO(OH)2
отсутствует
|
|
9
|
Осадок
3
|
Na2Sn(OH)4
|
Черный
осадок не выпадает
|
Bi3+
отсутствует
|
|
10
|
Осадок
3
|
K4[Fe(CN)6]
|
Образуется
синий осадок
|
Обнаружено
присутствие Fe3+
|
|
11
|
Раствор
4
|
H2SO4
(2M) до кислой реакции, упарить + H2O+ Na2S2O3 x 5H2O тв. (to)
|
Образуется
осадок желтого цвета - это сера
|
Cu2+
и Hg2+ отсутствуют
|
|
12
|
Раствор
5
|
NH4Cl
+ Na2HPO4 + NH3 водный
|
Образуется
белая муть
|
В
образце имеется небольшое содержание Mg2+
|
|
13
|
Раствор
5
|
NH3 + NH4Cl
+ (NH4)2CO3
|
Слабое
помутнение
|
В
образце имеется небольшое содержание Ca2+
|
|
14
|
Раствор
5
|
H2SO4
(2M) до сильно кислой реакции + Na2S + NH3 (10%)
|
Желтый
осадок не образуется
|
Cd2+
отсутствует
|
титрование
раствор дихромат
1.3 Вывод
В образце присутствуют: Fe3+,
Mg2+, Ca2+. Ca2+
и Mg2+ присутствуют в
маленьком количестве. Данный образец представляет собой железную руду - бурые
железняки с содержанием Fe ≈ 60% и примесями Mg2+, Ca2+
и SiO2.
Раздел 2. Обоснование выбора методики для
проведения количественного анализа образца
Основным компонентом смеси, который был выбран
для количественного анализа, является Fe3+. Главным требованием к анализу было
использование гравиметрической или титриметрической методики.
Гравиметрические
Осаждение в виде гидроксида железа (III)
Железо осаждают в виде водного гидроксида,
смещая вправо протолитические реакции добавлением аммиака:
[Fe(H2O)6]3+ + H2O =
[Fe(OH)(H2O)5]2+ + H3O+
[Fe(OH)(H2O)5]2+ + H2O =
[Fe(OH)2(H2O)4]+ + H3O+
[Fe(OH)2(H2O)4]+ + H2O =
[Fe(OH)3(H2O)3] + H3O+
Гидроксид железа прокаливают на горелке при
температуре 800oC до оксида Fe2O3, гравиметрический фактор FFe = 0,6994. Прокаливание
осадка при температуре около 1200oC может привести к погрешностям определения
за счет реакции:
Fe2O3 = 4Fe3O4 + O2
Если анализируемый раствор содержит железо(II),
то его предварительно окисляют азотной кислотой.
Титриметрические
Комплексонометрическое титрование
В сильнокислой среде при pH < 0,9 комплексы
железа(III) с ЭДТА образуются в соответствии с уравнением:
Fe3+ + H5Y+ = FeHY + 4H+
При pH > 1,3 преобладает комплекс FeY- c Kуст
= 1,26·1025 (ионная сила 0,1; 20oC).
Комплексонат железа(II) значительно менее
устойчив (Kуст = 2,0·1014 в тех же условиях) и крайне неустойчив по отношению к
окислителям. Уже кислородом воздуха окисляется до комплексоната железа(III).
Поэтому комплексонометрически определяют только железо(III). В качестве
металлоиндикаторов используют тайрон, салициловую или сульфосалициловую
кислоты, гидроксамовые кислоты. Эти индикаторы в растворах бесцветны, но
образуют с железом(III) интенсивно окрашенные комплексы: красного цвета с
тайроном, фиолетового цвета с салициловой или сульфосалициловой кислотами,
сине-фиолетового - с гидроксамовой кислотой.
Окислительно-восстановительное титрование
1. Дихроматометрия
Титрование железа (II) основано на реакции:
6Fe2+ + Cr2O72- + 14H+ = 6Fe3+ + 2
Cr3+ + 7H2O
В процессе титрования повышается концентрация
ионов железа(III), и потенциал системы Fe3+/Fe2+ возрастает, что приводит к
преждевременному окислению индикатора дифениламина. Если прибавить к титруемому
раствору фосфорную кислоту, то окраска индикатора изменяется резко в конечной
точке титрования. Фосфорная кислота понижает окслительно-восстановительный
потенциал системы Fe3+/Fe2+, образуя устойчивый комплекс с ионами железа(III).
Растворы солей железа(II) часто содержат ионы
железа(III), поэтому перед титрованием ионы железа(III) необходимо
восстановить. Для восстановления применяются металлы (Zn, Cd и др.), SnCl2,
H2S, SO2 и другие восстановители.
2. Перманганатометрия
Титрование железа (II) основано на реакции
5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2+ +
4H2O
Титровать можно в сернокислой или солянокислой
средах. В первом случае не наблюдается никаких осложнений. Присутствие в
титруемом растворе хлорид-ионов приводит к перерасходу перманганата и получению
нечеткого конца титрования. Это вызвано тем, что реакция между железом(II) и
перманганатом индуцирует реакцию между MnO4- и хлорид-ионами. Индуцированной
реакции не возникает, если в растворе присутствуют в достаточных количествах
фосфорная кислота и марганец(II). Поэтому перед титрованием в раствор добавляют
смесь Рейнгарда-Циммермана, состоящую из серной, фосфорной кислот и сульфата
марганца(II). Присутствие в этой смеси H2SO4 создает требуемую концентрацию
протонов в титруемом растворе, H3PO4 необходима для связывания железа(III) в
бесцветный комплекс (если железо не маскировать, то окраска его комплексных
хлоридов будет затруднять наблюдение в конце титрования бледно-розовой окраски
перманганата) и образования фосфатных комплексов марганца(III). Железо(III)
перед титрованием необходимо восстановить до железа(II).
В данной работе было отдано предпочтение
окислительно-восстановительному (дихроматному) методу определения железа. Такой
выбор обусловлен несколькими причинами:
1. Гравиметрический
метод сложно осуществим из-за своих условий проведения (очень высокие
температуры), очень трудоемок и затрачивает большое количество времени.
2. Перманганатометрический
метод неудобен тем, что для начала необходимо стандартизовать раствор
перманганата калия, и только потом проводить титрование железа. К тому же при
титровании в солянокислых средах наблюдаются некоторые осложнения.
3. Комплексонометрический
метод мог бы тоже быть использован, но условия проведения дихроматного метода
оказались более удобными.
.1 Расчет массы навески
Образец содержит примерно 60% железа. Так как
реакция строго стехиометрична, то отношение количеств прореагировавших веществ
будет равно единице. Тогда найдем необходимую массу по следующей формуле
Находим массу чистого железа:
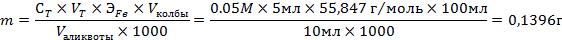
В таком случае масса навески равна: 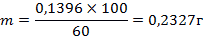
Измерение массы выданной навески:
m1 (бюкса с
навеской) = 9,2723г
m2 (бюкса) = 8,9946г
m0 (навески) =
0,2777г
.2 Схема определения
Навеска
Растворение в смеси кислот HCl + HNO3
Раствор (подготовленный для титрования)
Отбор аликвоты
Титриметрическое определение железа
Расчет содержания железа
3.3 Растворение образца
Следующим этапом являлось растворение пробы. В
данной работе был выбран следующий ход анализа:
1. растворение точно взвешенного количества
руды;
2. доведение
до метки в мерной колбе;
. отбор
аликвоты на титриметрическое определение.
Масса навески анализируемого объекта на
аналитических весах составила 0,2777г.
Растворение проводили по следующей методике [1]:
Навеску анализируемого материала поместили в
жаростойкий стакан вместимостью 300 мл, прибавили 40 мл HCl(1:4),
закрыли часовым стеклом и растворили при нагревании на песочной бане. Затем
добавили 5 мл конц. HNO3
и продолжили нагревание. Растворение пробы считалось законченным, когда на дне
стакана остался серый осадок, состоящий, по-видимому, в основном из кремниевой
кислоты и угля. Выпарили до влажных солей, остаток обработали 10 мл конц. HCl
и снова выпарили раствор. Операцию выпаривания с конц. HCl
повторили два раза, затем добавили 4 мл конц. HCl
и разбавили горячей водой примерно до 50 мл. Раствор отфильтровали через фильтр
«белая лента» в мерную колбу вместимостью 200.0 мл. Хорошо промыли фильтр
горячей 0.05 М HCl,
разбавили водой до метки и перемешали.
FeO + 2HCl = FeCl2 + H2O
Fe2O3 + 6HCl = 2FeCl3 + 3H2O+
2HCl = CaCl2 + H2O+
2HCl = MgCl2 + H2O
FeCl2 + 4HNO3конц.
= Fe(NO3)3 + 2HCl + NO2↑ + H2O
3.4 Приготовление стандартного
раствора дихромата калия
0,05M раствор K2Cr2O7 в 200 мл
содержит 0,4903 г сухого дихромата калия.
Готовим навеску:
m (пустого стакана)
= 8,220 г;
m (стакан +
вещество) = 8,71 г (на аналитических весах 8,7069 г);
Пересыпаем вещество в колбу 200 мл;
m (пустого стакана
на аналитических весах) = 8,2203 г;(навески) = 0,4866 г.
Получается, что концентрация дихромата в 200 мл
раствора равна 0, 04962M.
.5 Количественное определение железа
Аликвотную часть раствора 10,00 мл пипеткой
переносят в коническую колбу, вместимостью 100мл, добавляют 5 мл конц. HCl.
Закрывают колбу маленькой воронкой, вносят в колбу 5-6 гранул металлического цинка,
нагревают на песочной бане до обесцвечивания раствора и полного растворения
цинка. Охлаждают струей воды под краном, добавляют 3 - 4 мл H2SO4, снова
охлаждают, вводят 5 мл H3PO4, 15 - 20 мл воды, 2 капли раствора дифениламина и
медленно титруют раствором дихромата калия до появления синей окраски раствора.
Таблица 2. Результаты титрования
|
№
|
VК2Сr2O7,
мл
|
|
1
|
3,3
|
|
2
|
3,2
|
|
3
|
3,2
|
|
Среднее
|
3,233
|
Масса железа рассчитывается по формуле:
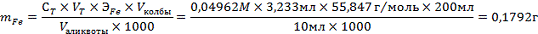
Тогда процентное содержание Fe в навеске равно:
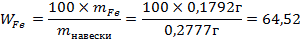
.6 Выводы
По результатам проведенного количественного
анализа можно сделать вывод, что содержание железа в образце составляет 64,52%.
Список литературы
1. Основы
аналитической химии. Практическое руководство: Учебное пособие для вузов/ В. И.
Фадеева, Т. Н. Шеховцова, В. М. Иванов и др.; Под ред. Ю. А. Золотова. - 2-е
изд., испр. - М.: Высш. шк., 2003. - 463с.: ил.
2. Сырокомский
В.С. Методы анализа железных и марганцевых руд. Сверд.-М.: Металлургиздат,
1950. 240с.
3. Пономарев
А. И. Методы химического анализа железных, титаномагнетитовых и хромовых руд.
М.: Наука, 1966. 406с.