Технология получения циклогексана
Реферат
на тему:
«Технология получения циклогексана»
1. Химия и технология процессов гидрирования
В промышленности основного органического и нефтехимического синтеза
широко используют процессы гидрирования углеводородов, кислородсодержащих и
азотистых соединений с целью получения главным образом насыщенных
углеводородов, кетонов, карбоновых кислот, спиртов и аминов.
2. Гидрирование ароматических углеводородов
Катализаторами гидрирования ароматических систем могут быть все металлы
восьмой группы, но в промышленности применяют главным образом никель на
носителях, особенно на Cr2O3. С таким контактом достаточная скорость процесса
достигается при 120-2000 С. При этом в отличие от олефинов,
необходимо повышенное давление (1-5 МПа) - не только для ускорения реакции, но
и для увеличения равновесной степени конверсии, так как термодинамические
отношения в этом случае менее благоприятны для гидрирования. Ароматические
углеводороды нужно предварительно очищать от соединений серы, являющихся
контактными ядрами.
Сравнительная стабильность ароматической системы обуславливает ее меньшую
реакционную способность при гидрировании по сравнению с олефинами. Так,
относительные скорости гидрирования бензола в ядро, циклоолефина и двойных
связей в боковой цепи арилолефина таковы (в условных единицах):
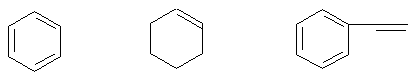
1
150 900
По этой причине и даже не смотря на последовательно-параллельный тип
реакции со ступенчатым насыщением связей
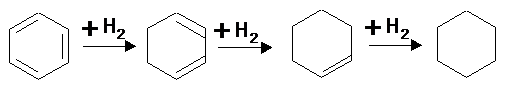
В
реакционной массе не обнаруживается циклических олефинов. Однако в специальных
условиях из бензола можно получить циклогексен (нагомогенных катализаторах) или
циклогексилбензол (на гетерогенных бифункциональных катализаторах):
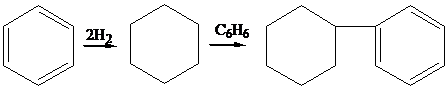
Гомологи
бензола гидрируются с меньшей скоростью, чем сам бензол, что является еще одним
проявлением дезактивирующего влияния заместителей при гидрируемых связях. При
наличии в ароматическом углеводороде ненасыщенной боковой цепи она гидрируется
в первую очередь. В присутствии медного катализатора, не катализирующего
гидрирование ароматических систем, насыщаются только боковые цепи, а на
никелевом при избытке водорода происходит полное гидрирование, например,
стирола:
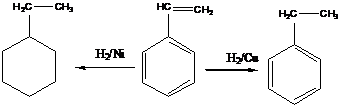
Условия гидрирования ароматических углеродов во многом определяются
побочными реакциями гидрогенолиза с расщеплением боковых цепей и циклов. Так,
из бензола на никелевом катализаторе при 2900 С образуются метан (до
71 %) и свободный углерод:
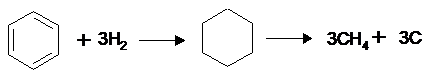
Еще
легче расщепляются боковые цепи, особенно более длинные. Например, из
н-пропилбензола при гидрировании можно получить не только пропилциклогексан, но
также этил- и метилзамещенные, циклогексан и низшие парафиновые углеводороды.
Эти побочные реакции определяют верхний предел температуры при гидрировании
ароматических углеводородов.
В
промышленности процессы гидрирования ароматических углеродов применяют для
синтеза нескольких практически важных продуктов, в особенности циклогексана.
Циклогексан
С6Н12 (жидкость; т.кип 80,70 С) содержится в
небольшом количестве в бензиновых фракциях нефти, и его можно извлекать из
легких нефтяных фракций экстрактивной перегонкой, фракционной кристаллизацией.
На практике эти методы используют редко. Это объясняется трудностями,
связанными с выделением чистого циклогексана из нефтяного сырья. Главным
методом получения циклогексана в промышленности является гидрирование бензола:
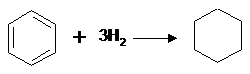
Гидрирование
бензола протекает с выделением тепла (ΔН= -49 ккал). Гидрирование бензола проводят при атмосферном давлении,
так и при среднем и высоком давлении. Наиболее выгодно в техноэкономическом
отношении является, по-видимому, проведение процесса при высоком давлении: при
200-300 атм и 260 - 3600 С. При более низких температурах равновесие
обратимой реакции сдвигается вправо, но значительно уменьшается скорость
реакции, и поэтому снижается производительность катализатора. Повышение
температуры приводит, наряду с ускорением основной реакции, и к ускорению
побочной - изомеризации циклогексана в метилциклопентан:
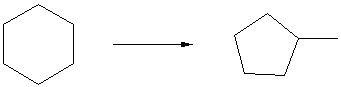
Если
исходный бензол не содержит сернистых соединений, синтез циклогексана проводят
при 100 атм и 2700 С в присутствии никелевого катализатора (окись
никеля, нанесенная на окись алюминия). Через 1л такого катализатора можно
пропустить в час 2,7 л бензола и 20 л водорода, сжатого до 200 атм.
Если
в исходном бензоле содержатся сернистые соединения, то используют
комбинированный катализатор, состоящий из сульфида никеля и сульфида вольфрама.
Сульфиды наносят на носитель - активную окись алюминия; однако возможно
применение сульфидов без носителя - в этом случае съем продуктов с единицы
объема катализатора выше. Сульфидные катализатор, обладая высокой активностью и
селективностью, не отравляется сернистыми соединениями. Наоборот, для его
нормальной работы необходимо избегать обессеривания, поэтому вместе с исходными
реагентами в контактный слой непрерывно вводят в небольших количествах
сероуглерод или сероводород.
В
последнее время циклогексан приобрел важное значение для производства
циклогексанона, капролактама и адипиновой кислоты.
3. Технология жидкофазного гидрирования
Жидкофазное гидрирование проводят путем барботирования водорода через жидкую реакционную массу. Этим
способом всегда гидрируют высококипящие вещества (жиры, высшие карбоновые
кислоты и их эфиры, динитрилы), поскольку для их перевода в состояние
насыщенного пара потребовались бы чрезмерный избыток водорода и излишнее
экономические затраты. Однако при высоком давлении в жидкой фазе можно
гидрировать и более летучее вещества.
Процессы жидкофазного гидрирования классифицируют по
нескольким основным признакам.
По составу жидкой фазы их можно разделить на следующие группы.
. Гидрирование в среде гидрируемого соединения без посторонних
добавок.
. Гидрирование в растворе веществ, инертных в условиях реакции.
. Гидрирование в эмульсиях, например восстановление ароматических
динитросоединений в водной эмульсии.
В зависимости от того, в какой форме применяется катализатор, жидкофазные
процессы гидрирования можно разделить на три группы.
. С тонкодиспергированным катализатором, нередко получаемым
непосредственно в массе гидрируемого вещества.
. С суспендированным в реакционной массе катализатором,
измельченным до определенного размера.
. С неподвижным (стационарным) катализатором, используемым в виде
гранул разной формы, достаточно крупных, чтобы их не уносили потоки газа и
жидкости
4. Технология газового гидрирования
Гидрирование в жидкой фазе осуществляют, пропуская смесь
водорода с парами органического вещества через гетерогенный контакт. Этот
процесс применяют для веществ, летучесть которых при температуре реакции
достаточно для создания необходимо парциального давления их в парогазовой
смеси. При большом избытке водорода, высокой температуре и снижении общего давления
этим путем можно гидрировать и менее летучее вещества.
Подавляющее большинство реакций газофазного гидрирования проводится со
стационарном катализатором в виде шариков, таблеток и в других формах, размером
3-5 мм. Только в редких случаях применяют мелкодиспергированный контакт - для
процесса псевдоожиженным катализатором.
. Технологическая схема жидкофазного гидрирования
Технологические схемы большинства процессов жидкофазного гидрирования
имеют много общих черт, обусловленных применением высокого давления, избытка
рециркулирующего водорода и гетерогенного катализатора (суспендированный в
жидкости или стационарный ), а также способом разделения продуктов, зависящим
от их физических свойств. Гидрирование обычно проводят в жидкой фазе в
присутствии никелевого катализатора: никель Ренея (сплав никеля и алюминия в
соотношении 1:1, который обрабатывается концентрированным гидроксидом натрия); Ni/Al2O3; Ni/кизельгур (гидротированная SiO2); благородные металлы Pt/Al2O3 или Ru/Al2O3.Соотношение бензола с водородом 1:3.
Свежий и рециркулирующий водород сжимают компрессорами 1 и 2 до 30 МПа,
смешивают и подогревают в теплообменнике 3 (горячими реакционными газами) и в
трубчатой печи 4 (топочными газами). предварительно подготовленный бензол
подают на реакцию насосом 5 через паровой подогреватель 6, а катализатор -
насосом 16. перед реактором 7 все компоненты смешивают; за счет тепла водорода
смесь приобретает необходимую температуру (3000 С).
Продукты реакции вместе с катализатором и избыточным водородом выходят с верха
реактора 7 и разделяется в горячем сепараторе 8 на жидкую и газовую фазы.
Газовая фаза отдает свое тепло водороду в теплообменнике 3 и
дополнительно охлаждается водой в холодильнике 9; образовавшийся конденсат
отделяют от водорода в сепараторе 10 высокого давления. Этот водород
возвращается на гидрирование.
Жидкую фазу из сепаратора 8 дросселируют до давления, близкого к
атмосферному, охлаждают водой в холодильнике 11 и отделяют от выделившегося при
дросселировании газа в сепараторе 12 низкого давления. Жидкость поступает на
центрифугу 13, где оседают более крупные частички катализатора. Этот шлам
шнеком 14 транспортируют в смеситель 15, куда добавляют свежий катализатор.
Полученную смесь подают в реактор 7 насосом 16. Таким путем приблизительно 85 %
катализатора циркулирует и возвращается в процесс. Остальное его количество
находится в чрезмерном измельченном виде (в результате истирания зерен) и
выходит из центрифуги 13 вместе с главной массой продуктов, отфильтровываясь от
них на фильтр-прессе 17. этот катализаторный шлам выбрасывают.
Жидкую фазу из сепаратора 10 дросселируют и отделяют от газа в сепараторе
18 низкого давления. Газ объединяют с газом из сепаратора 12 и используют в
качестве топливного газа. Жидкость из сепаратора 18 отделяют от небольшого
количества воды в сепараторе 19, объединяют со смесью продуктов после
фильтр-пресса 17 и направляют на дальнейшую переработку.
Технологическая схема

Рис. № 1. Технологическая схема гидрирования бензола.
,2 - компрессоры; 3 - теплообменник; 4 - трубчатая печь; 5, 16 - насосы;
6 - паровой подогреватель; 7 - реактор; 8, 10, 12, 18, 19 - сепараторы; 9, 11 -
холодильники; 13 - центрифуга; 14 - шнек; 15 - смеситель; 17 - фильтр-пресс.
Структурная схема
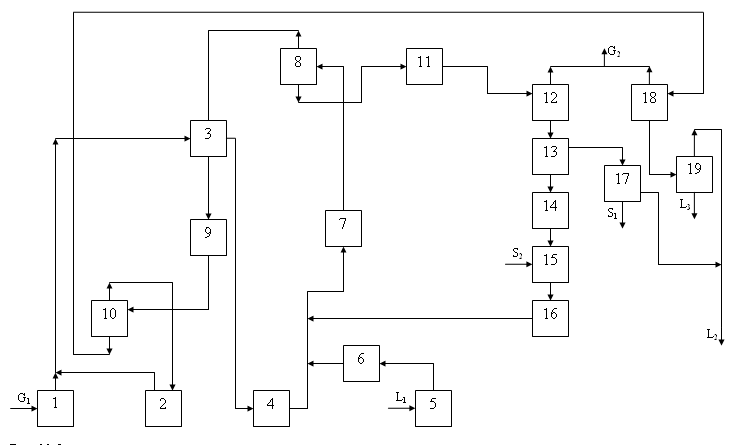
Рис. № 2.Материальные потоки:
G1 водород
G2 топливный газ
S1 шлам
S2 катализатор
L1 бензол
L2 циклогексан
L3 вод
Элементы системы:
1. Компрессор
2. компрессор
. теплообменник
. трубчатая печь
. насос
. паровой подогреватель
. реактор
. сепаратор
. холодильник
. сепаратор
. холодильник
. сепаратор
. центрифуга
. шнек
. насос
. фильтр-пресс
. сепаратор
. сепаратор
углеводород
циклогексан гидрирование бензол
Функциональная схема
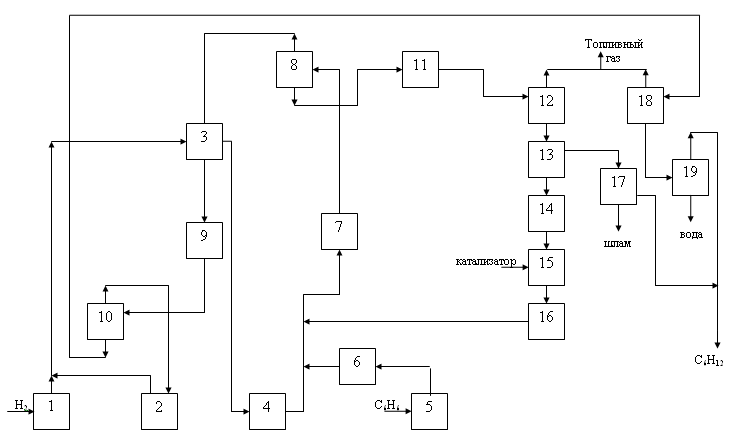
Рис. № 3.
1. Сжатие водорода
2. Сжатие водорода
. нагревание водорода
. нагревание водорода
. добавление бензола
. нагревание бензола
. гидрирование бензола
. разделение продуктов на газовую и жидкую фазы
. охлаждение газовой фазы
. разделение водорода и конденсата
. охлаждение жидкой фазы
12. разделение на газовую и жидкую фазы
13. отделение катализатора
14. отделение шлама и катализатора
. добавление новой порции катализатора
. добавление катализатора в реакционную смесь
. удаление остатков катализатора
18. разделение на газовую и жидкую фазы
19. отделение продуктов реакции от воды
Операторная схема
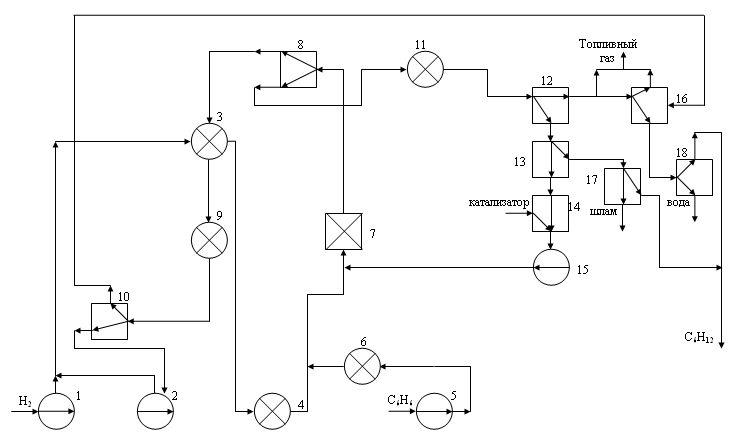
Рис. № 4.
1. Сжатие водорода
2. Сжатие водорода
. нагревание водорода
. нагревание водорода
. добавление бензола
. нагревание бензола
. гидрирование бензола
. разделение продуктов на газовую и жидкую фазы
. охлаждение газовой фазы
. разделение водорода и конденсата
. охлаждение жидкой фазы
. разделение на газовую и жидкую фазы
. отделение катализатора
. добавление новой порции катализатора
. добавление катализатора в реакционную смесь
. удаление остатков катализатора
. отделение шлама и разделение на газовую и жидкую фазы
. отделение продуктов реакции от воды
Выводы
Циклогексан - жидкость с температурой кипения 80,70 С. В
небольших количествах содержится в бензиновых фракциях нефти. Применяется
преимущественно (95%) в производстве найлона, также увеличивается применение
продуктов окисления циклогексана адипиновой кислоты. В производстве
пенопластов, пластификаторов, и эластомеров (каучуков). Главным и практически
единственным способом получения является реакция гидрирования бензола, реакция
обратима и сильно экзотермична, поэтому необходимо ее проводить при температуре
179-1800С и давлении 2,5-3 МПа.
В заключении хотелось бы сказать, что в последнее время циклогексан
приобрел важное значение для производства циклогексанона, капролактама и
адипиновой кислоты.
Литература
1. Лебедев
Н.Н.: Химия и технология основного органического синтеза. - М.; Химия, 1981
г.-608с., ил.
2. Мухленов
И.П., Горштейн А.Е., Тумаркина Е.С.: Основы химической технологии: Учебник для
студентов спец. вузов. - М.: Высш.шк.,1991.-463с.: ил.
. Кутепов
А.М., Бондарева Т.И., Беренгартер М.Г.: Общая химическая технология: Учеб. Для
техн. Вузов. - М.: Высш.шк., 1990.-520с.; ил.