Сульфидные катализаторы гидроочистки
Содержание
Введение
Современные методы исследования
наноструктурированных катализаторов
.1 Электронная микроскопия
.2 Рентгеновская спектроскопия и
дифракция
.3 Определение химического состава
катализаторов
Состав и структура активной фазы
катализаторов
3 Строение активных центров Со(Ni)MoS
катализатора
4 Анализ генезиса катализаторов
гидроочистки
Характеристики некоторых брим
катализаторов
Список использованных источников
Введение
Рынок топливных продуктов непрерывно ставит
задачи получения нефтяных фракций с низким содержание серы, получение таких
малосернистых топлив достигается путем глубокой гидроочистки соответствующих
нефтяных фракций или сырья для их получения. Получение малосернистых
нефтепродуктов возможно только при использовании высокоактивных катализаторов,
обеспечивающих степень гидрообессеривания, не менее 99% для дизельных топлив и
бензинов и не менее 97% для вакуумного газойля. Такая степень обессеривания
достижима только на современных катализаторах последнего поколения.
1 Современные методы исследования
наноструктурированных катализаторов
Одной из важнейших характеристик катализаторов
является характеристика пористой структуры: удельная поверхность, объем пор,
распределение пор по размерам.
Распределение пор по размерам необходимо знать
для того, чтобы можно было предсказать эффективные коэффициенты диффузии в
пористом катализаторе и оценить легкость проникания реагирующих молекул внутрь
таблеток катализатора.
Размеры пор определяют двумя методами: с помощью
физической адсорбции газа можно изучать поры диаметром до 60 нм, ртутная
порометрия применима при диаметрах пор больше 3,5 нм.
Изучая распределение узких пор по размерам, чаще
всего измеряют зависимость величины адсорбции или десорбции газа от давления.
Метод основан на том, что давление, при котором пар конденсируется или
испаряется, зависит от кривизны мениска жидкости, сконденсированной в порах.
При изучении пористости в качестве адсорбата чаще всего выбирают азот.
Для определения радиусов более крупных пор
адсорбентов, поверхность которых не смачивается ртутью, используют ртутную
порометрию.
Если пористую гранулу адсорбента и катализатора
поместить в герметическую ампулу и откачать воздух, находящийся в ней, а затем
с помощью специального устройства заполнить ампулу ртутью, то последняя будет
лишь облегать гранулу со всех сторон, не входя в ее поры, даже если они будут
очень широки. Для заполнения пор необходимо приложить внешнее давление. При
этом последовательно будут заполняться ртутью сначала очень широкие поры, затем
все более узкие в строгом соответствии с давлением. Атмосферное давление обычно
достаточно лишь для заполнения самых широких пор, поэтому ампулу помещают в
стальную бомбу и после герметизации повышают в ней давление до значений,
составляющих сотни тысяч килопаскалей (несколько тысяч атмосфер), чтобы
заполнить поры в грануле вплоть до размера в несколько нанометров. В
цилиндрической поре (обычно принимают, что поры имеют цилиндрическую форму)
сила, препятствующая прониканию в пору, действует вдоль круговой линии контакта.
.1 Электронная микроскопия
В электронном микроскопе электроны сначала
ускоряются в электрическом поле между катодом и анодом, имеющим форму кольца.
Длина волны ускоренных таким образом электронов может составлять несколько
сотых долей ангстрема (т.е. быть порядка 10‾12 м).
Затем электроны попадают в колонну микроскопа,
где движутся в магнитном поле, создаваемом катушками индуктивности. Изменяя
силу тока в катушках, можно управлять магнитными полями, а значит, изменять
траектории электронов и очень точно фокусировать их поток. Таким образом,
катушки выступают в роли своеобразных магнитных линз. Для того чтобы избежать
рассеяния электронов на молекулах газа, внутри электронного микроскопа
поддерживается высокий вакуум.
Благодаря малой длине волны электронов, а также
постоянно совершенствующимся системам магнитных линз, современные электронные
микроскопы обладают субнанометровым (меньше 10‾ м) и даже субангстремным
(меньше 10‾¹ м)
разрешением.
В электронной микроскопии выделяют два основных
метода исследования:
· сканирующая (растровая) электронная микроскопия;
· просвечивающая электронная микроскопия
Применение электронной микроскопии в катализе
имеет преимущества в возможности использования этого метода и прямого
наблюдения за атомной структурой активных центров на поверхности.
.2 Рентгеновская спектроскопия и дифракция
Рентгеновское излучение может взаимодействовать
с веществом за счет упругих и неупругих процессов. Упругое (без потери
энергии), когерентное рассеяние рентгеновских фотонов определяется их
взаимодействием с электронной оболочкой атомов и сопровождается дифракцией
рентгеновского излучения, которое лежит в основе рентгеноструктурного анализа.
Трансляционная симметрия кристаллической решетки вызывает возникновение
интенсивности максимумов рассеянной волны - дифракционных рефлексов. Кроме
этого, ближний порядок в окружении атомов порождает гладкие синусоидальные
колебания упруго рассеянного фона при увеличении угла рассеяния. На явлениях
дифракции основаны методы определения атомной структуры вещества, локального
окружения, надмолекулярной организации, элементов частичного упорядочения и
мало углового рассеяния.
Неупругие процессы поглощения или рассеяния
рентгеновского излучения включают в себя возбуждение коллективных колебаний
атомных ядер (фононов) в кристаллической решетке, носителей зарядов -
электронов и дырок (плазмонов), возбуждение и удаление электронов валентной
зоны и внутренних оболочек атомов.
Существует три классических метода получения
дифракционного эффекта от кристалла:
· полихроматический метод (метод
Лауэ), основанный на использовании сплошного спектра рентгеновского излучения:
· метод вращающегося монокристалла,
основанный на использовании монохроматического излучения;
· метод порошка Шеррера, в котором
условия дифракции монохроматического рентгеновского излучения обусловлены
большим числом различно ориентированных систем плоскостей.
.3 Определение химического состава катализаторов
Определение содержания Мо, Ni,
Со и модификаторов, а также сульфидной S,
возможно ренггенофлюоресцентным методом с использованием сертифицированных
образцов.
Определение содержания Мо возможно так же с
помощью метода фотоколориметрического определения МоО3 в виде комплекса
пятивалентного молибдена с роданистым калием K[MoO(CNS)₅],
окрашенного в красно-оранжевый цвет.
2 Состав и структура активной фазы катализаторов
Традиционный сульфидный катализатор гидроочистки
нефтяных топливных фракций состава Ni-(Co)-Mo(W)-S/γ-Al2O3,
используют
уже более 50 лет, готовят методом пропитки пористого носителя (γ-Al2O3)
раствором
активного компонента (соли молибдена, вольфрама, кобальта, никеля). После
стадии пропитки следуют стадии сушки, окисления и активирования системы в
восстановительной среде посредством сульфидирования сероводородом или
диметилдисульфидом при температурах 400-800°C .
ü Достоинство этой системы в том, что
она обладает значительной гибкостью и способна в широких пределах менять свою
активность и селективность при изменении способа синтеза, введении различных
модифицирующих добавок, изменении условий сульфидирования, применении различных
носителей.
ü Недостатком нанесенных
каталитических систем является сложность и трудоемкость отдельных стадий
изготовления, низкая экологичность процедуры изготовления (большое количество
отходов - водных растворов неорганических реагентов), а также умеренная
десульфирующая способность получаемых каталитических систем.
Развитие современных нанесенных катализаторов на
основе Ni-(Co)-Mo(W)-S/γ-Al2O3
реализуется в направлении их совершенствования посредством использования
дополнительных рецептурных и технологических приемов, а именно путем внесения в
состав различных добавок - цеолитов, соединений циркония, ванадия, титана;
повышения концентрации активного компонента путем двухэтапной пропитки
предварительно прокаленного носителя или использования хелатных соединений и
т.д. Указанные подходы в итоге не позволяют повысить активность катализаторов
более чем в 1,5-1,7 раза, что, в свою очередь, препятствует получению топливных
фракций с ультранизким содержанием серы.
Известны также катализаторы, активность которых
выше по сравнению с нанесенными катализаторами в 3 - 4 раза. Это катализаторы
гидроочистки, которые получают на основе дисульфида молибдена. Поскольку
дисульфиды молибдена и вольфрама в крупнокристаллическом состоянии
характеризуются химической и каталитической инактивностью, то используют метод
механохимической активации сульфидных компонентов. Установленным является тот
факт, что перевод MoS2 в наноразмерное состояние сопровождается изменением не
только размера, формы и морфологии кристаллов, но и электронной структуры, их
реакционной способности и каталитической активности. Недостатком описанных
сульфидных систем является то, что выполненные исследования в основном содержат
результаты применительно к оценке активной поверхности лишь одиночных
кристаллов дисульфидов молибдена различной формы или же кристаллитов MoS2,
размещенных на подложках из золота, углерода или полученных в виде
фуреленоподобных структур и нано трубок. При этом приводимые результаты соотносятся
с активностью такого рода каталитических систем в модельных реакциях
относительно индивидуальных веществ - в реакциях изомеризации и гидрирования
алкенов, гидродесульфирования тиофена, дибензтиофена и их производных.
В середине 80-х годов прошлого столетия
установлено, что наиболее активным компонентом Co(Ni)Mo(S)/AlO
катализаторов являются небольшие кристаллиты MoS,
представляющие собой короткие слоистые упаковки, связанные сульфидными
мостиками с атомами промотора Co(Ni).
Распределение соединений кобальта в зависимости
от соотношения Co/Mo
(слева) и состав отдельных фаз Co
соединений на поверхности носителя (справа).
Компания Haldor Topsoe
<https://www.google.ru/url?sa=t&rct=j&q=&esrc=s&source=web&cd=2&cad=rja&uact=8&ved=0CDIQFjAB&url=http%3A%2F%2Fwww.topsoe.com%2F&ei=aqwvU63bPIqO4gSZ44B4&usg=AFQjCNHgWMQOIdl5JZ8iRQjUpCHJhjHIew&bvm=bv.62922401,d.bGE>
(г. Дания, основана в 1940 г. доктором Хальдор Топсе) с сотрудниками при
исследовании CoMo
катализаторов различного состава с помощью Мёссбауэровской спектроскопии
показали, что помимо отдельных, ранее известных фаз кобальта - CoAlO и CoS - в спектре
наблюдались новые фазы, которые предположили отнести к CoMoS фазе.
С помощью метода спектроскопии
(метод исследования локальной атомной структуры перспективных материалов) было
установлено, что каталитическая активность катализаторов гидроочистки связана
именно с концентрацией этой новой фазы и подтверждено её точное строение.
Обнаруженное ранее оптимальное мольное соотношение Co/(Co+Mo) = 0,3
объясняется тем, что все краевые позиции кристаллита MoS покрыты Co или Ni.
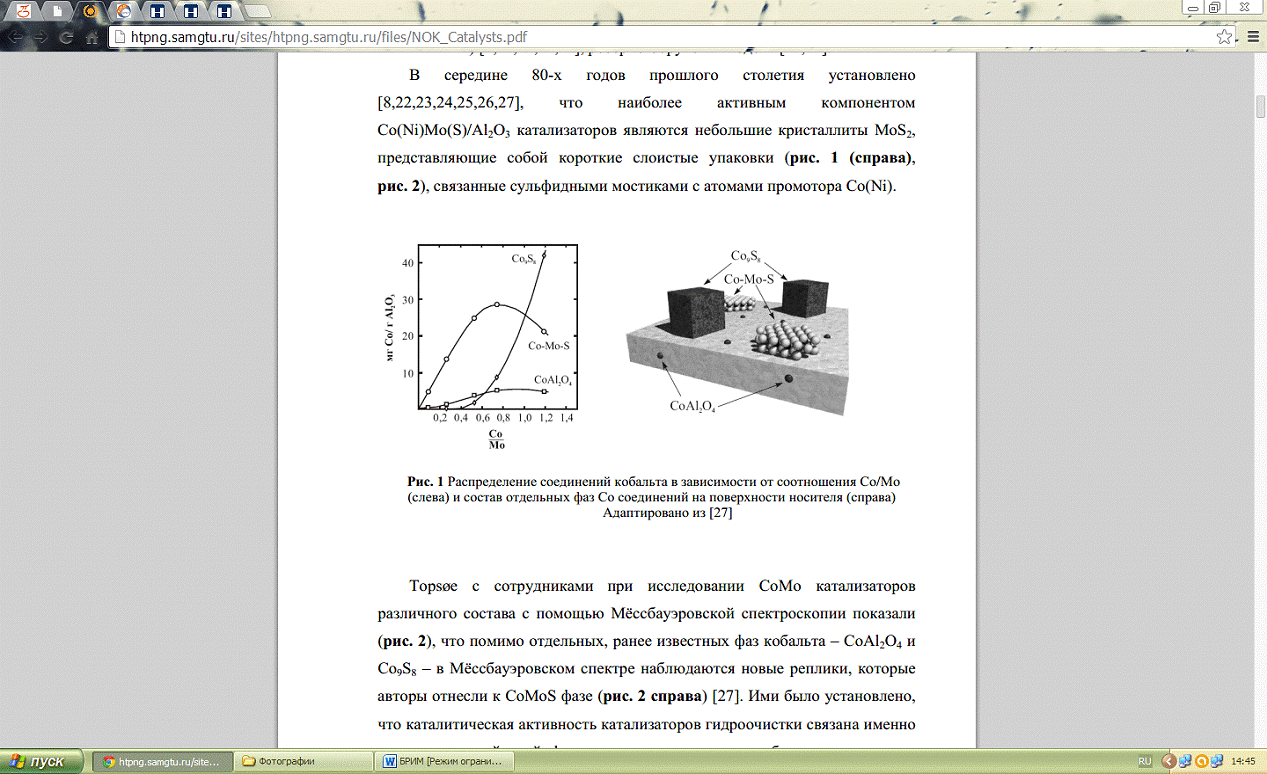
Изображения многослойных CoMoS
и NiMoS нанокластеров.
Снизу изображены их модели.
Жёлтые шары - атомы S,
красные (зелёные) - промотора, синие - Mo.
Было найдено, что константа скорости реакции
гидродесульфуризации тиофена прямо пропорциональна содержанию катионов
промотора в фазе CoMoS.
Но не весь введенный в катализатор промотор находится в составе CoMoS
фазы: часть атомов Со может мигрировать в неактивные шпинели или(и)
образовывать отдельные кристаллиты малоактивных сульфидов. Кроме того, было
установлено, что при высокотемпературном сульфидировании (400 °С и выше)
образуется другая, более активная CoMoS
фаза второго типа.
Различие свойств CoMoS
фаз (фазы первого и второго типа) заключалось во взаимодействии с подложкой.
Взаимодействие уменьшается в CoMoS
фазе второго типа, и характер связей металл-сера становится более ковалентным,
приводя к увеличению активности катализатора в реакции гидродесульфуризации. CoMoS
фаза этого типа формируется в виде многослойных плит MoS.
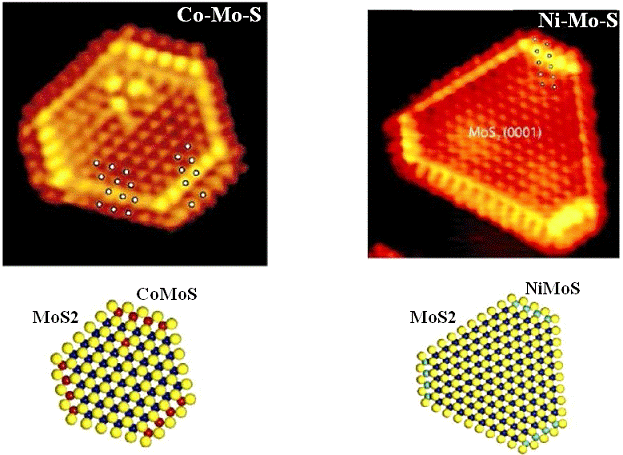
Снимок MoS
кристаллитов на поверхности AlO
(слева) и кристаллит MoS
в виде шаровой модели (справа).
Вид сбоку - упаковка из четырёх плит. Жёлтые
шары - атомы S, синие - Mo.
3 Строение активных центров Со(Ni)MoS2
катализатора
Сульфид молибдена имеет слоистую структуру, в
которой единичные слои Мо4+ расположены между двумя слоями плотно упакованных
анионов S²‾.
В кристаллите слоистой структуры каждый атом Мо окружен шестью атомами серы в
тригонально-призматической координации, где каждый атом серы сильно связан с
тремя атомами Мо.
Толщина кристаллитов MоS,
нанесенных на носитель, меняется от одного до шести слоев, и большая их часть
обладает длиной от 3,33 до 4,59 нм.
Считается, что активные центры сульфидов
располагаются на поверхности ребер и содержат координационно-ненасыщенные атомы
молибдена и атомы серы. Структура дисульфида молибдена в виде связей позволяет
детально представить поверхностные атомы серы и молибдена.
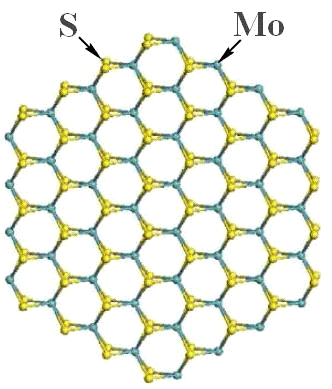
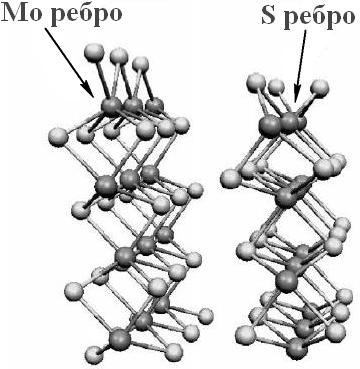
Кристаллит MoS
гексагональной формы
На Мо ребре, т.е. на ребре, ограниченном атомами
молибдена, каждый атом Мо координирован на четыре атома серы, а на ребре,
ограниченном серой (S ребро)
каждый атом S координирован на
два атома Мо.
В условиях взаимодействия плит MoS
с H2S,
Н2, H/HS,
рёбра MoS
каталитически нестабильны. Водород может реагировать с серой, расположенной на S
ребрах, образуя анионные вакансии или координационно-ненасыщенные центры -
атомы молибдена, а сероводород может диссоциированно адсорбироваться на
координационно-ненасыщенные центры молибдена Мо ребер.
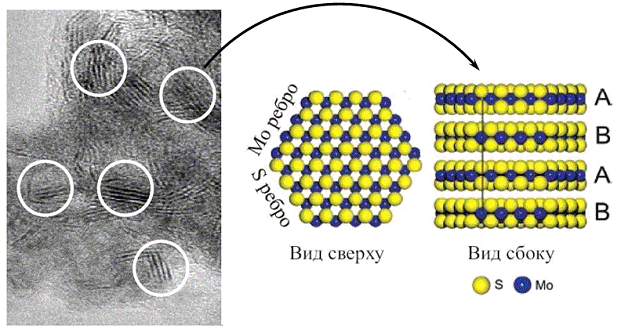
Ребра кристаллитов MoS2
в условиях реакции.
Светлые шары - атомы S,
тёмные - Mo.
На поверхности активной фазы сульфидного
СоМо-катализатора существуют анионные вакансии, SH
группы, диссоциативно адсорбированный водород и адсорбированный молекулярный
водород. Для катализатора характерно определенное соотношение между числом
вакансий и SH групп. В
процессе образования вакансий на Мо и на S
ребрах ключевую роль играет стадия гетеролитической диссоциации молекулярного
водорода.
Cодержание
сероводорода в газовой фазе оказывает существенное влияние на форму
кристаллитов MoS2. При
высокой концентрации НS
кристаллиты имеют треугольную форму, а при низкой концентрации HS
- гексагональную. Таким образом, в зависимости от состава газовой фазы и
внешних условий происходит изменение морфологии MоS
частиц, т.е. атомы серы и молибдена в составе наноструктурированных частиц
способны перестраиваться.
Введение кобальта или никеля в структуру MоS
существенно влияет на структуру и реакционную способность активных центров.
Согласно модели CoMoS-фазы,
наиболее вероятными местами расположения атомов промотора являются ребра
кристаллита MоS.
Замещение молибдена кобальтом уменьшает энергию
связи серы с поверхностью ребра. В одинаковых условиях покрытие серой
поверхности ребер уменьшается, а число вакансий растет в следующем ряду:
MоS
> CoMoS > NiMoS.
Этим объясняется высокая каталитическая активность промотированных Ni(Co)MoS
катализаторов.
4 Анализ генезиса катализаторов гидроочистки
Основными стадиями приготовления нанесенных
сульфидных катализаторов гидроочистки являются:
1. Пропитка
носителя солями предшественников активной фазы;
2. Сушка
и(или) прокаливание катализатора (оксидная форма);
3. Сульфидирование
оксидной формы катализатора.
Важным этапом синтеза катализатора является
создание оксидной формы, которая в дальнейшем будет определять свойства
готового сульфидного катализатора. Оксидная фаза катализаторов представляет
собой, как правило, смешанные оксиды Мо и Ni
(или Со) связанные с AIO.
В процессе сульфидирования катализатора на его
поверхности образуются сульфиднрованные Ni
(или Со) более не связанные с AIO;
Мо-оксисульфид еще связан с AIO.
При дальнейшем сульфидированин часть Мо уже не связана с AIO.
Далее образуются маленькие MoS2
кристаллиты, окруженные Ni
(или Со) и еще якорно связанные с AIO₃.
При полном сульфидировании Мо полностью сульфидирован и кристаллиты MоS,
окруженные Ni (или Со)
сульфидными частицами, становятся подвижными.
Маленькие кристаллиты MoS,
окруженные Ni (или Со)
сульфидными частицами, способны спекаться с образованием больших конгломератов
(стадия деактивации), ребра этих частиц не способны удерживать Ni
(или Со), в результате чего происходит разделение Мо- и Ni(Co)
сульфидов на две фазы. При окислительной регенерации катализатора возможны три
варианта: конгломераты редиспергируются с образованием кристаллитов MоS
и Ni (или Со)
сульфидных частиц, большие кристаллиты MоS,
расположенные на поверхности, окисляются; маленькие структуры полностью
окисляются и почти переходят в исходное состояние.
Сульфидирование оксидных предшественников
оказывает значительное влияние на вид активной фазы (CoMoS
фаза I или II типа). Высокотемпературное сульфидирование приводит к
формированию CoMoS фазы II
типа за счет разрыва связей Mo-O-Al.
Haldor Topsoe
с помощью расчетов показали, что при наличии химической связи с носителем энергия
образования анионных вакансий повышается в 4 - 7 раз в зависимости от числа
анионных вакансий. При высокотемпературном сульфидировании Мо сульфидируется
настолько быстро, что промежуточными стадиями можно пренебречь. Однако при этом
происходит интенсивное спекание активных компонентов с образованием отдельных
фаз сульфидов металлов (Co₉S₈
и MоS),
и этот способ приготовления CoMoS
фазы II типа считается не лучшим.
В настоящее время развиваются способы,
позволяющие получать эту фазу и при мягких условиях сульфидирования. Так
приготовление NiMoS фазы с
использованием комплексонов (нитрилотриуксусной кислоты (НТА),
этилендиаминтетрауксусной кислоты (ЭДТА) и др.) приводит к полному
сульфидированию металлов, при этом не образуются неактивные шпинели.
При традиционном способе приготовления
оксометаллаты и Мо, и Ni
начинают сульфидироваться при 150 °С, в то время как использование ЭДТА
позволяет «связать» атом промотора в комплекс, устойчивый в условиях
сульфидирования до 250°С. При этом температура начала сульфидирования Мо не
изменяется, т.е. равна 150°С. В результате такого эффекта оксометаллаты Мо
сульфидируются быстрее, чем атомы промотора, а с повышением температуры
комплекс ЭДТА с Ni
разрушается, и атомы промотора селективно закрепляются на сформированных плитах
MoS.

Характеристики некоторых брим катализаторов
|
ТК-560
BRIM
|
CoMo
катализатор, с активностью и стабильностью равной катализатору ТК -558 брим,
но с более низким содержанием металлов и показателями заполнения объёма.
TK-560 брим является оптимальным выбором, где стоимость заполнения также
важна, как и производительность.
|
|
ТК-561
BRIM
|
NiMo
катализатор, используемый для гидроочистки нафты и керосина. TK -561 брим
является хорошим катализатором для гидроденитрогенирования. Активно
используется для удаления азота при сохранении высокой HDS активности.
|
|
ТК-562
BRIM
|
Высокоактивный
CoMo катализатор, активность которого на 10% выше по сравнению активностью ТК
-558 брим катализатора, обладает той же высокой устойчивость. Используется
для удаления азота при сохранении высокой HDS активности.
|
|
ТК-563
BRIM
|
Усовершенствованный
брим катализатор. Обеспечивает высокую ГДН и HDS
активность. Катализатор высоко стабилен при обработке как прямогонных
фракций, так и вакуумного газойля.
|
|
ТК-568
BRIM
|
Катализатор,
разработанный для очистки продуктов с малым содержанием серы в топливе и
керосине. Стабилен при обработке как прямогонных фракций, так и дистиллятных
фракций.
|
Список использованных источников
катализатор
сульфидирование гидроочистка
1 Старцев, А.Н. Сульфидные
катализаторы гидроочистки: синтез, структура, свойства / Ин-т катализа им. Г.К.
Борескова СО РАН.- Новосибирск: Академическое из-во «Гео», 2008. - С. 206.
Сайт компании HALDOR
TOPSØE.