Определение содержания свинца в пищевых продуктах, сравнение с ПДК
Реферат
Курсовая работа содержит: ___ страниц, 4
таблицы, 2 рисунка, 8 литературных источника. Объектом исследования в курсовой
работе являются пищевые продукты сложного химического состава.
Цель работы - определить содержание свинца
в пищевых продуктах и сравнить с ПДК.
Метод исследования - атомно-абсорбционный.
Приведены способы пробоподготовки.
Проанализированы и обобщены данные по содержанию соединений свинца в пищевых
объектах (объектов).
Область применения - аналитическая и
токсикологическая химия, лаборатории по стандартизации и качеству пищевых
продуктов, выпускаемых легкой промышленностью, фармацевтическая химия.
Ключевые слова: СВИНЕЦ,
АТОМНО-АБСОРБЦИОННАЯ СПЕКТРОСКОПИЯ, АБСОРБЦИЯ, СТАНДАРТНЫЙ РАСТВОР,
ГРАДУИРОВОЧНЫЙ ГРАФИК, СОДЕРЖАНИЕ, ПДК
Содержание
Введение
1. Литературный обзор
1.1 Химические свойства свинца
1.2 Физиологическая роль свинца
1.3 Пробоподготовка
1.4 Методики определения свинца
1.4.1 Концентрирование следовых количеств иона свинца с помощью
нанометровых частиц диоксида титана (анатаза) с целью последующего их
определения методом атомно-эмиссионной спектрометрии с индуктивно связанной
плазмой с электротермическим испарением пробы
1.4.2 Определение свинца комбинирующем в реальном времени
концентрирование с последующей обращено-фазовой ВЭЖХ
1.4.3 Инверсионно-вольтамперометрическое определение свинца с
использованием стеклоуглеродной электродной системы
1.4.4 Атомно-абсорбционное определение свинца методом дозирования
суспензий карбонизованных образцов с применением Pd-содержащего активированного
угля в качестве модификатора
1.4.5 Фотометрическое определение и концентрирование свинца
2. Экспериментальная часть
Выводы
Список использованной литературы
Введение
Применение материалов, содержащих свинец и его соединения,
привело к загрязнению многих объектов окружающей среды. Определение свинца в
продуктах металлургического производства, биологических материалах, почвах и
т.д. представляет трудности, поскольку ему, как правило, сопутствуют другие
двухвалентные металлы. Для решения такой аналитической задачи распространение
получил атомно-абсорбционный метод определения благодаря доступности
аппаратуры, высокой чувствительности и достаточной точности.
Пищевые продукты могут содержать не только полезные вещества,
но и довольно вредные и опасные для организма человека. Поэтому основной
задачей аналитической химии является контроль качества пищевых продуктов.
А именно в данной курсовой работе используется
атомно-абсорбционный метод определения свинца в кофе.
1.
Литературный обзор
1.1 Химические
свойства свинца
В периодической таблице Д.И. Менделеева свинец располагается
в IV группе, главной подгруппе и имеет атомный вес 207, 19. Свинец в своих
соединениях может находиться в степени окисления +4, однако наиболее
характерная для него +2.
В природе свинец встречается в виде различных соединений,
наиболее важное из которых свинцовый блеск PbS. Распространенность свинца в
земной коре составляет 0,0016 вес. %.
Свинец представляет собой голубовато-белый тяжелый металл
плотностью 11,344 г/см3. Он очень мягок, легко режется ножом.
Температура плавления свинца 327,3 оС. На воздухе свинец быстро
покрывается тонким слоем окисла, защищающим его от дальнейшего окисления. В
ряду напряжения свинец стоит непосредственно перед водородом; его нормальный
потенциал равен - 0,126 В.
Вода сама по себе не взаимодействует со свинцом, но в
присутствии воздуха свинец постепенно разрушается водой с образованием
гидроокиси свинца:
Pb + O2 + H2O = 2Pb (OH) 2
Однако при соприкосновении с жесткой водой свинец покрывается
защитной пленкой нерастворимых солей (главным образом сульфата и основного
карбоната свинца), препятствующей дальнейшему действию воды и образованию
гидроокиси.
Разбавленная соляная и серная кислоты не действуют на свинец
вследствие малой растворимости соответствующих свинцовых солей. Легко
растворяется свинец в азотной кислоте. Органические кислоты, особенно уксусная,
также растворяют свинец в присутствии кислорода воздуха.
Свинец растворяется также в щелочах, образуя плюмбиты. [1]
1.2
Физиологическая роль свинца
Обмен свинца в организме человека и животных изучен крайне
мало. Биологическая роль его также полностью не ясна. Известно, что в организм
свинец поступает с пищей (0,22 мг), водой (0,1 мг) и пылью (0,08мг). Обычно
содержание свинца в организме мужчины составляет около 30мкг %, а у женщин
около 25,5 мкг %.
С физиологической точки зрения свинец и почти все его
соединения токсичны для человека и животных. Свинец даже в очень малых дозах
накапливается в человеческом организме, и его токсическое действие постепенно
усиливается. При отравлении свинцом на деснах появляются серые пятна,
нарушаются функции нервной системы, ощущается боль во внутренних органах.
Острое отравление приводит к тяжелым поражениям пищевода. У людей, работающих
со свинцом, его сплавами или соединениями (например, у типографских
работников), отравление свинцом является профессиональным заболеванием. Опасная
доза для взрослого человека лежит в пределах 30-60 г РЬ (СН3СОО) 2 *
3Н2О [3].
1.3
Пробоподготовка
Отбор и подготовка лабораторной пробы производят в
соответствии с НТД на данный вид продукции. Из объединенной лабораторной пробы
отбирают две параллельные навески.
Продукты с высоким содержанием сахара (кондитерские изделия,
джемы, компоты) обрабатывают серной кислотой (1: 9) из расчета 5 см3 кислоты
на 1 г сухого вещества и выдерживают 2 дня.
Продукты с содержанием жира 20-60% (сыр, масличные семена)
обрабатывают азотной кислотой (1:
) из расчета 1.5 см3 кислоты на 10 г сухого
вещества и выдерживают 15 мин.
Пробы высушивают в сушильном шкафу при 150 оС
(если отсутствуют агрессивные кислотные пары) на электроплитке со слабым
нагревом. Для ускорения сушки проб можно применять одновременное облучение проб
ИК - лампой.
Высушенные пробы осторожно обугливают на электроплитке или
газовой горелке до прекращения выделения дыма, не допуская воспламенения и
выбросов.
Помещают тигли в холодную электропечь и, повышая ее
температуру на 50 оС каждые полчаса, доводят температуру печи до 450
оС. При этой температуре продолжают минерализацию до получения серой
золы.
Охлажденную до комнатной температуры золу смачивают по каплям
азотной кислотой (1:
) из расчета 0.5-1 см3 кислоты на навеску,
выпаривают на водяпой бане и досушивают на электроплитке со слабым нагревом.
Помещают золу в электропечь, доводят ее температуру до 300 оС и
выдерживают 0.5 ч. Этот цикл (обработка кислотой, сушка, озоление) может быть
повторен несколько раз.
Минерализацию считают законченной, когда зола станет белого
или слегка окрашенного цвета без обугленных частиц [3].
Мокрая минерализация. Способ основан на
полном разложении органических веществ пробы при нагревании в смеси
концентрированных азотной кислоты, серной кислоты и перекиси водорода и
предназначен для всех видов продуктов корме сливочного масла и животных жиров.
Навеску жидких и пюреобразных продуктов вносят в плоскодонную
колбу, смачивая стенки стакана 10-15 см3 бидистиллированной воды.
Можно брать навеску непосредственно в плоскодонную колбу.
Навеску твердых и пастообразных продуктов берут на
обеззоленный фильтр, заворачивают в него и стеклянной палочкой помещают на дно
плоскодонной колбы.
Пробы напитков отбирают пипеткой, переносят в колбу Кьельдаля
и выпаривают на электроплитке до 10-15 см3.
Навеску сухих продуктов (желатин, яичный порошок) помещают в
колбу и добавляют 15 см3 бидистиллированной воды, перемешивают.
Желатин оставляют на 1 ч для набухания.
Минерализация проб. Минерализация проб сырья
и пищевых продуктов кроме растительных масел, маргарина, пищевых жиров:
В колбу вносят азотную кислоту на расчет 10 см3 на
каждые 5 г продукта и выдерживают не менее 15 мин, затем вносят 2-3 чистых
стеклянных шарика, закрывают грушевидной пробкой и нагревают на электроплитке
вначале слабо, затем сильнее, упаривая содержимое колбы до объема 5 см3.
Колбу охлаждают, вносят 10 см3 азотной кислоты,
упаривают до 5 см3. Этот цикл повторяют 2-4 раза до прекращения
бурых паров.
В колбу вносят 10 см3 азотной кислоты, 2 см3
серной кислоты и 2 см3 перекиси водорода на каждые 5 г продукта
(минерализацию молочных продуктов проводят без добавления серной кислоты).
Для удаления остатков кислот в охлажденную колбу добавляют 10
см3 бидистиллированной воды, нагревают до появления белых паров и
после этого кипятят еще 10 мин. Охлаждают. Добавление воды и нагревание
повторяют еще 2 раза.
Если при этом образуется осадок, в колбу вносят 10 см3
бидистиллированной воды, 2 см3 серной кислоты, 5 см3
соляной кислоты и кипятят до растворения осадка, дополняя испаряющуюся воду.
После растворения осадка раствор упаривают на водяной бане до влажных солей.
Минерализация растительных масел, маргарина, пищевых жиров:
свинец пищевой продукт химия
Колбу с навеской нагревают на электроплитке 7-8 часов до
образования вязкой массы, охлаждают, добавляют 25 см3 азотной
кислоты и вновь осторожно нагревают, избегая бурного вспенивания. После
прекращения вспенивания в охлажденную колбу добавляют 25см3 азотной
кислоты и 12 см3 перекиси водорода и нагревают до получения
бесцветной жидкости. Если жидкость темнеет, к ней периодически добавляют по 5
см3 азотной кислоты, продолжая нагревание до завершения
минерализации. Минерализацию считают законченной, если раствор после охлаждения
остается бесцветным.
Кислотная экстракция. Способ основан на
экстракции токсичных элементов с разбавленной (1:
) по объему соляной кислотой или разбавленной (1: 2) по
объему азотной кислотой и предназначен для растительного и сливочного масел,
маргарина, пищевых жиров и сыров.
Экстракция проводится в термостойкой с навеской продукта. В
колбу цилиндром вносят 40 см3 раствора соляной кислоты в
бидистиллированной воде (1:
) по объему и столько же азотной кислоты (1: 2). В колбу
добавляют несколько стеклянных шариков, вставляют в нее холодильник, помещают
на электроплитку, и кипятят в течении 1.5 часа с момента закипания. Затем
содержимое колбы медленно охлаждают до комнатной температуры, не вынимая
холодильника.
Колбу с экстракционной смесью сливочного масла, жиров или
маргарина с кислотой помещают в холодную водяную баню для затвердения жира.
Затвердевший жир прокалывают стеклянной палочкой, жидкость фильтруют через
фильтр, смоченный используемой для экстракции кислотой, в кварцевую или
фарфоровую чашу. Оставшийся в колбе жир расплавляют на водяной бане, добавляют
10 см3 кислоты, встряхивают, охлаждают, после охлаждения жир
прокаливают и жидкость сливают через тот же фильтр в ту же чашу, затем
промывают 5-7 см3 бидистиллированной воды.
Экстракционную смесь растительного масла с кислотой переносят
в делительную воронку. Колбу ополаскивают 10 см3 кислоты, которую
сливают в ту же воронку. После разделения фаз нижний водный слой сливают через
смоченный кислотой фильтр в кварцевую или фарфоровую чашу, фильтр промывают 5-7
см3 бидистиллированной воды.
Экстракционную смесь сыра с кислотой фильтруют через
смоченный кислотой фильтр в кварцевую или фарфоровую чашу. Колбу ополаскивают
10 см3 кислоты, которую фильтруют через тот же фильтр, затем фильтр
промывают 5-7 см3 бидистиллированной воды.
Профильтрованный экстракт осторожно выпаривают и обугливают
на электроплитке, а затем озоляют в электропечи.
1.4 Методики
определения свинца
1.4.1
Концентрирование следовых количеств иона свинца с помощью нанометровых частиц
диоксида титана (анатаза) с целью последующего их определения методом
атомно-эмиссионной спектрометрии с индуктивно связанной плазмой с
электротермическим испарением пробы
Атомно-эмиссионная спектрометрия с
индуктивно связанной плазмой (ИСП-АЭС) - широко применяемый и весьма
перспективный метод элементного анализа. Однако он имеет некоторые недостатки,
среди которых сравнительно низкая чувствительность определения, низкая
эффективность распыления, спектральные помехи и другие матричные эффекты.
Поэтому ИСП-АЭС не всегда удовлетворяет требованиям современной науки и
технологии. Сочетание ИСП-АЭС с электротермическим испарением пробы
(ЭТИ-ИСП-АЭС) существенно расширяет возможности метода. Путем оптимизации
температуры пиролиза и испарения можно последовательно испарять определяемые
элементы, отделяя их от матрицы пробы. Этот метод имеет такие преимущества, как
высокая эффективность ввода пробы, возможность анализа малых количеств
образцов, низкие абсолютные пределы обнаружения и возможность прямого анализа
твердых проб.
Инструменты и условия
анализа. Использовали
генератор ИСП мощностью 2 кВт с частотой 27 ± 3 МГц; горелку ИСП; графитовую
печь WF-1А; дифракционный спектрометр РО5-2 с дифракционной решеткой 1300
штрихов/мм с линейной дисперсией 0.8 нм/мм; рН-метр Mettle Toledo 320-S;
осадительную центрифугу модели 800.
Использовали Тритон Х-100 реагентной
чистоты (США). Остальные использованные реагенты были спектроскопической
чистоты; вода дважды дистиллированная. Наночастицы диоксида титана диаметром
менее 30 нм.
Методика анализа. Необходимый объем
раствора, содержащего ионы металла, помещают в градуированную пробирку емк.10
мл и доводят значение рН до 8.0 с помощью 0.1 М НС1 и водного раствора NН3.
Затем в пробирку вносят 20 мг наночастиц диоксида титана. Пробирку встряхивают
в течение 10 мин. (предварительные эксперименты показали, что этого достаточно
для достижения равновесия адсорбции). Пробирку оставляют на 30 мин., затем
удаляют жидкую фазу с помощью центрифуги. После промывания осадка водой к нему
добавляют 0.1 мл 60% -ной суспензии политетрафторэтилена, 0.5 мл 0.1% -ного
раствора агара, 0.1 мл. Тритона Х-100 и разбавляют водой до 2.0 мл. Затем смесь
диспергируют с помощью ультразвукового вибратора в течение 20 мин для
достижения однородности суспензии перед ее вводом в испаритель. В графитовую
печь вносят 20 мкл суспензии после прогрева и стабилизации ИСП. После
высушивания, пиролиза и испарения пары образца переносятся в ИСП током
газа-носителя (аргона); сигналы атомной эмиссии регистрируются. Перед каждым
вводом пробы графитовую печь прогревают до 2700°С для ее очистки.
Применение метода. Разработанный метод
применяют для определения Pb2+ в образцах природной озерной воды и
речной воды. Образцы воды фильтровали через 0.45 мкм мембранный фильтр
немедленно после пробоотбора и затем анализировали.
1.4.2
Определение свинца комбинирующем в реальном времени концентрирование с
последующей обращено-фазовой ВЭЖХ
Приборы и реагенты. Схема системы ВЭЖХ с
концентрированием в режиме реального времени ("on-line") приведена на
рис.1.1 Система состоит из насоса Waters 2690 Alliance (на схеме 2), насоса
Waters 515 (1), детектора с фотодиодной матрицей Waters 996 (7), шестиходового
переключающего крана (4), устройства ввода большого объема (вмещает до 5.0 мл
пробы) (3) и колонок (5,6). Концентрирующая колонка была Waters Xterra™ RP18
(5 мкм,20 х 3.9 мм), аналитическая колонка Waters Xterra™ RP18 (5
мкм, 150 х 3.9 мм). рН определяли рН-метром Beckman Ф-200, оптическую плотность
измеряли спектрофотометром Shimadzu UV-2401.
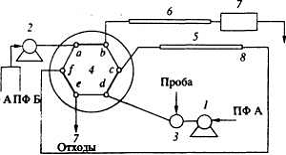
Рис 1.1 Схема системы
концентрирования в режиме реального времени с использованием переключающего
крана
Все растворы готовили на ультрачистой
воде, полученной с помощью системы Milli-Q50 Sp Reagent Water System (Millipore
Corporation). Стандартный раствор свинца (П) с концентрацией 1.0 мг/мл, рабочие
растворы с концентрацией ионов 0.2 мкг/мл готовят разбавлением стандартных.
Используют тетрагидрофуран (ТГФ) для ВЭЖХ (Fisher Corporation),
пирролидин-уксуснокислый буферный раствор концентрации 0.05 моль/л. Стеклянную
посуду перед использованием вымачивали в течение длительного времени в 5% -ном
растворе азотной кислоты и промывают чистой водой.
Методика эксперимента. Необходимый объем
стандартного раствора или пробы вносят в мерную колбу емкостью 25 см3,
додают 6 мл раствора Т4ХФП с концентрацией 1 х10-4 моль/л
в ТГФ и 4 мл раствора пирролидин-уксуснокислого буферного раствора
концентрацией 1 х10-4 моль/л и рН 10, разбавляют до метки водой и
тщательно перемешивают. Смесь нагревают на кипящей водяной бане в течение 10
мин. После с охлаждения разбавляют до метки ТГФ для последующего анализа.
Раствор (5.0 мл) вводят в дозатор, направляют в концентрирующую колонку с
помощью подвижной фазы А со скоростью 2 см3/мин. По окончании концентрирования
путем исключения шестиходового крана хелаты металлов с Т4ХФП,
адсорбированные в верхней части концентрирующей колонки, элюируются потоком
подвижных фаз А и Б со скоростью 1 мл/мин в обратном направлении и направляются
в аналитическую колонку. Трехмерную хроматограмму регистрировали в диапазоне
длин волн максимума поглощения 465 нм с помощью детектора с фотодиодной
матрицей.
1.4.3
Инверсионно-вольтамперометрическое определение свинца с использованием
стеклоуглеродной электродной системы
Приборы и реагенты. Для исследований
использовали электродную систему, представляющую собой сборку из трех
одинаковых стеклоутлеродных (СУ) электродов (индикаторный, вспомогательный,
сравнения), запрессованных в общий корпус из тетрафторэтилена. Длина каждого электрода,
выступающего из корпуса, равна 5 мм. Поверхность одного из них, выбранного в
качестве индикаторного электрохимически обрабатывали асимметричным током при
плотностях в интервале 0.1-5 кА/м2, рекомендуемых для металлов.
Оптимальное время обновления поверхности найдено экспериментально и составляло
10-20 с. Индикаторный электрод служил анодом, а электрод из нержавеющей стали -
катодом. Использовали 0.1 М водные растворы кислот, солей, щелочей, а также 0.1
М растворы щелочей или солей в смеси органических растворителей с водой в
соотношении 1: 19 по объему. За состоянием обработанной поверхности наблюдали
визуально с помощью микроскопа "Neophot 21” с увеличением порядка 3000.
Методика анализа. После обработки
электродную сборку использовали для определения 3*10-6 М свинца (II)
методом инверсионной вольтамперометрии на фоне 1*10-3 М HNO3.
После электролиза при - 1.5 В в течение 3 мин при перемешивании магнитной
мешалкой регистрировали вольтамперограмму на полярографе ПА-2. Потенциал
анодного пика свинца оставался постоянным и составлял - 0.7 В. Скорость
линейной развертки потенциала 20 мВ/с, амплитуда развертки 1.5 В,
чувствительность по току 2 * 10-7 А/мм.
Водные растворы LiNO3, NaNO3,
KNO3 в качестве обрабатывающего электролита позволяют получить
стабильные высоты уже при втором измерении при удовлетворительной
воспроизводимости (2.0, 2.9 и 5.4 % соответственно). Наибольшая
чувствительность показаний достигается при использовании электролита, имеющего
катион меньших размеров.
1.4.4
Атомно-абсорбционное определение свинца методом дозирования суспензий
карбонизованных образцов с применением Pd-содержащего активированного угля в
качестве модификатора
Аналитические измерения проводили на
атомно-абсорбционном спектрометре SpectrAA-800 с электротермическим атомизатором
GTA-100 и автодозатором PSD-97 ("Varian", Австралия). Использовали
графитовые трубки с пиропокрыти-ем и интегрированной платформой
("Varian", Германия), лампы с полым катодом на свинец
("Hitachi", Япония) и кадмий (C'Varian", Австралия). Измерения
интегральной абсорбционности с коррекцией неселективного поглощения света
(дейтериевая система) проводили при спектральной ширине щели 0.5 нм и длине
волны 283.3 нм. В качестве защитного газа служил аргон "сорт высший".
Температурная программа работы атомизатора приведена в табл.1.1
Табл. 1.1 Температурная программа работы электротермического
атомизатора GTA-100
|
Стадия
|
Температура,°С
|
|
Высушивание 1
|
90
|
|
Высушивание 2
|
120
|
|
Пиролиз
|
1300
|
|
Охлаждение
|
50
|
|
Атомизация
|
23ОО
|
|
Очистка
|
2500
|
В качестве модификаторов для
атомно-абсорбционного определения РЬ в графитовой печи исследовали
палладийсодержащие композиции на основе активированного угля и карбонизованной
скорлупы ореха-фундука. Содержание металла в них составляло 0.5-4%. Для оценки
изменений, происходящих с компонентами синтезированных модификаторов в
восстановительных условиях, реализуемых в процессе выполнения анализа,
материалы обрабатывали водородом при комнатной температуре.
Раствор с известной концентрацией РЬ
готовили разбавлением ГСО № 7778-2000 и № 7773-2000 3% HNO3.
Диапазон концентраций рабочих стандартных растворов элемента для построения
градуировочных зависимостей составил 5.0-100 нг/мл. Для приготовления растворов
использовали деионизованную воду.
При построении кривых пиролиза и
атомизации использовали как стандартный раствор элемента, так и карбонизованный
"Стандартный образец состава зерна пшеницы молотой ЗПМ-01". В первом
случае в пластиковом стаканчике автодозатора смешивали 1.5 мл стандартного
раствора элемента (50 нг/мл Pd в 5% HNO3) и 10-12 мг
палладийсодержащего активированного угля; суспензию гомогенизировали и
дозировали в графитовую печь. Во втором - такое же количество модификатора
добавляли к подготовленной суспензии карбонизованной пробы (5-10 мг образца в
1-2 мл 5% HNO3).
1.4.5
Фотометрическое определение и концентрирование свинца
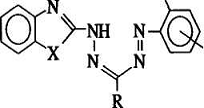
В работе использован ацетат свинца ч. д.
а. Соединения (рис.1, являющиеся двухосновными кислотами) получены
азосочетанием раствора хлорида 2-гидрокси-4 (5) - нитрофенилдиазония и
соответствующего гидразона. Растворы формазанов в этаноле готовили по точной
навеске.
Оптическую плотность растворов измеряли на
спектрофотометре UV-5270 фирмы Веckman в кварцевых кюветах (l = 1 см). Концентрацию
ионов водорода измеряли на иономере И-120М.
Реагенты взаимодействуют с ионами свинца,
образуя окрашенные соединения. Батохромный эффект при комплексообразовании
составляет 175 - 270 нм. На комплексообразование влияет характер растворителя и
строение реагентов (рис.1).
Оптимальными условиями для определения
свинца являются водно-этанольная среда (1:
) и рН 5.5-6.0, создаваемая
аммиачно-ацетатным буферным раствором. Предел обнаружения свинца равен 0.16
мкг/мл. Продолжительность анализа 5 мин.
Наиболее интересно использование формазана
в качестве реагента для концентрирования и последующего фотометрического
определения свинца. Суть концентрирования и последующего определения свинца
(II) с помощью формазана заключается в том, что из водно-этанольного раствора в
присутствии ионов Ni, Zn, Hg, Co, Cd, Cr, Fe, хлороформным раствором формазана
экстрагируют комплекс свинца.
Для сравнения использовали методику
определения свинца сульфарсазеном (ГОСТ, МУ вып 15, № 2013-79). Полученные
результаты анализа модельных растворов двумя методиками приведены в табл.1.2
Сравнение дисперсий по F-критерию показало, что Fэксп < Fтеор (Р =
0.95; f1 =f2 = 5); значит, дисперсии однородны.
Табл. 1.2 результаты определения свинца в
модельных растворах (n=6; P=0.95)
|
Введено, мкг/мл
|
Найдено
|
Найдено
|
Fэксп
|
F теор
|
|
сульфарсазеном,
мкг/мл
|
Sr
|
формазаном,
мкг/мл
|
Sr
|
|
|
|
4.14 2.10 3.99
|
4.04 ±0.28
2.06±0.29 3.92 ±0.17 0.29 3.92 ±0.17
|
2.8 5.5 1.7
|
4.14 ±0.07 2.10
±0.08 3.99 ± 0.07
|
2.1 *10-2 2.5*10-2
2.1*10-2
|
3.97 3.57 3.37
|
4.53
|
2.
Экспериментальная часть
Средства измерений, реактивы и материалы:
При выполнении по данной методике используют следующие
средства измерений, устройства, реактивы и материалы:
· Атомно-абсорбционный спектрометр
· Лампа спектральная с полым катодом
· Компрессор для подачи сжатого воздуха
· Редуктор - по ГОСТ 2405
· Стаканы лабораторные, емкостью 25-50 см3
- по ГОСТ 25336
· Колбы мерные второго класса точности
емкостью 25-100 см3
· Воронки лабораторные по ГОСТ 25336
· Вода дистиллированная
· Кислота азотная концентрированная, х. ч.,
ГОСТ 4461-77
· Стандартный раствор свинца (с = 10-1
г/л)
Условья определения:
§ Длина волны при определении свинца λ =283,3 нм
§ Сила тока лампы 10 мА
Метод измерения:
Атомно-абсорбционная спектроскопия основана на поглощении
излучения оптического диапазона невозбужденными свободными атомами свинца,
образующимися при введении анализируемой пробы в пламя при длине волны λ =283,3 нм [2].
Требования безопасности:
При выполнении всех операций необходимо строго соблюдать
правила техники безопасности при работе в химической лаборатории,
соответствующие ГОСТ 126-77 "Основные правила безопасности в химической
лаборатории", включая правила безопасной работы с электротехническими
устройствами с напряжением до 1000 вольт.
Приготовление градуировочных растворов свинца:
Растворы готовят, используя стандартный раствор свинца с
концентрацией
с= 10-1 г/л.
Для построения градуировочного графика используют растворы
следующих концентраций:
*10-4, 3*10-4, 5*10-4, 7*10-4,
10*10-4 г/л
Стандартный раствор объемом 10 см3 вносят в колбу
вместимостью 100 мл, доводять до метки дистиллированной водой. В 5 мерных колб
вместимостью 100мл вносять соответственно 1, 3, 5, 7, 10 мл промежуточного
раствора (раствор концентрации 10-2 г/л). Доводять до метки
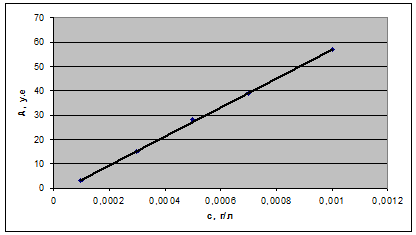
дистиллированной водой. Строят гардуировачный график в координатах А, у. е от
с, г/л
Табл.2.1 Результаты измерений
|
концентрация,
г/л
|
Сигнал, у. е.
|
|
0,0001
|
3
|
|
0,0003
|
15
|
|
0,0005
|
28
|
|
0,0007
|
39
|
|
0,0010
|
57
|
Пробоподготовка:
Беру навеску кофе массой 1.9975 г.
Вношу ее в стакан емкостью 100 мл.
Растворяю навеску в 20 мл концентрированной азотоной кислоты.
Выпариваю содержимое стакана на водяной бане до половины исходного
объема, периодами помешивая.
Раствор в стакане после выпаривания мутный, следовательно с
помощью лабораторной воронки и бумажного фильтра отфильтровываю содержимое
стакана в стакан емкостью 25 мл.
Отфильтрованный раствор вношу в колбу емкостью 25 мл и довожу до
метки дистилированой водой.
Тщательно перемешиваю содержимое колбы.
Вношу часть раствора с колбы в пипетку, что и служит пробой для
определения содержания свинца.
Для определения неизвестной концентрации, раствор вводят в
атомизатор и после 10-15 секунд регистрируют показания прибора. Усредненные
показания прибора откладывают на оси ординат градуировочного графика, и на оси
абсцисс находят соответственное значение концентрации, сх г/л
Для расчета концентрации в образце использую расчетную формулу:
С =0.025*Сх*10-4*1000/ Mнав (кг)
Табл 2.2 Результаты измерений
|
Проба
|
Сигнал, у. е.
|
Среднее
|
Сх,
г/л
|
|
|
1
|
2
|
3
|
|
|
|
кофе
|
15
|
14
|
15
|
14,66667
|
2.9*10-4
|
|
сырок
|
0
|
0
|
0
|
0
|
0
|
|
ябл. сок
|
0
|
0
|
0
|
0
|
0
|
|
виногр. сок
|
0
|
0
|
0
|
0
|
|
крем
|
3
|
2
|
2
|
2.33333
|
7.8*10-5
|
|
вода
|
0
|
0
|
0
|
0
|
0
|
|
шампунь
|
0
|
0
|
0
|
0
|
0
|
Исходя из табличных данных, рассчитываю
концентрацию свинца в образцах:
|
Образец
|
ПДК, мг/кг
|
|
кофе
|
10
|
|
крем
|
|
С (Pb в пробе кофе) = 3.6 мг/кг
С (Pb в пробе крем) = 0.98 мг/кг
Выводы
В работе изложены методики определения свинца различными физико-химическими
методами.
Приведены методы пробоподготовки для ряда пищевых объектов.
На основе литературных данных выбран наиболее удобный и
оптимальный метод определения свинца в различных пищевых продуктах и природных
объектах.
Использованный метод отличается высокой чувствительностью и
точностью наряду с отсутствием отклика на присутствие других элементов, что
позволяет получать истинные значения содержания искомого элемента с высокой
степенью достоверности.
Выбранный метод позволяет также проводить исследования без
особых трудностей в пробоподготовке и не нуждается в маскировании других
элементов. Кроме этого, метод позволяет определять и содержание других
элементов в исследуемой пробе.
По экспериментальной части можно сделать вывод, что
содержание свинца в кофе "Черная карта" не превышает предельно
допустимой концентрации, следовательно продукт пригоден для поступления в
продажу.
Список
использованной литературы
1.
Глинка Н.И. Общая химия. - М.: Наука, 1978. - 403 с.
.
Золотов Ю.А. Основы аналитической химии. - М.: Высш. шк.; 2002. - 494 с.
.
Реми Г. Курс общей химии. - М: Изд. иностр. лит., 1963. - 587 с.
.
ГОСТ № 30178 - 96
.
Йипинг Ханг. // Журн. аналит. хим., 2003, Т.58, № 11, с.1172
.
Лианг Ванг. // Журн. аналит. хим., 2003, Т.58, № 11, с.1177
.
Невоструев В.А. // Журн. аналит. хим., 2000, Т.55, № 1, с.79
.
Бурилин М.Ю. // Журн. аналит. хим., 2004, Т.61, № 1, с.43
.
Маслакова Т.И. // Журн. аналит. хим., 1997, Т.52, № 9, с.931