Определение карбоксильных групп в различных системах
Министерство
образования Республики Беларусь
Учреждение
образования
«Могилёвский
государственный университет имени А.А. Кулешова»
Выпускная
работа
по
анализу биологических объектов
Определение
карбоксильных групп в различных системах
студенток 4-ого
курса
дневная форма
обучения
группа 4 «Х»
Н.Д. Городецкая,
Е.В. Сказецкая
Научный
руководитель
канд. хим. наук
доцент
Н.А.Клебанова
Могилёв
г
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
ГЛАВА
I. ОБЗОР ЛИТЕРАТУРЫ
.1
Химический состав, структура, характерные
показатели и применение пектина
.2
Строение, образование и применение глюкозы
.3
Влияние микроорганизмов на различные
системы
ГЛАВА
II. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1
Титриметрическое определение содержания карбоксильных групп в пектине
СПИСОК
ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
карбоксильный пектин глюкоза титриметрическое
ВВЕДЕНИЕ
В настоящее время люди потребляют большое
количество пищевых волокон, но не происходит дополнительного употребления
бифидобактерий для разложения большого количества волокон. В литературе было
показано, что бифидобактерии продуцируют большое количество органических кислот
(молочной, уксусной, янтарной) и летучих жирных кислот (уксусная, пропионовая,
масляная, изомасляная, валериановая, изовалериановая, капроновая,
изокапроновая), за счет которых подавляется рост и размножение патогенных и
условно патогенных бактерий.
В последнее время широко используются пищевые
волокна (пектин), которые также могут быть субстратами для бифидобактерий.
Пектин - водорастворимое вещество, свободное от
целлюлозы и состоящее из частично или полностью метоксилированных остатков
полигалактуроновой кислоты.
В процессе метаболизма за счёт образования
карбоновых кислот содержание карбоксильных групп должно возрастать.
Поэтому, целью нашей исследовательской работы,
было определение количества карбоксильных групп в различных системах.
Передо мной были поставлены следующие задачи:
определение количества карбоксильных групп в
пектине
определение количества карбоксильных групп в
системе пектин-бифидобактерии
определение количества карбоксильных групп в
глюкозе
определение количества карбоксильных групп в
системе глюкоза-бифидобактерии
ГЛАВА I. ОБЗОР
ЛИТЕРАТУРЫ
.1 Химический состав, детоксицирующие свойства,
структура, характерными показатели и применение пектина
Пектины это природные полисахариды, которые
содержатся почти во всех растениях. Как вещество, пектин был открыт более 200
лет назад и впервые получен из корнеплода топинамбура (земляной груши) [13].
Наиболее распространенным в нашей стране
пектинсодержащим сырьем являются яблоки, сахарная свекла, цитрусовые,
подсолнечник, клубни топинамбура и др [5,17].
Пектин способен сорбировать и выводить из
организма микроорганизмы и выделяемые ими токсины, биогенные токсины,
анаболики, ксенобиотики, продукты метаболизма, а также биологически вредные
вещества, способные накапливаться в организме: холестерин, желчные кислоты,
мочевину, билирубин, серотонин, гистамин, продукты тучных клеток [8]. В
процессе усвоения пищи деметоксилизация пектина способствует превращению его в
полигалактуроновую кислоту, которая соединяется с определенными тяжелыми
металлами и радионуклидами, в результате чего образуются нерастворимые соли, не
всасывающиеся через слизистую желудочно-кишечного тракта и выделяющиеся из
организма вместе с калом [16].
Для оценки детоксицирующих свойств пектина имеют
значение такие показатели как: молярная масса, уронидная составляющая, степень
этерификации, содержание свободных карбоксильных групп, связывающая
способность, сорбционная способность, полная статистическая обменная емкость и
др [1,8].
Пектины представляют собой полисахариды
клеточных стенок. Основным компонентом пектиновых полисахаридов являются
полиуроновые кислоты. У высших растений они состоят из остатков
D-галактуроновой кислоты, связанных С-1®С-4-связями, на долю
которой в зависимости от источника происхождения пектиновых веществ приходится
от 83 до 90 % [14].
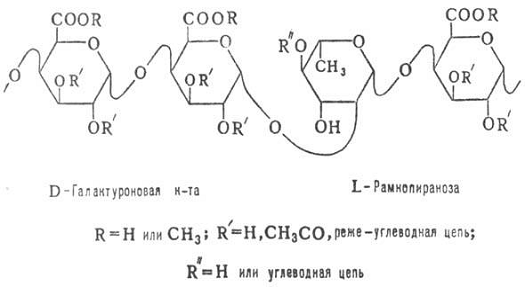
Карбоксильная группа каждого остатка
D-галактуроновой кислоты может существовать в разных состояниях: образовывать
соли с ионами определенных металлов, чаще всего кальция (пектат), причем атомы
двух- и трехвалентных металлов могут связывать несколько цепей
полигалактуроновой кислоты; соль может быть одновременно и метоксилирована
(пектинат), или оставаться немодифицированной (пектовая кислота -
основа всех видов пектиновых веществ), или быть частично метоксилированной (эту
форму обычно называют пектином) , что изображено на рисунке 1.1.1: [1]
Рисунок 1.1.1
Незначительную часть в составе пектиновых
веществ составляют нейтральные полисахариды - арабинаны и
галактаны, что и обусловливает гетерополисахаридный характер пектина [14].
Арабинаны представляют собой разветвленные полимеры, состоящие из остатков
L-арабофуранозы, соединенные между собой α-С-1®С-5-связями.
Галактаны - неразветвленные цепи, образованные из остатков
D-галактопиранозы, соединенных b-С-1®С-4-связями.
При этом возможно, что часть карбоксильных групп галактуроновой кислоты
этерифицирована указанными нейтральными полисахаридами. Молекулярная масса
пектиновых веществ достигает 200000.
Согласно современным представлениям пектин имеет
линейную структуру, в которой остатки D-галактуроновой кислоты имеют пиранозную
конфигурацию. Используют и другой способ изображения молекулы пектина, в
котором отдельные кольца повернуты относительно друг друга и лежат в различных
плоскостях. Структурная формула пектина предствлена на рисунке 1.1.2: [6].
Рисунок 1.1.2
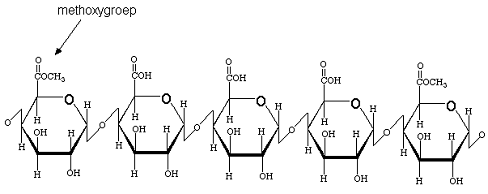
Пектин (pectin) - водорастворимое вещество,
свободное от целлюлозы и состоящее из частично или полностью метоксилированных
остатков полигалактуроновой кислоты. В зависимости от количества метоксильных
групп и степени полимеризации существуют различные пектины. Н-пектин (H-pectin)
- высокоэтерифицированный пектин. Имеет степень этерификации, т. е. отношение
числа этерифицированных карбоксильных групп на каждые 100 карбоксильных групп
пектиновой кислоты, более 50 %; L-пектин (L-pectin) - низкоэтерифицированный
пектин. Имеет степень этерификации менее 50 %;
Структура и химический состав пектиновых веществ
определяют пространственную форму их молекул и характер взаимодействия с
другими соединениями. Установлено, что пектиновые вещества обладают структурой
с ограниченной гибкостью, стабилизируемой водородными и гидрофобными связями [9].
Пектиновые растворы оптически активные,
правовращающие, удельное вращение постоянно при значении рН около от 3,0 до 6,5
[5].
Характерными показателями пектина являются:
Молекулярный вес, метоксильное число, ацетильное
число, растворимость в воде, вязкость золя, желеобразующая способность [4].
Содержание метоксильных групп является важным
показателем пектиновых веществ. Степень этерификации полигалактуроновой кислоты
меняется в широких пределах в зависимости от источника получения и способа
извлечения - от полностью лишенной метоксильных групп (пектовой кислоты) до
полностью замещенных всех карбоксильных остатков полигалактуроновой кислоты
[6]. Пектины, полученные из разных растений, значительно различаются по степени
этерификации [1].
Метоксильное число имеет большое значение для
желирующих свойств пектина. Для желеобразующего пектина установлена норма
содержания метоксильных групп не ниже 7 %. Количество карбоксильных груп
достигает до 3,7% (свекловичный пектин содержит наибольшее количество
карбоксильных групп).
Значительно в меньшем количестве содержатся в
пектине ацетильные группы. Ацетильное число колеблется в широких пределах: от
сотых долей процента до 2,5 %. Ацетильные группы оказывают отрицательное
влияние на желирование. Установлены допустимые пределы содержания ацетильных
групп для студнеобразующего пектина - не более 1 %.
Наилучшим растворителем пектиновых веществ
является вода. Растворяются они также в 84%-ной фосфорной кислоте и жидком
аммиаке; в глицерине и формамиде - набухают. В остальных органических и
неорганических растворителях они практически нерастворимы [7].
Растворимость пектина в воде возрастает с
увеличением степени этерификации и с уменьшением степени полимеризации. Из двух
пектинов с одинаковой длиной цепи легче растворим тот, у которого выше
метоксильное число; из двух пектинов одинаковой степени этерификации легче
растворим обладающий меньшим молекулярным весом [10].
Желирующая способность пектина растительного,
широко используемая пищевой промышленностью, у разных растений далеко не
одинакова и зависит от относительной молекулярной массы пектина, от степени
метоксилирования остатков галактуроновой кислоты и количества сопутствующих
балластных веществ, концентрации сахара в растворе, температуры и рН среды [5].
Между карбоксильными и гидроксильными группами
цепей пектиновой кислоты возникают водородные связи. Возможно, что водородные
связи образуются также между карбоксильными и гидроксильными группами
пектиновых молекул и полярными группами сахара [12].
При повышении температуры пектины разрушаются
[5]. Этот процесс сопровождается уменьшением вязкости и желирующей способности.
Понижение вязкости и желирующей способности вызывается разрушением
суперструктуры пектиновых веществ. Оптимальной для сушки пектиновых веществ
является температура, приблизительно равная 80°С. При сушке
выше этой температуры желеобразование пектина ухудшается в связи с происходящей
деградацией.
Под действием кислот молекулы растворимых
пектиновых веществ могут претерпевать одновременно два существенных изменения
[2]:
а) омыление этерифицированных карбоксильных
групп;
б) разрушение молекулы вследствие разрыва
гликозидной связи между остатками D-галактуроновой кислоты.
При действии сильной минеральной кислоты на
высокоэтерифицированную пектиновую даже при комнатной температуре через
несколько недель происходит ее омыление до нерастворимой полигалактуроновой
кислоты, выпадающей в осадок. Одновременно с метоксильными омыляются и
ацетильные группы пектиновой молекулы. При повышении температуры кислотное
омыление происходит быстрее. При дальнейшем же повышении температуры скорость
этого процесса еще более возрастает, но вместе с тем начавшийся распад
макромолекул по главным валентностям увеличивается настолько, что деградация
начинает преобладать над омылением [6]. В присутствии сахарозы окислительный
распад пектиновых веществ подавляется, т.е. сахароза является ингибитором
окисления пектиновых веществ [5].
Карбоксильные и гидроксильные группы пектиновой
или пектовой кислот могут вступать в химические реакции; полученные при этом
соединения рассматриваются как соответствующие производные двух видов [16].
Карбоксильные группы пектина могут
восстанавливаться до первичных спиртовых групп с помощью алюмогидрида лития или
боргидрида натрия. Довольно легко происходит сшивка пектиновых веществ
формальдегидом в присутствии соляной кислоты как катализатора, в результате
чего образуется метилольный полуацеталь пектина [3].
При взаимодействии пектиновых веществ с
полифункциональными соединениями образуются пространственные трехмерные
структуры. В качестве связующих агентов используют диметилдихлорсилан,
глиоксаль, дихлорэтилсульфамид и др [11].
Объединенный комитет экспертов ФАО/ВОЗ по
пищевым добавкам рекомендует пектин как безопасную добавку без ограничения
приемлемой дозы ежедневного потребления [16]. Одно из направлений применения
пектинов связано с их использованием в фармацевтических технологиях. Вместе с
тем большой интерес вызывают результаты экспериментальных и клинических
исследований, свидетельствующие о том, что пектины способны проявлять лечебные
и профилактические свойства при ряде заболеваний, не уступая по эффективности
некоторым лекарственным препаратам.
В медицине пектин используется при лечении
желудочно-кишечного тракта, для профилактики сахарного диабета, онкозаболеваний
[17]. Пектин способствует снижению кровяного давления, выведению из организма
холестерина, нормализации обменных процессов, улучшает периферическое
кровообращение, перистальтику кишечника, рекомендуется для диетического питания
[17].Установлено, что пектиновые вещества тормозят процессы гниения в кишечнике
больше, чем искусственно введенные дезинфицирующие вещества [15].
Пектин обладает способностью очищать организм от
вредных веществ, не нарушая при этом бактериологический баланс организма.
Благодаря способности пектиновых веществ не расщепляться под действием
ферментов желудка, а также взаимодействовать с ионами различных металлов, они
используются как профилактическое средство при интоксикации организма тяжелыми
металлами [7].
Наличие в составе пектиновых веществ уроновых
кислот повышает сопротивляемость организма [6].
Пектины являются вспомогательным средством при
приготовлении многих лекарственных форм, служат основой для получения пастилок,
суппозиториев, являются исходным сырьем в приготовлении гидрогелей, таблеток,
мягких желатиновых и ректальных капсул, свечей. Используется их
пролонгированное действие в таблетках, микстурах с разными лекарственными
препаратам [9].
.2Строение, образование и применение глюкозы
Глюкоза - моносахарид, одна из восьми изомерных
альдогексоз. Глюкоза в виде D-формы (декстоза, виноградный сахар) является
самым распространённым углеводом. D-глюкоза (обычно её называют просто
глюкозой) встречается в свободном виде и в виде олигосахаридов (тростниковый
сахар, молочный сахар) , полисахаридов (крахмал, гликоген, целлюлоза, декстран)
, гликозидов и других производных. В свободном виде D-глюкоза содержится в
плодах, цветах и других органах растений, а также в животных тканях (в крови,
мозгу и др.) . D-глюкоза является важнейшим источником энергии в организмах
животных и микроорганизмов.
Продуктом полного гидролиза крахмала и целлюлозы
является глюкоза. При разрыве полуацетальной (гликозидной) связи образуются
гидроксильная и альдегидная (в полуацетальной форме) группы. Образование
глюкозы после гидролиза крахмала и целлюлозы представлено на рисунке 1.3.1:
Рисунок 1.3.1
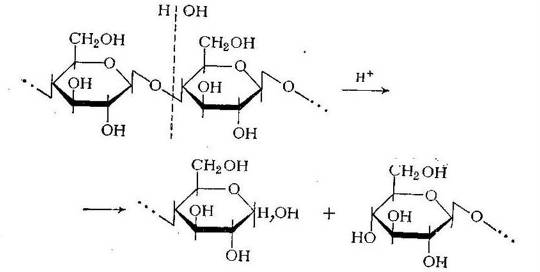
Катализаторами реакции гидролиза полисахаридов
являются водородные ионы. Гидроксильные ионы не ускоряют этой реакции,
благодаря чему полисахариды относительно стойки в щелочной среде и нестойки в
кислой. Катализаторами реакции гидролиза полисахаридов служат также ферменты:
а-глюкозидаза для крахмала и р-глюкозидаза для целлюлозы [18].
Глюкоза является альдегидоспиртом, так как атомы
углерода связаны между собой сигма-связью, возможно вращение частей молекулы
относительно сигма-связей. При этом альдегидная функциональная группа
взаимодействует со спиртовым гидроксилом пятого углеродного атома, и образуется
циклическая форма глюкозы, которая пердствлена на рисунке 1.3.1:
Рисунок 1.3.1
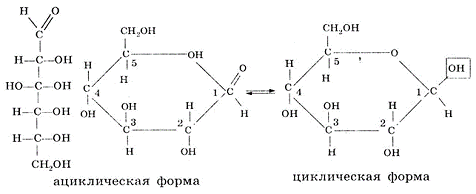
В растворе ациклическая (альдегидная) форма
глюкозы находится в равновесии с циклической (полуацетальной) формой. При
переходе ациклической формы в циклическую полуацетальную форму у первого
углеродного атома формируется полуацетальная - гликозидная гидроксигруппа. По
своим свойствам эта группа отличается от спиртовой. В циклической глюкозе,
которая имеет строение кресла или лодки, полуацетальный гидроксил жестко
расположен в пространстве относительно плоскости [19].
Применение глюкозы:
Глюкоза является ценным питательным продуктом. В
организме она подвергается сложным биохимическим превращениям в результате
которых образуется диоксид углерода и вода, при это выделяется энергия согласно
итоговому уравнению: C6H12O6 + 6O2 = 6H2O + 6CO2 + 2800 кДж. Этот процесс
протекает ступенчато, и поэтому энергия выделяется медленно.
Так как глюкоза легко усваивается организмом, её
используют в медицине в качестве укрепляющего лечебного средства при явлениях
сердечной слабости, шоке, она входит в состав кровозаменяющих и противошоковых
жидкостей. Широко применяют глюкозу в кондитерском деле (изготовление
мармелада, карамели, пряников и т.д.), в текстильной промышленности в качестве
восстановителя, в качестве исходного продукта при производстве аскорбиновых и
гликоновых кислот, для синтеза ряда производных сахаров и т.д.
Большое значение имеют процессы брожения
глюкозы. Так, например, при квашении капусты, огурцов, молока происходит
молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если
подвергаемая силосованию масса недостаточно уплотнена, то под влиянием
проникшего воздуха происходит маслянокислое брожение и корм становится
непригоден к применению.
.3Влияние микроорганизмов на
различные
системы
Морфологически бифидобактерии представляют собой
неспорообразующие, грамположительные палочки, в старых культурах могут
встречаться грамотрицательные варианты.
Для большинства штаммов оптимальной является
температура 36- 38°С, рост почти всех штаммов прекращается при 20°С и ниже,
максимальная температура находится в пределах 45-50°С. Оптимальным для развития
бифидобактерии является рН 6-7. При рН ниже 5,5 рост этих микроорганизмов
приостанавливается. Основными продуктами метаболизма при сбраживании глюкозы
являются уксусная кислота и L( + )-молочная кислота с небольшой примесью
муравьиной и янтарной кислот. Масляная и пропионовая кислоты и углекислый газ
не образуются. Некоторые штаммы бифидобактерии продуцируют ферменты,
полисахариды с различными свойствами и составом.
Наибольшее значение для организма человека
имеют: Bifidobacterium bifidum, Bifidobacterium lonngum.Их содержание о
организме - 10*8-10*12 КОЕ в 1 мл кишечного содержимого и составляют 90-98% от
общего объема нормофлоры кишечника ( в зависимости от возраста).
Бифидобактерии участвуют в утилизации пищевых
субстратов, улучшают процессы гидролиза и всасывания белков, углеводов,
активизируют пищеварение и стимулирауют перистальтику толстого кишечника.
Обладают детоксикационными свойствами, разлагают 50% мочевины, снимая нагрузку
с почек. Оказывают стимулирующее влияние на функции печени путем обеспечения
кишечно-печеночной циркуляции органических и неорганических соединений,
гормонов, цитокинов, ведущих компонентов желчи-солейжелчных кислот, желчных
пигментов, холестерина, кобальта, цинка.
Бифидобактерии продуцируют большое количество
органических кислот (молочной, уксусной, янтарной ) и летучих жирных кислот
(уксусная, пропионовая, масляная, изомасляная, валериановая, изовалериановая,
капроновая, изокапроновая), за счет которых подавляется рост и размножение
патогенных и условно патогенных бактерий.
Бифидобактерии способны перерабатывать
моносахариды (глюкозу, галактозу и фруктозу). Для большинства бифидобактерий
оптимальной является температура 36-38°С, рН 6-7.
При гидролизе пектиновой кислоты пектиназой в
течение первых стадий разложения аккумулируются только небольшие количества
свободной D-галактуроновой кислоты. Обычно ферментами разлагаются ди-, три -,
тетра - и пентагалактуроновые кислоты. В последующие стадии гидролиза длинные
молекулы распадаются под влиянием каталитической деятельности пектиназы и
накапливаются свободная D-галактуроновая кислота и другие соединения.
Распад пектиновой кислоты может быть выражен
следующей схемой:
С46Н68О40 + nН20 = СНО(СНОН)4СООН+С6Н12О6 +
С5Н10О5 + С5Н10 О5 + СН3ОН + СН3СООН
Продукты распада пектиновой кислоты (галактоза,
арабиноза и др.) подвергаются окислению или сбраживанию разнообразными
микроорганизмами. В частности, при анаэробиозе они сбраживаются бактериями.
Продуктами брожения являются органические кислоты (уксусная, молочная), а также
газы Н2 и СО2, кроме указанных веществ, образует и небольшое количество ацетона
и бутилового спирта.
ЧАСТЬ II. ЭКСПРИМЕНТАЛЬНАЯ
.1Титриметрическое определение содержания
карбоксильных групп в пектине
Методика определения содержания свободных
карбоксильных групп(ОСТ 18-62-72):
Около 1 г промытого и высушенного пектина
помещают в колбу на 300 мл, смачивают чистым 96%-ным этиловым спиртом для
предотвращения комкования и добавляют 100 мл дистиллированной воды,
перемешивают и оставляют на ночь для полного растворения пектина. Раствор
титруют 0,1 н NaOH до появления красного окрашивания, не исчезающего в течение
1 минуты, при добавлении 6 капель индикатора Хинтона (для его приготовления
смешивают 1 объем 0,4 % бромтимолблау, 1 объем 0,4%-ного красного крезола, 3
объема 0,4% красного фенола и 1 объем дистиллированной воды).
Содержание свободных карбоксильных групп Кс, %,
рассчитывают по формуле (1).
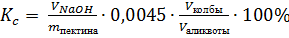 (1)
(1)
Для проведения эксперимента нами был выбран в
качестве бактерий препарат «Бифидумбактерин форте». Этот препарат представляет
собой микробную массу живых бактерий антоганистически активного штамма
Bifidobacterium bifidum №1, сорбированных на частицах активированного угля,
лиофилизированную, смешанную с лактозой.
Система пектин-бактерии:
В качестве субстрата нами был использован
свекловичный пектин, который растворяли на водном термостате при температуре
40°С что известно из литературы.
Для приготовления системы брали раствор пектина,
концентрацией 1 грамм на 100 миллилитров, и аккуратно всыпали бактерии (в одном
пакетике не менее 50 млн колониеобразующих единиц) в колбу. Один пакетик
препарата на 100 мл раствора.
Первый эксперимент проводился в течение 28
часов, результаты исследования представлены в таблице 2.1.1.
Таблица 2.1.1
|
Время,
мин
|
V(NaOH)б,
мл
|
V(колбы),
мл
|
V(аликвоты),
мл
|
m(пектина),
г
|
Кс
б, %
|
V(NaOH)
без б, мл
|
Кс
без б, %
|
∆Кс,
%
|
|
0
|
1,415
|
500
|
10
|
5,11
|
6,2304
|
1,415
|
6,2304
|
0
|
|
120
|
1,525
|
500
|
10
|
5,11
|
6,7148
|
1,5
|
6,6047
|
1,67
|
|
240
|
500
|
10
|
5,11
|
7,0450
|
1,5
|
6,6047
|
6,67
|
|
480
|
1,6
|
500
|
10
|
5,11
|
7,0450
|
1,5
|
6,6047
|
6,67
|
|
600
|
1,615
|
500
|
10
|
5,11
|
7,1111
|
1,5
|
6,6047
|
7,67
|
|
1440
|
1,62
|
500
|
10
|
5,11
|
7,1331
|
1,5
|
6,6047
|
8
|
|
1680
|
1,655
|
500
|
10
|
5,11
|
7,2872
|
1,5
|
6,6047
|
10,33
|
Второй эксперимент проводился в течение 29 часов
30 минут, результаты исследования представлены в таблице 2.1.2.
Таблица 2.1.2
|
Время,
мин
|
V(NaOH)б,
мл
|
V(колбы),
мл
|
V
(аликвоты),
мл
|
m(пектина),
г
|
Кс
б, %
|
V(NaOH)
без б, мл
|
Кс
без б, %
|
∆Кс,
%
|
|
0
|
1,43
|
500
|
10
|
5,13
|
6,2719
|
1,43
|
6,2719
|
0
|
|
120
|
1,515
|
500
|
10
|
5,13
|
6,6447
|
1,5
|
1
|
|
180
|
1,61
|
500
|
10
|
5,13
|
7,0614
|
1,505
|
6,6009
|
6,98
|
|
390
|
1,61
|
500
|
10
|
5,13
|
7,0614
|
1,505
|
6,6009
|
6,98
|
|
600
|
1,615
|
500
|
10
|
5,13
|
7,0833
|
1,505
|
6,6009
|
7,31
|
|
1440
|
1,62
|
500
|
10
|
5,13
|
7,1053
|
1,505
|
6,6009
|
7,64
|
|
1590
|
1,625
|
500
|
10
|
5,13
|
7,1272
|
1,505
|
6,6009
|
7,97
|
|
1770
|
1,635
|
500
|
10
|
5,13
|
7,1711
|
1,52
|
6,6667
|
7,57
|
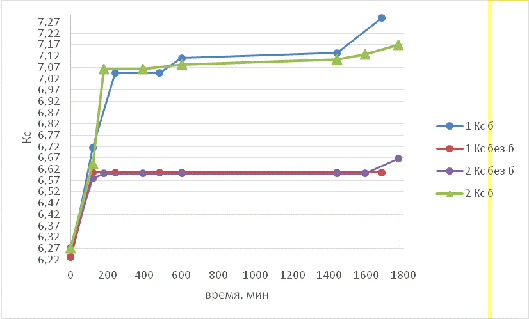
На графике 2.1.1 представлены результаты 2-х
опытов:
График 2.1.1
Система глюкоза-бактерии:
В качестве субстрата нами была использована
глюкоза.
Для приготовления системы брали раствор глюкозы,
концентрацией 1 грамм на 100 миллилитров, и аккуратно всыпали бактерии (в одном
пакетике не менее 50 млн колониеобразующих единиц) в колбу. Один пакетик
препарата на 100 мл раствора.
Опыт проводился в течение 28 часов, результаты
исследования представлены в таблице 2.1.3:
Таблица 2.1.3
|
Время,
мин
|
V(NaOH)б,
мл
|
V(колбы),
мл
|
V
(аликвоты),
мл
|
M
(глюкозы),
г
|
Кс
б, %
|
V(NaOH)
без б, мл
|
∆Кс,
%
|
|
0
|
0
|
500
|
20
|
5,0022
|
0
|
0
|
0
|
0
|
|
120
|
0,23
|
500
|
20
|
5,0022
|
0,5178
|
0
|
0
|
0,5172
|
|
240
|
0,26
|
500
|
20
|
5,0022
|
0,5847
|
0
|
0
|
0,5847
|
|
480
|
0,28
|
500
|
20
|
5,0022
|
0,6297
|
0
|
0
|
0,6297
|
|
600
|
0,29
|
500
|
20
|
5,0022
|
0,6522
|
0
|
0
|
0,6522
|
|
1440
|
0,35
|
500
|
20
|
5,0022
|
0,7871537
|
0
|
0
|
0,7872
|
|
1680
|
0,45
|
500
|
20
|
5,0022
|
2,9237136
|
0
|
0
|
1,01
|
Опыт проводился в течение 29 часов 30 минут,
результаты исследования представлены в таблице 2.1.4:
Таблица 2.1.4
|
Время,
мин
|
V(NaOH)б,
мл
|
V(колбы),
мл
|
V(аликвоты),
мл
|
Кс
б, %
|
V(NaOH)
без б, мл
|
Кс
без б, %
|
∆Кс,
%
|
|
0
|
0
|
500
|
20
|
5,0047
|
0
|
0
|
0
|
0
|
|
120
|
0,15
|
500
|
20
|
5,0047
|
0,3372
|
0
|
0
|
0,3372
|
|
180
|
0,23
|
500
|
20
|
5,0047
|
0,5170
|
0
|
0
|
0,5170
|
|
390
|
0,24
|
500
|
20
|
5,13
|
0,5263
|
0
|
0
|
0,5263
|
|
600
|
0,25
|
500
|
20
|
5,13
|
0,5482
|
0
|
0
|
0,5482
|
|
1440
|
0,27
|
500
|
20
|
5,13
|
0,5921
|
0
|
0
|
0,5921
|
|
1590
|
0,31
|
500
|
20
|
5,0055
|
0,6967
|
0
|
0
|
0,6967
|
|
1770
|
0,42
|
500
|
5,0055
|
0,9440
|
0
|
0
|
0,9440
|
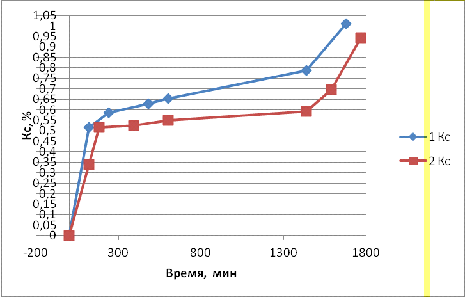
Результаты двух опытов представлены на графике
2.1.2:
График 2.1.2:
Результаты проведенной работы представлены на
графике 2.1.3:
График 2.1.3
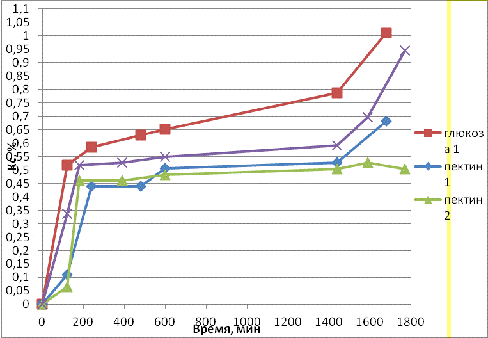
В результате было получено, что бифидобактерии
увеличивают число карбоксильных групп в течении 28 часов до 10,33%.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
Арасимович,
В.В. Методы анализа пектиновых веществ, гемицеллюлоз и пектолитических
ферментов в плодах / В.В. Арасимович, С.В. Балтага, Н.П. Пономарева.- Кишинев:
АН Молд. ССР, 1970.- 84 с.
Бек,
М.М. Химия реакций комплексообразования / М.М. Бек.- М.: Мир, 1973.- 279 с.
Березин,
И.В. Практический курс химической и ферментативной кинетики / И.В. Березин.-
М.: Изд-во МГУ, 1976.- 320 с.
Василенко,
Ю.К. Получение и изучение физико-химических и гепатопротекторных свойств
пектиновых веществ / Ю.К. Василенко, С.В. Москаленко, Н.Ш. Кайшева // Хим.-
фармац. журн.- 1997.- Т.31, № 6.- С. 28-29.
Государственная
фармакопея РФ.- 12-е изд.- М.: Науч. центр экспертизы средств мед. применения,
2007.- Ч. 1.- 704 с.
Зависимость
колориметрической реакции галактуроновой кислоты и нейтральных моносахаридов с
карбазолом от условий её проведения / М.П. Филиппов [и др.] // Изв. АНМолд.
ССР. Серия биолог. и хим. наук.- 1986.- №1.- С. 75.
Исследование
взаимодействия пектиновых веществ с солями меди, ртути, цинка и кадмия / Г.П.
Кацева [и др.] // Химия природ. соединений.- 1988.- № 2.- С. 171-175.
Комиссаренко,
С.Н. Пектины - их свойства и применение / С.Н. Комиссаренко, В.Н. Спиридонов //
Раст. ресурсы.- 1998.- Т. 34, вып. 1.- С. 111-119.
Мелвин-Хьюз,
Е.А. Равновесие и кинетика реакций в растворах / Е.А. Мелвин-Хьюз.- М.: Химия,
1975.- 472 с.
Оводов,
Ю.С. Современные представления о пектиновых веществах / Ю.С. Оводов //
Биоорган. химия.- 2009.- Т.5, № 3.- С. 293-310.
Определение
комплексообразующей способности пектинов и пектинсодержащих препаратов / В.А.
Компанцев [и др.] // Охрана окружающей среды.- 1991.- Вып. 3.- С. 25-27.
Пат.
2206089 Российская Федерация, МПК G01 N31/16. Способ определения массовой доли
функциональных групп полиуронидов / Н.Ш. Кайшева (РФ). - № 2001134132/04;
заявл. 13.12.2001; опубл. 10.06.2003. [Электронный ресурс].- Режим доступа:
http://ru-patent.info/21/80-84/2181551.html.- Загл. с экрана.
Пектин.
Тенденции научных и прикладных исследований / И.Л. Новосельская [и др.] //
Химия природ. соединений.- 2000.- №1.- С. 3-11
Пектин.
ВФС 42-3433.- Введ. 1999.- 08.10.- М., 1999.- 4 с.
Природные
свойства топинамбура // Новые лекарственные препараты.- 2003.- Вып. 12.- С.
6-19.
Рациональное
питание. Рекомендуемые уровни потребления пищевых и биологически активных
веществ: методические рекомендации МР 2.3.1. 19150.- Введ. 2004.- 02.06.- М.:
Медицина, 2004.- 25 с.
Разработка
пищевых продуктов и лечебных препаратов на основе клубней и травы топинамбура /
Н.С. Зяблицева [и др.].- Пятигорск, 2009.- 25 с.- Деп. в ВИНИТИ РАН 27.07.2009,
№ 497- В2009.
Грасси
Н. химия процессов деструкции полимеров. М. Издатинлит, 1959.
В.Г.
Жиряков «Органическая химия». - Москва - 1986 г.