Трансдермальные терапевтические системы
Курсовая
работа
Трансдермальные
терапевтические системы
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
. ТРАНСДЕРМАЛЬНЫЕ
ТЕРАПЕВТИЧЕСКИЕ СИСТЕМЫ КАК НОВЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ
.1 Кожа как проводник
лекарственных веществ
.2 Понятие трансдермальных
терапевтических систем
. КОНСТРУКЦИЯ И ВИДЫ
ТРАНСДЕРМАЛЬНЫХ ТЕРАПЕВТИЧЕСКИХ СИСТЕМ
.1 Конструкция
трансдермальных терапевтических систем
.2 Виды трансдермальных
терапевтических систем
ЗАКЛЮЧЕНИЕ
СПИСОК ИСПОЛЬЗОВАННОЙ
ЛИТЕРАТУРЫ
ПРИЛОЖЕНИЕ
ВВЕДЕНИЕ
Актуальность темы исследования обусловлена технологическим прорывом в
области фармацевтики, где разрабатываются не только лекарственные препараты, но
и способы их введения в организм. Ретроспективный анализ фармации, проведенный
В. Н. Тохмахчи, показал, на первых этапах ее развития, вплоть до XX века,
лекарственной форме придавалось отнюдь не первостепенное значение при поиске
новых препаратов. Главным было лекарственное вещество - действующее начало, от
которого и зависела активность препарата. Но опыт применения показал, что активные
в форме ингаляций, не действуют при пероральном приеме. Другие лекарственные
вещества активные парэнтерально, в значительной мере разрушаются в кислой среде
желудка.
Принципиальные изменения произошли в последней трети XX века, когда А.
Дзаффарони была разработана концепция технологии контролируемого высвобождения
действующего начала из лекарственной формы, наиболее удачными и популярными из
которых оказались трансдермальные терапевтические системы (ТТС), которым и
посвящена эта работа.
Цель данной курсовой работы исследовать особенности конструкции и
действия трансдермальных терапевтических систем.
Для достижения цели необходимо решить следующие задачи:
. рассмотреть кожу как проводник лекарственных средств;
. дать определение понятию «трансдермальные терапевтические системы»;
. изучить конструкцию трансдермальных терапевтических систем;
. представить виды трансдермальных терапевтических систем.
Структурно работа представлена введением, двумя главами, заключением,
списком литературы и приложением.
1. ТРАНСДЕРМАЛЬНЫЕ ТЕРАПЕВТИЧЕСКИЕ СИСТЕМЫ КАК НОВЫЕ
ЛЕКАРСТВЕННЫЕ ФОРМЫ
1.1 Кожа как проводник лекарственных веществ
С древних времен китайским целителям были известны свойства кожи, как
регулятора разнообразных физиологических функций. Кожу называют «центральной
нервной системой», вынесенной на периферию. Это самый большой орган человека,
имеющий множество функций и отвечающий за материальный и энергетический обмен с
окружающей средой [14].
Кожа является очень сложной и до конца не изученной частью человеческого
организма. Она имеет тесную взаимосвязь с внутренними органами, которая
определяется способностью кожи выполнять свои функции. Например, при болезнях
печени кожа желтеет, при заболеваниях сердечно - сосудистой системы кожа
становится сухой и шелушащейся, при болезнях почек, кожа под глазами
истончается.
Кожа является естественным барьером, стоящим на пути действия химических,
физических и микробных факторов внешней среды, участвует в процессах дыхания,
теплорегуляции, синтезе биологически активных веществ, очистке организма от
шлаков. Кожа также обладает способностью впитывать до полутора литров воды во
время приема ванн и купания воду, а так же натуральные вещества.
Кожа защищает тело от неблагоприятного внешнего воздействия. Это
обеспечивается за счет труднопреодолимого барьера, который удерживает
чужеродные молекулы от проникновения в организм. Также кожа является
вместилищем для тканей и органов, регулирует температуру тела и первичную
сенсорную чувствительность. Крайний слой кожи (роговой слой - stratum corneum)
- основной компонент барьера для проникающих веществ. На рис. 1 представлена
гистологическая структура кожи.
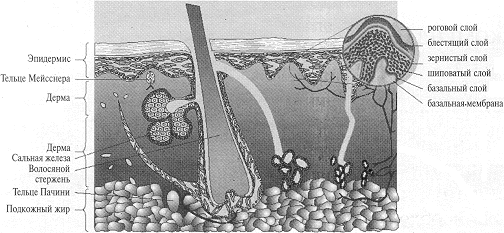
Рисунок 1. Структура кожи.
Огромное количество фармацевтических продуктов наносится на кожу. Такие
препараты называют топическими, или дерматологическими, средствами. Несмотря на
это, молекулы с соответствующими физико-химическими свойствами могут в
небольшом количестве проникать через роговой слой, вызывая системный эффект.
Эти продукты могут быть использованы в трансдермалъных системах доставки
лекарств, или трансдермальных терапевтических системах.
1.2 Понятие трансдермальных терапевтических систем
Трансдермальные терапевтические системы (ТТС) обеспечивают альтернативный
способ назначения препаратов, которые не могут быть введены иначе, или их
традиционный пероральный путь введения менее эффективен из-за их нестабильности
в ЖКТ, узкого терапевтического коридора или короткого периода полувыведения. В
ТТС лекарственная молекула диффундирует из медикамента в поверхность кожи,
затем препарат проходит сквозь роговой слой и достигает эпидермиса, а потом и
дермы, где васкулярная сеть переносит его молекулы к органам [4].
ТТС предназначены для непрерывной атравматической подачи ЛВ в системный
кровоток с заранее заданной скоростью в течение длительного времени. Тем самым
ТТС представляют собой значительно упрощенный аналог инфузионного насоса или,
как мы его называем, «сухую капельницу». От последней они отличаются
значительно более длительным действием при однократном применении,
атравматичностью, отсутствием необходимости иммобилизации больного и наличия
медицинского персонала при их применении. Однако подача адекватных объемов
жидкости с помощью ТТС невозможна, поэтому ТТС - «сухая капельница», подающая
ЛВ без заметного количества жидкости.
Применение ТТС для лечения хронических больных позволяет значительно
повысить качество жизни, а в ряде случаев является наиболее эффективным методом
терапии (например, в случае сердечнососудистых заболеваний, таких как
стенокардия или гипертония, или облегчение менопаузального синдрома) [2].
Основной частью многих ТТС является полимерная матрица, содержащая ЛВ и
определяющая скорость и характер его высвобождения на кожу.
Трансдермальные терапевтические системы представляют собой альтернативный
способ назначения тех лекарств, которые не могут быть введены иначе, или их
традиционный пероральный путь назначения является менее эффективным. Кожа
обладает превосходным барьерным свойством, что ограничивает типы молекул, которые
могут быть через нее введены.
Тем не менее, для лекарств, обладающих этими свойствами, способ
трансдермальной доставки препарата обеспечивает непрерывное дозирование на
протяжении продолжительного периода времени.
Физические и химические свойства трансдермалъных систем доставки
позволяют назначать лекарства с большими размерами молекул, такие как протеины
и другие биотехнологические продукты, которые на сегодняшний день могут
вводиться в организм только с помощью болезненных и неудобных инъекций.
Трансдермальная доставка лекарств имеет несколько преимуществ.
• В сравнении с пероральным назначением возможность обеспечить более
быстрое действие лекарств.
• Возможность избежать проблем, связанных с пероральным приемом:
инактивация или снижение активности лекарства в результате первого пассажа и
желудочного метаболизма, а также связанные с этим неблагоприятные реакции.
• Возможность немедленного прекращения лечения при развитии
неблагоприятных реакций.
• Обеспечение постоянной концентрации препарата в крови, без колебаний
концентрации и связанных с этим неблагоприятных реакций.
• Снижение частоты назначения за счет доставки необходимой дозы препарата
в более продолжительный период времени.
• Улучшение комплаентности пациентов (легкий способ применения препарата).
• Уменьшение необходимой дозы препарата, так как снижаются потери
препарата, связанные с метаболизмом [2].
Трансдермальная доставка лекарств имеет несколько ограничений.
• Возможно раздражение или контактная сенсибилизация кожи, причиной
которых является неблагоприятное взаимодействие активных или неактивных
компонентов системы с кожей.
• Необходимо больше времени для начала действия лекарств по сравнению с
инъекционными формами.
• Только небольшой процент лекарства может проникнуть в кожу из пластыря.
Это означает, что лишнее количество лекарства должно быть изготовлено и введено
в систему, что приводит к увеличению стоимости системы.
• Трансдермальная система доставки препаратов может быть использована
только для достаточно сильнодействующих лекарств, требующих небольших доз, и
для веществ, обладающих определенными физико-химическими свойствами, для
проникновения в кожу в терапевтически эффективном количестве [7]. Несколько
факторов определяют, какое из лекарственных средств пригодно для ТТС. Допуская,
что лекарство является достаточно мощным и отвечает требованиям дозирования,
исследователи изучают его физико-химические свойства для определения
возможности проникновения лекарства через кожу в терапевтически эффективном
количестве, медицинскую необходимость, возможность технологического
осуществления и практического применения.
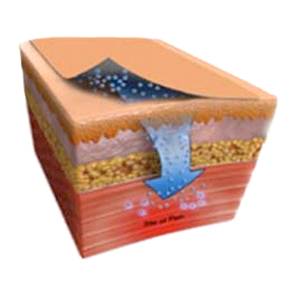
Рисунок 2. Способность лекарственного вещества к проникновению через
несколько слоев кожи
Физико-химические свойства лекарства стоят на первом месте, т.к. молекула
препарата должна пройти через несколько слоев кожи, каждый из которых имеет
свои отличительные особенности. Для эффективной трансдермальной доставки
требуется молекула лекарства, которая обладает сродством и к гидрофобному роговому
слою, и к гидрофильной дерме.
Молекула лекарства должна быть нейтральной, так как позитивный или
негативный заряд молекулы может затормозить ее продвижение через гидрофобную
среду. К тому же она должна обладать достаточной растворимостью в гидрофобной и
гидрофильной среде. Наконец, лекарственная молекула должна быть небольшой
(молекулярный вес не должен превышать 500 Дальтон), для того чтобы обеспечить
необходимую скорость ее продвижения [3].
Доставка лекарств через кожу подчинена существенным взаимосвязям, которые
ограничивают общее применение этой технологии. Сегодня исследуется много
подходов, чтобы преодолеть барьерные свойства кожи и улучшить возможности
применения ТТС. Чтобы достичь нового уровня, необходимо разработать технологии,
посредством которых проницаемость лекарственного средства могла бы стать
обратимой, предсказуемой и контролируемой. Усилия по усовершенствованию
технологий делятся на три категории: химические, биохимические и физические.
Химическое усовершенствование трансдермальных систем доставки
лекарственного средства ведет к использованию внешних химических субстанций,
для того чтобы помочь лекарствам проникнуть через кожный барьер, путем
разрушения упорядоченной структуры межклеточного жирового слоя stratum corneum.
Эта модификация ведет к улучшению текучести этого слоя и растворимости
лекарства в роговом слое. Многочисленные химические соединения использовались
или оценивались по их способности расширить проникновение молекул
лекарственного средства сквозь кожу. Они расположены следующим образом: от
многоатомных спиртов до жирных кислот и сложных эфиров жирных кислот к
терпенам. Несмотря на перспективы химических веществ, усиливающих проникновение
молекул лекарств через кожу, лишь немногие из них использовались в коммерческих
трансдермальных системах доставки, главным образом из-за затрат, связанных с
регулирующими регистрационными требованиями (доказательство увеличения
проникающей способности; исследования их краткосрочной и долгосрочной
безопасности и токсичности) [15].
Фармкомпании достигают все большего понимания механизмов действия
химических "веществ-усилителей" и их продолжительных и
кратковременных эффектов, эти средства будут шире использоваться, потому что
они позволяют обеспечить наилегчайший путь усовершенствования ТТС.
Усовершенствование биохимических составляющих ТТС.
При биохимическом усовершенствовании молекула лекарственного средства
подвергается кратковременному физико-химическому изменению, которое облегчает
ее движение через роговой слой. Измененная молекула лекарственного средства
(про-лекарство) терапевтически неактивна. После проникновения в роговой слой
она подвергается гидролитической или ферментативной биотрансформации, чтобы
восстановить исходное терапевтически активное лекарственное вещество.
Возможность применения этого подхода была доказана с различными лекарствами.
Однако эта область разработок все еще находится на ранней стадии развития, и
пока не существует коммерческого использования таких трансдермальных систем
доставки лекарственного средства, но этот подход скоро будет разработан.
Разработчик нового пролекарства должен будет собрать всю информацию, связанную
с безопасностью, токсичностью и эффективностью, необходимыми для регистрации
препарата. Стоимость и время, необходимые для этого, значительны [9].
Еще один вариант - использование везикул жира, сохраняющих лекарственные
средства (подобно липосомам), которые могут проникать сквозь кожу и
самостоятельно депонироваться в роговом слое. Там они могут действовать как
системы с контролируемым высвобождением. Исследовательские усилия по расширению
эффективности жировых везикул все еще находятся на ранних стадиях изучения.
Однако многие парентеральные системы, использующие жировые везикулы, уже много
лет применяются на практике. Такие везикулы были хорошо изучены, и значительная
информация относительно их безопасности, токсичности и способности к
биологическому распаду уже доступна. Если молекула лекарственного средства была
просто инкапсулирована, без изменения физических или химических свойств, то при
регистрации таких трансдермальных форм потребуется меньше формальностей.
Следовательно, этот подход расширения применения является многообещающим.
При физическом усовершенствовании трансдермальных систем доставки
лекарственных средств внешние стимулы или сила, используемая для проведения
лекарственного средства через кожу, особенно через самый наружный слой. Внешние
силы производят обратимые физические изменения в пределах рогового слоя.
Используются три подхода: ионофорез, сонофорез и электрофорез. Эти подходы могут
позволять трансдермальным системам доставлять большие ионные молекулы пептидов
или белков, которые не могут быть доставлены пассивной диффузией сквозь кожу. К
тому же уровень доставки хорошо контролируется величиной и продолжительностью
внешних стимулов. Наконец, как и в случае с парентеральными препаратами, начало
действия лекарства очень быстрое из-за относительно короткого времени,
необходимого для того, чтобы лекарство попало в кровь. Быстрое начало действия
очень важно для терапии раковых болей, диабета и других состояний [5].
Ионофорез - использование внешнего электрического тока для того, чтобы
транспортировать заряженную молекулу сквозь кожу. В этом процессе, который уже
известен более ста лет, ионная молекула несет заряд через мембрану кожного барьера,
чтобы замкнуть цепь. В настоящее время проводится много исследований, изучающих
использование этой методики для доставки больших молекул лекарственных средств
или наркотиков, для купирования раковой боли.
Сонофорез использует ультразвуковые волны для того, чтобы разорвать
роговой слой и вызвать раскрытие пор, что облегчает транспорт лекарственных
молекул. Хотя возможность такого подхода была доказана, системы доставки
лекарственного средства, использующие сонофорез, все еще находятся на ранней
стадии развития, а коммерческое использование не ожидается в ближайшем будущем.
Электрофорез использует высоковольтный милли-секундный импульс для создания
транзитных путей сквозь роговой слой, чтобы облегчить проникновение больших
молекул лекарственного средства. Возможность применения этого подхода была
доказана. Однако методы доставки лекарственного средства, использующие эту
технологию, все еще находятся на ранней стадии развития, а огромное количество
проблем с безопасностью еще не разрешены, т.к. электрофорез использует
высоковольтный внешний импульс, который может вызывать длительное повреждение
кожи [8].
Эти технологии достаточно хорошо изучены, но ни один из методов
трансдермальных систем доставки не стал настолько популярным и крупным
достижением, чтобы заменить другие пути введения лекарств. Однако всего лишь 20
лет назад не было никакой возможности доставлять лекарства через кожу для
системного действия. Может быть, в последующие годы некоторые многообещающие
достижения в технологиях позволят усовершенствовать этот путь доставки.
2. КОНСТРУКЦИЯ И ВИДЫ ТРАНСДЕРМАЛЬНЫХ ТЕРАПЕВТИЧЕСКИХ СИСТЕМ
2.1 Конструкция трансдермальных терапевтических систем
Самая простая форма ТТС состоит из следующих компонентов:
• Основная мембрана, предотвращающая высвобождение лекарства в окружающую
среду и попадание влаги из вне.
• Лекарственный резервуар для растворения, хранения и высвобождения
препарата.
• Мембрана, обеспечивающая оптимальную скорость высвобождения лекарства.
• Клей, склеивающийся при надавливании, используемый для удержания
системы в адекватном контакте с кожей.
• Защитная пленка для хранения системы.
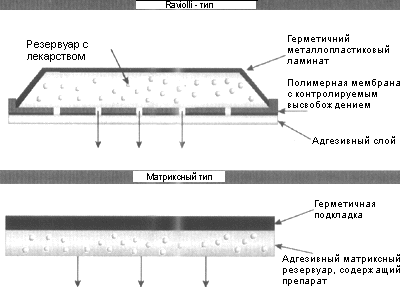
В ранних моделях ТТС каждая функция обеспечивалась отдельно одним из
компонентов (рис. 3). Эти системы, известные как "равиолли" (raviolli
systems), изготавливаются путем введения раствора или геля с лекарством в
пространство между основной мембраной и резервуаром с лекарством, затем
термоспособом их сваривают с мембраной, контролирующей уровень высвобождения
лекарства, по периметру покрывают клеем, склеивающимся при надавливании, и
защитной пленкой. Процесс изготовления неудобен, а сам пластырь довольно
громоздкий.
В новых ТТС, так называемых матриксных системах (matrix systems), клей,
склеивающий при надавливании, выполняет различные функции: прилипание,
хранение, высвобождение лекарства и контроль за уровнем высвобождения препарата
(см. рис. 3). Процесс изготовления матриксной системы сравнительно прост, а
пластырь очень тонкий. Однако иногда сложно найти клей, который на протяжении
времени действия ТТС может растворить лекарство и высвободить его без
кристаллизации или фазы сепарации. Более того, растворение и высвобождение
препарата могут снизить силу склеивания и сцепления с кожей.
Согласно характеристике данной в зарубежных фармакопеях, ТТС, как
правило, состоят из следующих основных компонентов [8]:
. Полимерный матрикс/Резервуар активных веществ. Полимеры являются
основой пэтча, именно они контролируют процесс высвобождения активных
ингредиентов. В настоящий момент используются натуральные полимеры (производные
целлюлозы, хитозан и т.д.) и синтетические полимеры (полиакрилат, полипропилен
и т.д.)
Активные вещества - в зависимости от поставленной задачи могут быть разнообразными.
Так в антицеллюлитных системах используется L-карнитин и кофеин, для достижения
противоотечного эффекта экстракты водорослей и растений, для повышения
упругости кожи и омолаживающих эффектов эластин, аминокислотные и пептидные
комплексы.
. Энхансеры - повышают проходимость рогового слоя, взаимодействуя со
структурными компонентами эпидермиса (протеинами, липидами) 4. Адгезивный слой
- обеспечивает тесный контакт между трансдермальной системой и поверхностью
кожи. Он должен хорошо прилипать и держаться, но при этом легко сниматься, не
причиняя травмы коже. Для этой цели широко используют полиакрилаты и силикон.
. Ламинат - должен обладать высокой гибкостью, пропускать кислород и не
мешать испарению влаги. Из материалов предпочтительны винил, полиэтилен и
полиэстер.
. Защитный слой - удаляется непосредственно перед нанесением
трансдермального пэтча на кожу.

Рис. 4. Схема строения трансдермальных транспортных систем ТТС делят на
две группы: матричные и мембранные [12].
Мембранные ТТС состоят из непроницаемой подложки, резервуара с
лекарственным веществом, мембраны, регулирующей высвобождение лекарственного
средства и адгезивного (клейкого) слоя. Лекарственное вещество находится в
резервуаре в виде суспензии в жидкости или геле. Резервуар располагается между
непроницаемой подложкой и мембраной из пористой полимерной фольги, которая
определяет скорость высвобождения лекарственного вещества. В системах этого
типа резервуар лекарственного вещества заключен в плоскую камеру, произведенную
из непроницаемой для вещества подложки и полимерной мембраны, ограничивающей
скорость высвобождения. Молекулы вещества могут проникать только через эту
полимерную мембрану, которая может быть микропористой или сплошной. На внешней
поверхности мембраны может быть нанесен тонкий слой гипоаллергенного
адгезивного полимера, совместимого с лекарственным веществом (например,
силиконовый или полиакриловый клей), для обеспечения плотного контакта системы
с кожей. Скорость высвобождения лекарственного вещества из подобной системы
может быть подстроена путем изменения состава полимера, коэффициента
проницаемости и толщины ограничивающей скорость высвобождения мембраны и
адгезива (рис. 5). Примерами трансдермальных терапевтических систем служат нитроглицерин
содержащие трансдермальные терапевтические системы, такие как Transderm-Nitro
(Ciba), скополамин содержащие трансдермальные терапевтические системы, такие
как Transderm-Scop (Ciba), клонидинсодержащие трансдермальные терапевтические
системы, такие как Catapres (Boehringer Ingelheim) [13].
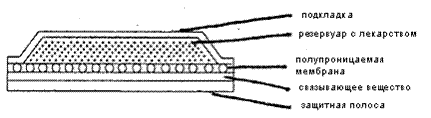
Рис. 5. ТТС, ограниченная мембраной
В матричных ТТС лекарственное вещество помещается в матрицу, состоящую из
геля или полимерной пленки. Высвобождение лекарственного вещества из такой
системы определяется его диффузией из материала матрицы. Адгезивные системы,
контролируемые диффузией.
В этом случае резервуар лекарственного вещества формируется путем прямого
диспергирования лекарственного вещества в адгезивном полимере и его последующего
распределения путем отливки по плоскому листу непроницаемой для лекарственного
вещества подложки. Для производства адгезивной системы высвобождения
лекарственного вещества, контролируемой диффузией, на поверхность подложки
наносятся слои не содержащего лекарственного вещества, ограничивающего скорость
высвобождения адгезивного полимера постоянной толщины. Примерами
трансдермальных терапевтических систем такого типа служат
нитроглицеринсодержащие трансдермальные терапевтические системы, такие как
Deponit (Pharma-Shwartz) и содержащие изосорбида динитрат трансдермальные
терапевтические системы, такие как лента Frandol (Toaeiyo). ТТС Deponit,
матричная система, выполненная в виде полимерной пленки из полиизобутилена и
смолистого вещества, которая нанесена на фольгу-подложку. Матрица состоит из
7-ми слоев. Каждый слой содержит различную концентрацию нитроглицерина,
адсорбированного на лактозе, что позволяет поддерживать активную концентрацию в
крови длительное время.
Системы дисперсионного типа с наполнителем. В системах такого типа
резервуар лекарственного вещества формируется путем приготовления гомогенной
взвеси лекарственных веществ в гидрофильном или липофильном полимерном
наполнителе. После этого полимер, содержащий лекарственное вещество, выплавляют
в форме диска с определенной площадью поверхности и толщиной, который затем
наклеивается на закупоривающую пластину в камере, сделанной из непроницаемого
для лекарственного вещества материала. Адгезивный полимер распределяется по
окружности, образуя клейкую полосу на диске с медикаментом. Примерами таких
трансдермальных терапевтических систем служат нитроглицеринсодержащие
трансдермальные терапевтические системы, такие как Nitro-Dur (Key
Pharmaceuticals. (рис. 6)
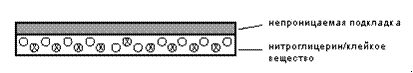
Рис. 6. ТТС Nitro-Dur
В системе Nitro-Dur нитроглицерин адсорбирован на лактозе и диспергировн
в гидрогеле, состоящем из воды, глицерина, ПВС и ПВП.
Микрорезервуарные системы. В системах такого типа резервуар
лекарственного вещества формируется путем приготовления суспензии частиц
лекарственного вещества в растворе водорастворимого полимера, а затем
приготовления гомогенной взвеси в липофильном полимере с использованием высокой
силы механического перемешивания, в результате чего формируется большое количество
не подверженных выщелачиванию микроскопических сферических резервуаров
лекарственного вещества. Термодинамически нестабильная взвесь быстро
стабилизируется путем немедленного сшивания полимера на месте, в результате
чего формируется полимерный диск с лекарственным веществом, который имеет
постоянную площадь поверхности и фиксированную толщину. В полученной
трансдермальной терапевтической системе диск с медикаментом находится в центре
и окружен клейкой полосой. Примерами таких трансдермальных терапевтических
систем служат нитроглицеринсодержащие трансдермальные терапевтические системы,
такие как Nitrodisc (Searle). ТТС Nitrodisc характеризуется большим количеством
микровключений из смеси нитроглицерина и лактозы в водном растворе ПЭГ-400.
Размер включений составляет от 10 до 200 мкм. Они запрессованы в матрицу из
полимерного кремнийорганического соединения.
В середине 90-х годов были разработаны ТТС принципиально нового типа
действия. Так, ТТС американской фирмы Drug Delivery Systems, названной
“Powerpatch”. Система представляет собой пластырь, площадью 70 см2, содержит
два, изолированных друг от друга резервуара для действующего вещества. Один из
резервуаров присоединен к катоду, а другой - к аноду. При нанесении системы на
кожу под действием электрического тока происходит высвобождение лекарственного
вещества. В этом случае повышается биодоступность лекарственной формы, так как
электроток повышает проницаемость ороговевшего слоя кожи [2].
Специалистами фирмы Thera Tech (США) и Ciba Corporation разработана система
трансдермальной доставки лекарственных веществ, не обладающих способностью
проникать через кожу. Эта система представляет собой многокамерную конструкцию,
в которой резервуар с лекарственным веществом отделен от активатора
перегородкой, не проницаемой для обоих компонентов. Система активизируется
непосредственно потребителем посредством нажатия на эту перегородку, которая
разрушается. В результате этого лекарственное вещество смешивается с
активатором, превращаясь в активную форму, способную проникать через кожу [2].
В отечественной фармакопее отсутствуют как общая, так и частные статьи на
ТТС, что весьма затрудняет исследования в этом актуальном для фармации и
медицины направлении. ТТС перспективны в онкологии, а также для лечения астмы,
при контрацепции, для гормонозависимой терапии, для местной и даже общей
анестезии. Отечественные трансдермальные системы представлены на
фармацевтическом рынке России такими фирмами как «Биотехнология», «Алтай
федеральный центр НПЦ», НПЦ «Лекбиотех» и то всего с одним наименованием
каждая. Зарубежные трансдермальные терапевтические системы, в свою очередь,
представлены такими фирмами как «Schwarz Pharma», «Janssen Pharmaceutica N.V.»,
«Schering», «Rhone-Poulenc Rorer», «SmithKline Beecham Consumer Healthcare»,
«Ciba-Geigy», «Searle», «Schering-Plough», «Rugby», «Novartis Pharma Services»,
«Grunenthal» и др. с достаточно широким ассортиментом трансдермальных
пластырей, приносящих им огромный коммерческий успех [13].
ТТС являются популярными во всем мире. В табл. 1 перечислены
трасндермальные препараты, зарегистрированные в России, а в табл. 2 и 3
-зарегистрированные в других странах или находящиеся на разных стадиях
разработки.
2.2 Виды трансдермальных терапевтических систем
На сегодняшний день достаточно широко используются несколько видов
пластырей, относящихся к трансдермальным системам лечения.
Пластыри для контрацепции. Наклеивается раз в неделю и, благодаря
постоянной поставке необходимых гормонов, поддерживающий их концентрацию в
крови, уберегают от ситуаций, когда женщина «забыла принять очередную
таблетку».
Пластыри для заместительной гормональной терапии у женщин. Используется
для лечения симптомов тяжело протекающей менопаузы. Удобен в применении т.к.
меняется раз в неделю.
Пластырь для лечения сердечнососудистых заболеваний с нитроглицерином.
Нитроглицерин очень быстро выводится их организма и поэтому требует частого
приема. Пластырь же позволяет поддерживать его нужную концентрацию в крови в
течение суток.
Никотиновые пластыри, помогающие отвыкнуть от курения. Они построены на
принципе замещения никотина, зависимость от которого и побуждает курильщика
браться за сигарету. Жевательные резинки и таблетки с никотином опять же
обеспечивают неравномерную доставку никотина в организм, а пластырь в течение
24 часов поддерживает его постоянный уровень и дает человеку забыть о желании
закурить. При этом человек не получает продукты сгорания табака в свои
дыхательные пути.
Косметологические пластыри «от целлюлита», «от морщин» «для тонуса кожи»
и т.д. Содержащие те же активные вещества, что и косметические кремы, а именно,
гиалуроновую кислоту, кофеин, коэнзимы, про-ретинол, экстракты самых разных
растений и т.д., причем процент проникновения в кожу этих веществ выше, чем при
использовании перечисленных выше форм. Анальгетики. Пластыри с
сильнодействующим опиоидным веществом фентанилом весьма удобны в применении к
онкобольным. Один пластырь на три дня позволяет избежать нескольких болезненных
инъекций подобного препарата.
Сегодня выводятся на рынок также пластыри для защиты от укусов насекомых,
пластыри с хондроитином против воспалений в суставах, а в разработке находится
целый перечень трансдермальных пластырей, предназначенных для терапии самых
разных заболеваний. Это и интерфероновые пластыри для лечения вирусных инфекций,
и пластыри с диклофенаком для избавления от ревматических болей, и
ксаномелиновые пластыри для лечения болезни Альцгеймера и прочие
траснсдермальные системы, применяемые в онкологии, неврологии, кардиологии,
психиатрии, дерматологии, урологии, андрологии, гинекологии, эндокринологии и
других сферах медицины.
Рассмотрим их более подробно.
Терапия стенокардии и гипертонии обычно длится в течение многих лет. При
лечении этих заболеваний очень важна комплаентность пациентов, поэтому
трансдермальные формы лекарств столь необходимы. Нитроглицерин используется уже
более века, но его короткий период полувыведения требует частого назначения.
Трансдермальное назначение позволяет поддерживать необходимую системную
концентрацию в крови в течение 12-14 ч.
Другим сердечнососудистым препаратом в форме ТТС является клонидин
(клофелин), который используется для терапии мягкой/умеренной гипертонии.
Оральное назначение клонидина требует 2-3-разового приема, а его
трансдермальная форма позволяет назначать один пластырь на 7 дней. Также ТТС
позволяет поддерживать равномерную дозировку в плазме крови в течение 7 дней, в
то время как при оральном приеме концентрация меняется "пилообразно".
В России клонидин в форме ТТС пока не применяется.
Заместительная гормональная терапия. Для заместительной гормональной
терапии используются два лекарственных препарата - эстрадиол и тестостерон.
Эстрадиол используется для терапии симптомов, связанных с менопаузой. При
оральном назначении эстрадиола большая его часть превращается в печени в малоактивный
метаболит - эстрон. Трансдермальная доставка эстрадиола поддерживает
желательный физиологический уровень баланса эстрадиола/эстрона. К тому же при
использовании этой формы препарата концентрация его в крови составляет 1/6
часть от введенной дозы, в отличие от 1/20 концентрации при оральном приеме.
ТТС с эстрадиолом может высвобождать эстрадиол до 7 дней.
Другой препарат - тестостерон - используется в заместительной
гормональной терапии мужского гипогонадизма.В России ТТС для заместительной
гормональной терапии пока не применяются.
Заместительная терапия никотиновой зависимости. Эффективная помощь при
прекращении курения - замещение никотина - требует использования медицинских
препаратов, содержащих никотин. Жевательные резинки с никотином существуют уже
более 20 лет. Однако жевательные резинки обеспечивают неравномерную доставку
никотина и ассоциируются с окрашиванием зубов, неприятным вкусом, зубной болью,
стоматологическими проблемами и желудочно-кишечными расстройствами.
Трансдермальная доставка никотина обходит эти потенциальные проблемы и
обеспечивает легкость применения. К тому же одна аппликация поддерживает
постоянный уровень никотина в крови в течение 24 ч.
Анальгетики. Трансдермальная доставка анальгетиков для терапии
хронической боли является важной альтернативой для перорального и внутривенного
назначения. Например, длительное 3-дневное действие трансдермальной формы
фентанила. Эта форма обеспечивает купирование хронической боли у онкологических
пациентов, а также позволяет избежать затрат на 3-4-разовое введение инъекций
морфина, на вызов медицинской сестры, бригады скорой помощи, назначения
противорвотных средств, на расходные материалы, а также другие материальные и
нематериальные затраты родственников, и ликвидации некоторых неблагоприятных
реакций морфина.
Несмотря на достаточно большую популярность ТТС во всем мире (всего
зарегистрировано несколько десятков ТТС с различными лекарственными
веществами), в России их ассортимент более чем скромен. Отечественные ТТС
представлены на фармацевтическом рынке России такими фирмами как
«Биотехнология», «Алтай федеральный центр НПЦ», НПЦ «Лекбиотех» и то всего с
одним наименованием каждая. Зарубежные ТТС, в свою очередь, представлены такими
фирмами как «Schwarz Pharma», «Janssen Pharmaceutica N.V.», «Schering»,
«Rhone-Poulenc Rorer», «SmithKline Beecham Consumer Healthcare», «Ciba-Geigy»,
«Searle», «Schering-Plough», «Rugby», «Novartis Pharma Services», «Grunenthal»
и др. с достаточно широким ассортиментом трансдермальных пластырей, приносящих
им огромный коммерческий успех. Поэтому на сегодняшний день актуален вопрос по
разработкам и производству новых отечественных трансдермальных терапевтических
систем.
В ТТС практически всегда применяют хорошо зарекомендовавшие себя
дженерики. Однако трансдермальная подача может менять фармакологическое
действие ЛВ, смягчая его, а иногда изменяя основной эффект.
ЗАКЛЮЧЕНИЕ
Трансдермальная терапевтическая система (ТТС) - дозированная мягкая
лекарственная форма для наружного применения в форме пластырей или плёнок,
замедленно высвобождающая лекарственное средство. Трансдермальная форма удобна
тем, что пластырь (или плёнка для трансбуккального применения) наклеивается на
кожу, и лекарство через верхние слои кожи (дерма) быстро проникает в кровь
(кровеносные сосуды).
Преимущества ТТС: удобство применения, лекарство быстро попадает в кровь,
возможность регулировать скорость высвобождения лекарства, возможность
использовать гидрофильные и липофильные вещества.
Это сравнительно новая лекарственная форма, из самых известных примеров -
ТТС с нитроглицерином (Тринитролонг) и ТТС с женскими гормонами (Евра).
Для некоторых лекарств трансдермальная доставка является единственным
способом введения. Для некоторых - альтернативой парентеральному и пероральному
введению. Причем альтернативой весьма привлекательной. Хотя бы потому, что в
сравнении с пероральным приемом трансдермальное введение обеспечивает более
быстрое действие препарата и помогает избежать проблем, связанных со снижением
его активности в результате первого пассажа и желудочного метаболизма. Мало
того, при таком введении появляется возможность снизить частоту назначения
лекарства, уменьшить необходимые дозы и при этом избежать колебаний его
концентрации в крови, а при развитии нежелательных реакций - немедленно прекратить
лечение. К тому же трансдермальное введение намного удобнее для пациентов.
Особенно страдающих хроническими заболеваниями, требующими постоянного
медикаментозного лечения. В то же время трансдермальная доставка имеет ряд
ограничений. Во-первых, трансдермальные формы лекарств могут вызвать
раздражение кожи по причине аллергической реакции на действующие вещества или
неактивные компоненты системы. Во-вторых, для начала их действия требуется
больше времени по сравнению с инъекционными формами. В-третьих, таким способом
можно доставлять лишь сильнодействующие лекарственные вещества, обладающие
вполне определенными физико-химическими свойствами. Прежде всего, молекула
лекарства должна быть нейтральной, поскольку заряд - как отрицательный, так и
положительный - может воспрепятствовать ее продвижению по гидрофобному роговому
слою. Кроме того, лекарство должно обладать достаточной растворимостью в
гидрофобном роговом слое и гидрофильной дерме. И, наконец, лекарственная
молекула должна быть относительно небольшой - ее молекулярная масса не должна
превышать 500 Д. Однако, несмотря на все эти ограничения, использование
трансдермальных систем считается чрезвычайно перспективным: по оценкам
специалистов, анализирующих фармацевтический рынок, мировые продажи трансдермальных
лекарств будут расти как по причине разработки новых лекарств, так и по причине
увеличения количества самих трансдермальных систем доставки.
Несмотря на тесную физико-химическую взаимозависимость, трасндермальная
доставка лекарственного средства имеет большие перспективы как альтернатива
перорального и внутривенного назначения. Возможность управляемо ввести
определенное количество лекарственного средства в течение продолжительного
периода времени сделает привлекательными ТТС для пациентов, страдающих от
хронических состояний, особенно для терапии хронических болей у инкурабельных
онкологических больных, а также для лечения астмы. Кроме того, эти системы
могут использоваться для гормонозаместительной терапии и контрацепции. В силу
того, что трасндермальная доставка является простой в назначении, этот подход
будет особенно привлекательным для пожилых пациентов, где комплаентность
является одной из важных проблем.
В области гормонзаместительной терапии и контрацепции разработчики
лекарственных средств пытаются использовать новые трансдермальные системы
доставки для введения нескольких гормонов одновременно, следовательно, уменьшая
неблагоприятные реакции, появляющиеся при введении только эстрогена.
Комбинированные пластыри, которые доставляют эстроген и прогестерон
одновременно, находятся на заключительных стадиях разработки.
Усовершенствование технологий даст возможность увеличить разнообразие
препаратов, которые могут быть доставлены трансдермально, особенно для больших
и ионизированных молекул биотехнологических лекарственных средств, которые в
настоящее время могут быть введены только через болезненные инъекционные
процедуры. Кроме того, трансдермальная форма доставки лекарств дает
фармацевтическим компаниям конкурентные преимущества на пути разработки
лекарственных веществ: по затратам и наименьшему времени, необходимым для
разработки, в патентной защите, защите от демпингующих генериковых компаний. По
оценкам специалистов по анализу фармацевтического рынка, мировые объемы продаж
трандермальных систем доставки лекарств будут расти. Это будет связано как с
разработкой новых лекарств, так и с увеличением количества трансдермальных
систем доставки.
трансдермальный
терапевтический лекарственный кожа
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Басок
Ю. Б., Саломатина Л. А., Алексеева О. С., Зайцева М. А., Севастьянов В. И.
Исследование фармакокинетики ацетилсалициловой кислоты, хлорпропамида и ацизола
при аппликации трансдермальных терапевтических систем. Материалы 3-ей
международной научной конференции «Экспериментальная и клиническая
фармакология», республика Беларусь, г. Минск, 23-24 июня 2009, С. 18-20.
. Бесова
Н.С., Горбунова В.А., Салтанов А.И. Результаты клинического испытания препарата
Дюрогезик при лечении болевого синдрома опухолевого происхождения у пациентов,
получавших ранее сильные опиоиды. - Новые лекарственные средства,2000, №2,
с.3-11
3. Брюзгин В.В.
Инновационные технологии в лечении хронического болевого синдрома у
онкологических больных: трансдермальные терапевтические системы [Электронный
ресурс] <http://www.rmj.ru/articles_5679.htm> (дата обращения 09.09.2014)
. Брюзгин В.В., Новые
технологии в лечении хронической боли. - Материалы IV съезда онкологов и
радиологов, Баку, 2006
. Бухникашвили, К.О.
Трансдермальные лекарственные формы (обзор) / К.О. Бухникашвили, Т.Д. Даргаева,
Д.Т. Берашвили // Хим. - фармац. журнал. - 1992. - Т 26, № 9 - 10. - С. 46 -
51.
. Васильев, А.Е.
Трансдермальные терапевтические системы доставки лекарственных веществ (обзор)
/ А.Е. Васильев, И.И. Краснюк, С. Равикумар // Хим. - фармац. журнал. - 2001. -
Т 35,№ 11. - С. 29 - 42.
. Исакова М.Е.,
Трансдермальный фентанил (Дюрогезик): длительная терапия хронического болевого
синдрома у онкологических больных, РМЖ, т.14, №14, 2006, стр.1057-1060
. Кругликова-Львова
Р.П., Авакумов В.М. // Новые лекарственные препараты. 1982. №6. С. 9-16.
. Львова Л.В.
Трансдермальные терапевтические системы [Электронный ресурс]
http://www.provisor.com.ua/archive/2004/N17/art_26.php(дата обращения
09.09.2014)
. Морозов Ю.А.
Конструирование и биофармацевтические исследования трансдермального пластыря
гиполипидемического действия с дипромонием // Фундаментальные исследования. -
2006. - № 10 - стр. 88-90
. Осипова Н.А. Новиков
Г.А. Прохоров Б.М. Анальгетики центрального действия. Москва, Издательство «Медицина»,
1998
. Практическое
применение трансдермальной терпевтической системы фентанила для лечения
хронической боли у онкологических больных. Учебное пособие. Москва, 2002
. Строение
трансдермальных терапевтических [Электронный ресурс] системhttp://www.medsuccess.ru/onfs-116-2.html(дата
обращения 09.09.2014)
. Тер-Вартаньян С. Х.
Применение локальной терапии в лечении больных с плечелопаточным периартритом
[Электронный ресурс] www.mif-ua.com(дата обращения 09.09.2014)
. Тихомиров А. Л.,
Дубинин Д. М. Местные гормональные препараты в лечении доброкачественных
заболеваний молочной железы, сопровождающихся масталгией [Электронный ресурс]
www.med. ru(дата обращения 09.09.2014)
. Трансдермальные
пластыри [Электронный ресурс] http://www.zdorovieinfo.ru/ya-mama/beremennost/stati/planirovanie_semi/Transdermalnye_plastyri/(дата
обращения 09.09.2014)
. Трансдермальные
терапевтические системы // Качественная клиническая практика.- 2001.- № 1.
. Щеткина Н. И.,
Талалаева Г. В. Адаптогенный эффект трансдермальных ванн с кристаллами «Легран»
и применение их в бальнеологии www.sgen.ru(дата обращения 09.09.2014)
ПРИЛОЖЕНИЕ
Таблица 1.Трасндермальные терапевтические системы, зарегистрированные в
России (Реестр лекарственных средств, 2001)
|
Активный ингредиент
|
Фирма
|
Название
|
Растворитель
|
Тип
|
|
Никотин
|
Novartis Consumer Health
|
Никотинелл
|
24 ч.
|
Нет
|
Матрикс
|
|
Нитроглицерин
|
Schering-Plough
|
Нитро-дур
|
12- 14 ч.
|
Нет
|
Матрикс
|
|
Нитроглицерин
|
Schwarz Pharma
|
Депонит
|
12-14 ч.
|
Нет
|
Матрикс
|
|
Фентанил
|
Janssen Cilag
|
Дюрогезик
|
3 дня
|
Этанол
|
Raviolli
|
Таблица 2. Трасндермальные терапевтические системы, зарегистрированные в
других странах
|
Активный ингредиент
|
Фирма
|
Название
|
Продолж. назначения
|
Растворитель
|
Тип
|
|
17 b-эстрадиол
|
Berlex Labs
|
Climara
|
7 дней
|
Этерифицированная жирная кислота
|
Матрикс
|
|
17 b-эстрадиол
|
Novartis
|
Estraderm
|
3 дня
|
Нет
|
Raviolli
|
|
17 b-эстрадиол
|
Novartis, Procter& Gamble,
Rhone-Poulenc Rorer, Novo Nordisk
|
Menorest, Vivelle
|
3-4 дня
|
Олеиновая кислота, пропиленгликоль
|
Матрикс
|
|
17 b-эстрадиол
|
Parke-Davis
|
FemPatch
|
7 дней
|
Этерифицированная жирная кислота
|
Матрикс
|
|
17 b-эстрадиол
|
Procter & Gamble
|
Alora
|
4 дня
|
Сорбитан монолеат
|
Матрикс
|
|
Клонидин
|
Boehringer Ingelheim
|
Catapres TTS
|
7 дней
|
Нет
|
Матрикс
|
|
Никотин
|
Prostep
|
24ч.
|
Нет
|
Матрикс
|
|
Никотин
|
Novartis
|
Habitrol
|
24ч.
|
Нет
|
Матрикс
|
|
Никотин
|
SmithKline Beecham
|
Nicoderm CQ
|
24 ч.
|
Нет
|
Матрикс
|
|
Никотин
|
Warner-Lambert
|
Nicotrol
|
16 ч.
|
Нет
|
Матрикс
|
|
Нитроглицерин
|
Berlex Labs
|
Minitran
|
12- 14 ч.
|
Этерифициро-ванная жирная кислота
|
Матрикс
|
|
Нитроглицерин
|
Novartis
|
TransdermNitro
|
12- 14 ч.
|
Нет
|
Raviolli
|
|
Нитроглицерин
|
Schering-Plough
|
Nitrodur
|
12-14 ч.
|
Нет
|
Матрикс
|
|
Нитроглицерин
|
Schwarz Pharma
|
Deponit
|
12-14 ч.
|
Нет
|
Матрикс
|
|
Нитроглицерин
|
Searle
|
Nitrodisc
|
12-14 ч.
|
Нет
|
Матрикс
|
|
Скополамин
|
Novartis
|
Transderm Scop
|
3 дня
|
Нет
|
Raviolli
|
|
Тестостерон
|
Novartis
|
Testoderm
|
24 ч.
|
Нет
|
Raviolli
|
|
Тестостерон
|
SmithKline Beecham
|
Androderm
|
24 ч.
|
Этанол, глицерил монолеат, метил лауреат, глицерин
|
Raviolli
|
Janssen Silag
|
Durogesic
|
3 дня
|
Этанол
|
Raviolli
|
Таблица 3.Трансдермальные терапевтические системы, находящиеся на
различных стадиях разработки
|
Препарат
|
Показания
|
Компании разработчики
|
|
а-Интерферон
|
Рак, вирусная инфекция
|
Helix BioPharma
|
|
GP2128
|
Сердечная недостаточность
|
Gensia
|
|
KB R6806
|
Рвота
|
Organon
|
|
N0923
|
Болезнь Паркинсона
|
Discovery Therapeutics
|
|
Альпростадил
|
Сексуальные расстройства
|
MacroChem
|
|
Бупренорфин
|
Боль
|
Gruenenthal
|
|
Буспирон
|
Тревога, депрессия, расстройство внимания
|
Sano
|
|
Ветепорфин
|
Рак, псориаз, артрит, ретинопатия
|
British Columbia University
|
|
Диклофенак
|
Боль, воспаление
|
Noven
|
|
Ибупрофен
|
Остеоартриты
|
MacroChem
|
|
Изорбит динитрат
|
Стенокардия
|
Rotta
|
|
Инсулин
|
Диабет
|
Dong Shin, Helix BioPharma, IDEA
|
|
Кетопрофен
|
Боль, воспаление
|
Noven
|
|
Кеторолак
|
Боль
|
Pharmetrix
|
|
Клонидин
|
Гипертония
|
Maruho
|
|
Ксаномелин
|
Болезнь Альцгеймера
|
Eli Lilly
|
|
Лидокаин
|
Боль, мигрень
|
American Pharmed, TheraTech
|
|
Метилфенидат
|
Расстройство внимания
|
Noven
|
|
Миконазол
|
Микозы
|
Noven
|
|
Никотин
|
Никотиновая зависимость
|
Cygnus, Hercon, Noven, Pharmacia
& Upjohn
|
|
Никотин и мекамиламин
|
Sano
|
|
Нитрат
|
Стенокардия
|
Pharmetrix
|
|
Нитроглицерин
|
Стенокардия
|
Hercon, Noven
|
|
Норэтистерон ацетат
|
Дефицит гормонов
|
Ethical
|
|
Норэтистерон и эстрадиол
|
Дефицит гормонов
|
Rotta
|
|
Оксибутин
|
Недержание мочи
|
Alza
|
|
Перголид
|
Болезнь Паркинсона
|
Athena Neurosciences
|
|
Пироксикам
|
Боль, воспаление
|
Noven
|
|
Празозин
|
Доброкачественная гипертрофия предстательной железы
|
Cygnus
|
|
Прогестоген
|
Дефицит гормонов
|
Noven
|
|
Сальбутамол
|
Астма
|
Noven
|
|
Сальбутамол + альбутерол
|
Астма
|
Sano
|
|
Селегилин
|
Болезнь Альцгеймера, депрессия
|
Somerset Laboratories
|
|
Синтетический прогестоген
|
Контрацепция, дефицит гормонов
|
Population Council
|
|
Скополамин
|
Рвота
|
Noven, Sano
|
|
Тестостерон
|
Гипогонадизм
|
Fabre
|
|
Тестостерон
|
Гипогонадизм, остеопороз
|
Ethical
|
|
Тестостерон
|
Дефицит гормонов
|
TheraTech
|
|
Тестостерон и эстрадиол
|
Дефицит гормонов
|
TheraTech
|
|
Тиатолсерин
|
Болезнь Альцгеймера
|
Axonyx
|
|
Тиацимсерин
|
Болезнь Альцгеймера
|
Axonyx
|
|
Тулобутерол
|
Астма
|
Hokuriku
|
|
Фенопрофен
|
Боль, воспаление
|
Noven
|
|
Физостигмин
|
Болезнь Альцгеймера
|
Pharmetrix
|
Боль, воспаление
|
Noven
|
|
Эстрадиол
|
Дефицит гормонов
|
Cygnus, Fabre, Hercon, Nitto
Electric,Pharmetrix, Servier
|
|
Эстрадиол и левоноргестрел
|
Дефицит гормонов
|
Gruenenthal
|
|
Эстрадиол и норэтистерон
|
Дефицит гормонов
|
Ethical, Novartis
|
|
Эстрадиол и прогестин
|
Дефицит гормонов
|
Cygnus, TheraTech
|
|
Эстрадиол с синтетическим прогестогеном
|
Дефицит гормонов
|
Sano
|
|
Эстроген
|
Дефицит гормонов
|
Elan
|
|
Эстроген и прогестин
|
Дефицит гормонов
|
Hercon
|
|
Эстроген и прогестоген
|
Дефицит гормонов
|
Fournier, Sano
|
|
Эстроген и прогестоген
|
Контрацепция
|
Cygnus, Pharmetrix
|
|
Этинилэстрадиол
|
Дефицит гормонов
|
Cygnus
|
|
Этинилэстрадиол и нортинодрон ацетат
|
Дефицит гормонов
|
Warner- Lambert
|