|
Возможно излечить с помощью химиотерапии
|
Химиотерапия дает высокую частоту регрессии и продление
жизни; излечение наступает менее, чем у 10% больных
|
Достигается регрессия опухоли у 20-50% больных,
редко-продление жизни
|
Малочувствительны к химиотерапии
|
|
· Хорионэпителиома матки · Опухоль Беркитта · Острый лимфобластный лейкоз · Злокачественные опухоли яичка · Лимфогранулематоз · Хронический миелолейкоз
|
· Острые лейкозы · Миеломная болезнь · Эритремия · Саркома Юинга · Рак
предстательной железы · Рак
яичников · Рак легкого
(мелкоклеточный) · Рак
тела матки · Опухоль
Вильмса · Эмбриональная
рабдомиосаркома · Лимфосарком
· Ретинобластома
|
· Рак желудка и толстой кишки · Хронические лейкозы · Нейробластома · Меланома · Рак молочной железы · Плоскоклеточный рак головы и шеи · Рак гортани · Рак мочевого пузыря · Саркома мягких тканей · Остеогенная саркома · Глиобластома · Кортикостерома
|
· Немелкоклеточный рак легкого · Рак пищевода · Рак печени · Рак поджелудочной железы · Рак щитовидной железы · Рак почки · Рак шейки матки · Рак
влагалища
|
.История развития противоопухолевых препаратов
Известно, что попытки использования лекарственных средств для лечения
больных раком предпринимались очень давно, начиная с Парацельса, а возможно, и
ранее. Например, в одном из папирусов, датированным 1500 годом до н. э., сообщалось
о применении мышьяка для лечения опухоли. Все эти попытки носили эмпирический
характер и были безуспешными. П. Эрлих, признанный основоположник химиотерапии,
автор самого термина «химиотерапия», определил ее как лечение системных
паразитарных заболеваний химическими веществами. Под паразитарными
заболеваниями он понимал болезни, вызываемые глистами, грибами, простейшими,
бактериями, риккетсиями, вирусами. Позже термин «химиотерапия» был
распространен на лечение опухолей. П. Эрлиху принадлежит также идея
систематического скрининга химических веществ на наличие у них необходимых для
химиотерапевтических препаратов свойств и формулирование методологии
исследования химиотерапевтических агентов на соответствующих моделях.
Противоопухолевая химиотерапия как раздел медицинской науки, включающий
разработку и изучение новых препаратов и их практическое применение, имеет
сравнительно короткую историю. До второй мировой войны очень немного соединений
было изучено на наличие противоопухолевой активности; это были соединения
мышьяка, некоторые металлы, токсины, колхицин и другие митотические яды.
Интерес к этим исследованиям во второй половине XX в. был стимулирован классическими работами О. Варбурга, в
которых впервые были отмечены определенные различия между опухолевыми и
нормальными тканями.
Первые крупные успехи в области современной химиотерапии онкологических
заболеваний были достигнуты в 40-х годах, когда во время второй мировой войны
стали подробно изучать влияние на организм боевых отравляющих веществ: иприта,
или бис-(в-хлорэтил) сульфида, и азотистого иприта, или трихлорэтиламина. Еще
ранее (в 1919 г.) стало известно, что азотистый иприт вызывает лейкопению и
аплазию костного мозга.
Дальнейшие исследования показали, что азотистый иприт оказывает
специфическое цитотоксическое влияние на лимфоидные ткани и обладает
противоопухолевой активностью при лимфосаркоме у мышей. В 1942 г. были начаты
клинические испытания трихлорэтиламина, что положило начало эре современной
химиотерапии опухолей.
Вскоре, был синтезирован ряд производных бис-(в-хлорэтил) амина, или
бис-(2- хлорэтил) - амина, и некоторые из них нашли применение в качестве
противоопухолевых средств.
Вслед за бис-(в-хлорэтил)-аминами были получены первые цитостатические
алкилирующие соединения иных химических групп: этиленимины, алкилированные
сульфонаты, триазуны.
В начале 1960-х гг. обнаружены противоопухолевые вещества другого
механизма действия-антиметаболиты. Метотрексат, имеющий структурное сходство с
фолиевой кислотой и являющийся ее антиметаболитом, оказался эффективным при
некоторых опухолях человека, особенно при хориокарциноме у женщин и при острой
лейкемии. Вслед за этим были обнаружены противоопухолевые свойства других
антиметаболитов: аналогов пурина (меркаптопурин, тиогуанин) и пиримидина (фторурацил,
цитарабин).
В дальнейшем в качестве противоопухолевых средств нашел применение ряд
антибиотиков (адриамицин, оливомицин, дактиномицин), ферменты (L-аспарагиназа), некоторые алкалоиды
(винбластин, винкристин) и иные средства растительного происхождения.
В 1970-х гг. были открыты противоопухолевые свойства препаратов платины.
Для лечения гормонозависимых опухолей широкое применение получил ряд
эстрогенных, андрогенных и гестагенных препаратов, а также антагонисты
эстрогенов, например, тамоксифен, и андрогенов (флютамид).
В последние годы большое внимание стали привлекать эндогенные
противоопухолевые соединения. Обнаружена эффективность при некоторых видах
опухолей интерферонов, моноклональных антител, изучается противоопухолевая
активность других лимфокинов.
Таким образом, каждое десятилетие шестидесятилетнего периода может быть
названо именем той группы препаратов, к которой в этот время было приковано
наибольшее внимание химиотерапевтов и с которой связывали наибольшие надежды.
4.
Определение и классификация
Дадим
определение понятию “цитостатические препараты”.
Цитостатики-это
группа противоопухолевых препаратов, которые вызывают некроз раковых клеток.
Цитостатики повреждают клетки, находящиеся в стадии митоза (деление клетки, в
ходе которого хромосомы одинаково распределяются между ядрами, что обеспечивает
образование генетически идентичных дочерних клеток). Быстро размножающиеся
клетки опухоли подвергаются действию препарата в первую очередь. Нарушение
течения стадий деления препятствует пролиферации, а также приводит к некрозу
раковых клеток. При некрозе повреждаются оболочка, ядро и другие её компоненты,
что ведет к смерти клетки.
В настоящее
время цитостатические препараты включают целый ряд средств различной химической
структуры и разного фармокологического действия.
В основном их
можно разделить на следующие группы и соответствующие им классы веществ:
· Алкилирующие
соединения и препараты, аналогичные им по действию
. Хлорэтиламины
. Этиленимины
. Производные
метансульфоновой кислоты
. Производные
нитрозомочевины
. Триазины
и метилгидразины
. Соединения
платины
· Антиметаболиты
. Антагонисты
фолиевой кислоты
. Антагонисты
пурина
. Антагонисты
пиримидина
· Противоопухолевые
антибиотики
. Актиномицины:
дактиномицин
. Антрациклины:
рубомицин, доксорубицин, эпирубицин
. Флеомицины:
блеомицин, блеомицетин
· Алкалоиды
и другие вещества растительного происхождения
. Алкалоиды
барвинка розовог: винбластин, винкристин, винорельбин
. Алкалоиды
тисового дерева (таксаны): паклитаксел (таксол), таксотер
. Подофиллотоксины,
выделяемые из подофилла щитовидного: этопозид, тенипозид
. Ингибиторы
топоизомеразы I:иринотекан
. Алкалоиды
безвременника великолепного: колхамин
· Ферментные
препараты: L-аспарагиназа
· Гормоны
и их антагонисты
. Андрогены:
тестостерона пропионат, медротестрона пропионат, тетрастерон
. Эстрогены:
диэтилстильбэстрол, фосфэстрол, этинилэстрадиол
. Гестагены:
оксипрогестерона капронат, медроксипрогестерона ацетат
. Антагонисты
эстрогенов (антиэстрогены): тамоксифен, торемифен, фульвестрант
. Антагонисты
андрогенов (антиандрогены): флутамид, андрокур
. Агонисты
гипоталамического гормона, стимулирующего высвобождение гонадотропных гормонов:
госерелин, лейпрорелин
. Ингибиторы
ароматазы: аминоглютетимид, летрозол
. Глюкокортикоиды:
преднизолон, дексаметазон
· Интерфероны
и интерлейкины: б-и в-интерфероны, альдеслейкин
· Моноклональные
антитела: трастузумаб (герцептин), ритуксимаб (мабтера), бевацизумаб (авастин)
· Ингибиторы
тирозинкиназ: иматиниб (гливек), гифетиниб (иресса), эрлотиниб (тарцева)
. Механизмы
действия
Рассмотрим
механизмы действия цитостатиков на примере наиболее изученных групп, а именно
алкилирующих цитостатиков, антиметаболитов и некоторых природных соединений. В
большинстве своем они основаны на поперечном связывании молекул ДНК и
повреждении их матрицы, блокировании микротрубочек веретена деления,
блокировании фермента дигидрофолатредуктазы, практически полной остановке
синтеза ДНК/РНК или на синтезе аномальных нуклеиновых кислот. Также напомним,
что митозу предшествует удвоение хромосом (синтез ДНК) и усиление белков
(синтез РНК). ДНК клетки представляет собой матрицу для нового синтеза ДНК и
РНК.
.
Алкилирующие цитостатики
Алкилирующие
цитостатики-это реакционноспособные соединения, предоставляющие свой алкильный
остаток, который связывается с ДНК ковалентной связью. Например, атомы хлора из
молекул хлорэтиламинов могут обмениваться на азотистые основания, при этом
образуется электрофильный карбониевый ион, который переходит в этиленимоний.
Последний также образует функционально активный карбониевый ион,
взаимодействующий, согласно имеющимся представлениям, с нуклеофильными
структурами ДНК (с гуанином, фосфатными, аминосульфгидрильными группами и др.).
Таким образом, происходит алкилирование субстрата (отсюда и термин
«алкилирующие средства»). По аналогичному принципу, очевидно, действуют и
другие представители этой группы противобластомных средств.

В результате
подобных манипуляция образуются сшивки между нитями ДНК. Более наглядно этот
процесс изображен на Рисунке 1.
Взаимодействие
алкилирующих веществ с ДНК, в том числе поперечное связывание молекул ДНК,
нарушает ее стабильность, вязкость и впоследствии целостность. Все это приводит
к резкому угнетению жизнедеятельности клеток. Их способность к делению
подавляется, многие клетки гибнут. Алкилирующие средства действуют на клетки в
интерфазе. Особенно выражено их цитостатическое влияние в отношении
быстропролиферирующих клеток.
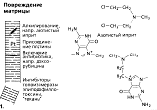
Рисунок 1. Действие алкилирующих цитостатиков, антибиотиков
Антиметаболиты
По
химическому строению антиметаболиты лишь похожи на естественные метаболиты, но
не идентичны им. В связи с этим они вызывают нарушение синтеза нуклеиновых
кислот. Это отрицательно сказывается на процессе деления опухолевых клеток и
приводит их к гибели. Действуют антиметаболиты на разных этапах синтеза
нуклеиновых кислот.
Один из
механизмов действия антиметаболитов основан на ингибировании синтеза оснований.
Например, для синтеза пуриновых оснований и тимидина необходима
тетрагидрофолиевая кислота(ТГФК). Она образуется из фолиевой кислоты при помощи
фермента дигидрофолатредуктазы. Аналог фолиевой кислоты метотрексат блокирует
фермент и таким образом создает дефицит ТГФК в клетках, тем самым нарушая
синтез РНК. Восстановить дефицит ТГФК можно путем введения фолиновой
кислоты(5-формил-ТГФК).
Другим
способом блокирования синтеза ДНК и РНК является включение аналогов оснований
(таких как 6-меркаптопурин, 5-фторурацил) или нуклеозидов с аномальными
сахарами (цитарабин).
Некоторые
природные соединения: винбластин и винкристин
Как мы знаем,
перед делением клетки веретено деления растягивает удвоенные хромосомы. На этот
этап воздействуют так называемые “антимитотические яды”, к которым относятся винбластин
и винкристин. Одним из элементов веретена деления являются микротрубочки,
образование которых и блокируют вышеупомянутые яды. Микротрубочки состоят из
белков б- и в-тубулина. Ненужные трубочки разрушаются, а их составные части
снова преобразуются для повторного использования. Винбластин и винкристин
ингибируют полимеризацию компонентов тубулина в микротрубочки. Паклитаксел же
ингибирует разборку микротрубочек и индуцирует образование атипичных
микротрубочек, блокирую тем самым преобразование тубулина в микротрубочки с
нормальными функциями.
Побочные
эффекты
Как
упоминалось ранее, быстро размножающиеся клетки опухоли подвергаются действию
препаратов в первую очередь. Ткани же, имеющие меньшую скорость клеточного
деления, то есть большинство здоровых тканей, не подвергаются действию
препаратов. Однако это же относится и к низкодифференцированным (твердым)
опухолям с редко делящимися клетками.
В то же время
клетки некоторых здоровых (интактных) тканей имеют физиологически обусловленную
высокую частоту деления и повреждаются под действием цитостатической терапии,
вследствие которой и наблюдаются типичные побочные эффекты.
Побочные
эффекты противораковых веществ, действующих на интактные делящиеся ткани, можно
прогнозировать. К ним относятся воздействия на:) Костный мозг и клетки
ретикулоэндотелиальной системы (панцитопения и иммунодепрессия; подавление, как
образования антител, так и клеточного иммунитета).
Подавление
функции костного мозга относится к единственному, наиболее важному фактору,
лимитирующему дозы препаратов. Необходимы повторные анализы крови, трансфузия
всех ее форменных элементов, например, тромбоцитной массы при
тромбоцитопеническом кровотечении или при числе тромбоцитов менее 25*109
на литр. Блеомицин и винкристин сравнительно малотоксичны для костного мозга.
Развитие септицемии (часто
оппортунистическая инфекция, вызванная граммотрициательными бактериями,
представляющими собственную флору, например, кишечника при его повреждении
препаратами) требует проведения энергичного лечения противобактериальными
средствами, часто комбинированными. Полезны также трансфузии лейкоцитной массы.
Повышается частота сопутствующих инфекций, вызванных вирусами (опоясывающий
лишай), грибами (кандидоз), и простейшими (пневмоцисты). При повышении
температуры тела у больного раком, которому проводится химиотерапия, необходимо
произвести микробиологическое исследование и назначить срочно соответствующее
лечение.) Слизистые оболочки, выстилающие кишечник и другие органы (диарея,
язвы).) Волосяные фоликулы (алопеция; восстановление происходит через 2-6
месяцев после прекращения лечения; выпадение волос может быть сведено к
минимуму охлаждением волосистой части головы, в результате чего уменьшается
приток крови и замедляются химические реакции).) Заживление ран (замедление);) Мочевую
систему (например, уратная нефропатия: быстрое разрушение большого числа
злокачественных клеток приводит к образованию большого количества пуринов и
пиримидинов, превращающихся в мочевую кислоту, которая затем может
кристаллизоваться в моче; этого можно избежать, если принимать большие
количества жидкости, подщелачивать мочу и принимать аллопуринол на первых
этапах химиотерапии; на практике это случается только тогда, когда масса
опухоли велика и она очень чувствительна к препаратам, например, при остром
лимфоцитарном лейкозе или лимфоме).) Половые клетки.
Воздействие на половые клетки
может привести к уменьшению полового влечения и стерильности. В связи с
мутагенным действием противораковых веществ следует предупреждать зачатие во
время лечения и в течение нескольких месяцев после его окончания, так как
следует иметь в виду, что репродуктивная функция как у мужчин, так и у женщин
сохраняется. Также если цитостатики назначаются во время беременности, то
нарушается развитие плода (тератогенное действие).) Разные ткани
(канцерогенность, вторичные опухоли).
Многие цитостатические
препараты канцерогенны, поэтому можно, излечив больного от первичной опухоли,
через 5 лет диагностировать у него вторичный, индуцированный проведенной
химиотерапией, рак. Особенно это свойство присуще алкилирующим средствам,
некоторым антиметаболитам (меркаптопурин) и антибиотикам (доксорубицин). Риск
лейкоза, лимфомы и чешуйчатой карциномы при этом в 20-30 раз превышает таковой
у лиц, не лечившихся этими препаратами. Синергического канцерогенное действие
может быть обусловлено сочетанием химиотерапии и облучения.
При применении
противоопухолевых препаратов также часто наблюдаются тошнота, рвота, аноресия,
диарея, возможны алопеция и иные побочные явления. Некоторые противоопухолевые
антибиотики обладают кардиотоксичностью (доксорубицин, рубицина хлорид и другие
антрациклиновые антибиотики), нефро- и ототоксичностью. Эстрогены, андрогены,
их аналоги и антагонисты способны вызывать гормональные расстройства.
Вследствие того, что
большинство цитостатических средств вызывает ряд побочных эффектов,
лимитирующих их применение, чтобы в какой-то степени нивелировать эти
осложнения или предупредить их, используется целый комплексвспомогательных
средств, применяемых при химиотерапии опухолевых заболеваний. К ним относятся
следующие группы: . Средства, стимулирующие кроветворение-колониестимулирующие
факторы
. Стимуляторы лейкопоэза:
молграмостим, филграстим
. Стимуляторы эритропоэза:
эритропоэтин . Противорвотные средства: ондансетрон, трописетрон, метоклопрамид
. Средства, повышающие иммунную защиту организма: интерфероны, интерлейкины,
препараты тимуса, левамизол . Средства, подавляющие проявления карциноидного
синдрома, при злокачественных нейроэндокринных опухолях: октреотид . Средства,
препятствующие остеопорозу при метастазах опухолей в кости: бисфосфонаты
(памидронат, клодронат, золедронат1 и др.)
Представители цитостатиков
Как было показано выше, цитостатические препараты в изобилии представлены
различными классами веществ. Рассмотрим наиболее важных представителей групп
цитостатиков.
Алкилирующие вещества
В большинстве своем этот класс цитостатиков представлен производными
бис-(в-хлорэтилсульфида). В механизме противоопухолевого действия таких
соединений существенную роль играет их алкилирующие свойства. Они способны
реагировать с нуклеофильными центрами белковых молекул, нарушая синтез ДНК (в
меньшей степени РНК), в результате чего нарушается жизнедеятельность клеток и
блокируется их митотическое деление. Высокой чувствительностью к этим веществам
обладают ядра клеток гиперплазмированных опухолевых тканей и лимфоидной ткани.
В то же время эти производные легко взаимодействуют с нуклеопротеидами
клеточных ядер кроветворных тканей, вследствие чего подавляется процесс
кроветворения.
Хлорэтиламины обладают высокой токсичностью и в дозах, близких к
лечебным, могут вызывать побочные явления, выражающиеся в сильном угнетении
костномозгового кроветворения и нарушениях функции ЖКТ. При попадании на кожу и
слизистые оболочеи они действуют раздражающе, что приводит к абсцессам, при
введении же растворов под кожу происходит некроз тканей.
Первым из соединений данной группы, предложенным для использования в
медицинской практике, был гидрохлорид метил-бис-(в-хлорэтил)-амина, получивший
название Эмбихин. В дальнейшем были созданы другие соединения этого ряда,
нашедшие применение в качестве противоопухолевых препаратов, которые в связи с
особенностями их физико-хмических свойств, распределения в тканях, метаболизма
и другими частично различаются как по характеру действия, так и по
переносимости.
Этиленимины по механизму действия близки к производным
бис-(в-хлорэтил)-амина. В последнее время в связи с появлением новых
противоопухолевых препаратов область этих препаратов несколько сузилась.
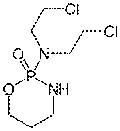
Циклофосфан
Производное
бис-(в-хлорэтил)-амина. Противоопухолевое средство алкилирующего действия,
оказывает также иммунодепрессивное действие. Это часто применяемый препарат из
группы хлорэтиламинов. Сам циклофосфан не оказывает цитостатического действия.
В результате химических превращений в печени из него образуются активные
метаболиты (фосфамид и акролеин), которые и обеспечивают противоопухолевый
эффект. Препарат вызывает более или менее длительные ремиссии при гемобластозах
(в том числе при остром лимфолейкозе), множественной миеломе. Кроме того, его
применяют при раке яичников, молочной железы, мелкоклеточном раке легкого.
Допан и хлорбутин вводят внутрь, циклофосфан и сарколизин - парентерально и
энтерально.
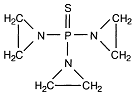
Тиофосфамид
Этиленимин.
Оказывает цитостатическое действие и угнетает развитие пролиферирующей, в том
числе злокачественной, ткани. При введении в организм быстро метаболизируется с
образованием активного и стойкого метаболита триэтилениминофосфамида(ТЕРА).
Механизм цитостатического действия основного вещества и его метаболита связан с
образованием комплексных связей с ДНК, ее алкилированием и блокадой
митотического деления пролиферирующих клеток.
Применение:
рак яичников, молочной железы, мочевого пузыря, щитовидной железы и некоторых
других опухолей (мезотелиомы, ретинобластомы). Использование тиофосфамида
способствует уменьшению числа рецедивов и метастазов после радикальной
мастэктомии. Также возможно применение препарата при хроническом лимфолейкозе и
хроническом миелолейкозе, лимфогранулематозе, ретикулосаркоме,
лимфосаркоматозе.
Побочные
эффекты: диспепсические расстройства, анорексия, гематурия, аменорея, угнетение
сперматогенеза. В случае резкого угнетения костномозгового кроветворения во
время лечения препаратом немедленно прекращают его введенеие, назначают
переливание крови или лейкоцитной и тромбоцитной массы, а также стимуляторы
кроветворения.
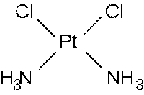
Цисплатин
Соединение
платины. Противоопухолевое средство алкилирующего типа, производное платины. Этот
комплекс платины в настоящее время широко применяется в медицине как
противораковое средство. Противораковая активность цисплатина была обнаружена
Барнеттом Розенбергом в 1969 году. Эффективным является только цис-изомер.
Угнетает синтез ДНК (связывается с ДНК клеток с образованием внутри- и
межспиральных сшивок, которые изменяют структуру ДНК), что ведет к длительному
подавлению синтеза нуклеиновых кислот и гибели клетки. В меньшей степени
подавляет синтез белка и РНК. Не обладает фазовой специфичностью. Комплексы
платины с цис-расположением атомов галогенов могут образовывать устойчивые
хелатные комплексы с пуриновыми и пиримидиновыми компонентами молекулы
нуклеиновых кислот, формируя связи внутри одной нити или параллельных нитей
двойной спирали ДНК. Противоопухолевому действию отчасти способствует
иммунодепрессивное влияние. Терапевтический эффект сохраняется в течение
нескольких дней после введения.
Применение:
отдельно или в комплексной терапии (в сочетании с метотрексатом, циклофосфаном,
тиогуанином, противоопухолевыми антибиотиками) при злокачественных опухолях
яичка и яичников, раке шейки и тела матки, легкого, желудка, пищевода, кожи,
мочевого пузыря, плоскоклеточном раке области головы и шеи, остеогенной
саркоме, меланоме, нейробластоме. Используют также в комплексной терапии
лимфогранулематоза и лимфосарком.
Побочные
эффекты: при применении циспластина возможны нарушения функция печени и почек,
тошнота, рвота, анорексия, головокружение, снижение слуха, аллергические, в том
числе, анафилактические, реакции, лейкопения, тромбоцитопения, анемия,
обратимая алопеция.
Антиметаболиты
Антиметаболитами
называют вещества, близкие по химической структуре к природным продуктам обмена
веществ (метаболитам) и ингибирующие превращения и физиологическую активность
этих эндогенных соединений.
К
антиметаболитам, применяемым в качестве противоопухолевых средств, относится
ряд препаратов, являющихся структурными аналогами фолиевой кислоты
(метотрексат), пуринов (меркаптопурин, тиогуанин), пиримидинов (фторурацил).
Цитостатическое
действие всех этих препаратов связано с нарушением синтеза нуклеиновых кислот
(ДНК и РНК).
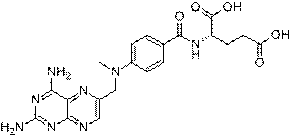
Метотрексат
Антагонист
фолиевой кислоты. Противоопухолевое, цитостатическое средство группы
антиметаболитов, действие метотрексата объясняется ингибированием активности
фермента дигидрофолатредуктазы, обуславливающей превращение фолиевой кислоты в
ее активную форму-тетрагидрофиолиевую кислоту, участвующую в биосинтезе
нуклеиновых кислот. Тормозит синтез, репарацию ДНК и клеточный митоз. Особо
чувствительны к действию быстро пролиферирующие ткани: клетки злокачественных
опухолей, костного мозга, эмбриональные клетки, эпителиальные клетки слизистой
оболочки кишечника, мочевого пузыря, полости рта. Наряду с противоопухолевым
обладает иммунодепрессивным действием.
Применение:
при остром лимфобластомном лейкозе, хориокарциноме матки, раке шейки матки,
опухолях головы и шеи, раке мочевого пузыря, легких, верхних дыхательных путей,
молочной железы, опухоли яичка.
Побочные
эффекты: при применении метотрексата возможны нейтропения, тромбоцитопения,
анемия, анорексия, рвота, диарея, стоматит, кожная сыпь и другие побочные
явления. Развитию побочных эффектов метотрексата препятствует кальция фолинат.
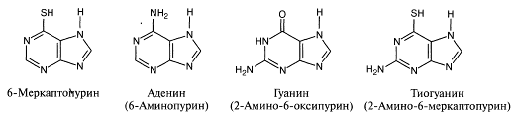
Меркаптопурин
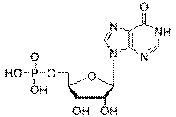
Инозиновая кислота
Антагонист пуринов. Противоопухолевое средство, антиметаболит. По
структуре близок к пуриновым основаниям (гуанину, аденину, тиогуанину,
гипоксантину, входящим в состав нуклеиновых кислот), является тиоловым
производным, конкурентным антагонистом гипоксантина. Включение в
соответствующие метаболические реакции нарушает синтез нуклеиновых кислот,
играющих важную роль в процессах пролиферации тканей, в том числе опухолевых.
Конкурирует с гипоксантином и гуанином за
гипоксанингуанинфосфорибозилтрансферазу, переводящую препарат в тиоинозиновую
кислоту (ТИК). ТИК подавляет ряд реакций с участием инозиновой кислоты (ИК),
включая превращение ИК в ксантиновую и адениловую кислоты. Кроме того, в ходе
метилирования ТИК образуется вещество, блокирующее наряду с самой ТИК
глутамин-5-фосфорибозилпирофосфатаминотрансферазу-фермент, инициирующий путь
пуринового синтеза рибонуклеотидов. Резистентность опухолей зачастую связана с
потерей способности клеток образовывать ТИК.
Применение: при остром лейкозе, для обеспечения ремиссия при остром
лимфобластомном и миелобластомном лейкозах, при хроническом миелолейкозе, а
также при полицитемии и болезни Крона.
Побочные эффекты: при применении препарата иногда наблюдаются поражения
слизистой оболочки рта, диспепсическия явления, гиперурикемия, нарушение
функций печени и почек, холестаз, гиперпигментация кожи. Как и другие
цитостатики, меркаптопурин может вызывать лейко- и тромбоцитопению, анемию.
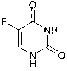
Фторурацил
Аналог
пиримидина. Противоопухолевая активность препарата определяется его
превращением в опухолевых тканях в 5-фтор-2-дезоксиуридин-5’-монофосфат,
являющийся конкурентным ингибитором фермента тимидилатсинтетазы, принимающей
участие в синтезе нуклеиновых кислот. Применение: рак желудка, пищевода,
поджелудочной железы, толстой и прямой кишки, молочной железы, яичников, шейки
матки, мочевого пузыря, опухолях головы и шеи. Побочные эффекты: фторурацил
обладает высокой токсичностью. При его применении вероятны угнетение
кроветворения, язвенный стоматит, снижение аппетита, рвота, диарея, реже-
дерматиты, эзофагит, проктит, сонливость, атаксия, нарушения зрения,
провоцирование стенокардии и инфаркта миокарда, нарушение функций печени и
почек.
Противоопухолевые
антибиотики
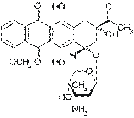
Рубомицин
Антрациклиновый
антибиотик. Противоопухолевый антибиотик антрациклинового ряда. Действует на
S-фазу митоза. Блокирует матричную функцию ДНК, нарушая синтез нуклеиновых
кислот и белка. Противоопухолевая активность реализуется также через
взаимодействие с мембранами и образование свободных радикалов семихинонного
типа. Характеризуется высокой антимитотической активностью и низкой
избирательностью действия. Терапевтический эффект при острых лейкозах
развивается после 2-3 инъекций (значительно уменьшается число бластных клеток в
крови и костном мозге). Снижение общего количества лейкоцитов продолжается на
протяжении 2 недель после окончания курса. Токсичность наиболее высока при
внутрибрюшинном способе введения.
Применение:
при остром лейкозе, ретикулосаркоме, хориоэпителиоме матки, лимфосаркоме,
солидных опухолях, опухоли Вильмса, хроническом миелолейкозе.
Возможно
применение рубомицина в комбинации с другими противоопухолевыми препаратами
(циклофосфан, метотрексат, меркаптопурин), лучевой терапией.
Побочные
эффекты: может вызвать лейкопению, тромбоцитопению, анемию. Наблюдается
тошнота, рвота, анорексия, диарея, стоматит, ротоглоточный кандидоз, изъявление
слизистых ЖКТ, гиперурикемия, уратная нефропатия, алопеция, аллергические
реакции.
7.
Вещества растительного происхождения
опухоль цитостатический препарат
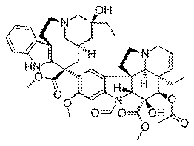
Винкристин
Алкалоид. Идентичен винбластину. Противоопухолевое средство растительного
происхождения, алкалоид из барвинка розового (Vinca rosea L.). Способен
связываться с молекулами тубулина, тормозить образование митозного веретена,
блокируя тем самым деление клеток, то есть митоз на стадии метафазы.
Применение: при лимфогранулематозе, лимфомах, саркоме Юинга,
рабдомиосаркоме, саркомах мягких тканей, нейробластоме, опухоли Вильмса, остром
лимфобластомном лейкозе, раке молочной железы, легкого, идиопатической
тромбоцитопенической пурпуре.
Побочные эффекты: может оказывать нейротоксическое влияние и вызывать
парестезии, переферические невриты, двигательные расстройства, очаговые
повреждения ЦНС. Вероятные также парез кишечника, алопеция, лейкопения,
язвенный стоматит, атаксия, потеря массы тела, тошнота, рвота, повышение
температуры тела.
. Противоопухолевые гормональные препараты
В онкологической практике применяется ряд гормональных препаратов,
андрогены, эстрогены, глюкокортикостероиды, а также препараты, тормозящие
действие эстрогенов (антиэстрогены) и андрогенов (антиандрогены). Все эти
препараты применяют преимущественно при гормонозависимых опухолях. Эстрогены
назначают, когда показано подавление действия в организме андрогенов или
усиление активности эстрогенов (рак предстательной железы). Андрогены применяют
для повышения активности андрогенов или уменьшения активности эстрогенов (при
раке молочной железы). Глюкокортикостероиды в связи с их лимфолитическим
действием и способностью угнетать митоз лимфоцитов назначают преимущественно
при острых лейкозах и злокачественных лимфомах.
По механизму действия гормональные препараты отличаются от большинства
цитостатических препаратов. Основная их роль- восстановление нарушенной
гуморальной регуляции функции клеток. Вместе с тем не исключается и
специфическое влияние на опухолевые клетки: они в определенной степени тормозят
деление клеток и способствуют их дифференцированию. Важную роль в механизме
противоопухолевого действия гормонов играет их связывание со специфическими для
них рецепторами, наличие которых обнаружено не только в нормальных тканях-мишенях,
но и в некоторых опухолях.
Для практического применения в онкологии отобран ряд препаратов с
наиболее выигрышными терапевтическими и токсикологическими показателями.
Тамоксифен
Антагонист
эстрогена. Противоопухолевое антиэстрогенное средство. Конкурентно ингибирует
рецепторы эстрогенов в органах-мишенях и опухолях, происходящих из этих
органов. В результате возникает комплекс (препарат-рецептор-кофактор переноса),
который после транслокации в клеточное ядро предотвращает гипертрофию клеток,
зависящих от эстрогенного регулирования. Обладает антигонадотропными
свойствами, подавляет синтез простогландина (Pg) в опухолевой
ткани.
Тормозит
прогрессирование опухолевого процесса, стимулируемого эстрогенами. Способность
блокировать эстрогены может сохраняться в течение нескольких недель после
однократной дозы. Кроме того, тамоксифен может вызывать овуляцию у женщин при
ее отсутствии, стимулируя высвобождение из гипоталамуса ГРФ, стимулирующий
высвобождение гонадотропных гормонов гипофиза. У мужчин с олигоспермией
повышает концентрацию ЛГ и ФСГ, тестостерона и эстрогенов в сыворотке крови.
Тамоксифен и некоторые его метаболиты (N-дезметилтамоксифен,
4-гидрокситамоксифен) являются сильными ингибиторами оксидаз смешанной функции
системы цитохрома P450 печени, однако клиническое значение этих эффектов не
определено.
Применение:
рак молочной железы, меланома, рак эндометрия, предстательной железы, почки,
яичников, саркоме мягких тканей, опухолях гипофиза.
Побочные
эффекты: желудочно-кишечные расстройства, анорексия, головокружение,
тромбоцитопения, гиперкальцемия.
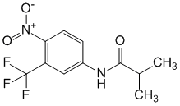
Флутамид
Антиандроген.
Противоопухолевое средств. Конкурентно блокирует взаимодействие андрогенов с их
клеточными рецепторами; препятствует проявлению биологических эффектов мужских
половых гормонов в андрогенчувствительных органах. Взаимодействуя с рецепторами
андрогенов в гипоталамусе и гипофизе, прерывает отрицательную обратную связь
между семенниками и гипоталамо-гипофизарной системой. В результате
растормаживается секреция гонадотропных гормонов и возрастает их концентрация в
крови и моче, а также тестостерона в плазме. Способность флутамида
препятствовать действию тестостерона на клеточном уровне служит дополнением к
лекарственной "кастрации", вызываемой агонистами ЛГ-рилизинг гормона
(ЛГРФ). Не обладает эстрогенной, антиэстрогенной, гестагенной и антигестагенной
активностью.
Применения:
рак предстательной железы.
Побочные
эффекты: диспепсические явления, гинекомастия, галакторея, анемия, задержка
жидкости в организме, нарушение функций печени и почек.
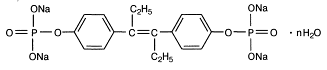
Фосфэстрол
Применение:
рак предстательной железы. Считается специфическим средством, действующим при
всех стадиях рака это локализации, чувствительного к эстрогенным препаратам.
Побочные
эффекты: препарат обычно хорошо переносится больными. В первые дни иногда
отмечается тошнота, рвота, ухудшение общего состояния, которые проходят в
процессе дальнейшего лечения.
Заключение
Развитие
химиотерапии за последние 60 лет происходило скачками - внедрение каждого
нового лекарственного средства знаменовало новую, как правило, более высокую
ступень развития этой науки, поскольку предоставляло новые возможности для
терапии опухолей. Каждое новое лекарство и создаваемый на его основе новый
класс препаратов открывали новую страницу в истории противоопухолевой
химиотерапии. Эта страница могла оставаться последней более или менее
длительное время, но неизбежно за ней открывалась следующая страница, появлялся
еще один класс противоопухолевых препаратов, и, как следствие, лекарственное
лечение рака поднималось еще на одну ступень.
Эффективные
старые препараты при этом не теряли своего клинического значения, что приводило
к возрастающему разнообразию арсенала лекарственных средств, находящихся в
распоряжении онколога-химиотерапевта, и это значительно увеличивало его
возможности в терапии больных. Важно отметить, что с каждым десятилетием
страницы истории противоопухолевой химиотерапии переворачивались все быстрее, и
это позволяет надеяться, что в сравнительно недалеком будущем будут созданы
препараты, которые позволят осуществить мечту больных и здоровых людей -
излечивать рак с помощью лекарств.
Эта
мечта может осуществиться с помощью цитостатических препаратов, которые широко
используются в терапии злокачественных новообразований. Их применение
лимитируются большим спектр побочных эффектов, которые, однако, с каждым годом
все легче стабилизировать с помощью комплекс впомогательных средств, цитостатики
имеют сравнительно (с другими методами лечения опухолей) небольшой перечень
противопоказаний. Вред, нанесенный пациенту в процессе лечения, в большинстве
случаев можно нивелировать. Тем самым развитие этой группы противоопухолевых
препаратов является приоритетным ввиду ее эффективности на фоне хирургического
вмешательства, биотерапии и лучевой терапии.
Литература
1. Люльман Х. Наглядная фармакология. / Х. Люльман, К. Мор,
Л. Хайн; Пер. с нем- М: Мир, 2008.-383 с.
2. Лоуренс Д.Р., Беннит П.Н. Клиническая фармакология: в
2-х т. Т. 1: Пер. с англ.-М.:Медицина, 1993.- 640 с.
. Машковский М.Д. Лекарственные средства.-16-е изд.,
перераб., испр. и доп.-М.: Новая волна, 2012.-1216 с.
. Харкевич Д.А. Фармакология.-10-е изд.-М.:
ГЭОТАР-Медиа, 2010. - 908 с.
. Логинова Н.В. Металлокомплексы в медицине: от
дизайна к химиотерапии и диагностике / Н.В. Логинова.-Минск: БГУ, 2006.-203 с.
. Корман Д.Б. Основы противоопухолевой химиотерапии /
Д.Б. Корман.-М: Практическая медецина, 2006.-512с.
. Ганцев Ш.К. Онкология: Учебник для студентов
медицинских вузов. - М.: ООО «Медицинское информационное агентство», 2006. -
488 с.
. Галицкий В.А. Канцерогенез и механизмы
внутриклеточной передачи сигналов // Вопросы онкологии.- 2003.- Т.49, № 3.-
С.278-293.
. Граник В.Г. Основы медицинской химии.-М.: Вузовская
книга, 2001.- 384 с.
. Глущенко Н.Н. Фармацевтическая химия: Учебник для
студ. сред. проф. учеб. заведений / Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков;
Под ред. Т.В. Плетеневой.-М.: Издательский центр “Академия”, 2004.- 384с.