Электролиз воды
Введение
За последние десятилетия созданы
сотни установок электролиза воды для получения водорода и кислорода,
оборудованных электролизерами, которые работают как при атмосферном, так и при
повышенном давлении. В настоящее время только на электростанциях работает около
тысячи электролизеров различного типа.
Для удовлетворения нужд народного
хозяйства в электролитическом водороде в ближайшие годы дополнительно
потребуется значительное количество мощных электролизеров производительностью
по 500 - 650 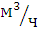 водорода
и более мелких электролизеров для выработки небольших количеств водорода.
водорода
и более мелких электролизеров для выработки небольших количеств водорода.
Во многих странах электролизные
установки использовались для получения тяжелой воды в качестве побочного
продукта. В последующем были разработаны более эффективные методы её
производства, однако побочное получение побочной воды на крупных электролизных
установках в ряде случаев целесообразно.
1. Общие сведения о
процессе электролиза воды
Как известно, при прохождении
электрического тока через растворы электролитов на электродах происходит разряд
ионов и протекают связанные с этим химические реакции. Протекания процесса
электролиза определяется переносом электрического тока в жидкости и условиями
разряда присутствующих в растворе ионов электролита.
Процесс электролиза воды с
получением водорода и кислорода описывается следующим суммарным уравнением:
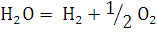
Чистую воду нельзя непосредственно
подвергать электролизу, так как её электропроводность очень мала. Удельная
электропроводность водопроводной воды близка к 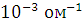 *
* 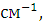 очень
чистой дистиллированной воды около 4*
очень
чистой дистиллированной воды около 4*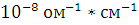 . Поэтому при электролизе применяют водные растворы электролитов -
кислот, щелочей, солей.
. Поэтому при электролизе применяют водные растворы электролитов -
кислот, щелочей, солей.
Изменяя состав, концентрацию и
температуру электролита и подбирая условия, определяющие величину
перенапряжения, можно изменять протекания электродных процессов в желательном
направлении.
В промышленных процессах электролиза
воды в настоящее время применяются только щелочные электролиты - едкое кали и
едкий нарт. Если в качестве электролитов используются технический щелочи, в их
растворах присутствуют примеси ионов 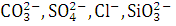 и т.д. Возможно также присутствие в электролите небольших
количеств железа и других загрязнений.
и т.д. Возможно также присутствие в электролите небольших
количеств железа и других загрязнений.
При длительной эксплуатации
установок электролиза воды в растворе электролита накапливаются посторонние
ионы, вносимые с примесями, содержащиеся в питательной воде. Если какая-либо
примесь, например ионы 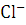 ,
постоянно поступает в раствор электролита, то при достаточной продолжительности
процесса электролиза достигается предельная концентрация этой примеси, которая
определяется из равенства её прихода и расхода в электролизере за единицу
времени.
,
постоянно поступает в раствор электролита, то при достаточной продолжительности
процесса электролиза достигается предельная концентрация этой примеси, которая
определяется из равенства её прихода и расхода в электролизере за единицу
времени.
При питании электролизера
дистиллированной водой содержание простых ионов в электролите обычно очень
невелико и в сумме не превышает 1 - 5 г/л, исключая карбонаты, содержание
которых в 1 л раствора электролита может достигать десятков граммов. В
электролизерах с открытым зеркалом электролита, соприкасающимися с воздухом,
концентрация карбонатов может быть ещё больше. Для электролизеров некоторых
конструкций электролит приготавливают в герметичных баках с азотной подушкой,
что предотвращает загрязнение его карбонатами.
При электролизе воды на катоде
выделяется водород, аноде - кислород. В зависимости от условий ведения
катодного процесса возможны два механизма его протекания. В кислых растворах с
высоким содержанием ионов водорода его выделение происходит за счет разряда
ионов 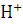 с образованием атомарного водорода, который адсорбируется на
поверхности катода, что может быть описано выражением:
с образованием атомарного водорода, который адсорбируется на
поверхности катода, что может быть описано выражением:
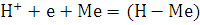
Поскольку ион водорода в растворе
гидратирован, стадию его разряда можно представить в виде:
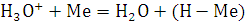
Следующая стадия катодного процесса
- рекомбинация атомарного водорода в молекулярный протекающая по
каталитическому механизму.
2 (Н - Ме)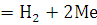
В определенных условиях обе стадии
катодного процесса - разряд ионов 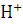 и выделение молекулярного водорода - могут протекать одновременно.
и выделение молекулярного водорода - могут протекать одновременно.
Выделение на аноде кислорода при
электролизе воды происходит в результате разряда гидроксильных ионов или
молекул воды. Присутствующие в электролите небольшие количества 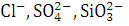 и других ионов, а также ионы
и других ионов, а также ионы 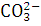 при достаточно высокой концентрации щелочи в растворе (200 - 300
г./л и более) не могут разряжаться, так как для этого в данных условиях
необходим более высокий потенциал, чем для разряда ионов
при достаточно высокой концентрации щелочи в растворе (200 - 300
г./л и более) не могут разряжаться, так как для этого в данных условиях
необходим более высокий потенциал, чем для разряда ионов 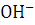 или молекул воды. В щелочных растворах при умеренных плотностях
тока подвод ионов гидроксила к аноду не является лимитирующим процессом и они
разряжаются на аноде по реакции:
или молекул воды. В щелочных растворах при умеренных плотностях
тока подвод ионов гидроксила к аноду не является лимитирующим процессом и они
разряжаются на аноде по реакции:
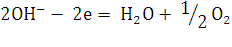
В кислых растворах при любых
плотностях тока и в щелочных растворах при высоких плотностях тока подвод ионов
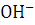 является лимитирующей стадией и для разряда их предложен второй
механизм:
является лимитирующей стадией и для разряда их предложен второй
механизм:
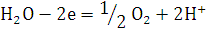
При электролизе в переносе тока
принимают участие все находящиеся в электролите ионы. Доля их участия определяется
относительной концентрацией и подвижностью ионов. В щелочных электролитах
вследствие очень низкой концентрации ионов водорода перенос тока осуществляется
почти исключительно ионами 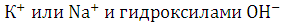 .
.
На катоде разряжаются практически
только молекулы воды, на аноде - ионы 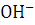 . При этом на каждую молекулу выделявшегося на катоде водорода
распадается две молекулы воды с образованием двух молекул
. При этом на каждую молекулу выделявшегося на катоде водорода
распадается две молекулы воды с образованием двух молекул 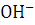 . Ионы
. Ионы 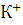 и
и 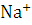 , участвующие в переносе тока к катоду, так же как
, участвующие в переносе тока к катоду, так же как 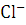 ,
, 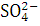 и
другие анионы, участвующие в переносе тока к аноду, на электродах не разряжаются.
и
другие анионы, участвующие в переносе тока к аноду, на электродах не разряжаются.
В связи с тем, что в процессе
электролиза воды на обоих электродах выделяются газы, прилегающий к электроду
слой электролита интенсивно перемешивается. Поэтому на поверхности анода
маловероятно образование локальных зон с сильно пониженной концентрацией КОН и
соответственно с повышенной концентрацией ионов 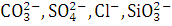 и др. Однако в глубине узких щелей между электродом и
прилегающими к нему деталями или под шламом у поверхности электрода возможно
значительное изменение концентрации ионов по ранее рассмотренным причинам.
Такие концентрационные изменения, по-видимому, вызывают местную интенсивную
электрохимическую коррозию некоторых деталей электролизеров.
и др. Однако в глубине узких щелей между электродом и
прилегающими к нему деталями или под шламом у поверхности электрода возможно
значительное изменение концентрации ионов по ранее рассмотренным причинам.
Такие концентрационные изменения, по-видимому, вызывают местную интенсивную
электрохимическую коррозию некоторых деталей электролизеров.
Как и в других электрохимических
процессах, затраты электрической энергии при электролизе воды велики и часто
определяют экономику этого процесса. Поэтому вопросам расхода энергии на
электролиз и снижению величины напряжения на электролитической ячейки всегда
уделяется большое внимание.
. Электрохимические
ячейки
Электрохимическая ячейка обычно
состоит из двух полуэлементов, каждый из которых представляет собой электрод,
погруженный в свой электролит. Электроды изготавливают из электропроводящего
материала (металла или углерода), реже из полупроводника. Носителями заряда в
электродах являются электроны, а в электролите - ионы. Являющийся электролитом
водный раствор поваренной соли (хлорида натрия NaCl) содержит заряженные
частицы: катионы натрия Na+ и анионы хлора Cl- Если
поместить такой раствор в электрическое поле, то ионы Na+ будут
двигаться к отрицательному полюсу, ионы Cl- - к положительному.
Расплавы солей, например NaCl, тоже электролиты. Электролитами могут быть и
твердые вещества, например b-глинозем (полиалюминат натрия), содержащий
подвижные ионы натрия, или ионообменные полимеры.
Полуэлементы разделяются
перегородкой, которая не мешает движению ионов, но предотвращает перемешивание
электролитов. Роль такой перегородки может выполнять солевой мостик, трубка с
водным раствором, закрытая с обоих концов стекловатой, ионообменная мембрана,
пластина из пористого стекла. Оба электрода электролитической ячейки могут быть
погружены в один электролит.
Электрохимические ячейки бывают двух
типов: гальванические элементы и электролитические ячейки (электролизеры).
В электролитической ячейке протекают
те же реакции, что и в промышленных электролизерах для получения хлора и
щелочи: превращение рассола (концентрированного водного раствора хлорида
натрия) в хлор и гидроксид натрия NaOH:
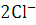 +
+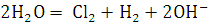
электролиз
окисление ион
Хлорид-ионы на графитовом электроде
окисляются до газообразного хлора, а вода на железном электроде
восстанавливается до водорода и гидроксид-иона. Электролиты остаются
электронейтральными благодаря перемещению ионов натрия через перегородку -
ионообменную мембрану. Электрод, на котором осуществляется окисление,
называется анодом, а электрод, на котором происходит восстановление, - катодом.
Список литературы
1. О.Д. Хвольсон, Курс физики, РСФСР, Госиздат, Берлин, 1923, т.
4.
. А.И. Левин, Теоретические основы электрохимии, Гос. Научно-техн.
Издат., Москва, 1963.
. А.П. Соколов, ЖРФХО, т. 28, с. 129, 1896.
. Л.М. Якименко и др., Электролиз воды, изд. «химия», Москва,
1970.