Принципы квантовой механики
Реферат
тема: «Принципы квантовой механики»
Москва 2014
Содержание
Введение
1. Соотношения неопределенностей
. Уравнение Шредингера
. Частица в потенциальной яме
. Прохождение частицы через
потенциальный барьер
. Атом водорода в квантовой механике
. Состояния электрона в атоме
водорода
. Излучение атома водорода
Список использованной литературы и
источников
Введение
В классической механике движение тел описывается
уравнением Ньютона
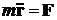
Решая это уравнение, можно
определить функцию r(t),
описывающую положение тела в любой момент времени. Дифференцируя эту функцию,
можно найти скорость и ускорение тела.
При рассмотрении малых частиц (r~10-8
см) многие принципы классической механики не выполняются, и для описания
движения таких частиц необходимо использовать законы квантовой механики. В
основе квантовой механики лежит уравнение Шредингера, которое в квантовой
механике играет ту же роль, что и уравнение Ньютона в классической механике.
Из уравнения Шредингера вытекает,
что состояние частицы описывается волновой функцией, которая позволяет
определить значения основных физических величин. При этом почти все физические
величины имеют дискретные значения, в отличие от классической физики, где они
обычно непрерывны.
В рамках квантовой механики частицы
материи обладают как корпускулярными, так и волновыми свойствами. Так, электрон
или протон могут вести себя как волны, а электромагнитное излучение
(рентгеновское, γ-излучение)
обладает корпускулярными свойствами - волна может, например, быть локализована
в одной точке пространства.
В квантовой механике используется
достаточно сложный математический аппарат, поэтому мы будем излагать основные
принципы упрощенно, опуская сложные математические выкладки.
В атомной физике в качестве единицы
измерения энергии обычно используется электрон-вольт. Электрон-вольт - это
энергия, которую приобретает электрон, пройдя разность потенциалов в 1 В: 1 эВ
= 1,6∙10 - 19 Дж.
шредингер потенциальный атом
электрон
1. Соотношения неопределенностей
В классической механике для
движущейся частицы в любой момент времени точно фиксированы ее координаты и
импульс. Если частица обладает волновыми свойствами, то нельзя задавать ее
положение в пространстве с точностью, превышающей длину волны.
Монохроматическая волна в фиксированный момент времени представляет собой
бесконечную синусоиду 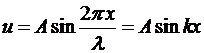 и говорить
о ее координате бессмысленно. Здесь
и говорить
о ее координате бессмысленно. Здесь 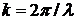 - волновое число.
- волновое число.
Понятие «длина волны» в данной точке
лишено смысла. На расстояниях меньших длины волны бессмысленно говорить об
одновременных значениях координаты и импульса частицы. Это утверждение вытекает
из соотношения де Бройля
p=h/λ.
Частицы вещества, рассматриваемые с
точки зрения волновых свойств, называют волнами де Бройля. Для таких частиц
можно ввести волновые характеристики: частоту и длину волны, групповую и
фазовую скорости и др.
Полагая неопределенность координаты 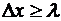 , а
неопределенность импульса Δpx , получим
, а
неопределенность импульса Δpx , получим
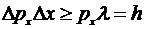 .
.
Аналогичные соотношения получим для
других компонент:
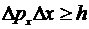 ,
,
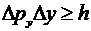 ,
,
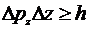 .
.
Эти соотношения были получены
Гейзенбергом и называются соотношениями неопределенностей Гейзенберга. Смысл
неравенств заключается в том, что координаты и импульсы не могут быть
одновременно определены абсолютно точно. Произведение неопределенностей
координаты и соответствующего ей импульса не может быть меньше величины h.
Соотношение неопределенности
является квантовым ограничением применимости классической физики. Рассмотрим,
например, движение электрона вокруг ядра в атоме водорода. Известно, что радиус
атома водорода 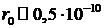 м. Скорость
электрона, движущегося по круговой орбите, определим из условия
м. Скорость
электрона, движущегося по круговой орбите, определим из условия
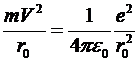 .
.
Отсюда получим 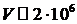 м/с. С
другой стороны, используя принцип неопределенности, найдем неопределенность
величины скорости
м/с. С
другой стороны, используя принцип неопределенности, найдем неопределенность
величины скорости
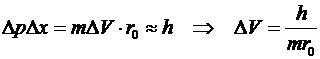 .
.
Подставляя числовые значения,
получим 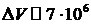 м/с, т.е.
неопределенность скорости в несколько раз превышает саму скорость. Поэтому
говорить о траектории движения электрона в атоме не имеет смысла. Можно
говорить только о вероятности нахождения электрона на определенном расстоянии
от ядра.
м/с, т.е.
неопределенность скорости в несколько раз превышает саму скорость. Поэтому
говорить о траектории движения электрона в атоме не имеет смысла. Можно
говорить только о вероятности нахождения электрона на определенном расстоянии
от ядра.
Для макроскопических тел
неопределенности в определении координат и импульсов настолько малы, что не
могут быть обнаружены никакими приборами. Поэтому в классической физике можно
говорить о траектории частицы, ее скорости и ускорении.
Интерпретация принципа
неопределенности является довольно сложной и неоднозначной. Различные физики
по-разному трактовали этот принцип.
) Н. Бор показал, что любое
измерение вносит погрешность в результаты. Если очень точно измерять координату
х, то появляется большая погрешность в определении импульса. Точное измерение
импульса приводит к большой погрешности в определении координаты 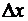 . При этом
всегда выполняется неравенство
. При этом
всегда выполняется неравенство
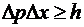 .
.
) В. Гейзенберг, Паули, де Бройль и
другие считали, что волновые свойства частиц приводят к тому, что говорить о
траектории частиц на расстояниях 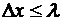 бессмысленно. В микромире
траекторий не существует.
бессмысленно. В микромире
траекторий не существует.
) А. Эйнштейн считал, что существуют
некоторые скрытые параметры, которые определяют траекторию в микромире.
Возможно, будет создана теория, в которой эти параметры можно будет определить
и полностью описать состояние физической системы.
При этом все ученые признавали
справедливость полученных формул, но давали им различную интерпретацию.
Соотношения неопределенности
справедливы не только для координат и импульсов, но и для других сопряженных
величин. Если ΔE -
неопределенность энергии системы в момент измерения, а Δt -
неопределенность длительности процесса измерения, то справедливо неравенство
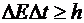 .
.
Например, для короткоживущих
элементарных частиц, имеющих время жизни τ, неопределенность в
определении величины энергии составит
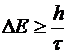 .
.
2. Уравнение
Шредингера
В классической физике движение частицы
описывается с использованием законов Ньютона. Основным уравнением движения
частицы является уравнение, вытекающее из второго закона Ньютона
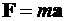 .
.
В квантовой механике основным
уравнением движения частицы является уравнение Шредингера. Согласно Шредингеру,
положение частицы описывается функцией Ψ(r,t) (пси -
функцией), которая зависит от координат и времени.
Уравнение Шредингера формулируется
для волновой функции Ψ(r,t) и имеет
вид
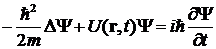 ,
,
где
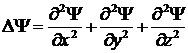
оператор Лапласа, 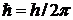 , m - масса
частицы, i - мнимая
единица, U(r,t) -
потенциальная энергия частицы. Если потенциальная энергия не зависит от
времени, то это уравнение можно упростить. Полагая
, m - масса
частицы, i - мнимая
единица, U(r,t) -
потенциальная энергия частицы. Если потенциальная энергия не зависит от
времени, то это уравнение можно упростить. Полагая
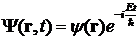 ,
,
где 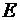 - энергия частицы, получим
- энергия частицы, получим
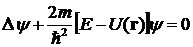 .
.
Последнее уравнение называют
уравнением Шредингера для стационарных состояний. Для однозначного определения
функции Ψ(r,t) уравнение
Шредингера следует дополнить граничными условиями, т.е. условиями для функции Ψ(r,t) на границе
области задания функции.
Смысл Ψ - функции:
квадрат модуля Ψ - функции
определяет вероятность того, что частица находится в элементе объема 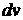
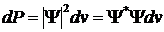 .
.
Из смысла Ψ - функции
вытекает, что описание частиц в квантовой механике является вероятностным.
Соответственно, в квантовой механике изменяется принцип причинности. Если в
классической физике при известных начальных условиях поведение механической
системы было полностью предопределено, то в квантовой механике на первое место
выходит случайность, и физические соотношения имеют вероятностный смысл.
Из вероятностного смысла Ψ - функции
вытекает условие нормировки
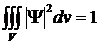 ,
,
которому должна удовлетворять Ψ - функция.
В уравнение Шредингера в качестве параметра входит энергия частицы Е. Можно
строго математически показать, что если движение частицы ограничено, то энергия
квантуется, т.е. принимает только дискретные значения.
В простейшем случае одномерного движения
уравнение Шредингера имеет вид
Если потенциальная энергия не
зависит от времени, то можно сделать замену переменных
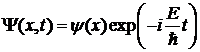 ,
,
где Е - полная энергия частицы.
Подставляя это выражение в уравнение Шредингера, получим уравнение для функции ψ(x)
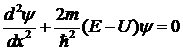 .
.
Уравнение Шредингера является
уравнением в частных производных и, вообще говоря, является более сложным, чем
уравнение Ньютона. В качестве простейшего примера рассмотрим свободное движение
частицы, т.е. случай 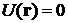 . Направляя
ось х вдоль линии движения частицы, получим стационарное уравнение Шредингера
. Направляя
ось х вдоль линии движения частицы, получим стационарное уравнение Шредингера
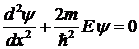 ,
,
решением которого будет функция
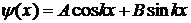 ,
,
где введено обозначение
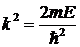 .
.
Положение частицы описывается
плоской монохроматической волной. Вероятность нахождения частицы во всех точках
пространства одна и та же, т.е. при свободном движении частицы ее координаты не
могут быть определены однозначно. Этот неожиданный с точки зрения классической
физики вывод связан с принципом неопределенности. Импульс частицы связан с
волновым вектором k соотношением
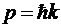 ,
,
и точное задание k приводит к
точному значению импульса 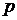 . На
основании принципа неопределенности Гейзенберга величина
. На
основании принципа неопределенности Гейзенберга величина 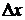 должна быть
бесконечно большой, что приводит к неопределенности значения х.
должна быть
бесконечно большой, что приводит к неопределенности значения х.
3. Частица в потенциальной яме
Рассмотрим простейший случай
движения частицы в одномерной потенциальной яме с бесконечно высокими
«стенками».
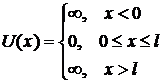

Уравнение Шредингера для частицы в яме имеет вид
(U = 0)
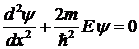
или
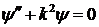 ,
,
где
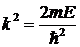 .
.
Для 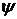 - функции на границах должны
выполняться условия непрерывности:
- функции на границах должны
выполняться условия непрерывности:
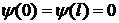 .
.
Общее решение дифференциального
уравнения
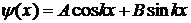 .
.
Из граничных условий получим
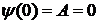 ,
,
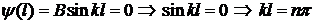 .
.
Для определения решения уравнения
Шредингера получим набор собственных функций
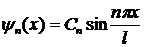 .
.
Общее решение имеет вид
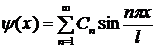 .
.
Коэффициенты 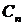 можно
определить из условия нормировки.
можно
определить из условия нормировки.
Важным является тот факт, что
энергия принимает дискретные значения (квантуется)
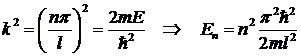 .
.
При этом число п называется главным
квантовым числом, а значения Еп называются уровнями энергии.
Энергетические уровни можно показать на графике

Здесь
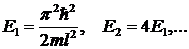
Интервал между соседними
энергетическими уровнями
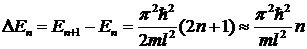 .
.
Для электрона на отрезке 10 см
(электрон в куске металла) получим
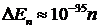 Дж = 10 - 16п эВ,
Дж = 10 - 16п эВ,
т.е. энергетический спектр можно
считать почти непрерывным. Если в качестве l взять
размеры атома, то получим 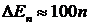 эВ - явно
дискретные значения энергии. Эффект квантования энергии проявляется только для
тел малой массы, ограниченных в микроскопических объемах.
эВ - явно
дискретные значения энергии. Эффект квантования энергии проявляется только для
тел малой массы, ограниченных в микроскопических объемах.
. Прохождение частицы через
потенциальный барьер
Рассмотрим потенциальный барьер
прямоугольной формы для одномерного движения частицы.
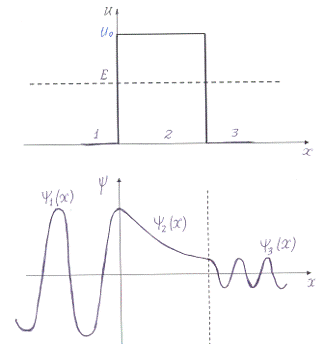
В данной задаче потенциал
описывается выражением
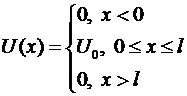
В классической механике частица,
имеющая энергию 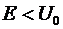 , не может
проникнуть за барьер - она отразится от него. В квантовой механике существует
определенная вероятность проникновения частицы через барьер. Для описания
движения частицы в рамках квантовой механики запишем уравнения Шредингера для
каждой из областей
, не может
проникнуть за барьер - она отразится от него. В квантовой механике существует
определенная вероятность проникновения частицы через барьер. Для описания
движения частицы в рамках квантовой механики запишем уравнения Шредингера для
каждой из областей
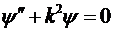 , где
, где 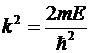
для областей 1 и 3,
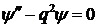 , где
, где 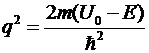
для области 2.
Решая эти уравнения и сшивая
полученные решения на границах, получим выражения для Ψ - функций
во всех областях. Решение показывает, что в области I существуют
падающая и отраженная волны различной амплитуды, в области 3 - существует одна
распространяющаяся волна, а в области 2 функция ψ(x) монотонно
убывает с ростом х. Условный график функции ψ(х) показан на рисунке.
В рамках квантовой механики частица
может проникать через барьер. Это явление называется туннельным эффектом. Для
характеристики туннельного эффекта вводят понятие коэффициента прозрачности.
Коэффициентом прозрачности D называется
отношение квадратов модулей прошедшей и падающей волн
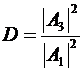 .
.
Коэффициент прозрачности определяет
вероятность прохождения частицы через барьер. Можно показать, что для D
справедливо выражение
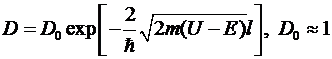 .
.
Туннельный эффект является чисто
квантовым эффектом. Он связан с тем, что в квантовой механике нельзя однозначно
разделить энергию на кинетическую и потенциальную. Кинетическая энергия связана
с импульсом частицы, а потенциальная - с координатами. В силу принципа
неопределенности эти величины не определяются однозначно, поэтому нельзя
утверждать, что внутри барьера частица имеет отрицательную кинетическую
энергию. Соответственно из соотношения 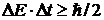 следует, что в течение малых
интервалов времени может нарушаться закон сохранения энергии.
следует, что в течение малых
интервалов времени может нарушаться закон сохранения энергии.
Туннельный эффект играет важную роль
в описании различных процессов, происходящих на атомном уровне. Процессы
радиоактивного распада, термоядерные реакции, многие свойства твердого тела
объясняются существованием туннельного эффекта.
. Атом водорода в квантовой механике
Используя уравнение Шредингера, можно описать
основные свойства атома водорода. Рассмотрим водородоподобный атом, т.е. атом,
состоящий из положительно заряженного ядра и связанного с ним одного электрона.
Это может быть атом водорода Н, однократно ионизованный атом гелия Не+,
двукратно ионизованный атом лития Li++
и др.
Потенциальная энергия взаимодействия ядра с
электроном
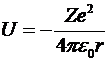 .
.
Графическая зависимость U(r) имеет вид

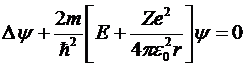 .
.
Это уравнение обычно решают в
сферической системе координат. Опуская математические выкладки, проанализируем
результаты решения уравнения и выводы, которые из него вытекают:
) При положительных значениях
энергии (E > 0)
электрон не связан жестко с ядром, он может удаляться от ядра на бесконечное
расстояние. Значения Е > 0 соответствуют электронам, пролетающим вблизи ядра
и не образующим с ним атом.
) При Е < 0 решения уравнения
Шредингера существуют только для дискретных значений энергии
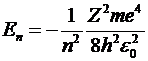 .
.
Эта формула совпадает с аналогичной
формулой, полученной с использованием постулатов Бора. Соответствующие уровни
энергии Еп показаны на графике. Случай E < 0
соответствует электрону, связанному с атомом, т.к. для каждого п значения 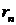 конечные -
это радиус атома.
конечные -
это радиус атома.
Нижний уровень энергии Е1
называется основным, остальные уровни называют возбужденными. При En <0
движение электрона является связанным, при En>0 -
свободным. Энергия ионизации водорода
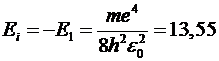 эВ.
эВ.
Это энергия, которая требуется,
чтобы оторвать электрон от атома.
Можно показать, что уравнению
Шредингера для атома водорода в сферических координатах удовлетворяют функции 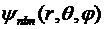 , зависящие
от трех квантовых чисел: n, l и m. Эти числа
определяют положение электрона в атоме и имеют определенный физический смысл.
, зависящие
от трех квантовых чисел: n, l и m. Эти числа
определяют положение электрона в атоме и имеют определенный физический смысл.
Главное квантовое число п определяет
энергетические уровни электрона и принимает значения п=1, 2, 3,…
Орбитальное (азимутальное) квантовое
число l определяет
момент импульса электрона
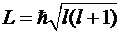 .
.
Параметр l может
принимать значения l = 0, 1, …, п-1. Отсюда следует, что
для каждого состояния п момент импульса электрона может принимать п различных
значений.
Состояния с заданным моментом
импульса обозначаются малыми латинскими буквами:
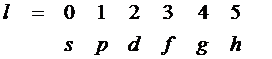
Магнитное квантовое число m определяет
проекцию момента импульса электрона на заданное направление
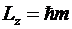 .
.
Параметр 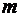 может принимать
значения
может принимать
значения 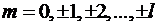 , т.е.
импульс электрона в атоме может принимать 2l+1 различных
ориентаций.
, т.е.
импульс электрона в атоме может принимать 2l+1 различных
ориентаций.
Схематически положения электрона
можно представить с помощью векторной модели.
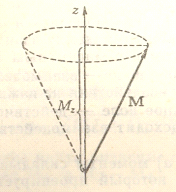
Здесь предполагается, что в точке О
расположено ядро, вокруг которого по круговой орбите вращается электрон. Радиус
орбиты и энергия электрона зависят от главного квантового числа п. Для каждого
п существуют различные формы орбит, которые различаются величиной и направлением
момента импульса 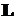 при
различных значениях орбитального квантового числа l. Проекции
момента импульса
при
различных значениях орбитального квантового числа l. Проекции
момента импульса 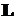 на
выделенную ось z имеют дискретные значения
на
выделенную ось z имеют дискретные значения 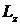 , которые
определяются магнитным квантовым числом
, которые
определяются магнитным квантовым числом 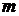 . Итак, состояние электрона
описывается различными ψ-функциями.
Простейшие случаи показаны в таблице
. Итак, состояние электрона
описывается различными ψ-функциями.
Простейшие случаи показаны в таблице
Таблица 1
|
n
|
l
|
m
|
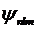 EL EL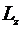
|
|
|
|
|
1
|
0
|
0
|
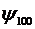 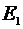 00 00
|
|
|
|
|
2
|
0
|
0
|
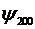 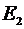 00 00
|
|
|
|
|
1
|
-1
|
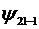 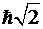 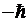
|
|
|
|
|
|
0
|
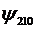 0 0
|
|
|
|
|
|
1
|
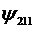 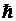
|
|
|
|
Можно показать, что во внешнем магнитном поле,
направленном вдоль оси z,
происходит прецессия орбиты электрона. Следует иметь в виду, что эта схема
условна. На самом деле ни орбит, ни траекторий для электронов не существует, в
частности, они запрещены принципом неопределенности. Правильной является лишь
математическая форма описания, даваемая уравнением Шредингера.
Энергия электрона определяется одним
квантовым числом п, поэтому различным волновым функциям 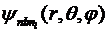 с одним и
тем же значением п, но различными l или ml ,
соответствуют одинаковые значения энергии. Нетрудно посчитать, что для каждого
п существует
с одним и
тем же значением п, но различными l или ml ,
соответствуют одинаковые значения энергии. Нетрудно посчитать, что для каждого
п существует
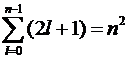
различных ψ -
состояний.
. Состояния электрона в атоме
водорода
Состояние электрона в атоме водорода
определяется четырьмя квантовыми числами: 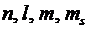 , где
, где 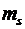 - спиновое квантовое число. Из
уравнения Шредингера наличие спина не вытекает, поэтому мы здесь его не будем
учитывать.
- спиновое квантовое число. Из
уравнения Шредингера наличие спина не вытекает, поэтому мы здесь его не будем
учитывать.
Вероятность появления в данной точке
пространства электрона, обладающего заданными значениями квантовых чисел,
определяется квадратом модуля волновой функции. Положение электрона в атоме
можно представить в виде облака, плотность которого пропорциональна вероятности
появления электрона в данной точке.
В атомной физике, химии,
спектроскопии для описания состояния электрона используются специальные
обозначения:
l=0, s -
состояние, s - электрон;
l=1, p -
состояние, p - электрон;=2, d - состояние,=3, f - состояние.
Значение главного квантового числа
указывается перед условным обозначением орбитального квантового числа.
Например,
запись 2s означает,
что п=2, l=0; запись 3p означает,
что п=3, l=1.
Возможны следующие состояния
электрона:
s
s, 2p
s, 3p, 3d
s, 4p, 4d,
4f
и т.д.
Рассмотрим более детально положения
электронов в различных состояниях. При этом будем использовать упрощенные
представления о движении электронов по заданным орбитам.
Энергия электрона определяется
главным квантовым числом 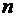 . Можно
считать, что каждому значению энергии соответствует свой радиус орбиты, на
которой располагается электрон. Положение орбиты (ее наклон к выбранной оси
. Можно
считать, что каждому значению энергии соответствует свой радиус орбиты, на
которой располагается электрон. Положение орбиты (ее наклон к выбранной оси 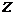 )
определяется квантовыми числами
)
определяется квантовыми числами 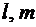 . Рассмотрим простейшие электронные
состояния и соответствующие орбиты.
. Рассмотрим простейшие электронные
состояния и соответствующие орбиты.
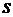 -состояние соответствует значению
-состояние соответствует значению 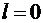 . При этом
магнитное число
. При этом
магнитное число 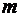 принимает
единственное значение
принимает
единственное значение 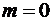 . Можно
показать, что плотность вероятности найти электрон на расстоянии
. Можно
показать, что плотность вероятности найти электрон на расстоянии 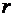 от ядра
является радиально-симметричной и определяется функцией
от ядра
является радиально-симметричной и определяется функцией 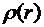 , показанной
на графике.
, показанной
на графике.
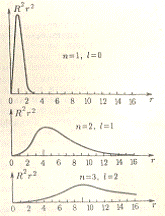
В 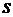 -состоянии области существования
электрона ограничены сферами определенных радиусов (сферически симметричный
слой). С увеличением
-состоянии области существования
электрона ограничены сферами определенных радиусов (сферически симметричный
слой). С увеличением 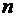 толщина
слоя возрастает.
толщина
слоя возрастает.
р-состояние соответствует значению 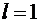 . При этом
магнитное число
. При этом
магнитное число 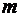 принимает
три значения
принимает
три значения 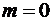 ,
, 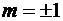 . В этом
случае плотность вероятности найти электрон на расстоянии
. В этом
случае плотность вероятности найти электрон на расстоянии 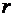 от ядра
зависит от угла
от ядра
зависит от угла 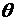 между
выбранной осью z и радиус-вектором и определяется
функцией
между
выбранной осью z и радиус-вектором и определяется
функцией 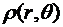 .
.
Если рассматривать электрон
вращающимся по орбите, то можно считать, что электрон обладает моментом
импульса. Для 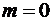 момент
импульса перпендикулярен оси z и его проекция равна нулю. Для
момент
импульса перпендикулярен оси z и его проекция равна нулю. Для 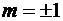 проекции
момента импульса направлены вдоль оси z в различных
направлениях (электрон вращается в различных направлениях).
проекции
момента импульса направлены вдоль оси z в различных
направлениях (электрон вращается в различных направлениях).
Радиальная зависимость определяется
величиной п и соответственно накладывается на угловую зависимость. Т.о. можно
считать, что на заданном расстоянии r существуют
различные орбиты для электрона. Положения этих орбит определяются квантовыми
числами 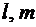 .
.
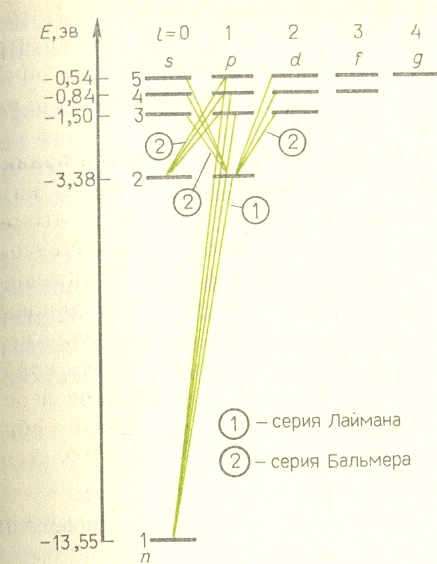
. Излучение атома водорода
Анализ решения уравнения Шредингера
для атома водорода позволяет исследовать спектр излучения водорода. При этом в
рамках квантовой механики удается полностью описать все особенности излучения и
поглощения водорода.
Для атома водорода возможны только
такие переходы, которые удовлетворяют условиям:
1) изменение
орбитального квантового числа удовлетворяет условиям
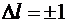 ;
;
1) изменение
магнитного квантового числа удовлетворяет условиям
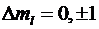 .
.
Соответствующие переходы показаны на
схеме. Отметим, что условие 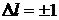 является следствием закона
сохранения момента импульса. Фотон, обладает собственным моментом импульса
(спином) равным
является следствием закона
сохранения момента импульса. Фотон, обладает собственным моментом импульса
(спином) равным 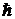 и при
поглощении или излучении фотона момент импульса атома меняется на эту величину.
и при
поглощении или излучении фотона момент импульса атома меняется на эту величину.
Используя введенные ранее
обозначения, можно записать переходы для серии Лаймана
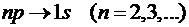 ;
;
серии Бальмера
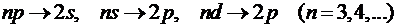
и других серий.
Приведенная схема переходов электронов и
связанные с ней спектры излучения и поглощения справедливы для атома водорода.
Для других химических элементов схема усложняется. Причина усложнения -
взаимодействие электронов, окружающих ядро, с ядром и между собой. При наличии
внешних электрических и магнитных полей характер переходов может измениться,
что приведет к изменению спектров излучения и поглощения.
. Простейшие формулы квантовой механики
1. Соотношение де Бройля 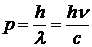 .
.
. Соотношения
неопределенности Гейзенберга
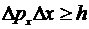 ,
, 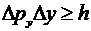 ,
, 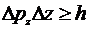 ;
;
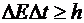 .
.
3. Уравнение Шредингера для стационарных
состояний
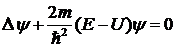 .
.
. Вероятность нахождения
частицы в элементе объема 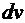
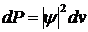 .
.
5. Условие нормировки
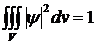 .
.
6. Энергия частицы в потенциальной яме
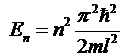 .
.
7. Коэффициент прозрачности
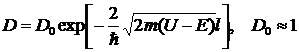 .
.
8. Момент импульса электрона
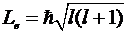 .
.
. Проекция момента импульса
электрона
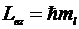 .
.
Список использованной литературы и
источников.
1. Трофимова Т.И. Курс физики, М.:
Высшая школа, 1998, 478 с.
. Трофимова Т.И. Сборник задач по
курсу физики, М.: Высшая школа, 1996, 304 с.
. Волькенштейн В.С. Сборник задач по
общему курсу физики, СПб.: «Специальная литература», 1999, 328 с.
. Трофимова Т.И., Павлова З.Г.
Сборник задач по курсу физики с решениями, М.: Высшая школа, 1999, 592 с.
. Все решения к «Сборнику задач по
общему курсу физики» В.С. Волькенштейн, М.: Аст, 1999, книга 1, 430 с., книга
2, 588 с.
. Красильников О.М. Физика.
Методическое руководство по обработке результатов наблюдений. М.: МИСиС, 2002,
29 с.
7. Супрун И.Т., Абрамова С.С.
Физика. Методические указания по выполнению лабораторных работ, Электросталь:
ЭПИ МИСиС, 2004, 54 с.