Технология катализаторов конверсии монооксида углерода (НТК-4)
Федеральное агентство по образованию
Государственное образовательное
учреждение
Высшего профессионального образования
"НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ
ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ"
Факультет - Институт природных
ресурсов
Направление (специальность) -
химическая технология и биотехнология
Кафедра - общая химическая технология
Технология катализаторов конверсии
монооксида углерода (НТК-4)
Студент гр. О.М. Рюмина
Руководитель, канд. хим. наук Д.А. Горлушко
Томск - 2013г.
Содержание
Введение
1. Технология катализаторов конверсии монооксида углерода
2. Характеристики низкотемпературного катализатора
3. Исходное сырье
4. Метод получения и технологическая схема производства
5. Пассивация катализаторов
6. Условия эксплуатации катализаторов
7. Промышленные катализаторы
8. Восстановление медьсодержащих катализаторов низкотемпературной
конверсии монооксида углерода
Заключение
Список использованной литературы
Введение
Переработка природного газа, состоящего в основном из метана,
является основным промышленным методом получения водорода для использования в
синтезе аммиака, процессах гидрирования нефтепродуктов (гидроочистка,
гидрокрекинг и т.д.) и других органических соединений, а в последнее время в
качестве топлива в экологически чистом производстве энергии на топливных
элементах [1,2]. От способа конверсии метана зависит содержание монооксида
углерода в получаемом водородсодержащем газе. Высококонцентрированный по СО
газ, содержащий СО до 34-30 об. %, получают парциальным окислением метана,
паровая конверсия метана приводит к получению газа с содержанием СО 15-10 об. %
[3].
Реакция паровой конверсии монооксида углерода является
следующей стадией в схеме получения водорода. Реакция протекает с выделением
тепла, степень превращения СО ограничена термодинамическим равновесием, которое
зависит от температуры в слое катализатора. Высокая степень превращения СО
может быть достигнута только при низких температурах, например, остаточное СО
менее 0.3 об. % можно получить только при температурах менее 250° С. Наиболее
распространенным способом осуществления процесса паровой конверсии СО в
промышленности является двухстадийный процесс, в котором превращение СО
проводят последовательно при высоких температурах 350-450° С на малоактивном,
но термостабильном железохромовом катализаторе, и при низких температурах
180-250°С на высокоактивном, но устойчивом только до 300-350° С Cu-Zn-Al (Сг)
оксидном катализаторе [4].
Использование катализаторов, устойчиво и эффективно
работающих в широкой области температур, позволит улучшить показатели процесса.
Для увеличения степени переработки СО широко проводятся
исследования по разработке катализаторов низкотемпературной конверсии (НТК) на
основе медь-цинковой системы, которые будут стабильны при температурах выше
350°С.
В качестве термостабильных катализаторов НТК сообщается о
ряде катализаторов на основе драгоценных металлов и оксидных катализаторов,
содержащих различные металлы. Активность таких катализаторов превышает
активность известных медьцинковых катализаторов только в области температур
выше 250°С. Обещающие результаты получены для катализаторов на основе меди.
Промотирование медь-цинковых катализаторов алюминием, хромом, марганцем,
магнием позволило существенно повысить устойчивость катализаторов при высоких
температурах вплоть до 350°С.
Традиционная двухстадийная схема с использованием
адиабатических реакторов довольно громоздка. Улучшить массогабаритные
характеристики процесса паровой конверсии СО можно проведением процесса в
одностадийном трубчатом реакторе с управляемым температурным профилем вдоль
катализаторного слоя, осуществляемого за счет непрерывного съема тепла. Такая
организация процесса возможна, если использовать катализаторы высокоактивные в
широком температурном интервале. В настоящее время одностадийную схему
предлагается осуществлять организацией нескольких изотермических слоев.
Осуществление одностадийного процесса паровой конверсии СО в
последнее время актуально в связи с созданием энергоустановок на топливных
элементах, использующих в качестве топлива водород, получаемый из
углеводородного сырья. Компактность составляющих стадий энергоустановки
является важным требованием при ее создании.
Исследования медьсодержащих катализаторов с целью расширения
их рабочей температурной области может иметь перспективы для создания
компактного одностадийного реактора паровой конверсии СО.
В улучшении показателей процесса паровой конверсии СО
немаловажную роль может сыграть теплопроводность катализаторного слоя.
Теплопередача по слою катализатора и от поверхности катализатора к стенке
реактора осуществляется посредством реакционного газа. Низкий коэффициент
теплопередачи твердое тело - газ определяет низкую теплопроводность слоя. В
промышленных реакторах теплопроводность катализаторного слоя в радиальном
направлении при загрузке катализатора в виде традиционных таблеток размером 5 х
5 мм или в виде экструдата не высока, что приводит к большим перепадам
температур в радиальном направлении. Известный прием для улучшения теплоотвода
- применение трубчатых реакторов и уменьшение диаметра реактора, но даже при
диаметре трубки 20-30 мм перепад температур в радиальном направлении по сечению
трубки в процессе паровой конверсии СО может достигать 10-20°С [5].
Цель работы
Целью работы является изучение технологии катализаторов
конверсии монооксида углерода, а также подбор состава катализатора
низкотемпературной конверсии, обеспечивающий оптимизацию температурного режима.
1. Технология
катализаторов конверсии монооксида углерода
Конверсия монооксида углерода является составной частью
процесса производства водорода и технологических газов для синтеза аммиака,
спиртов, моторных топлив и других продуктов. Паровая конверсия протекает по
реакции
СО + Н2О↔СО2+Н2+41кДж/моль.
(1.1)
В условиях промышленного осуществления процесса кроме реакции
(1.1) возможно протекание побочных реакций, из которых наиболее
термодинамически вероятными являются:
2СО↔С + СО2+172,5кДж /
моль, (1.2)
СО + 3Н2↔СН4 + Н2О
+ 206,4кДж / моль. (1.3)
Реакция конверсии СО в отсутствии катализаторов при температурах
до 600° С, так же как и реакции (1.2) и (1.3), практически не протекает.
Значительно увеличить скорость основной реакции (1.1) позволяет применение
катализаторов, а температура процесса определяется их активностью. Неполный ряд
активности металлов и оксидов металлов в отношении реакции (1.1) можно
представить в следующем виде:
Pt, Pd > Ag > MgO, Co2O4,
CuO > NiO > Fe2O3>Cr2O3>
V2O5 > ZnO
Используемые катализаторы кроме высокой активности должны обладать
селективными свойствами, характеризующимися умеренной гидрирующей функцией [5].
Это необходимо для достижения соответствующих скоростей реакций без заметного
метанообразования (1.3), которое в значительной степени катализируют кобальт и
металлическое железо, образующееся в результате перевосстановления оксидного
железосодержащего катализатора при недостатке в реакционной смеси водяного
пара. Кроме селективности, катализатор должен обладать высокой стабильностью в
реакционной среде и минимальной стоимостью, что ограничивает применение
различных веществ до соединений Cu, Fe, Cr, Zn.
В промышленности процесс конверсии монооксида углерода на
катализаторах осуществляется в интервале температур 200-450°С и давлении
0,1-3,0 МПа.
В зависимости от температурных условий работы различают
среднетемпературные (СТК) и низкотемпературные (НТК) катализаторы. С целью
обеспечения более высокой степени превращения и снижения остаточного содержания
монооксида углерода в газе процесс, как правило, проводят в две ступени: первая
- среднетемпературная конверсия на катализаторах СТК, на второй используются
низкотемпературные катализаторы серии НТК.
2.
Характеристики низкотемпературного катализатора
С целью обеспечения более высокой степени превращения и
снижения остаточного содержания монооксида углерода в газе в качестве контактов
второй ступени конверсии СО в крупнотоннажных агрегатах синтеза аммиака
используются низкотемпературные катализаторы серии НТК, содержащие оксиды меди,
цинка, алюминия и хрома.
Характеристики катализатора НТК-4 приведены в табл. 1 [6].
Таблица 1
Характеристики катализатора НТК-4
|
Показатель
|
Значение
показателя
|
|
Внешний вид
|
Таблетки
цилиндрической формы черного цвета
|
|
Размер
таблеток, мм Диаметр, высота
|
5-6 5-4
|
|
Содержание, %
мас.: CuO
|
51,0-57,0
|
|
Cr2O3
|
12,5-15,5
|
|
ZnO
|
9,5-12,5
|
|
Al2O3
|
17,6-21,6
|
|
Плотность
насыпная, г/см
|
1,5-1,6
|
|
Механическая
прочность (разрушающее усилие на торец), МПа
|
28
|
|
Удельная
площадь поверхности, м /г
|
|
Объем пор, % не
менее
|
35-40
|
3. Исходное
сырье
Для приготовления контактной массы НТК используются следующие
основные виды сырья [6]:
Хромовый ангидрид - Cr2O3.
Оксид цинка - ZnO.
Гидроксид алюминия - Al (OH) 3.
Гидроксокарбонат меди (малахит) - CuCO3∙Cu (OH) 2.
Графит марки С1 или С2.
4. Метод
получения и технологическая схема производства
Катализатор получают методом механического смешения исходных
компонентов по "мокрому" способу [6].
Последовательность производственных стадий приготовления
контактной массы НТК-4 можно представить следующим образом:
• приготовление рабочих растворов и суспензий;
• смешение исходных составляющих;
• термообработка (сушка и прокаливание) катализаторной массы;
• смешение прокаленной контактной массы с раствором бихромата
меди и графитом;
• таблетирование контактной массы;
• восстановление катализатора.
Технологическая схема производства катализатора НТК-4
приведена на рис. 1.
Приготовление рабочих растворов и суспензий. В реактор (1)
предварительно заливается конденсат, и при включенной мешалке загружается оксид
цинка. Водная суспензия оксида цинка перемешивается в течение 22 ч, затем
центробежным насосом (2) подается в мерник (3), из которого дозируется в
реактор (4).
Растворение хромового ангидрида производится в специальном
аппарате (5). Полученный раствор хромовой кислоты насосом (6) перекачивается в
реактор (7), где конденсатом доводиться до нужной концентрации, а затем
перекачивается в мерник (8), откуда он дозируется в реактор (9). В реакторе
раствор подогревается до температуры 80-90°С.
Смешение исходных составляющих. Вакуум-пневмотранспортом
гидроксид алюминия подается в циклон-разгрузитель (10), из которого через
емкость-бункер (11) питателем (12) загружается в бункер, установленный на
платформенных весах (13). Здесь отвешивается определенная порция Al (OН) 3 и
подается в реактор (9). В нем масса перемешивается в течение 2 ч и выгружается
в реактор (4).
катализатор конверсия монооксид углерод
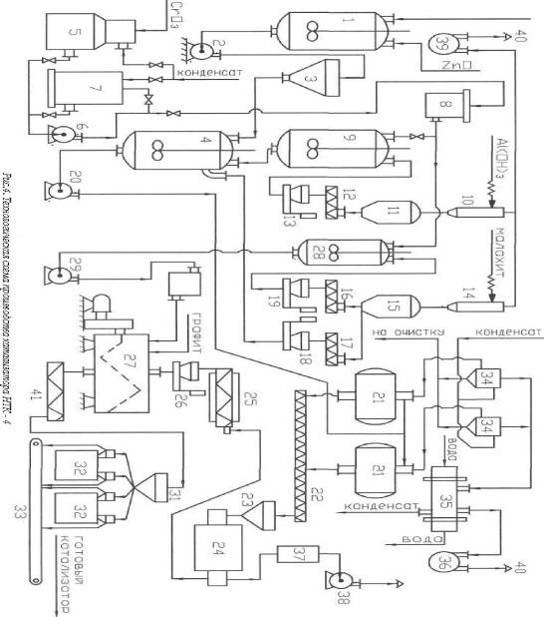
Спецификация к рис.1.1, 4, 7, 28 - реакторы; 2, 6, 20, 29 -
центробежные насосы; 3 - мерник суспензии оксида цинка; 5 - аппарат для
растворения CrO3; 8, 30 - мерники; 9 - реактор смешения; 10, 14 -
циклоны-разгрузители; 11, 15 - емкости-бункеры; 12, 16, 17 - шнековые питатели;
13, 18, 19, 26 - платформенные весы; 21 - вакуум-гребковые сушилки; 22, 24, 41
- шнеки транспортные; 23 - бункер с вибратором; 24 - электропечь; 25 -
охлаждаемый шнек; 27 - смеситель; 31 - бункер-уплотнитель; 32 - таблетмашина;
33 - ленточный конвейер; 34 - мокрый пылеуловитель; 35 - конденсатор; 36, 39 -
вакуум-насосы; 37 - фильтр рукавный; 38 - центробежный вентилятор; 40 -
выхлопная труба.
- Измельченный малахит вакуум-пневмотранспортом через циклон -
разгрузитель (14) подается в емкость-бункер (15), оттуда питателем (17)
направляется в бункер платформенных весов (18). Отвешенное количество малахита
небольшими порциями питателем загружается в реактор (4).
- Масса в реакторе (4) перемешивается в течение 2 ч при
температуре 80-90°С. При этом в реакторе протекает реакция с выделением
диоксида углерода
3Cu2CO3 (OH) 2+2H2CrO4=2
[CuCrO4-2CuO-2H2O] +3CO2+H2O.
- Термообработка (сушка и прокаливание) катализаторной массы.
Готовая катализаторная масса насосом (20) подается в вакуум - гребковые сушилки
(21), где сушится в течение 12-16 ч при остаточном давлении 500 мм рт. ст. с
постепенным подъемом температуры до 100-120°С. Высушенная катализаторная масса
с влажностью 10 % мас. транспортным шнеком (22) подается в бункер с вибратором
(23), из которого непрерывно загружается в прокалочную электропечь (24).
Прокаливание проводится при t=450-500°С в течение 6-8 ч и сопровождается следующими
реакциями:
2Al (OH) 3→Al2O3+3H2O,3
∙ Cu (OH) 2→2CuO+CO2+H2O,
[CuCrO4∙2CuO∙2H2O]
→Cr2O3+6CuO+1,5O2+4H2O.
Образующаяся в процессе сушки в вакуум-гребковых сушилках
(21) паровоздушная смесь проходит мокрые пылеуловители (34), конденсатор (35),
где конденсируются пары воды, а воздух вакуум - насосом (36) выбрасывается
через выхлопную трубу (40) в атмосферу. Конденсат сокового пара из конденсатора
(35) собирается и направляется далее в реактор (1) на приготовление суспензии
оксида цинка, в аппарат (5) и реактор (7) для приготовления раствора хромовой
кислоты.
Промывная вода из мокрых пылеуловителей (34), содержащая пыль
катализаторной массы, собирается в сборник (на схеме не показан), где
отстаивается. Осветленная часть промывных вод вновь направляется на орошение
мокрых пылеуловителей (34). Сгущенная масса из сборника направляется в реактор
(4).
Реакционные газы после прокалочной электропечи (24)
разбавляются воздухом до t=200-250°С, очищаются в рукавном фильтре из стеклоткани (37)
и вентилятором (38) выбрасываются через трубу (40) в атмосферу, предварительно
разбавленные воздухом до t=80°С. Разрежение в циклонах-разгрузителях (10, 14) создается
вакуум - насосом (39).
Смешение прокаленной контактной массы с раствором бихромата
меди и графитом. Прокаленная катализаторная масса через охлаждаемый шнек (25)
подается в дозировочный бункер, установленный на платформенных весах (26), где
взвешивается и ссыпается в смеситель (27). Сюда же загружается графит и
заливается отмеренное количество раствора бихромата меди, который готовится в
реакторе (28). В этом реакторе хромовая кислота, залитая из мерника (8),
растворяет небольшие порции малахита, подаваемые из емкости - бункера (15)
питателем (16) через бункер платформенных весов (19). Растворение малахита в
хромовой кислоте протекает при t=70-80°С в течение одного часа по реакции
Cu2CO3 (OH) 2+4H2CrO4=2
[CuCr2O7∙2H2O] +CO2+H2O.
Таблетирование контактной массы. Готовый раствор насосом (29)
перекачивается в мерник (30), из которого заливается в смеситель (27). Масса в
смесителе перемешивается в течение 10-15 мин и выгружается через транспортный
шнек (41) в бункер-уплотнитель (31), где уплотняется и направляется на
таблетирование в таблетмашины (32). Таблетки катализатора с ленточного
конвейера (33) засыпаются в барабаны, которые направляются на склад готовой
продукции.
Восстановление катализатора. Свежеприготовленная контактная
масса содержит в своем составе оксиды металлов, однако каталитическую
активность проявляет металлическая медь. С целью активации катализатора его
восстановление проводится в реакторе периодического действия или промышленном
конверторе при атмосферном давлении. В качестве восстанавливающего агента
используется азотоводородная смесь (АВС). Восстановление протекает по реакции:
CuO+H2=Cu+H2O.
Условия выбираются таким образом, чтобы оксиды других
металлов не восстанавливались. Процесс восстановления в промышленном агрегате
подразделяется на следующие стадии [6]:
. Разогрев катализатора циркулирующим азотом до 180-200°С со
скоростью 30°С/ч.
2. Начальный период восстановления при концентрации водорода в
АВС ~ 0,3 % об. Время восстановления 3-4 ч.
3. Увеличение содержания водорода в АВС до 1,0-1,2 % об. и
температуры до 230°С в течение 3-4 ч. Восстановление катализатора при этих
условиях 5-6 ч.
4. Увеличение концентрации водорода в АВС до 4-5 % об. Выдержка
катализатора 3-4 ч.
5. Увеличение концентрации водорода в АВС до 10-20 % об. и
выдержка катализатора в течение 3 ч для достижения полного восстановления.
Процесс восстановления катализатора на месте его производства
проводится в несколько стадий, а именно: загрузка, продувка, разогрев
катализатора, восстановление, охлаждение, пассивация, вновь охлаждение и
выгрузка катализатора. На все операции затрачивается около 86 ч. На рис.2
приведена схема восстановления катализатора в реакторе периодического действия.
Чистый азот после газодувки (4) проходит теплообменник -
рекуператор (5), где подогревается отходящими газами до t=190°С, и поступает в
электроподогреватель (6) для подогрева до t=240°С. Подогретый газ
направляется в колонну (1) для разогрева катализатора, который продолжается в
течение 4-5 ч, после чего начинается восстановление. Для восстановления в
циркулирующий газ дозируются азотоводородная смесь или водород таким образом,
чтобы концентрация водорода постепенно повышалась и достигала ~ 8 % об.
Отработанный газ проходит циклоны (2) и направляется в
теплообменник (5) для рекуперации тепла. Затем газ охлаждается до t=35°С в холодильнике (3),
проходит влагоотделитель (7) и поступает снова на вход газодувок (4).
Восстановление считается законченным, когда начинается
медленное снижение температуры контакта, и состав восстанавливающего газа до и
после слоя катализатора остается постоянным.
Восстановленный катализатор охлаждают до t=50°С чистым
циркулирующим по схеме азотом в течение 6 ч.
5. Пассивация
катализаторов
Восстановленный катализатор марки НТК пирофорен и перед
выгрузкой из реактора он должен быть частично окислен. Целью этой операции
является поверхностная пассивация - окисление восстановленных элементов,
находящихся в непосредственной близости от поверхности, кислородом воздуха [6].
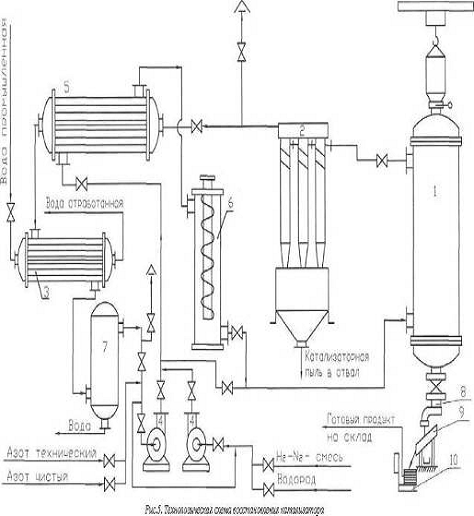
Спецификация к рис. 2.1 - колонна восстановления; 2 - группа
их 3-х циклонов; 3 - холодильник; 4 - газодувки; 5 - теплообменник-рекуператор;
6 - электроподогреватель; 7 - влагоотделитель; 8 - течка; 9 - бункер рассева;
10 - платформенные весы.
Окисление железохромовых и медьсодержащих катализаторов
осуществляется по реакциям:
Fe3O4+O2=6 Fe2O3+Q,
Cu+O2=2CuO+Q
и сопровождается выделением значительного количества тепла.
Пассивация НТК, восстановленного в реакторе периодического действия,
производится непосредственно в том же реакторе кислородом, присутствующим в
техническом азоте, дозируемым в чистый азот. Концентрация кислорода постепенно
увеличивается от 0,1 до 3,0 % об. Продолжительность пассивации составляет 20
час. Условия пассивации низкотемпературных катализаторов приведены в табл.2.
Таблица 2
Условия пассивации катализаторов
|
Параметры
процесса
|
Катализатор
|
|
НТК
|
|
Температура
охлаждения катализатора циркулирующим азотом,°С
|
100-120
|
|
Содержание
кислорода в циркулирующем азоте, % об.
|
0,1-3,0
|
|
Температура
пассивации,°С
|
<230
|
|
Температура
охлаждения после пассивации,°С
|
50
|
При параметрах, указанных в табл.2, окисляется до 20 %
восстановленных центров поверхности. Восстановленные и запассивированные
катализаторы охлаждаются до 50°С и по течке (8) направляются в бункер рассева
(9), где отделяется пыль. Упаковка в герметичные барабаны осуществляется на
платформенных весах (10). В случае проведения процесса восстановления контактов
в промышленных конверторах пассивация катализаторов не проводится. Конверторы
постепенно переводятся на рабочий режим.
Таблица 3
Основные эксплуатационные показатели катализатора НТК
|
Показатель
|
Катализатор
|
|
СТК
|
НТК
|
|
Температура,°C
|
|
|
|
максимально
возможная на входе в слой
|
|
|
|
катализатора,
|
320
|
190-200
|
|
максимально
допустимая в слое
|
|
|
|
катализатора
|
520
|
250-280
|
|
Объемная
скорость, ч-1
|
2500-3000
|
2000-5000
|
|
Соотношение
пар: газ
|
0,4-1,5
|
0,5-0,7
|
|
Степень
превращения СО, %
|
до 95
|
90-98
|
|
Срок службы
катализатора, годы
|
2-8
|
2-5
|
Несмотря на то, что медьсодержащие контакты (НТК) активны при
низких температурах (200-280°С), катализаторы СТК имеют более продолжительный
срок службы. Это объясняется их меньшей чувствительностью к контактным ядам и
процессам рекристаллизации при увеличении температуры.
7.
Промышленные катализаторы
В настоящее время отечественные производители наладили выпуск
катализаторов с более продолжительным сроком эксплуатации. К таким
катализаторам относятся НТК-4У, НТК-10А и НТК-8. Катализатор НТК-4У применяется
для проведения каталитического процесса конверсии моноксида углерода с водяным
паром при температуре 200-300°C, давлении до 3,0 МПа, соотношении пар: газ, равном 0,4-0,8,
объемной скорости 2000-3000 ч-1 по сухому конвертированному газу,
объемной доле СО в исходном газе не более 2,0-3,5 %. Он обеспечивает остаточное
содержание моноксида углерода в конвертированном газе не более 0,5 % об.
Катализатор состоит в основном из оксидов меди (CuO), цинка (ZnO), алюминия (Al2O3), хрома (Cr2O3) и выпускается в виде
цилиндрических гранул (таблеток) [6].
Катализатор НТК-8 является наиболее эффективным из
катализаторов подобного типа. Например, по сравнению с НТК-4, его активность и
стабильность выше в 2-3 раза. Кроме того, катализатор способен сохранять свою активность
после перегревов в реакционной среде до 550°С (против 400-450°С у НТК-4).
Большим преимуществом НТК-8 является его бифункциональная способность [6]:
• ускорять реакцию конверсии монооксида углерода с водяным
паром, начиная с 200°С;
• поглощать каталитические яды своим лобовым слоем, предохраняя
от отравления основную массу катализатора, значительно удлиняя срок его службы.
НТК-10А (медьцинкалюминиевый) используется в технологической
линии синтеза аммиака в агрегате с единичной мощностью 3 тыс. тонн/сут для
процессов средне - и низкотемпературной конверсии моноксида углерода водяным
паром. НТК-10А по своим основным показателям - активности, стабильности,
пористости, насыпной плотности превосходит катализатор НТК-4.
Можно отметить новые модификации катализаторов
низкотемпературной конверсии моноксида углерода, обладающие повышенной
активностью, разработанные Новомосковским институтом азотной промышленности, -
НТК-10-2ФМ и НТК-10-2ЛФ. Оптимальный режим восстановления катализаторов
предусматривает его активацию в течение 32-36 ч.
Выпускают также трех - и четырехкомпонентные катализаторы
конверсии моноксида углерода: медьцинкалюминиевый марки ГСНК-2 и
медьцинкалюмокальциевый марки КСО-С.
Катализатор СТА используют вместо катализатора СТК. По своим
свойствам он близок к катализатору НТК-8, в том числе обладает бифункциональной
способностью: сохраняет свою активность после перегревов в реакционной среде до
600°С.
Использование пары катализаторов СТА-НТК-8 в аммиачных
агрегатах вместо СТК-НТК-4 позволяет в течение 4-5 лет без перегрузки получать
остаточное содержание моноксида углерода 0,1 - 0,2 % об. (вместо 0,4 % об. при
использовании НТК-4 и СТК, срок службы которых около 2-х и 4-х лет,
соответственно) и экономить при этом 20-30 м3 природного газа на 1
тонну аммиака.
8.
Восстановление медьсодержащих катализаторов низкотемпературной конверсии
монооксида углерода
Перед эксплуатацией низкотемпературный катализатор подвергают
восстановлению, которое сопровождается выделением большого количества тепла
(1050 кДж/кг катализатора). В связи с этим газ-восстановитель разбавляют
инертным газом. В качестве восстановителя чаще всего применяют азотоводородную
смесь. Для разбавления (понижения концентрации восстановителя) используют
преимущественно азот с минимальным содержанием примесей. Для уменьшения расхода
азота осуществляется его циркуляция. Условно, применительно к промышленным
агрегатам, процесс можно разбить на 4 этапа [7]:
. Разогрев катализатора циркулирующим азотом со скоростью 30 0С/ч
до температуры в лобовом слое катализатора 200 0С, а в последнем по
ходу газа - не менее 180 0С.
. Начальный период восстановления при максимальной циркуляции
азота (объемная скорость 200-250 ч-1) и дозировке АВС в него в таком
количестве, чтобы концентрация водорода была не более 0,3 % об. Постепенно, в
течение 2-3 ч увеличивают содержание водорода в циркулирующем азоте со
скоростью 0,2-0,3 % об. в ч и доводят до 1,0-1,2 % об. при температуре не выше
230 0С.
. Восстановление катализатора во всем объеме при концентрации
водорода в азоте 1,0-1,2 % об. и температуре до 230 0С.
. Увеличение содержания водорода до 4-5 % об. Выдержка
катализатора 3-4 ч. Затем содержание водорода увеличивается до 10-20% об.
Выдержка составляет 3 ч для достижения полного восстановления катализатора.
Исследованиями установлено, что при восстановлении
катализаторов НТК значительная часть меди восстанавливается до металлической,
которая находится или в рентгеноаморфном, или в мелкодисперсном состоянии.
Небольшая часть остается в частично восстановленной форме одновалентной меди.
Практически такие же режимы для восстановления катализаторов
среднетемпературной и низкотемпературной конверсии СО используют на
катализаторных фабриках, с той лишь разницей, что для проведения процессов
используют не промышленные агрегаты, а реакторы периодического действия, в
которые загружают катализатор.
Восстановленный низкотемпературный катализатор конверсии СО
пирофорен, поэтому перед выгрузкой из контактного аппарата после отработки
срока эксплуатации он должен быть окислен. Процессы окисления НТК в
промышленных реакторах имеют ряд общих стадий, но различаются технологическими
режимами.
Для окисления катализатора НТК применяют схему, используемую
для восстановления, и проводят окисление воздухом, дозируемым в циркулирующий
азот.
Условно процесс окисления представляет собой следующую
последовательность этапов [7]:
. Охлаждение катализатора до 100-120 0С
циркулирующим азотом.
. Окисление катализатора воздухом, дозируемым в циркулирующий
азот в количестве 1 % об.; при этом не допускается подъем температуры выше 230 0С.
В случае повышения температуры прекращают подачу воздуха в систему.
. Завершение процесса окисления (после выравнивания
температуры на входе и в слоях катализатора) путем постепенного увеличения
концентрации кислорода в циркулирующем азоте до 10 % об.
. Охлаждение катализатора воздухом до 50 0С.
Восстановленный на катализаторной фабрике катализатор перед
выгрузкой окисляют только частично с целью устранения возможности
самовоспламенения во время транспортировки и перегрузки. Для этого окисляют
только часть поверхности катализатора кислородом, содержащимся в техническом
азоте. Последний в необходимом количестве дозируют в чистый азот. При этом
окислению подвергается примерно 20 % поверхности от общего количества. Такой процесс
называется пассивацией. Концентрация кислорода в газе в процессе пассивации
увеличивается от 0,1 до 3,0 % об. при объемной скорости 1000 ч-1.
Продолжительность пассивации составляет около 20 ч. Восстановленный и
запассивированный катализатор охлаждают до 30 С чистым азотом и упаковывают в
герметичные стальные барабаны, внутренняя поверхность которых окрашивается
бесцветным бакелитовым лаком.
Заключение
Реакция конверсии монооксида углерода привлекает повышенное
внимание как в отношении катализаторов, так и в отношении технологии процесса,
благодаря потребности в чистом водороде как в традиционных промышленных схемах,
например, синтеза аммиака, процессов гидрирования, так и в качестве топлива для
топливных элементов, используемых в транспортных средствах и в стационарных
энергетических установках. Глубина протекания реакции паровой конверсии СО
ограничена термодинамическим равновесием, поэтому состав выходящего газа
определяется в значительной степени температурой процесса. В промышленности
процесс осуществляется в две стадии: среднетемпературной СТК (330-500°С) и
низкотемпературной НТК (180-240°С). Традиционно, на стадии СТК используется
малоактивный в области низких температур, но устойчивый при высоких
температурах, Fe-Cr катализатор; на стадии НТК используется Cu-Zn-Al
катализатор, обладающий высокой активностью в области температур до 300°С, но
низкой термостабильностью в области температур выше 350°С. Хотя требуемое
низкое содержание СО на выходе после конвертора СО определяется условиями
осуществления стадии НТК, показатели стадии СТК в значительной степени
определяют эффективность процесса в целом. Традиционная схема проведения
процесса паровой конверсии СО в две стадии является громоздкой.
Для улучшения массогабаритных характеристик реактора паровой
конверсии СО в литературе рассматриваются варианты проведения процесса по
одностадийной схеме.
Одностадийную схему проведения процесса в настоящее время
предполагается осуществлять на традиционных катализаторах, но повышение
эффективности процесса, в частности в результате создания компактных аппаратов,
может быть достигнуто разработкой высокоактивных катализаторов, способных
работать в широкой области температур.
В направлении получения термостабильного катализатора
процесса низкотемпературной паровой конверсии СО сообщается, что получен ряд
катализаторов на основе драгоценных металлов и оксидных катализаторов,
содержащих переходные металлы. Однако эти катализаторы по своей активности
превышают активность известных Cu-Zn катализаторов только в области температур
выше 250°С. Катализаторы на основе драгоценных металлов имеют очень высокую
стоимость.
Список
использованной литературы
1.
М.К. Письмен, Производство водорода в нефтеперерабатывающей промышленности.
Москва "Химия" - 1976.
.
Производство технологического газа для синтеза аммиака и метанола из
углеводородных газов. /Под ред.А.Г. Лейбуш.М., Химия, 1971 - 286с.
.
Справочник азотчика. 2-е изд. перераб., М.: Химия, (1986) 512с.
.
Катализаторы, применяемые в азотной промышленности. Каталог/ Под общ. ред.А.М.
Алексеева. Черкассы, НИИТЭхим. 1979-23с.
.
Г.К. Боресков, Гетерогенный катализ. Москва "Наука" (1988).
.
Технология катализаторов. Часть I. Методы приготовления катализаторов: учебное
пособие / В.В. Коробочкин, Д.А. Горлушко. - Томск: Изд-во Томского
политехнического университета, 2013. - 85 с.
.
Технология катализаторов. Часть II. Технологические схемы приготовления
промышленных катализаторов: учебное пособие/В.В. Коробочкин, Д.А. Горлушко. -
Томск: Изд-во Томского политехнического университета, 2013. - 90 с.