Изменения окислительно-восстановительного потенциала среды
Изменения
окислительно-восстановительного потенциала среды культивирования устойчивой к
тяжелым металлам бактерии Pseudomonas diminuta: взаимосвязь с выделением
из клеток металлотионеинподобных белков
Особое положение тяжелых
металлов (ТМ) среди загрязнителей связано как с возможностью их накопления
организмами и передачи по пищевым цепям, так и с высокой токсичностью (Reddy,
Prasad, 1990). Воздействие ТМ прежде всего сказывается на первичных продуцентах
- микроводорослях и цианобактериях, которые наравне с гетеротрофными
микроорганизмами могут использоваться для детоксикации и извлечения ценных
металлов, поскольку способны аккумулировать их из водной среды и донных отложений
в количестве, многократно превышающем потребность в них, как в компонентах
минерального питания (Nagase et al., 1994). Наибольшей устойчивостью к ТМ
отличаются микроорганизмы, выделенные в местах, содержащих промышленные
загрязнения, либо месторождения соответствующего металла (Горленко и др.,
1977).
Ванадий, как один из
широко распространенных ТМ, используется зелеными, желто-зелеными и бурыми
водорослями, содержится в альтернативных нитрогеназах некоторых почвенных
бактерий, но не является необходимым элементом для развития большинства
прокариотных микроорганизмов, среди которых наиболее активными
биоаккумуляторами ванадия являются бактерии рода Pseudomonas, а также
ряд цианобактерий (Rehder, 1991). Его токсический эффект обусловлен главным
образом тем, что восстанавливаясь в клетках, он стимулирует образование
свободнорадикальных состояний О2 (Popper et al., 1991).
Ионы ТМ образуют
меркаптиды с SH-группами тиоловых соединений клеток: реакция обратима, но
равновесие ее смещено в сторону слабодиссоциирующих металлтиолатов (Торчинский,
1977). Устойчивость фототрофных и других микроорганизмов к действию ТМ в
наибольшей степени обусловлена специфическим связыванием основной части
поглощенных клетками ТМ смежными остатками цистеина в молекуле специализированных
белков - металлотионеинов (МТ). Общим для этих белков является молекулярная
масса до 10 кДа и высокое содержание тиоловых групп. В спектре оптического
поглощения МТ в УФ-области около 250 нм, наблюдаются типичные для
металлтиолатных комплексов шиpокие полосы, которые исчезают пpи удалении
металла (Ang, Wong, 1992). Цианобактерии, культивируемые в присутствии высоких
концентраций ванадата синтезируют связывающий ионы металла МТ второго класса
(Саванина и др., 1995).
В настоящей работе
установлена корреляция между зависимым от ванадата накоплением в среде
культивирования бактерий Ps. diminuta низкомолекулярных, богатых
SH-группами белков и изменениями окислительно-восстановительного потенциала (Eh)
среды.
Материалы
и методы
В работе использовали
гетеротрофные бактерии, выделенные из придонного осадка ванадийсодержащего
промышленного водоема и идентифицированные нами как Ps. diminuta
(Саванина и др., 1998). Бактерии культивировали при температуре 25-27° в
конических колбах на среде, содержащей в 100 мл водопроводной воды глюкозу и
пептон в концентрации по 1 г/л (pH 7,2).
Для определения в
культуральной жидкости Ps. diminuta содержания низкомолекулярных белков
и SH-групп пробы диализовали 24 час при 0о против 50 мМ Трис-HCl буфера, pH
7,6, включающего 10 мМ ЭДТА с использованием мембраны фирмы Serva (Германия) с
диаметром пор, пропускающих молекулы массой <10-15 кД. В присутствии ЭДТА,
сульфгидрильные группы МТ и других SH-содержащих соединений освобождаются от
большей части связанного ванадия и становятся реакционноспособными.
Плотность клеточных
суспензий определяли нефелометрически при 540 нм на спектрофотометре фирмы
Hitachi (Япония), модель U-2000. Для определения концентрации ванадия в
биологическом материале и культуральной жидкости использовали цветную реакцию
ванадия с 4-(2-пиридилазо)-резорцином. Клетки предварительно трижды отмывали от
среды культивирования и озоляли азотной кислотой. Оптическую плотность измеряли
на том же спектрофотометре при 520 нм используя коэффициент молярной экстинкции
24500 М-1см-1. Содержание диализованных
низкомолекулярных белков определяли по Лоури (Lowry et al., 1951). Концентрацию
тиоловых групп в этих белках и других соединениях определяли с реактивом Элмана
(5,5'-дитиобис(2-нитробензойная) кислота) в присутствии ЭДТА (Веревкина и др.,
1977) и регистрировали при длине волны 412 нм на том же спектрофотометре
используя коэффициент молярной экстикции 11400 М-1см-1.
Величины pH и Eh среды култивирования измеряли на электрометре фирмы
Cole-Parmer (США), модель DigipHase, pH определяли с помощью комбинированного
стеклянного электрода с двойным Ag/AgCl электродом сравнения фирмы Radiometer
(Голландия); для определения Eh использовали Pt-электрод, а в
качестве электрода сравнения - Ag/AgCl (оба электрода Российского
производства); потенциал электрода сравнения относительно нормального
водородного электрода, измеренный как в работе (Barsky, Samuilov, 1979),
составляет 225±10 мВ. Таким образом, истинная величина Eh среды
представляет собой сумму измеряемой величины Eh и потенциала электрода
сравнения.
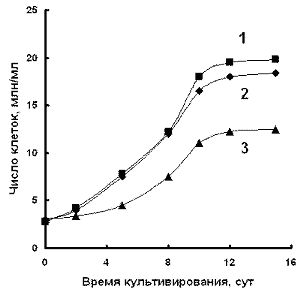
Рис.
1. Эффект ванадата на рост культуры Ps. diminuta; 1 - контроль; 2, 3 - в
присутствии 100 и 700 мг/л ванадата соответственно.
Результаты
и их обсуждение
Клетки Ps. diminuta,
изолированные из пробы придонного осадка промышленного водоема, сбросовые воды
которого содержат как отходы металлургического производства ванадий в
концентрации 100-700 мг/л, хорошо растут как без ванадата, так и в его
присутствии; при этом максимальное количество клеток бактерий достигает 2x107
кл/мл среды через 12-16 суток культивирования (рис. 1). Ванадат в концентрации
700 мг/л снижает накопление биомассы Ps. diminuta на 30-40%. В
дальнейших опытах ванадат добавляли в концентрации 100 мг/л, поскольку не
оказывая заметного влияния на рост бактерий, ванадат в этой концентрации
значительно стимулировал выделение из клеток низкомолекулярных белков.
Применение метода
диализного (смешанно-раздельного) культивирования фототрофных микроорганизмов -
цианобактерий или микроводорослей с гетеротрофными бактериями рода Pseudomonas
(Гусев и др., 1988) позволило выявить ряд закономерностей роста двух различных культур,
разделенных полупроницаемой мембраной. При культивировании фототрофного
компонента в присутствии ванадата клетки активно выделяют в среду углеводы и
гликолат. Эти соединения используются для роста гетеротрофным компонентом в
качестве субстратов окисления. При этом бактерии эффективно поглощают ванадат,
существенно снижая его концентрацию в среде (Саванина и др., 1994; Гусев и др.,
1997).
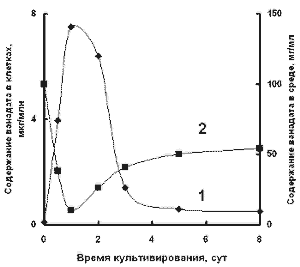
Рис.
2. Содержание ванадата в клетках (1) и в среде (2) в зависимости от возраста
культуры Ps. diminuta.
Действительно, как
показывают наши опыты содержание ванадата в клетках Ps. diminuta, в
течение первых 2 суток культивирования быстро увеличивается от 0 до 5-6 мкг/млн
клеток, а затем снижается приблизительно в 10 раз (рис. 2, кривая 1). Иная
картина наблюдается относительно концентрации ванадата в культуральной
жидкости. За первые двое суток культивирования Ps. diminuta содержание
ванадата в среде падает от 100 до 10-12 мг/л, а затем начинает постепенно
увеличиваться по мере развития культуры; причем в среду возвращается до 60%
ванадата (рис. 2, кривая 2). Как видно, накопление ионов ванадия в клетках коррелирует
c его содержанием в культуральной жидкости: увеличение концентрации ванадата в
клетках сопровождается ее снижением в среде культивирования и наоборот.
Столь значительное
увеличение концентрации ванадата в среде по мере выхода кривой роста на стационарный
уровень может быть обусловлено тем, что ванадат выделяется из нативных и
разрушенных клеток вместе с компонентами связывающими металл. Такими
компонентами прежде всего являются низкомолекулярные богатые SH-группами белки;
могут быть и другие тиоловые соединения, к которым относятся глутатион,
цистеин, тиогликолевая кислота, дитиоэтанол, дитиопропанол и т.д.
Известно, что
специфическую устойчивость фототрофных микроорганизмов к действию ТМ
обеспечивает наличие в клетках SH-содержащих белков с мол. м. до 10 кДа,
связывающих большую часть поглощенных клетками ТМ (Obata et al., 1994).
Содержание низкомолекулярных белков и коррелирующее с ним содержание SH-групп в
клетках цианобактерий возрастает под действием ванадата (Лебедева и др., 1993).
Выделенный из клеток Anacystis nidulans белок был идентифицирован как МТ II
класса, связывающий ванадий (Саванина и др., 1995). Известно, что МТ
большинства прокариот как правило состоят из одной полипептидной цепи с мол. м.
до 7-10 кДа и высоким содержанием цистеина (в среднем до 30%) (Kagi, 1993).
Клетки Ps. fluorescens выделяют в среду связывающие ионы Zn полипептиды
с мол. м. 1-3,5 кДа. (Appana, Whitmore, 1995). Поскольку клетки Ps. diminuta
выделены из ванадийсодержащего промышленного водоема и по данным рис. 1
устойчивы к действию ванадата, представляет интерес определение содержания
низкомолекулярных белков и SH-групп в культуральной жидкости Ps. diminuta
в динамике развития культуры.
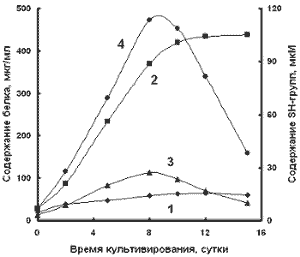
Рис.
3. Зависимость содержания низкомолекулярных белков (1, 2) и SH-групп (3, 4) в
среде от возраста культуры Ps. diminuta. 1, 3 - контроль; 2, 4 - в
присутствии 100 мг/л ванадата.
Как видно из рис. 3 в
среде культивирования Ps. diminuta наблюдается накопление
низкомолекулярных белков, содержание которых к 12 суткам составляет около 50
мкг/мл (кривая 1). В присутствии ванадата количество белка к этому периоду
времени возрастает до 450 мкг/мл (кривая 2). Это согласуется с ранее
полученными данными о стимуляции синтеза МТ у цианобактерий (Лебедева и др.,
1993; Саванина и др., 1995) и в клетках животных организмов (Gachot et al.,
1994).
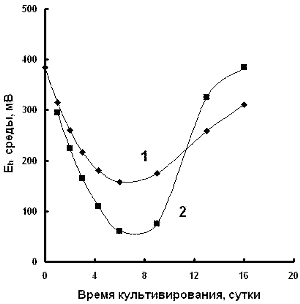
Рис.
4. Изменения величины Eh среды в динамике развития культуры Ps.
diminuta. 1 - контроль; 2 - в присутствии 100 мг/л ванадата.
Колоколообразная
зависимость накопления SH-групп в среде от возраста культуры Ps. diminuta
сопровождается сходной зависимостью снижения Eh среды. По мере
развития культуры величина Eh уменьшается и достигает минимума
(180-200 мВ) к 6-8 суткам, а затем вновь возрастает (рис. 4, кривая 1). В
присутствии ванадата минимальное значение Eh достигает 80 - 90 мВ
(кривая 2). Столь низкие значения Eh в аэробных условиях могут быть
обусловлены только наличием в среде значительных количеств тиолсодержащих
соединений, стандартный редокс-потенциал которых в анаэробных условиях
существенно ниже 0 мВ. Так, например, 1,4-дитиотреитол, эффективно
восстанавливающий SH-группы ферментов и кофакторов, имеет стандартный потенциал
-330 мВ при pH 7; сходными окислительно-восстановительными свойствами
обладают тиогликолевая кислота, 2-меркаптоэтанол, димеркаптопропанол и др.
(Досон и др., 1991).
В отличие от тиолов
такие соединения, как органические кислоты, имеют стандартные редокс-потенциалы
в интервале от 50 до 250 мВ. Согласно нашим данным (рис. 5) для достижения
величины Eh около 200 мВ содержание аскорбата в среде в аэробных
условиях должно составлять несколько мМ (кривая 2), а в случае гликолата его
концентрация при Eh около 300 мВ достигает 200-400 мМ (кривая 3).
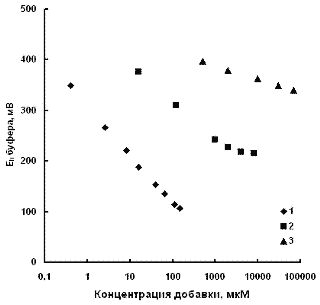
Рис.
5. Зависимость величины Eh от концентрации SH-групп цистеина,
инкубируемого в 20 мМ буфере морфолинопропансульфонате (pH 7,0).
На рис. 5 также показана
зависимость величины Eh буферного раствора от концентрации SH-групп
цистеина (кривая 1). Видно, что величинам Eh около 200 и 100 мВ
соответствуют концентрации SH-групп около 20 и 120 мкМ. Эти значения
согласуются с величинами Eh (рис. 4) и концентрациями SH-групп (рис.
3) в культуральной жидкости Ps. diminuta.
Таким образом,
полученная корреляции между содержанием ванадата в клетках и культуральной
жидкости Ps. diminuta, накоплением низкомолекулярных белков и SH-групп и
изменениями Eh среды культивирования бактерий позволяют полагать,
что ионы ванадия, поглощенные клетками Ps. diminuta стимулируют
образование тионеинподобных белков, связываются с ними с участием SH-групп и
выделяются из клеток вместе с белками, продуктами их деградации или с другими
тиоловыми соединениями.
Список
литературы
- Веревкина И.В., Точилкин А.И.,
Попова Н.А. 1977. Современные методы в биохимии, М.
- Горленко В.М., Дубинина Г.А.,
Кузнецов С.И. 1977. Экология водных микроорганизмов, М.
- Гусев М.В., Вольберг М.М.,
Лебедева А.Ф., Савельев И.Б. 1988. Использование метода диализного
культивирования для подбора симбиотических альгобактериальных пар//Биол. науки,
№ 1, 103-106.
- Гусев М.В., Лебедева А.Ф.,
Саванина Я.В., Барский Е.Л. 1997. Устойчивость культур цианобактерии Anacystis
nidulans и микроводоросли Dunaliella maritima к токсическому
действию ванадия: влияние фосфата, железа и цистеина//Вестн. МГУ. Сер.
Биология, № 3, 12-17.
- Досон Р., Эллиот Д., Эллиот У.,
Джонс К. 1991. Справочник биохимика, М.
- Лебедева А.Ф., Саванина Я.В.,
Савельев И.Б. 1993. Распрeделение ванадия в клетках цианобактерий Anacystis
nidulans и Nostoc muscorum: взаимосвязь с SH-содержащими
низкомолекулярными белками//Вестн. МГУ. Сер. Биология, № 4, 58-61.
- Саванина Я.В., Лебедева А.Ф.,
Савельев И.Б. 1994. Смешанно-раздельное культивирование цианобактерий Anacystis
nidulans и Nostoc muscorum и бактерий рода Pseudomonas в присутствии
ванадия//Вестн. МГУ. Сер. Биология, № 2, 29-34.
- Саванина Я.В., Адани А.Г.,
Лебедева А.Ф., Савельев И.Б., Гусев М.В. 1995. Образование
ванадий-тионеина клетками Anacystis nidulans при высоких
концентрациях металла//Вестн. МГУ. Сер. Биология, № 1, 38-46.
- Саванина Я.В., Пахомкина Б.С.,
Лебедева А.Ф., Дольникова Г.А. 1998. Смешанно-раздельное культивирование
цианобактерий Anacystis nidulans, Anabaena variabilis и Nostoc
muscorum с бактериями, выделенными из ванадийсодержащего промышленного
водоема. Тез. докл. на V Международной конференции "Новые
информационные технологии в медицине и экологии" Гурзуф.
- Торчинский Ю.М. 1977. Сера в
белках, М.
- Ang S.G., Wong V.W. 1992.
Chromatographic analysis of low-molecularmass copper-binding ligands from
the crab-spesies Scylla serrata and Portunus pelagicus//J.
Chromatogr., 599, № 1-2, 21-24.
- Appana V.D., Whitmore L. 1995.
Biotransformation of zinc by Pseudomonas fluorescens//Microbios.,
82, № 332, 149-155.
- Barsky E.L., Samuilov V.D. 1979.
Blue and red shifts of bacteriochlorophyll absorption band around 880 nm
in Rhodospirillum rubrum//Biochim. Biophys. Acta, 548, 448-457.
- Barsky E.L., Kamilova F.D.,
Samuillov V.D. 1985. Do cyanobacteria contain a membrane bound cysteine
oxidase?//Z. Naturforsch, 40 c, 176-178.
- Gachot B., Tauc M., Wanstoc F.,
Morat L., Poujeol Ph. 1994. Zinc transport and metallothionein induction
in primary cultures of rabbit kidney proximal cells//Biochem. Biophys.
Acta, 1191, № 2, 291-298.
- Kagi J.N.R. 1993. Purification
and primary structure of snail metallothionein. Similarity of the
N-terminal sequence with histones H4 and H2A//Eur.
J. Biochem., 216, № 3, 739-746.
- Lowry O., Rosenbourg R., Farr A.,
Randal R. 1951. Protein measurement with Folin phenol reagent//J. Biol.
Chem., 193, 265-275.
- Nagase H., Inthorn D., Miuamoto
K. 1994. Use of photosynthetical organisms in biological
purification//Jap. J. Toxicol. and Environ. Health, 40, № 6, 479-485.
- Obata H., Inoue N., Imai K.,
Umebauashi M. 1994. Cadmium tolerance of calli induced from roots of
plants with differences in cadmium tolerance//Soil. Sci. and Plant. Nutr.,
40, № 3, 351-354.
- Popper H.H., Woldrich A., Grigar
E. 1991. Comparison of chromate and vanadate toxicity and its relationship
to oxigen radical formation//Zentralb. Hyg. und Umweltmed, 194, № 4,
373-379.
- Reddy G.N., Prasad M.N.V. 1990.
Heavy metal binding proteine. Polypeptide: occurence, structure, synthesis
and function//Environ. Exp. Bot. 30, N 3. 251-264 Rehder D. 1991.
Bioorganisme Chemie des Vanadiums//Angev. Chem., 103, № 2, 152-172.