Исследование изменений метаболизма эритроцитов донорской крови после взятия ее из организма
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР
§ 1.1 Система крови
§ 1.2 Основные функции крови
§ 1.3 Форма и строение
эритроцитов
§ 1.4 Строение и функции
гемоглобина
§1.5 Разрушение эритроцитов
§1.6 Процессы энергетического
метаболизма и основные энергетические параметры эритроцитов
ГЛАВА 2. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
§ 2.1 Выбор физической модели
кинетики энергетического метаболизма
§ 2.2 Факторы, способствующие
переходу метаболизма эритроцитов из состояния с высокой концентрацией АТФ в
устойчивое состояние с низкой концентрацией АТФ
§ 2.3 Постановка
экспериментальных задач
§ 2.4 Неравновесные процессы,
протекающие в плазме пробы крови после ее взятия у донора, приводящие к
изменению метаболизма эритроцитов
ГЛАВА 3. ЭКСПЕРИМЕНТАЛЬНАЯ
ЧАСТЬ
§ 3.1 Цели экспериментальных
работ
§ 3.2 Используемые приборы и
установки
§ 3.3 Используемые материалы
§ 3.4 Методики проведения
экспериментальных работ
§ 3.5 Результаты
экспериментов и их обсуждение
§ 3.6 Выводы
§ 3.7 Некоторые практически
важные замечания
Заключение
СПИСОК ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Данная работа посвящена
исследованию, имеющему непосредственное отношение к медицинской практике. В
этой работе представлен теоретический анализ биохимических и физических
процессов, протекающих в пробе крови, взятой из организма, а также представлены
результаты соответствующих экспериментов. Значимость таких исследований
определяется в настоящее время проблемами, связанными с постепенной утратой
функциональных свойств крови по мере ее хранения. Поэтому удлинение сроков
хранения донорской крови - актуальнейшая задача.
Основным содержанием данной работы является исследование изменений
кинетики метаболизма эритроцитов. Эритроцит, как физическая система, является
простой моделью, на которой можно исследовать нюансы таких изменений и других
клеток. В этом заключается фундаментальная ценность данной работы. Часто не
удается количественно связать изменения в метаболизме клеток с их физиологией,
со способностью их к поддержанию гомеостаза, функционированием и
жизнеспособностью. К тому же определение количественных зависимостей между
скоростями изменения параметров и самими параметрами метаболических систем
клетки представляет собой непростую задачу. Однако ее решение может иметь
большую значимость для ряда прикладных вопросов. Для эритроцитов, как для
наиболее просто устроенных клеток, часто эти трудности преодолимы.
Цель работы. На основе анализа кинетики гомеостатирования
основных параметров метаболизма эритроцитов исследовать возможность реализации
второго устойчивого состояния эритроцитов, характеризующегося низкой
концентрацией АТФ, по сравнению с высокой концентрацией АТФ, реализующейся в
эритроцитах in vivo. Переход из одного состояния метаболизма эритроцита в
другое может сопровождаться нарушением кислородно-транспортной функции
эритроцитов. Причинами такого нарушения могут быть накопление гемоглобина в
метформе и изменение неспецифической проницаемости мембран, а также и изменение
других параметров, которое обусловлено переходом эритроцитов на новый уровень
гомеостатирования параметров.
Основные задачи исследования
1. Выбор физической модели для теоретического исследования кинетики
гомеостатирования основных параметров энергетического метаболизма эритроцитов in vivo с целью выяснения условий существования устойчивых
состояний и их числа.
. Выяснение условий, при которых может происходить переход
метаболизма эритроцитов из одной устойчивой точки в другую.
. Выявление процессов, протекающих при взятии крови из организма,
способствующих указанным переходам.
. Экспериментальная проверка возможности перехода метаболизма
эритроцитов из состояния in vivo в другое состояние после взятия
крови из организма.
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР
§ 1.1 Система крови
К обобщенной «системе крови» по Л.Ф. Лангу [1] относят:
. кровь и лимфу;
. органы кроветворения и кроверазрушения - красный костный мозг,
тимус, селезенку, лимфатические узлы, а также,
. нейрогуморальный аппарат регуляции их деятельности.
Кровь и лимфа вместе с интерстициальной (межклеточной), спинномозговой
(ликвором) и синовиальной (межорганной) жидкостью образуют внутреннюю среду
организма. Кровь - это жидкая соединительная ткань, находящаяся в постоянном
движении, между клетками которой нет механической связи. Кровь состоит из
плазмы (жидкого межклеточного вещества) и взвешенных в ней форменных элементов.
Плазма составляет 55-60% объема крови, форменные элементы - 40-45% [1].
Отношение объема форменных элементов ко всему объему крови называется
показателем гематокрита.
Плазма крови - это электролит, ионный и белковый состав которого подробно
описан в работе по реологии крови [2]. В этой работе также освещены механические свойства, оптические
характеристики, методы
исследования и реологические свойства крови. Приведены данные по ее электро- и теплопроводности.
Особенно подробно описаны такие свойства эритроцитов, как их деформируемость и
агрегация.
Плазма крови содержит 90% воды, около 6,6-8,5% белков и другие
органические и минеральные соединения - промежуточные или конечные продукты
обмена веществ, переносимые из одних органов в другие. К белкам плазмы крови
относятся [2]:
) альбумины, которые связывают и переносят различные вещества
крови и обуславливают около 80% общего осмотического давления ее коллоидов;
) глобулины, разделяющиеся на α-, β-,
γ-фракции,
важнейшая роль которых состоит в транспорте липидов и других веществ,
нерастворимых в свободном состоянии. γ-глобулины составляют антитела,
вырабатываемые иммунной системой;
) фибриноген - растворимая форма фибрина, - фибриллярный белок
плазмы крови, образующий волокна при повышении свертываемости крови (например,
при образовании тромба). Главная роль фибриногена - обеспечение свертываемости
крови.
Плазма также содержит варьирующееся число липидов, не только связанных
белками (липопротеиды), но и свободных, многие из которых поверхностно-активны.
Одним из классов липопротеидов являются хиломикроны - микросферы, диаметром 100
нм, обнаруживаемые, главным образом, после приема жирной пищи [2].
Известно, что постоянство количества клеток (подавляющего большинства их
видов) в тканях и органах поддерживается за счет проточного равновесия. При
этом скорость деления клеток равна скорости их гибели по одному из двух путей -
апоптозу или некрозу. В результате гибели клеток по пути некроза в кровь
постоянно поступают белки, входящие ранее в состав цитомембран этих клеток.
Кроме того, в плазму крови поступают различные секреты, выделяемые
специализированными клетками (например, гормоны и ферменты) и другие вещества,
попадающие в организм с пищей.
§ 1.2 Основные функции крови [1]
· транспортная функция - перенос и доставка клеткам-мишеням
различных веществ, растворенных в крови:
) перенос кислорода из легких во все органы и углекислоты из
органов в легкие - дыхательная функция;
) доставка органам питательных веществ - трофическая функция;
) удаление и транспортировка в почки продуктов обмена веществ -
выделительная, или экскреторная функция;
) транспорт биологически активных веществ (гормонов, регуляторных
субстанций и анаболиков);
) терморегуляторная функция - поддержание температуры тела,
особенно в условиях повышенной или пониженной температуры окружающей среды.
Вследствие большой теплоёмкости кровь переносит тепло от более нагретых
участков к менее нагретым участкам тела и органам, регулируя, таким образом,
физическую теплоотдачу.
· защитная функция (обеспечение гуморального и клеточного
иммунитета, свертывание крови при травмах);
· гомеостатическая функция (поддержание постоянства внутренней
среды организма, в том числе теплового и иммунного гомеостаза).
Все эти функции определяют важнейшую роль крови в организме. Клинический
анализ крови в медицинской практике является одним из основных в постановке
диагноза.
Данная работа будет касаться дыхательной функции крови. Следовательно,
главным объектом исследования будет эритроцит, его гомеостаз (постоянство
состава) и функции.
По данным авторов работы [2] эритроциты представлены в крови человека в
количестве около 5 x 1012 в 1 литре крови. Как уже говорилось выше,
основная функция эритроцитов - дыхательная - транспортировка кислорода и
углекислоты [3]. Эта функция обеспечивается дыхательным пигментом -
гемоглобином. Средняя продолжительность жизни эритроцитов в крови около 100
дней (в некоторых источниках от 80 до 120 дней), а затем они разрушаются. В
организме ежедневно разрушается (и образуется) около 200 млрд. эритроцитов.
§ 1.3 Форма и строение эритроцитов
Популяция эритроцитов неоднородна по форме и размерам. Форма стойко
сохраняется не только целым эритроцитом, но и его стромой после выхода
гемоглобина. В кровеносном русле при нормальных физиологических условиях
основную массу составляют эритроциты двояковогнутой формы - дискоциты (80-90%).
Кроме того, имеются планоциты (с плоской поверхностью) и стареющие формы
эритроцитов - шиповидные эритроциты, или эхиноциты, куполообразные, или
стоматоциты, и шаровидные, или сфероциты.
Одним из проявлений процессов старения эритроцитов является их гемолиз,
сопровождающийся выходом гемоглобина; при этом в крови обнаруживаются так
называемые «тени» эритроцитов - их оболочки [3].
Обязательной составной частью популяции эритроцитов являются их молодые
формы, называемые ретикулоцитами, или полихроматофильными эритроцитами. В норме
их содержание в плазме крови достигает 1-5 % от общего количества всех
эритроцитов. В них сохраняются рибосомы и эндоплазматическая сеть, формирующие
зернистые и сетчатые структуры, которые выявляются при специальной окраске.
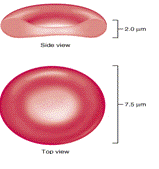
Размеры эритроцитов в нормальной крови варьируются. Диаметр эритроцита
колеблется от 5,0 до 9,0 мкм (рис.1). Размеры эритроцитов человека различаются
в зависимости от пола и возраста, климатогеографических условий проживания.
Большинство эритроцитов имеют диаметр около 7,5 мкм и называются нормоцитами.
Остальная часть эритроцитов представлена микроцитами и макроцитами.
Эритроцит человека и других млекопитающих является монофазной клеткой, т.
е. не имеет эндоплазматических мембран. Снаружи эритроцит окружен
белково-липидной мембраной. Цитоплазма эритроцита состоит из воды (60%) и
сухого остатка (40%), содержащего, в основном, гемоглобин, молекулы которого
вблизи от мембраны расположены упорядоченно, а в более глубоких слоях -
хаотично. Плотность "упаковки" молекул гемоглобина в эритроците
такова, что даже в центральных частях подвижность его каждой молекулы
ограничена пространством в 10 Å. Количество гемоглобина в одном
эритроците называют цветовым показателем. При электронной микроскопии
гемоглобин выявляется в гиалоплазме эритроцита в виде многочисленных плотных
гранул диаметром 4-5 нм [3].
§ 1.4 Строение и функции гемоглобина
Гемоглобин - главный компонент эритроцита и основной дыхательный
пигмент, обеспечивающий перенос кислорода (О2) из легких к тканям в
организмах позвоночных животных, и, в меньшей степени, углекислого газа (СО2)
от тканей в легкие. Главным образом, углекислота переносится в виде 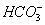 в плазме крови. Подсчитано, что в одном эритроците
содержится ~ 340.000.000 молекул гемоглобина, каждая из которых состоит
примерно из 103 атомов. В крови человека в среднем содержится ~ 750г
гемоглобина [3].
в плазме крови. Подсчитано, что в одном эритроците
содержится ~ 340.000.000 молекул гемоглобина, каждая из которых состоит
примерно из 103 атомов. В крови человека в среднем содержится ~ 750г
гемоглобина [3].
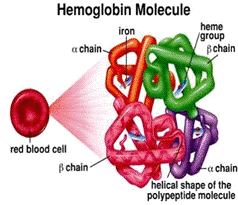
Гемоглобин
представляет собой сложный белок, относящийся к группе гемопротеинов. Белковый
компонент его представлен глобином, состоящим из двух a и двух b субъединиц и, соответственно, содержит четыре
полипептидные цепочки двух сортов. Небелковый компонент (так называемая
простетическая группа) представлен четырьмя одинаковыми железопорфириновыми
соединениями - гемами.
Иржак
Л.И. в своей работе [4] описал большинство физиологических свойств гемоглобина,
его виды и подвиды. Основное внимание в этой работе уделено описанию процессов
связывания кислорода гемоглобином в норме и при некоторых патологиях. Также
приведена кривая диссоциации оксигемоглобина и описан эффект Бора.
Наиболее
подробно физико-химические свойства гемоглобина изучены и представлены в
работах Блюменфельда Л.А. [5, 6]. В них большое внимание уделено зарядовым
характеристикам молекул гемоглобина. Эти характеристики в значительной степени
определяют адгезивные свойства молекул гемоглобина (комплексование и ассоциацию
с липидной мембраной). В указанных работах приведены теоретические и
экспериментальные исследования, в которых сравниваются свойства окси- и
деоксигемоглобина, а также гемоглобина и миоглобина.
При
взаимодействии молекулярного кислорода с гемоглобином в условиях in vivo существует небольшая, но конечная вероятность
окисления гема двухвалентного железом до трехвалентного, причем молекула О2
не присоединяется, но окисляет железо: Fe2+ + O2 Þ Fe3+ O2-. Поэтому при
дыхании в эритроцитах непрерывно образуется метгемоглобин, который не способен
переносить О2. Восстановление Fe3+ метгемоглобина до Fe2+ происходит с затратами энергии и обеспечивается
ферментом - метгемоглобинредуктазой [3].
В
ходе метаболизма глюкозы, протекающего в эритроците по побочному пути
гликолиза, контролируемого ферментом дифосфоглицератмутазой, в эритроците
образуется 2,3-дифосфоглицерат (2,3-ДФГ). Основное его значение заключается в
уменьшении сродства гемоглобина к кислороду. 2,3-ДФГ связывается с β-цепями гемоглобина, облегчая отсоединение О2
от молекулы гемоглобина [3].
Большое
количество опубликованных работ посвящено строению мембран клеток, в том числе
и эритроцитов. В одной из классических работ [7] приведены данные по количеству
и белковому составу мембран эритроцитов и функциональному назначению этих
белков, архитектонике липидного бислоя.
Спектрин
является белком цитоскелета, связанным с внутренней стороной мембраны. Он
участвует в поддержании двояковогнутой формы эритроцита.
Гликофорин
- белок, относящийся к классу мембранных гликопротеинов, по мнению авторов
работ [9, 10, 11], играет важную роль в механизме авторегуляции неспецефической
проницаемости цитоплазматической мембраны эритроцита. Этот белок пронизывает
мембрану в виде одиночной спирали. Большая его часть выступает с наружной
поверхности эритроцита, где к нему присоединены 15 отдельных цепей
олигосахаридов, на ветвях которых расположены сиаловые кислоты, несущие
отрицательные заряды. В распрямленном виде максимальное удаление ветвей гликофорина
от поверхности эритроцита может достигать 200 нм, что больше поляризационной
длины плазмы крови (радиуса экранировки Дебая). В результате этого отдельные
отрицательные заряды экранированы противоионами плазмы, так что нити
гликофорина не взаимодействует с поверхностью своей мембраны. Так как
противоионы могут быть общими для гликофоринов различных эритроцитов, то
эритроциты могут образовывать монетные столбики.
Белок
полосы 3 представляет собой трансмембранный гликопротеид, полипептидная цепь
которого много раз пересекает бислой липидов. Этот гликопротеид участвует в
обмене кислородом и углекислотой.
§1.5 Разрушение эритроцитов
Известно, что эритроциты живут 2-3 месяца [3]. Основной причиной ухода их
из кровяного русла является потеря отрицательных зарядов сиаловых кислот. Отбор
из кровяного русла функционально неспособных эритроцитов осуществляется по
нативности сиаловых кислот на нитях гликофорина в тонких (2-3 мкм диаметр)
капиллярах микроциркуляционной сети крови, в основном в селезенке, а также легких
и печени [3].
§1.6 Процессы энергетического метаболизма и основные
энергетические параметры эритроцитов
В цитоплазме эритроцитов в процессах анаэробного усвоения молекул глюкозы
синтезируются основной макроэрг - АТФ и энергетические потенциалы НАДФ-Н и
НАД-Н. С помощью этих соединений обеспечиваются энергией главные процессы,
связанные с жизнеобеспечением и функциональной деятельностью эритроцитов.
Концентрация АТФ (в дальнейшем, nАТФ)
является основным энергетическим параметром эритроцита. Энергия, выделяющаяся
при разрыве макроэргической связи АТФ, обеспечивает активный транспорт катионов
через мембрану, поддержание оптимального соотношения концентраций К+
и Na+ (поддержание нормальной работы Na+/К+каналов),
сохранение формы и целостности мембраны эритроцита. НАД-Н участвует в
метаболизме гемоглобина, предотвращая окисление его в метгемоглобин, а НАДФ-Н
участвует в метаболизме липидов.
Атауллаханов Ф.И. выполнил ряд фундаментальных работ [12, 13], в которых
использовал и усовершенствовал модель кинетики метаболизма эритроцитов,
представленную в работах Селькова Е.Е. [14]. Он провел теоретические и
экспериментальные исследования, касающиеся процессов энергетического
метаболизма эритроцитов. В полном объеме представил биохимию этих процессов, описал соответствующие реакции и
участвующие в них ферменты. В частности, исследовал процессы поддержания постоянства объема
эритроцитов, обеспечивающие их целостность клеток. Рассмотрел кинетику обмена
АТФ в этих клетках и связал ее с механизмом, обеспечивающим постоянство объема
эритроцитов. Показал, что постоянство объема связано с поддержанием на
постоянном уровне величины энергетического заряда
φ=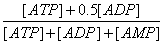 ,
,
где
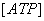 ,
, 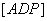 ,
,  - концентрации АТФ, АДФ и АМФ соответственно.
- концентрации АТФ, АДФ и АМФ соответственно.
Фок
М.В. в своих исследованиях [10] кинетики процессов метаболизма клеток, в том
числе эритроцитов, графическим методом показал кинетику основных процессов
метаболизма, обеспечивающих гомеостаз величин кислотности (рН) и концентрации
АТФ (nАТФ) в цитоплазме клеток в состоянии покоя. На
основании этого он объяснил принцип действия механизма стабилизации этих
параметров. Для этого была рассмотрена кинетика метаболизма эритроцитов
изменения каждого из указанных параметров как функции рН и nАТФ,
при постоянстве всех других параметров клетки:
1. скоростей притока (V+) и стока (V-) ионов Н+ от значений самих параметров рН
и nАТФ в цитоплазме;
. скоростей синтеза (V+) и расхода
(V-) молекул АТФ от рН и nАТФ в цитоплазме.
ГЛАВА 2. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
§ 2.1 Выбор физической модели кинетики энергетического
метаболизма
Метаболизм большинства соматических клеток, выполняющих определенные
функции в организме, описывается огромным количеством параметров, что, как
правило, существенным образом затрудняет создание математической модели их
состояний. Исключение составляют только отдельные виды клеток с простейшим метаболизмом,
к которым относится эритроцит. Однако физические модели, основанные на
качественном анализе закономерностей протекания конкретных процессов
метаболизма, могут дать значимые результаты для решения фундаментальных и
прикладных задач. В данной работе использовались только физические модели,
которые более просты и наглядны.
В литературе наиболее известна модель Селькова [14], используемая в
работе Атауллаханова. Математическая модель сложного равновесного процесса
усвоения глюкозы по пути Эмбдена-Мейэргофа представлена системой уравнений,
описывающих каждую реакцию последовательного превращения молекулы глюкозы в
лактат. Расчеты приводятся при постоянном значении рН и при постоянстве пула
ферментов и регуляторных субстанций, участвующих в этих реакциях. В результате
получают зависимость скоростей утилизации глюкозы от концентрации АТФ в
цитоплазме эритроцита, то есть зависимость скорости V+ синтеза АТФ от его концентрации nАТФ. В модели принято, что расход АТФ обусловлен суммарной
тратой этого макроэрга в простых ферментативных реакциях. Следовательно,
скорость V- трат АТФ в зависимости от nАТФ в цитоплазме эритроцита изменяется по закону
Михаэлиса-Ментен:
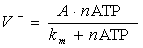 ,
,
где
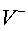 - скорость
траты АТФ,
- скорость
траты АТФ, 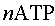 - концентрация АТФ, величины km и
А - константы. В данной модели km>> nАТФ, тогда
- концентрация АТФ, величины km и
А - константы. В данной модели km>> nАТФ, тогда
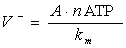
Данная
модель представлена на рис.3.
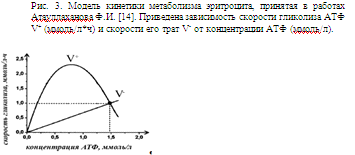
При
пересечении кривых V+ и V- реализуется только одна стационарная точка.
Устойчивость точки определяется по двум условиям устойчивости по Ляпунову:
(1) - первое условие устойчивости,
где
αi
- рассматриваемый параметр, 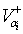 и
и 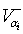 -соответственно, скорости притока и убыли данного
параметра, αj -
параметр, по которому проверяется устойчивость, при этом i может быть равно j.
-соответственно, скорости притока и убыли данного
параметра, αj -
параметр, по которому проверяется устойчивость, при этом i может быть равно j.
(2) - второе условие устойчивости.
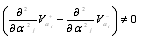
Стационарная точка является устойчивой по условию (1). Видно, что данная
модель не допускает существования большего количества устойчивых стационарных
точек.
Следовательно, можно заключить, что для установления возможности
существования устойчивых точек с помощью моделей, в которых допускается
свободной одна переменная, достаточно знать вид кривых зависимостей скоростей
синтеза V+ и расхода V- АТФ от его
концентрации и их взаимное расположение. Такой графический метод анализа
кинетики метаболизма наиболее нагляден и позволяет на качественном уровне
устанавливать наличие устойчивых стационарных точек, поэтому в дальнейшем будет
решаться поставленная задача данным методом, без привлечения сложных
математических уравнений.
Другой физической моделью, схожей с предыдущей, является модель,
приведенная в работах Фока М.В. и его соавторов [10]. Она используется для
анализа кинетики энергетического метаболизма и представлена на рис. 4. Данная
модель принята за основную в данном исследовании.
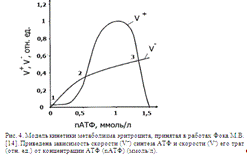
Зависимости скоростей синтеза (V+) и расхода
(V-) АТФ от его концентрации (nАТФ) в цитоплазме при постоянстве всех остальных параметров,
таких как рН, концентраций всех ферментов, количества аденозиновых оснований
(АДФ и АМФ) и запасов неорганического фосфата, имеют вид, представленный на
рис. 4. Свободным параметром, также как и в первой модели, является
концентрация АТФ в цитоплазме.
Кривая зависимости V+ от nАТФ имеет колоколообразную форму с максимумом. При нулевой
концентрации АТФ в цитоплазме скорость синтеза V+ АТФ имеет ненулевое значение. Это обусловлено тем, что в
рассматриваемых условиях (заданном значении рН, концентрации АДФ, ограниченном
запасе неорганического фосфата и при нулевом значении концентрации АТФ) в
результате теплового движения субстраты (АДФ и молекул фосфата) сталкиваются,
вследствие чего преодолевается активационный барьер, и в результате, происходит
синтез АТФ. Дальнейший ход кривой зависимости скорости (V+) синтеза АТФ от nАТФ определяется автокаталитической реакцией синтеза, в
которой часть выработанного АТФ расходуется в процессах гликолитических
реакций. Поэтому скорость синтеза АТФ сначала зависит линейно от nАТФ, а затем экспоненциально. Далее
по мере истощения запасов органического фосфата достигается максимум скорости
синтеза АТФ. Дальнейший спад кривой зависимости V+ АТФ от nАТФ
обусловлен, в основном, истощением запасов неорганического фосфата. При нулевой
скорости синтеза в области высоких значений nАТФ все запасы неорганического фосфата израсходованы.
Зависимость скорости V- расхода АТФ от nАТФ, также как и в первой модели
изменяется по закону Михаэлиса-Ментен:
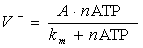 ,
,
где
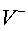 - скорость
траты АТФ,
- скорость
траты АТФ, 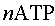 - концентрация АТФ, величины km и
А - константы. В данной модели нет условия km>>
nАТФ, и кривая скорости расхода V- при высоких значениях nАТФ, отклоняясь
от прямой, выходит на постоянный уровень.
- концентрация АТФ, величины km и
А - константы. В данной модели нет условия km>>
nАТФ, и кривая скорости расхода V- при высоких значениях nАТФ, отклоняясь
от прямой, выходит на постоянный уровень.
Рис.
4 демонстрирует один из возможных вариантов взаимного расположения кривых
зависимостей скоростей V+ синтеза
АТФ и расхода V- АТФ от nАТФ,
которые при пересечении дают три стационарные точки: две из которых (1 и 3),
устойчивы по условию (1), одна (точка 2) неустойчивая и является
дискриминационной. Таким образом, вторая модель допускает существование второй
устойчивой точки в областях низких значений nАТФ.
Если
кинетику метаболизма эритроцитов крови в организме можно представить в виде,
приведенном на рис. 4, то их состоянию in vivo
соответствует точка 3. Это доказывают эксперименты с отмытыми эритроцитами,
приведенные в работах Атауллаханова Ф.И. [12, 13].
С
помощью данной модели Фока М.В. можно проанализировать возможность перехода
метаболизма эритроцита из одного устойчивого состояния в другое. Первый способ
осуществления перехода - это запуск быстрых неравновесных процессов (например,
при добавлении в пробу крови ингибиторов АТФ), которые могут привести к
существенному уменьшению концентрации АТФ, причем значения других параметров не
успевают изменяться. При этом метаболизм эритроцитов перейдет в другое
устойчивое состояние с гомеостазом концентрации АТФ в области низких значений.
Но на практике такой вариант трудно реализуем.
Другой
способ осуществления перехода - это кратковременное изменение регулирования
(активации или ингибирования) процессов синтеза и трат АТФ, в результате
которого изменяется взаимное расположение кривых V+ и V-. Рис. 5
иллюстрирует такое изменение кинетики процессов, которое приводят к упомянутому
выше переходу. Условия, при которых производится анализ этих изменений,
соответствуют условиям основной модели, используемой в данной модели.
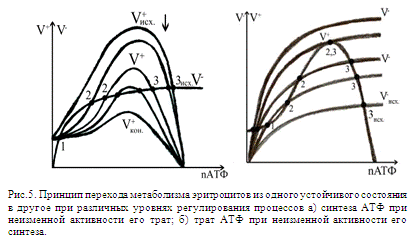
На
рис. 5 показаны семейства кривых зависимостей скоростей синтеза V+ и расхода V- АТФ от nАТФ при различных уровнях регулирования процессов
энергетического метаболизма эритроцитов. На рис. 5а изображено семейство кривых
V+,
соответствующих разным уровням активности процесса синтеза АТФ, при неизменном
уровне активности процесса трат АТФ. При этом положение кривой зависимости
скорости расхода V- от nАТФ
неизменно для всех рассматриваемых кривых V+. На рис. 5б показано семейство кривых V-, соответствующих разным уровням активности процессов
трат АТФ при неизменном уровне активности процесса синтеза АТФ. Соответственно,
положение кривой V+ неизменно для всех рассматриваемых кривых V-.
Рассмотрим
случай регулирования активности процесса синтеза АТФ (рис. 5а). Пусть процесс
синтеза АТФ активирован. Этому соответствует верхняя кривая на рис.5а. Система
имеет одну устойчивую стационарную точку 3. Допустим, что активирование
постепенно снимается. Кривая V+
переходит в положение под кривой V+исх.. Видно, что появляются ещё 2 стационарные точки, одна
(точка 1) из которых, при низких значениях, устойчива, а вторая (точка 2) - не
устойчива (дискриминационная). Дальнейшее смещение кривой V+ может быть обеспечено продолжающимся снятием
активирования и включением ингибирования процесса синтеза АТФ. При смещении
кривой V+ вниз, в
сторону все более низких скоростей гликолиза, устойчивая точка 3 смещается в
сторону низких значений nАТФ, а дискриминационная точка 2 в сторону высоких его
значений, затем 2-я и 3-я точки сливаются, а при дальнейшем усилении
ингибирования исчезают. В конечном итоге остается одна устойчивая точка 1 в
области низких концентраций АТФ. Рассмотренная картина смены состояний
обратима. Постепенное снятие ингибирования процесса синтеза АТФ и последующая
его активация этого процесса, переводят систему из конечного состояния в начальное.
На
рис. 5б рассмотрен другой случай регулирования энергетического метаболизма,
когда процесс синтеза АТФ не регулируется, а процесс трат постепенно
активируется. В исходном состоянии системы второй процесс подавлен, и кривая V-исх.
занимает самое нижнее положение, а положение кривой V+ не меняется. Система имеет одну устойчивую
стационарную точку. При постепенной активации процессов трат АТФ кривая V- смещается в сторону высоких скоростей расхода АТФ.
При касании V- с кривой
V+
появляется вторая точка 2 неустойчивая по условию (2). При дальнейшем смещении
кривой V-
появляется ещё одна точка - 1, которая устойчива по первому условию Ляпунова.
При этом устойчивая точка 3 смещается в сторону низких значений nАТФ,
а дискриминационная точка 2 в сторону высоких его значений. Затем 2-я и 3-я
точки сливаются и при дальнейшем активировании процессов расхода АТФ исчезают.
В конечном итоге остается одна устойчивая точка - 1 в области низких значений
концентрации АТФ. Подобно предыдущему рассмотренному случаю, данная картина
перехода обратима.
Таким
образом, изменяя скорости протекания процессов синтеза и трат АТФ с помощью их
активации и ингибирования, можно переводить систему из одного устойчивого
состояния в другое, если данная физическая модель допускает существование двух
устойчивых состояний энергетического метаболизма эритроцита.
В
свете изложенного выше, взаимные переходы между состояниями эритроцита с
высокой и низкой концентрацией АТФ осуществляются тогда, когда кривые V+ синтеза и V- расхода АТФ смещаются в противоположные стороны
(сближаются либо расходятся). Это смещение может достигаться за счет
ингибирования процесса синтеза АТФ и одновременной активации процесса его трат.
На основе анализа кинетики метаболизма эритроцитов с помощью выбранной за
основу физической модели нельзя утверждать, что всегда существует вторая
устойчивая точка, лежащая в области низких значений АТФ, поскольку эта модель
допускает варианты, когда такой точки не существует. Для данного исследования
интересны не все возможные ситуации, а только те, когда энергетический
метаболизм эритроцитов близок к in vivo. Для прояснения вопроса о
том, всегда ли существует состояние эритроцитов с низкой nАТФ,
требуется привлечение более точной модели, которая возможно даст однозначный
ответ о наличии в этих условиях указанной устойчивой точки.
Рассмотрим
модель равновесных процессов метаболизма, предложенную Фоком М.В. и соавторами
в работе [10], дополнив ее некоторыми деталями и назвав обобщенной моделью, как
это сделано в работе [15]. В этой работе [15] рассматривается состояние покоя
клеток, режимы их активности и деления. Нас интересует только состояние покоя,
в котором достигается гомеостаз всех параметров, обеспечивающий
жизнеспособность и жизнедеятельность клеток.
В
обобщенной модели основными параметрами при анализе кинетики энергетического
метаболизма выбраны показатель кислотности рН цитоплазмы, концентрация АТФ в
ней и количество липидов C в мембране. Первые два параметра относятся к
быстроменяющимся параметрам, так как величины их могут изменяться за доли
секунды, то есть значительно быстрее времени обращения крови по большому кругу.
В отличие от этих параметров, количество липидов в мембране эритроцитов
меняется медленно, но также является важным энергетическим параметром, который
определяет жизнеспособность и целостность клетки. Количество ферментов, запасы
глюкозы в цитоплазме, объем эритроцитов и др. в модели приняты постоянными.
Свободными же оставляют 2 переменные - nАТФ и рН
цитоплазмы, которые определяют скорости таких энергозависимых процессов в
эритроцитах как скорости синтеза и распада АТФ, скорости подкисления и
подщелачивания цитоплазмы, а также скорости синтеза и распада липидов. Эти
скорости будут функциями только двух указанных переменных.
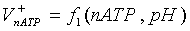 ,
,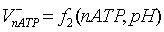 - скорости синтеза и расхода АТФ;
- скорости синтеза и расхода АТФ;
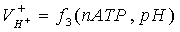 ,
,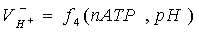 - скорости подкисления подщелачивания цитоплазмы;
- скорости подкисления подщелачивания цитоплазмы;
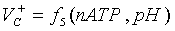 ,
,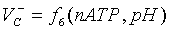 - скорости синтеза и распада липидов.
- скорости синтеза и распада липидов.
Зависимости
скоростей каждого из перечисленных процессов от рН и nАТФ в трехмерном
пространстве величин (pH, nАТФ, V - скорости процессов) могут быть представлены
сложными поверхностями [15, 16]. На линиях пересечения поверхностей, полученных
для каждых двух противоположно направленных процессов (синтез и расход АТФ,
подкисление и подщелачивание цитоплазмы, синтез и распад липидов в мембранных
структурах), достигается баланс их скоростей.
На
рис. 6 представлены участки этих поверхностей. Их линии пересечения трехмерны.
Пара участков поверхностей V+АТФ и V-АТФ дают линию пересечения, в точках которой скорость синтеза
АТФ равна скорости расхода АТФ; пара поверхностей V+рН и V-рН дают
линию пересечения, в точках которой скорость подкисления равна скорости
подщелачивания цитоплазмы; пара поверхностей V+С и V-С дают
линию пересечения, в каждой точке которой скорость увеличения равна скорости
уменьшения количества липидов в мембране. Следами этих линий пересечения (в
проекции на плоскость (nАТФ; рН)) являются кривые АВ, MN и KL,
соответственно, для каждой из перечисленных выше линий пересечения. Как видно
из рис. 6, эти кривые попарно пересекаются, что отражает рассогласованность
процессов метаболизма.
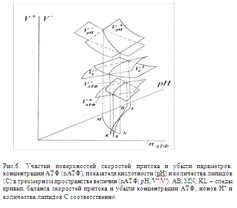
На
рис. 7. эти следы показаны на фазовой плоскости (nАТФ; рН) для случая
согласования процессов метаболизма. При значениях рН и nАТФ, соответствующих
точкам на этих кривых,
V+ = V- ≡ Vобмена (Vобмена -
скорость обмена параметра).
Скорость
обмена является важнейшей характеристикой проточного равновесия противоположно
направленных процессов клеточного метаболизма в состоянии покоя.
Как
видно из рис. 7 кривые АВ и КL монотонно возрастают, а МN спадает, при
этом все кривые пересекаются в точке О. Такая конфигурация и взаимное
расположение кривых определяют устойчивость точки О по всем трем параметрам.
Рассмотрим
устойчивость точки О по концентрации АТФ. В области над кривой АВ преобладают
скорость V+ синтеза
АТФ, а под кривой скорость V- его
трат, следовательно, частная производная Vобмена концентрации АТФ по nАТФ
отрицательна. При отклонении состояния метаболизма от точки О в сторону меньших
концентраций АТФ, то, начнут преобладать процессы синтеза АТФ и состояние
вернется в исходное устойчивое положение. То есть концентрация АТФ возрастает в
результате интенсификации окислении субстратов и цитоплазма подкисляется.
Можно
показать также, что точка О устойчива по рН согласно условию (1). Как
говорилось, кривая МN монотонно спадает. Над кривой баланса MN
преобладает скорость притока V+ ионов
водорода Н+ в цитоплазму, а под кривой - скорость V- убыли Н+, значит, частная производная Vобмена ионов Н+ по рН отрицательна. При
отклонении состояния метаболизма от точки О вверх по рН будут преобладать
процессы подкисляющие цитоплазму, в результате которых значение рН возвращается
к исходному.
Проведя
аналогичные рассуждения можно заключить, что точка О также устойчива по
количеству липидов в цитоплазматической мембране. Над кривой баланса KL
преобладает скорость V+ синтеза
липидов, а под кривой - скорость V- их
ферментативного распада. При переходе через точку О слева направо частная
производная Vобмена
количества липидов по nАТФ отрицательна, также при переходе через точку О
снизу вверх частная производная по рН также отрицательна. Следовательно,
согласно условию (1) эта точка устойчива по количеству липидов С в
цитомембране.
Для
дальнейшего анализа кинетики метаболизма эритроцитов важно получить указанные
следы кривых баланса скоростей V- и V+ для основных параметров, используемых в принятой за
основу модели, во всем физиологическом диапазоне изменений концентрации АТФ и
рН, включая область больших, чем в состоянии покоя, значений концентрации АТФ.
Ясно, что конфигурации и взаимное расположение кривых, обеспечивающих
устойчивость новой точки 3 с координатами (nАТФ3,рН3),
в случае согласованности процессов метаболизма, будут подобны рассмотренному
выше случаю для состояния покоя клетки. Для эритроцитов это имеет
место. Для подавляющего большинства соматических клеток (кроме возбудимых
клеток) согласно работе [16] в области высоких значений nАТФ
устойчивости состояний метаболизма по рН нет. Поэтому для дальнейшего анализа
кинетики метаболизма эритроцитов мы воспользуемся следующей моделью, которая
проиллюстрирована на рис. 8.
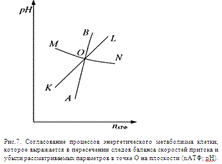
Кривая
ABCD на фазовой плоскости (nАТФ; рН)
является следом кривой баланса скоростей синтеза V+ и расхода V- АТФ. Форма этой кривой имеет зигзагообразный вид.
Точки ветвей АВ и CD устойчивы по условию (1), кроме точек В и С, которые
неустойчивы по условию (2). Точки ветви ВС не устойчивы по условию (1).
Из
таких же соображений получена форма кривой KLК1L1. Точки ветвей участков кривой KL и
К1L1
устойчивы по условию (1), а точки ветви LK1 не устойчивы по этому условию. Точки L и K1 неустойчивы по условию (2).
Для
качественного анализа (достаточного для получения необходимых результатов) хода
кривой баланса MN не требуется строить соответствующие поверхности.
Расположение и характерную конфигурацию кривой MN можно
получить аналитически. Имея начальную точку, для определения конфигурации и
расположения на плоскости (nАТФ, рН) кривой MN, можно
воспользоваться известной зависимостью рН цитоплазмы от величины
трансмембранного потенциала.
Поскольку
цитомембрана не представляет значительного препятствия для ионов Н+,
то можно использовать соотношение Больцмана:
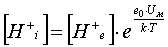 (3),
(3),
где
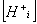 - концентрация ионов
- концентрация ионов 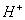 в
цитоплазме эритроцитов;
в
цитоплазме эритроцитов; 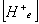 - концентрация ионов
- концентрация ионов 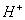 в плазме
крови;
в плазме
крови; 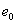 - элементарный заряд;
- элементарный заряд; 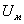 -
трансмембранный потенциал; k - постоянная Больцмана; T - температура.
Прологарифмировав соотношение (1), получим зависимость рН цитоплазмы от
концентрации АТФ(4):
-
трансмембранный потенциал; k - постоянная Больцмана; T - температура.
Прологарифмировав соотношение (1), получим зависимость рН цитоплазмы от
концентрации АТФ(4):
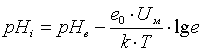 (4),
(4),
где
величина Uм является
функцией рН и nАТФ.
Обычно
in vivo кислотность плазмы крови 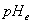 =7,45; а
=7,45; а 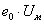 ~25 мэВ и
~25 мэВ и
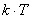 =26мэВ, т.о. из (4) следует, что в норме в цитоплазме
эритроцитов
=26мэВ, т.о. из (4) следует, что в норме в цитоплазме
эритроцитов 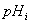 =7,05.
=7,05.
Трансмембранная
разность потенциалов состоит из трех компонент
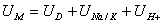 ,
,
где
UD - потенциал термодинамического равновесия Доннана; UNa/K - величина
трансмембранного потенциала, обусловленного деятельностью молекулярных K+/Na+ насосов,
зависящая от концентрации АТФ по закону Михаэлиса-Ментен; UH+ -
величина трансмембранного потенциала, которая определяется выходом части ионов
Н+ при накоплении кислых продуктов при протекании реакций гликолиза.
Последней составляющей можно пренебречь.
При
нулевом значении концентрации АТФ величина трансмембранного потенциала
ненулевая, соответствует потенциалу Доннана и составляет 10 мВ [16]. В
организме строго поддерживается рН межклеточной жидкости и плазмы крови на
уровне рНе=7,35-7,45. Следовательно, рН цитоплазмы эритроцита ниже, чем рН
плазмы на величину
ΔрН=0,05, обусловленную наличием
доннановского потенциала, и имеет значение рНД=7,3. Тогда кривая MN
взяв начало в точке (0, рНд) далее спадает, постепенно доходя до
насыщения в области высоких значений концентрации АТФ, как это показано на
рис.8.
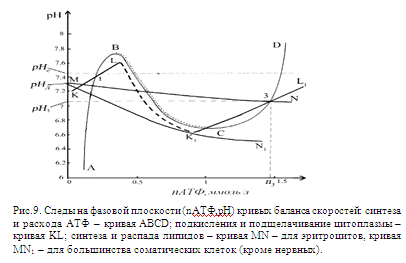
Для
всех соматических клеток (кроме, нейронов), кривая MN обязательно
пересекает участок АВ следа АВСD, расположенный в области низких значений АТФ,
поскольку у всех этих клеток есть состояние покоя (рис. 9). Ретикулоцит в этом
отношении от этих клеток не отличается, поскольку имеет ядро и все признаки
обычной соматической клетки. Эта клетка, несомненно, может также находиться в
состоянии покоя, и соответствующая ему точка лежит в области низких значений
концентраций АТФ. Эритроцит значительно проще своего предшественника. Его
энергетическая база ослаблена, поскольку гликолиз является единственным
источником энерговыделения. Интенсивность трат АТФ значительно меньше. Эти
факторы влияют на взаимное расположение следов кривых в рассматриваемой
качественной модели энергетического метаболизма. Подробный анализ изменений
энергетического метаболизма ретикулоцита при превращении его в эритроцит,
выполненный с помощью обобщенной модели, не позволяет однозначно ответить на
вопрос о существовании второй устойчивой точки в области низких значений АТФ в
условиях, близких к in vivo. Для этих целей необходимы
эксперименты с цельной кровью.
§ 2.2 Факторы, способствующие переходу метаболизма
эритроцитов из состояния с высокой концентрацией АТФ в устойчивое состояние с
низкой концентрацией АТФ
Способы перевода энергетического метаболизма эритроцитов на новый уровень
можно разделить на две группы: равновесные и неравновесные.
Поскольку исходное высокоэнергетическое состояние имеет определенный
диапазон устойчивости по двум указанным свободным параметрам рН и nАТФ, то тактика равновесного перевода
должна включать постепенное приближение (за счет регулирования процессов
метаболизма) к границе устойчивости и переход за нее. Далее система сама
обеспечит достижение низкоэнергетического состояния, если такое имеется. Рис.
10 иллюстрирует кинетику возможного перехода метаболизма эритроцита из одного
устойчивого состояния в другое состояние в результате изменения регулирования скоростей
протекания равновесных процессов.
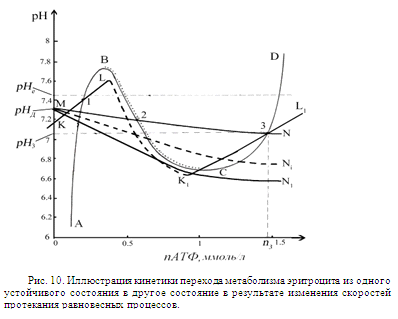
На этом рисунке на фазовой плоскости (nАТФ, рН) представлены следы кривых баланса скоростей притока
и убыли основных параметров: АВСD -
концентрации АТФ в цитоплазме, КLK1L1 - количества липидов С в мембране эритроцитов, МN - концентрации ионов Н+ в
цитоплазме. Точка 3 на этом рисунке иллюстрирует взаимное расположение кривых,
определяющее исходное состояние системы до изменения регулирования процессов.
Для того, чтобы осуществился переход в область низких значений nАТФ необходимо, чтобы в результате
регулирования активности равновесных процессов кривые АВСD и КLK1L1 смещались в сторону увеличения рН, а
MN в сторону меньших значений этой
величины. Так как для перехода важно только изменение взаимного расположения
указанных кривых, то для простоты и ясности рассмотрения, можно положить, что 2
зигзагообразные кривые не меняют своего положения, а меняется только положение
кривой МN. При смещении кривой MNi происходит постепенное приближение
ее к границе устойчивости, что означает приближение точки Ni к точке С. Такое смещение приводит к
рассогласованию рассматриваемых процессов, в результате чего появляются
автоколебания параметров (рис. 11). Исследование этих колебательных процессов не
является предметом рассмотрения данной работы.
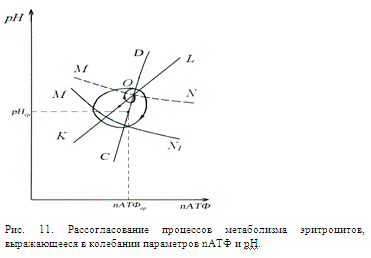
Колебания, изображенные на рис.11, облегчают переход системы в указанное
выше низкоэнергетическое состояние. На этом рисунке представлены участки кривых
на фазовой плоскости (nАТФ,
рН), показанных на рис. 10, относящихся к исходному состоянию системы.
Обозначения кривых те же, что и на предыдущем рисунке. Рассогласование
процессов проявляется в том, что участки кривых не пересекаются в одной точке.
За счет обратных связей между скоростями процессов и самими значениями
параметров и за счет инерционности процессов, режим метаболизма системы будет
характеризоваться непрерывным изменением как скоростей, так и значений самих
параметров. Возникают их незатухающие колебания. Непрерывная смена значений рН
и концентрации АТФ определяет на фазовой плоскости замкнутую траекторию.
Процессы смены указанных величин существенно неравновесны, но среднее значение
параметров за цикл «равновесно» в том смысле, что система ведет себя так, как будто
строго гомеостатируется величина каждого из этих изменяющихся параметров.
Соответственно, средние за цикл значения параметров рН и nАТФ для каждого отрезка кривых CD, K1L1 и MNi, находятся на каждом из них. Таким
образом, достигается стабилизация процессов. Значение параметров рН, nАТФ, С и их скоростей роста V+ и убыли V- параметров
стабилизированы в пределах значений точек траектории. Устойчивость будет
нарушена, когда точка (nАТФср,
рНср) отрезка СD,
соответствующая среднему значению концентрации АТФ за цикл, достигнет точки С и
перейдет за нее. Последующий переход в низкоэнергетческое состояние может
сопровождаться гемолизом эритроцитов, в зависимости от взаимного расположения
точек К1 и С. Чем выше ордината точки К1 по сравнению с
ординатой точки С, тем выше вероятность гемолиза, так как при таком
расположении может нарушится баланс скоростей уменьшения и увеличения
количества в мембране липидов в сторону преобладания скоростей уменьшения
количества липидов. Подробное исследование не входит в данную работу.
Рассмотрим теперь неравновесный переход энергетического метаболизма
эритроцитов на новый уровень. Обратимся к рис. 12. На нем представлены те же
самые кривые, что на рис. 8.
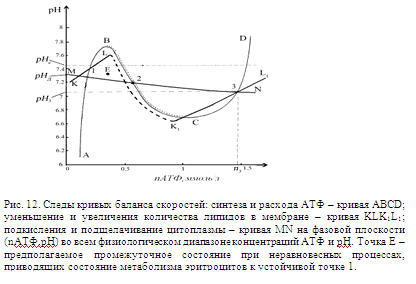
Если неравновесными процессами изменить концентрацию АТФ и рН так, что
соответствующая точка будет левее отрезка ВС, то возможен переход в устойчивое
состояние, соответствующее точке Е. Поскольку под кривой АВСD преобладает скорость расхода АТФ, то
последующее уменьшение концентрации АТФ приближает состояние эритроцита к
устойчивой точке 1. Одновременно точка оказывается под кривой KL, где доминируют процессы распада
липидов. Следовательно, при движении состояния системы к устойчивой точке 1,
возможно достижение критически минимального значения количества липидов, когда
клетка превратится в сферу и распадется. Вероятность распада тем больше, чем
дальше точка находится от кривой KL.
Итак, для проведения теоретического исследования кинетики энергетического
метаболизма эритроцитов in vivo с целью выяснения наличия устойчивых
состояний и их числа за основу была выбрана основная физическая модель,
предложенная в работе [15]. Эта модель была нами дополнена элементами,
приближающими рассмотрение метаболизма эритроцитов к in vivo. Дополненная (обобщенная) модель допускает
существование второй устойчивой точки гомеостатирования параметров (рН, nАТФ и С) при низкой концентрации АТФ.
Исследование выбранной модели позволило выяснить условия, при которых может
происходить переход метаболизма эритроцитов из одной устойчивой точки в другую.
Для надежного установления этого факта необходимо провести
экспериментальное исследование.
§ 2.3 Постановка экспериментальных задач
С целью экспериментальной проверки нашей гипотезы о возможности
реализации двух устойчивых состояний метаболизма эритроцитов необходимо
первоначально определить, каков их метаболизм эритроцитов in vitro после взятия пробы крови у пациента. Исследования
необходимо проводить на цельной крови, что гарантирует наибольшее приближение к
условиям in vivo. Для предотвращения свертывания крови следует
использовать гепарин, добавление которого в кровь существенным образом не
нарушает естественный ход процессов метаболизма эритроцитов. Возможно, при
нарушении связи «кровь-организм» при взятии крови из организма будут протекать
неравновесные процессы релаксации системы к новому состоянию. В конечном итоге
метаболизм эритроцитов может оказаться в одном из двух, указанных выше,
состояний.
§ 2.4 Неравновесные процессы, протекающие в плазме пробы
крови после ее взятия у донора, приводящие к изменению метаболизма эритроцитов
Когда кровь находится в организме, все процессы метаболизма в эритроцитах
согласованы, что соответствует точке 3 на рис. 8. После взятия пробы крови
нарушается работа регуляторных механизмов, стабилизирующих процессы метаболизма
клеток крови. Это происходит из-за распада сложных органических соединений в
плазме крови в результате деятельности протеолитических ферментов (пептидаз).
Поэтому для того, чтобы замедлить процессы ферментативного распада в
лабораторной практике используют специальные вещества, ингибирующие эти
процессы, - антипептидазы (ингибиторы протеолитических ферментов). Следствием
деятельности пептидаз в плазме пробы крови является повышение ее осмолярности.
В свою очередь такое повышение, если оно существенно по сравнению с уровнем
осмолярности внутренней среды, гомеостатируемой в организме, может нарушить
согласование равновесных процессов метаболизма эритроцитов, вызвав уменьшение
объема эритроцитов. Соответственно, в плазме крови концентрации всех веществ,
которые проходят через мембрану медленнее воды, понизятся, в том числе и
концентрация глюкозы. Изменения объема эритроцитов и уровня глюкозы в плазме
пробы крови можно контролировать с помощью известных приборов. В цитоплазме
эритроцитов концентрации биологически активных веществ, таких как ферменты,
регуляторные субстанции и др., не способных покинуть ее за время установления
нового равновесия по воде, наоборот возрастут. Наиболее важным следствием
протекания быстрых неравновесных процессов распада пептидов может оказаться
повышение концентрации АТФ. Тогда дальнейшая цепочка причинно-следственных
связей, приводящая к нарушению согласования метаболических процессов, будет
следующая. Повышение концентрации АТФ вызовет усиление деятельности K+/Na+-АТФазы, которое приведет к повышению
трансмембранной разности потенциалов. В свою очередь, такое изменение вызовет
увеличение напряженности поля в липидах, а это, согласно работе М.В. Фока [15],
приведет к уменьшению неспецифической проницаемости мембран эритроцитов для
кислорода. Из-за высокой проницаемости цитомембран для ионов Н+
концентрации их между плазмой крови и цитоплазмой эритроцита устанавливаются
практически в соответствии с соотношением Больцмана (4).
В организме рН плазмы крови гомеостатируется специальными системами,
поддерживающими проточный гомеостаз баланса процессов подкисления (ацидоз)
внутренней среды и ее подщелачивания (алкалоз). Алкалоз осуществляется,
благодаря процессам, происходящим в легких, тонкой кишке и коже, а ацидоз
обусловлен окислительными процессами во всех живых клетках. При взятии пробы
крови связь между организмом и кровью в пробе прекращается. Генерируемая на
мембране эритроцитов разность потенциалов между плазмой и цитоплазмой
распределяется по буферной емкости указанных двух сред (~40% - плазма, ~60% -
эритроциты). Поэтому, если какие-то процессы вызвали рост трансмембранной
разности потенциалов, то рН плазмы крови понижается и, наоборот, при уменьшении
трансмембранной разности потенциалов на мембране эритроцитов величина рН плазмы
крови будет повышаться. Изменения величины рН плазмы крови можно контролировать
с помощью известных приборов. Заметим, что после взятия пробы крови из
организма плазма крови по вышесказанной причине подкисляется, и устанавливается
новое равновесие по ионам Н+ между цитоплазмой и плазмой. рН плазмы
при этом будет ниже, чем in vivo. Чем ниже установившееся значение рН
плазмы крови, тем выше трансмембранная разность потенциалов на мембране
эритроцитов пробы.
В свете рассмотренных выше цепочек причинно-следственных связей
протекания процессов в крови, изменение кинетики энергетического метаболизма
эритроцитов, в рамках нашей модели (рис.8), представляется смещением кривой MN на фазовой плоскости в кислую
сторону. Если такое смещение имеет место, то нарушение согласования будет
проявляться в появлении колебаний параметров эритроцитов и связанных с этим
изменений концентрации глюкозы в плазме крови и объема эритроцитов. Наиболее
значимо для нас колебание рН плазмы крови и цитоплазмы эритроцитов, так как эти
колебания неизбежно вызывают быстрые неравновесные процессы ассоциации и
диссоциации осмотически активных частиц. Следствием протекания осмотических
процессов, в свою очередь, являются изменения концентрации глюкозы в плазме крови
и объема эритроцитов, которые можно наблюдать, и по ним судить о появлении
таких колебаний. Сродство отдельных соединений друг к другу и, следовательно,
способность образовывать комплексы, может сильно зависеть от величины рН.
Таким образом, согласно нашей модели после взятия пробы крови рН плазмы
устанавливается на более низком уровне, чем in vivo. Возрастание осмолярности плазмы крови вследствие
деятельности пептидаз приводит к новому осмотическому равновесию, которому
соответствует меньший объем эритроцитов и более высокая концентрация АТФ. При
этом нарушается согласование метаболических процессов эритроцитов, что
сопровождается колебаниями основных параметров рН, nАТФ. Рассмотренные причинно-следственные связи протекающих
неравновесных процессов показывают, что при этом должны наблюдаться колебания
концентрации глюкозы в плазме крови и объема эритроцитов. Временной ход величин
этих параметров можно наблюдать на опыте.
Итак, процессы устойчивого подкисления цитоплазмы, напрямую не связанные
с окислительными процессами утилизации глюкозы, способствуют переходу
метаболизма эритроцитов в низкоэнергетическое состояние после взятия пробы
крови.
Дальнейшие события могут развиваться по двум сценариям. В первом случае:
подкисление цитоплазмы эритроцитов не достигает критического уровня, указанного
в нашей модели (рис. 8). Тогда метаболизм эритроцитов останется на уровне,
близком к in vivo, то есть будет соответствовать высокой концентрации
АТФ, высокой величине трансмембранного потенциала и более низкому значению рН
плазмы по отношению к рН in vivo. Но из-за рассогласования процессов
неизбежны колебания основных параметров рН и nАТФ, а как их следствие, колебания измеряемых величин -
концентрации глюкозы в плазме и объема эритроцитов. Кроме того, высоким значениям
концентрации АТФ будут соответствовать высокие значения трансмембранного
потенциала и низкие значения неспецифической проницаемости эритроцитарных
мембран для кислорода.
Во втором случае: если рН цитоплазмы достигнет критически низкого уровня,
то состояние метаболизма эритроцитов может потерять устойчивость. Тогда
метаболизм эритроцитов перейдет в новое состояние, характеризующееся низкой
концентрации АТФ, низкой величиной трансмембранного потенциала и меньшей
скоростью подкисления цитоплазмы эритроцитов, чем в первом рассмотренном
случае. Из-за рассогласования процессов неизбежны колебания основных параметров
рН и nАТФ, и как их следствие, колебания
измеряемых величин концентрации глюкозы в плазме и объема эритроцитов. Кроме
того, низким значениям концентрации АТФ будут соответствовать низкие значения
трансмембранного потенциала и высокие значения неспецифической проницаемости
мембран для кислорода по сравнению с первым рассмотренным случаем.
Важным выводом теоретического исследования нашей качественной модели
энергетического метаболизма эритроцитов является возможность перехода системы
на другой устойчивый уровень вследствие протекания в ней естественных
релаксационных процессов непосредственно после взятия пробы крови из организма.
Поэтому в первую очередь необходимо проверить это положение. Основными
критериями для установления состояния метаболизма, в котором находится
эритроцит, являются различия следующих параметров в различных состояниях:
. рН;
. уровень глюкозы;
. показатель гематокрита - объем
Различия в величинах этих параметров необходимо устанавливать, анализируя
их временной ход после взятия пробы крови, так как мы не знали, осуществляется
ли указанный переход вообще. Если переход происходит, то в какой момент
времени. Надежно обнаружив и установив, что этот переход уже произошел и
система близка к стационарному состоянию, то подтверждением будут различия в
величине неспецифической проницаемости эритроцитарных мембран для двух
установившихся вариантов устойчивого метаболизма.
Для того чтобы производить сравнения нужно получить пробу крови с
состоянием метаболизма эритроцитов, близким к in vivo. Для этого необходимо устранить первопричину
нарушения метаболизма эритроцитов - осмотическое неравновесие, возникающее
после взятия пробы крови из организма. Для этого можно использовать препараты,
ингибирующие ферментативный распад соединений в плазме крови (антипептидаз).
Для надежности полученных результатов при сравнении следует также
получить пробу с заведомо низким энергетическим метаболизмом, добавляя в кровь
препараты, ингибирующие гликолиз. Мы применяли этиловый спирт.
Объем исследований позволяет достигнуть поставленной цели и надежно
установить возможность существования второго устойчивого состояния, либо его
отсутствия.
ГЛАВА 3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
§ 3.1 Цели экспериментальных работ
· Регистрация осмотического сжатия эритроцитов пробы крови,
непосредственно после ее взятия из организма, которое дает начало неравновесным
процессам установления нового уровня метаболизма эритроцитов.
· Регистрация колебательных процессов при установлении нового
уровня метаболизма, обусловленных рассогласованием процессов, определяющих
кинетику гомеостатирования основных параметров эритроцитов.
· Регистрация факта совершившегося перехода метаболизма
эритроцитов из состояния с высокой концентрацией АТФ в состояние с низкой его
концентрацией по выявлению отличий параметров различных проб крови.
Для достижения поставленных целей были проведены следующие
экспериментальные работы:
. Наблюдение временного хода концентрации глюкозы nгл в плазме пробы крови, которое
позволило по изменениям величины nгл судить о скорости синтеза АТФ в
эритроцитах, а также о протекании осмотических процессов в пробе крови, которые
происходят на временах меньших характерного времени прохождения глюкозы в
эритроцит (10 мин).
. Наблюдение временного хода показателя гематокрита Н пробы крови,
которое позволило по изменениям величины Н судить о протекании осмотических
процессов в пробе крови, идущих с характерными временами выше и сравнимыми с 15
мин.
. Наблюдение временного хода показателя кислотности рН плазмы
пробы крови, которое позволило по изменению величины рН судить об изменении
интенсивности энерговыделений в цитоплазме эритроцитов, изменении величины
трансмембранной разности потенциалов и, следовательно, об изменении
неспецифической проницаемости мембран эритроцитов.
. Измерение неспецифической проницаемости мембран эритроцитов,
которое позволило по величине этого параметра судить о величине трансмембранной
разности потенциалов и, в конечном итоге, об изменении уровня метаболизма
эритроцитов и изменении концентрации АТФ.
§ 3.2 Используемые приборы и установки
. Для измерения концентрации глюкозы в плазме крови использовался
глюкометр IME-DC с одноразовыми полосками, принцип действия которого основан
на измерении электропроводности пробы крови. Время одного измерения ~ 40 сек.
Подготовка глюкометра к экспериментам включала проверку его
работоспособности согласно инструкции. До проведения эксперимента брали каплю
крови из пальца здорового человека на специальную полоску. Затем с помощью
прибора определяли концентрацию глюкозы в плазме крови этой капли. Если
показания прибора попадали в физиологический диапазон значений измеряемой
величины, то считалось, что прибор работоспособен.
. Для измерения показателя гематокрита пробы крови использовалась
гематокритная центрифуга СМ-70 sky line. Частота
вращения - 5000 об/мин, время центрифугирования - 5 мин.
Подготовка гематокритной центрифуги СМ-70 sky line. Для работы центрифуги использовались гепаринизированные
капилляры длиной 75 мм, объемом - 60-75 мкл. Для закупорки одной стороны
капилляров использовался пластилин.
. Для измерения показателя кислотности рН использовался рН-метр с
водородным электродом. Время одного измерения ~ 5мин.
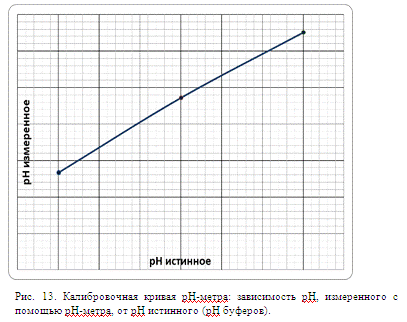
Для подготовки к эксперименту была снята калибровочная кривая рН-метра.
Для этого использовались три стандартных раствора с известным рН: рН1=10,01;
рН2=4,01; рН3=7,01. Калибровочная кривая представлена на
рис. 13. Она построена по трем точкам, которые получены для каждого из буферов
путем усреднения по 5 измерениям рН. Погрешность каждой экспериментальной точки
не превышает 1%.
4. Для измерения величины неспецифической проницаемости
использовалась установка КИНОКС, которая включает в себя прибор КИНОКС (схема
его действия представлена на рис. 14) и персональный компьютер.
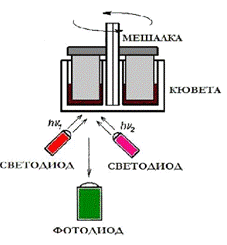

Принцип действия прибора «КИНОКС»
В приборе КИНОКС наблюдается процесс обмена кислородом между цитоплазмой
эритроцита и плазмой крови, в которую, в свою очередь, кислород поступает из
контактирующей с кровью газовой среды. Основным параметром, регистрируемым
прибором, является степень насыщенности крови кислородом, определяемая
оптическим путем. В результате находят зависимость этой величины от времени. В
результате анализа полученных зависимостей можно судить о кислородной
проницаемости мембран эритроцитов крови [17, 18].
Основные узлы и элементы прибора «КИНОКС»:
. Оптоэлектронный блок, включающий в себя светодиоды, работающие в
красной и инфракрасной областях спектра (на длинах волн 0,65 мкм и 0,96 мкм
соответственно), и фотодиод.
. Кювета, выполненная из прозрачного материала (оргстекла).
. Механическая мешалка с двумя лепестками, выполненными из гибкого
пластика, толщину и жесткость которых можно варьировать.
. Шаговый двигатель, с помощью которого вертится мешалка.
. Термостат, позволяющий поддерживать температуру кюветы на уровне
27 ˚С.
В кювете имитируются процессы кислородного обмена между эритроцитами и
тканями-потребителями кислорода. При этом взаимодействие эритроцитов со
стенками кюветы и лепестками мешалки имитирует взаимодействие со стенками
капилляров. Степень этого взаимодействия определяет величину неспецифической
проницаемости мембран эритроцитов.
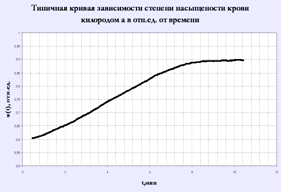
На рис. 15 представлена типичная кривая зависимости степени насыщенности
крови кислородом от времени. Производная по времени в каждой точки данной
кривой прямо коррелирует с величиной неспецифической проницаемости
эритроцитарных мембран для кислорода.

Подготовка установки КИНОКС проводилась без использования пробы крови.
Проверка его работоспособности включала запуск вращения мешалки. Если мешалка
работает, то прибор готов к проверке действия программы управления
экспериментом. При включении программы на дисплее ЭВМ должны появляться
горизонтальные линии. Если прибор работоспособен, то эти линии со временем
удлиняются и срабатывает команда на окончание работы прибора, когда
заканчивается время, указанное программе.
Инструментальная погрешность отдельного измерения, оцененная в более
ранних исследованиях, составляет менее 1%.
§ 3.3 Используемые материалы
В исследованиях использовалась цельная кровь, взятая из вены здорового
человека в 4 шприца, по 9мл в каждый. До взятия крови в каждый из шприцов были
добавлены следующие вещества:
№1. гепарин - 1мл;
№3. гепарин - 1 мл, стандартный раствора антипептидаз объемом 250, 500
и 1000 мкл для различных серий экспериментов;
№4. гепарин - 1мл, в первой серии экспериментов - 1 мл цитрата натрия;
во второй и третьей серии экспериментов - этиловый спирт объемом 500 мкл и 100
мкл соответственно.
Из шприцов подготовленная таким образом кровь, выливалась в пробирки с
соответствующей нумерацией.
Для подготовки этих проб крови использовались следующие растворы:
· раствор Рингера (300 мОсм):
Дистиллированная вода 100 мл;
NaCl6,8
г/л * 100 мл = 0,68 г;
KCl0,22
г/л * 100 мл = 0,022 г;
CaCl20,11 г/л *
100 мл = 0,011 г;
NaHCO3 0,17 г/л *
100 мл = 0,017 г.
· раствор цитрата натрия (300 мОсм):
Дистиллированная вода 50 мл;
Цитрат Na(50 г / 100 %) * 3,8 % = 1,9 г.
§ 3.4 Методики проведения экспериментальных работ
· Получение временного хода концентрации глюкозы для каждой
пробы, приготовленной по описанию в § 3.3 «Используемые материалы», включало в
себя получение 10-12 экспериментальных точек за 3 часа. Перед началом
эксперимента концентрацию глюкозы измеряли в капле крови, взятой из пальца того
же человека. Это измерение производится гораздо быстрее, чем аналогичное
измерение для пробы крови, взятой из вены. Поэтому полученное значение
концентрации глюкозы в плазме крови, взятой из пальца, можно считать наиболее
близким к in vivo. В сериях экспериментов интервалы между получаемыми
точками варьировались в зависимости от поставленной цели. Когда требовалось
убедиться в наличии колебаний в пробе крови, вызванных быстрыми осмотическими процессами,
происходящими за время, меньшее характерного времени прохождения глюкозы в
эритроцит (10 мин) [19], то интервалы устанавливались менее 10 мин. Когда этого
не требовалось, то интервалы устанавливались большие.
Так как показания глюкометра иногда были нестабильны и наблюдались
выбросы (как в сторону уменьшения, так и в сторону увеличения показаний), то
для устранения ошибок для каждой точки проводилось по 2 измерения, а если
показания прибора при этом не совпадали в определенных пределах, то проводили и
третье измерение. В этом случае при формировании экспериментальной точки,
усредняя ее по измеренным величинам, выброс не учитывался. Одно измерение
концентрации глюкозы занимало ~40 сек, следовательно, получение одной
экспериментальной точки, как правило, ~80 сек, а при наличие выброса ~120 сек.
Средняя ошибка одного измерения концентрации глюкозы определялась на
стабилизированной крови посредством пяти измерений концентрации глюкозы в ней,
и вычислялась по формуле (5):
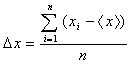 ,
,
где
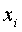 - значение концентрации глюкозы в каждом из пяти
измерений,
- значение концентрации глюкозы в каждом из пяти
измерений, 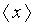 - среднее значение концентрации глюкозы по пяти
измерениям, n - количество измерений.
- среднее значение концентрации глюкозы по пяти
измерениям, n - количество измерений.
· Методика наблюдения временного хода показателя гематокрита в
пробах крови. Гематокритная центрифуга позволяет проводить измерение для 12
капилляров. Как правило, одновременно получали экспериментальные точки для 4
проб крови, при этом центрифугировали по 3 капилляра для каждой из проб. Если
одновременно экспериментальная точка определялась для двух проб, то
центрифугировали по 6 капилляров для каждой пробы крови. Усреднением по
измеренным значениям (3-м или 6-ти капиллярам) показателя гематокрита получали
экспериментальную точку и оценивали среднюю ошибку измерения по формуле (5).
Одно измерение показателя гематокрита занимало не менее 20 минут,
поскольку включало набор крови в капилляры - 8-10 минут, центрифугирование - 5
минут, измерение длины столба осевших эритроцитов и полной длины столба крови в
капилляре - 5 минут. Поэтому за 3 часа наблюдений получали 7-8
экспериментальных точек. Таким образом, получали ход величины показателя
гематокрита, усредненный по возможным быстрым осмотическим колебаниям объема
эритроцитов, если такие были.
· Методика наблюдения временного хода показателя кислотности рН
в пробах крови. Одно измерение рН в плазме пробы крови занимало ~ 1 мин.
Подготовка рН-метра к измерению рН следующей пробы крови занимало ~ 2 мин. За 3
часа наблюдений для каждой пробы крови было получено 6-8 точек.
· Методика измерения неспецифической проницаемости мембран
эритроцитов проб крови для кислорода. С помощью прибора КИНОКС были выполнены
отдельные измерения для регистрации факта перехода метаболизма эритроцитов из
состояния, близкого к in vivo, в состояние с низкой концентрацией
АТФ. В первой и второй серии экспериментов проницаемость мембран эритроцитов не
измерялась. По данным этих серий было выяснено, через какое время t после взятия крови из организма
параметр (концентрация глюкозы) относительно стабилизируется. В третьей серии
первое измерение проницаемости проводилось через это время t для каждой из проб, а второе ее
измерение проводилось через 3 часа после начала эксперимента. Характерное время
получения кривой оксигенации составляло ~ 8 мин.
Инструментальная погрешность отдельного измерения, оцененная в других
исследованиях, составляла менее 1%. Случайный разброс от образцов крови получен
в предыдущих исследованиях с данным прибором, составляет несколько больше (1-2%).
§ 3.5 Результаты экспериментов и их обсуждение
Для регистрации осмотического сжатия эритроцитов пробы крови - были
получены временные ходы концентрации глюкозы и показателя гематокрита в пробе
крови, подготовленной по описанию пробы №1 в § 3.3 «Используемые материалы».
Измерения указанных характеристик проводились параллельно в течение 3-х часов
после взятия пробы крови из организма. Методика проведения этих экспериментов
описана в § 3.4 «Методики проведения экспериментальных работ» в пунктах 1, 2.
Типичный результат первых опытов (рассмотрено более 10 проб крови от
различных доноров), полученных ранее сотрудниками нашей группы [20],
представлен на рис. 16. На нем показан временной ход концентрации глюкозы
(верхняя кривая) и временной ход показателя гематокрита (нижняя кривая) пробы
крови.
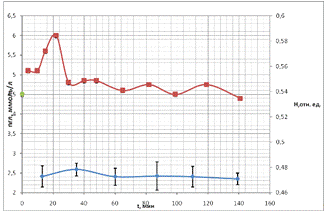

Из графика видно, что начальная экспериментальная точка во всех опытах
измерения концентрации глюкозы, полученная в пробе крови, оказывалась выше, чем
в пробе крови, взятой непосредственно из пальца (она показана на оси ординат,
где представлены значения концентрации глюкозы). Первая экспериментальная точка
из пробы была получена через 3-4 минуты после измерения концентрации глюкозы в
плазме крови, полученной из пальца. Погрешность измерения концентрации глюкозы
была посчитана по формуле (5) и ее значение не выходит за размеры точки на
графике.
Временной ход показателя гематокрита, как видно из рис. 16, в пределах
погрешности меняется незначительно. Следовательно, по этой характеристике
нельзя судить о первоначальном изменении объема эритроцитов.
Теоретический анализ показывает, что первоначальное осмотическое сжатие
эритроцитов имеет место из-за распада пептидов в плазме пробы крови,
осуществляемого пептидазами. Однако в представленном эксперименте это сжатие не
наблюдалось. Было сделано предположение о том, что осмотические процессы
настолько быстры, что мы не успеваем их увидеть за время, прошедшее от взятия
крови из вены до первого измерения (не менее 2-х минут).
Для того чтобы убедиться в правильности этого предположения, была
проведена отдельная серия опытов. Были получены временные ходы концентрации
глюкозы в пробах крови, подготовленных по описанию проб №1, №2 (с 50 мкл
антипептидаз) в § 3.3 «Используемые материалы». Антипептидазы ингибируют
ферментативный распад пептидов на отдельные аминокислоты, тем самым увеличивая
время, за которое происходит этот распад.
Типичный результат показан на рис. 17 приведены результаты такого опыта.
Временной ход показателя гематокрита не приводится из-за его не
информативности, так как время одного измерения больше характерного времени
протекания быстрых осмотических процессов, описанных выше.
гемоглобин
эритроцит метаболизм энергетический
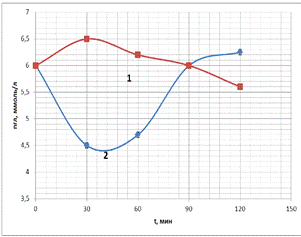

На рис. 17 представлены временные ходы концентрации глюкозы в плазме
пробы крови: 1 - без добавления антипептидаз, 2 - с добавлением антипептидаз.
Видно, что кривая 2 имеет «провал» в значениях концентрации глюкозы в первый
час наблюдения. Ход кривой 1 не отличался от хода кривых в экспериментах,
сделанных ранее.
Такое уменьшение концентрации глюкозы в пробе крови с применением
антипептидаз свидетельствует о наличии сжатия эритроцитов. Таким образом, наше
предположение о том, что ферментативный распад пептидов в плазме крови вызывает
осмотическое сжатие эритроцитов и, что эти процессы происходят очень быстро (за
время меньшее 5 мин), верно. Такое первоначальное осмотическое сжатие может
дать начало неравновесным процессам, впоследствии приводящим к установлению
нового уровня энергетического метаболизма.
В опытах, ставящих своей целью регистрацию колебательных процессов, были
получены временные ходы концентрации глюкозы в пробах крови, подготовленных по
описанию проб №1, №2 (с 50 мкл антипептидаз), №3 (250 мкл антипептидаз), №4 (с
цитратом натрия) в § 3.3 «Используемые материалы». Время наблюдения колебаний
продолжалось в течение 1 часа. Чтобы получить осмотические колебания,
предсказанные теоретическим анализом, получали экспериментальные точки через
максимально короткий промежуток времени для всех 4-х пробирок параллельно (раз
в 2 минуты). Временные ходы концентрации глюкозы для 4 проб показаны на рис.18
(а, б, в, г) в течение одного часа. Во всех 4-х пробах крови наблюдались
осмотические колебания.
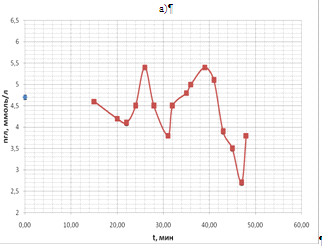
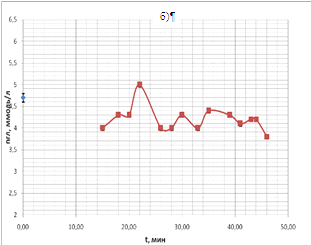
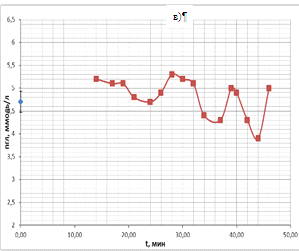
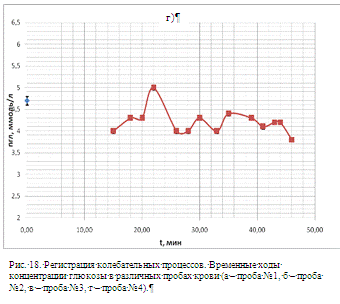
Таким образом, из этих экспериментов видно, что в пробах крови происходят
быстрые колебательные процессы, связанные с рассогласованием процессов
энергетического метаболизма, как это предсказано теоретическим анализом.
Для того, чтобы определить оптимальное время после взятия крови из
организма для проведения измерения неспецифической проницаемости эритроцитарных
мембран для кислорода, была проведена следующая серия экспериментов. Были
получены временные ходы концентрации глюкозы в пробах крови, подготовленных по
описанию проб №1, №2 (с 250 мкл антипептидаз), №3 (500 мкл антипептидаз) в §
3.3 «Используемые материалы». Полученные кривые представлены на рис. 19 (а, б,
в).
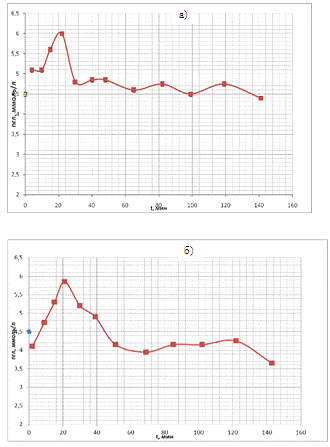
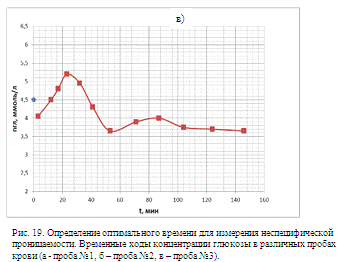
Из рисунков видно, что через час после взятия крови из организма
происходит относительная стабилизация концентрации глюкозы в плазме проб крови,
когда колебания этого параметра становятся много меньше колебаний, происходящих
в первый час наблюдений. Таким образом, проницаемость в следующей серии опытов
необходимо измерять через час после взятия крови из организма. Следующая серия экспериментов ставила своей целью регистрацию
факта совершившегося перехода метаболизма эритроцитов из состояния с высокой
концентрацией АТФ в состояние с низкой его концентрацией по выявленным отличиям
параметров различных проб крови. Теоретический анализ показывает, что этот
переход должен совершиться быстрее в пробах, в которых нет антипептидаз, по
сравнению с пробами, в которых они есть. Были получены временные ходы
концентрации глюкозы и показателя кислотности рН в пробах крови, подготовленных
по описанию проб №1, №2 (с 500 мкл антипептидаз), №3 (1000 мкл антипептидаз),
№4 (с этиловым спиртом) в § 3.3 «Используемые материалы». В данной серии
использовался спирт из-за того, что он лучше проходит в эритроциты, чем цитрат
натрия. Наблюдения временных ходов концентрации глюкозы и рН для каждой пробы
проводились параллельно.
Дополнительно через час после начала наблюдений и по окончании
эксперимента (через 3 часа после взятия крови из организма) измерялась величина
неспецифической проницаемости мембран для кислорода с помощью прибора КИНОКС
каждой пробы.
Временные ходы концентрации глюкозы приведены на рис. 20 (а, б, в, г).
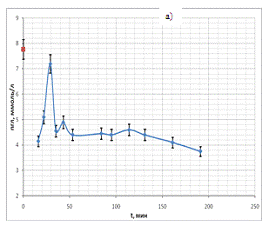
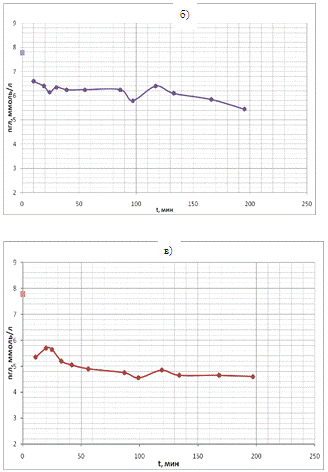
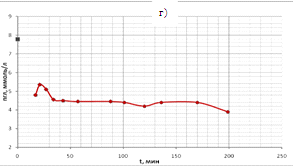

Характер хода кривых концентрации глюкозы в данной серии экспериментов
существенным образом не отличался от ходов кривых, полученных в предыдущих
опытах, но есть отличия в мелких деталях.
На рис. 21 представлены временные ходы показателей кислотности рН для
всех проб.
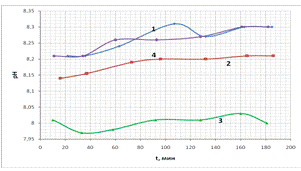

Наиболее значимыми являются начальные точки, полученные через 10-20 минут
после взятия крови из организма. За это время произошло подкисление плазмы за
счет выхода ионов Н+ из эритроцитов (кислые продукты гликолиза,
накапливаемые в цитоплазме, выходят в плазму крови). С другой стороны,
происходит подщелачивание плазмы крови за счет распада бикарбонатов и выхода
образующегося СО2 в атмосферу, поскольку специальных мер для
задержки его мы не предпринимали. Перемешивание крови в пробах производилось с
одинаковой интенсивностью. Видно, что начальные точки значений рН для пробы
крови без добавления антипептидаз и с добавлением спирта практически совпадают.
Начальные точки для проб с добавлением антипептидаз существенно ниже по рН, чем
начальные точки, полученные для остальных двух проб (1 и 4). Этот факт
свидетельствует о том, что переход уже совершился в 1-й и 4-й пробе крови.
Такой переход во второй и третьей пробе не произошел, так как состояние
метаболизма эритроцитов в этих пробах наиболее близко к in vivo (за счет замедления неравновесных осмотических
процессов). Это соответствует предположению, сделанному в теоретическом
анализе, о том, что рН нового состояния метаболизма эритроцитов выше, чем в
состоянии in vivo.
Еще до измерения проницаемости было замечено, что при перемешивании крови
для предотвращения оседания эритроцитов, кровь в 1-й и 4-й пробе быстрее
насыщалась кислородом, чем во 2-й и 3-й пробе. Об этом мы судили по цвету крови
в пробирках: в 1-й и 4-й - алая, во 2-й и 3-й - темная. На фотографии,
сделанной в день эксперимента, это хорошо было видно (см.фото1).


Последующее определение проницаемости мембран подтвердило, что величина
проницаемости мембран эритроцитов в пробах 1, 4 значительно выше, нежели чем во
второй и третьей.
На рис. 22 представлен временной ход величины степени насыщения крови
кислородом для 3-х проб крови (2,3,4). Номера кривых соответствуют номерам проб
крови.
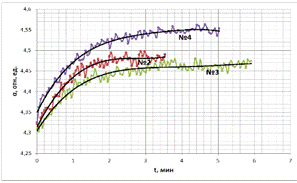

Как известно из работ Фока М.В. [17, 18] по мере насыщения крови
кислородом на заключительном этапе процесса оксигенации проницаемость мембран
эритроцитов резко уменьшается. Сравнение степени насыщения проб крови было затруднено
тем обстоятельством, что 1 и 4 пробы были уже в значительной мере насыщены
кислородом. В то время как кровь во 2-й и 3-й пробе была практически не
оксигенирована. Поэтому сравнение проницаемости проводилось при одной и той же
степени насыщения крови кислородом, что и представлено на рис. 22. Временной
ход степени насыщения первой пробы кислородом не представлен на данном графике,
так как эта проба крови находилась в насыщении кислородом, и уровень сигнала
находился на более высоком уровне, что препятствовало сравнению. Значимы
начальные участки кривых, чем больше угол наклона кривой к горизонтальной оси,
тем выше проницаемость мембран для кислорода.
Результат сравнения говорит о том, что проницаемость мембран эритроцитов
1-й и 4-й пробы выше, нежели чем для 2-й и 3-й. Совокупность результатов в этой
серии экспериментов позволяет нам утверждать, что переход состояния метаболизма
эритроцитов в пробах 1-й и 4-й уже произошел, и мы наблюдали следствия этого
перехода. Состояния метаболизма эритроцитов пробы 2-й и 3-й практически
соответствует состоянию in vivo. Интенсивность энерговыделения при
утилизации глюкозы эритроцитами в 1-й и 4-й пробе ниже и, следовательно,
подкисления крови существенно ниже, чем в пробах 2 и 3. Значит, в 1-й и 4-й
пробе метаболизму эритроцитов соответствует состояние с низкой концентрацией
АТФ, а метаболизму в пробах 2 и 3 - состояние с высокой концентрацией АТФ, как
и было предсказано теоретическим анализом.
§ 3.6 Выводы
Итак, в данной работе теоретически и экспериментально доказано
существование двух устойчивых состояний метаболизма эритроцитов.
Низкоэнергетическое состояние наблюдалось in vitro. Высокоэнергетическое состояние подробно рассмотрено
в других работах, и наиболее полно в работе Атауллаханова Ф.И.
Для теоретического исследования возможности существования второго
устойчивого состояния энергетического метаболизма эритроцитов в данной работе
была выбрана физическая модель, соответствующая состоянию крови in vivo. При анализе кинетики гомеостатирования основных
параметров эритроцитов согласно этой модели были выяснены условия, при которых
может происходить переход метаболизма эритроцитов из одной устойчивой точки в
другую. Выявлены процессы, протекающие при взятии крови из организма,
способствующие указанному переходу. Ведущим процессом, обуславливающим переход
эритроцитов в новое низкоэнергетическое состояние, является их осмотическое
сжатие в результате деятельности в плазме крови протеолитических ферментов -
пептидаз. Обнаружены колебательные процессы в цельной крови после ее взятия из
организма, как это предсказывал теоретический анализ. Был зарегистрирован факт
совершившегося перехода в экспериментах по выявленным отличиям параметров проб
крови, в которых, по нашему мнению, этот переход мог произойти, от тех проб, в
которых искусственно этот переход с помощью добавления соответствующих доз
антипептидаз был задержан.
Показано, что переход метаболизма эритроцитов в низкоэнергетическое
состояние при длительном хранении консервированной крови неизбежен. Так как в
эритроцитах в результате их энергетического метаболизма непрерывно
накапливаются кислые продукты, и цитоплазма эритроцитов подкисляется. По
достижению критически низкого уровня значения кислотности рН, неизбежно
происходит быстрый переход в низкоэнергетическое состояние. При этом в
эритроцитах и плазме крови протекают быстрые неравновесные процессы, которые мы
наблюдали на опыте. Однако изучение этих переходных процессов не являлось
предметом данного исследования.
Обнаружено, что нарушение устойчивости высокоэнергетического состояния
происходит менее чем за 10 минут. Вещества, ингибирующие гликолиз, могут
ускорять процессы потери устойчивости высокоэнергетического состояния, в то
время как добавки, ингибирующие первичный рост осмолярности, затягивают
процессы перехода. Подробное изучение переходных процессов не являлось
предметом нашего исследования.
§ 3.7 Некоторые практически важные замечания
С позиций результатов, полученных в данной работе, стратегия разработки
методов, улучшающих функциональные характеристики крови при ее консервации, и
разработанные методом проб и ошибок методики сводятся к тому, чтобы как можно
большее время сохранить высокую концентрацию АТФ, замедляя переход метаболизма
эритроцитов из высокоэнергетического состояния в низкоэнергетический.
Добавление аденозина в консервированную кровь и хранение эритроцитарной массы
отдельно от плазмы, улучшившие показатели функциональной способности
эритроцитов, продлевают промежуток времени до указанного перехода. Конечно,
кровь, находящаяся в низкоэнергетическом состоянии, не способна в полной мере
выполнять свою основную транспортную функцию. Однако при хранении такая кровь
значительно медленнее подкисляется. Поэтому нам кажутся перспективными
разработки методик, переводящих эритроциты в высокоэнергетическое состояние
непосредственно перед переливанием.
Заключение
Переливание крови в медицинской практике распространено очень широко,
потребность в донорской крови непрерывно возрастает. Зачастую от наличия крови,
годной к переливанию, особенно в больших объемах, зависит жизнь пациента.
Поэтому любые продвижения в исследованиях поддержания функциональной
способности эритроцитов в донорской крови чрезвычайно актуальны. В этом
заключается ценность данной работы.
СПИСОК ЛИТЕРАТУРЫ
1. Физиология
в рисунках и таблицах: вопросы и ответы./ Под ред. В. М. Смирнова.
М.:Медицинское информационное агентство, 2007
. ЛевтовВ.А.,
Регирер С.А., Шадрина Н.Х. Реология крови. М.: Медицина, 1982;
. Нормальная
физиология человека./ Под ред. академика РАМН Б.И. Ткаченко. М.: Медицина, 2005
. Иржак
Л. И. Гемоглобины и их свойства. М.: Наука, 1975;
. Блюменфельд
Л.А. Гемоглобин и обратимое присоединение кислорода. М.: Сов. Наука, 1957;
. Блюменфельд
Л.А. Гемоглобин.// Соросовский образовательный журнал. - 1998. - №4;
. Зенгбуш
П., Молекулярная и клеточная биология в 3-х томах. Под ред. В.А. Энгельгарда
М.: Мир, 1982;
. Гааль
Э., Медьеши Г., Верецки Л. Электрофорез в разделении биохимических
макромолекул. - М.;
. Фок
М.В. Некоторые аспекты биохимической физики, важные для медицины. М.:Физматлит,
2007;
. Фок
М.В., Зарицкий А.Р. Авторегуляция, как основа гомеостаза клеток. М.:
Космосинформ, 1997;
. Фок
М.В., Зарицкий А.Р., Зарицкая Г.А., Переведенцева Е.В. Авторегуляция
неспецифической проницаемости мембраны эритроцита. М.: Наука, 1999;
12. Ataullakhanov
FI, Vitvitsky VM. What determines the intracellular ATP concentration. Biosci
Rep. 2002; 22(5-6):501-11. Review.
. Атауллаханов
Ф.И. Регуляция метаболизма в эритроцитах.// Диссертация на соискание ученой
степени д. ф.-м. н. М.: 1982;
. Кайманчиков
Н.П., Сельков Е.Е. Автокатализ в стехиометрической модели энергетического
метаболизма. - Биофизика, 1976, т.21, с.220-226;
. Зарицкий
А.Р., Пронин В.С. Биофизика основных режимов клеточного метаболизма.
Функциональные режимы клетки: состояние покоя и активность. М.// Краткие
сообщения по физике ФИАН №12, 2006, с. 8-18
. Виноградова
М.А., Зарицкий А.Р., Пронин В.С., Распопов Н.А., Фок М.В. Необратимое изменение
метаболизма эритроцитов как основная причина возникновения стресса у больного
при переливании ему консервированной донорской крови. Краткие сообщения по
физике ФИАН 35(6), 39 (2008).
. Фок
М.В., Зарицкий А.Р., Зарицкая Г.А., Переведенцева Е.В. Биофизическая кинетика
переноса кислорода кровью// Успехи физических наук. 1994. Т. 164, № 3;
. Фок
М.В., Зарицкий А.Р., Прокопенко Г.А. Динамика оксигенации эритроцитов in vitro// Биофизика. 1988. Т. 33, вып. 4.
. Фок
М.В., Зарицкий А.Р., Переведенцева Е.В. и др. Исследование диффузии глюкозы
через мембрану эритроцитов// Биофизика. 1994. Т. 39, вып. 5.
. С.П.
Баранов, М.А. Виноградова, А.Р. Зарицкий, М.Н. Маслова, В.С. Пронин, Н.А.
Распопов, Д.А.Семёнов, Л.Л. Чайков, М.Н.Черноусова. Исследование процессов
утилизации глюкозы и проницаемости эритроцитарных мембран in vitro. М. // Краткие сообщения по физике ФИАН, № 11, 2008,
с. 42-51.