Теоретические основы теплотехники
ВВЕДЕНИЕ
В настоящее время во всех сферах человеческой
деятельности используется тепло. Ученые давно изучили основные закономерности
переноса и использования теплоты. Но как научиться правильно использовать
тепло? Как получить новые и эффективные источники тепла? Именно эти вопросы
помогает решить термодинамика. Термодинамика представляет собой науку о
закономерностях превращения энергии. Основным содержанием технической
термодинамики является изучение процессов взаимного преобразования тепловой и
механической энергии.
При изучении термодинамики особое внимание
следует уделить усвоению термодинамического метода исследования, который имеет
следующие особенности. Во-первых, термодинамика строится по дедуктивному
принципу, т. е. от общего к частному. Её основной особенностью являются два
закона (начала), установленных опытным путём. Первый из них представляет
специфическую форму закона сохранения и превращения энергии и имеет, поэтому
всеобщий характер, второй - устанавливает качественную направленность процессов,
осуществляемых в физических системах. С помощью математического аппарата
термодинамики получают соотношения, позволяющие решать конкретные задачи
(например, рассчитывать термодинамические процессы). Во-вторых, термодинамика
имеет дело только с макроскопическими величинами. Процессы здесь
рассматриваются как непрерывная последовательность состояний равновесия.
Термодинамика рассматривает равновесные процессы
и равновесные состояния, так как только равновесные состояния могут быть
описаны количественно с помощью уравнений состояния. Лишь равновесные процессы
изменения состояния термодинамической системы можно изображать графически.
Цель выполнения работы - закрепление и
углубление полученных знаний, ознакомление с необходимой справочной
литературой, государственными и отраслевыми стандартами, получение навыков
самостоятельного решения инженерных задач и технически грамотного изложения
пояснительной записки.
Расчеты в курсовой работе иллюстрированы
графиками и рисунками, рассмотрены газовые процессы, циклы, паросиловые
установки, а также циклы трансформаторного тепла.
1.
ГАЗОВЫЕ ПРОЦЕССЫ
физический термодинамический теплота
энергия
1.1 Задача 1
Газ с начальной температурой Т1 = 300
К и давлением р1 = 0.1 МПа политропно сжимается в компрессоре до
давления р2. Определить недостающие начальные параметры v1,
u1, h1, s1, конечные параметры T2,
v2, u2, h2, s2, тепло q1-2,
работу l1-2, изменение параметров в процессе ∆u1-2,
∆h1-2, ∆s1-2. Построить процесс в диаграммах
p, v и T, s (в масштабе).

Решение:
Для расчетов неизвестных параметров необходимо
рассчитать газовую постоянную. Газовая постоянная является индивидуальной для
каждого газа, то есть зависит от молекулярной массы газа и рассчитывается по
формуле:
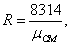 (1.1)
(1.1)
где mсм - это
кажущаяся молекулярная масса, она зависит от пропорции компонентов, из которых
состоит смесь газа.
В данном случае имеется газ О2,
и для него газовая постоянная будет равна:
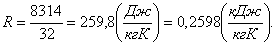
Так же понадобится для расчетов
изобарная (ср) и изохорная (сv) теплоемкости. Так как
данный газ О2 - двухатомный, следовательно изобарная теплоемкость
равна:
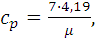
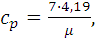 (1.2)
(1.2)
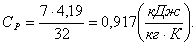
а изохорная теплоемкость равна:
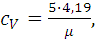
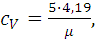 (1.3)
(1.3)
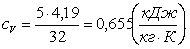
Объем при нормальных условиях будет
равен:
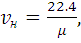
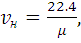 (1.4)
(1.4)
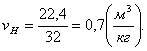
Определение недостающих начальных
параметров.
Определим начальный объем v1
Из уравнения Клапейрона:
= RT, (1.5)
Для данного случая начальный объем
будет равен:
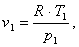 (1.6)
(1.6)
где R - газовая постоянная, кДж/кгК;
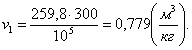
Т1 - начальная
температура, К;
р1 - начальное давление,
Па.
Найдём начальную внутреннюю энергию
u1.
Величина внутренней энергии газа
зависит как от скорости движения молекул и атомов, так и от расстояния между
ними. Скорость движения микрочастиц вещества зависит от температуры тела, а
силы взаимодействия между ними - от удельного объема. Поэтому внутреннюю
энергию можно представить в виде:
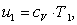 (1.7)
(1.7)
где сv - изохорная теплоемкость газа,
кДж/кгК;
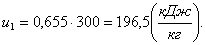
Определим энтальпию h1 в начале
процесса.
Энтальпия газа так же, как и внутренняя энергия,
зависит только от температуры. Следовательно, энтальпия h1 в начале
процесса рассчитывается по формуле:
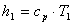 , (1.8)
, (1.8)
где ср - изобарная теплоемкость газа,
кДж/кгК;
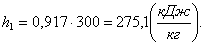
Вычислим энтропию s1 в
начале процесса.
В уравнении первого закона
термодинамики dq = du + pdv только du полным является дифференциалом внутренней
энергии u. Введением множителя 1/Т можно привести это уравнение к уравнению в
полных дифференциалах:
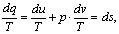 (1.9)
(1.9)
где ds - полный дифференциал параметра s, то
есть энтропии.
Для идеальных газов pv = RT, du = cvdT,
поэтому
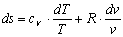 . (1.10)
. (1.10)
После интегрирования (1.10) получаем расчетную
формулу для определения энтропии:
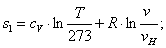 (1.11)
(1.11)
где v-
начальный объем, м3/кг.
Согласно формуле (1.11) энтропию s1
в данном случае рассчитаем по формуле:
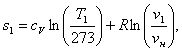 (1.12)
(1.12)
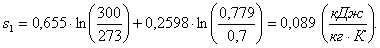
Определение недостающих конечных параметров.
Определим конечную температуру Т2.
Температуру Т2 найдем из соотношения
между параметрами политропного процесса:
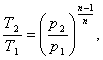 (1.13)
(1.13)
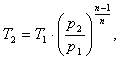 (1.14)
(1.14)
где Т2 - конечная температура, К;
р2 - конечное давление, Па;-
показатель политропы.
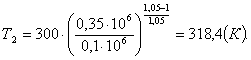
Найдём конечный объем v2.
Из формулы (1.5) для данного случая
найдем конечный объем v2:
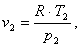 (1.15)
(1.15)

Определим конечную внутреннюю
энергию u2.
Аналогично u1 найдем
конечную внутреннюю энергию u2 по формуле:
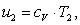 (1.16)
(1.16)
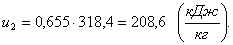
Определим энтальпию h2 в конце
процесса.
Аналогично h1 найдем энтальпию h2
в конце процесса по формуле:
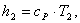 (1.17)
(1.17)
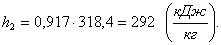
Найдём энтропию s2 в конце процесса.
Аналогично s1 находим энтропию s2
в конце процесса по формуле:
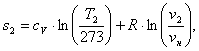 (1.18)
(1.18)
где v2 - конечный объем, м3/кг,
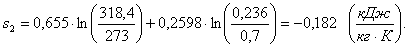
Определение тепла, работы и
изменения параметров внутренней энергии, энтальпии и энтропии.
Определим тепло q1-2 в
данном процессе.
Количество тепла в политропном
процессе рассчитывается по формуле:
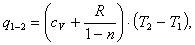 (1.19)
(1.19)
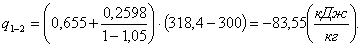
Вычислим работу l1-2 в
данном процессе.
Для политропного процесса работа
рассчитывается по формуле:
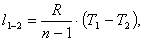 (1.20)
(1.20)
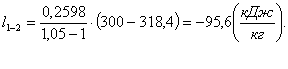
Определим изменение внутренней
энергии ∆u1-2.
Изменение внутренней энергии можно
рассчитать по формулам:
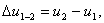 (1.21),
(1.21), 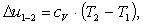 (1.22)
(1.22)
∆u1-2 находим по
формуле (1.22):
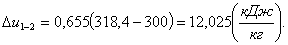
Определим изменение энтальпии ∆h1-2.
Аналогично изменение внутренней
энергии ∆u1-2 можно рассчитать изменение энтальпии ∆h1-2
по формулам:
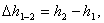 (1.23)
(1.23)
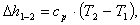 (1.24)
(1.24)
∆h1-2 находим по
формуле (1.24):
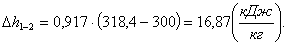
Определим изменение энтропии ∆s1-2.
Как и изменение внутренней энергии,
изменение энтропии ∆s1-2 можно рассчитать:
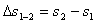 , (1.25)
, (1.25)
или
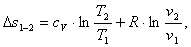 (1.26)
(1.26)
∆s1-2 находим по
формуле (1.26):
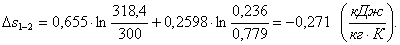
Все ответы приведены в таблице 1.1
Таблица 1.1 - Результаты начальных и
конечных параметров, тепло, работа, изменение параметров.
|
Неизвестные
параметры
|
Р1,
МПа
|
Т1,
К
|
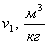 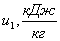 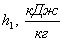 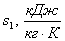
|
|
|
|
|
Полученный
результат
|
0,1
|
300
|
0,779
|
196,5
|
275,1
|
0,089
|
|
Неизвестные
параметры
|
Р2,
МПа
|
Т2,
К
|
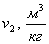 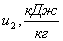 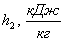 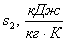
|
|
|
|
|
Полученный
результат
|
0,35
|
318,4
|
0,236
|
208,55
|
291,97
|
-0,182
|
|
Неизвестные
параметры
|
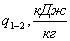 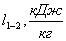 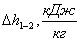 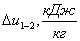 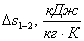
|
|
|
|
|
|
Полученный
результат
|
-85,55
|
-95,6
|
16,87
|
12,052
|
-0,271
|
Таблица 1.2 - Промежуточные точки для p,v
- диаграммы.
|
Точки
|
Давление
р, Па
|
Удельный
объём 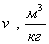
|
|
A
|
0,115
|
0,68
|
|
B
|
0,136
|
0,58
|
|
C
|
0,166
|
0,48
|
|
D
|
0,212
|
0,38
|
|
E
|
0,282
|
0,29
|
Таблица 1.3 - Промежуточные точки для Т, S-
диаграммы.
|
Точки
|
Температура
Т, Па
|
Энтропия
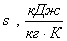
|
|
A
|
315
|
-0,135
|
|
B
|
311
|
-0,073
|
|
C
|
307
|
-0,021
|
|
D
|
304
|
0,022
|
|
E
|
302
|
0,064
|
Вывод: Политропный процесс носит обобщающий
характер, так как здесь не накладывается какого-либо ограничения, например
постоянство одного из параметров в изохорном, изобарном и изотермическом
процессах или отсутствия теплообмена в адиабатном процессе.
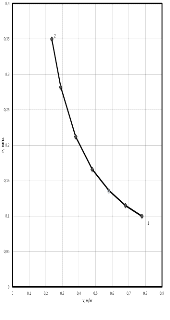
Рисунок 1.1.- Диаграмма в p,v
- координатах.
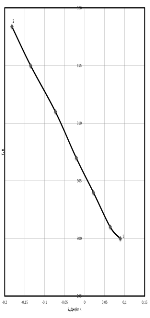
Рисунок 1.2. - Диаграмма в T,S
- координатах.
1.2 Задача 2
В процессе 1-2 с показателем политропы n
к 1 кг газа с начальными параметрами р1 = 0,1МПа, Т1 =
300 К подводится тепло q.
Определить недостающие начальные параметры v1,
u1, h1,
s1, конечные
параметры р2, Т2, v2,
u2,
h2,
s2,
изменение параметров в процессе ∆u1-2,
∆h1-2,
∆s1-2
и работу l1-2.
Построить процесс в p, v
- и T, s
- диаграммах.

Решение:
Для расчетов неизвестных параметров необходимо
рассчитать газовую постоянную. Газовая постоянная является индивидуальной для
каждого газа, то есть зависит от молекулярной массы газа и рассчитывается по
формуле:
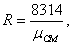 (1.27)
(1.27)
где mсм - это
кажущаяся молекулярная масса, она зависит от пропорции компонентов, из которых
состоит смесь газа. В данном случае имеется газ СО2, и для него
газовая постоянная будет равна:
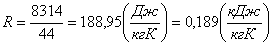 .
.
Так же понадобится для расчетов изобарная (ср)
и изохорная (сv) теплоемкости. Так как данный газ - трёхатомный,
следовательно изобарная теплоемкость равна:
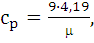
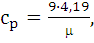 (1.28)
(1.28)
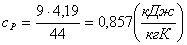
а изохорная теплоемкость равна:
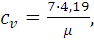
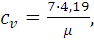 (1.29)
(1.29)
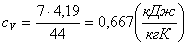 .
.
Объем при нормальных условиях будет равен:
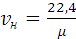
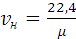 , (1.30)
, (1.30)
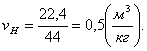
Определение недостающих начальных
параметров.
Определим начальный объем v1
Из уравнения Клапейрона:
=RT, (1.31)
можно найти объем, выразив его.
Для данного случая начальный объем будет равен:
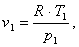 (1.32)
(1.32)
где R - газовая постоянная, кДж/кгК;
Т1 - начальная температура, К;
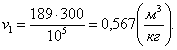
р1 - начальное давление,
Па.
Определим начальную внутреннюю
энергию u1
Величина внутренней энергии газа
зависит как от скорости движения молекул и атомов, так и от расстояния между
ними. Скорость движения микрочастиц вещества зависит от температуры тела, а
силы взаимодействия между ними - от удельного объема. Поэтому внутреннюю
энергию можно представить в виде:
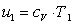 , (1.33)
, (1.33)
где сv - изохорная теплоемкость газа,
кДж/кгК;
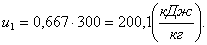
Определим энтальпию h1 в начале
процесс.
Энтальпия газа так же, как и внутренняя энергия,
зависит только от температуры. Следовательно, энтальпия h1 в начале
процесса рассчитывается по формуле:
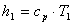 , (1.34)
, (1.34)
где ср - изобарная теплоемкость газа,
кДж/кгК;
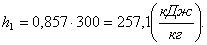
Определим энтропию s1 в
начале процесса.
В уравнении первого закона
термодинамики dq = du + pdv только du является полным дифференциалом внутренней
энергии u. Введением множителя 1/Т можно привести это уравнение к уравнению в
полных дифференциалах:
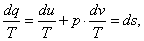 (1.35)
(1.35)
где ds - полный дифференциал параметра s, то
есть энтропии.
Для идеальных газов pv = RT, du = cvdT,
поэтому
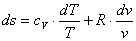 , (1.36)
, (1.36)
После интегрирования (1.36) получаем расчетную
формулу для определения энтропии:
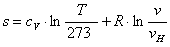 , (1.37)
, (1.37)
где v - начальный объем, м3/кг.
Согласно формуле (1.37) энтропию s1
в данном случае рассчитаем по формуле:
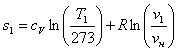 , (1.38)
, (1.38)
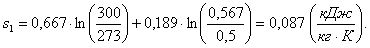
Определение недостающих конечных параметров.
Определим конечную температуру Т2.
Так как известно количество тепла q
и начальная температура Т1, можно найти конечную температуру Т2.
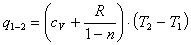 , (1.39)
, (1.39)
Из формулы (1.39) температура Т2
будет равна:
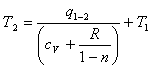 , (1.40)
, (1.40)
где q1-2
- подводимое тепло, кДж/кг;
n - показатель
политропы.
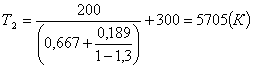 .
.
Определим конечное давление р2.
Давление р2 в конце процесса
найдем из соотношения параметров:
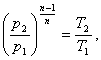 (1,41)
(1,41)
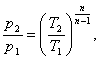 (1.42)
(1.42)
Отсюда давление р2 будет равно:
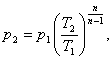 (1.43)
(1.43)
где Т2 - конечная температура, К.
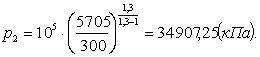
Определим конечный объем v2.
Из формулы (1.6) для данного случая
найдем конечный объем:
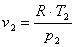 , (1.44)
, (1.44)
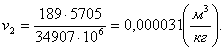
Найдём конечную внутреннюю энергию u2.
Аналогично u1 найдем
конечную внутреннюю энергию u2 по формуле:
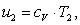 (1.45)
(1.45)
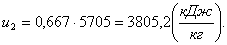
Определим энтальпию h2 в конце
процесса.
Аналогично h1 найдем энтальпию h2
в конце процесса по формуле:
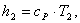 (1.46)
(1.46)
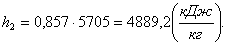
Определим энтропию s2 в
конце процесса.
Аналогично s1 находим
энтропию s2 в конце процесса по формуле:
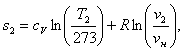 (1.47)
(1.47)
где v2 - конечный объем, м3/кг.
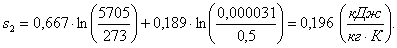
Определение работы и изменения
параметров: внутренней энергии, энтальпии и энтропии.
Вычислим изменение внутренней энергии ∆u1-2.
Изменение внутренней энергии можно рассчитать по
формуле:
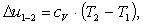 (1.48)
(1.48)
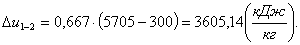
Определим изменение энтальпии ∆h1-2.
Изменение внутренней энергии ∆u1-2,
можно рассчитать, как и изменение энтальпии ∆h1-2:
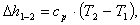 (1.49)
(1.49)
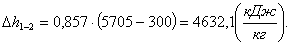
Вычислим изменение энтропии ∆s1-2.
Аналогично изменению внутренней
энергии и изменению энтальпии можно рассчитать изменение энтропии ∆s1-2.
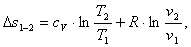 (1.50)
(1.50)
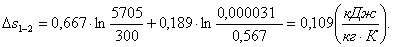
Найдём работу l1-2 в данном процессе.
Для политропного процесса работа рассчитывается
по формуле:
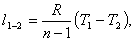 (1.51)
(1.51)
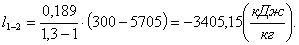
Таблица 1.4 - Результаты начальных и
конечных параметров, тепло, работа, изменение параметров.
|
Неизвестные
параметры
|
Р1,
МПа
|
Т1,
К
|
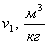 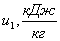 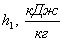 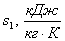
|
|
|
|
|
Полученный
результат
|
0,1
|
300
|
0,567
|
200,1
|
257,1
|
0,087
|
|
Неизвестные
параметры
|
Р2,
МПа
|
Т2,
К
|
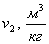 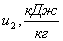 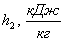 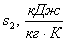
|
|
|
|
|
Полученный
результат
|
34907,25
|
5705
|
0,000031
|
3805,2
|
4889,2
|
0,196
|
|
Неизвестные
параметры
|
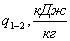 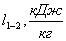 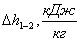 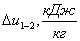 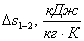
|
|
|
|
|
|
Полученный
результат
|
200
|
-3405,15
|
4632,1
|
3605,14
|
0,109
|
Таблица 1.5 - Промежуточные точки для p,v
- диаграммы.
|
Точки
|
Давление
р, Па
|
Удельный
объём 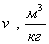
|
|
A
|
0,118525
|
0,5
|
|
B
|
0,157181
|
0,4
|
|
C
|
0,228421
|
0,3
|
|
D
|
0,387143
|
0,2
|
|
E
|
0,955148
|
0,1
|
Таблица 1.6- Промежуточные точки для Т, S-
диаграммы.
|
Точки
|
Температура
Т, Па
|
Энтропия
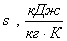
|
|
A
|
312
|
0,089
|
|
B
|
333
|
0,09
|
|
C
|
363
|
0,094
|
410
|
0,098
|
|
E
|
505
|
0,106
|
Вывод: политропный процесс является обобщающим
для всех процессов. При расчётах политропного процесса требуется знание
политропы.
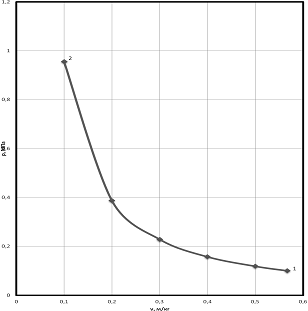
Рисунок 1.3. - диаграмма в p,v-
координатах.
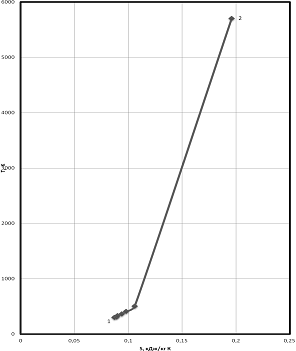
Рисунок 1.4 - диаграмма в T,S
- координатах.
2.
ГАЗОВЫЕ ЦИКЛЫ
Рассчитать теоретические циклы ДВС и ГТУ в
соответствии с исходными данными.
2.1 Задача 1
Определить:- параметры газа в переходных точках
цикла ДВС (результаты расчёта свести в табл.);
тепло, работу и изменение параметров ∆u, ∆h,
∆s, в каждом процессе;
полезную работу, подведённое и отведенное тепло
в цикле ДВС, его КПД (двумя способами);
построить цикл в масштабе в диаграммах p,v и
T,s.

Решение:
Для расчетов неизвестных параметров необходимо
рассчитать газовую постоянную. Газовая постоянная является индивидуальной для
каждого газа, то есть зависит от молекулярной массы газа и рассчитывается по
формуле:
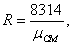 (2.1)
(2.1)
где mсм - это
кажущаяся молекулярная масса, она зависит от пропорции компонентов, из которых
состоит смесь газа.
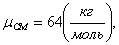
Для воздуха газовая постоянная будет равна:
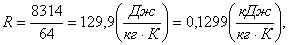
Так же понадобится для расчетов
изобарная (ср) и изохорная (сv) теплоемкости, показатель
адиабаты и объем при нормальных условиях. Так как данный газ воздух -
трёхатомный, следовательно, изобарная теплоемкость равна:
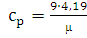
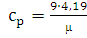 , (2.2)
, (2.2)
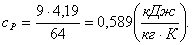
а изохорная теплоемкость равна:

 , (2.3)
, (2.3)
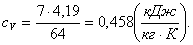
Показатель адиабаты равен:
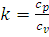
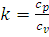 , (2.4)
, (2.4)
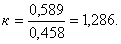
Объем при нормальных условиях будет равен:
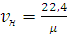
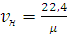 , (2.5)
, (2.5)
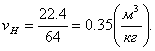
Определение параметров газа в
переходных точках цикла.
Определим параметры газа в точке 1.
Найдем объем v1 из
уравнения Клапейрона:
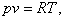 (2.6)
(2.6)
Для данной точки объем будет равен:
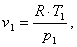 (2.7)
(2.7)
где R - газовая постоянная, кДж/кг*К;
Т1 - температура в точке
1, К;
р1 - давление в точке 1,
Па.
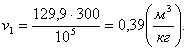
Вычислим внутреннюю энергию u1.
Величина внутренней энергии газа зависит, как от
скорости движения молекул и атомов, так и от расстояния между ними. Скорость
движения микрочастиц вещества зависит от температуры тела, а силы
взаимодействия между ними - от удельного объема. Поэтому внутреннюю энергию
можно представить в виде:
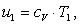 (2.8)
(2.8)
где сv - изохорная
теплоемкость газа, кДж/кгК.
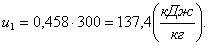
Определим энтальпию h1.
Энтальпия газа так же, как и внутренняя энергия,
зависит только от температуры. Следовательно, энтальпия h1
рассчитывается по формуле:
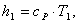 (2.9)
(2.9)
где ср - изобарная
теплоемкость газа, кДж/кгК.
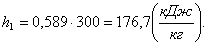
Найдем энтропию s1.
В уравнении первого закона
термодинамики dq = du + pdv только du является полным дифференциалом внутренней
энергии u. Введением множителя 1/Т можно привести это уравнение к уравнению в
полных дифференциалах:
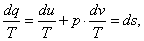 (2.10)
(2.10)
где ds - полный дифференциал
параметра s, то есть энтропии.
Для идеальных газов pv = RT, du = cvdT,
поэтому
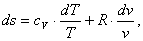 (2.11)
(2.11)
После интегрирования (2.11) получаем
расчетную формулу для определения энтропии:
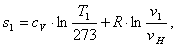 (2.12)
(2.12)
где v1 - объем точки 1, м3/кг;н
- объем при нормальных условиях, м3/кг.
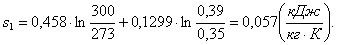
Определим параметры газа в точке 2.
Найдем объем v2 с помощью
степени сжатия e.
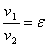 , (2.13)
, (2.13)
Отсюда выразим v2:
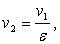 (2.14)
(2.14)
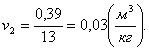
Найдем температуру Т2 по формуле:
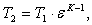 (2.15)
(2.15)
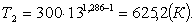
Найдем из уравнения Клапейрона pv = RT давление
p2:
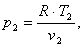 (2.16)
(2.16)
где Т2 - температура в
точке 2, К;2 - объем в точке 2, м3/кг.
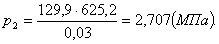
Найдем внутреннюю энергию u2
аналогично u1:
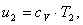 (2.17)
(2.17)
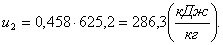
Вычислим энтальпию h2
аналогично h1:
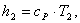 (2.18)
(2.18)
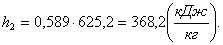
Найдем энтропию s2
аналогично s1:
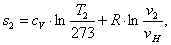 (2.19)
(2.19)
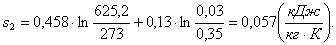
Определим параметры газа в точке z.
Найдем температуру ТZ через
степень повышения давления l
из соотношения:
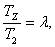 (2.20)
(2.20)
отсюда выразим ТZ:
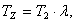 (2.21)
(2.21)
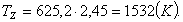
Определим давление рZ через
степень повышения давления l
из соотношения:
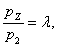 (2.22)
(2.22)
отсюда выразим рZ:
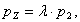 (2.23)
(2.23)
где р2 - давление в точке
2; МПа.
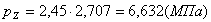 .
.
Определим объём 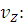
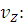
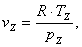 (2.24)
(2.24)
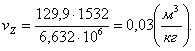
Найдем внутреннюю энергию uZ аналогично
u1:
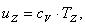 (2.25)
(2.25)
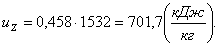
Вычислим энтальпию hZ аналогично
h1:
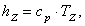 (2.26)
(2.26)
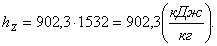
Найдем энтропию sZ аналогично
s1:
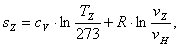 (2.27)
(2.27)
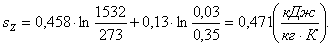
Определим параметры газа в точке 3.
Найдем температуру Т3
через степень повышения давления r
из соотношения:
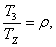 (2.28)
(2.28)
отсюда выразим Т3:
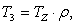 (2.29)
(2.29)
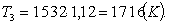
Найдём давление 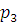
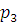 из условия, что процесс z-3 является
изобарическим:
из условия, что процесс z-3 является
изобарическим:
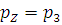
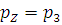 , (2.30)
, (2.30)
Отсюда
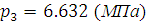
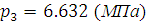 .
.
Вычислим из уравнения Клапейрона: pv = RT объем
v3:
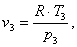 (2.31)
(2.31)
где Т3 - температура в
точке 3; К,
р3 - давление в точке 3;
МПа.
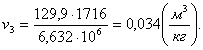
Найдем внутреннюю энергию u3
аналогично u1:
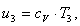 (2.32)
(2.32)
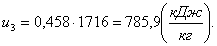
Определим энтальпию h3
аналогично h1:
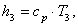 (2.33)
(2.33)
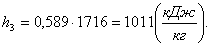
Вычислим энтропию s3
аналогично s1:
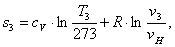 (2.34)
(2.34)
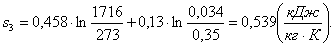
Определим параметры газа в точке 4.
Найдем температуру Т4 из соотношения:
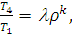
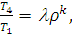 (2.35)
(2.35)
Отсюда:

 , (2.36)
, (2.36)
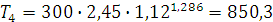
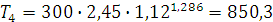 (К).
(К).
Вычислим давление р4,
выразив его из формулы:
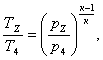 (2.37)
(2.37)
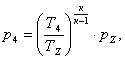 (2.38)
(2.38)
Отсюда
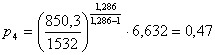 (МПа).
(МПа).
Найдем из уравнения Клапейрона pv =
RT объем v4:
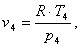 (2.39)
(2.39)
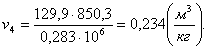
Определим внутреннюю энергию u4
аналогично u1:
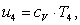 (2.40)
(2.40)
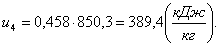
Найдем энтальпию h4
аналогично h1:
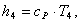 (2.41)
(2.41)
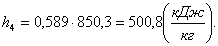
Найдем энтропию s4
аналогично s1:
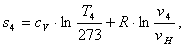 (2.42)
(2.42)
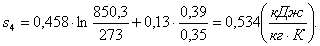
Определение тепла q, работы l и изменения
параметров: внутренней энергии Δu, энтальпии
Δh,
энтропии
Δs,
в
каждом процессе.
Процесс 1-2 (s
= const).
Тепло q1-2 равно нулю:
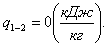
Найдем работу l1-2:
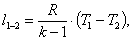 (2.43)
(2.43)
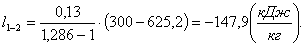
Вычислим изменение внутренней
энергии Δu1-2:
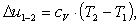 (2.44)
(2.44)
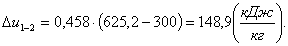
Определим изменение энтальпии Δh1-2:
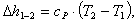 (2.45)
(2.45)

Найдем изменение энтропии Δs1-2:
 (2.46)
(2.46)
Процесс 2 - z (v = const).
Найдем тепло q2-Z:
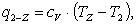 (2.47)
(2.47)
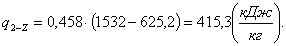
Работа l2-Z равна нулю:
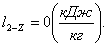 (2.48)
(2.48)
Найдем изменение внутренней энергии Δu2-Z:
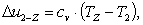 (2.49)
(2.49)
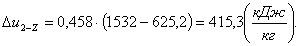
Найдем изменение энтальпии Δh2-Z:
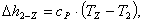 (2.50)
(2.50)
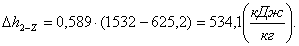
Вычислим изменение энтропии Δs2-Z:
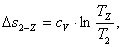 (2.51)
(2.51)
Процесс z - 3 (p = const).
Найдем тепло qZ-3:
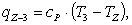 (2.52)
(2.52)
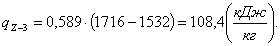
Найдём работу lZ-3 :
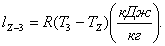 (2.53)
(2.53)
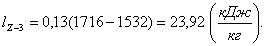
Определим изменение внутренней
энергии ΔuZ-3:
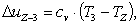 (2.54)
(2.54)
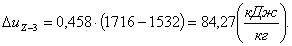
Вычислим изменение энтальпии ΔhZ-3:
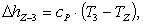 (2.55)
(2.55)
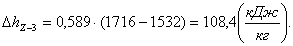
Найдем изменение энтропии ΔsZ-3:
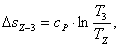 (2.56)
(2.56)
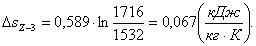
Процесс 3 - 4 (s = const).
Тепло q3-4 равно нулю:
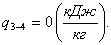 (2.57)
(2.57)
Найдем работу l3-4:
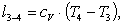 (2.58)
(2.58)
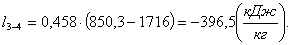
Вычислим изменение внутренней энергии Δu3-4:
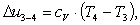 (2.59)
(2.59)
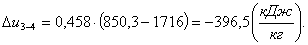
Определим изменение энтальпии Δh3-4:
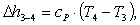 (2.60)
(2.60)
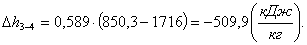
В адиабатном процессе 3-4 изменение
энтропии Δs3-4 равно нулю:
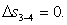 (2.61)
(2.61)
Процесс 4 - 1 (v = const).
Найдем отведенное тепло q4-1:
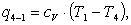 (2.62)
(2.62)
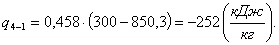
Найдём работу
4-1=о. (2.63)
Найдем изменение внутренней энергии Δu4-1:
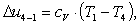 (2.64)
(2.64)
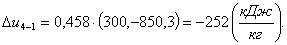
Найдем изменение энтальпии Δh4-1:
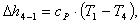 (2.64)
(2.64)
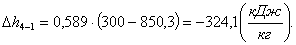
Найдем изменение энтропии Δs4-1:
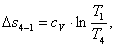 (2.65)
(2.65)
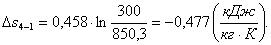
Определение полезной работы l, подведённого и
отведённого тепла, КПД ht
(двумя способами).
Найдем подведенное тепло q1:
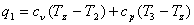 , (2.66)
, (2.66)
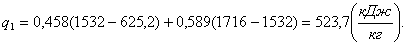
Найдем отведенное тепло q2:
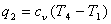 , (2.67)
, (2.67)
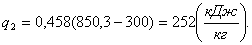
Найдем полезную работу l:
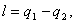 (2.68)
(2.68)
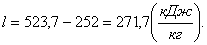
Вычислим КПД:
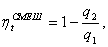 (2.69)
(2.69)
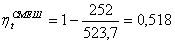 .
.
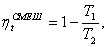 (2.70)
(2.70)
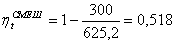 .
.
Таблица 2.1 - Расчёт параметров в переходных
точках циклах.
|
Точка
|
p, МПа
|
Т,
К
|
v, м3/кг
|
u, кДж/кг
|
h, кДж/кг
|
s, кДж/кгК
|
|
1
|
0,1
|
300
|
0,39
|
137,4
|
176,7
|
0,057
|
|
2
|
2,707
|
625,2
|
0,03
|
286,3
|
368,2
|
0,057
|
|
Z
|
6,632
|
1532
|
0,03
|
701,7
|
902,3
|
0,471
|
|
3
|
6,632
|
1716
|
0,034
|
785,9
|
1011
|
0,539
|
|
4
|
0,283
|
850,3
|
0,39
|
389,4
|
500,8
|
0,534
|
Таблица 2.2 - Результаты расчёта тепла, работы и
изменения параметров.
|
Процесс
|
q, кДж/кг
|
l, кДж/кг
|
Δu, кДж/кг
|
Δh, кДж/кг
|
Δs, кДж/кг К
|
|
1-2
|
0
|
-148,9
|
148,9
|
191,5
|
0
|
|
2-z
|
415,3
|
0
|
415,3
|
534,1
|
0,41
|
|
z-3
|
108,4
|
23,92
|
84,27
|
108,4
|
0,067
|
|
3-4
|
0
|
396,5
|
-396,5
|
-509,9
|
0
|
|
4-1
|
-252
|
0
|
-252
|
-324,1
|
-0,477
|
Таблица 2.3 - результаты расчётов полезной
работы, подведённого и отведённого тепла в цикле, его КПД
|
l, кДж/кг
|
q1, кДж/кг
|
q2, кДж/кг
|
ht
|
|
271,7
|
523,7
|
-252
|
0,518
|
Таблица 2.4- расчёт параметров промежуточных
точек.
|
Точка
|
Р,
Мпа
|
v, м3/кг
|
Точка
|
s, кДж/кгК
|
Т,
К
|
|
А
|
0,138
|
0,36
|
И
|
1087
|
|
Б
|
0,1605
|
0,27
|
К
|
0,4705
|
1532
|
|
С
|
1,1102
|
0,06
|
Л
|
0,5085
|
1634
|
|
Д
|
6,6339
|
0,003
|
М
|
0,527
|
1685
|
|
Е
|
2,0731
|
0,084
|
Н
|
0,3344
|
549
|
|
Ж
|
0,6623
|
0,204
|
О
|
0,1882
|
399
|
|
З
|
0,3145
|
0,364
|
|
|
|
Вывод: термический КПД цикла ДВС со смешанным
подводом тепла имеет обобщающий характер.
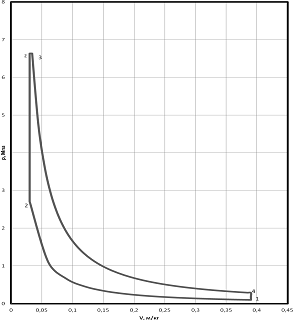
Рисунок - 2.1 Диаграмма в p,v-
координатах.
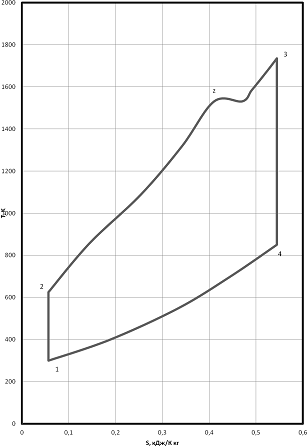
Рисунок 2.2 - диаграмма в T,s
- координатах.
2.2 Задача 2
Определить:
параметры газа в переходных точках цикла ГТУ
(результаты расчёта свести в табл.);
тепло, работу и изменение параметров ∆u, ∆h,
∆s, в каждом процессе;
полезную работу, подведённое и отведенное тепло
в цикле ГТУ, его КПД (двумя способами);
построить цикл в масштабе в диаграммах p,v и
T,s.

Решение:
Для расчетов неизвестных параметров необходимо
рассчитать газовую постоянную. Газовая постоянная является индивидуальной для
каждого газа, то есть зависит от молекулярной массы газа и рассчитывается по
формуле:
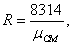 (2.71)
(2.71)
где mсм - это
кажущаяся молекулярная масса, она зависит от пропорции компонентов, из которых
состоит смесь газа.
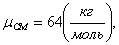
Для воздуха газовая постоянная будет равна:
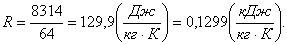
Так же понадобится для расчетов
изобарная (ср) и изохорная (сv) теплоемкости, показатель адиабаты
и объем при нормальных условиях. Так как данный газ воздух - трёхатомный,
следовательно, изобарная теплоемкость равна:
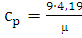
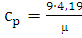 , (2.72)
, (2.72)
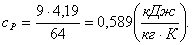
а изохорная теплоемкость равна:
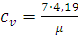
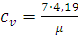 , (2.73)
, (2.73)
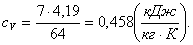
Показатель адиабаты равен:
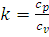
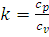 , (2.74)
, (2.74)
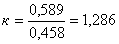
Объем при нормальных условиях будет равен:
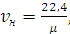
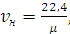 (2.75),
(2.75), 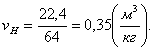
Определение параметров газа в переходных точках
цикла.
Найдем объем v1 из уравнения
Клапейрона:
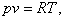 (2.76)
(2.76)
Для данной точки объем будет равен:
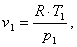 (2.77)
(2.77)
Где R - газовая постоянная, кДж/кг*К;
Т1 - температура в точке
1, К;
р1 - давление в точке 1,
Па.
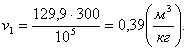
Найдем внутреннюю энергию u1.
Величина внутренней энергии газа зависит, как от
скорости движения молекул и атомов, так и от расстояния между ними. Скорость
движения микрочастиц вещества зависит от температуры тела, а силы
взаимодействия между ними - от удельного объема. Поэтому внутреннюю энергию
можно представить в виде:
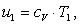 (2.78)
(2.78)
где сv - изохорная
теплоемкость газа, кДж/кгК.
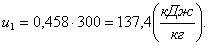
Вычислим энтальпию h1.
Энтальпия газа так же, как и внутренняя энергия,
зависит только от температуры. Следовательно, энтальпия h1
рассчитывается по формуле:
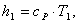 (2.79)
(2.79)
где ср - изобарная
теплоемкость газа, кДж/кгК.
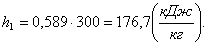
Найдем энтропию s1.
В уравнении первого закона
термодинамики dq = du + pdv только du является полным дифференциалом внутренней
энергии u. Введением множителя 1/Т можно привести это уравнение к уравнению в
полных дифференциалах:
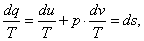 (2.80)
(2.80)
где ds - полный дифференциал
параметра s, то есть энтропии.
Для идеальных газов pv = RT, du = cvdT,
поэтому
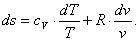 (2.81)
(2.81)
После интегрирования (2.78) получаем
расчетную формулу для определения энтропии:
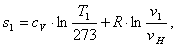 (2.82)
(2.82)
Где v1 - объем точки 1, м3/кг;н
- объем при нормальных условиях, м3/кг.
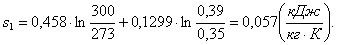
Определим параметры газа в точке 2
По изобаре 2-3 определяем, что Р2=Р3,
отсюда р2=0,5 МПа.
Из условия, что процесс 1-2 является адиабатным,
имеем:
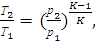
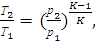 (2.83)
(2.83)
Получаем:
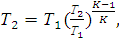
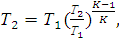 (2.84)
(2.84)
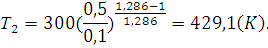
Объём найдём из уравнения
Клайперона-Менделеева:
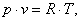 (2.85)
(2.85)
Для данной точки объем будет равен:
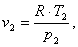 (2.86)
(2.86)
Где Т2 - температура в
точке 2, К;
р2 - давление в точке 2,
Па.
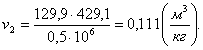
Найдем внутреннюю энергию u2
аналогично u1:
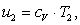 (2.87)
(2.87)
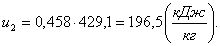
Определим энтальпию h2
аналогично h1:
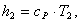 (2.88)
(2.88)
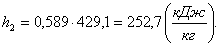
Найдем энтропию s2
аналогично s1:
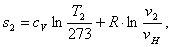 (2.89)
(2.89)
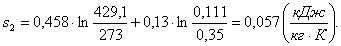
Определим параметры газа в точке 3
Найдем объем v3 аналогично v1:
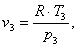 (2.90)
(2.90)
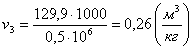 .
.
Вычислим внутреннюю энергию u3
аналогично u1:
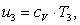 (2.91)
(2.91)
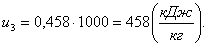
Найдем энтальпию h3
аналогично h1:
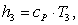 (2.92)
(2.92)

Вычислим энтропию s3
аналогично s1:
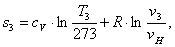 (2.93)
(2.93)
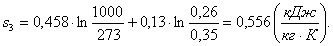
Определим параметры газа в точке 4
Так как процесс 3-4 является адиабатным:
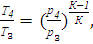
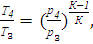 (2.94)
(2.94)
Отсюда
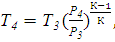
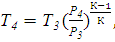 (2.95)
(2.95)
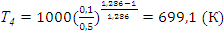
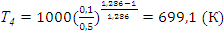 .
.
Вычислим объем v4 аналогично v1:
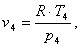 (2.96)
(2.96)
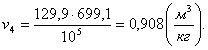
Найдем внутреннюю энергию u4 аналогично
u1:
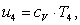 (2.97)
(2.97)
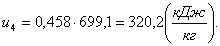
Определим энтальпию h4
аналогично h1:
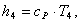 (2.98)
(2.98)
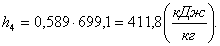
Вычислим энтропию s4
аналогично s1:
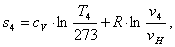 (2.99)
(2.99)
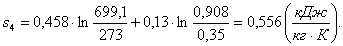
Определение тепла q, работы l и
изменения параметров: внутренней энергии Δu, энтальпии Δh, энтропии Δs в каждом
процессе.
Процесс 1 - 2 (s = const).
Тепло q1-2 равно нулю:
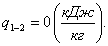 (2.100)
(2.100)
Определим работу l1-2:
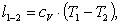 (2.101)
(2.101)
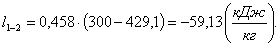
Найдем изменение внутренней энергии Δu1-2:
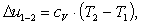 (2.102)
(2.102)
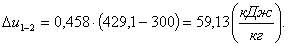
Вычислим изменение энтальпии Δh1-2:
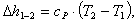 (2.103)
(2.103)
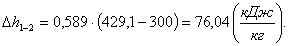
В адиабатном процессе 1-2 изменение
энтропии Δs1-2 равно нулю:
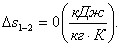 (2.104)
(2.104)
Процесс 2 - 3 (р = const)
Найдем подведенное тепло q2-3:
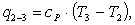 (2.105)
(2.105)
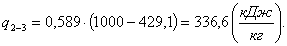
Найдем работу l2-3:
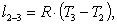 (2.106)
(2.106)
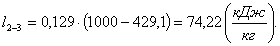
Найдем изменение внутренней энергии Δu2-3:
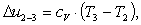 (2.107)
(2.107)
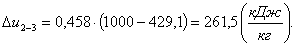
Определим изменение энтальпии Δh2-3:
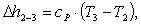 (2.108)
(2.108)
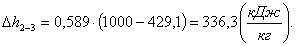
Найдем изменение энтропии Δs2-3:
 (2.109)
(2.109)
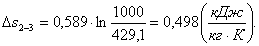
Процесс 3 - 4 (s = const).
Тепло q3-4 равно нулю:
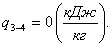 (2.110)
(2.110)
Вычислим работу l3-4:
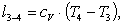 (2.111)
(2.111)
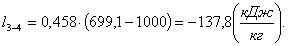
Найдем изменение внутренней энергии Δu3-4:
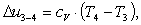 (2.112)
(2.112)
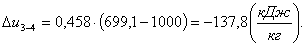
Найдем изменение энтальпии Δh3-4:
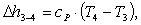 (2.113)
(2.113)
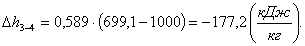
В адиабатном процессе 3-4 изменение
энтропии Δs3-4 равно нулю:
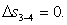 (2.114)
(2.114)
Процесс 4 - 1 (р = const).
Определим отведенное тепло q4-1:
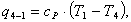 (2.115)
(2.115)
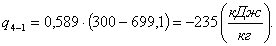
Вычислим работу l4-1:
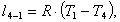 (2.116)
(2.116)
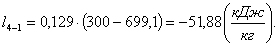
Найдем изменение внутренней энергии Δu4-1:
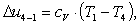 (2.117)
(2.117)
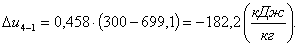
Определим изменение энтальпии Δh4-1:
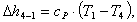 (2.118)
(2.118)
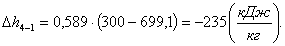
Найдем изменение энтропии Δs4-1:
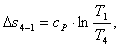 (2.119)
(2.119)
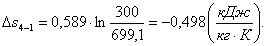
Определение полезной работы l, КПД ht
(двумя способами).
Найдем полезную работу l:
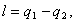 (2.120)
(2.120)
гдe
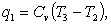 (2.121)
(2.121)
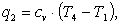 (2.122)
(2.122)
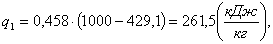

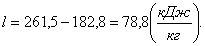
Найдем КПД:
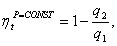 (2.123)
(2.123)
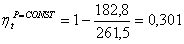 .
.
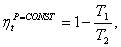 (2.124)
(2.124)
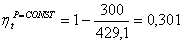 .
.
Таблица 2.5 - Расчёт параметров в переходных
точках циклах
|
Точка
|
p, МПа
|
Т,
К
|
v, м3/кг
|
u, кДж/кг
|
h, кДж/кг
|
s, кДж/кгК
|
|
1
|
0,1
|
300
|
0,39
|
137,4
|
176,7
|
0,057
|
|
2
|
0,5
|
429,1
|
0,111
|
196,5
|
252,7
|
0,057
|
|
3
|
0,5
|
1000
|
0,26
|
458
|
589
|
0,556
|
|
4
|
0,1
|
699,1
|
0,908
|
320,2
|
411,8
|
0,556
|
Таблица 2.6 - Результаты расчёта тепла, работы и
изменения параметров.
|
Процесс
|
q, кДж/кг
|
l, кДж/кг
|
Δu, кДж/кг
|
Δh, кДж/кг
|
Δs, кДж/кг К
|
|
1-2
|
0
|
-59,13
|
59,13
|
76,04
|
0
|
|
2-3
|
336,3
|
74,22
|
261,5
|
336,3
|
0,498
|
|
3-4
|
0
|
137,8
|
-137,8
|
-177,2
|
0
|
|
4-1
|
-235
|
-51,88
|
-182,2
|
-235
|
-0,498
|
Таблица 2.7 - Результаты расчётов полезной
работы, подведённого и отведённого тепла в цикле, его КПД
|
l, кДж/кг
|
q1, кДж/кг
|
q2, кДж/кг
|
ht
|
|
78,8
|
261,5
|
-182,2
|
0,301
|
Таблица 2.8- расчёт параметров промежуточных
точек
|
Точка
|
Р,
Мпа
|
v, м3/кг
|
Точка
|
s, кДж/кгК
|
Т,
К
|
|
А
|
0,1193
|
0,34
|
И
|
0,2745
|
619,7
|
|
Б
|
0,1867
|
0,24
|
К
|
0,5563
|
1001
|
|
С
|
0,3734
|
0,14
|
Л
|
0,4859
|
622
|
|
Д
|
0,3312
|
0,36
|
М
|
0,3187
|
468
|
|
Е
|
0,1876
|
0,56
|
Н
|
0,2130
|
391
|
|
Ж
|
0,1519
|
0,66
|
О
|
0,0841
|
314
|
|
З
|
0,1081
|
0,86
|
|
|
|
Вывод: с увеличением степени повышения давления e
и показателя адиабаты k,
КПД ГТУ с подводом теплоты в процессе при постоянном давлении возрастает.
Однако термический КПД еще не может служить мерой экономичности установки. Эту
роль выполняет эффективный КПД ГТУ.

Рисунок 2.3 - диаграмма в p,v
- координатах.
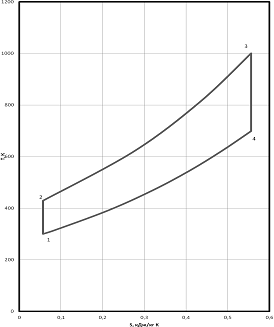
Рисунок 2.4 - диаграмма в T,
s - координатах.
.1 Задача 1
В цикле паросиловой установки осуществляется
одноступенчатый промежуточный перегрев пара до температуры t1.
Определить термический КПД цикла при различных значениях давления промперегрева
рп (2.0; 1.0; 0.5; 0.2; 0.1 МПа), построить зависимость ht
= f(рп),
сравнить с термическим КПД без промперегрева. Построить цикл в T,
s - и h,
s - диаграммах.

Решение:
Термический КПД цикла с промежуточным перегревом
пара определяем по формуле:
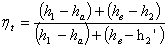 , (3.1)
, (3.1)
где h1 - энтальпия
в точке 1, кДж/кг;
hа - энтальпия
в точке а, кДж/кг;
hв - энтальпия
в точке в, кДж/кг;
h2 - энтальпия
в точке 2, кДж/кг;
h2' = h3 = 4.19 t2 - энтальпия
в точке 3, кДж/кг.
Рассчитаем термический КПД для каждого случая
отдельно.
Расчет термического КПД при давлении
промперегрева рп = 20 бар.
По h,
s - диаграмме для
водяного пара находим энтальпии:
h1
= 3172 кДж/кг,
hа
= 2937 кДж/кг,
hв
= 3226 кДж/кг,
h2
= 2138 кДж/кг,
h2'
= 4.19 t2
= 4.19·29=121,51 кДж/кг.
Энтальпии h1
и h2'
в каждом рассмотренном нами случае будут одинаковы. Подставим значения
энтальпий в формулу (3.1):
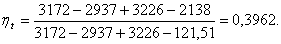
Расчет термического КПД при давлении
промперегрева рп = 10 бар.
Аналогично находим энтальпии:
hа = 2789
кДж/кг,
hв = 3243
кДж/кг,
h2 = 2240
кДж/кг.
Подставим значения энтальпии в
формулу (3.1):
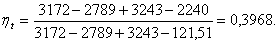
Расчет термического КПД при давлении
промперегрева рп = 5 бар.
Аналогично находим энтальпии:
hа = 2659
кДж/кг,
hв = 3252
кДж/кг,
h2 = 2339
кДж/кг.
Подставим значения энтальпии в
формулу (3.1):
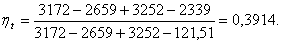
Расчет термического КПД при давлении
промперегрева рп = 2 бар.
Аналогично находим энтальпии:
hа = 2503
кДж/кг,
hв = 3256
кДж/кг,
h2 = 2469
кДж/кг.
Подставим значения энтальпий в
формулу (3.1):
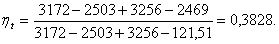
Расчет термического КПД при давлении
промперегрева рп = 1 бар.
Аналогично найдем энтальпии:
hа = 2396
кДж/кг,
hв = 3258
кДж/кг,
h2 =
2566кДж/кг.
Подставим значения энтальпий в
формулу (3.1):
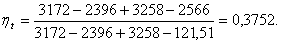
Расчет термического КПД без
промперегрева.
По h, s - диаграмме определим
энтальпии:
h1 = 3172
кДж/кг,
h2 = 1991
кДж/кг,
t2 = 29оС.
Термическое КПД без промперегрева
можно посчитать по формуле:
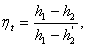 (3.2)
(3.2)
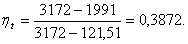
Найденные значения КПД приведены в табл. 3.1.
Таблица З.1 - Зависимости ht
= f(рп) и
термического КПД без промперегрева.
|
рп,
бар
|
20
|
10
|
5
|
2
|
1
|
без
п.
|
|
ηt
|
0,3962
|
0,3968
|
0,3914
|
0,3828
|
0,3752
|
0,3872
|
Построение зависимости ht
= f(рп) и
сравнение с термическим КПД без промперегрева.
График зависимости ht
= f(рп)
показан на рисунке 3.1.
Вывод: из T,s
- диаграммы видно, что промежуточный перегрев позволяет значительно увеличить
сухость пара на выходе из турбины, это сказывается на благоприятные условия
турбины.
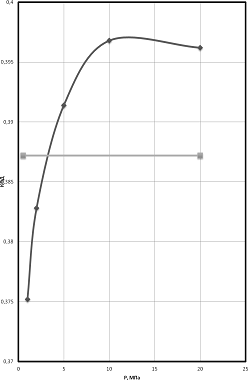
Рисунок 3.1 - график зависимости ht
= f(рп).
3.2 Задача 2
Паросиловая установка работает по циклу с
двухступенчатым подогревом питательной воды в смесительных теплообменных
аппаратах, давление первого отбора р01 = 0.3 МПа, второго отбора р02
= 0.12 МПа. Определить термический КПД регенеративного цикла, построить цикл в T,
s - и h,
s - диаграммах,
сравнить с КПД обычного цикла Ренкина.

Решение:
Термический КПД регенеративного цикла рассчитаем
по формулам:
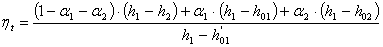 , (3.3)
, (3.3)
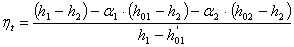 , (3.4)
, (3.4)
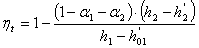 , (3.5)
, (3.5)
где
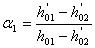 , (3.6)
, (3.6)
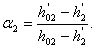 (3.7)
(3.7)
h1 - энтальпия
в точке 1, кДж/кг;
h2 - энтальпия
в точке 2, кДж/кг;
h01 - энтальпия
в точке О1,кДж/кг;
h02 - энтальпия
в точке О2, кДж/кг;
h'01 = 4.19 t01,
h'02 = 4.19 t02,
h'2 = 4.19 t2.
По h,
s - диаграмме
находим нужные для расчета энтальпии и температуры:
h1
= 3247 кДж/кг, t1
= 440 oC,
h2
= 2053 кДж/кг, t2
= 44 оС,
h01
= 2534 кДж/кг, t01
= 134 оС,
h02
= 2390 кДж/кг, t02
= 105 оС.
Расчёт энтальпии h'01, h'02,
h'2
h'01 = =561,46кДж/кг,
=561,46кДж/кг,
h'02 =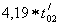 = 439,95
кДж/кг,
= 439,95
кДж/кг,
h'2 =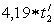 = 184,36
кДж/кг.
= 184,36
кДж/кг.
Расчёт a1 и a2.
a1 рассчитаем по формуле (3.6):
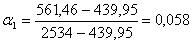 ,
,
a2 рассчитаем по формуле (3.7):
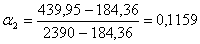 .
.
Расчет термического КПД
регенеративного цикла.
Рассчитаем термический КПД по
формуле (3.3):
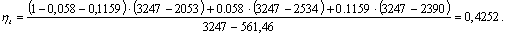 .
.
Теперь рассчитаем термический КПД по
формуле (3.4):
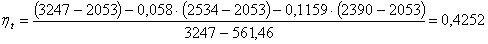 .
.
Найдём термический КПД по формуле
(3.5):
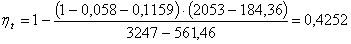 .
.
Расчет термического КПД обычного
цикла Ренкина.
Термический КПД цикла Ренкина
рассчитаем по формуле:
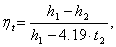 (3.8)
(3.8)
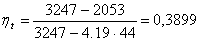 .
.
4. ЦИКЛЫ ТРАНСФОРМАТОРНОГО ТЕПЛА
4.1 Задача 1
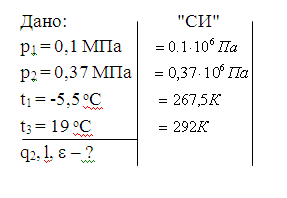
В газовой холодильной установке в качестве
рабочего тела используется воздух с давлением перед компрессором р1
= 0.1 МПа. Определить затрачиваемую в теоретическом цикле работу l, удельную
холодопроизводительность q2, и холодильный коэффициент e.
Решение:
Для того, чтобы найти затрачиваемую в
теоретическом цикле работу, удельную холодопроизводительность и холодильный
коэффициент нам необходимо рассчитать молекулярную массу вещества, изохорную и
изобарную теплоемкости и показатель адиабаты.
Итак, молекулярная масса воздуха будет равна:
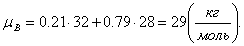
Так как воздух - двухатомный газ, тогда
изобарная теплоемкость будет находиться следующим образом:
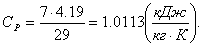
Изохорная теплоемкость будет равна:
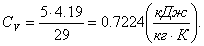
Показатель адиабаты будет равен отношению
изобарной теплоемкости к изохорной:
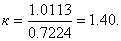
Расчет удельной холодопроизводительности в
цикле.
Удельную холодопроизводительность рассчитаем по
формуле:
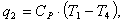 (4.1)
(4.1)
где СР - изобарная
теплоемкость, кДж/кгК;
Т1 - температура в точке 1,
К;
Т4 - температура в точке
4, К.
Так как процессы 2 - 3 и 4 - 1 - p =
const, тогда следует, что
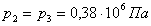 и
и 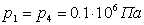 .
.
Тогда можно найти температуры Т2
и Т4.
Температуру Т2 можно
рассчитать по формуле:
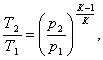 (4.2)
(4.2)
отсюда Т2 будет равна:
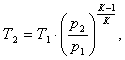 (4.3)
(4.3)
Где р2 - давление в точке 2, Па;
р1 - давление в точке 1, Па;
к - показатель адиабаты.
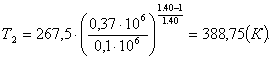
Температуру Т4 можно
рассчитать по формуле:
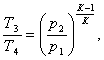 (4.4)
(4.4)
откуда Т4 будет равна:
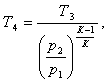 (4.5)
(4.5)
где Т3 - температура в
точке 3, К.
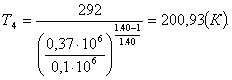
Теперь рассчитаем удельную
холодопроизводительность:
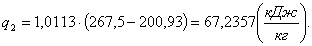
Расчет затраченной работы в цикле.
Затраченная работа рассчитывается по формуле:
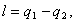 (4.6)
(4.6)
где 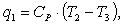 кДж/кг;
кДж/кг;
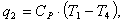 кДж/кг.
кДж/кг.
Подставив q1 и q2 получим
следующую формулу:
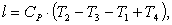 (4.7)
(4.7)
где Т2 - температура в
точке 2, К;
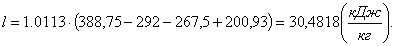
Расчет холодильного коэффициента в цикле.
Холодильный коэффициент можно рассчитать по
формуле:
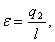 (4.8)
(4.8)
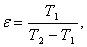 (4.9)
(4.9)
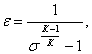 (4.10)
(4.10)
где 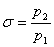 - степень повышения давления в
компрессоре.
- степень повышения давления в
компрессоре.
Итак, рассчитаем холодильный
коэффициент по формуле (4.8):
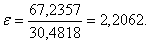
Рассчитаем холодильный коэффициент
по формуле (4.9):

Теперь рассчитаем холодильный
коэффициент по формуле (4.10):
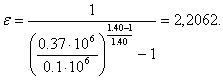
Результаты сведены в таблице4.1.
Таблица 4.1
|
q2, кДж/кг
|
l, кДж/кг
|
ε
|
|
67,2357
|
30,4818
|
2,2062
|
Вывод: более низкий холодильный коэффициент
цикла газовой холодильной установки объясняется необратимостью теплообмена в
изобарных процессах отвода (2 - 3) и подвода (4 - 1) теплоты к рабочему телу,
так как эти процессы протекают при конечной разности температур.
4.2 Задача 2
Парокомпрессорная холодильная установка работает
на хладоагенте R12 при температуре испарения tИ, оС и
температуре конденсации tК, оС. После сжатия в
компрессоре пар сухой насыщенный. Расширение сконденсированного фреона
осуществляется в дросселе. Определить холодильный коэффициент установки,
построить циклы в диаграммах T, s и ln
p, h.
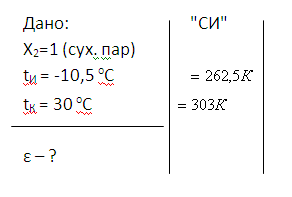
Решение:
Холодильный коэффициент рассчитывается по
формуле:
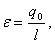 (4.11)
(4.11)
где q 0 - удельная
холодопроизводительность, кДж/кг;- затраченная работа, кДж/кг.
Удельная холодопроизводительность
будет равна:
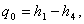 (4.12)
(4.12)
Где h1 - энтальпия в
точке 1, кДж/кг;4 - энтальпия в точке 4, кДж/кг.
Затраченная работа будет равна:
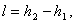 (4.13)
(4.13)
Где h2 - энтальпия в
точке 2, кДж/кг.
Подставим выражения (4.12) и (4.13)
в формулу (4.11) и получим:
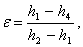 (4.14)
(4.14)
По ln р, h - диаграмме находим
нужные энтальпии:
h1 = 545
кДж/кг;
h2 = 565
кДж/кг;
h3 = h4 = 430
кДж/кг.
Подставим значения энтальпий в
формулу (4.14) и рассчитаем холодильный коэффициент:
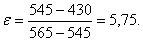
Вывод: холодильный коэффициент
паровой компрессорной холодильной установки значительно выше, чем у газовых
холодильных машин.
ЗАКЛЮЧЕНИЕ
В ходе этой работы я рассмотрела
газовые процессы и циклы, паросиловые установки, а также циклы
трансформаторного тепла. И выяснила, что в изотермическом процессе изменение
внутренней энергии равно нулю 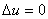 и изменение энтальпии равно нулю
и изменение энтальпии равно нулю 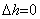 ; конечная
энтропия получилась на много меньше начальной, потому что удельный объём в ходе
процесса на много увеличился. Работа получается отрицательной, потому что в
ходе процесса температура увеличилась. Энтропия и изменение энтропии в большей
степени зависит от температуры, чем от объёма. С увеличением температуры,
увеличивается и энтальпия, и внутренняя энергия.
; конечная
энтропия получилась на много меньше начальной, потому что удельный объём в ходе
процесса на много увеличился. Работа получается отрицательной, потому что в
ходе процесса температура увеличилась. Энтропия и изменение энтропии в большей
степени зависит от температуры, чем от объёма. С увеличением температуры,
увеличивается и энтальпия, и внутренняя энергия.
Из анализа работы реального
двигателя видно, что рабочий процесс не является замкнутым и в нём присутствуют
все признаки необратимых процессов: трение, теплообмен при конечной разности
температур, конечной скорости поршня и др.
Паросиловые установки отличаются от
газотурбинных двигателей и двигателей внутреннего сгорания тем, что рабочим
телом служит пар какой-либо жидкости (обычно водяной пар), а продукты сгорания
топлива являются лишь промежуточным теплоносителем.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1.
В.Н.
Кузнецов. Транспортная теплотехника. Часть 1. Техническая термодинамика. М.:
Энергоатомиздат, 1983.
2.
А.И.
Андрющенко. Основы термодинамических циклов теплоэнергетических установок.
М.:Высшая школа., 1968.
3.
А.М.
Литвин. Техническая термодинамика. Госэнергоиздат, 1963.
4.
В.А.
Кудинов. Техническая термодинамика. М.:Высшая школа.,2005.