Синтез 4-нитро-2-(фенилэтинилсульфонил)анилина
Курсовая работа
по курсу: Органическая химия
тема: Синтез 4-нитро-2-(фенилэтинилсульфонил)анилина
Введение
Химия сульфонов тщательно изучена и
широко используется в органическом синтезе на протяжении последних нескольких
десятилетий. Сульфоны с различными ненасыщенными углеводородными заместителями,
как правило, с винилом, часто используют в различных синтезах в качестве
активирующей группы, от которой впоследствии можно избавиться
десульфонилированием. Однако, в настоящее время все больше внимания привлекают
ранее мало изученные ацетиленовые сульфоны.
Сульфонильная группа обладает
сильной электроноакцепторной способностью и поэтому способна активировать
соседние группы и стабилизировать α-карбанион. Поэтому ненасыщенные сульфоны способны к реакциям
сопряженного присоединения нуклеофилов в β-положение и к последующему электрофильному присоединению к α-карбаниону. А
ацетиленовые сульфоны в этом плане выигрывают по сравнению с виниловыми,
поскольку ацетиленовые сульфоны более реакционно-способны к одинарному
присоединению, а также способны, в отличие о виниловых, к двойному
присоединению нуклеофилов в β-положение и, соответственно, к одинарному или двойному
электрофильному присоединению к α-карбаниону.
Свойства ацетиленовых сульфонов
применяют не только в химии, но и в медицине. Так высокая способность к
нуклеофильным присоединениям и малая токсичность делает их хорошими
противоопухолевыми и противогрибковыми препаратами. Лечебные свойства
ацетиленовых сульфонов делают их важными органическими соединениями. И именно
поэтому на сегодняшний день эта область химии бурно развивается.
Целью курсовой работы является
синтез 4-нитро-2-(фенилэтинил-сульфонил)анилина, который ранее нигде не описан
и возможно обладает лечебными свойствами.
Глава 1. Литературный обзор
.1 Получение
ацетиленовых сульфонов
Одними из первых способов получения
ацетиленовых сульфонов были реакции окисления соответствующих сульфидов.
Необходимые сульфиды получают действием тиолят-ионов на галогениды ацетиленов
(с последующей основно-катализируемой изомеризацией), сульфонилированием
ацетиленидов (дисульфидами, сульфонилхлоридами, дихлоридом серы [с получением
бисацетиленовых сульфидов], тиофталимидами, тиосульфонатами или тиоцианатами),
алкилированием ацетиленидов соответствующих терминальных ацетиленовых
сульфидов, дегидрогалогенированием галогенвинил производных сульфидов.
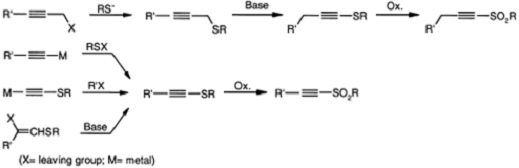
В качестве окислителей используют
м-хлорнадбензойную кислоту, пероксид водорода, пербензойную кислоту,
надуксусную кислоту и др. При использовании одного эквивалента окислителя
получают ацетиленовые сульфоксиды.
Свободно-радикальное присоединение
сульфонил хлоридов, бромидов и иодидов к терминальному ацетилену приводит к β-галогенвиниловым
сульфонам, дегидрогалогенированием которых основаниями, такими как триэтиламин,
основной оксид алюминия или фторида калия в ацетонитриле получают ацетиленовые
сульфоны.
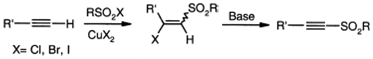
Присутствие хлорида или бромида меди
(II) выступает катализатором присоединения соответствующих сульфонил
галогенидов, а присоединению сульфонил йодида может способствовать
фотоинициирование.
Селенсульфонаты также присоединяются
к ацетиленам по свободно-радикальному механизму. Реакция инициируется
фотохимически (солнечным светом или лампой солнечного света) или нагреванием с
азобисизобутиронитрилом (AIBN). В результате аддукты с терминальными
ацетиленами образуются с высокой регио- и стереоселективностью, предоставляя
продукты анти-присоединения. Поскольку фенилселеновая группа и виниловый
атом водорода цис-ориентированы, окисление и син-элиминирование
селеноксида протекает в мягких условиях, часто обеспечивая почти количественный
выход ацетиленовых сульфонов.
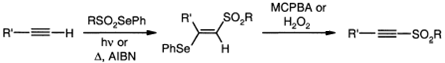
Селенсульфонаты получают окислением
бензолселеновой кислотой сульфонилгидразидов или сульфиновых кислот.
Ацетиленовые трифлаты
(трифторметилсульфоны) получают реакцией ацетиленида лития с трифлатовым
ангидридом.
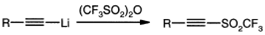
Реакция ацетиленового реактива
Гриньяра с трифлатовым ангидридом приводит к соответствующему ацетиленовому
галогениду в качестве основного продукта, а не к трифлату.
Ацетиленовые сульфоны получают из
полностью обезвоженных соответствующих β-кетосульфонов их реакцией с трифлатовым ангидридом и диизопропилэтиламином
или же реакцией с диэтилхлорфосфатом и трет-бутилатом калия.
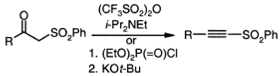
Для получение арилпроизводных
ацетиленовых сульфонов используют сульфонилфосфонат в реакции Виттига-Хорнера.
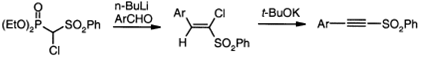
Другой подход основан на превращении
β-кетосульфона в его
семикарбазон, с последующим окислением диоксидом селена. В результате
селендиазол может быть подвергнут пиролизу для получения желаемого ацетилена.
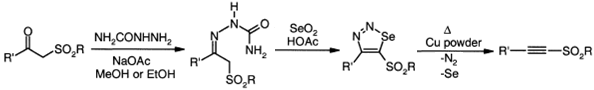
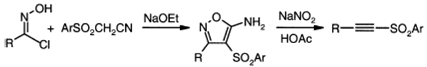
Кроме того, диазотированием
5-аминоизоксазолов, полученных из сульфонилацетонитрилов, также получают
ацетиленовые сульфоны.
Реакцией ацетилендикарбоксилата с
HgCl2 и арилсульфинатом натрия получают β-сульфанилвинил
производные ртути, которые подвергают окислительной демеркуризации и
декарбоксилированию, образуя тем самым соответствующие ацетилены.
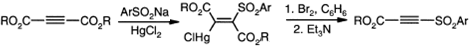
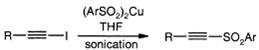
Йодид ацетилена переводят в
ацетиленовые сульфоны сульфинатом меди (II) в ТГФ под действием ультразвука.
Широко используется метод получения
арилсульфонилацетиленов катализируемой AlCl3 реакцией
арилсульфонилхлоридов с ди(триметилсилил)ацетиленом, с последующим гидролизом
оставшихся силильных остатков.
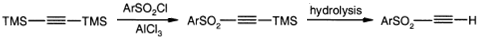
При гидролизе используют силикагель
или NaF.
.2 Химические свойства
ацетиленовых сульфонов
Для ацетиленовых сульфонов
характерны реакции присоединения нуклеофилов (AdN) по тройной С-С
связи. Этому способствует стягивание электронной плотности смежной
электронно-дефицитной сульфонильной группой и стабилизация ею полученного
аниона. Однако такие процессы часто осложнены основно-катализируемой
прототропной изомеризацией ацетиленовых сульфонов до атаки нуклеофила.

Пропаргиловый сульфон, который
содержит неактивированную тройную связь, реагирует с нуклеофилами, образуя
сначала более активный алленовый изомер. В результате образуются продукты анти-присоединения,
а в кинетическом режиме - цис-аддукты (цис положение нуклеофила
относительно сульфон группы), которые часто переходят в более стабильные транс-изомеры.
.2.1 Присоединение
N-нуклеофилов
Из-за основно-катализируемой
прототропной изомеризации ацетиленовый и пропаргиловый сульфоны оказываются
синтетическими эквивалентами, и реакция аминов с каждым типом сульфона приводит
к одному енамин продукту.
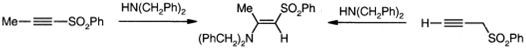
Исследование стереохимии
присоединения к ацетиленовым сульфонам показали, что первичные амины обычно
образуют цис-аддукты анти-присоединением в кинетическом режиме,
после частичной изомеризации получается смесь цис- и транс-изомеров.
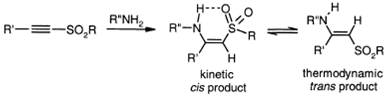
Соотношение геометрических изомеров
в конечном продукте зависит от растворителя, температуры и от природы
заместителей в исходных реагентах. Стабилизация цис-аддукта происходит
за счет внутримолекулярной водородной связи протонов NH с атомом кислорода
сульфона. Вторичные амины преимущественно образуют транс-аддукты из-за
отсутствия такой водородной связи и из-за дипольного и пространственного
отталкивания между амином и сульфоном.

Присоединение азиридина является
аномальным, потому что он иногда образует кинетический цис-аддукт
преимущественно или полностью в результате подавления изомеризации.
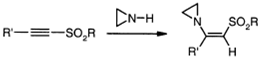
Ацетиленовые бисульфоны способны к
двойному присоединению первичных и вторичных аминов, в том числе анилина.
Второе присоединение амина сопровождается отщеплением сульфинат аниона.
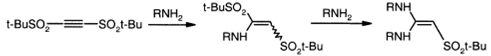
Ацетиленовые трифлаты, обладающие
сильной электрофильностью образуют енамин аддукты с простыми аминами, а также с
фталимидом, где амид образует дипольный интермедиат, который подвергаются
трансацилированию.
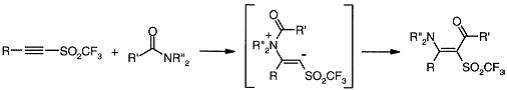
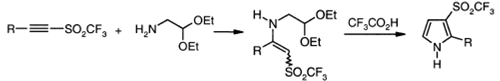
Присоединением аминоацеталя к
ацетиленовому трифлату получают енамин, при внутримолекулярной конденсацией
которого образуется пиррол.
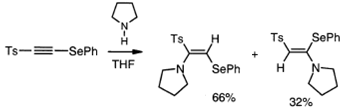
Селенацетиленовый сульфон отражает
аномальную региохимию в его реакции с пирролидином, предоставляя анти-Михаэля
(по отношению к сульфону) аддукт, в качестве основного продукта, что
обусловливается влиянием фенилселенильной группы в преобладании над фрагментом
сульфона в регулировании положения атаки.
А присоединение диэтиламина к
алкинилфосфонату идет в β-положение сульфона
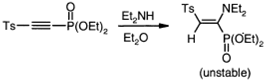
ацетиленовый сульфон синтез анилин
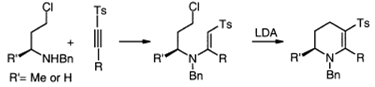
Сопряженное присоединение аминов к ацетиленовым
сульфонам также используется в сочетании с дальнейшими превращениями, чтобы
получить более сложное нужное соединение. Таким образом, различные пиперидины,
пирролизидины, индолизидины и хинолизидины были получены сопряженным
присоединением соответствующих β- или γ-хлораминов к ацетиленовым сульфонам, с последующим
внутримолекулярным алкилированием.
.2.2 Присоединение
спиртов и карбоновых кислот
Как и в случае аминов, алкоксиды
могут реагировать с изомерными ацетиленовым или пропаргиловым сульфонами с
образованием идентичных продуктов сопряженного присоединения из-за
основно-катализируемой изомеризации. Оба изомера (где Ar=Ph) реагируют с
метоксидом натрия с образованием β-(винилметокси)сульфона, а прямое присоединение алкоксида к
сульфонам в кинетическом режиме, с последующей изомеризацией дает транс-продукт β-метоксивинил сульфон.
В более принужденных условиях в результате двойного присоединения
алкоксидов к ацетиленовым сульфонам образуются соответствующие кетали.
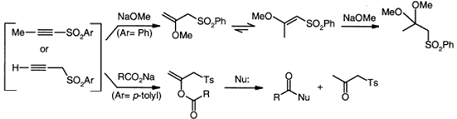
Карбоксилаты присоединяются
аналогично, образуя енольные эфиры, которые функционируют, как активные агенты
ацилирующие нуклеофилы, такие как амины. Терминальный ацетиленовый сульфон
образует цис-изомер прямым анти-присоединением алкоксида.
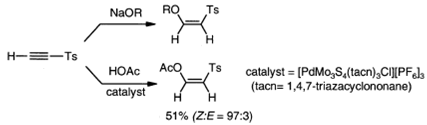
Присоединение же уксусной кислоты
дает аддукт, полученный преимущественно в виде цис-изомера, в
присутствии катализатора.
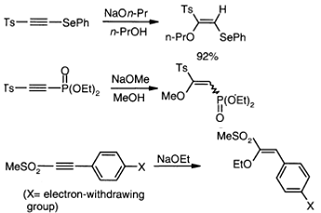
В случае β-арилацетиленового
сульфона, также наблюдается дальнейшая реакция с алкоксидом с замещением
сульфонильного фрагмента.
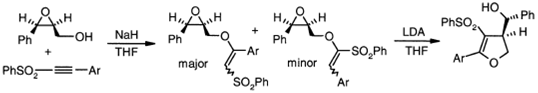
Сопряженное присоединение хирального
эпоксидного спирта к ацетиленовому сульфону при условии энантиоселективного
пути приводит к смеси региоизомеров. Внутримолекулярным алкилированием
основного транс-аддукта получают соответствующий дигидрофуран.
.2.3 Присоединение
тиолов
Как и в случае с азотными и
кислородными нуклеофилами, сценарий с серными нуклеофилами вновь осложняется
равновесием исходных компонентов и их изомерами. Присоединение тиолов к
ацетиленовым сульфонам в присутствии каталитического количества амина дает цис-продукт,
анти-присоединение в кинетическом режиме, а затем изомеризация дает
преимущественно или исключительно соответствующий транс-аддукт.
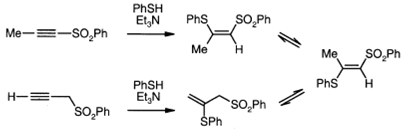
Дальнейшее окисление продуктов в
соответствующие β-сульфонилвиниловые сульфоны может быть достигнуто перекисью
водорода в уксусной кислоте, или перфталевой кислотой. анти-Михаэль
региохимия наблюдается в присоединениях тиолятов к ацетиленовым сульфонам
содержащих β-арильную
или неактивированную группу, такую как фенил.
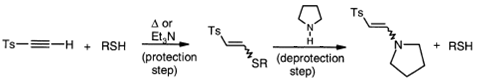
Ацетиленовые сульфоны можно
использовать в качестве защитной группы тиола. Восстанавливают оригинальный
тиол из аддукта пирролидином.
Соответствующие гетероциклические
продукты были получены, когда фосфинилацетилен обработали тиомочевиной,
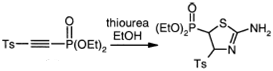
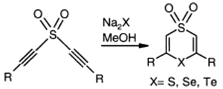
или когда халькогенид натрия был
присоединен к бис(ацетиленовому) сульфону.
.2.4 Алкилирование
ацетиленовых сульфонов
Некоторые металлоорганические
реагенты служат для введения алкильных групп и других заместителей в β-положение ацетиленовых
сульфонов. Реактивы Гриньяра с CuBr, органокупраты (R2CuLi), Me3SiCH2Cu,
и диэтилцинк в присутствии Cu(BF4)2 присоединяются к
ацетиленовым сульфонам образуя продукты преимущественно син-присоединения.
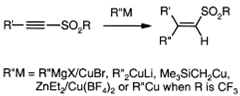
Медьорганические реагенты RCu
присоединяются так же к ацетиленовым трифлатам. Двойное присоединение к
терминальному ацетиленовому сульфону, может быть достигнуто последовательным
присоединением двух медных реагентов.
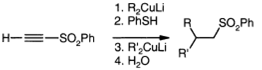
Присоединением RCu к ацетиленовым
сульфоксидам, с последующим окислением м-хлорнадбензойной кислотой,
синтезированы те же продукты, что и полученные от подобных присоединений к
соответствующим сульфонам. Силилацетиленовый сульфон с Me2CuLi дает
продукт нормального присоединения, но его реакция с реактивами Гриньяра или
литийорганическими соединениями дает продукт замещения сульфонильного
фрагмента.
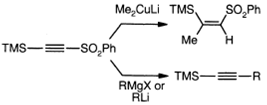
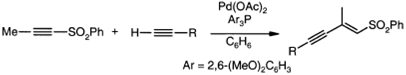
Присоединением терминального ацетилена к
ацетиленовому сульфону при помощи стереоселективного палладиевого катализатора
получают соответствующий енин.
Альдегиды реагируют с ацетиленовыми
трифлатами с образованием ацетиленовых кетонов и дизамещенных ацетиленов,
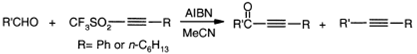
а алкилиодиды дают
алкилтриизопропилсилилацетилен при восстановлении соответствующих ацетиленовых
трифлатов в присутствии гексабутилдистанната.
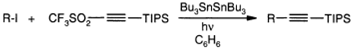
Ацетиленовые сульфоны могут быть
подвержены пиролитической экструзии S02 и рекомбинации, с
образованием соответствующих ацетиленов.
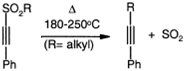
.2.5 Присоединение
галогенов
Ацетиленовые трифлаты реагируют с
LiBr в трифторуксусной кислоте, с LiI в уксусной или с HF в пиридине, образуя
соответствующие β-галогенвинил сульфоны, преимущественно в Z-конфигурации, которые
можно перевести в Е-форму фотохимической изомеризацией аддуктов.
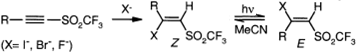
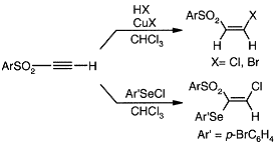
Сухой HCl или HBr присоединяется к
ацетиленовому сульфону в присутствии галогенида меди (I) образуя соответственно
β-хлор- или β-бромвиниловый сульфон.
Селенилхлорид присоединяется аналогично и оба процесса регио- и стереоселективные.
.2.6 Гидролиз
ацетиленовых сульфонов
Ацетиленовые сульфоны подвергаются
кислотно-катализируемому гидролизу с образованием β-кето сульфонов.
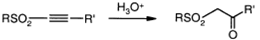
Ацетиленовые трифлаты гидролизуются
в отсутствии катализатора. Предварительный перевод ацетиленовых сульфонов в их
кеталь или енамин производные сопряженного присоединения алкоксидов или аминов,
с последующим гидролизом в более мягких условиях также приводит к
соответствующим β-кетосульфонам. Окислительное расщепление ацетиленовых сульфонов до
соответствующей кислоты идет через оксирановый интермедиат.
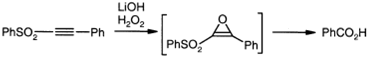
.2.7 Восстановление
ацетиленовых сульфонов
Гидрирование ацетиленовых сульфонов
в присутствии катализатора (палладий на угле) обычно приводит к насыщенным
сульфонам.
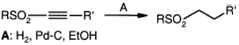
Восстановление различных
ацетиленовых сульфонов до соответствующих цис-виниловых сульфонов
осуществляют с помощью MeEt2SiH/Cu(BF4)2, TaCl5/Zn/пиридин,
(Cod)2Ni и затем уксусной кислотой или с использованием катализатора
Lindlar.
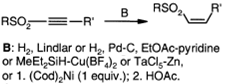
Тогда как использование
натрийборгидрида, диизобутилалюмогидрида (DIBAL) или гидроцирконирование с
последующей обработкой водой, приводит, как правило, к транс-винил
сульфонам.
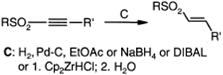
Танталвиниловые интермедиаты,
полученные восстановлением TaCl5/Zn присоединяются к карбонильному
углероду альдегидов или кетонов с образованием соответствующего карбинола.
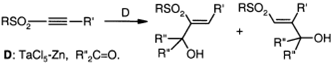
Гашением винилциркониевого
интермедиата, полученного гидроцирконированием ацетиленового сульфона, аллил-
или ацилгалогенидом, или N-галогенсукцинимидом получают виниловый сульфон с
соответствующим аллил-, ацил- или галоген-заместителем в β-положении.
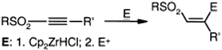
Фотохимическое присоединение
алкилиодидов к терминальному ацетиленовому сульфону в присутствии
гексабутилдистанната приводит к α-йодвиниловым сульфонам, которые переводят в виниловые сульфоны
цинком в уксусной кислоте.
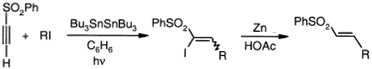
.3 Биологическая
активность ацетиленовых сульфонов
Лечебные свойства сульфонов
обусловлено сильным антигрибковым действием против возбудителей болезней кожи,
а также за счет противовоспалительного, мягчительного, сосудорасширяющего
действия. Установлено, что сульфоны, обладая достаточно высокой
противогрибковой активностью, не проявляют антимикробной активности и мало
токсичны.
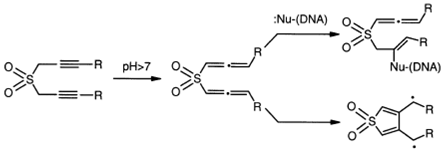
Некоторые бисацетиленовые сульфоны
выступают в качестве ДНК-расщепляющих агентов, что делает их потенциальными,
представляющими интерес противоопухолевыми препаратами. Расщепление ДНК
достигается двумя путями. В первом случае прототропной изомеризацией до
соответствующего алленового сульфона с последующим алкилированием ДНК путем
сопряженного присоединения к электрофильному аллену. Во втором случае,
циклизацией алленового сульфона, что дает бирадикальный интермедиат, который
оказывает цитотоксическое действие.
Некоторые стероидные пропаргиловые
сульфоны рассматривают в качестве потенциальных ингибиторов фермента
глюкозо-6-фосфатдегидрогеназы (Г6ФДГ), изомеризация которых в соответствующие
алленовые сульфоны с последующим сопряженным присоединением к ферменту,
приводит к его деактивации. Снижение уровня Г6ФДГ является профилактическим
эффектом на некоторые виды рака.
.4 Стратегия синтеза
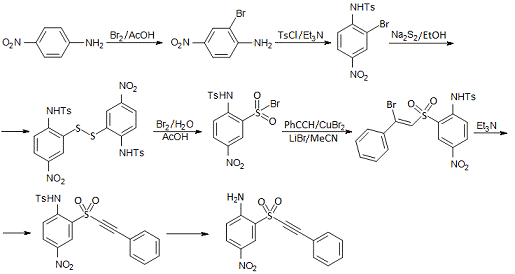
Получать
4-нитро-2-(фенилэтинилсульфонил)анилин будем из п-нитроанилина 7-и стадийным
синтезом. На первой стадии синтезируем 2-бром-4-нитроанилин. На второй -
защитим тозилом аминогруппу. Третья и четвертая стадии заключаются в
нуклеофильном замещении бромида на дисульфид с образованием
ди[5-нитро-2-(п-толуолсульфоамино)фенил] дисульфида и его окислении бромом в
присутствии воды, получив тем самым
5-нитро-2-(п-толуолсульфоамино)бензолсульфобромид. На пятой стадии присоединим
сульфобромид к фенилацетилену, получив β-бромвиниловый сульфон, а на шестой - проведем элиминирование
гидробромида триэтиламином. Заключительная стадия - снятие тозильной защиты с
ацетиленового сульфона.
Глава 2.
Экспериментальная часть
.1 Синтез
2-бром-4-нитроанилина
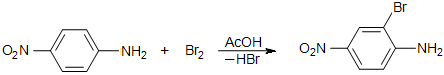
В литровой круглодонной колбе
растворили 34,5 г (0,25 моль) п-нитроанилина в 500 мл уксусной кислоты. Колбу
снарядили обратным холодильником и поместили ее в кипящую водяную баню. В колбу
с реакционной смесью начали приливать небольшими порциями раствор 13,4 мл (0,26
моль) брома в 36 мл уксусной кислоты через выходное отверстие холодильника, при
этом наблюдалось обесцвечивание брома и выделение осадка. После перенесения
всего раствора брома реакционную колбу нагревали на водяной бане 40 мин, а
затем остудили при комнатной температуре. Осадок отфильтровали и промыли
небольшим количеством воды. Полученный продукт растворили при нагревании в
растворе 350 мл изопропилового спирта и 350 мл воды и оставили
кристаллизоваться в холодильнике. Выпавший желтый осадок отфильтровали и отжали
между листами фильтровальной бумаги. При внесении продукта на прокаленной
медной проволоке в пламя горелки наблюдалось зеленое окрашивание пламени, что
свидетельствует о наличие галогена в составе соединения. Выход 73%, т.пл.104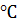 . ИК-спектор получившегося соединения представлен в приложении.
. ИК-спектор получившегося соединения представлен в приложении.
2.2 Синтез
N-(2-бром-4-нитрофенил)-4-метилбензолсульфоамида
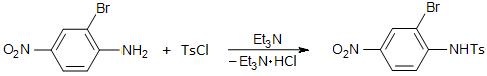
В двугорлой колбе растворили 9,8 г
(0,045 моль) 2-бром-4-нитроанилина в 100 мл хлористого метилена. В
стакан на 50 мл поместили 7,3 мл (0,053 моль) триэтиламина и 30 мл хлористого
метилена. В стакане на 100 мл растворил 8,6 г (0,045 моль)
п-толуолсульфохлорида в 40 мл хлористого метилена. Приготовленные растворы
выдержали в холодильнике 4 часа. После этого колбу с раствором
2-бром-4-нитроанилина поместили в кристаллизатор со смесью льда и соли и
снарядили ее термометром. Перенесли в колбу раствор триэтиламина, а затем стали
приливать небольшими порциями раствор п-толуолсульфохлорида, следя за
температурой, чтобы она не поднималась выше 10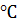 . После этого охлаждение убрали и оставили реакционную колбу с
закрытыми горловинами при комнатной температуре на двое суток. Почерневший за
это время раствор упарили на половину, охладили в холодильнике и отфильтровали
выпавший осадок. Фильтрат перенесли в фарфоровую чашку и испаряли растворитель
при комнатной температуре. Продукт - коричнево-красная маслянистая жидкость.
. После этого охлаждение убрали и оставили реакционную колбу с
закрытыми горловинами при комнатной температуре на двое суток. Почерневший за
это время раствор упарили на половину, охладили в холодильнике и отфильтровали
выпавший осадок. Фильтрат перенесли в фарфоровую чашку и испаряли растворитель
при комнатной температуре. Продукт - коричнево-красная маслянистая жидкость.
.3 Синтез
ди[5-нитро-2-(п-толуолсульфоамино)фенил]дисульфида
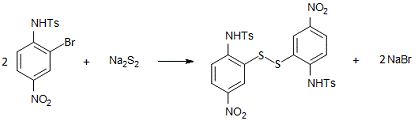
В стакане на 100 мл смешали при
нагревании 9,3 г (0,039 моль) кристаллического сульфида натрия с 50 мл
этилового спирта. Затем сюда же внесли 1,3 г (0,040 моль) измельченной серы и
кипятили 1 час до полного растворения. В процессе приготовления раствора
дисульфида отделился более тяжелый слой его водного раствора. Верхний слой
слили и в горячем состоянии перенесли его в реакционную колбу с кипящим
N-(2-бром-4-нитрофенил)-4-метилбензолсульфоамидом.
.4 Синтез
5-нитро-2-(п-толуолсульфоамино)бензолсульфобромида
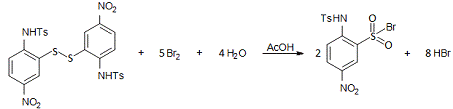
К раствору 3,8 г (6 ммоль)
ди[5-нитро-2-(п-толуолсульфоамино) фенил]дисульфида в 50 мл безводной уксусной
кислоте добавили 1,52 мл (30 ммоль) брома, при этом бром сразу обесцветился и
выпал осадок. Затем к раствору прилили 10 мл воды и выдержали смесь при
комнатной температуре и постоянном перемешивании 30 мин. Прилили к смеси 50 мл
воды, отфильтровали осадок и промыли его 50 мл воды. Осадок
зеленовато-коричневого цвета. При внесении продукта на прокаленной медной проволоке
в пламя горелки наблюдалось зеленое окрашивание пламени, что свидетельствует о
наличие галогена в составе соединения. Выход 70%, т. пл. 197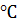 . ИК-спектор получившегося соединения представлен в приложении.
. ИК-спектор получившегося соединения представлен в приложении.
Заключение
Ацетиленовые сульфоны содержат
активированную тройную и связь, что дает большое разнообразие реакций
присоединений, имеющие большую синтетическую полезность. Их легко получить с
помощью различных методов. Биологическая активность ацетиленовых сульфонов мало
изучена, но цитотоксическое действие оказываемое на опухолевые клетки и
расщепление их ДНК дает предпосылки к созданию противораковых препаратов на
основе ацетиленовых сульфонов и их изомеров.
К сожалению, из-за несовершенства
методик и недостатка времени получить 4-нитро-2-(фенилэтинилсульфонил)анилин не
удалось.
Литература
1. Wuts, Peter G.M.
Greene’s protective groups in organic synthesis. - 4th ed. / Peter G.M. Wuts,
Theodora W. Greene / A John Wiley & Sons, Inc. - 2007.
. Back T.G. The
chemistry of acetylenic and allenic sulfones // Tetrahedron. -2001.-V. 57.-P. 5263-5301.
. Химия и медицина:
тезисы докладов VIII Всероссийской конференции с международным участием. - Уфа:
АН РБ, Гилем. - 2010. - С. 231 ISBN 978-5-7501-1124-4