Температура плавления полученного в
результате синтеза соединения 143-144ºC. Данная реакция описана
так же в книге [14]. Присутствие нитрогруппы в соединении было подтверждено ИК
и УФ спектрами. УФ-спектр, λ max/нм (lg ε): 270 (3.31), 405 (3.73). ИК-спектр (КBr), ν/см-1: 1527, 1357 (NO2), Температура плавления
полученного соединения, соответствует литературным данным.
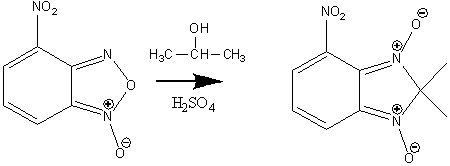
Следующей стадией было взаимодействие полученного соединения
с изопропанолом в серной кислоте, которое приводит к образованию
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксида
27 28
В ИК спектре соединения наблюдаются полосы поглощения при
1537 см- 1, 1357 относящие к колебаниям нитрогруппы. В спектре ПМР
наблюдаются сигналы протонов в виде синглета двух метильных групп в области
1,68 м. д., также наблюдается сигналы протонов ароматического цикла в области
6,87-6,93 дублет дублетов один протон, в области 7,29 дублет один протон, 7,40
дублет еще один протон. В спектре ЯМР 13C наблюдаем сигналы атомов
углерода при 24,42 м. д. двух метильных групп, при 99,01 м. д. сигнал С-2 атома
углерода, при 120, 20, 126,79 и 127,87 м. д. сигналы атомов углерода
ароматического цикла связанных с водородом, при 137,16 и 128,87 м. д. сигналы
атомов углеродов связанные с атомами азота имидазольного цикла. Сигнал атома
при 140,14 м. д. мы отнесли к углероду ароматического цикла связанному с
нитрогруппой. Элементный анализ полученного соединения, соответствует брутто
формуле C9H9N3O4. На основании этих
данных, данному соединению приписали строение 2,2-диметил-4-нитро-2Н-бензимидазол-1,3-диоксида.
Заключительной стадией было изучение фотохромных свойств
соединения.
Для изучения данных свойств мы нагревали полученное вещество
в хлорбензоле до кипения (t=133 ºC) и затем кипятили,
следя по ТСХ за ходом реакции в системе этилацетат-гексан. При нагревании мы
наблюдаем, что в исходное вещество превращается с течением времени в два
соединения, одно из которых бензоксодиазин, а второе моно-н-оксид. Превращение
представлено на рисунке 2.

Рис. 2. Хроматографическая пластинка. (Sorbfil): 1 - исходное
соединение, 2 - моно-н-оксид, 3 - бензоксодиазин
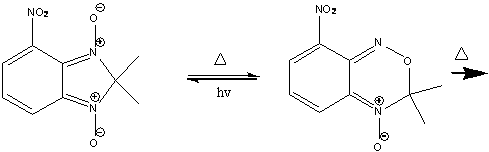
Колоночной хроматографией на силикагеле с 70% выходом был
выделен 8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазин-4-оксид. При дальнейшем
нагревании соединение разлагается по схеме приведенной ниже, механизм
дальнейшего разложения неизвестен.
29 30
32
Заключение о строении данного вещества можно сделать,
сославшись на следующие данные:
При нагревании соединения возможно образование 2х изомерных
бензоксодиазинов. Однако для данной реакции мы наблюдаем образование только
одного бензоксодиазина. Заключение о том, что именно это соединение получено в
реакции, сделано на основании следующего:
Известно, что при нагревании 4-бром-6-нитро-спиро
[бензимидазол-2,1-циклогексан] - 1,3-диоксида образуется только один
бензоксодиазин имеющий по данным РСА строение 8-Бром-6-нитроспиро
[2,1,4-бензоксадиазин-3,1'-циклогексан] - 4-оксид, по аналогии с этими данными
мы приписали строение полученному нами бензоксодиазину строение
8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазин-4-оксид [15].
В ИК спектре соединения наблюдаются полосы поглощения при
1529 см - 1,1344 относящие к валентным колебаниям нитрогруппы. В УФ
спектре имеется полоса поглощения 404 (3.30). В спектре ПМР наблюдается сигналы
протонов двух метильных групп в виде синглета в области 1,61 м. д. наблюдаются
сигналы протонов ароматического кольца в виде мультиплетов в области 7,42 -
один протон, 7,53 м. д. - один протон и 6,73 один протон. В спектре ЯМР 13C
имеются сигналы углерода при 19,90 м. д. двух метильных групп, 95,95 м. д. сигнал
С-2 атома углерода, при 123,91, 124,43 и 128,31 м. д. сигналы атомов углерода
ароматического цикла связанных с водородом, при 129,37 и 143,80, 143,18 м. д.
сигналы атомов углеродов ароматического цикла.
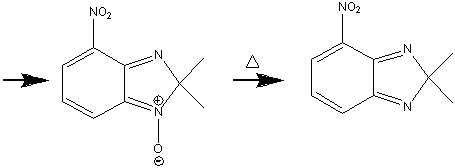
Заключительной стадией было обратное превращение
8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазина в
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид
Под действием солнечного света. Для этого мы растворили
бензоксодиазин в хлороформе и оставили раствор на солнечном свете, раствор
изменил цвет с красного на фиолетовый. По ТСХ в реакционной смеси наблюдается
только один продукт - исходный
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид.
Таким образом мы синтезировали соединение
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид (фиолетовое), которое при нагревании
изомеризуется в 8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазина (красное), а в
свою очередь под действием солнечного света наблюдается изомеризация
8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазина (красное) в
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид (фиолетовое).
3.
Экспериментальная часть
ИК спектры зарегистрированы на приборе "Bruker
Vector" в KBr (концентрация - 0,25 %). Приведены наиболее характерные и
информативные полосы поглощения в спектре.
Спектры ЯМР 1Н и 13С регистрировали на
приборе "Bruker AM 400" (400,13 (1Н) и 100,61 MГц (13С)
в CDCl3 и ДМСО-d6 для 10% растворов при 25 оС.
Химические сдвиги измерены относительно остаточных сигналов растворителя: СНCl3
(δH 7,24 м. д. и δС 76,90 м. д) ДМСО-d6
(δH 2,50 м. д. и δС 39,50 м. д). Мультиплетность
сигналов в спектрах ЯМР 13С определяли в режиме J-модуляции (JMOD).
Контроль за ходом реакций и индивидуальностью соединений
осуществляли методом ТСХ на пластинках Sorbfil UV-254. Проявление хроматограмм
осуществляли УФ светом. Хроматографическое выделение соединений осуществляли на
силикогеле MN - Kiselgel 60 (70-230 mesh)
Температуры плавления определялись на микронагревательном
столике Кофлера.
4-нитро [2,1,3] бензоксадиазол-1-оксида
К раствору 13,6 г (0,1 моль) [2,1,3] бензоксадиазол-1-оксида в
44,5 мл концентрированной серной кислоты. При охлаждении на водяной бане со
льдом и солью до температуры смеси 5-12ºС постепенно прикапывают смесь концентрированной серной (20 мл) и
концентрированной азотной кислот d=1,5 (5 мл, 0,12 моль), перемешивая на
механической мешалке. При этом температура смеси не должна подниматься выше 12ºС. Выдержали 30 минут и массу перенесли в 150 г колотого льда.
Выпавший осадок отфильтровали, промыли водой и
перекристаллизовали из 100 мл уксусной кислоты.
Получили 9г (50%) соединения. Температура плавления 143-144 ºC. Температура плавления литературная 141-143 ºC. (ссылка)
ИК спектр, ν, см-1: 1595
(С=N), 1357, 1537 (NO2)
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид
К раствору 3,62 г (0,02 моль) 4-нитро [2,1,3] бензоксадиазол-1-оксида
в 20 мл концентрированной серной кислоты прибавили по каплям 2.36 г (0,04 моль)
изопропилового спирта. Реакционную смесь перемешивали на магнитной мешалке 1
час 20 минут. Завершение реакции определили по ТСХ. Затем массу вылили в 300 мл
холодной воды и экстрагировали продукта хлороформом (3х50мл). Хлороформенный
экстракт промыли водой и сушили над MgSO4. Растворитель отогнали в
вакууме на выпарке, остаток хроматографировали на силикагеле. Элюент
этилацетат: гексан = 1: 3. Получили 0,33 г чистого
2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксида и 1,1 г этого же
соединения с примесью. Суммарный выход 72%.
т. пл.136-138 оС. ИК спектр, ν, см-1: 1595 (С=N), 1357, 1537 (NO2) УФ
спектр, λ макс., нм. (lg ε): 254 (3.90), 547
(3.80). Спектр ЯМР 1Н (СDCl3), δ, м. д.: 1.68 c (6Н, 2СН3), 6.84 - 6.95 м (1Н, СН), 7.29
д (1Н, СН, J=7.4 Гц).7.40 д (1Н, СН, J=9.4 Гц). Спектр ЯМР 13С, δ, м. д.: 24.40 (СН3), 99.01 (С2), 120.20,
126.80, 127.87 (все СН), 127.09, 137.16, 140.14 (все С).
Термолиз 2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксида
0.5г 2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид
растворили в 5 мл хлорбензола. Реакционную смесь нагрели до 133 ºC и оставили кипеть, делая каждые 5 минут отметки на пластинке
ТСХ. Через 15 минут кипячения мы наблюдали максимальное количество
8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазин 4-оксида. Растворитель отогнали в
вакууме. Остаток хроматографировали на силикагеле. Элюент этилацетат: гексан =
1: 3. В первых фракциях выделили с 63% выходом 8-нитро-3H-бензо - [с] - [1,2,5]
- оксодиазин-4-оксид.8-Нитро-3,3-диметил-3Н-бензо [1,2,5] оксадиазин-4-оксид
Выход (63 %) бензоксодиазина. т. пл. - .55-57. ИК спектр, ν, см-1: 1344, 1529 (С-NO2). УФ спектр, λ макс., нм. (lg ε): 404 (3.30). Спектр ЯМР
1Н (CDCl3), δ, м. д.: 1.59 c (6Н, 2СН3),
6.78 м (1Н, СН), 7.38 м (1Н, СН).7.53 м (1Н, СН). Спектр ЯМР 13С, δ, м. д.: 19.90 (2СН3),95.95 (С2), 123.91,
124.44, 128.31 (все СН), 129.37, 143.18, 143.80, (все С).
Фотолиз 8-нитро-3H-бензо - [с] - [1,2,5] -
оксодиазин-4-оксида
Растворили 100 мг 8-нитро-3H-бензо - [с] - [1,2,5] -
оксодиазин-4-оксида в хлороформе и оставили его на неделю на солнечном свете,
раствор изменил цвет с красного на фиолетовый. По ТСХ в реакционной смеси
наблюдается только один продукт - исходный 2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид.
Выводы
Таким образом мы синтезировали новое соединение проявляющее
фотохромные свойства - 2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид. Данное
соединение при нагревании изомеризуется с изменением цвета в 8-нитро-3H-бензо -
[с] - [1,2,5] - оксодиазин-4-оксид, которое при облучении солнечным светом
изомеризуется в исходный 2,2,-диметил-4-нитро-2Н-бензимидазол-1,3-диоксид.
Рис 3. Фильтровальная бумага была пропитана раствором
8-нитро-3H-бензо - [с] - [1,2,5] - оксодиазин-4-оксида в хлороформе, высушена и
выставлена на солнечный свет с наложенным трафаретом. Получено темно-синее
изображение на оранжевом фоне.
Список
литературы
1.
Boiani M., Boiani L., Denicola A., Torres de Ortiz S., Serna E., Bilbao N. V.,
Sanabria L., Yaluff G., Nakayama H., Arias A. R., Vega C., Rolan M.,
Gomez-Barrio A., Cerecetto H., Gonzalez M.2Н-Benzimidazole 1,3-Dioxide
Derivatives: A New Family of Water-Soluble Anti-Trypanosomatid Agents. // J.
Med. Chem. - 2006. - V.49. - P.3215-3224.
.
Aguirre G., Boiani M., Cerecetto H., Gerpe A., Gonzalez M., Sainz Y. F.,
Denicola A., Ocariz Carmen Ochoa de, Nogal J. J., Montero D., Escario J. A.
Novel Antiprotozoal Products: Imidazole and Benzimidazole N-Oxide Derivatives
and Relater Compounds. // Arch. Pharm. Pharm. Med. Chem. - 2004. -
V.337. - P.259-270.
.
Part of this research is presented in the Uruguayan patent of invention: Boiani
M., Cerecetto H., Gonzalez M., Merlino A. Derivados de 1,3-dioxido de
benzimidazol. Procedimiento de preparacion y utilizacion (Benzimidazole
1,3-dioxide derivatives. Preparation procedure and utilization). UR Patent
No.29076, 2005.
4.
Volkamer K., Zimmermann H. W. Uber arylsubstituierte 1-Hydroxy-imidazole und
1-Hydroxy-imidazol-N-3-oxide. // Chem. Ber. - 1969. - Bd.102. - N.12. -
S.4177-4187.
.
Marwan J. Abu El-Haj. Novel Synthesis of 1-Hydroxy-1H-benzimidazole 3 - Oxides
and 2,2-Dialkyl-2H-benzimidazole 1,3-Dioxides. // J.org. Chem. - 1972. -
V.37. - P.2519-2520.
.
Latham D. W. S., Meth-Cohn O., Suschitzky H., Herbert J. A. L. Benzofurazan
N-Oxides as Synthetic Precursors. Part 2. Conversion of Benzofurazan N-Oxides
into 2H-Benzimidazoles and Some Unusual Reachtions of 2H-Benzimidazoles. // J.
Chem. Soc. Perkin. Trans.1. - 1977. - N.5. - P.470-478.
.
Bulacinski A. B., Screven E. F. V., Suschitzky H. The reaction of benzofuroxan
with p-anisylazide: trapping of the o-dinitrosointermediate. // Tetrahedron
Lett. - 1975. - N.41. - P.3577-3578.
.
Garner G. V., Suschitzky H. The thermal uncatalysed cyclisation of
N-cyclohexyl-o-nitroaniline: the question of a nitrene versus an aci-nitro
mechanism. // Tetrahedron Lett. - 1971. - N.2. - P.169-172.
.
Dirlam J. P., Cue B. W., Combatz K. J. Thermal decomposition of
2-azidoquinoxaline N-oxides. // J.org. Chem. - 1978. - V.43. - N.1. -
P.76-79.
.
Самсонов В.А., Володарский Л.Б. Взаимодействие производных N-окисей
4,7-дибром-2Н-бензимидазола с аминами. // Ж. орг. химии. - 1982. - Т.18.
- Вып.3. - c.656-662.
.
Самсонов В.А., Володарский Л.Б., Шамирзаева О.В. Образование
2Н-бензимидазол-1,3-диоксидов при взаимодействии бензофуроксанов со спиртами и
галогеналканами в присутствии кислот. ХГС - 1994. - N.4. - с.524-528.
.
Громов С.П. Фотохромные свойства органических молекул. Москва 2008.
.
Mallory. F. B. Varimbi S. P. J.org. chem. 1963. v28. p.1656-1662.
.
"Химия фуроксанов. Реакции и применение” Хмельницкий А.И. Новиков С.С.
Годовикова Т.И. изд "Наука" 1983 г. стр.227.
.
Samsonov V. A., Gatilov Yu. V., Savel'ev, V. A, Russian journal of organic
chemistry, 2013, Vol.49, No.8, pp.1223−1229.