Ветеринарно-санитарная оценка туш и внутренних органов сельскохозяйственных животных при отравлении их солями тяжелых металлов
Министерство
сельского хозяйства Российской Федерации
ФГОУ ВПО
Донской
Государственный Аграрный Университет
Кафедра
паразитологии, Эпизоотологии и Ветсанэкспертизы
курсовая
работа
на тему:
Ветеринарно-санитарная
оценка туш и внутренних органов скльскохозяйственных животных при отравлении их
солями тяжелых металлов
Выполнил: ст-ка 4 курса ВСЭ, гр. 1б
Билая К.А.
Проверил: доцент Соловьёв Н.А.
п.
Персиановский
г.
Содержание
Введение
Этиология
отравлений
Характеристика
отравляющего вещества
Диагностика
отравления
Ориентировочные
параметры концентрации тяжелых металлов в продуктах животноводства, мг/кг
Ветеринарно-санитарный
осмотр
Лабораторные
исследования
Определение
солей тяжёлых металлов в тушах и органах
Ветеринарно-санитарная
оценка
Гигиенические
нормативы качества и безопасности продовольственного сырья и пищевых продуктов.
СанПиН 2.3.2,560-96
Список
используемой литературы
Введение
В организм животных минеральные вещества поступают с кормами и питьевой
водой, обеспечивая в большинстве случаях оптимальный обмен веществ и энергии,
образование гормонов, костной и других тканей, также в организм попадают и
тяжелые металлы. Тяжелые металлы, аккумулируясь растениями и микроорганизмами,
попадают в организм животных, что может стать причиной контаминации продуктов
животноводства и, как следствие пищевых токсикозов у человека. При этом нельзя
исключать мутагенные и канцерогенные эффекты тяжелых металлов. Соли тяжелых
металлов способны накапливаться в организме и не разрушаются при длительном хранении
мяса и обработке высокими и низкими температурами.
В мясе происходят глубокие изменения физико-коллоидной структуры белка,
что приводит к уменьшению вкусовых и питательных качеств мяса. Дисбаланс
минеральных элементов в продуктах убоя также оказывает отрицательное действие
на органолептические показатели мяса.
Этиология отравлений
Несмотря на существующее запрещение, в отдельных хозяйствах используются
остатки протравленного зерна для кормовых целей. Имеются факты нарушения правил
хранения, транспортировки и применения ядохимикатов. Неправильное применение
лекарственных препаратов, антигельминтиков и акарицидов ведет к попаданию
отравляющих веществ в организм животных. Отравляющие вещества попадают в
организм через слизистые оболочки, кожу и желудочно-кишечный тракт, аэрозольно,
контактно, алиментарно.
Характеристика отравляющего вещества
Ртуть классический тиоловый яд. Проникая через клетки, реагирует с
сульфгидрильными группами окислительно-восстановительных ферментов, блокируя их
активность. Подавляется функциональное состояние центральной нервной системы,
печени, почек, желез внутренней секреции, пищеварительного тракта,
мочевыводящих путей. Является иммунодепресантом.
Свинец классический кумулятивный яд. Свинец и его соединения реагируя с
кислотой образует растворимые соли, которые связываясь с белками образуют
альбуминаты. В крови свинец проникает в эритроциты, что ведет к снижению
резистентности эритроцитов и их гемолизу. Увеличение проницаемости клеточных
мембран ведёт к потере воды и калия.
Мышьяк, сильно действующий цитоплазматический яд общего действия. В
организме образует прочные циклические соединения, в результате развиваются
дистрофические изменения и некроз тканей, понижается тонус стенок сосудов и
капилляров, это ведет к падению кровяного давления и ослаблению
сердечно-сосудистой деятельности.
Медь подавляет активность многих ферментов, вызывает гемолиз эритроцитов,
анемию, гастроэнтерит.
Диагностика отравления
отравление тяжелый металл орган
В зависимости от дозы и кратности поступления отравляющего вещества в
организм отравления у сельскохозяйственных животных могут протекать остро,
подостро и хронически. Следует иметь в виду, что почти каждый случай острого
заболевания характеризуется внезапностью заболевания группы животных. Общие характеристики
отравления состояние угнетенное, исхудание, наблюдается отсутствие аппетита,
Состояние животных при отравлении ртутью угнетенное, исхудание,
наблюдается отсутствие аппетита, рвота, понос, частые дыхание и пульс,
нарушение координации движений, судороги, парезы, параличи прекращение
выделения мочи. Смерть от паралича дыхательного центра или сердечно-сосудистой
недостаточности.
Отравление свинцом характеризуется беспокойством, сменяющимся угнетением,
мышечной дрожью, судорожным состоянием, слюнотечением, поносом, жаждой,
припухлостью суставов, возможна анурия, судороги. На деснах появляется
красно-серая кайма.
Отравление мышьяком может протекать в паралитической и желудочно-кишечной
форме. Общее возбуждение сменяется апатией, приступами судорог, рвотой,
сердечно-сосудистой недостаточностью, слюнотечением, поносом.
Отравление медью сопровождается потерей аппетита, слюнотечением, рвотой,
поносом / могут быть окрашены в голубовато-зеленый цвет с примесью крови /,
общей слабостью, параличами, судорогами, анемией, желтушностью слизистых.
Окончательное заключение только после лабораторного исследования.
Химический анализ определяется данными сопроводительного документа и
патанатомического исследования.
Ориентировочные параметры концентрации тяжелых металлов в продуктах
животноводства, мг/кг
Таблица 1.
|
Наименование органов и
тканей
|
Pb
|
Cd
|
Cr
|
Sn
|
Ni
|
Al
|
Ti
|
Sr
|
|
|
в продуктах скотоводства
|
|
|
Мясо говядина min opt max скелет
(ребро) min opt
max лёгкие
min opt max
|
0,10 0,19 0,50 0,100,15
0,30 0,081 0,11 0,16
|
0 0,012 0,058 отс. 0,006
0,03 0,12
|
0,05 0,10 0,20 0,049 0,078
0,10 0,037 0,103 0,230
|
5,04 6,60 8,21 2,90 10,10
16,16 10,99 27,69 39,88
|
0,077 0,15 0,34 0,15 0,17
0,23 0,045 0,139 0,180
|
3,33 8,84 14,24 9,58 15,10
23,24 5,39 26,01 32,30
|
0,03 0,46 1,81 отс.
0,049 0,337 1,16
|
0,12 0,39 1,40 88,92
109,01 140,04 0,15 1,355 5,30
|
|
Мясо свинина min opt max скелет
(ребро) min opt
max легкие
min opt max почки min opt max печень min opt max сердце min opt max жир
подкожный min opt max жир внутренний min opt max
|
0,10 0,11 0,17
0,50 1,28 2,04 0,10 0,10 0,10 0,10 0,12 0,20 0,09 0,14 0,21 0,11 0,20 0,38
0,05 0,11 0,19 0,06 0,13 0,21
|
0,008 0,03 0,121 отс.
0,016 0,14 0,039 0,008 0,07 0,14 0,021 0,03 0,05 0,01 0,027 0 0,0008 0,005 0
0,004 0,008
|
0,015 0,017 0,75 1,21 2,05
4,04 0,015 0,02 0,05 0,015 0,13 0,67 0,15 0,47 1,84 0 0,28 0,58 0 0,51 1,46
0,20 0,54 1,20
|
0,25 0,35 0,60 4,91 7,14
9,94 0,11 0,26 0,48 0,10 0,23 0,66 0,09 1,08 1,43 0,19 2,39 3,92 0 0,92 2,41
1,04 1,50 2,20
|
0,13 0,21 0,32 0 0,17 0,64
0,07 0,15 0,49 0,11 0,18 0,39 0,10 2,74 15,79 0,06 0,26 0,41 0,07 0,61 2,92
0,08 0,18 0,47
|
11,48 36,84 53,41 0 13,28
39,50 14,42 29,59 50,06 15,85 26,61 37,07 9,60 21,55 54,7 3,70 12,16 34,0
5,20 12,52 25,10 11,0 23,95 40,5
|
0,11 0,23 0,39 10,66 50,61
94,47 0,15 0,29 0,35 0,092 0,18 0,26 0,124 4,89 6,46 5,97 8,83 14,64 0,76
1,04 1,36 2,24 3,15 4,17
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Указанные в таблице параметры (мин., макс., опт.) экологически допустимой
концентрации тяжелых металлов тесно связаны со сложившимися технологиями
производства продуктов животноводства.
Степень загрязнения мяса свинины тяжелыми металлами выглядит в убывающей
последовательности следующим образом (%): 97,12- алюминий, 0,92- олово, 0,60-
стронций, 0,55- никель, 0,44- хром, 0,29- свинец, 0,08- кадмий, сурьма в мясе
свиней массой 130-133кг обнаружен не был. Мясо свиней по общей сумме всех
тяжелых металлов в нем является самым чистым (13,10мг/кг).
По степени накопления никеля органы и ткани располагаются в следующей
последовательности: почки- печень- легкие- длиннейшая мышца спины; свинца:
мышца- печень- почки- легкие; кадмия: почки- мышцы- печень- легкие.
Для ВСЭ и ВСО имеет значение характер отравления так как концентрация
ядов и ядохимикатов (особенно обладающих кумулятивными свойствами) в мясе
различных видов животных различна. Т.о. вет. Специалист должен правильно
составить сопроводительную записку, с указанием предварительного диагноза и
вида отравляющего вещества (по клиничечким признакам).
Ветеринарно-санитарный осмотр
При послеубойной экспертизе необходимо иметь в виду, что патанатомические
изменения в туше и внутренних органах имеют общие признаки с мясом больных
животных. Послеубойный ветеренарно-санитарный осмотр проводят по общепринятой
методике. Но при осмотре органов во всех случаях подозрения на отравление
делают глубокий продольный разрез почки для исследования корки и мозгового
слоев и слизистой оболочки почечной лоханки, а также обязательно вскрывают
желудок, кишечник и мочевой пузырь, чего не делают при обычной экспертизе.
При остром и подостром отравлении при ВСЭ находили:
место зареза ровное, слабо инфильтровано кровью
На эпи- и эндокарде точечные кровоизлияния, сердечная мышца неравномерно
окрашена, серо-красного цвета. В сердечной сорочке скопление небольшого
количества жидкости соломенного цвета.
Слизистая оболочка трахеи, бронхов несколько покрасневшая, в просвете
пенистое содержимое. Легкие в большинстве случаев полнокровны, темно-красного
цвета, с поверхности разреза стекает пенистая темно-красная жидкость.
Печень полнокровна, часто дряблая, глиняная или темно-коричневого цвета,
неравномерно окрашена с поверхности и на разрезе. Желчный пузырь умеренно
наполнен вязкой желчью, слизистая желто-зеленого цвета, с точечными
кровоизлияниями.
Почки с поверхности от бледно- до желто-коричневого цвета. Местами видны
различной величины красные пятна, на разрезе границы слоев сглажены.
Селезёнка чаще без видимых изменений, в единичных случаях в капсуле видны
точки буроватого цвета.
В пищеводе изменений не обнаружено. В сетке, рубце и книжке могут быть
различной формы и величины серо-белого цвета участки некроза. Стенки сычуга,
тонкого и толстого отделов кишечника покрасневшие, утолщены, отечны, в просвете
жидкое содержимое со слизью. Сосуды брыжейки резко инъецированы, лимфатические
узлы несколько увеличены в объеме, сочные. В слепой и прямой кишках
кровоизлияния.
Легкие отечны, ателектаз.
Дисбаланс минеральных элементов в продуктах убоя оказывает отрицательное
действие на органолептические показатели мяса:
недостаточное обескровливание, проявляющееся темно-красной окраской туш и
наличием остатков крови под серозными покровами в просвечивающихся сосудах, и
розовый цвет подкожного жира;
слабо выражена корочка подсыхания, указывающая на нарушение процессов созревания
вследствие накопления в мясе недоокисленных продуктов обмена, в результате
создается благоприятные условия для развития микрофлоры и, как следствие
нестойкость при хранении.
Лабораторные исследования
Для лабораторного исследования отбирают пробы мышц из разных участков
туши общей массой 500г. внутренних органов (печень, почки, селезенка, легкие) -
массой 250г. Каждый образец упаковывают отдельно и указывают, откуда взята
проба, её количество причину направления на исследование. Тару с образцами
опечатывают или пломбируют. Материал отправляют в не консервированном виде.
Биохимические показатели как у больных животных:
Пробы мяса в день убоя биохимическому анализу подвергать не следует.
уменьшение концентрации водородных ионов, сохраняющееся и на вторые
сутки.
положительная формольная проба
сомнительная цветная окислительная реакция
Обнаружена грамположительная кокковая микрофлора.
Методика определения солей тяжелых металлов в тушах и внутренних органах
Минерализация материала. Металлические яды и мышьяк в биологическом
материале находятся в прочно связанном состоянии с белками. Для их определения
нужно разрушить эти комплексы (альбуминаты). Это достигается окислением
исследуемого материала серной и азотной кислотами (мокрая минерализация).
Оборудование и реактивы. Органы и мясо отравленных животных или мясо, в
которое инъецированы растворы ядовитых веществ,-100 г; колба Кьельдаля на 500
мл; лабораторный штатив; электроплитка или газовая горелка; ступка; фарфоровая
луночка; пинцет, ножницы, делительная воронка; стакан на 200 мл; мерная колба
на 200 мл; мерный цилиндр на 100 мл; пипетка, бумажный фильтр;
концентрированная серная и азотная кислота, разбавленная азотная кислота (1 :
1); формалин; 42 %-ный раствор хлорной кислоты; раствор дифениламина в серной
кислоте (0,5 г дифениламина растворяют в смеси, состоящей из 100 частей х. ч.
концентрированной серной кислоты и 20 частей дистиллированной воды).
Исследуемый материал (100 г) тщательно измельчают в ступке, помещают в
колбу Кьельдаля и приливают по 25 мл дистиллированной воды, концентрированных
азотной и серной кислот (можно заранее приготовить смесь из этих ингредиентов и
прилить ее 75 мл). Для ускорения минерализации добавляют 25 мл 42 %-ного
раствора хлорной кислоты. Если последней нет, то минерализацию можно проводить
и без нее. Колбу закрепляют в вертикальном положении в лабораторном штативе,
над ней фиксируют делительную воронку с разбавленной азотной кислотой (1:1).
После прекращения вспенивания колбу нагревают на газовой горелке или плитке (при
постепенном усилении нагревания) до начала потемнения жидкости. Затем при
постоянном нагревании по каплям добавляют разбавленную азотную кислоту, пока
содержимое колбы не станет бесцветным и не будет изменяться по цвету при
добавлении HN03. После этого продолжают нагревание
без добавления HN03 до появления
белых паров SO2. Колбу охлаждают и ее содержимое
переносят в стакан емкостью 200 мл, несколько раз сполоснув водой.
Наличие окислов азота в минерализате, мешающих дальнейшему исследованию,
определяют при помощи раствора дифениламина в серной кислоте. В фарфоровой
луночке каплю минерализата смешивают с раствором дифениламина. При присутствии
окислов азота появляется синее окрашивание. Освобождаются от них формалином. К
нагретому до кипения минерализату по каплям добавляют формалин до прекращения
выделения пузырьков газа. Окончание денитрации определяют пробой с
дифениламином. Остатки формалина удаляют нагреванием жидкости в течение 5-10
мин. Остывшую жидкость разбавляют водой до 180-190 мл, оставляют на 18-20 ч при
комнатной температуре. Свинец и барий в виде сульфатов выпадают в осадок. Его
отфильтровывают на бумажном фильтре. Фильтрат в мерной колбе доводят водой до
200 мл и исследуют на марганец, хром, серебро, медь, цинк, мышьяк и др.
При небольшом количестве исследуемого материала можно брать его 50 или
25г, соответственно уменьшив количество реактивов, используемых для
минерализации. Описанная методика минерализации непригодна для определения
ртути, так как последняя в значительной степени теряется за счет испарения.
Обнаружение
свинца. Методы основаны на растворении свинца в ацетате аммония с последующей
постановкой цветной реакции с дитизоном или микрокристаллоскопических реакций.
Оборудование и реактивы. Бумажный фильтр с осадком, полученным после фильтрования
минерализата; микроскоп; спиртовка; колба, две пробирки; предметные стекла;
глазные пипетки; раствор ацетата аммония (насыщенный раствор ацетата аммония
разбавляют равным объемом воды и на каждый литр раствора добавляют 30 мл
ледяной уксусной кислоты); 0,2 н. раствора серной кислоты; 0,01 %-ный раствор
дитизона в хлороформе; 30 %-ный раствор уксусной кислоты; хлористый цезий;
йодистый калий; нитрит калия; 1 %-ный раствор ацетата меди.
Бумажный
фильтр с осадком, полученным после фильтрования минерализата, промывают 15-20
мл 0,2 н. раствора серной кислоты, а затем 10 мл воды (жидкость не собирают).
Осадок на фильтре обрабатывают кипящим раствором ацетата аммония (от 0,5 до 10
мл в зависимости от величины осадка). Сульфат свинца растворяется и переходит в
фильтрат. Последний собирают в пробирку.
Реакция с дитизоном. В пробирке смешивают встряхиванием 1-2 мл фильтрата
с равным объемом 0,01 %-ного раствора дитизона в хлороформе. При наличии свинца
(рН 7-10) появляется пурпурно-красное окрашивание слоя органического
растворителя.
Микрокристаллические реакции. По 0,5 мл фильтрата распределяют на двух
предметных стеклах и упаривают капли на пламени спиртовки.
1. К остатку добавляют 2-3 капли 30 %-ной уксусной
кислоты. С одной стороны капли вносят 2-3 кристаллика хлористого цезия, а с
другой - несколько кристаллов йодистого калия. При наличии свинца через
несколько минут под малым увеличением микроскопа обнаруживают желто-зеленые
игольчатые кристаллы, часто собранные в пучки и сфероиды.
2. К остатку прибавляют 1-2 капли 1 %-ного раствора
ацетата меди и упаривают досуха. Наносят 2-3 капли 30 %-ной уксусной кислоты.
На край капли помещают несколько кристаллов нитрита калия. При наличии свинца
через несколько минут под микроскопом выявляются черные или коричневые
кристаллы в виде кубов.
Обнаружение бария. Метод основан на способности сульфата бария
образовывать характерные кристаллы.
Оборудование и реактивы. Остаток на фильтре после обработки его ацетатом
аммония; микроскоп; спиртовка; предметное стекло; платиновая петля; глазная
пипетка; концентрированная серная кислота (уд. масса 1,84).
Часть осадка BaS04 (при малых количествах полностью)
платиновой петлей переносят на предметное стекло, наносят на него 2-3 капли
концентрированной серной кислоты и нагревают на пламени спиртовки до появления
паров серного ангидрида. Охлаждают при комнатной температуре. Через 10-20 мин
под микроскопом обнаруживают бесцветные кристаллы BaS04 в виде крестов или пластинок с вытянутыми углами.
Обнаружение
меди. Метод основан на экстрагировании меди из минерализата хлороформом в виде
диэтилдитиокарбамината меди, последующего вытеснения ее из этого соединения в
водный слой ртутью, где она и обнаруживается соответствующими цветными
реакциями.
Оборудование
и реактивы. Фильтрат минерализата (после отделения сульфатов свинца и бария);
лабораторный штатив; делительная воронка, колба, две пробирки; технохимические
весы; 25 %-ный раствор гидроокиси аммония (NH4OH),
тетрароданомеркурат аммония (5 г хлорида ртути и 5 г роданида аммония
растворяют в 6 мл воды); 1 %-ный спиртовый раствор 2,4-дииитрофенола
(индикатор); 5 %-ный раствор ферроцианида калия; 2 %-ный раствор хлорида
кадмия; 6 н. раствор соляной кислоты; 1 %-ный раствор хлорида ртути (HgCl2); хлороформный раствор
диэтилдитиокарбамината свинца - РЬ(ДДТК)2 (0,5 г ацетата свинца растворяют в
воде, добавляют 25 мл 10 %-ного раствора нитрата калия и 0,5 г растворенного в
воде Ка(ДДТК), образовавшийся белый осадок РЬ(ДДТК)2 экстрагируют хлороформом,
водный раствор, свободный от белого осадка РЬ(ДДТК)2, отбрасывают, хлороформный
слой фильтруют и добавляют к нему хлороформа до 250 мл); хлороформ, сульфат
цинка.
В делительную воронку помещают 10 мл минерализата, прибавляют несколько
капель 1 %-ного спиртового раствора 2,4-динитрофенола и по каплям 25 %-ный
раствор гидроокиси аммония до появления желтого окрашивания. Приливают 5 мл
хлороформного раствора диэтилдитиокарбамината свинца и энергично встряхивают,
Хлороформный слой окрашивается от желтого до коричневого цвета (возможно за
счет естественного содержания меди в мясе и органах). Хлороформный экстракт
промывают 6 н, раствором соляной кислоты, затем дистиллированной водой.
Добавляют к нему по каплям (периодически встряхивая) 1%-ный раствор хлорида
ртути (0,5-1 мл) до обесцвечивания. Приливают 0,5-1 мл воды, встряхивают и
водный слой отделяют. Делят его на две равные части, переносят в пробирки и
ставят реакции.
1. Добавляют 0,2 г сульфата цинка и несколько капель раствора
тетрароданомеркурата аммония. При наличии меди осадок окрашивается в
розово-лиловый цвет.
2. Добавляют 10 капель 2 %-ного раствора хлорида кадмия и 1-2
капли 3 %-ного раствора ферроцианида калия. При наличии меди осадок
окрашивается в лиловый цвет.
Обнаружение цинка. Метод основан на экстракции цинка из минерализата
хлороформом, связывании ионов кадмия и меди (мешающих обнаружению цинка)
тиосульфатом натрия или тиомочевиной, образовании цинка с дитизоном окрашенного
соединения - дитизоната цинка.
Оборудование и реактивы. Минерализат; пробирки, пипетка, универсальная
индикаторная бумага; насыщенный раствор тиомочевины или насыщенный раствор
тиосульфата натрия; 10 %-ный раствор едкого кали или натра; ацетатный буфер
(4,2 г ацетата натрия, 3,2 г уксусной кислоты, до 1 л воды); 0,01 %-ный раствор
дитизона в хлороформе; хлороформ.
В пробирку берут 0,5 мл минерализата, прибавляют 0,25 мл насыщенного
раствора тиосульфата натрия (или тиомочевины) для связывания ионов кадмия, по
каплям добавляют 10 %- ный раствор едкого калия или едкого натра до рН смеси
5--5,5 (рН устанавливают универсальной индикаторной бумажкой). Добавляют 1 мл
ацетатного буфера, 2-3 капли 0,01 %-ного раствора дитизона в хлороформе и 1 мл
хлороформа. Смесь энергично встряхивают. При наличии цинка зеленый цвет
хлороформного слоя переходит в розовый или красно-фиолетовый (в зависимости от
его количества).
Качественное и количественное определение мышьяка (по Зангер-Блеку).
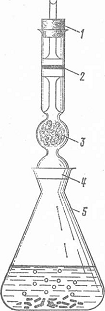
Рис. 1.
Прибор Зангер -- Блека для определения мышьяка:
- пробка; 2 -
кожух реактивной бумаги; 3- вата, пропитанная уксуснокислым свинцом; 4- шлифт;
5 - редукционная колба.
Метод основан на восстановлении мышьяка до мышьяковистого водорода (AsH3J), который при взаимодействии с хлоридом IHgCbJ или бромидом (HgBr2) ртути образует окрашенное в желтый
или желтовато-коричневый цвет соединение (As2Hg3).
Оборудование и реактивы. Минерализат (измельченный продукт); прибор
Зангер-Блека (рис.1.); 6 колб к прибору емкостью 50 мл; 20 %ный раствор серной
кислоты; 10 %-ный раствор хлорида олова в 15 н. серной или 6 н. соляной кислоте
(при растворении подогревают); купрированный мелкогранулированный цинк (гранулы
цинка на несколько секунд, до потемнения, погружают в 0,05 %-ный раствор
сульфата меди и затем промывают дистиллированной водой); бромортутная или
хлорортутная бумага (полоски фильтровальной бумаги смачивают 5 %-ным спиртовым
раствором хлорида или бромида ртути и высушивают при комнатной температуре в
вытяжном шкафу); вата, смоченная 5%:ным раствором уксуснокислого свинца и
высушенная на воздухе; стандартный раствор мышьяка.
Стандартный раствор мышьяка: 0,1321 г перекристаллизованного
мышьяковистого ангидрида растворяют в возможно малом количестве 10 %-ного
едкого натра. Полученный раствор переносят в мерную колбу емкостью 100 мл,
нейтрализуют серной кислотой в присутствии фенолфталеина и доводят объем
дистиллированной водой до 100 мл. Из нее берут 1 мл и разводят водой в мерной
колбе до 100 мл. Полученный второй раствор будет содержать в ОД мл 0,001 мг
мышьяка. В 6 колб прибора Зангер-Блека последовательно вносят 0,1 (1-я колба),
0,3; 0,5; 0,7; 1 и 2,5 мл стандартного раствора мышьяка.
В коническую
колбу прибора Зангер-Блека вносят 2 мл минерализата или 5 г измельченного
продукта, 10 мл 20 %-ной серной кислоты, 5 мл дистиллированной воды, 1 мл 10
%-ного раствора хлорида олова (в серной или соляной кислоте) и около 2 г
купрированного мелкогранулированного цинка. Колбу закрывают хорошо
пришлифованной насадкой, в которую помещают комочек ваты, смоченной 5 %-ным
раствором уксуснокислого свинца и высушенной на воздухе (для поглощения сероводорода).
Выше размещают бромо- или хлорортутную бумагу. Колбу с насадкой оставляют на
час, после чего реактивную бумагу снимают и осматривают. При наличии в пробе
мышьяка бумага окрашивается в желтый или коричневый цвет.
Для количественного определения мышьяка в исследуемом материале в такой
же последовательности проводят работу с колбами, в которых вместо минерализата
находится разное количество стандартного раствора. Из полученных окрашенных
реактивных бумажек составляют стандартную шкалу, в которой возрастающей
интенсивности окраски соответствует увеличивающееся (точно известное)
количество мышьяка, выделившееся из стандартного раствора. Приготовленная
стандартная шкала в темном месте может храниться 5-6 мес. и ею можно
пользоваться многократно. Полученную после исследования продуктов убоя животных
окрашенную хлоро- или бромортутную бумажку сравнивают со стандартной шкалой,
устанавливают количество связанного ею мышьяка, а затем проводят перерасчет на
100 г продукта в естественном состоянии.
Качественное и количественное определение ртути (по А. Н. Крыловой в
модификации МТИММП). Метод основан на деструкции исследуемого материала,
осаждении ртути йодидом меди (для уменьшения ее потерь), образовании
окрашенного соединения - тетрайодидомеркурата меди с последующим
колориметрическим исследованием.
Оборудование и реактивы. Мясо животных, отравленных препаратом ртути или
в которое он специально введен; водяная баня; ножницы, пинцет, фарфоровая
чашка; колбы термостойкие на 750 мл; воронки стеклянные диаметром 3-5 см;
пипетки на 1, 5, 10 мл; колориметрические пробирки с притертыми пробками на
10-15мл; бюретка на 50 мл; фильтры бумажные, универсальная индикаторная бумага;
ацетон; этиловый спирт 96°-ный; кислота азотная и серная концентрированные;
натрий сернокислый 1 %-ный раствор; натрий сернистокислый - 2,5 н. раствора
(свежеприготовленный); йод, предварительно очищенный возгонкой, 0,25 и 0,35
%-ные растворы в 3 %-ном растворе йодистого калия.
Взвесь йодида меди; 212 г йодистого калия растворяют в 1-2 л
дистиллированной воды, смешивают с раствором сернокислой меди (160 г в 1 л
дистиллированной воды) и оставляют на 30 мин. Надосадочную жидкость сливают;
осадок многократно промывают дистиллированной водой (по 2-3 л до светло-желтого
цвета промывных вод). К жидкости с осадком добавляют 2,5н. раствора
сернистокислого натрия до обесцвечивания надосадочной жидкости и осадка, а
затем насыщенный раствор сернокислого натрия до коагуляции осадка (10-15 мл).
Надосадочную жидкость сливают. Осадок переносят на фильтр, вложенный в большую
воронку (15-16 см), промывают дистиллированной водой до почти отрицательной
реакции на сульфат-ион с 20%-ным раствором хлористого бария, Фильтр прокалывают
и взвесь смывают в мерный цилиндр, добавляют воды до 1 л и хранят в темной
склянке (до месяца).
Составной раствор готовится перед употреблением смешиванием 10 %-ного
раствора сернокислой меди с 2,5 н. раствором сернистокислого натрия (1:5).
Смесь перемешивают до растворения образовавшегося осадка и почти полного
обесцвечивания. Добавляют 1,5 объема (от объема раствора сульфата меди) 8%-ного
раствора бикарбоната натрия.
Стандартный раствор ртути: 0,0135 г перекристаллизованного хлорида ртути
или 0,0226 г йодида ртути растворяют в 100 мл 0,25 %-ного раствора йода (0,1 мг
ртути в 1 мл); рабочий раствор готовят разведением его в 100 раз 0,25 %-ным
раствором йода (1 мкг ртути в 1 мл), хранят до 15 дн.
В коническую колбу емкостью 750 мл последовательно помещают 40 г
измельченного мяса, 1 мл 96°-ного этилового спирта, 15 мл дистиллированной воды
и 15 мл концентрированной азотной кислоты, перемешивают и оставляют на 10 мин
при комнатной температуре. Колбу закрывают воронкой (диаметром 3-5 см) и по
каплям добавляют 25 мл концентрированной серной кислоты с такой скоростью,
чтобы постоянно поддерживалась реакция разложения азотной кислоты, но не
выделялись окислы азота из колбы.
Колбу оставляют в вытяжном шкафу на 15 мин при комнатной температуре до
прекращения выделения бурых паров окислов азота, после чего ее нагревают 45-60
мин на кипящей бане. При бурном течении реакции (выделение окислов азота или
сильное пенообразование), в колбу приливают 30-50 мл кипящей дистиллированной
воды или снимают ее на 1-2 мин с водяной бани.
Деструкцию проводят до полного просветления придонного слоя жидкости в
колбе. Горячий деструктат фильтруют в колбу, содержащую 10 мл 2,5 н.
сернистокислого натрия, через увлажненный двойной бумажный фильтр. Колбу и
фильтр несколько раз промывают кипящей дистиллированной водой. Общий объем
деструктата и промывных вод 250-300 мл. В колбу с охлажденным деструктатом
добавляют 10 мл взвеси йодида меди.
Если содержимое колбы окрашивается в бурый цвет вследствие выделения
йода, добавляют 5-10 мл 2,5 н. раствора сернистокислого натрия. Содержимое
колбы тщательно перемешивают и оставляют до полного осаждения осадка.
Максимально возможную часть жидкости сливают, а остальную - фильтруют через
бумажный фильтр. На него же полностью переносят осадок из колбы и промывают
сначала смесью ацетона с 1 %-ным сернокислым натрием (1:1) - около 50 мл, затем
1 %-ным сернокислым натрием до исчезновения желтой окраски промывных вод и до
рН не менее 3 (по универсальной индикаторной бумаге). Осадок подсушивают на
воздухе 15 мин. Затем его обрабатывают на фильтре 0,35 %-ным раствором йода в
количестве, зависящем от цвета осадка (белый - 10 мл, с розоватым оттенком -
15, бледно-розовый - 25 мл). Полученный фильтрат доводят до выбранного объема.
Его можно хранить в пробирках с притертыми пробками в темном месте в течение
суток.
Количественное определение ртути проводят визуально сравнением со
стандартной шкалой. Соответствующую часть раствора анализируемой пробы (1-6 мл)
помещают в пробирку, доводят до 6 мл 0,25 %-ного с раствором йода, прибавляют
из бюретки 3 мл составного раствора и тщательно перемешивают. Одновременно
готовят стандартную шкалу. Для этого в пробирки, отобранные для
колориметрирования, вносят точное количество рабочего раствора ртути (1мкг/мл),
указанное в таблице 1, доводят до 6 мл 0,25 %-ного с раствором йода, добавляют
составной раствор (3 мл) и тщательно перемешивают.
Таблица 2.
Схема подготовки стандартной шкалы
|
Количество рабочего
раствора ртути, мл
|
Количество раствора
0,25%-ного йода, мл
|
Содержание ртути, мкг
|
Количество рабочего
раствора ртути, мл
|
Количество раствора
0,25%-ного йода, мл
|
Содержание ртути, мкг
|
|
0
|
0
|
1,25
|
4,75
|
1,25
|
|
0,25
|
5,75
|
0,25
|
1,50
|
4,50
|
1,50
|
|
0,50
|
5,50
|
0,50
|
1,75
|
4,25
|
1,75
|
|
■ 0,75
|
5,25
|
0,75
|
2,00
|
4,00
|
2,00
|
|
1,00
|
5,00
|
1,00
|
5,00
|
1,00
|
5,00
|
Визуальное сравнение окраски осадка пробы со стандартной шкалой проводят
через 15 мин после добавления составного раствора. Количество ртути в
исследуемом мясе (X, мг/кг) определяют по формуле:
X= aY1*1000/Y2M*1000,
где a - количество ртути, установленное по
стандартной шкале; Y1 - количество
раствора йода, использованного для обработки осадка на фильтре, мл;Y2 - количество анализируемого
раствора, взятого для колориметрирования, мл; М - масса навески образца, г (по
описанной выше методике); 1000 - коэффициенты для пересчета количества ртути в
мг/кг.
Ветеринарно-санитарная оценка
Туши и внутренние органы животных, подвергшихся отравлению и вынужденно
убитых в состоянии агонии, использовать на пищевые цели запрещается. Их
утилизируют или с учетом степени отравления используют для кормления животных,
но только после бактериологического исследования и постановки биопробы на
небольшой группе животных.
При удовлетворительных органолептических показателях и результатах
физико-химического и бактериологического исследования санитарная оценка мяса
зависит от свойств и вида токсических веществ, вызвавших отравление. Их делят
на три группы:
К первой относят токсические вещества, содержание которых в мясе и
субпродуктах недопустимо. Необходимо учитывать естественный уровень токсических
веществ в организме, например ртути в печени не более 0,03мг/кг, мышьяка в мясе
до 0,5мг/кг (ртуть).
Вторая группа ядохимикаты и вещества, для которых установлена максимально
допустимые уровни в мясе и мясных продуктах. В случае обнаружения в мышечной
ткани вынужденно убитых животных токсических веществ, являющихся причиной
отравления, в пределах допустимых остаточных количеств мясо выпускают только
после проварки, а все внутренние органы утилизируют. Свинец до 1мг/кг мясо
допускают в пищу при удалении всех лимфатических узлов и внутренних органов,
срок употребления до 5 дней. Бария до 30 мг/кг. Сурьмы до 40 мг/кг.
Третью группу составляют вещества, при отравлении которыми мясо выпускают
для пищевых целей, но реализуют как условно годное после обеззараживания
проваркой или направляют на изготовление мясных хлебов (соли цинка и меди).
Внутренние органы, мозг, вымя, ткани, куда проник яд - во всех случаях
бракуют.
Гигиенические нормативы качества и безопасности продовольственного сырья
и пищевых продуктов. СанПиН2.3.2,560-96
Допустимые значения содержания в мясе всех видов убойных, промысловых и
диких животных.
Токсических элементов (мг/кг не более):
свинец 0,5
мышьяк 0,1
кадмий 0,05
ртуть 0,03
медь 5,0
цинк 70,
Список используемой литературы
1.
Ветеринарно-санитарная экспертиза с основами технологии переработки продуктов
животноводства (Х.С.Горегляд, В.А.Макаров, И.Е.Чеботарев и др., под редакцией
Х.С.Горегляда, 2-ое издание, переработанное и дополненное, М., Колос, 1981 г.).
.
Ветеринарно-санитарный осмотр продуктов убоя животных. Ветеринарные
методические указания. (ВМУ). М., 2000г.
.Правила
ветеринарного осмотра убойных животных и ветеринарно-санитарной экспертизы мяса
и мясных продуктов (под редакцией И.А.Рыбина) М., ВО Агропромиздат, 1988г.
.Производственно-ветеринарный
контроль в мясной промышленности (Д.М.Тетерник; Ф.П.Лаптев, М.Б.Коган.) М.,
Пищепромиздат 1986 г.
. Практикум
по ветеринарно-санитарной экспертизе с основами технологии продуктов
животноводства; под ред. Макарова В.А., М., «Агропромиздат» 1987г., 271с.