Взаимодействие 3-арил(гетарил)гидразоно–3Н-фуран-2-онов с бензиламином
Курсовая
работа
Взаимодействие
3-арил(гетарил)гидразоно-3Н-фуран-2-онов с бензиламином
Содержание
Введение
.
Литературный обзор
. Цель
исследования и обсуждение результатов
.
Экспериментальная часть
3.1
Используемые реактивы
3.2 Основные физико-химические
методы анализа, используемые в работе
.3 Методики
синтезов
.4 Получение
4-оксо-4-арилбутановых кислот
.5 Получение
5-арил-3Н-фуран-2-онов
.6 Получение
солей диазония
.7 Реакции
азосочетания
.8 Реакции с
бензиламином
. Техника
безопасности
Выводы
Список
используемой литературы
Введение
-Гидразонозамещенные 3Н-фуран-2-оны являются важными строительными
блоками в органическом синтезе. На их основе могут быть получены разнообразные
открыто цепные, карбо- и гетероциклические соединения, которые находят широкое
практическое применение в медицине, промышленности. Наличие в молекулах
3-гидразоно-3Н-фуран-2-онов нескольких электроно-дефицитных атомов приводит к
возможности образования разнообразных ациклических и гетероциклических
соединений. Возможность варьирования заместителей в гидразоной функции и в
гетероцикле еще более увеличивают их препаративную ценность. В этой связи,
работа в области синтеза , изучения химических свойств, и получения на их
основе биологически активных веществ является актуальной. /1/
1. Литературный обзор
Арил(гетарил)-гидразоно-1,3-дикарбонильные соединения содержат два
электрофильных центра, по которым происходит атака нуклеофильных реагентов с
образованием региоизомерных продуктов.
Была описана конденсации 2-гидразонозамещенного ацетоуксусного эфира с
аминами на матрице ионов меди и никеля, приводящим к тетраазахелатным
комплексам.
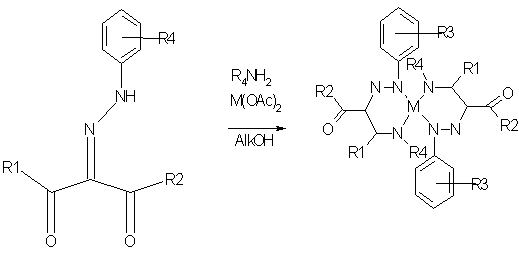
R1 =Me,OEt; R2=Me,Ph;R3=H, 3-Me, 4-Me, 3-OMe,
4-OMe,3-NO2,4-NO2;3-Cl,4-Cl; R4=Me,Et,Prn,Bun,Ar;
M=Cu,Ni
Реакции
фторалкилсодержащих 2-арилгидразонов 1,2,3-трионов с метиламином происходят
неоднозначно в зависимости от их строения. Арилгдразоны, имеющие фторалкилный
заместитель меньше 2 - «короткий», реагируют по карбонильной группе при
нефторированном атоме, давая 2-ариларилазо-3-аминеноны. Превращения
алкилгидразонов, содержащие «длинный» фторалкильный и объемный углеводородный
заместители неселективны. В этом случае по мимо 2-ариларилазо-3-аминенонов
образуются N-мети-2-арилгидразоно-3-оксобутанамиды, которые
образуются в результате присоединения амина по карбонильной группе при
фторированном заместителе с последующим галофобным расщеплением интермедиатов
путем эллиминирования фторалкана. Продуктами реакций арилгидразонов, содержащих
полифторалкильный (n>3) и объемные трет-бутильный или фенильный
заместитель (R2=But,Ph), являются только амиды.
R1 = (CF2)nX (X=F: n=1, 3, 4;
X=H: n=2,3);R2= Me, Ph, Bun, But; R3=H,Me,OMe
Было
показано, что 2-арилгидразоны 1,2,3-трионов, имеющий короткий фторалкильный
заместитель, реагируют с метиаламином при нагревании в этаноле с образованием
продуктов моноконденсации - 2-арилдеазинил-1,3-енаминокетонов. Синтез
проводиться с избытком метиамина в течении 20 мин. Контроль над ходом реакции
осуществляется методом ТСХ до полной конверсии арилгидразона. Использование в
качестве растворителя хлороформа не привело к образованию каких-либо продуктов
реакции. Региоизомерное строение соединений было установлено на основе спектров
ЯМР. Так, присутствие в спектрах ЯМР 13С продуктов реакции,
измеренных в СDCl3,
слабопольного мультиплетного сигнала в области 176-180 м.д., соответствующего
атому углерода полифторацильной группе, свидетельствующей о том, что амины
являются результатом конденсации по карбонильной группе при нефторированнои
заместителе /2/.
В
темплатной конденсации 2-арилгидразонов 1,2,3-трионов с метиламином на матрице
ионов Ni(II) образуются металлокомплексы. Преимуществом
темплатного метода является возможность получения металлохелатов с лигандами,
имеющих длинный полифторалкильный и объемный углеводородный заместители.
Альтернативным методом получения хелатов является обработка
2-арилазо-3-метиламино-1-(полифторалкил)енонов с солями металлов.
реакция
ацетоуксусный эфир растворитель
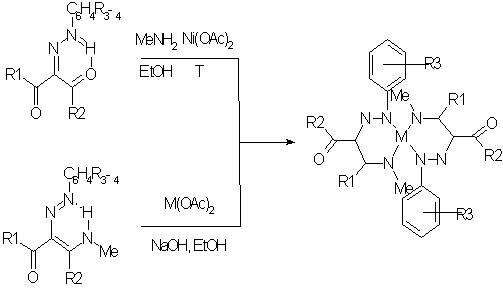
R1= CF3, (CF2)2H, C3F7;R2=Me,Ph;
R3=H,Me,OMe; M=Ni,Cu
Основным
процессом при взаимодействии 2-арилгидразоно-3-оксоэфиров с метиламином
является конденсация амина по сложноэфирной группе с образованием амидов.
Однако для эфиров, имеющих нанофторбутильный и тридекафторгексильный
заместители, это направление не является единственным, поскольку реакция
сопровождается присоединением амина по фторацильному фрагменту с последующим
галоформным расщеплением и образованием диамида/3/.
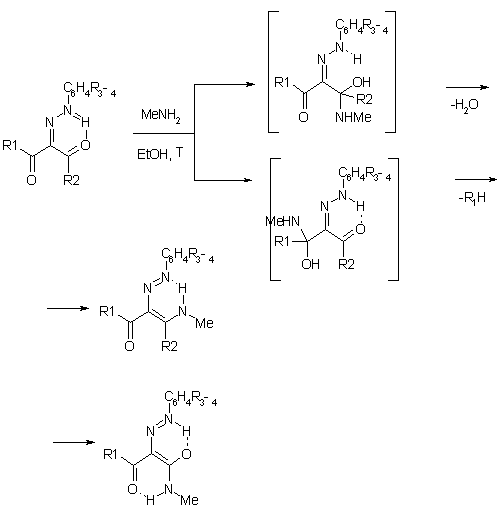
Было
показано, что арилгидразоны, содержащие два неэквивалентных электрофильных
центра, способны присоединять метиламин по обоим карбонильным атомам, с
промежуточным образованием полуамиалей А и Б. Очевидно, что стабилизация
интермидиата А происходит быстро за счет элиминирования молекулы воды с
образованием амина. Для интермидиата Б с “длинными” полифторалкильными
заместителями появляется возможность к стабилизации за счет отщепления
фторалканы с образованием амидов. Предпочтительное образование амидов в
реакциях арилгидразонов может быть объяснено стерическими препятствиями,
создаваемыми объемным фенильным или тре-бутильными заместителями к атаке
нуклеофилом соседнего карбонильного атома углерода/2/
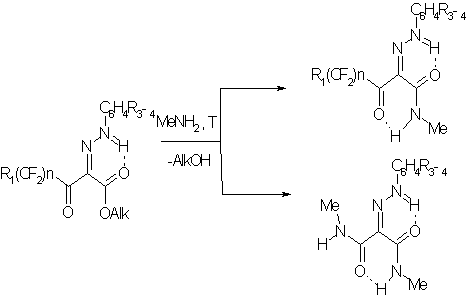
R1=H:n=1,2,4; R1=F,n=3,4,6; R2=H,Me,OMe
Амиды проявляют комплексообразующие свойства по отношению к катионам
переходных металлов, и из них могут быть получены металлокомплексы. Возможен
синтез этих хелатов с темплатной конденсацией эфиров с метиламином на матрице
ионов никеля(II). Темпларный метод применяют для
синтеза амидов с длинными полифторированными алкильными заместителями./3/

R1 =H: n=1,2;R1=F:n=3,4;R2=H,Me;OMe;M=Ni,Cu
Так
как фторалкилсодержащие 2-аригидразоны 1,2,3-трионов являются перспективными
строительными блоками для создания гетероциклических молекул различных классов,
для планирования синтеза на осонове этих веществ важным представляются вопросы
их строения.
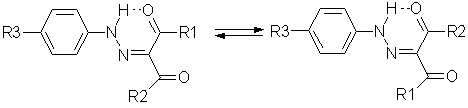 1=R2=CH3
1=R2=CH3
Было
обнаружено, что 3-Арилгидразоны пентан-2,3,4-триона и полифторалкилсодержащие
2-арилгидразоны 1,2,3-трионовсуществуют как в кристаллах, та и в растворах СDCl3 и (CD3)2CO в
виде арилгидразонов. Проанализировав спектры ЯМР трифторацетил содержащих
2-арилгидразонов 1,2,3-трионов были обнаружены общие закономерности.
Три-
и тетрафторзамещенные 2-арилгидразоны 1,2,3-трионов , содержащих объемную
бензоильную группировку, имеют в спектрах ЯМР в растворе (CD2)3CO два набора сигналов, а в
растворе CDCl3 один
набор сигналов. Сравнение химических сдвигов карбонильных ядер углерода
бензоильного и тетрафторацильного заместителей двух присутствующих в растворе (CD3)2 изомеров соединения позволяет говорить о
приобладании изомера А со свободным полифторацильным фрагментом.
Согласно
данным рентгеноструктурного анализа, в почти плоской молекуле реализуется
эффективная ВВС между протоном арилгидразонного заместителя и атомом кислорода
карбонильной группы пентаноильного фрагмента. Так, внутримолекулярное
расстояние О5…Н1 составляет 1.85Å, углы N1-H1…O5
и С5-О5…Н1
равны 134(1) и 104(1). Эти параметры однозначно свидетельствую о наличии ВВС.
Установлено,
что существование трифторметилзамещенных 2-арилгидразонов 1,2,3-трионов в виде изомера
А можно объяснить влиянием электронного фактора. По-видимому, этот же фактор
является основным и для других полифторалкилзамещенных 2-арилгидразонов
1,2,3-трионов/4/
Показано,
что 1,5- диметил-4-(2-оксо-5-фенилфуран-3-илиден-амино)-2-фенил-1,2-дигидропиразол-3-он
при взаимодействии с метил-,этил-,фенилгидразинами или с 1,2-дифенилгидразином
в инертном растворителе рециклизуется с образованием
4-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-илимино)-6-фенил-1,4-дигидро-2Н-пиридазин-3-онов/5/
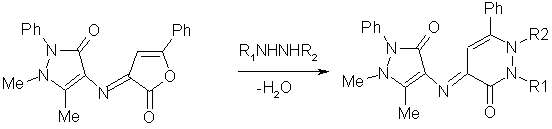
R1=H,Ph;R2=Me,Et,Ph
Образование
соединений происходит, вероятно, вследствие раскрытия фуранового цикла после
атаки аминогруппы гидразина на атом С(2) фуранона. Образующийся интермедиат
циклизуется в результате атаки вторичной аминогруппы -NНR2
на атом С(5) с одновременны
отщеплением воды/6/
Ненасыщенные
пятичленные гетероциклы/7/ занимают особое место в органической химии в связи с
их обнаружением в виде фрагментов природных соединений, а также получением на
их основе веществ с различной биологической активностью./8/
2. Цель исследования и обсуждение результатов
Целью данной работы является разработка условий и изучение взаимодействия
3-арил(гетарил)гидразоно-3Н-фуран-2-онов с бензиламином.
Нами в качестве исходных соединений для синтеза 5-Аr-3Н-фуран-2-онов использовались
4-(фенил)- и 4-(толил)-4-оксобутановые кислоты 1а-b, полученные ацилированием ароматических колец бензола и
толуола янтарным ангидридом в присутствии хлорида алюминия/10/.
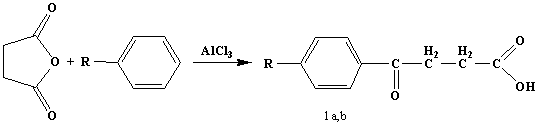
1a,b R= H; CH3
Способность их к енолизации является необходимым условием для получения
3Н-фуран-2-онов. Реакцию проводили в этиловом спирте при нагревании.
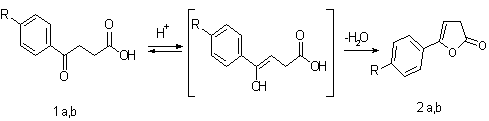
1,2a: R= H, b: R=CH3
Физико-химические характеристики полученных соединений соответствуют
литературным данным/10/.
Для изучения реакционной способности
3-арил(гетарил)гидразоно-3Н-фуран-2-онов была проведена реакция последних с
бензиламином. 5-Арил-3-арил(гетарил)гидразоно-3Н-фуран-2оны синтезировались на основе
реакций азосочетания солями арил(гетарил)диазония.

2a: R= C6H5, b: R=C6H4CH3
3a-c R=Tol, a Ar=o-O2NC6H4,
b Ar=м-O2NC6H4,
c Ar=п-O2NC6H4;
d-h R=Ph, , d Ar=o-O2NC6H4,
e Ar=м-O2NC6H4,
f Ar=п-O2NC6H4,
h C7H6N2
Ряд соединений 3 a-h получены с выходом до 93%,
физико-химические характеристики соответствуют литературным данным /9/. Из
ранее проведенных работ известно, что соединения 3 a-h существуют в
форме гидразона.
Для изучения реакционной способности 3-арил(гетарил)гидразоно-3Н-фуран-2-онов
были проведены квантово-механические расчеты в программе HyperChem методом MNDO.

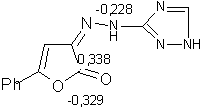
Показано,
что наиболее электрофильным центром является атом С лактонной группы
Проведение реакции в спирте, при соотношении реагентов 1:1, приводит к
продуктам 4 a-h с выходом до 83%.
3a-c
R=Tol, a Ar=o-O2NC6H4, b Ar=м-O2NC6H4,
c Ar=п-O2NC6H4;
d-h R=Ph, , d Ar=o-O2NC6H4,
e Ar=м-O2NC6H4,
f Ar=п-O2NC6H4,
h C7H6N2
4a-c R=Tol, a Ar=o-O2NC6H4,
b Ar=м-O2NC6H4,
c Ar=п-O2NC6H4;
d-h R=Ph, , d Ar=o-O2NC6H4,
e Ar=м-O2NC6H4,
f Ar=п-O2NC6H4,
h C7H6N2
На основании данных физико-химических исследований установлено, что
продуктами взаимодействия являются N-бензил-5-арил-3- арил(гетарил)гидразоно-3Н-пиррол-2-оны( 4a-h).
В ИК-спектрах отмечены полосы поглощения:
· С=О групп амидного фрагмента в области 1662-1651 см-1,
· полосы поглощения С=N групп при 1662-1641 см-1.
В ИК-спектрах не наблюдаются полосы поглощения группы “амид II”.
В ЯМР1Н-спектрах соединений N-бензил-5-арил-3- арил(гетарил)гидразоно-3Н-пиррол-2-оны( 4a-h) отмечена
· серия мультиплетов ароматических протонов в области 7,512
м.д.
· синглет протона при азота при 9,59 м.д., 8,57 м.д.
· синглет протона метиленовой группы при 2,26-2,31 м.д.
· синглет протона при sp2-гибридизованом
атоме С пирро-2онового цикла 6,085 м.д.
Наличие сигналов протонов метиленового звена при 2,26-2,31 м.д. позволяет
подтвердить структуру 4a-h
Учитывая многоцентровость изучаемых соединений можно было ожидать
образование различных продуктов, с участием различных реакционных центров, нами
предложена следующая схема взаимодействия.

Нуклеофильный
реагент - бензиламин - раскрывает цикл с образованием амида А, который способен
гетероциклизоваться по нескольким направлениям: с образованием продуктов
гетероциклизации с участием атома азота гидразонного фрагмента, что приводит к
замещенным пиразолам (путь a). Учитывая, что амиды незамещенных оксокислот
способны гетероциклизоваться с использованием амидного атома азота, нами
предложена схема гетероциклизации с использованием этого реакционного центра
(Путь b). Реализация этого направления и приводит к
образованию 3-арил(гетарил)гидразоно-3Н-пиррол-2-онов.
Спектральные
характеристики и квантово-химические расчеты полностью подтверждают образование
производных N-бензил-5-арил-3-
арил(гетарил)гидразоно-3Н-пиррол-2-онов.
Таким
образом, были проведено взаимодействие 3-арил(гетарил)гидразоно-3Н-фуран-2-онов
с бензиламином. Впервые получены N-гетероаналоги гидразонозамещенных 3-фуран-2-онов и
охарактеризованы с привлечением данных физико-химических исследований
представляют интерес в качестве потенциальных биологически активных веществ.
3. Экспериментальная часть
3.1 Используемые реактивы
|
реактивы
|
марка
|
ГОСТ
|
|
ацетон
|
ч
|
ГОСТ 2603-71
|
|
кислота соляная
|
хч
|
ГОСТ 3181-67
|
|
нитрит натрия
|
чда
|
ГОСТ 4197-77
|
|
спирт этиловый
|
ч
|
ТУ 19П-36-69
|
|
уксусная кислота
|
ч
|
ГОСТ 4523-65
|
|
уксусный ангидрид
|
ч
|
ГОСТ 58-15-69
|
|
хлористый алюминий
|
осч
|
ТУ 6-09-2267-72
|
|
бензол
|
чда
|
ГОСТ 5139-63
|
|
толуол
|
чда
|
ГОСТ 5789-69
|
|
янтарный ангидрид
|
ч
|
ТУ 6-09-3611-74
|
|
спирт изопропиловый
|
ч
|
ТУ 16П-8-71
|
|
серная кислота
|
хч
|
ГОСТ 3181-32
|
|
м-фенилендиамин
|
чда
|
ГОСТ 5826-78
|
|
п-фенилендиамин
|
ч
|
ТУ 6-09-995-76
|
|
реактивы
|
марка
|
ГОСТ
|
хч
|
ТУ-6-09-3375-73
|
|
Диизопропиловый эфир
|
хч
|
ТУ-6-09-234-65
|
.2 Основные физико-химические методы анализа, используемые в
работе
Контроль за ходом реакции, качественный анализ состава реакционных
смесей, идентификация выделяемых соединений осуществлялись при помощи методов
тонкослойной хроматографии, элементного анализа, ИК-спектроскопии.
. Анализ методом ТСХ проводился на пластинках Silufol-UV
254; элюент - гексан : ацетилацетат : хлороформ (2:2:1), проявитель - пары
йода.
. ИК-спектры снимали на ИК фурье-спектрометре ФСМ 1201 в таблетках KBr.
. Спектр ЯМР 1Н записан на приборе
Bruker MSL-400, рабочая
частота - 400 МГц, внутренний стандарт - ТМС, растворитель - дейтерохлороформ;
3.3 Методики синтезов. Получение 4-оксо-4-арилбутановых
кислот. Фенил-4-оксобутановая кислота (1а)
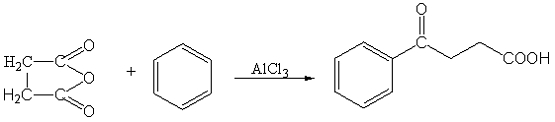
а
В литровую трехгорлую колбу с мешалкой и обратным холодильником помещают
34 г (0.34 моль) ангидрида янтарной кислоты и 175 г (2,25 моль, 250 мл)
бензола. При перемешивании в колбу прибавляют 100 г (0,75 моль) безводного
хлорида алюминия. Если колба нагревается, то охлаждают водяной баней
(реакционная смесь желтого цвета). Происходит выделение паров HCl. По окончании прибавления хлорида
алюминия смесь нагревают в течении 1часа (реакционная смесь коричневого цвета).
К охлажденному раствору (перемешивание продолжается) прикапывают 150 мл
холодной воды, происходит разогрев, выделяются пары HCl (реакционная смесь твердеет и темнеет). В охлажденную
колбу прикапывают 50 мл концентрированную соляную кислоту (реакционная смесь
светлеет, перемешивается легче). Конечный продукт выделяется в виде масла,
загрязненного примесями. Затвердевает при охлаждении.
Стадии очистки:
1. Твердый продукт переносят из колбы в термостойкие стаканы (объемом
250-500 мл). Остатки вымывают холодной смесью 25 мл концентрированной соляной
кислоты и 75 мл воды, затем еще 100 мл воды.
. Смесь кипятят. Кипящий раствор пропускают через бумажный фильтр,
не допуская охлаждения.
. Фильтрат оставляют в колбе на сутки. Выпавшие после охлаждения
кристаллы (белые хлопья) отфильтровывают на воронке Бюхнера.
Белые кристаллы. Выход 37,3г (59%). Тпл=112-1130С.
Литературные данные /10/ Тпл= 112-114 оС.
(4-Метилфенил)-4-оксобутановая кислота (1б)
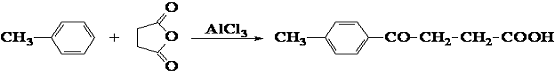
По методике, аналогичной вышеуказанной, исходя 25 г (0,25 моль) янтарного
ангидрида, 155 г (1,68 моль, 105 мл) толуола, 73 г (0,55 моль) безводного AlCl3.
Тпл = 123-124 0С, выход 42 г (60%).
Литературные данные /10 /: Тпл=122-123 0С
.4 Получение 5-арил-3Н-фуран-2-онов
Фенил-3Н-фуран-2-он (2a)
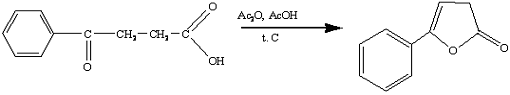
1а
2а
В круглодонную колбу объемом 50мл, снабженную обратным холодильником помещают
2г (0,0112 моль) 4-фенил-4-оксобутановой кислоты, затем добавляют 5мл (0,0896
моль) уксусной кислоты и 4,85мл (0,0336) уксусного ангидрида. Реакционную смесь
греют в течение 2 часов и оставляют на сутки. После этого реакционную смесь
нейтрализуют насыщенным раствором кальцинированной соды, выпадают кристаллы
оранжевого цвета.
Выход - 1.85г (85%) Т пл. 83-850С
Литературные данные /10/ Т пл.= 83-840С.
олил-3Н-фуран-2-он (2b)
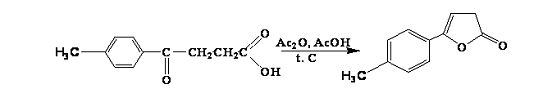
1б
2b
По методике, аналогичной вышеуказанной, получают 5-толил-3Н-фуран-2-он из
2г (0,01041моль) 4-толил-4-оксобутановой кислоты , 4.95мл (0,08328 моль)
уксусной кислоты и 4.75мл (0,03124 моль) уксусного ангидрида.
Выход =1,81г (83%)Тпл.= 88-900С /12/.
Литературные данные /10/Тпл.= 89-900С.
3.5 Получение солей диазония
О-нитроанилиндиазоний гидросульфат
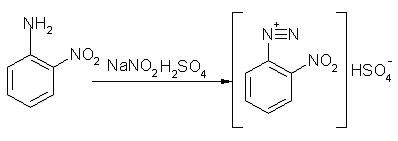
Стеклянный стаканчик объемом 100 мл помешают в баню с «сухим» льдом,
добавляют 0,2 г. (0,00185моль) о-нитроанилина и раствор серной кислоты(0,54мл Н2SO4 + 0,23мл Н2О) при постоянном перемешивании
до полного растворения. Затем к полученной смеси приливают раствор NaNO2 массой 0,38г и 2мл H2O,
перемешивают в течении 5 минут оставляют еще на 10 минут, после чего делают
пробу на йодкрахмальную бумажку (должна быть положительной) и нейтрализуют
кристаллическим ацетатом натрия до тех пор, пока индикаторная бумажка не
перестанет синеть. Далее соль, без дополнительного выделения использовалась в
качестве диазокомпоненты в реакциях азосочетания с фуран-2-онами.
М-нитроанилиндиазоний гидросульфат
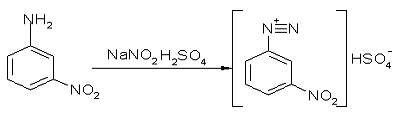
Методика получения аналогична методике указанной выше. Далее соль, без
дополнительного выделения использовалась в качестве диазокомпоненты в реакциях
азосочетания с фуран-2-онами.
П-нитроанилиндиазоний гидросульфат
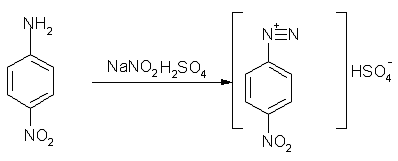
Методика получения аналогична методике указанной выше. Далее соль, без
дополнительного выделения использовалась в качестве диазокомпоненты в реакциях
азосочетания с фуран-2-онами.
Бензоимидазолдиазоний гидросульфат
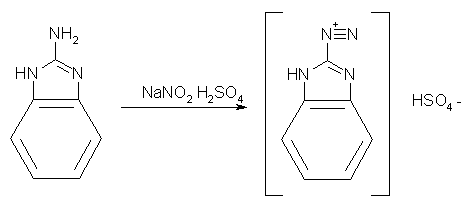
Методика
получения аналогична методике указанной выше. Далее соль, без дополнительного
выделения использовалась в качестве диазокомпоненты в реакциях азосочетания с
фуран-2-онами.
3.6 Азосочетание 5-Аr-3Н-фуран-2-онов с солями диазония
-(2-(2-нитрофенил)гидразоно)-5-толил-3Н-фуран-2-он (5b)
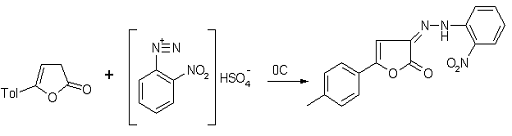
Методика получения
3-(2-(2-гидроксифенил)гидрозоно)-5-толил-3Н-фуран-2-она, аналогична методике
указанной выше.
Выход - 1.67г (92%) Т пл. 244-2460С
Литературные данные /9/ Т пл.= Тпл. 244-2460С
3-(2-(2-нитрофенил)гидразоно)-5-фенил-3Н-фуран-2-он (5e)
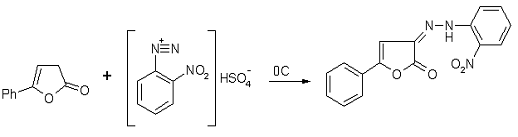
Методика получения 3-(2-(2-нитрофенил)гидрозоно)-5-фенил-3Н-фуран-2-она,
аналогична методике указанной выше.
Выход - 1.51г (81%) Т пл. 220-2220С
Литературные данные /9/ Т пл.= Тпл =220-2220С
3-(2-(3-нитрофенил)гидразоно)-5-толил-3Н-фуран-2-он (5c)
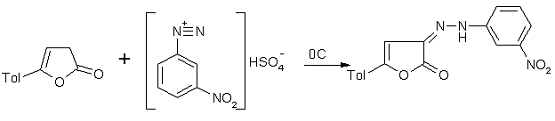
Методика получения 3-(2-(3-нитрофенил)гидрозоно)-5-толил-3Н-фуран-2-она,
аналогична методике указанной выше.
Выход - 1.63г (95%) Т пл. 244-2460С
Литературные данные /9/ Т пл.= Тпл. 244-2460С
-(2-(3-нитрофенил)гидразоно)-5-фенил-3Н-фуран-2-он (5f)
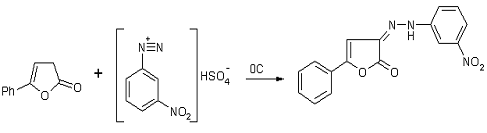
Методика получения
3-(2-(3-нитроксифенил)гидрозоно)-5-фенил-3Н-фуран-2-она, аналогична методике
указанной выше.
Литературные данные /9/ Т пл.= Тпл. 220-2220С
-(2-(4-нитрофенил)гидразоно)-5-толил-3Н-фуран-2-он (5d)

Методика получения 3-(2-(4-нитрофенил)гидрозоно)-5-толил-3Н-фуран-2-она,
аналогична методике указанной выше.
Выход - 1.61г (90%) Т пл. 244-2460С
Литературные данные /9/ Т пл.= Тпл. 244-2460С
-(2-(4-нитрофенил)гидразоно)-5-фенил-3Н-фуран-2-он (5h)
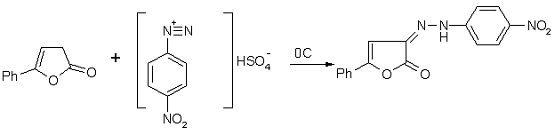
Методика получения
3-(2-(4-нитроксифенил)гидрозоно)-5-фенил-3Н-фуран-2-она, аналогична методике
указанной выше.
Выход - 1.57г (85%) Т пл. 220-2220С
Литературные данные /9/ Т пл.= Тпл. 220-2220С
3-((бензоимидазол)гидразоно)-5-фенил-3Н-фуран-2-он
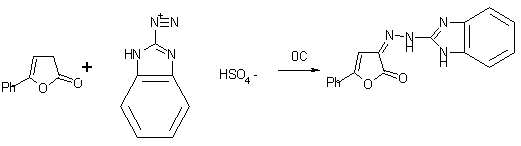
Методика
получения 3-((бензоимидазол)гидразоно)-5-фенил-3Н-фуран-2-он, аналогична
методике указанной выше.
Выход - 1.60 г (87%) Т пл. 210-2120С
Литературные данные /9/ Т пл.= Тпл. 210-2120С
3.7 Реакции с бензиламином
N-бенил-3-(2-(4-нитрофенил)гидразоно)-5-толил-3Н-пиррол -2-он
(5b)
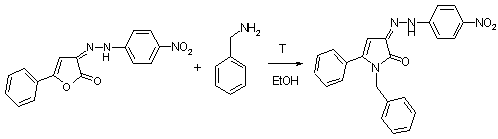
В круглодонную колбу, объемом 50 мл,снабженную обратным холодильником
помещают 0.3 г (0,0025 моль) и 1 мл (0,0091 моль) бензиламина. Растворитель - этиловый
спирт. Смесь нагревают в течении 10 часов. Затем реакционную смесь подкисляют
соляной кислотой до pH=7. Затем
реакционную смесь переносят в стакан с водой. Получены кристаллы
светло-коричневого цвета.
Выход 83%, Тпл 100-1010С
Найдено, % С =69,45 , N
=14,01 , H = 4,61
Вычислено, % С =69,89 , N
=13,58 , H =4,89 , C24H20N4O3
ИК -спектр, ν, см-1: 1682 (C=O), 3064 (NH), 1648 (C=N)
ЯМР1Н - спектр, м.д. ( c, H, -CH- )=4.5, (c, H, -NH)=6,137, (c, 2H, CH2)=3,35,
N-бензил-3-(2-(4-нитрофенил)гидразоно)-5-фенил-3Н-пиррол-2-он

Методика получения N-бензил-3-(2-(4-нитрофенил)гидразоно)-5-фенил-3Н-пиррол-2-он,
аналогична указанной выше
Выход 85% Тпл=120-121
Найдено, % , N = 13,23
Вычислено, % С =69,89 , N
=13,58 , H =4,89 , C24H20N4O3
ИК -спектр, ν, см-1: 1681 (C=O), 3065 (NH), 1645 (C=N)
ЯМР1Н - спектр, м.д. ( c, H, =CH- )=4.51, (c, H, -NH)=6,129, (c 2H, -CH2-)=3,36, (3H, -CH3)=2,63
N-бензил-3-(2-(3-нитрофенил)гидразоно)-5-толил-3Н-пиррол-2-он

Методика
получения N-бензил-3-(2-(3-нитрофенил)гидразоно)-5-толил
-3Н-пиррол-2-он, аналогична указанной выше
Выход
80% Тпл=119-120
Найдено,
% N = 13,78
Вычислено,
% С =69,89 , N =13,58 , H =4,89 , C24H20N4O3
ИК
-спектр, ν,
см-1: 1670 (C=O),
1574 (C=N),3062 (-NH-)
ЯМР1Н
- спектр, м.д. (c, 3H, -CH3)=1,99; (c, 2H, -CH2-)=4,658; (c, H, =CH-)=6,085
N-бензил-3-(2-(3-нитрофенил)гидразоно)-5-фенил-3Н-пиррол-2-он
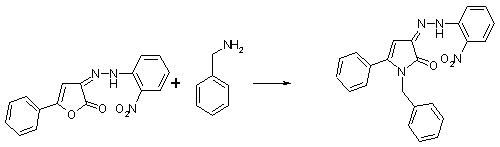
Методика
получения N-бензил-3-(2-(3-нитрофенил)гидразоно)-5-фенил-3Н-пиррол-2-он,
аналогична указанной выше
Выход
87%, Тпл=99-1000с
Найдено,
% С =70,01 , N =13,22 , H =5,12
Вычислено,
% С =69,89 , N =13,58 , H =4,89 , C24H20N4O3
ИК
-спектр, ν,
см-1: 1653 (C=O);1527
(C=N); 3063 (-NH)
ЯМР1Н
- спектр, м.д. (c, 2H, -CH2-)=4,658;
(c, H, =CH-)=6,085
N-бензил-3-(2-бензоимидазол)гидразоно)-5-фенил-3Н-пиррол-2-он

Методика
получения N-бензил-3-(2-фенил)гидразоно)-5-фенил-3Н-пиррол-2-он,
аналогична указанной выше
Выход
75%, Тпл=98-990
Найдено,
%, N = 17,34
Вычислено,
% С =73,27 , N =17,80 , H =4,87 , C24H19N5O
ИК
-спектр, ν,
см-1: 1653 (C=O),3061
(NH) 1644 (C=N)
ЯМР1Н
- спектр,(δ м.д.) (c,
H, =CH-)=1,225,(c, H - NH-)=7,950,(c, 2H, -CH2-)=2,605
4. Техника безопасности
1. Работа с легколетучими растворителями.
При работе с легколетучими растворителями всегда нужно иметь
под рукой листовой асбест, песок и другие средства тушения. На рабочем столе и
соседних столах не должно быть открытого пламени. Особую осторожность следует
соблюдать при работе с эфиром. При отгонке эфира водяную баню следует наливать
водой, нагреваемую в стороне от места работы с эфиром. К приемнику присоединяют
резиновую трубку, конец которой опущен под рабочий стол.
При возникновении пожара надо немедленно удалить легковоспламеняющиеся
вещества и тушить пламя, накрывая его влажным одеялом или засыпая песком.
На рабочем месте нужно иметь количество растворителя, не превышающего
суточную потребность. Большее количество хранить в сейфе или специально
отведенных местах.
2. Работа с кислотами и щелочами
Крепкие кислоты, щелочи и крепкие их растворы при попадании на тело могут
вызывать сильные ожоги. Поэтому при работе с ними следует соблюдать следующие
меры предосторожности:
а) работать в очках и резиновых перчатках;
б) обеспечить удобное хранение кислот и щелочей;
в) приливать кислоту в воду, а не наоборот;
г) при переливании из склянки в склянку пользоваться воронкой.
При ожогах кислотой обожженное место промыть большими порциями воды и
обработать 2% растворам бикарбоната натрия.
3 Работа с электроприборами
Работа с электрическими и электронагревательными приборами требует особо
внимательного и точного соблюдения правил по технике безопасности. Это связано
с тем, что при особых условиях (большая влажность, отсутствии исправной
изоляции), поражение может быть нанесено током 36В, или 12В.
Первым и необходимым условием безопасности является устройство защитного
заземления. Работать разрешается только при исправном оборудовании.
1. Проверять на ощупь наличие напряжения
и нагрев токоведущих частей прибора.
2. Применять для соединения блоков и
приборов провода с поврежденной изоляцией.
3. Снимать кожух прибора, включенного в
сеть 220В.
При поражении электрическим током человека, необходимо отключить
установку с помощью выключателя, освободить пострадавшего от действия электрического
тока, оказать ему первую помощь.
Выводы
. Расширен ряд 3-арил(гетарил)гидразоно-3Н-фуран-2-онов на основе
реакции азосочетания солей арилдиазония с 5-арил-3Н-фуран-2-онами
. Впервые разработаны условия и проведено взаимодействие
3-арил(гетарил)гидразоно-3Н-фуран-2-онов с бензиламином.
. Показано, что атака первичного амина направлена на атом углерода
карбонильной группы субстрата, дальнейшая гетероциклизация осуществляется с
участием атома амидного фрагмента
Список используемой литературы
1. Рубцов
А.Е. Синтез и химические превращения N - замещенных 3-имино-3Н-фуран-2-онов//автореферат.-2007, Пермь
. Щегольков
Е.В., Слепухин П.А., Кажева О.Н., Шилов Г.В., Дьяченко О.А, Салоутин В.И.
Конденсация фторалкилсодержащих 2-арилгидразонов 1,2,3-трионов с
метиламином//Журнал органической химии 2007. Т.43.Вып.12.
. Щегольков
Е.В. ,. Бургарт Я.В,.Хундина О.Г, Салоутин В.И., Чупахин О.Н.
2-(Гет)арилгидразоно-1,3-дикарбонильные соединения в органическом
синтезе//Успехи химии 79(1) 2010
. Щегольков
Е.В., Слепухин П.А., Кажева О.Н., Шилов Г.В., Дьяченко О.А, Салоутин
В.И.,Кодесс М.И.Потемкин В.А., Гришина М.А. Исследование геометрической
изомерии в ряду фторалкисодержащих 2-арилгидразонов 1,2,3-трионов.//Журнал
органической химии. 2007. Т.43. Вып.3
. Масливцев
А.Н., Тарасова О.П., Адрейчиков Ю.С. 4,5-дифенил-2,3-дигидро-2,3-фурандион:
синтез и реакции с аминосоединениями//ЖорХ, 28 1287 (1992)
. Рубцов
Е.А.Залесов В.В. Синтез
4-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-илимино)-6-фенил-1,4-дигидро-2Н-пиридазин-3-онов//ХГС
2003. №3. С.625
. Пономарев
А.А., Синтезы и реакции фурановых веществ, Изд-во СГУ,Саратов, 1960 г.
8. A.Maxwell,
D. Rampersad, A new Amide from piper demerarum// J. Natur. Prod., 52, 891
(1989)
9. Гавкус
Д.Н. - Реакция азосочетания солей диазония с 3Н-фуран-2-онами рециклизация
продуктов под действием нуклеофильных реагентов - дипл. раб, Саратов, 2008
. Егорова
А.Ю.Замещенные 3Н-фуран-2-оны, их N,S-гетероаналоги. Синтез и реакции -
дис.раб. Саратов 2001