Графит и его соединения включения
Графит
и его соединения включения
Введение
Несмотря на весьма продолжительную историю
соединений включения (в том числе клатратных соединений) и созвездие выдающихся
ученых, их исследовавших, эти соединения долгое время оставались загадкой для
химиков и определенная доля экзотичности сохраняется за ними и в настоящее
время.
На заре развития химии, когда причины
образования соединений не были ясны, соединения включения рассматривались
химиками на общих основаниях. Но развитие теорий химической связи, все лучше и
лучше описывающих подавляющее большинство разнообразных химических веществ,
поставило как бы вне закона рассматриваемые соединения, поскольку ни одно из
них не подчинялось хорошо проверенным законам.
Ореол загадочности был снят с них английским
кристаллохимиком Г.Пауэллом в 1947-1948 годах. Пауэлл обнаружил, понял и описал
принципиально новую, более высокого уровня организацию химической материи. Были
обнаружены соединения, в которых между гостевыми и хозяйскими молекулами
существует химическое взаимодействие.
В 1973 году французский химик Жан-Мари Лен,
подчеркивая важную роль, которую играют невалентные взаимодействия в
формировании подобных соединений и обсуждая их свойства, ввел термин
"супрамолекулярная (надмолекулярная) химия", а в 1987 году ему,
американцам Чарлзу Педерсену и Доналду Крэму была вручена Нобелевская премия по
химии за достигнутые успехи в этой области знаний.
Понятие «соединения включения»
СОЕДИНЕНИЯ ВКЛЮЧЕНИЯ -
вещества, занимающие промежуточное положение между твёрдыми растворами
внедрения и истинными соединениями химическими.
Термин "соединение включения" ввел В.
Шленк в 1949 году.
Соединения включения - особый вид комплексных
соединений. Соединения включения образуются в результате внедрения молекул
одного вида в полости кристаллической решётки или молекул другого вида. Первые
молекулы получили название «гостей», вторые - «хозяев».
Способность вещества образовывать соединения
включения определяется наличием в нём полостей молекулярных размеров. Молекулы
включаемого вещества должны обладать конфигурацией, соответствующей форме
полости. Включенные молекулы удерживаются в соединениях включения силами
межмолекулярного взаимодействия.
Так как в соединения включения связываются друг
с другом не отдельные молекулы, а группы молекул, то целочисленного соотношения
между включаемым и включающими веществами, как правило, не существует.
Высокомолекулярные вещества позволяют получать
соединения включения за счёт полостей между цепями макромолекул. Часто
соединения включения образуются уже при смешении компонентов, иногда при
растирании. Они нестойки, в растворах обычно распадаются на исходные вещества.
Различают молекулярные соединения включения,
которые образуются при наличии полостей в единичных молекулах («хозяевах»)
относительно небольшой молекулярной массы. И различают решётчатые соединения
включения, в которых полости возникают при образовании кристаллической решётки,
иногда только в присутствии включаемого вещества; такие соединения могут быть
канальными (полости в форме канала) или клатратными (полости в форме клетки).
Клатратные соединения включения
КЛАТРАТЫ
(от лат. clathratus - защищенный решеткой) - соединения включения. Термин
"клатрат" ввел Г. Пауэлл в 1948году.
Различают решетчатые клатраты и молекулярные
клатраты.
Решетчатые клатраты образованы
включением молекул <#"530610.files/image001.gif"> <#"530610.files/image002.gif"> <#"530610.files/image003.gif">
<#"530610.files/image004.gif">
Рис. Кристаллическая решетка С8К;
темные кружки - атомы углерода, светлые - калия.
Во многих реакциях графитовые слои не
разрушаются и ведут себя как гигантские молекулы, которые при разложении
соединения сохраняют свою индивидуальность. Графитовый слой может выступать как
акцептор электронов при взаимодействии с сильными восстановителями и, наоборот,
как донор электронов при взаимодействии с окислителями.
Интеркалаты графита в значительной мере
образуются за счет переноса заряда от гостевой подсистемы к хозяйской или
наоборот. Однако соединения графита с щелочными металлами могут включать многие
органические молекулы, образуя тройные соединения.
графит химический углеродный
кристаллический
Разновидности соединений включения
графита
· Соединения со щелочными металлами
Соединения со щелочными металлами могут иметь
составы: С8М, С16М, С24М, С36М, С40М,
С64М. Металл в решетке находится в виде атома. При его ионизации
происходит перенос электронов в зону проводимости графита.
У соединения С8М атомы металла
располагаются над центрами гексаген, колец из атомов углерода. В соединении С16М
атомы металла расположены так же, но только между каждой парой слоев графита.
Аналогично построены и другие соединения.
В отличие от других щелочных
металлов, Na образует соединения с большим избытком углерода: из природного
графита получены C120Na, C64Na, C36Na, из
искусственно полученного графита - 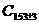 Na.
Na.
По уменьшению деформирующего
действия на решетку графита при образовании слоистых соединений щелочные
металлы располагаются в ряд: Cs, Rb, К, Na, Li.
Соединения с графитом образуют также
другие металлы - Ва, Sr, Zn, Cd и многие РЗЭ.
· Соединения с галогенами
В соединениях с галогенами происходит перенос
электронов из зоны проводимости графита к атомам галогена, в результате чего
образуются положительно заряженные дырки.
Наиболее известны бромсодержащие соединения
графита (например, С8Вr). Синтезированы соединения с фтором состава
CF0,676-CF0,998, C2F и C4F.
· Соединения с галогенидами
Весьма многочисленны соединения с галогенидами
(например, с А1С13, FeCl3, ZrCl4, UC14,
МоС15, MoF6, BrF3, IC1), оксигалогенидами (СrО2С12,
CrO2F2, UO2C12, XeOF2),
оксидами и сульфидами металлов.
Их часто называют "молекулярными
комплексами", т. к. они образуются при внедрении галогенидов в решетку
графита в виде молекул.
Из соединений с галогенидами металлов наиболее
изучено соединение с FeCl3, в котором содержание хлорида может
достигать 56%; при этом возможные для заполнения слои заняты только на 92%. В
случае А1С13 соединение имеет формулу С+m[АlС14
+ nАlС13], где соотношение m:(n+l) составляет 1:9, 1:18 или 1:36.
Сульфид или хлорид металла с переменной валентностью при внедрении в графит приобретает
более высокую степень окисления.
· Соединения с кислотами
Получены соединения графита с
кислородсодержащими кислотами, (например, C24HSO4 - *H2SO4
(гидросульфат графита)). H2SO4 внедряется в решетку
графита в виде ионов HSO4 или молекул. Известны соединения с HF
(например, C+24HF-2 *2H2F2).
Соединения с небольшим содержанием внедрившегося
вещества имеют черный цвет и по внешнему виду мало отличаются от исходного
графита. По мере увеличения содержания их цвет меняется сначала на
сине-голубой, затем на желто-оранжевый.
Наиболее интересное свойство
соединений графита - высокая электрическая проводимость, приближающаяся к
проводимости C<http://www.xumuk.ru/encyklopedia/2/4044.html> или Ag, a в
ряде случаев даже превышающая ее в 2-5 раз. Максимальная проводимость
характерна для соединений с акцепторами электронов. Эти значения в 70 раз
превышают электрическую проводимость исходного пиролитического графита и близки
к проводимости Аu. С понижением температуры электрическая проводимость
соединений графита увеличивается. Соединения с К, Rb и Cs обладают
сверхпроводящими свойствами.
Особенность соединений графита с
галогенами, некоторыми галогенидами металлов и др. - способность удерживать
часть внедрившихся атомов или молекул даже при высоких температурах. Такие
соединения называют "остаточными". Они устойчивы даже при нагревании
в нейтральных средах и в вакууме до 1200-1500 °С. Предполагают, что
внедрившиеся атомы и молекулы закрепляются на дефектах кристаллической решетки
графита.
Соединения графита образуются, как
правило, при нагревании графита с внедряющимися веществами, например с
хлоридами металлов - при 230 - 280°С, с щелочными металлами - при 300°С и выше.
С бромом графит реагирует при
комнатной температуре. В некоторых случаях требуется "катализатор"
(например, С12), роль которого сводится к обмену электронами с
реагентами в случае отсутствия такой способности (по отношению к графиту) у
внедряющегося вещества. Катализаторы входят в состав соединений графита. Так,
при образовании соединений с А1С13 один атом С1 приходится на три
молекулы хлорида, в случае InС13 или GdCl3 - нa шесть
молекул хлорида.
Наиболее подробно изучено
образование слоистых соединений с концентрированной H2SO4
в присутствии окислителей - NO3, CrO3, КМnО4 и
др. Гидросульфат графита получают в виде достаточно крупных образцов в
сравнительно больших масштабах, используя анодное окисление пиролитического
графита.
Интенсивно изучается синтез слоистых
соединений графита с галогенидами при давлениях до 10 МПа. В этом случае
следует ожидать получения соединений,Называющихся невнедряющимися в графит
галогенидами, например, с SeCl4, PC15, AsCl3.
Такие соединения могут быть основой новых неорганических материалов.
Промышленное применение соединений
графита очень быстро расширяется.
Соединения с кислотами используют в
химическом машиностроении в качестве антифрикционных материалов и химически
стойких прокладок.
На основе соединений с Li создаются
батареи высокой емкости.
Соединения с галогенами применяют в
органическом синтезе в качестве мягких фторирующих и хлорирующих агентов, с
фтором - как твердую смазку, материал катодов (в химических источниках тока) и
щеток для электродвигателей.
Из смесей соединений графита с медью
или алюминием изготавливают материалы, которые вследствие их малой плотности,
высокой электрической проводимости, сравнительной дешевизны применяют для
изготовления проводов.
Высокая электрическая проводимость
соединений графита позволяет применять их вместо графита в качестве
наполнителей пластмасс. Многие соединения являются катализаторами, в т.ч.
полимеризации, изомеризации.
Заключение
Итак, соединения включения являются типичными
представителями надмолекулярных образований, образованные включением молекул
одного сорта, называемых гостями, в полости кристаллического каркаса из молекул
другого сорта (или в полость одной большой молекулы), называемых хозяевами, без
образования какой-либо специфической химической связи между гостем и хозяином.
Способность графита включать ионы (атомы, молекулы)
разнообразных веществ позволяет в некоторых случаях существенно усилить его
полезные свойства.
Интеркаляция, как правило, приводит к
существенному увеличению электропроводности. Это обусловлено ростом
концентрации носителей тока по сравнению с графитом при сохранении их высокой
подвижности, связанной с двухмерным характером явления переноса. Если сравнить
электропроводность некоторых соединений включения графита наряду с
электропроводностью металлов, то можно увидеть перспективность использования
интеркалатов графита в качестве электропроводников, особенно если учесть, что
сейчас хорошо развито изготовление углеродных волокон и ведутся работы по
получению волоконных интеркалатов.
Основной недостаток этих материалов -
неустойчивость их работы во времени.
Второе перспективное направление - это
использование в качестве электродов в различных батареях и аккумуляторах.
Японская фирма "Sony" создала
аккумулятор, выдерживающий более 1000 циклов "заряд - полный разряд"
Кроме этого, хорошо просматривается возможность
применения интеркалатов графита как смазочных материалов в химически
агрессивных средах, как хранителей агрессивных веществ.
Список используемой литературы
. Коллонг
Р., Нестехиометрия, пер. с франц., М., 1974г.;
3. Свойства
конструкционных материалов на основе углерода
<http://www.xumuk.ru/encyklopedia/2/4636.html>. Справочник, под ред. В.
П. Соседова, М., 1975г.;
. Хаган
М., Клатратные соединения включения
<http://www.xumuk.ru/encyklopedia/2/4122.html>, пер. с англ., М., 1966г.;
. Пауэлл
Г. М., в кн.: Нестехиометрические соединения
<http://www.xumuk.ru/encyklopedia/2/2855.html>, пер. с англ., М., 1971г.;
. Крамер
Ф., Соединения включения пер. с англ. М., 1958г.;