Состояние исследований флавоноидов как группы БАВ в наше время
Содержание
Введение
1. Что такое флавоноиды?
2. Распространение флавоноидов
. Для чего нужны флавоноиды
. Антиоксидантное действие
флавоноидов
. Гепатопротекторное и
желчегонное действие
. Р-витаминное и
противовоспалительное действие флавоноидов
. Действие на
сердечно-сосудистую систему
. Гормоноподобное действие
флавоноидов
. Влияние флавоноидов на
иммунитет апоптоз
. Противоопухолевое действие
флавоноидов
. Другие эффекты флавоноидов
Заключение
Литература
Введение
флавоноид
иммунитет апоптоз
На земле произрастают тысячи разнообразных
растений. Среди них - большое количество лекарственных. Долгий путь проходит
каждое лекарственное растение, прежде чем начинает использоваться в клиниках.
Изучается его химический состав, определяются активно действующие вещества,
влияние их и растения в целом на функции различных органов и систем человека,
выявляется степень ядовитости отдельных химических веществ и всего растения,
устанавливается главное лечебное действие растения и его препаратов на
экспериментальных моделях различных заболеваний. И только тогда по специально
составленной инструкции новое лекарственное средство проходит испытания в
нескольких клиниках. При положительном результате фармакологический комитет
Минздрава здравоохранения РФ утверждает растение к широкому клиническому
применению, а его лечебные препараты- к промышленному производству.
Однако из десятков тысяч видов растений
исследовано не более двух тысяч. Многие медицинские работники не знакомы в
полной мере с их ценными свойствами. «Еще много тайн,- отмечает профессор
А.Ф.Герман,- хранят лекарственные растения, и еще многое обещают они человеку в
борьбе за его здоровье».
Благодаря громадным успехам синтетической химии,
были созданы сотни новых лечебных препаратов, которые с успехом стали применяться
при самых разнообразных заболеваниях. В связи с этим распространилось мнение,
что применение лекарственных трав - уже пройденный этап в современной медицине.
Однако скоро выяснилось, что не всегда химически
чистые синтетические препараты могут полностью заменить лекарственные растения
и растительные препараты. Вещества, входящие в состав растений, принципиально
более родственны человеческому организму по своей природе, нежели синтетические
препараты. Отсюда и значительно большая их биодоступность, и сравнительно
редкие случаи индивидуальной непереносимости, и проявления лекарственной
болезни. К тому же, изготовление лекарственных препаратов из растений
экономически выгоднее и технически менее сложно.
В последние десятилетия пристальное внимание
исследователей привлекают продукты вторичного метаболизма растений -
флавоноиды, в связи с широким спектром их биологического действия. Они широко
распространены в природе. Особенно богаты флавоноидами высшие растения:
встречаются они также у некоторых низших растений (зеленые водоросли - ряски),
у споровых (мхи, папоротники), у некоторых насекомых и микроорганизмов. Интерес
к флавоноидам как биологически активным веществам возник в 40-е годы ХХ века,
когда венгерский биохимик Суент-Доорди установил, что сумма флавоноидов из
околоплодника лимона обладает Р-витаминным действием, т.е. способностью
уменьшать хрупкость и проницаемость стенок капилляров. Интерес к этой группе
БАВ сохраняется и по сей день. Ученые открывают все новые и новые свойства
флавоноидов. Разнообразие функций флавоноидов, известных в настоящее время,
столь огромно, что совершенно невозможно утверждать наверняка, когда, где и
каким образом проявят себя данные соединения.
Актуальность работы: так как флавоноиды имеют
очень богатый спектр фармакологического действия, то это позволяет выпускать
большое количество лекарственных препаратов. А также дальнейшее изучение
свойств флавоноидов помогает ученым открывать все новые и новые действия этой
группы БАВ на организм.
Целью работы: изучить состояние исследований
флавоноидов как группы БАВ в наше время.
Задачи:
1. познакомиться с группой БАВ -
флавоноидами;
2. изучить их свойства;
. определить их фармакологические
действия на организм и состояние их исследования.
1. Что такое флавоноиды?
Итак, что же такое флавоноиды?
Флавоноидами называется группа природных
биологически активных соединений - производных бензо-y-пирона, в основе которых
лежит фенилпропановый скелет, состоящий из С6-С3-С6 углеродных единиц. Это
гетероциклические соединения с атомом кислорода в кольце.
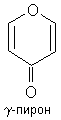
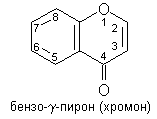
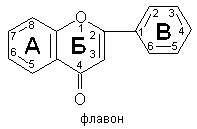
При замещении в хромоне атома
водорода в a-положении на фенильную группу образуется 2-фенил-(а)-бензо-y-пирон
или флавон, который состоит из 2 ароматических остатков А и В и трехуглеродного
звена (пропановый скелет).
Под термином флавоноиды (от лат.
flavus - желтый, так как первые выделенные из растений флавоноиды имели желтую
окраску, позднее установлено, что многие из них бесцветны) объединены различные
соединения, генетически связанные друг с другом, но обладающие различным
фармакологическим действием.
Впервые флавоноиды были исследованы
в 30-ых годах прошлого столетия американским биохимиком венгерского
происхождения Альбертом Сент-Дьёрди. За свои работы по биологическому окислению
Сент-Дьёрди в 1937 году был удостоен Нобелевской премии.
Изучение флавоноидов относится к
началу XIX в., когда в 1814 г. Шевроле выделил из коры особого вида дуба
кристаллическое вещество, названное кверцетрином. Спустя 40 лет Риганд
установил гликозидный характер этого вещества. и агликон назвал кверцетином. В
1842 г. Вайс сообщил о выделении рутина из Ruta graveolens. Впервые в 1864 г. в
индивидуальном виде был получен хризин из тополя; строение его было подтверждено
в 1898 г. Косанецким путем синтеза метилового эфира хорацетофенона с этиловым
эфиром бензойной кислоты. В 1903 г. Валяшко установил строение рутина.
Систематическое изучение строения природных флавоноидов многие годы проводили
польские химики. Большую работу по изучению антоцианов провел Вильштеттер.
Исследованиями катехинов занимались А. Л. Курсанов, М. Н. Запраметов, К.
Фрейденберг и др. Интерес к флавоноидным соединениям особенно возрос в 40-е
годы нашего столетия: флавоноиды привлекают внимание ученых разносторонней
биологической активностью и чрезвычайно низкой токсичностью. После 1970 г.
выделено свыше 1400 соединений, относящихся к флавоноидам. Перспективным
направлением является поиск биологически активных соединений группы ксантонов -
близких по строению к флавоноидам.[1]
Сегодня известно свыше 6500
флавонидов. Общепринято их деление на 10 подгрупп. Эти основные классы
обозначены в зависимости от степени окисления входящего в состав молекулы
флавонидов трехуглеродного фрагмента. Вот эти классы:
Лейкоантоцианидины (сюда относятся
флаван-3,4-диолы)
1) Катехины (производные флавана -
лейкоантоцианы и катехины, а так же флаван-3-олы)
1) дигидрохалконы
) халконы
) флаваноны (а так же производные флавона
- флаванонолы, флаваноны, флавонолы и флавоны)
) антоцианы и антоцианидины
) ауроны
) флавоны и изофлавоны
) флавононолы
) флавонолы
Но существует и другая классификация в
зависимости от гидроксилирования пропанового скелета С6-С3-С6 , положения
фенильного радикала и величины гетероцикла
I. Собственно флавоноиды (эуфлавоноиды) с
боковым фенильным радикалом у С2.
1) производные флавана (2 фенилхромана):
флаван, катехин, лейкоантоцианидин, антоцианидин.
2) производные флавона (2 фенилхромона):
флавон, флавонол, флавонон, флавононол.
) флавоноиды с раскрытым пироновым
кольцом: халкон, дигидрохалкон.
) ауроны.
II. Изофлавоноиды с фенильным радикалом у
С3: изофлаван, изофлавон, изофлаванон и др.
III. Неофлавоноиды с фенильным радикалом у
С4: 4-бензокумарин, 4-бензохроман (неофлаван). Бифлавоноиды: биофлавон.
. Распространение флавоноидов
Флавоноиды широко распространены в растительном
мире. Особенно богаты флавоноидами высшие растения, относящиеся к семействам
розоцветных (различные виды боярышников, черноплодная рябина), бобовых (софора
японская, стальник полевой, солодка), гречишных (различные виды горцев -
перечный, почечуйный, птичий: гречиха), астровых (бессмертник песчаный,
сушеница топяная, пижма), яснотковых (пустырник сердечный) и др. Более часто
флавоноиды встречаются в тропических и альпийских растениях. Обнаружены и у
низших растений: зеленые водоросли (ряски), споровые (мхи, папоротники), хвощи
(хвощ полевой), а также у некоторых насекомых (мраморно-белая бабочка).
Находятся флавоноиды в различных органах, но чаще в надземных: цветках, листьях,
плодах; значительно меньше их в стеблях и подземных органах (солодка, шлемник
байкальский, стальник полевой). Наиболее богаты ими молодые цветки, незрелые
плоды. Локализуются в клеточном соке в растворенном виде. Содержание
флавоноидов в растениях различно: в среднем 0,5-5%, иногда достигает 20% (в
цветках софоры японской).
В растениях флавоноидные соединения, кроме
катехинов и лейкоантоцианов, сравнительно редко встречаются в свободном
состоянии. Подавляющее большинство их представлено в виде разнообразных
гликозидов. Многообразие флавоноидных гликозидов обусловлено значительным
набором сахаров и возможностями присоединения их в ряде положений, а также тем,
что сахара могут иметь различную величину окисных циклов, конфигурацию
гликозидных связей порядок сочетаний между ними. Причём такие сложные смеси
часто встречаются в одном и том же растительном материале.
В качестве углеводной части могут быть моно-,
ди- и трисахариды. Моносахаридами являются обычные для растений сахара:
D-глюкоза, D-галактоза, D-ксилоза, L-рамноза и др. В некоторых случаях
встречаются специфические дисахариды: рутиноза (рамноза и глюкоза), софороза (2
молекулы глюкозы).
Все известные флавоноидные гликозиды разделяются
на следующие группы: Основную группу флавоноидов составляют О-гликозиды, в
которых сахара cвязаны с агликоном полуацетальной связью через атом кислорода.
О-гликозиды в зависимости от количества сахаров, положения и порядка
присоединения делятся на моногликозиды, биозиды, дигликозиды и смешанные
гликозиды. Вторую группу составляют С-гликозиды или гликофлавоноиды, которые
можно подразделить на С-моногликозиды, С-дигликозиды, С-О-дигликозиды,
С-О-биозиды. В гликофлавоноидах углеводные заместители связаны с агликоном
через углеродный атом в 6 или 8-м положении. К третьей группе флавоноидных
гликозидов относятся так называемые комплексные соединения. Они представляют
собой ацилированные гликозиды различных групп и в зависимости от положения
ацильного заместителя делятся на гликозиды депсиноидного типа и гликозиды со
сложноэфирной связью в сахарных заместителях. Из кислот, выделенных из
комплексных гликозидов, идентифицированы бензойная, n-оксибензойная, кофейная,
уксусная, пропионовая, n-оксикоричная и другие кислоты.
К флавоноидам относятся производные халкона,
катехины, антоцианидины, ауроны. Катехины относятся к полифенолам, входят в
состав конденсированных дубильных веществ. Катехины представляют собой наиболее
восстановленные флавоноидные соединения. Многие красные и синие окраски цветков
с различными оттенками обусловлены присутствием антоцианидинов. В зависимости
от рН среды окраска цветков меняется. В кислотной среде они образуют розовую,
красную окраску, в щелочной среде - от голубой до синей с разными оттенками.
Ауроны имеют разнообразную структуру. Они встречаются в растениях семейства
астровых. В растениях присутствуют в форме гликозидов.[1]
. Для чего нужны флавоноид
Естественные функции флавоноидов на сегодняшний
день не достаточно тщательно изучены. Способность винограда красных сортов
улучшать пищеварение, как и «дар» ягод черники повышать остроту зрения,
известны людям с незапамятных времен. Однако лишь в середине ХХ в стало
известно, что фармакологические механизмы действия и названных, и многих других
лекарственных растений связаны с высоким содержанием в них флавоноидов - группы
веществ, которые играют одну из важнейших функций в регулировании жизненного
цикла растений.
Так, именно флавоноиды определяют окраску цветов
и ягод. Кроме того, эти вещества участвуют в фотосинтезе, защищают растительные
клетки от избытка ультрафиолетового излучения летом, и необходимы для таких
процессов подготовки растений к холодам, как опадание листьев и «консервация»
почек. Яркая окраска цветов привлекает насекомых и способствует процессам
опыления. Известно, что флавоноиды повышают устойчивость растений к воздействию
некоторых патогенных грибов.
Многочисленные исследования показали, что
флавоноиды являются биологически активными соединениями и для человека, хотя и
не вырабатываются в организме животных.
Научно доказана способность многих флавоноидов
регулировать проницаемость стенок кровеносных сосудов и улучшать их
эластичность, а также предотвращать склеротические поражения.
Самый известный из флавоноидов, оказывающий
благотворное действие на сосуды - это рутин (иногда его еще называют витамином
Р или С2). Этот флавоноид (или его синтетический аналог) входит в состав многих
препаратов, которые уменьшают ломкость капилляров - например таких, как
аскорутин (Ascorutinum).
Однако, как показали исследования,
характеристиками, аналогичными рутину, обладают более сотни флавоноидов! Они в
изобилии содержатся в таких продуктах как зеленый чай, какао, айва, яблоки,
абрикосы, персики, земляника, смородина, малина и др.[3]
Достаточно широко используют фармакологи и
экстракт ягод черники, содержащий до 25% так называемых антоцианов
(флавоноидов, которые в растениях играют роль пигментов). Богатый флавоноидами
экстракт черники применяют как мягкое диуретическое средство, при
сердечно-сосудистых заболеваниях, варикозном расширении вен и в комплексной
терапии процессов, связанных с дистрофией и дегенерацией сетчатки.
Существует большое количество биологически
активных добавок, которые изготовлены на основе экстрактов растений, богатых
флавоноидами. Благодаря антиоксидантному действию флавоноидов, подобным БАДам
приписывают свойство замедлять старение и препятствовать возникновению
злокачественных новообразований.
В организме человека они способны выполнять ту
же функцию, что и в растениях - флавоноиды нейтрализуют свободные радикалы
(которые образуются под воздействием ультрафиолетового излучения и радиации),
защищая клетки от разрушения мембран и внутриклеточных структур. Поэтому
натуральные экстракты флавоноидов (к примеру, красное вино) в умеренных дозах
рекомендуют употреблять людям, которые живут в областях с повышенным
радиационным фоном: зона Чернобыльской катастрофы, высокогорные районы и т.д.
Эти же флавоноиды способны защищать ткани от
повреждений, вызванных избыточным выбросом так называемых гистаминов (веществ,
высвобождающихся при воспалительных процессах и аллергии), что дает
дополнительные возможности в лечении астмы и аллергических реакций.
В сое и ячменном солоде содержатся флавоноиды,
по структуре очень похожие на женские половые гормоны - эстрогены. По мнению
некоторых исследователей, эти вещества можно использовать для создания
препаратов, облегчающих климактерический синдром.
Пусть способность флавоноидов отсрочить старение
и не доказана, но то, что употребление продуктов, содержащих большое количество
флавоноидов, принесет лишь пользу, можно утверждать смело! Тем более что фрукты
и овощи, в которых содержатся флавоноиды, также богаты витаминами, целлюлозными
волокнами, пектиновыми веществами и обязательно должны входить в ежедневный
рацион.
Не следует переживать и о том, что большие
количества флавоноидов могут негативно отразиться на здоровье. Наш организм
обладает совершенными механизмами регулирования содержания флавоноидов, поэтому
их избыток будет быстро выведен из организма, не нанося вреда здоровью.
Опасность могут представлять лишь
концентрированные экстракты с большим содержанием флавоноидов, которые входят в
состав лекарственных средств и БАДов. В этом случае нужно четко придерживаться
рекомендаций врача или хотя бы дозировок и сроков приема, приведенных в инструкции
к препарату.
Спектр фармакологического действия различных
флавоноидов очень широк. Они обладают антиоксидантным, гепатопротекторным,
желчегонным, капилляроукрепляющим, противовоспалительным, гипотензивным,
картиотропным, гормоноподобным, противовирусным и многими другими дествиями.
. Антиоксидантное действие флавоноидов
Большое внимание в настоящее время уделяется
биофлавоноидам - большой группе соединений с полифенольной структурой. Имеются
сведения о их антиоксидантной активности. Антиоксиданты растительного
происхождения широко используют в медицине и пищевой промышленности в виде
экстрактов и натуральных масел.
В работах отечественных ученых (А.В. Шабров,
В.А. Дадали, В.Г. Макаров 2003г.) было показано, что растительные биофлавоноиды
обладают целым рядом уникальных особенностей:
Флавоноиды подавляют перекисные процессы в самой
первой - инициирующей стадии, выступая как «ловушки» супероксид- радикала и
перекиси водорода, предотвращая образование последующих более токсичных
продуктов. В этом плане флавоноиды аналогично антиоксидантному ферменту -
супероксиддисмутазе.
Флавоноиды функционируют как «ловушки» и
вторичных активных форм кислорода, пероксинитрита, перекисей липидов, а также
свободных радикалов, образующихся при действии на организм токсикантов,
например, хлорсодержащих. Это так называемая «цепьобрывающая» активность
флавоноидов.
Флавоноиды функционируют как эффективные
«хелаторы», связывающие ионы переходных металлов, в том числе стимулирующих
перекисные процессы, в силу чего эти соединения являются эффективными
ингибиторами металлкатализируемого перекисного окисления липидов, белков и
других веществ. По этому же механизму флавоноиды связывают и ионы токсичных
тяжелых металлов, способствуя их элиминированию из организма.
Флавоноиды ингибируют ферментативные реакции, в
которых продуцируются супероксид-радикал и перекись водорода (например,
ксантиноксидазу, пероксидазная активность которой существенно возрастает при
ишемии, и др.).
Флавоноиды оказывают защитное действие на
ферменты ферментативного звена антиоксидантной системы клетки, в частности,
ферменты первой линии антиоксидантной защиты - супероксиддисмутазу, пероксидазы
и др.[4]
Антиоксидантный эффект флавоноидов реализуется
по комбинированному механизму и обладает синергизмом с аскорбиновой кислотой и
витамином Е. Флавоноиды обладают еще и капилляростабилизирующим эффектом на
резистентность и проницаемость сосудистой стенки.
Флавоноиды ингибируют такие ферменты, как
гиалуронидазу и коллагеназу. Другой механизм, которым обладают флавоноиды - это
их окислительно-восстановительные свойства. Воздействие на ферменты тканевого
дыхания, утилизации кислорода и синтез АТФ в митохондриях.
Сегодня целый ряд отечественных и зарубежных
исследований в своих работах показали, что флавоноиды повышают кислородное и
энергетическое обеспечение клеток, оказывают влияние на функционирование одной
из важнейших систем организма - цитохром Р-450, который обеспечивает выведение
из организма чужеродных токсинов, обеспечивая биотрансформацию токсических
компонентов лекарств, предотвращая их воздействие на организм через механизм
детоксикации печени.
Антиоксидантное действие флавоноидов реализуется
через различные механизмы действия. Они могут реагировать, как классические
фенольные радикальные ингибиторы, взаимодействуя с липидными радикалами, либо
реагируя на активные формы кислорода. Другой путь воздействия на организм
связан со способностью ингибировать липоксигеназу или же образовывать комплексы
с ионами Fe 3+, которые, в свою очередь, активируют процесс свободнорадикального
окисления. Пивоваренко В.Г. и др. 1997 г. Эти же данные приводят и зарубежные
ученые (Das Mukul, Prasante 1988 г).[10]
. Гепатопротекторное и желчегонное
действие
Гепатопротекторный эффект флавоноидов
проявляется в ослаблении действия повреждающих факторов, в том числе некоторых
химических соединений (четыреххлористого углерода, хлороформа, бензола и др.).
Механизм действия флавоноидов заключается в ингибировании перекисного окисления
липидов, уплотнение сосудисто-тканевых мембран, сохранение уровня эндогенной
аскорбиновой кислоты и гликогена печени. Установлено, что под влиянием
кверцетина, лютеолина и других флавоноидов содержание гликогена в печени
увеличивается на 38,7-85,9% .
Немаловажное значение имеет способность
флавоноидных соединений образовывать комплексы с ионами тяжелых металлов, что
послужило основанием для успешного применения некоторых полифенолов в качестве
антидотов при отравлении тяжелыми металлами. В настоящее время самым популярным
лекарственным растением, как источника гепатопротекторов, является расторопша
пятнистая (легален, красил, силимар, силибор, экстракт расторопши жидкий и
др.).[8]
Механизм гепатопротекторного действия
кверцетина, флавоноида расторопши и некоторых других растений, обусловлен
связыванием токсичных свободных радикалов и стабилизацией клеточных мембран и
лизосом (что свойственно и другим флавоноидам). Кроме того, под влиянием
катергена происходит стимуляция биосинтеза АТФ в печени, тем самым облегчается
протекание биохимических реакций, связанных с затратой энергии и
фосфорилирование в печени. Он обладает мембраностабилизирующим действием,
уменьшая проницаемость клеточных мембран для низкомолекулярных водорастворимых
соединений, транспортируемых путем свободной и обменной диффузии.
· Механизм гепатопротекторного
действия флаволигнанов:
· обусловлен их способностью
взаимодействовать со свободными радикалами, реализующийся за счет наличия в их
структуре подвижного водорода, используемого для ликвидации свободных
радикалов.
· защита биологических мембран от
токсинов в результате ингибирования их захвата гепатоцитами;
· стабилизации клеточных мембран и
включения в них фосфолипидов (репарация мембран);
· повышение обезвреживающей функции
гепатоцитов, связанное с увеличением пула глутатиона в гепатоците и
возрастанием активности ферментов, участвующих в окислении ксенобиотиков (в
частности супероксиддисмутазы);
· повышение белково-синтетической
функции печени;
· ингибирование синтеза холестерина в
результате уменьшения активности микросомальной гидроксил-СоА-редуктазы;
противовоспалительное и иммуномоделирующее действие, обусловленное уменьшением
активности макрофагальных клеток, участвующих в презентации антигенов.
Ученые проводили много исследований на
подтверждение гепатопротектороного действия флавоноидов и сделали следующие
выводы:
1) флаваноиды оказывают выраженное
гепатопротекторное действие при поражении печени и длительной алкоголизации,
уменьшая синдромы цитолиза, холестаза, мезенхимального воспаления, жировой
дистрофии и печеночной недостаточности, вызванные развитием окислительного
стресса.
2) на фоне алкогольной интоксикации
наибольшая эффективность лечебно-профилактического действия отмечается у
флавицина, которые практически полностью устраняют признаки поражения печени
) гистоморфологические исследования подтверждают
наличие более выраженной гепатозащитной активности флавицина по сравнению с
карсилом при гепатитогепатозе и при алкогольном поражении печени, при введении
которых признаки воспаления, нарушения микроциркуляции и жировой дистрофии,
некрозы и нарушение цитоархитектоники печеночных балок, выражены в меньшей
степени, чем у животных, получавших карсил.
) флавоноиды улучшают
энергообеспеченность клеток печени, увеличивают содержание АТФ, повышают
N-деметилазную и n-гидроксилазную активностей в норме и в условиях острых
поражений печени СС14 и этанолом.[7]
. Р-витаминное и противовоспалительное
действие флавоноидов
Известно и изучено капилляроукрепляющее и
противовоспалительное действие флавоноидов растений (Н. К. Сибуль, М. М. Куль,
1960; А. П. Казанцев, 1968).
Свойство растений подавлять внутренние и
наружные воспалительные реакции известно испокон веков. В многочисленных
экспериментах доказано, что именно флавоноиды ответственны за
противовоспалительные свойства растений. Эксперимент Loggia является хорошей
иллюстрацией. В нем сравнивалось действие водного и масляного экстрактов
ромашки на воспаленный участок кожи у мышей. Водный раствор (содержащий
биофлавоноиды) оказался в 2 раза активнее, чем масляный (содержащий в основном
эссенциальные жирные кислоты). Очищенная биофлавонная фракция была в 12 раз
активнее, чем обычный водный экстракт. Исследователи также протестировали
отдельные флавоноиды и нашли, что кверцетин, леутеолин и апегенин особенно
сильны в блокировке воспалительной реакции. Противовоспалительное действие
объясняется их антиоксидантными свойствами. Одной из особенностей флавоноидов
является их способность ингибировать липооксигеназу - фермент, превращающий
арахидоновую кислоту в лейкотриены. Некоторые лейкотриены, такие как В4, напрямую
вовлечены в воспаление и их функция - привлекать нейтрофилы и другие белые
клетки крови к месту воспаления, и активировать их, запуская воспалительную
реакцию. Блокируя липооксигеназу, биофлавоноиды тем самым ослабляют воспаление.
Капилляроукрепляющее (Р-витаминное) действие
присуще разным флавоноидам, и в этом смысле витамин Р (от рermicabilitis -
проницаемость) не является индивидуальным веществом. Эти свойства выражены у
лейкоантоцианов и антоцианов многих окрашенных плодов и ягод. Практически во
всех растениях витамин Р встречается вместе с витамином С. Они потенцируют
капилляроукрепляющее действие друг друга, необходимы в биохимической
"связке", но не взаимозаменяемы. В конечном счете, различные
флавоноиды с Р-витаминной активностью (в разной степени она присутствует более
чем у 150 флавоноидных соединений) устраняют и предупреждают повышенную
хрупкость капилляров и проницаемость стенки не только при витаминной
недостаточности, но и при воспалительных процессах, капилляротоксикозах разного
генеза, аллергиях. Отсюда - широкий круг показаний к их применению в медицине.
Обязательными составными прополиса являются
флавоноиды (их выявлено 19) и секрет верхнечелюстных желез пчел, в состав
которого входит 10-окси-2-деценовая кислота.
Принимая во внимание относительно высокое
содержание фенольных соединений, к которым принадлежат флавоноиды (до 25 %) и
фенолокислоты, академиком О.И. Тихоновым в 1977 г. была выдвинута гипотеза, а
потом и доказано, что именно этот класс химических соединений определяет
направленность лечебных свойств прополиса. Это обстоятельство является важной
аргументацией выдвинутой акад. О.И. Тихоновым теории происхождения прополиса:
собранные пчелами вещества органического и неорганического характера являются
только исходным сырьем, которое целеустремленно, под действием физиологических
процессов организма, пчелы превращают в биологически активный комплекс
соединений химического состава и биологического действия. Он является одним из
крайне необходимых средств, обеспечивающих нормальное функционирование пчелиной
семьи.[5]
Для производства косметики, используют вещество
диквертин - представляет собой комплекс флавоноидов, содержит 90%
дигидрокверцитина, обладает ярко выраженной Р-витаминной активностью. Его
просто необходимо включать в косметические средства с регенерирующим,
антиоксидантным действием для оздоровления и омоложения кожи. Выделяют
диквертин из комлевой части древесины лиственницы даурской.
. Действие на сердечно-сосудистую систему
В кардиотропное действие мы условно объединяем
три вида активности: кардиотоническую, коронарорасширяющую и
противоаритмическую. Для такого, в общем произвольного, объединения есть свои
основания. Эти стороны действия сопутствуют друг другу, и каждое из них
выражено довольно умеренно. В то же время их сочетание полезно и эффективно при
легких формах нарушений сердечной деятельности (ослаблении сокращений,
экстрасистолиях, болевом синдроме и т. п.), при вегетососудистой дистонии и
невротических расстройствах, гипертонической болезни и т. д.
Кардиотропное действие сильнее выражено и лучше
изучено у флавоноидов цветков и плодов боярышника (различных видов). Растение
вырабатывает более 15 флавоноидов (в виде агликонов и гликозидов), из которых
наибольший интерес представляют гиперозид, кверцетин, витексин и его рамнозид.
Механизм кардиотонического действия гиперозида
связан с первичным положительным влиянием флавоноидов на энергетический обмен
миокарда (повышение утилизации глюкозы, коэффициента полезного действия
использования кислорода), обогащением сердца ионами калия. Другие растения,
также содержащие гиперозид, но имеющие иной состав прочих действующих начал,
оказывают менее выраженный кардиотонический эффект. Такое действие присутствует
у препаратов пустырника, коровяка, астрагала, зверобоя, копытня, цветков липы.
Флавоноиды отличает малая токсичность вообще и для больного в частности, что
позволяет применять их длительными курсами.
Известны растения, которые широко применяются в
народной медицине. Например, в странах юго-восточной Азии растения рода Chrysanthemum
используются в качестве средств, улучшающих коронарный кровоток; устраняющих
симптомы вегетососудистой дистонии; снижающих артериальное давление;
нормализующих обмен веществ; поддерживающих антитоксическую функцию печени; как
успокаивающее и антиаллергическое средство.
Хризантема корейская широко культивируется в
нашей стране как декоративное растение, но не используется в практических целях
в качестве источника биологически активных соединений. Причиной этого является
недостаточная изученность химического состава Chrysanthemum х koreanum Makai и
отсутствие исследований фармакологического действия препаратов, выделенных из
этого растения.[5]
С этой точки зрения углубленное изучение
химического состава, а также разработка доступных и легковоспроизводимых
способов получения суммарных фракций из хризантемы в качестве перспективных
источников для создания новых лечебно-профилактических средств является
актуальной проблемой.
Исследование Hertoy еще в 1998 г. показали, что
употребление 60-70 мг флавоноидов в день достоверно снижает смертность в 3 раза
от сердечно-сосудистых заболеваний.
Спазмолитическое и гипотензивное действие в
разной мере присуще флавоноидам многих растений и также обязано их комбинации с
другими действующими началами (эфирными маслами, хромонами, кумаринами и
прочими). Спазмолитические свойства флавоноидов проявляются в отношении
коронарных, меньше мозговых сосудов, кишечника, бронхов, желчевыводящих путей,
матки. По всей вероятности, они имеют миотропную природу. Флавоноиды разрешают
спазм гладкомышечных волокон, провоцируемый различными эндо- и экзогенными
факторами. К числу наиболее активных относится гиперин.
Некоторым растениям присуще и седативное
действие, что логически позволяет связать стабилизацию артериального давления и
с уменьшением стрессогенных влияний на сосудодвигательный центр. Наличие
умеренного мочегонного эффекта является полезным дополнением и может быть
усилено включением растений с более выраженным диуретическим действием.
. Гормоноподобное действие флавоноидов
Бодибилдерам, вероятно, знаком хризин - добавка,
увеличивающая синтез тестостерона в организме за счет активизации прогормонов.
Его относят к флавонам. Изначально он появился на рынке товаров для
бодибилдинга под загадочным названием «флавон икс» (flavone X). Исследования
показали, что флавон икс - это естественный ингибитор ароматазы, фермент,
содержащийся в теле человека в больших количествах, превращающий андрогены,
например тестостерон, в эстроген.
Предположение о том, что хризин способен
подавлять активность ароматазы, возникло на основе сравнительных исследований
эффективности различных флавоноидов и препарата-ингибитора ароматазы под
названием аминоглютетимид (торговые марки цитадрен и ориметен). Из одиннадцати
флавоноидов естественного происхождения ближе всех к цитадрену по эффективности
подавления ароматазы оказался хризин. Но дело в том, что действие хризина
изучалось на изолированных жировых клетках (in vitro). Оставалось лишь
догадываться, как он повел бы себя в теле человека.
Последнее исследование влияния хризина и других
флавоноидов на активность ароматазы проводилось на крысах. Чтобы воспроизвести
прием внутрь человеком хризиносодержащих добавок, крысы получали дозы препарата
перорально. Какого-либо действия флавоноидов на активность ароматазы исследование
не выявило. Такой же результат показали и исследования на людях, принимавших
хризиносодержащие добавки.
Это вовсе не значит, что флавоноиды не действуют
на активность гормонов. Как показало одно исследование, различные флавоноиды
влияют на работу ферментов печени, играющих роль в разложении тестостерона. Еще
предстоит выяснить, может ли употребление этих флавоноидов увеличить его
активность.
В ходе другого исследования выяснилось, что
флавоноид, полученный из средиземноморского тополя рорulus nigra, подавляет
энзим 5-альфа редуктазу, преобразущую тестостерон в дигидротестостерон
(DHT).связан с частичным облысением у мужчин, увеличением простаты и появлением
прыщей - частыми побочными эффектами применения анаболических стероидов.
Катехины, активные флавоноиды в чае, также подавляют превращение тестостерона
как в DHT, так и в эстроген, блокируя изменение 5-альфа редуктазы и ароматазы.
Содержащиеся в сое и других растениях
изофлавоны, такие как генистеин, по структуре сходны с эстрогеном и могут замещать
его на клеточных рецепторах или иным образом влиять на его активность. Так
называемые фитоэстрогены могут в зависимости от дозировки проявлять слабую или
сильную эстрогенную активность. Плюс в том, что изофлавоны и другие флавоноиды,
в том числе кверцетин, помогают предотвратить рак предстательной железы, а
также препятствуют действию средовых эстрогенов. И все же в количествах более
50 мг в день изофлавоны могут влиять на активность андрогена и даже вызывать
распад мышечной ткани. В еще больших количествах они, как это ни парадоксально,
способствуют появлению рака груди у некоторых женщин.
. Влияние флавоноидов на иммунитет и
апоптоз
В работе А.Н. Евстропова и соавт. (2004)
показано интерфероногенное и иммуностимулирующее действие водорастворимого полифенольного
комплекса из пятилистника кустарникового. Водный экстракт растения повышал
антителообразующую активность клеток селезенки мышей, иммунизированных
эритроцитами барана, и стимулировал клеточный иммунный ответ. Исследования А.А.
Чурина и соавт. (2005) в отношении полифенольного экстракта из бадана
толстолистного (Bergenia crassifolia Fritsch.) выявили нормализующий эффект
препарата на содержание антителообразующих клеток селезенки мышей при
иммунодепрессии и стимуляции гуморального иммунитета. Экстракт бадана снижал
выраженность воспалительных процессов в условиях реакции гиперчувствительности
замедленного типа, препятствуя накоплению Т-лимфоцитов в очаге воспаления и
подавляя способность этих клеток продуцировать провоспалительные цитокины.
Интересны также данные об иммуномодулирующих свойствах флавоноидов из
расторопши пятнистой при алкогольной болезни печени. Их длительное назначение
(около 6 мес.) угнетало активность цитотоксического звена иммунитета
(содержание цитотоксических лимфоцитов CD8+), уменьшало продукцию γ-глобулинов
и увеличивало скорость бласттрансформации лимфоцитов. M. Comalada etal. (2006)
показана стимуляция кверцетином и лютеолином экспрессии IL-10 костномозговыми
макрофагами, кроме того, данные соединения также ингибировали продукцию TNFα
и
оксида азота ЛПС-активированными макрофагами. Молекулярные механизмы про- и
антиапоптотического действия Ф изучены недостаточно. Обнаружены свойства
силибинина из Silybum marianum ингибировать изопротеренол-индуцированное
повреждение ДНК кардиомиоцитов мышей через блокирование каспазного пути
апоптоза и торможение фосфорилирования белка р53. Кверцетин и винные полифенолы
из Vitis vinifera L. in vitro предупреждали гибель эндотелиальных клеток,
нивелируя их дисфункцию, что иллюстрировалось в исследованиях in vivo снижением
кровяного давления у животных с моделью артериальной гипертензии. Однако,
некоторые полифенолы красных вин (морин, рутин, галловая кислота) ингибировали
рост культуры почечных LNCaP_клеток в различных концентрациях (от 10 до 175
мкмоль/мл) и индуцировали апоптотические изменения их ядер.
. Противоопухолевое действие флавоноидов
В последние годы появились сообщения о
противоопухолевом действии флавоноидов из-за их антиоксидантной активности,
способности подавлять свободные радикалы, уменьшать их концентрацию в клеточных
мембранах. Благодаря антиоксидантной и мембранопротекторной функции, они влияют
на иммунологические свойства, защищают молекулы ДНК от повреждающего действия
интермедиантов и переокисления. Кроме того, флавоноиды, оксикумарины при
окислении переходят в хиноидную форму, благодаря чему взаимодействуют с ДНК,
снижают антиокислительную активность липидов опухолевых клеток, т.е. снижают их
жизнеспособность. Растения, содержащие фенолгликозиды и флавоноиды, обладают мочегонным
и гепатопротекторным действием, что способствует обезвреживанию и удалению
токсинов и шлаков, в большом количестве накапливающихся при раковых
заболеваниях.
В настоящее время предпринимаются попытки
изучения молекулярно - клеточных механизмов, лежащих в основе фармакологических
эффектов фитопрепаратов. Показано, что средства растительного происхождения
оказывают влияние, как на клеточные, так и на гуморальные звенья иммунитета.
Существуют множество БАД, содержащих флавоноиды
растений, такие как Олексин, Детрикан, которые обладают противоопухолевой
активностью.
Данные о противоопухолевой активности препаратов
растительного происхождения, содержащих полифенолы (О. К. Кабиев, С. Б.
Балмуханов, 1975; В. А. Барабой, 1976), свидетельствуют о целесообразности
продолжать поиски новых лекарственных средств в этом направлении.[9]
Противоопухолевое действие Ф продемонстрировано
в ряде экспериментов in vitro и in vivo. Влияние данных соединений на
бластомные клетки обусловлено преимущественно торможением ангиогенеза, что
продемонстрировано в работах R.P.
Singh et
al. (2006) (силибинин
вызывал подавление роста уретан-индуцированной опухоли легких у мышей) и E.J.
Choi et al. (2006) (гесперидин тормозил формирование сосудистых структур в
культуре эмбриональных стволовых клеток мышей. Однако, в исследовании K.A.
Reynertson et al. (2006) обнаружено прямое цитотоксическое действие флавоноидоф
на раковые клетки. Ученые доказали, что полифенолы из Myrciaria cauliflora
проявляют цитотоксичность по отношению к злокачественным клеткам линий HT29 и
HCT116. Показано, что полифенольный комплекс из Vitis vinifera L. обладает
селективной направленностью против раковых клеток линии mcf-7, а флавоноид
генистеин из сои вида Soya hispida Moench. ингибирует первичный опухолевый рост
раковых клеток простаты линий PC-3 и RM-9. Хотя с другой стороны, есть данные о
противоположном эффекте, когда то же соединение стимулировало рост
эстрогенчувствительных опухолей, что, вероятно, свидетельствует о схожести
строения и рецепторных структур для этих веществ [2].
Исследования свойств золотого уса и ряда других
растений семейства коммелиновых стали проводиться сравнительно недавно, в
середине XX в. Ученые США и Канады пришли к выводу, что сок каллизии обладает
действием, направленным на замедление формирования раковых клеток в организме.
Но к сожалению научные исследования не закончены, они продолжаются и в
настоящее время. В России исследования свойств золотого уса начались в 1980-х
гг. в Иркутском медицинском институте под руководством профессора Семенова.В
настоящее время лекарственные свойства золотого уса все еще изучаются. В России
этим занимаются ученые кафедры биологии СПбГПУ им. А. И. Герцена. Специалисты
предупреждают, что это растение не является универсальным лекарствам, однако
многие схемы применения препаратов из каллизии уже одобрены и приняты
официальной медициной.
Учеными было доказано, что препараты золотого
уса действительно могут оказывать лечебное действие при многих заболеваниях,
однако возможны и некоторые побочные эффекты, которые чаще всего проявляются у
пациентов с пониженным иммунитетом или предрасположенностью к аллергии на
некоторые биологически активные вещества, которые имеются в золотом усе.
Поэтому всем, кто решил лечиться препаратами, в состав которых входит золотой ус,
настоятельно рекомендуется сначала посоветоваться с врачом.
Лечебный эффект от употребления препаратов
золотого уса обусловлен наличием таких групп биологически активных веществ, как
флавоноиды
Если у организма сильный иммунитет, он, как
правило, самостоятельно справляется с негативными процессами, которые
провоцируют свободные радикалы. Однако зачастую иммунитет бывает ослаблен
инфекционными заболеваниями, стрессами, физическим перенапряжением,
неблагоприятными условиями окружающей среды и др. В этом случае необходимо
использовать специальные препараты, в которых содержатся природные
антиоксиданты. К ним относятся и флавоноиды, которые входят в состав золотого
уса.
Флавоноиды укрепляют стенки капилляров,
участвуют в обменных процессах, связанных с усвоением витамина С, а также
обладают противовоспалительным, успокаивающим, желчегонным и противоопухолевым
действием.
В соке золотого уса учеными были обнаружены два
вещества из группы флавоноидов: кемпферол и кверцетин.
Кемпферол укрепляет стенки кровеносных сосудов и
капилляров и выводит из организма токсины. Это биологические активное вещество
обладает ярко выраженным общеукрепляющим, противовоспалительным и тонизирующим
действием, а также является диуретиком. Кемпферол включают в состав препаратов
для лечения различных заболеваний мочевыделительной системы, аллергии, а также
в состав противовоспалительных средств.
Кверцетин является одним из мощных
антиоксидантов. Помимо того что он предотвращает дальнейшее негативное
воздействие на организм свободных радикалов, кверцетин восстанавливает мембраны
поврежденных ими клеток. Но этим спектр действия кверцетина не исчерпывается. Это
биологически активное вещество обладает противовоспалительным, противоотечным,
спазмолитическим и антигистаминным действием. Как и кемпферол, кверцетин
является диуретиком, а также укрепляет стенки капилляров. Еще одним из свойств
кверцетина является то, что он замедляет процесс старения организма, и в первую
очередь клеток кожи, роговицы и сердечной мышцы. Препараты, в состав которых
входит кверцетин, применяются для лечения бронхиальной астмы и заболеваний
сердечно-сосудистой системы, а также ожогов, обморожений и различных
воспалений. Используется кверцетин и при лечении катаракты. Помимо этого, он
входит в состав препаратов, которые используют для профилактики атеросклероза и
заболеваний суставов, например артроза и артрита. Кверцетин входит в состав косметических
средств, замедляющих старение кожи.[6]
. Другие эффекты флавоноидов
Доказаны также и следующие фармакологические
действия флавоноидов:
Гипохолестеринемическое и антидиабетическое.
Механизм действия по улучшению обмена веществ
биологически активными молекулами флавоноидов изучен не полностью. Выяснено,
что биофлавоноиды обладают способностью стимулировать так называемые
пролифератор - активирующие системы (PPAR) пероксисом клеток, играющие ключевую
роль в регуляции липидного и глюкозного гомеостаза. Пероксисомы - клеточные
органеллы, в которых осуществляются окислительно- восстановительные процессы.
Набор функций пероксисом различается в клетках разных типов. Среди них:
окисление жирных кислот, фотодыхание, разрушение токсичных соединений, синтез
желчных кислот, холестерина,а также эфиросодержащих липидов и т.д. Наряду с
митохондриями пероксисомы являются главными потребителями кислорода в клетке.
Все эти процессы идут с потреблением энергии, то есть глюкозы. Повышение
количества пероксисом в клетках происходит при необходимости нейтрализовать
токсические продукты внутреннего и внешнего происхождения. Активность этих
процессов определяет интенсивность обмена жиров и глюкозы. Кроме того,
флавоноиды нормализуют холестериновый обмен на уровне клеток.
Схема равновесия холестерина в клетке включает в
себя фермент3-окси-3-метилглутарилкоэнзим-А-редуктазу (ОМГ-СоА-редуктазы),
который запускает и ускоряет синтез холестерина в клетке. При сниженном уровне
холестерина фермент активируется, при высоком - блокируется. Флавоноиды
способствуют снижению активности ОМГ-СоА-редуктазы, за счет нормализации
липидного обмена. Поэтому биофлавоноиды не провоцируют синдром отмены и не
вызывают резкого скачка уровня холестерина.[11]
Антиатерослеротическое действие.
Ценным свойством флавоноидов является
способность снижать риск развития атеросклероза и приостанавливать уже
имеющийся процесс. Происходит это за счет комплекса механизмов: нормализации
холестеринового обмена, улучшения углеводного обмена в клетках, приостановления
воспалительного процесса на стенках сосудов и капилляров, стабилизации
холестериновых отложений.
Регуляция активности ферментов.
Наряду с гистидиндекарбоксилазой, флавоноиды
инактивируют сукциноксидазу, холинэстеразу, карбоксилазу, повышают активность ксантиноксидазы
и пролиноксидазы.
В связи с тем, что флавоноиды являются
регуляторами активности ферментов разных классов, агонистами и антагонистами
рецепторов, они обладают исключительно широким спектром фармакологической
активности в плане влияния на обменные процессы в клетках и стабилизации
гомеостаза.
Кровоостанавливающее действие
Кровоостанавливающее действие эмпирически давно
установлено и широко используется в медицине для лечения маточных,
геморроидальных, кишечных и других немассивных кровотечений.
Кровоостанавливающими свойствами обладают препараты горцев перечного и
почечуйного, яснотки, пастушьей сумки, софоры японской и некоторых других
растений.
Антиаллергическое свойство.
Флавоноиды также обладают и антиаллерическими
свойствами. Оказывается, они ингибируют два фермента, которые участвуют в
высвобождении гистамина из тучных клеток - Са2+-АТФазу и цАМФ-фосфодиэстеразу.
В этом плане особенно сильны такие флавоноиды, как кверцетин, рутин, цианидин и
мирицетин. У некоторых флавоноидов (гесперидин, рутин и кверцетин) отмечено
действие предотвращения анафилактического шока.[11]
Заключение
В последние два десятилетия природные
полифенольные соединения привлекают всеобщее внимание исследователей не только
как объект химического изучения, но и в качестве перспективных веществ для
получения биологически активных препаратов и лекарственных средств. Об этом
свидетельствует возросший за последние годы интерес к веществам данной группы
как к источникам капилляроукрепляющих, противовоспалительных, желчегонных,
антисклеротических, противоопухолевых и других препаратов. Фенольным
соединением называется вещество, содержащее в своей молекуле ароматическое
(бензольное) кольцо, которое несет одну или более гидроксильных групп.
Образование фенольных соединений - одна из характерных особенностей
растительной клетки. Широкое изучение фенольных соединений показало, что
вещества данной группы обладают разносторонним действием на организмы животных
и человека. Ранее других было обнаружено их действие на стенки кровеносных
капилляров - Р-витаминоподобное действие]. Другими важными свойст-вами ряда
флавоноидов является их антиаггрегационная способность, противовоспалительное и
жаропонижающее действие. Для ряда флавоноидных соединений показана
антимикробная и противовирусная активность. Представители группы изофлавоноидов
обладают эстрогенным действием. Флавоноиды могут выступать в качестве
радиопротекторов и как радиопотенциирующие средства. Флавоноиды оказывают
положительное влияние на метаболизм печени, усиливая желчеотделение и повышая
детоксикационную функцию. Показана анаболизирующая активность некоторых
флавоноидных соединений, сахароснижающие свойства, нейротропное, адаптогенно,
антиатеросклеротическое действия. Одним из важных свойств производных пирона и
других полифенольных соединений является их противоопухолевое действие. В
настоящее время антиоксидантной активности флавоноидов уделяется огромное
внимание, как возможному механизму, через который реализуются биологические
эффекты данной группы соединений. Имеется большое количество работ, указывающих
на взаимосвязь адаптогенных, иммуномодулирующих, противоопухолевых и ряда
других свойств фенолов с их антиоксидантной активностью.
Существует множество лекарственных препаратов,
содержащих флавоноиды: Гепабене, Легалон, Карсил, Гепатофальк-планта, Силибор.
Фламин, Хофитол, Катерген (цианиданол), ЛИВ-52 (гепалив), Тыквеол, Леспефлан,
Кардиовален, Хелепин, Флакозид, Детралекс, Веноплант; а также БАД: «Уролизин»,
«Биосед», «Капилар», «Атероклефит», «Золотой ус», «Сосудистый доктор»,
«Желудочный доктор», «Имунофит», «Масло целебное с золотым корнем», «Биофеном
1», «Биофеном 3», «Биолан-жизнь», «Пеан - ресурс», «Артум», «Куперс».
«Олексин», «Детрикан» и др.
Следовательно, можно считать, что поставленные
перед нами задачи в начале работы можно считать выполненными. Мы разобрались,
что же такое флавоноиды, для чего они нам необходимы,какими действиями обладают
и каково состояние исследований этих веществ на сегодняшний день.
Литература
1. Муравьева Д.А., Самылина
И.А., Яковлев Г.П. Фармакогнозия. М.: Медицина, 2002.
2. Кабиев О.К., Балмуханов
С.Б. Природные фенолы - перспективный класс противоопухолевых и
радиопотенцирующих соединений. Медицина, М., 1999.
. Яковлев Г.П., Блинова К.Ф.
Лекарственное растительное сырье. Фармакогнозия: Учебное пособие. - СПб.:
СпецЛит, 2004.
. Максютина Н.П., Литвиненко
В.И. Методы выделения и исследования флавоноидных соединений // Фенольные
соединения и их биологические функции. М., 2001.
. Блинова К.Ф. Растения для
нас - «Учебная книга»
. Коноплева М.М.
Фармокогнозия: природные биологически активные вещества
. Изучение биохимических
основ защитного действия флавоноидов при экспериментальном поражении печени //
Отчет НИР. (Соавт. Василенко Ю.К., Парфентьева Е.П., Саджая Л.А., Скульте И.В.,
Мазурина М.В., Паукова Е. О).
. Шульпекова О.В. Флавоноиды
расторопши пятнистой в лечении заболеваний печени. // Российский Медицинский
Журнал, Том 12 № 5, 2004.
. Гершанович М.Л., Панкин
М.Д. Симптоматическое лечение при злокачественных новообразованиях. Москва: Медицина,
2000.
. Рогинский В.А. Фенольные
антиоксиданты: реакционная способность и эффективность / В.А. Рогинский - М.:
Наука, 2002.
. П.Б. Цыдендамбаев, Б.С.
Хышиктуев, С.М. Николаев «Биологические эффекты флавоноидов» Бюллетень ВСНЦ СО
РАМН, 2006, 6 (52)
12. <http://www.ilonacat.ru/zbk450.shtml>
. http://zdravoe.com/
. <http://www.herbarius.info>
. <http://www.chimavtomatika.ru/>
. <http://msk.visionbuy.com>
. <http://www.pudmeda.com>
. <http://kovalyova.taba.ru>
. <http://fictionbook.ru>
. <http://www.dnaekb.ru>
. <http://www.flicketyfit.com>