Гидродинамические характеристики стандартов полистиролсульфоната в растворах различной ионной силы
Санкт-Петербургский
государственный университет
Физический
факультет
Кафедра
физики полимеров
Гидродинамические
характеристики стандартов полистиролсульфоната в растворах различной ионной
силы
Выпускная
квалификационная работа
на
соискание академической степени магистра физики
Программа 403/11 Физика полимеров и
жидких кристаллов
Выполнена студентом
Смирновым Артемом
Михайловичем
Научные
руководители:
кандидат
физ.-мат. наук Зайцева И.И.
доктор
физ.-мат. наук Павлов Г.М.
Рецензент:
доцент,
кандидат физ.-мат. наук Мельников А.Б.
Санкт-Петербург
год
Введение
Молекулярные свойства полимеров определяют
физико-химические характеристики материалов, изготовленных на их основе.
Конформация и размеры молекул ДНК (дезоксирибонуклеиновой кислоты), РНК
(рибонуклеиновой кислоты) и белков оказывают прямое влияние на способность этих
молекул выполнять свои биологические функции. В связи с этим, изучение
молекулярных свойств полимеров имеет принципиальное значение для решения
прикладных и фундаментальных задач физикохимии высокомолекулярных соединений,
биофизики, химии, фармакологии и др.
Важнейшее свойство полимерных молекул - их
способность сворачиваться, изменять свою конформацию от палочкообразной до
клубковой при увеличении длины полимерной цепи, определяется их равновесной
жесткостью.
Для определения конформационных характеристик
полимерных цепей, к которым в первую очередь относится их равновесная
жесткость, разработан ряд физических методов, основанных на измерении
поступательного и вращательного трения макромолекул. К числу этих методов
следует отнести вискозиметрию, седиментацию и изотермическую поступательную
диффузию, динамическое рассеяние света, электрическое и динамическое двойное
лучепреломление и ряд других.
Целью настоящей работы было исследование
гидродинамических свойств узкодисперсных образцов полистирол сульфоната в
широких интервалах контурных длин и ионных сил растворов.
Глава
1. Теоретическо-литературный обзор
1.1
Основы статистики линейных полимерных цепей
Полимерные молекулы в основном являются цепями
атомов, соединенных простыми (единичными) связями одинаковой длины ℓ и
образующих друг с другом валентный угол и. Тепловое движение составляющих
полимерную цепь атомов, проявляющееся во вращении их вокруг направления
валентных связей, должно приводить к значительной свернутости цепи.
Клубкообразная структура не является единственно возможной для макромолекул. В
определенных случаях силы, действующие между соседними атомами цепи, столь
велики, что тепловое движение не может привести к изгибанию и скручиванию цепи.
При этом макромолекула имеет палочкообразную конформацию. Существенную роль в
стабилизации такой конформации играют водородные связи, действующие между
несоседними атомами цепи и приводящие к образованию внутримолекулярной структуры.
В других случаях макромолекула принимает форму жесткой глобулы, имеющей
приблизительно сферическую форму.
1.1.1 Идеальная
полимерная цепь
Модель идеальной макромолекулы играет в физике
полимеров такую же роль, как представление об идеальном газе в обычной
молекулярной физике. Эта модель представляет собой цепочку из бестелесных
звеньев; каждое из звеньев идеальной цепи соединено с двумя ближайшими по цепи
соседями, но не взаимодействует ни с молекулами растворителя, ни с другими
звеньями этой же или других макромолекул. Так же как существует много идеальных
газов (одноатомный, двухатомный и т.д. - важно лишь, чтобы молекулы не
взаимодействовали друг с другом), так есть и целый ряд моделей идеальных цепей;
они различаются структурой звеньев и устройством связей между ближайшими
соседями, но «идеальность» во всех случаях состоит в отсутствии объемных
взаимодействий. Круг реальных условий, при которых молекулы ведут себя как
идеальные, не очень широк - в основной это разбавленные растворы полимеров в так
называемых θ-растворителях, а
также полимерные расплавы. Тем не менее, идеальные модели очень полезны, так
как позволяют составить правильное представление о характере теплового движения
макромолекул, другими словами - об энтропийных свойствах полимерного вещества.
1.1.2 Свободно-сочлененная
цепь
Для описания конформационных свойств полимерных
молекул важное значение имеет модель свободно-сочлененной цепи, введенная в
рассмотрение и разработанная Куном и Марком. В этой модели реальная полимерная
цепь заменяется эквивалентной, состоящей из N
прямолинейных сегментов длиной A,
пространственные ориентации которых взаимно независимы. Полная длина
эквивалентной цепи L
принимается
равной длине полностью вытянутой (без деформации валентных углов) реальной цепи
(контурная длина):
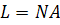 (1)
(1)
Вторым необходимым условием, которому должна
удовлетворять модельная эквивалентная цепь, является совпадение ее начала и
конца с началом и концом реальной цепи при любой конформации последней. Таким
образом, длина вектора h,
соединяющего концы цепи, имеет одно и то же значение для реальной и модельной
цепей. Величина h
служит важнейшей характеристикой конформационных свойств полимерной цепи.
Простейшая характеристика пространственного размера полимерной цепи - среднеквадратичной
расстояние между ее концами; сравнение размера с контурной длиной характеризует
степень свернутости цепи в пространстве.
Гибкость полимерной цепи ведет к тому, что
макромолекулы никогда не имеют прямолинейной формы - напротив, любая достаточно
длинная цепь, извиваясь, в любой момент имеет форму случайного запутанного
клубка. Размер клубка в пространстве не характеризуется контурной длиной цепи,
различие этих величин определяется тем, насколько свернута цепь. Именно поэтому
необходимо обсуждать вопрос о размерах клубкообразных конформаций цепей. Для
характеристики степени гибкости макромолекулы можно наряду с персистентной
длиной использовать величину сегмента Куна.
Поскольку ориентации сегментов свободно
сочлененной цепи взаимно независимы, они могут являться объектом применения
статистического метода.
Развитие статистики полимерных цепей на основе
свободно-сочлененной модели привело к установлению важной закономерности -
гауссова распределения расстояний h
в ансамбле длинных цепных молекул (каждая длиной L):
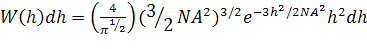 (2)
(2)
Здесь W(h)dh
- вероятность того, что для произвольно выбранной из ансамбля цепи (состоящей
из N
сегментов длиной A)
расстояние между ее концами лежит в пределах от h
до h+dh.
Цепи, удовлетворяющие этому распределению, называются гауссовыми. Из этой
формулы может быть получен любой из моментов распределения W(h).В
частности, для среднего квадрата h получается величина
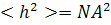 (3)
(3)
Отсюда следует, что средний квадрат расстояния
между концами гауссовой цепи равен
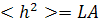 (4)
(4)
т.е. пропорционален ее контурной длине L.
Это свойство является основным для гауссовых цепей. Из последнего равенства
следует, что линейные статистические размеры гауссовой цепи (характеризуемые
величиной <h2>1/2)
при заданной контурной длине L
пропорциональны корню квадратному из длины сегмента Куна A.
Длина статистического сегмента служит мерой равновесной жесткости (гибкости)
полимерной цепи.
1.2.3
Гибкость полимерной цепи
Любая полимерная макромолекула обладает
гибкостью, но механизм гибкости у разных полимеров разный.
Гибкость свободно-сочлененной цепи обусловлена
шарнирными сочленениями между жесткими сегментами. Можно сказать, что вся
гибкость сосредоточена в точках сочленений. Этот так называемый
свободно-сочлененный механизм гибкости наиболее прост для описания, но
химически его реализовать трудно, и встречается он редко. Тем не менее,
существенной гибкостью обладают все достаточно длинные полимерные цепи, и
причина этого заключена как раз в большой их длине.
Допустим, что абсолютному минимуму энергии
соответствует прямолинейная конформация цепи и что все звенья и связи по своей
химической природе очень жесткие, так что тепловая энергия возбуждения
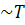
приводит лишь к малой деформации их
стереохимической структуры. При малых деформациях атомный каркас молекулы можно
рассматривать как классическую упругую конструкцию, т.е. для полимера - как
упругую однородную нить, подчиняющуюся при деформации закону Гука.
Такую модель полимера цепи называют
персистентной или червеобразной моделью.
1.2.4
Персистентная (червеобразная) модель Порода
Для описания конформационных свойств
жесткоцепных молекул наиболее подходящей является модель персистентной, или
червеобразной цепи Кратки-Порода, в которой в отличие от свободно-сочлененной
цепи Куна учитывается ориентационное близкодействие элементов, составляющих
цепь. В основе модели Порода (так же как и в модели Куна) лежит цепь длиной L,
состоящая из n
прямолинейных участков длиной ΔL,
так что L=nΔL.
Однако в отличие от свободно-сочлененной цепи пространственные ориентации
соседних элементов здесь не вполне взаимно независимы - направление первого
элемента в определенной мере передается по цепи. Корреляция между элементами
выражается в том, что среднее (по всем конформациям) значение 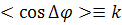 угла
между соседними элементами не равно нулю и одинаково для всех элементов цепи (в
случае свободно-сочлененной цепи k=0).
Таким образом, совокупность величин ΔL
и k является
мерой ориентационного близкодействия, т.е. корреляции для персистенции в цепи.
В итоге, угол
угла
между соседними элементами не равно нулю и одинаково для всех элементов цепи (в
случае свободно-сочлененной цепи k=0).
Таким образом, совокупность величин ΔL
и k является
мерой ориентационного близкодействия, т.е. корреляции для персистенции в цепи.
В итоге, угол 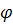 между элементами 1
и n определяется
соотношением
между элементами 1
и n определяется
соотношением
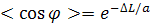 (5)
(5)
здесь a
- длина персистенции.
Если, оставляя постоянными значения L
и a, перейти к
пределу ΔL→0
(тогда 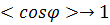 ),
то изломанная персистентная цепь превращается в непрерывную червеобразную цепь,
которая определяется соотношением
),
то изломанная персистентная цепь превращается в непрерывную червеобразную цепь,
которая определяется соотношением
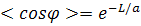 (6)
(6)
Таким образом, кривизна червеобразной кривой
одинакова во всех ее точках, определяясь величиной 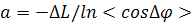 ,
тогда как направления искривлений в этих точках хаотичны. Иными словами,
червеобразную цепь можно охарактеризовать как пространственную линию постоянной
кривизны.
,
тогда как направления искривлений в этих точках хаотичны. Иными словами,
червеобразную цепь можно охарактеризовать как пространственную линию постоянной
кривизны.
1.2.5
Влияние эффектов исключенного объема
По сравнению с идеальной макромолекулой,
свойства реальных полимерных систем с объемными взаимодействиями намного
разнообразнее. Именно они представляют наибольший интерес и с теоретической, и
с практической точки зрения. Однако, как правило, прямому теоретическому
исследованию из первых принципов объемные эффекты не поддаются. В этой ситуации,
как всегда в теоретической физике, решающую роль приобретает выбор удачных
моделей исследуемого объекта и разработка соответствующих модельных
представлений.
Конформационные свойства цепных молекул,
рассмотренные выше, обсуждались в предположении, что взаимодействия между
элементами цепи, определяющие ее равновесную жесткость, имеют характер
близкодействия, т.е. осуществляются между соседними или близкими элементами в
цепи. Это подразумевается самим представлением о существовании персистенции
цепи.
Однако, поскольку всякая реальная цепная
молекула имеет большую или меньшую гибкость, при ее тепловом движении всегда
возможны случайные сближения атомов и групп, значительно удаленных друг от
друга по цепи. При таких сближениях неизбежно возникновение взаимодействия
между сблизившимися элементами цепи, имеющего характер их взаимного
отталкивания, тем большего, чем больший эффективный объем занимает
взаимодействующая пара элементов («исключенный объем»). Эти взаимодействия,
являющиеся взаимодействиями дальнего порядка, принято называть эффектами
исключенного объема, поскольку в их основе лежит невозможность для двух
элементов цепи одновременно занимать в пространстве один и тот же элемент
объема. Эффекты исключенного объема возмущают конформацию клубкообразной молекулы,
приводя (в силу возникающих отталкиваний) к увеличению средних расстояний между
ее элементами, в том числе и к увеличению 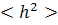 и
и
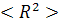 (радиус
инерции цепи). Количественно эти возмущения характеризуют коэффициентами αh
и αR
линейного увеличения размеров молекулярного клубка, определяемыми соотношениями
(радиус
инерции цепи). Количественно эти возмущения характеризуют коэффициентами αh
и αR
линейного увеличения размеров молекулярного клубка, определяемыми соотношениями
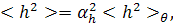 (7)
(7)
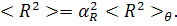 (8)
(8)
Здесь 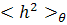 и
и
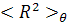 -
средний квадрат расстояния между концами цепи и ее радиус инерции в отсутствие
объемных эффектов;
-
средний квадрат расстояния между концами цепи и ее радиус инерции в отсутствие
объемных эффектов; 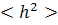 и
и 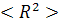 -
те же величины, возмущенные объемными эффектами.
-
те же величины, возмущенные объемными эффектами.
Конформации реальных полимерных молекул
изучаются в разбавленных растворах, где объемные эффекты существенно зависят от
взаимодействий молекул полимера с молекулами растворителя и для одного и того
же полимера могут быть весьма различны в различных растворителях. Подбором
достаточно «плохого» растворителя и соответствующей температуры («θ-температуры»)
влияние конечного объема мономерной единицы можно скомпенсировать взаимным притяжением
единиц цепи. В этих условиях эффекты исключенного объема отсутствуют, в
равенствах (7,8) коэффициенты 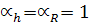 . С улучшением
термодинамического качества растворителя и соответствующим усилением
взаимодействий полимер-растворитель притяжение между элементами цепи не в
состоянии компенсировать их отталкивания, эффект исключенного объема
увеличивается и α становится
больше единицы. Причем возмущенные размеры молекул
. С улучшением
термодинамического качества растворителя и соответствующим усилением
взаимодействий полимер-растворитель притяжение между элементами цепи не в
состоянии компенсировать их отталкивания, эффект исключенного объема
увеличивается и α становится
больше единицы. Причем возмущенные размеры молекул 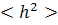 и
и
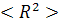 растут
быстрее, чем пропорционально длине цепи L.
В итоге получаем в грубом приближении
растут
быстрее, чем пропорционально длине цепи L.
В итоге получаем в грубом приближении
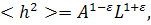 (9)
(9)
где е > 0.
Также стоит отметить, что при характеристике
конформационных свойств полимерных молекул в разбавленных растворах учет
влияния объемных эффектов имеет важнейшее значение, так как размеры этих
молекул в хороших растворителях могут в несколько раз превосходить их
невозмущенные размеры. Поэтому количественное определение параметров
равновесной жесткости цепей неизбежно связано с исключением влияния объемных
эффектов путем использования θ-растворителей
или применением процедур экстраполяции экспериментальных данных на область
низких молекулярных весов.
Стоит также отметить, что влияние эффектов
исключенного объема на конфигурацию молекул жесткоцепных полимеров значительно
слабее, чем в случае гибкоцепных полимеров. Это исходит из того факта, что
меньшая свернутость цепи жесткоцепной молекулы в растворе естественно должна
уменьшать вероятность контактов между ее элементами, удаленными по цепи.
1.2
Полиэлектролиты
Макромолекулы приобретают ряд характерных
электрических, конфигурационных и гидродинамических свойств, если мономерные
звенья полимерной цепи содержат ионногенные группы. Такие полимеры называются полиэлектролитами.
Макромолекула полиэлектролита в растворе состоит из полииона, окруженного
эквивалентным количеством противоионов (малых ионов с зарядами противоположного
знака). Размеры полииона на несколько порядков больше, чем противоионов.
Классификация полиэлектролитов
Полиэлектролиты делятся на поликислоты,
полиоснования и полиамфолиты.
Классические представители поликислот -
полиакриловая и полиметакриловая кислоты. В водном растворе благодаря ионизации
карбоксильных групп между мономерными звеньями возникают силы
электростатического отталкивания. Они будут тем сильнее, чем выше степень
ионизации, зависящая от pH
среды. Степень ионизации может быть повышена при превращении поликислоты в
соль, например при обработке поликислоты щелочью. Степень ионизации полученных
таким образом полимерных солей значительно выше, чем исходных поликислот. В
кислой области pH
карбоксилы остаются практически неионизованными, и поведение макромолекул ничем
не отличается от поведения макромолекул обычного линейного полимера. Однако в
нейтральной или щелочной области появление множества одноименно заряженных
групп в молекуле (карбоксилатных ионов, -COO-)
и соответствующих сил электростатического отталкивания приводит к развертыванию
макромолекулярных цепей и к сильному увеличению размеров клубков; при этом
возникают своеобразные концентрационные эффекты, проявляющиеся при измерениях
вязкости, седиментации и диффузии.
К рассматриваемому классу поликислот относятся
также многие полимеры биологического происхождения. Здесь стоит назвать в
первую очередь нуклеиновые кислоты - ДНК и РНК, передающие генетическую
информацию.
Другой класс полиэлектролитов - полиоснования.
Конфигурационные свойства полиоснований аналогичны свойствам поликислот. В
частности, полиоснования, как и поликислоты, сильнее ионизованы в солевой
форме.
Сочетание кислотных и основных групп в одной
цепи приводит к образованию полиамфолитов, составляющих третий класс
полиэлектролитов. Для каждого полиамфолита существует определенное, зависящее
от его состава, значение pH,
при котором количества положительных и отрицательных зарядов в цепи равны.
Иными словами, суммарный заряд полиамфолита в этой изоэлектрической точке (ИЭТ)
равен нулю. При pH
ниже ИЭТ в цепи начинают доминировать положительные заряды. При достаточно
низком pH ионизация
всех кислотных групп оказывается подавленной и полиамфолит превращается в
полиоснование. Наоборот, по мере повышения pH
над ИЭТ полиамфолит постепенно превращается в поликислоту. Полиамфолиты играют
огромную роль в природе: все белки относятся к полиамфолитам.
Размеры полиэлектролитов
Размеры полииона в водных растворах сильно
зависят от наличия кулоновских взаимодействий (отталкивания одноименно
заряженных групп в макромолекуле и притяжения контрионов к полииону). Благодаря
электростатическому отталкиванию между одноименно заряженными ионногенными
группами макромолекула полиэлектролита стремиться развернуться и приобрести
более асимметричную форму по сравнению с формой статистического клубка,
характерной для незаряженных цепей. Поэтому в растворах полиионы имеют большие
размеры и асимметрию.
Также размеры полииона сильно зависят от
линейной плотности заряда. Разворачивание цепи проявляется в возрастании
приведенной вязкости при уменьшении концентрации (полиэлектролитный эффект).
Это объясняется тем, что при разбавлении растворов полиэлектролитов
увеличивается объем, в котором распределяются контрионы, экранирующие
кулоновское отталкивание между фиксированными зарядами полииона, вследствие
чего возрастает их отталкивание и происходит развертывание полииона.
Конформация полиэлектролита определяется также
наличием в растворе низкомолекулярных электролитов, например солей. Наличие
таковых приводит к экранированию зарядов полииона. При значительных
концентрациях (например, больше 0.1 М), вклад кулоновских взаимодействий
существенно ослабевает, и размеры цепей сопоставимы с размерами неоинногенных
цепей той же природы.
Линейная плотность заряда,
конденсация контрионов, полиэлектролитное набухание
Полиэлектролиты обладают способностью
специфически связывать контрионы (образование ионных пар между заряженными
группами полиэлектролита и контрионами, ионных тройников и более сложных
комплексов). Теория Дебая-Хюккеля, строго говоря, неприменима к
полиэлектролитам. Дело в том, что при не очень малых степенях ионизации
электростатическое поле вокруг молекулы полиэлектролиты велико, его энергия в
несколько раз больше тепловой.
П. Флори построил теорию на основе объемных
эффектов [8]. Электростатическое отталкивание приводит к набуханию клубка,
зависящему от ионной силы. Флори предполагал, что клубок вместе с окружающим
его растворителем электрически нейтрален. Расчет показывает, что
электростатические взаимодействия не могут превратить клубок в вытянутую
молекулу, происходит лишь набухание.
О. Б. Птицын развил более строгую теорию [9].
Основное предположение - из-за большего экранирующего действия контрионов
заряженные группы макромолекулы, расположенные далеко друг от друга по цепи,
взаимодействуют лишь при случайном сближении в результате флуктуационного изгибания
цепи. Также, из этой теории следует, что конформационные свойства заряженных
макромолекул промежуточны между свойствами ненабухших клубков и жестких
стержней.
Макромолекула связывает контрионы. Поэтому
полиион при взаимодействии с другими полиионами ведет себя как нейтральная
система. Контрионы могут специфически связываться ионизованными группами
полиэлектролита. Следует отличать это связывание, сводящееся к образованию
солевых связей в фиксированных точках макромолекулы, от неспецифического связывания
- образования ионной атмосферы. В солевой связи контрион находится на
значительно меньшем расстоянии от полииона, чем то, на которое могут
приблизиться подвижные контрионы.
В растворе достаточно сильно заряженных
полиэлектролитов часть контрионов удерживается в непосредственной близости к
полимерным цепям, эффективно нейтрализуя их заряд - это конденсация контрионов.
Для слабо заряженных полиэлектролитов выраженная
конденсация происходит только в плохом растворителе, где блобы (определение
блоба исходит из того условия, что внутри блоба цепочка остается невозмущенной)
глобулярны и является лавинообразным процессом, приводящим к практически
полному осаждению контрионов на молекулах.
Далее следует рассмотреть исследованное как
экспериментально, так и теоретически так называемое полиэлектролитное
набухание. Причина полиэлектролитного набухания - электростатическое
отталкивание одноименно заряженных звеньев цепи, приводящее к развертыванию
клубков и увеличению их линейных размеров. Поскольку о размерах макромолекул
можно судить по характеристической вязкости [η],
пропорциональной объему клубков, первые оценки полиэлектролитного набухания
были произведены по измерениям [η]
в зависимости от степени ионизации. Было показано, в частности, что при полной
ионизации полиметакриловой кислоты [η]
может возрасти на два порядка, чему соответствует увеличение линейных размеров
клубков в 5-6 раз. Однако при этом сразу возникает вопрос, в какой степени
полиэлектролитное набухание можно считать изотропным?
Одна из первых теорий эффекта полиэлектролитного
набухания принадлежит А. Качальскому и Лифсону [10]. Они полагали, что функция
распределения расстояний между концами заряженной цепи имеет вид
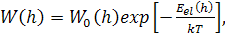 (10)
(10)
полимер раствор полистиролсульфонат
ионный
где индекс «0» соответствует незаряженной цепи,
а 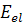 -
электростатическая энергия цепи, вычисляемая как сумма энергий отталкивания
-
электростатическая энергия цепи, вычисляемая как сумма энергий отталкивания 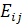 всех
пар заряженных звеньев. В первоначальном варианте теории, принадлежащем
Качальскому, Кюнцле и В. Куну [11], экранирование электростатических
взаимодействий, обусловленное образованием дебай-хюккелевской атмосферы
противоионов вокруг заряженных групп цепи, не принималось во внимание.
Основанием для подобного пренебрежения было следующее неправильное (как было
установлено позже) допущение. Плотность атмосферы противоионов, характеризуемая
параметром χ в теории
Дебая-Хюккеля, определяется ионной силой раствора μ:
всех
пар заряженных звеньев. В первоначальном варианте теории, принадлежащем
Качальскому, Кюнцле и В. Куну [11], экранирование электростатических
взаимодействий, обусловленное образованием дебай-хюккелевской атмосферы
противоионов вокруг заряженных групп цепи, не принималось во внимание.
Основанием для подобного пренебрежения было следующее неправильное (как было
установлено позже) допущение. Плотность атмосферы противоионов, характеризуемая
параметром χ в теории
Дебая-Хюккеля, определяется ионной силой раствора μ:
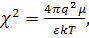 (11)
(11)
где
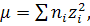 (12)
(12)
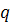 - заряд электрона,
- заряд электрона,
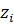 -
валентность иона сорта
-
валентность иона сорта 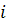 ,
, 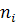 -
число таких ионов в 1 см3, е - диэлектрическая проницаемость раствора.
-
число таких ионов в 1 см3, е - диэлектрическая проницаемость раствора.
Если потенциальная энергия кулонова
взаимодействия двух полностью изолированных ионов равна
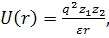 (13)
(13)
то в среде, содержащей ионы противоположного
знака (противоионы), благодаря образованию облака противоионов вокруг каждого
иона энергия взаимодействия ослабевает и определяется выражением
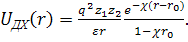 (14)
(14)
Здесь 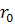 -
сумма вандерваальсовых радиусов ионов. Параметр ч имеет геометрический смысл
обратной величины эффективного радиуса ионной атмосферы, определяя расстояние
от иона, за пределом которого осуществляется полное экранирование
взаимодействий.
-
сумма вандерваальсовых радиусов ионов. Параметр ч имеет геометрический смысл
обратной величины эффективного радиуса ионной атмосферы, определяя расстояние
от иона, за пределом которого осуществляется полное экранирование
взаимодействий.
Качальский, Кюнцле и Кун предположили, что при
очень большом разбавлении множитель Дебая-Хюккеля 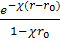 можно
принять равным единице, так как противоионы равномерно распределены в объеме
раствора, тогда как заряды сосредоточены в малых дискретных областях, занятых
макромолекулами. При этом экранирование действительно практически не должно
иметь места, и при расчете
можно
принять равным единице, так как противоионы равномерно распределены в объеме
раствора, тогда как заряды сосредоточены в малых дискретных областях, занятых
макромолекулами. При этом экранирование действительно практически не должно
иметь места, и при расчете 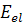 можно пользоваться
кулоновым потенциалом. Полагая, что W0(h)
- гауссова функция, они получили:
можно пользоваться
кулоновым потенциалом. Полагая, что W0(h)
- гауссова функция, они получили:
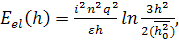 (15)
(15)
где n
- число ионногенных групп в макромолекуле, т.е. в случае гомополимеров степень
полимеризации, а i
- степень ионизации, определяемая значением pH
среды.
Это соотношение предсказывает анизотропное
развертывание цепочек с переходом к практически полностью вытянутым
конфигурациям. Предположение χ=0,
сделанное при выводе этого уравнения, оказалось неверным потому, что на самом
деле противоионы не распределены равномерно по объему раствора, а удерживаются
электростатическим полем клубка. Кроме того, следует учитывать хотя и слабую,
но все же конечную диссоциацию воды.
Электростатический вклад в
равновесную жесткость [2]
В теории полиэлектролитов рассматриваются две
характеристические длины - радиус Бьеррума 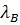 и
радиус экранирования Дебая-Хюккеля
и
радиус экранирования Дебая-Хюккеля 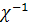 .
Радиус Бьеррума
.
Радиус Бьеррума 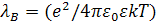 характеризует
экранирующее действие растворителя. Радиус экранирования Дебая - Хюккеля
характеризует
экранирующее действие растворителя. Радиус экранирования Дебая - Хюккеля 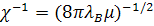 -
расстояние, на котором распространяется действие электрического поля отдельного
заряда, помещенного в среду, содержащую другие заряды. Здесь
-
расстояние, на котором распространяется действие электрического поля отдельного
заряда, помещенного в среду, содержащую другие заряды. Здесь 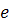 -
элементарный заряд,
-
элементарный заряд, 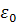 - электрическая
постоянная,
- электрическая
постоянная, 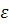 - диэлектрическая
проницаемость среды,
- диэлектрическая
проницаемость среды, 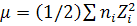 - ионная сила
раствора,
- ионная сила
раствора, 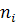 - число -тых ионов
в единице объема,
- число -тых ионов
в единице объема, 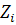 - заряд
- заряд 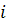 -того
иона в единицах
-того
иона в единицах 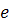 .
.
Заряды, находящиеся на расстоянии 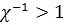 вдоль
цепи, вызывают дополнительное электростатическое близкодействие, которое
приводит к повышению жесткости цепи на величину
вдоль
цепи, вызывают дополнительное электростатическое близкодействие, которое
приводит к повышению жесткости цепи на величину 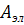 .
Последняя зависит от линейной плотности заряда и ионной силы раствора.
.
Последняя зависит от линейной плотности заряда и ионной силы раствора.
Глава
2. Вискозиметрия и поступательное трение цепных молекул
2.1 Гидродинамика
растворов полимеров, взаимодействия в цепи
При движении полимерной молекулы в растворителе
сопротивление, испытываемое ею со стороны последнего, зависит от размеров и
формы молекулы, поэтому изучение этого сопротивления может дать информацию о
конформационных характеристиках полимерной цепи. В качестве основных явлений,
используемых с этой целью, обычно служит поступательное и вращательное трение
макромолекул, проявляющееся при диффузии, седиментации и вискозиметрии
полимерных растворов. При этом для количественной интерпретации экспериментальных
данных на молекулярном уровне применяются теории, связывающие конформационные
характеристики молекул с их гидродинамическими свойствами, изучаемыми в
растворе. В каждой теории исследуемая полимерная молекула моделируется телом
той или иной конфигурации, поступательное и вращательное трение которого в
растворителе описывается с применением законов гидродинамики макроскопических
тел в вязкой среде.
Строгое решение гидродинамических задач о
поступательном и вращательном движении было получено лишь для модели сплошного
шара и эллипсоида вращения (сфероида). Что касается жесткоцепных полимеров,
моделируемых червеобразной цепью, асимптотическим пределом которой при L/A→0
является прямая палочка, то в этих предельных условиях вытянутый эллипсоид
вращения может служить довольно хорошей моделью для описания гидродинамических
свойств жесткоцепных молекул. Таким образом, основные уравнения теории
поступательного и вращательного трения эллипсоидов вращения имеют
непосредственное отношение к гидродинамическим свойствам жесткоцепных
макромолекул.
2.1.1
Поступательное трение
Количественной характеристикой трения при
поступательном движении тела в окружающей его жидкости является коэффициент
поступательного трения 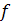 , определяемый
выражением
, определяемый
выражением
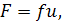 (16)
(16)
где 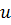 -
скорость движения теля, вызванного действием силы
-
скорость движения теля, вызванного действием силы 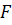 .
Направление
.
Направление 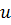 совпадает с
направлением
совпадает с
направлением 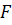
Строгое решение уравнений гидродинамики
Навье-Стокса для простейшего случая движения шара в вязкой жидкости приводит к
формуле
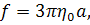 (17)
(17)
где 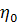 -
коэффициент вязкости окружающей жидкости;
-
коэффициент вязкости окружающей жидкости; 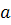 -
диаметр шара.
-
диаметр шара.
Это выражение получено при введении ряда
предположений, основными из которых являются отсутствие скольжения на границе
сферической частицы и окружающей жидкости, достаточно большие размеры частиц,
чтобы окружающую жидкость (растворитель) можно было рассматривать как сплошную
среду, отсутствие взаимодействия между частицами.
2.1.2 Вращательное
трение
Вращательное трение сферического тела в вязкой
среде с позиции классическое гидродинамики было изучено еще Стоксом,
показавшим, что при вращении сплошного шара вокруг оси, проходящей через центр,
с угловой скоростью 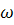 в вязкой жидкости,
он испытывает силы вращательного трения, момент которых
в вязкой жидкости,
он испытывает силы вращательного трения, момент которых 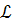 пропорционален
пропорционален
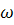 :
:
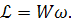 (18)
(18)
Коэффициент пропорциональности W
- коэффициент вращательного трения шара. Он пропорционален объему шара V
и вязкости растворителя η0,
согласно равенству
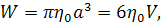 (19)
(19)
где a
- диаметр шара.
Для вытянутых эллипсоидов вращения (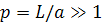 )
)
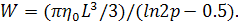 (20)
(20)
2.1.3
Основные понятия, характеристическая вязкость. Вискозиметрия полиэлектролитов
Характеристическая вязкость является одной из
самых широко используемых молекулярно-гидродинамических характеристик
полимеров. Это объясняется ее информативностью, а также сравнительной простотой
и доступностью метода.
Характеристическая вязкость раствора
высокомолекулярного вещества [η]
имеет размерность удельного объема и служит мерой дополнительных потерь
энергии, связанных с вращением макромолекул в потоке.
Внутреннее трение или вязкость всякой жидкости
проявляется в тех случаях, когда она находится в состоянии потока с отличным от
нуля градиентом скорости. Простейший пример такого потока - ламинарный поток с
постоянным градиентом скорости 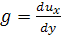 , направление
которого нормально направлению скорости. Скорость жидкости при этом
определяется выражениями
, направление
которого нормально направлению скорости. Скорость жидкости при этом
определяется выражениями
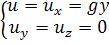 (21)
(21)
Чем больше внутреннее трение в жидкости, тем
большее напряжение сдвига τ
нужно приложить, чтобы поддерживать поток с заданным градиентом скорости 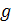 .
Последнее выражается формулой Ньютона:
.
Последнее выражается формулой Ньютона:
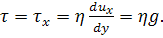 (22)
(22)
Коэффициент пропорциональности η
называют коэффициентом вязкости или просто вязкостью жидкости. Жидкости, для
которых η
не зависит от τ, называют
ньютоновыми.
Определение характеристической вязкости вытекает
из выражения
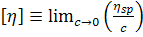 (23)
(23)
где 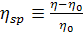 -
удельная вязкость раствора.
-
удельная вязкость раствора.
Можно также утверждать, что независимо от
модельных свойств частиц (макромолекул), характеристическая вязкость раствора
во всех случаях является мерой потерь энергии, вызванных вращением частиц в
среде растворителя. Именно поэтому она связана с вращательной подвижностью
частицы, а также пропорциональна удельному объему частицы в растворе.
Более или менее строгие теории вязкости
растворов цепных молекул (Кирквуда - Райзмана, Зимма) приводят при достаточно
большом числе сегментов в макромолекуле к совпадающему результату - соотношению
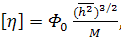 (24)
(24)
со значением коэффициента 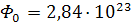 1/моль.
1/моль.
Для гауссовых клубков 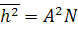 и
последнее уравнение переходит в [η]=KηMa
с
a=0.5. Такая
зависимость характеристической вязкости
и
последнее уравнение переходит в [η]=KηMa
с
a=0.5. Такая
зависимость характеристической вязкости 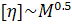 действительно
наблюдается в идеальных растворителях.
действительно
наблюдается в идеальных растворителях.
2.1.4
Теория вращательного трения для моделей червеобразного ожерелья и
персистентного цилиндра
Червеобразное ожерелье
Вращательное трение червеобразной цепи было рассмотрено
Хирстом, использовавшим и развившим формализм, разработанный Кирквудом, в его
теории вращательного трения палочкообразного ожерелья.
Положение центров гидродинамического
сопротивления (бусинок) с коэффициентом трения ж в используемой Хирстом модели
определяется в молекулярной системе координат XYZ,
начало которой совмещено со средней точкой молекулярной цепи, а направление оси
Z
совпадает с направлением цепи в этой точке. Предполагается
цилиндрически-симметричное распределение элементов цепи с осью симметрии Z.
Применяя методы, разработанные для червеобразной цепи, Хирст вычислил 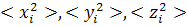 -
средние квадраты координат -го элемента цепи, удаленного по контуру цепи на
расстояние Li от начала
координат:
-
средние квадраты координат -го элемента цепи, удаленного по контуру цепи на
расстояние Li от начала
координат:
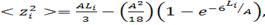 (25)
(25)
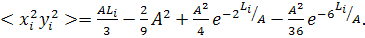 (26)
(26)
Эти выражения в области малых 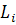 переходят
в соотношения
переходят
в соотношения
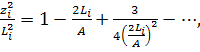 (27)
(27)
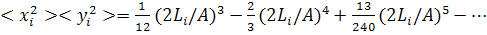 (28)
(28)
Откуда, при 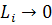 следует
следует
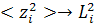 и
и
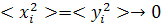 ,
что соответствует конформации прямой тонкой палочки. В области
,
что соответствует конформации прямой тонкой палочки. В области 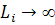 следует
следует
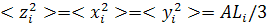 ,
что соответствует гауссову клубку с распределением сегментов, в средней
сферически-симметричным относительно средней точки цепи.
,
что соответствует гауссову клубку с распределением сегментов, в средней
сферически-симметричным относительно средней точки цепи.
Окончательные выражения для коэффициента
вращательного трения W
червеобразной цепи при ее вращении вокруг оси X
или Y
Хирст получает для двух предельных случаев.
Для коротких цепей, когда 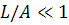 (слабо
изогнутая палочка):
(слабо
изогнутая палочка):
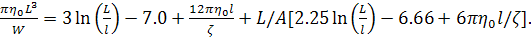 (29)
(29)
Для длинных цепей, когда 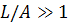 (червеобразный
клубок),
(червеобразный
клубок),
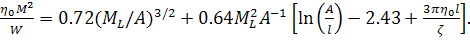 (30)
(30)
Если выразить 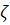 через
диаметр
через
диаметр 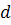 эквивалентной
стоксовой сферы
эквивалентной
стоксовой сферы 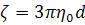 и принять модель
червеобразного ожерелья с соприкасающимися бусами
и принять модель
червеобразного ожерелья с соприкасающимися бусами 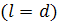 ,
то последние выражения трансформируются в выражения
,
то последние выражения трансформируются в выражения
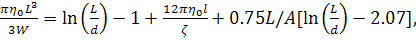 (31)
(31)
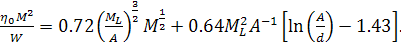 (32)
(32)
Эти выражения отличаются от формул Кирквуда для
палочкообразного ожерелья наличием члена, пропорционального 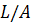 .
Этот член характеризует уменьшение вращательного трения
.
Этот член характеризует уменьшение вращательного трения 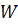 слабо
изогнутой палочки по сравнению с прямолинейной за счет ее гибкости.
слабо
изогнутой палочки по сравнению с прямолинейной за счет ее гибкости.
Эта молекулярная модель была использована также
при вычислении характеристической вязкости червеобразной цепи. Поскольку
применяемая модель молекулы асферична, необходимо определит функцию с
распределения молекул по ориентациям в сдвиговом поле потока. С этой целью
решается уравнение вращательной диффузии, полученное Петерлином
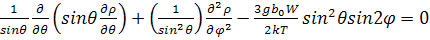 (33)
(33)
Полученное решение, как и следовало ожидать для
молекул с цилиндрической симметрией, совпадает с результатом Петерлина.
Выражения для характеристической вязкости в предельных случаях короткой и
длинной червеобразной цепи, согласно Хирсту и Тагами, имеют следующий вид:
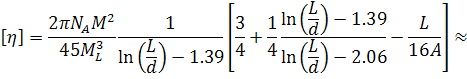
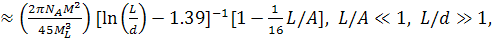 (34)
(34)
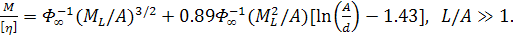 (35)
(35)
Первое из которых при очень больших значениях 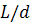 (тонкая
червеобразная цепь) и
(тонкая
червеобразная цепь) и 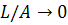 переходит в
формулу Кирквуда для палочкообразного ожерелья с соприкасающимися бусами.
переходит в
формулу Кирквуда для палочкообразного ожерелья с соприкасающимися бусами.
Все это показывает, что модель ожерелья,
введенная Кирквудом для описания гидродинамического взаимодействия и
характеристики гидродинамических свойств цепных молекул, может быть
использована в применении к макромолекулам с различной конформацией - от
прямолинейной палочки до гауссова клубка. При этом оказывается, что при увеличении
длины молекулярной цепи для палочкообразных молекул гидродинамическое
взаимодействие растет пропорционально логарифму их длины, а для гауссовых
клубков - пропорционально корню квадратному из длины цепи.
Персистентный цилиндр
Под червеобразным (персистентным) цилиндром
понимают цилиндр, изогнутый таким образом, что форма его осевой линии
описывается уравнением червеобразной цепи
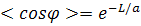 (36)
(36)
и соответственно расстояние между любыми двумя
его точками на осевой линии определяется по формуле
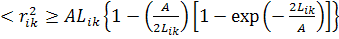 (37)
(37)
Гидродинамическое сопротивление, испытываемое
таким телом при его движении в вязкой жидкости, вычисляется методом Озеена -
Бюргерса.
Теория характеристической вязкости раствора
жесткоцепных молекул на основе модели червеобразного цилиндра была разработана
Ямакавой, применившим для этой цели метод Озеена - Бюргерса.
В первоначальном варианте были проведены
вычисления характеристической вязкости без учета краевых эффектов. В дальнейшем
они были дополнены теорией, учитывающей края червеобразного цилиндра, что
существенно для области малых значений 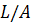 ,
когда молекула имеет форму слабоизогнутой палочки конечной толщины
,
когда молекула имеет форму слабоизогнутой палочки конечной толщины 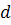 .
Таким образом, для этой области
.
Таким образом, для этой области 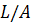 фрикционные
свойства молекул могут быть описаны комбинацией теории прямого сфероцилиндра,
учитывающей конечность
фрикционные
свойства молекул могут быть описаны комбинацией теории прямого сфероцилиндра,
учитывающей конечность 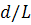 , и теории
червеобразного цилиндра, учитывающей гибкость (конечную величину
, и теории
червеобразного цилиндра, учитывающей гибкость (конечную величину 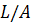 )
молекулярной цепи.
)
молекулярной цепи.
Пропуская все вычисления, можно сказать, что для
червеобразного сфероцилиндра (при L/A>>1)
с хорошим приближением может быть использовано выражение
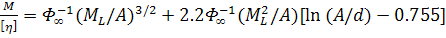 (38)
(38)
В заключении необходимо сказать, что для одних и
тех же экспериментальных данных (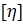 ,
,
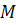 и
и
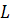 )
модель червеобразного цилиндра приводит к несколько меньшим значением A
и несколько большим значениям d
по равнению с тем, что можно получить, использую модель червеобразного
ожерелья.
)
модель червеобразного цилиндра приводит к несколько меньшим значением A
и несколько большим значениям d
по равнению с тем, что можно получить, использую модель червеобразного
ожерелья.
2.1.5
Эффект исключенного объема
Для типичных жесткоцепных полимеров в
практически доступной области молекулярных весов даже в термодинамически
хороших растворителях эффекты исключенного объема не оказывают существенного
влияния на размеры молекул, а потому не должны влиять и на их гидродинамические
свойства.
Однако в принципе при изучении жесткоцепных
полимеров очень высокого молекулярного веса не исключена возможность такого
влияния.
Поступательное трение жесткоцепного полимера,
моделируемого червеобразным ожерельем с учетом эффектов исключенного объема,
вычислялось в работе Грея-Блюмфельда-Хирста [6]. Вычисления проводились с
использованием параметра е, характеризующего отклонение статистических размеров
цепи от гауссовых свойств за счет объемных эффектов. Второй момент
распределения 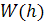 по расстояниям
по расстояниям 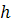 в
гауссовых цепях, возмущенных объемными эффектами, связан с невозмущенной
величиной
в
гауссовых цепях, возмущенных объемными эффектами, связан с невозмущенной
величиной 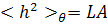 (в θ-условиях)
соотношением
(в θ-условиях)
соотношением
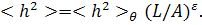 (39)
(39)
Для коэффициентов поступательного трения в
области больших 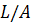 , в итоге, было
получено выражение
, в итоге, было
получено выражение
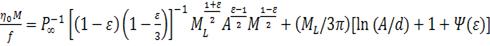 (40)
(40)
где функция 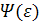 табулирована
в работе [6].
табулирована
в работе [6].
Таким образом, при наличии эффектов исключенного
объема в области больших 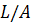 соотношение
соотношение 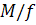 линейно
относительно
линейно
относительно 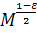 .
.
2.1.6 Использование
данных вискозиметрии для определения молекулярного веса и размеров макромолекул
Сравнительная простота измерений вязкости делает
определение молекулярного веса по данным вискозиметрии одним из самых
распространенных и доступных методов исследования полимеров. С другой стороны,
однако, следует иметь ввиду, что этот метод не является абсолютным и нуждается
в градуировке. При этом не всякие определения молекулярного веса оказываются
пригодными для градуировки, так как полимеры почти всегда полидисперсны, и
полидисперсность по-разному проявляется при измерениях 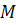 различными
методами.
различными
методами.
Другая возможность исследования полимеров, связанная
с измерениями 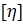 , заключается в
оценке размеров макромолекул, а следовательно, и равновесной жесткости цепей.
Однако и этот метод не является абсолютным, так как характеристическая вязкость
связана с молекулярным весом соотношением
, заключается в
оценке размеров макромолекул, а следовательно, и равновесной жесткости цепей.
Однако и этот метод не является абсолютным, так как характеристическая вязкость
связана с молекулярным весом соотношением
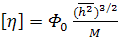 (41)
(41)
и определение 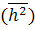 требует
независимого определения
требует
независимого определения 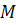 . Даже если эта
величина известна, препятствием к непосредственному использованию этой формулы
служит еще некоторая неопределенность параметра
. Даже если эта
величина известна, препятствием к непосредственному использованию этой формулы
служит еще некоторая неопределенность параметра 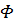 ,
который монотонно убывает при улучшении качества растворителя по формуле:
,
который монотонно убывает при улучшении качества растворителя по формуле:
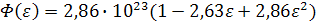 (42)
(42)
где 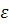 -
термодинамический параметр, характеризующий качество растворителя.
-
термодинамический параметр, характеризующий качество растворителя.
По этой причине для определения
среднеквадратичных размеров удобнее пользоваться коэффициентом диффузии 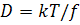 .
Входящий сюда коэффициент поступательного трения
.
Входящий сюда коэффициент поступательного трения
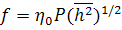 (43)
(43)
(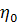 - вязкость
растворителя) зависит от M
только через
- вязкость
растворителя) зависит от M
только через 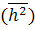 , что же касается
параметра P,
то он по сравнению с Ф слабо зависит от качества растворителя.
, что же касается
параметра P,
то он по сравнению с Ф слабо зависит от качества растворителя.
Широкое применение в полимерной науке и
технологии имеет соотношение Куна-Марка-Хаувинка-Сакурады:
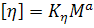 (44)
(44)
где 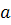 и
и
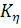 -
параметры, определенные и табулированные для многих систем
полимер-растворитель. Известен ряд экстраполяционных процедур, позволяющих
получать величину
-
параметры, определенные и табулированные для многих систем
полимер-растворитель. Известен ряд экстраполяционных процедур, позволяющих
получать величину 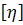 незаряженных
макромолекул. Наиболее известным является уравнение Хаггинса:
незаряженных
макромолекул. Наиболее известным является уравнение Хаггинса:
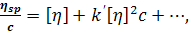 (45)
(45)
spºr-1
где 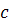 - концентрация
полимера в растворе,
- концентрация
полимера в растворе, 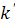 - безразмерный
параметр Хаггинса.
- безразмерный
параметр Хаггинса.
В паре с уравнением Хаггинса рассматривают
уравнение Крэмера
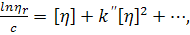 (46)
(46)
где 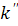 -
безразмерный параметр Крэмера.
-
безразмерный параметр Крэмера.
Сравнительно недавно Федорс [6] предложил
построение
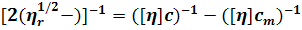 (47)
(47)
которое сохраняет линейный характер в широкой
области концентраций, когда 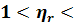 100, и позволяет
определять
100, и позволяет
определять 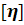 по наклону
соответствующей зависимости, где
по наклону
соответствующей зависимости, где 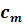 -
концентрация, соответствующая максимально плотной упаковке жестких
эквивалентных гидродинамических сфер.
-
концентрация, соответствующая максимально плотной упаковке жестких
эквивалентных гидродинамических сфер.
В то же время в реологии известно, что
динамическая вязкость раствора полимера в широком интервале концентраций может
быть представлена как
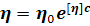
Из этого соотношения следует, что dlnηr/dc
в каждой точке зависимости lnηr
от c может
рассматриваться как текущее значение характеристической вязкости:
[]*º
dlnr/dc
Очевидно, то при 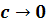 величина
величина
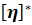 является
начальным наклоном зависимости
является
начальным наклоном зависимости 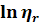 от
от 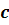 и
совпадает с величиной характеристической вязкости, описывающей поведение
изолированной макромолекулы.
и
совпадает с величиной характеристической вязкости, описывающей поведение
изолированной макромолекулы.
При конечной концентрации раствора полимера
величина 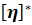 характеризует
удельный объем, занимаемый пробной макромолекулой, помещенной в раствор, в
котором равномерно распределены все остальные макромолекулы. Такой подход можно
рассматривать как экспериментальную реализацию концепции среднего поля.
характеризует
удельный объем, занимаемый пробной макромолекулой, помещенной в раствор, в
котором равномерно распределены все остальные макромолекулы. Такой подход можно
рассматривать как экспериментальную реализацию концепции среднего поля.
2.2
Седиментация
.2.1 Основные
понятия
В отличие от диффузии, где поступательное движение
молекул происходит под действием сил, вызванных градиентом осмотического
давления, при седиментации - это центробежная сила 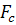 ,
вызванная вращением ротора ультрацентрифуги:
,
вызванная вращением ротора ультрацентрифуги:
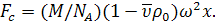 (48)
(48)
Здесь 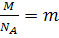 -
масса молекулы;
-
масса молекулы; 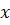 - расстояние ее от
оси вращения;
- расстояние ее от
оси вращения; 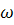 - угловая скорость
ротора;
- угловая скорость
ротора; 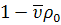 -
множитель плавучести, зависящий от плотности растворителя
-
множитель плавучести, зависящий от плотности растворителя 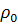 и
парциального удельного объема
и
парциального удельного объема 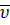 полимера.
полимера.
В достаточно сильных центробежных полях (высокие
скорости вращения), способных преодолеть броуново движение макромолекул,
возникает их направленный поток, в результате которого образуется граница между
чистым растворителем и раствором. Эта граница движется в радиальном
направлении, расплываясь со временем за счет диффузии и полидисперсности
изучаемого полимера.
В условиях скоростной седиментации центробежная
сила 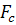 уравновешивается
силой трения
уравновешивается
силой трения 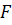 , действующей на
молекулу со стороны растворителя. Тогда, приравнивая
, действующей на
молекулу со стороны растворителя. Тогда, приравнивая 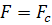 ,
получим
,
получим
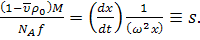 (49)
(49)
Эта формула показывает, что скорость
седиментации 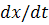 в точке
в точке 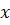 пропорциональна
центростремительному ускорению
пропорциональна
центростремительному ускорению 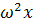 в этой точке, а
коэффициент пропорциональности
в этой точке, а
коэффициент пропорциональности 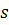 называют
коэффициентом седиментации. Единицей измерения в системе СГС является секунда.
Практической мерой является единица Сведберга (S)=
называют
коэффициентом седиментации. Единицей измерения в системе СГС является секунда.
Практической мерой является единица Сведберга (S)=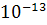 сек.
сек.
Из-за гидродинамических взаимодействий, носящих
в замкнутом сосуде довольно специфический характер, s
зависит от концентрации и не может служить однозначной характеристикой размеров
и формы молекул. Значение s,
экстраполированное к бесконечному разбавлению, называют константой седиментации
- 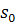 .
Поскольку в любое выражение для
.
Поскольку в любое выражение для 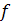 входит вязкость
растворителя
входит вязкость
растворителя 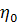 , для
характеристики размеров и формы макромолекул в разных растворителях вводят
величину
, для
характеристики размеров и формы макромолекул в разных растворителях вводят
величину 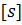 ,
не зависящую явным образом от плотности и вязкости растворителя
,
не зависящую явным образом от плотности и вязкости растворителя
[s]=s0η0/(1-υρ0)=M/NA(f/h0)
(50)
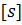 называется
характеристической или внутренней константой седиментации. Эта величина, так же
как и характеристическая вязкость, при заданном молекулярном весе зависит
только от размеров и формы макромолекул. Поэтому, сравнивая значения
называется
характеристической или внутренней константой седиментации. Эта величина, так же
как и характеристическая вязкость, при заданном молекулярном весе зависит
только от размеров и формы макромолекул. Поэтому, сравнивая значения 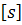 одного
и того же образца полимера в различных растворителях, можно получить
непосредственную информацию об изменениях геометрических и гидродинамических
параметров молекулы при изменении растворителя (или температуры).
одного
и того же образца полимера в различных растворителях, можно получить
непосредственную информацию об изменениях геометрических и гидродинамических
параметров молекулы при изменении растворителя (или температуры).
Коэффициент седиментации макромолекул
определяется экспериментально при скоростном центрифугировании путем
фиксирования положения (координата x)
седиментационной границы в соответствующие моменты времени 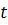 .
При этом используется выражение
.
При этом используется выражение
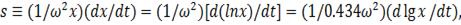 (51)
(51)
позволяющее определить 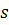 по
наклону кривой экспериментальной зависимости
по
наклону кривой экспериментальной зависимости 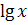 от
от
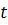 при
заданном значении
при
заданном значении 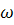 .
.
Другими формами этого выражения также являются
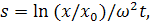 (52)
(52)
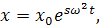 (53)
(53)
где 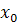 -
координата седиментационной границы в начальный момент времени (
-
координата седиментационной границы в начальный момент времени (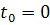 ).
).
Положение и ширина седиментационной границы
экспериментально фиксируются теми же методами, которые применяются при изучении
диффузии. В качестве координаты, определяющей положение границы «как целого»,
обычно принимается 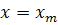 , соответствующее
максимуму кривой дифференциального распределения
, соответствующее
максимуму кривой дифференциального распределения 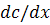 .
.
Зависимость коэффициента седиментации s
от концентрации c
исследуемого полимерного раствора обычно выражена значительно заметнее, чем в
случае диффузии; s
уменьшается с возрастанием c.
Поэтому для определения константы седиментации 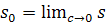 необходима
экстраполяция экспериментальных значений
необходима
экстраполяция экспериментальных значений 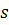 к условиям
предельно разбавленного раствора.
к условиям
предельно разбавленного раствора.
Последнее выполняется с использованием
эмпирического линейного соотношения
/s=(1/s0)(1+ksc)
(54)
Константа седиментации для монодисперсного
полимера, пропорциональна отношению M/f
:
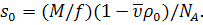 (55)
(55)
По самому определению, коэффициент
поступательного трения 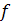 макромолекулы в
предельно разбавленном растворе должен иметь одно и то же значение в явлениях
седиментации и диффузии. Поэтому получим
макромолекулы в
предельно разбавленном растворе должен иметь одно и то же значение в явлениях
седиментации и диффузии. Поэтому получим
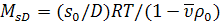 (56)
(56)
известную формулу Сведберга, позволяющую
определить молекулярный вес полимера по экспериментальным значениям 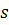 и
и
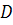 в
предельно разбавленных растворах. Важно, что эта формула не ограничена никакими
модельными представлениями о структуре молекул. Поэтому комбинация измерений седиментации
и диффузии является наряду со светорассеянием абсолютным методом определения
молекулярного веса.
в
предельно разбавленных растворах. Важно, что эта формула не ограничена никакими
модельными представлениями о структуре молекул. Поэтому комбинация измерений седиментации
и диффузии является наряду со светорассеянием абсолютным методом определения
молекулярного веса.
2.2.2Зависимость
коэффициента седиментации от молекулярного веса
В соответствии с гидродинамическими теориями
коэффициента поступательного трения, зависимость 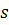 от
молекулярного веса
от
молекулярного веса 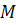 может быть
представлена формулами
может быть
представлена формулами
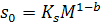 (57)
(57)
Это эмпирическое соотношение Марка - Куна -
Хаувинка, b - тот же
параметр, что в формулах 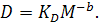
2.3
Диффузия макромолекул в растворах
Поступательная диффузия в растворах является
процессом, непосредственно связанным с тепловым движение молекул растворенного
вещества. Поэтому изучение диффузии в растворе высокомолекулярного вещества
может дать наиболее прямую информацию о подвижности растворенных макромолекул,
а следовательно, служить источником сведений об их геометрических и
гидродинамических характеристиках.
Преимущество метода диффузии по сравнению с
другими гидродинамическими методами (например, вискозиметрией) заключается в
том, что в диффузионных измерениях исследуемые макромолекулы изучаются
практически в их «естественном» состоянии, не возмущенном воздействиями внешних
сил (механических, электрических и т.п.).
Макроскопическая направленная диффузия в
растворе возникает при наличии градиента концентрации 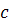 растворенного
вещества
растворенного
вещества 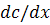 в
направлении
в
направлении 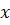 .
.
Согласно Эйнштейну, при стационарном процессе
диффузии, вызванном наличием градиента концентрации 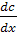 ,
«движущей силой» служит градиент
,
«движущей силой» служит градиент 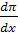 осмотического
давления
осмотического
давления 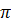 .
При этом сила, действующая на частицы в 1 см3 раствора, равна -
.
При этом сила, действующая на частицы в 1 см3 раствора, равна - 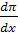 ,
а на одну частицу соответственно
,
а на одну частицу соответственно
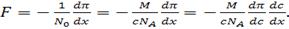 (58)
(58)
Под действием силы 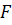 частицы
движутся со скоростью х и создают диффузионный поток вещества
частицы
движутся со скоростью х и создают диффузионный поток вещества
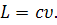 (59)
(59)
Сопоставляя предыдущие уравнения, получаем:
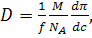 (60)
(60)
где 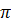 -
осмотическое давление раствора.
-
осмотическое давление раствора.
В случае идеального раствора невзаимодействующих
частиц осмотическое давление определяется законом Вант-Гоффа
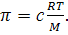 (61)
(61)
В этом случае «движущая сила» диффузии равна
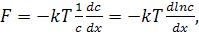 (62)
(62)
Отсюда получаем уравнение Эйнштейна
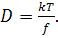 (63)
(63)
Таким образом, измеряя экспериментально скорость
диффузии (т.е. D) полимера в
растворе, можно определить коэффициент трения его молекулы 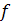 ,
непосредственно связанный с формой и размером последней.
,
непосредственно связанный с формой и размером последней.
Глава
3. Экспериментальные данные и их обсуждение
В работе было изучено гидродинамическое
поведение стандартов (производства фирмы Fluka)
полистиролсульфоната натрия в широком интервале молекулярных масс в чистой
воде, 0.2M и 4.17M
NaCl.
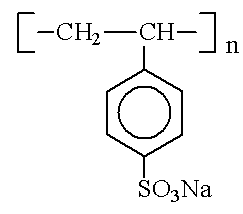
Рис. 1 Структурная формула
полистирол-4-сульфоната натрия (ПС)
Исследования вискозиметрии проводились с
применением капиллярных вискозиметров Оствальда.
Табл.1. Времена течения растворителей в
различных вискозиметрах в секундах
|
τ01
|
τ02
|
τ03
|
|
H2O
|
97.2
|
79.8
|
|
|
0.2M
NaCl
|
81.0
|
61.2
|
84.4
|
|
4.17M
NaCl
|
133.6
|
118.2
|
|
Зависимости sp/c
от концентрации с для образцов полистиролсульфонатов в 0.2M
NaCl и в 4.17M
NaCl представлены на
рис.2 и 3, соответственно.

Рис.2. Построения Хаггинса hsp/с (см3×г-1)-с (г×см-3) для
определения значений характеристической вязкости для полистиролсульфонатов
натрия в 0.2M NaCl при 250С.
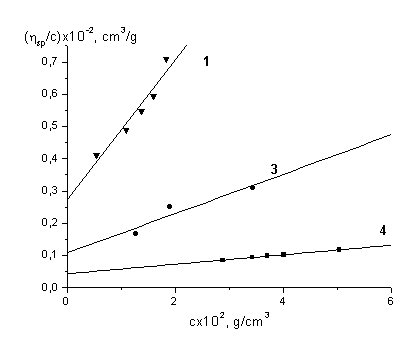
Рис.3. Построения Хаггинса hsp/с (см3×г-1)-с (г×см-3) для
определения значений характеристической вязкости для полистиролсульфонатов
натрия в 4.17M NaCl при 250С.
Характеристическая вязкость
рассчитывалась с помощью уравнений Хаггинса и Крэмера. Сравнение результатов
применения этих уравнений для двух образцов (№1 и №5) представлено на рис.4.
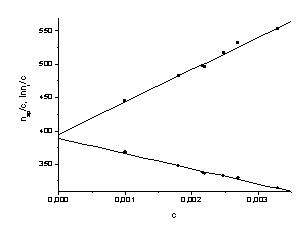
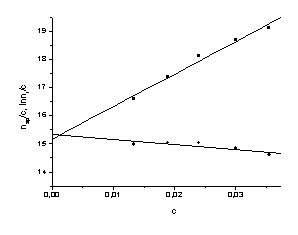
Рис.4. Построения Хаггинса и Крэмера
для образцов №1 и №5 в 0.2M NaCl
Определения величины 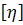 в
бессолевых растворах наталкивается на значительные трудности. В области малых
концентраций полиэлектролита величина
в
бессолевых растворах наталкивается на значительные трудности. В области малых
концентраций полиэлектролита величина 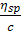 возрастает с уменьшением
возрастает с уменьшением 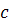 -
полиэлектролитный эффект. Этот эффект обусловлен тем, что при разбавлении
раствора увеличивается объем, в котором распределены противоионы. Вследствие
этого уменьшается экранирования фиксированных на цепи зарядов, возрастает их
взаимное отталкивание и происходит увеличение размеров полииона. Таким образом,
при уменьшении ионной силы раствора увеличение размеров цепи происходит за счет
электростатического отталкивания между ее мономерами.
-
полиэлектролитный эффект. Этот эффект обусловлен тем, что при разбавлении
раствора увеличивается объем, в котором распределены противоионы. Вследствие
этого уменьшается экранирования фиксированных на цепи зарядов, возрастает их
взаимное отталкивание и происходит увеличение размеров полииона. Таким образом,
при уменьшении ионной силы раствора увеличение размеров цепи происходит за счет
электростатического отталкивания между ее мономерами.
Как уже отмечалось, зависимость
размеров молекул полиэлектролитов от ионной силы отражается на их
гидродинамическом поведении, приводя к ряду концентрационных аномалий, когда
разбавление не является изоионным. Например, в воде наблюдается непрерывный
рост 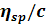 с
разбавлением, обусловленный полиэлектролитным набуханием клубков. По мере
увеличения ионной силы растворителя электростатическое отталкивание звеньев
ослабевает вследствие экранирования дебай-хюккелевской ионной атмосферой,
увеличение
с
разбавлением, обусловленный полиэлектролитным набуханием клубков. По мере
увеличения ионной силы растворителя электростатическое отталкивание звеньев
ослабевает вследствие экранирования дебай-хюккелевской ионной атмосферой,
увеличение 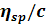 с
разбавлением становится менее выраженным, и на кривых появляется максимум,
смещающийся с увеличением ионной силы в сторону больших
с
разбавлением становится менее выраженным, и на кривых появляется максимум,
смещающийся с увеличением ионной силы в сторону больших 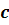 . При
достаточно больших ионных силах все специфические полиэлектролитные эффекты
оказываются подавленными. На графике
. При
достаточно больших ионных силах все специфические полиэлектролитные эффекты
оказываются подавленными. На графике 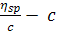 зависимость может быть
экстраполирована к оси ординат в точку, которая получается из начального
наклона зависимости
зависимость может быть
экстраполирована к оси ординат в точку, которая получается из начального
наклона зависимости 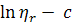 (рис.5).
(рис.5).
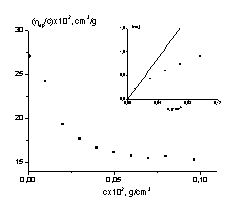
Рис.5. Зависимость ηsp/c - c и ln ηr - c для
растворов полиэлектролитов в водном бессолевом растворе для образца № 6. Точка
на оси Y
соответствует [h]*=dlnhr/dc при c=0

Рис.6. Зависимость lnhr - c для водных
бессолевых растворов
полистиролсульфонатов натрия при
250С.
Скоростную седиментацию изучали на
аналитической ультрацентрифуге Beckman XLI при частоте вращения ротора 55 000
об/мин в двухсекторных ячейках с Al вкладышем длиной 12 мм по
ходу луча.
Седиментационные сканы, полученные
при помощи интерференционной оптики, обрабатывали по программе Sedfit [12],
которая использует возможность уравнения Ламма [13] разделять расширения
седиментационной границы, возникающее из-за неоднородности образца и связанное
с процессами диффузии. Уравнение Ламма (59) описывает процесс седиментации
монодисперсного вещества в ячейке секториальной формы. Это дифференциальное
уравнение имеет следующий вид:
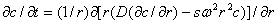
 (59)
(59)
где с - концентрация растворенного
вещества, t - время седиментации, r - радиальное расстояние, измеряемое от оси
вращения, w - угловая
скорость вращения, s и D, соответственно, коэффициенты седиментации и
поступательной диффузии растворенного вещества. Это уравнение не может быть
решено аналитически [12]. Программа Sedfit [12, 14] решает это уравнение
численно. Ищется такое решение уравнения, которое приводит к максимальному
совпадению расчетного и экспериментального профилей седиментационной границы.
Численный анализ проводится с применением соответствующих статистических
критериев, которые включают минимизацию суммы квадратов невязок между
экспериментальными и расчетными кривыми распределения концентрации вещества в
ячейке. При этом, необходимо введение в программу значений вязкости (0),
плотности (0) растворителя и парциального удельного объема полимера ().
Другими необходимыми параметрами
являются минимальное smin и максимальное smax значения коэффициентов
седиментации, которые наряду с числом разрешения (resolution) N определяют шаг
распределения s=(smax-smin)/N. В программе можно использовать по выбору
два метода регуляризации (сглаживания): метод максимальной энтропии или метод
Тихонова - Филипса. При регуляризации важен выбор доверительного уровня
(F-ratio), задаваемого оператором, и который определяет степень сглаживания
распределения. Обработка первичных экспериментальных данных, представляющих
собой оцифрованные интегральные распределения показателя преломления в
седиментационной ячейке, приводит к дифференциальному распределению образца по
коэффициентам седиментации (dc(s)/ds), которое в программе обозначено как c(s).
Площадь под кривой между значениями s1 и s2 дает концентрацию макромолекул в
этом интервале значений s, выраженную в числе интерференционных полос. В
результате получают средние значения коэффициента седиментации.
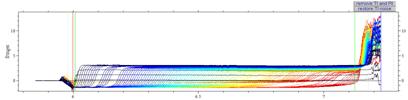

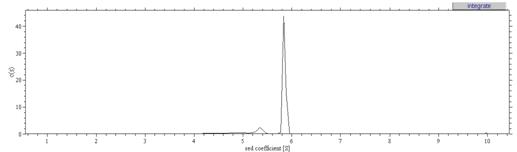
Рис.7. Седиментационный анализ
образца № 3 в 0.2M NaCl в программе Sedfit
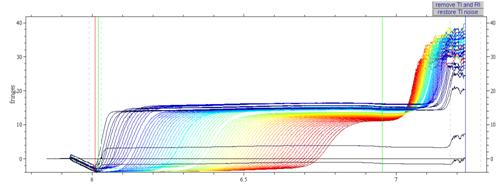

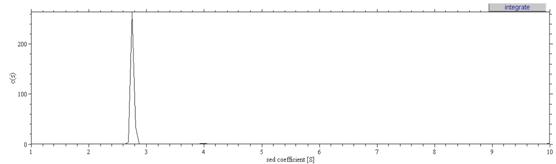
Рис.8.
Седиментационный анализ образца № 4 в 0.2M NaCl в программе Sedfit

Рис. 9. Концентрационная зависимость
коэффициента седиментации для образцов №2,3,4 в 0.2М NaCl при 20°С

Рис. 10. Концентрационная
зависимость коэффициента седиментации для образцов №2,3,4 в 4.17М NaCl при 20°С
С использованием значений
характеристических вязкостей, коэффициентов седиментации в 0.2М NaCl и значения
гидродинамического инварианта А0, полученного для образцов полистирол
сульфоната в 0.2М NaCl в работе [4], были рассчитаны
молекулярные массы Ms по соотношению:
Ms =
(R/A0)3/2[s]3/2[]1/2, (64)
где A0=3.15×10-10
, [s]=0/(1-0), [] в
100см3/г.
Молекулярные массы рассчитывали
также по значениям s0 и ks с
использованием седиментационного параметра s:
Mkss = (NA/s)3/2[s]3/2ks1/2,
(65)
где s=1.25×107 , [s]=0/(1-0), ks в см3/г.
Гидродинамические характеристики и
молекулярные массы приведены в таблице 2.
Таблица 2.Гидродинамические
характеристики и молекулярная масса образцов полистиролсульфоната натрия в
воде, в 0.2M NaCl и 4.17М NaCl
|
№
|
M Fluka
|
[]
|
[]
|
k’
|
k’’
|
s0
|
ks
|
Ms
|
Mks
|
[]
|
k’
|
k’’
|
|
|
|
H2O
|
0.2M NaCl
|
4.17M NaCl
|
|
1
|
2600
|
9300
|
398
|
0.30
|
-0.15
|
16.8
|
600
|
2450
|
30
|
1.8
|
0.4
|
|
2
|
780
|
4100
|
118
|
0.40
|
-0.035
|
9.95
|
260
|
640
|
640
|
|
|
|
|
3
|
350
|
3500
|
117
|
0.32
|
-0.156
|
7.72
|
204
|
430
|
440
|
11.5
|
5.3
|
1.2
|
|
4
|
77
|
830
|
28.5
|
0.6
|
-0.082
|
4.08
|
70
|
82
|
98
|
4
|
7.5
|
2.2
|
|
5
|
46
|
56
|
15
|
0.51
|
-0.074
|
3.09
|
40
|
39
|
50
|
|
|
|
|
6
|
13
|
27
|
6
|
2.0
|
-0.62
|
1.89
|
30
|
12
|
21
|
|
|
|
* - коэффициенты седиментации измерены при 200С
Прежде всего, были построены зависимости
Куна-Марка-Хаувинка-Сакурады (рис.11), т.е. получены скейлинговые соотношения,
связывающие гидродинамические характеристики с молекулярной массой. Оказалось,
что скейлинговый индекс, характеризующий зависимость характеристической
вязкости от молекулярной массы при переходе от бессолевого раствора к 0.2 M,
а затем к 4.17М NaCl
уменьшается. Таким образом, с увеличением ионной силы растворителя в макромолекуле
происходят конформационные изменения, что приводит к уменьшению объема
макромолекулярного клубка.
Кроме того, проведено сравнение с данными,
полученными в работе [4], и обнаружено хорошее соответствие с данными настоящей
работы (рис.12-14). Данные работы [4] представлены в табл.3
Табл.3 Гидродинамические характеристики при 20oС
и молекулярная масса поли-стирол-4-сульфоната натрия (из работы [4]).
|
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
|
MsD, 10-3
г/моль
|
|
847
|
607
|
605
|
448
|
375
|
124
|
84
|
53
|
|
[], см3/г
|
H2O
|
8900
|
8200
|
5100
|
5900
|
4800
|
660
|
260
|
125
|
|
[], см3/г
|
0.2M
NaCl
|
172
|
170
|
117
|
117
|
109
|
43.5
|
29.8
|
22.0
|
|
[], см3/г
|
4.17M NaCl
|
13.2
|
15.8
|
12.7
|
11.1
|
10.8
|
5.1
|
4.3
|
4.2
|
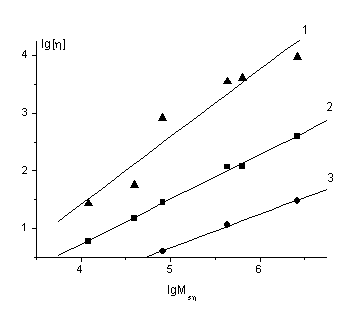
Рис.11. Зависимости
Куна-Марка-Хаувинка-Сакурады для трех растворителей (1 - H2O (bη=1.2±0.2),
2- 0.2M NaCl (bη=0.78±0.02),
3 - 4.17M NaCl (bη=0.58±0.03)).
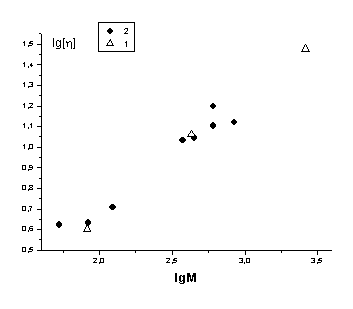
Рис.12. Построение Куна-Марка-Хаувинка-Сакурады
в H2O. Сравнение
данных настоящей работы - (1) и данных работы [4] - (2)

Рис.13. Построение
Куна-Марка-Хаувинка-Сакурады в 0.2M NaCl. Сравнение
данных настоящей работы - (1) и данных работы [4] - (2)

Рис.14. Построение
Куна-Марка-Хаувинка-Сакурады в 4.17M NaCl. Сравнение
данных настоящей работы - (1) и данных работы [4] - (2)
В результате анализа зависимости
между 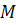
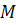 и
и 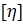
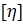 в двойном логарифмическом масштабе
(рис.11) получаем соотношения типа Куна-Марка-Хаувинка-Сакурады для молекул
полистиролсульфоната в 0,2 М растворе NaCl при 25
в двойном логарифмическом масштабе
(рис.11) получаем соотношения типа Куна-Марка-Хаувинка-Сакурады для молекул
полистиролсульфоната в 0,2 М растворе NaCl при 25 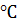
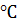 .
.
По величине скейлинговых индексов
может быть проведена оценка значения параметра, характеризующего
термодинамическое качество растворителя
= (2b-1)/3 = 1-2bs 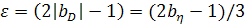 (66)
(66)
Для исследованной системы получаем
следующее значение ε=0.186,
которое использовали при дальнейшей интерпретации гидродинамических данных.
На основе теории
Грея-Блюмфельда-Хирста, описывающей гидродинамическое поведение червеобразных
цепей с учетом, как эффектов протекания, так и эффектов исключенного объема,
проведены оценки длины статистического сегмента и гидродинамического
поперечника молекул полистирол сульфоната натрия.
Для определения длины
статистического сегмента Куна использовали соотношение:
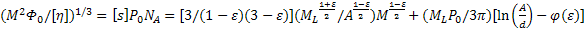
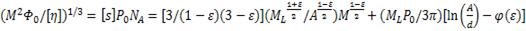 (67)
(67)
где 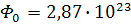
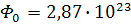 моль-1 - вязкостный параметр Флори,
моль-1 - вязкостный параметр Флори,
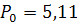
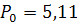 - гидродинамический параметр Флори,
- гидродинамический параметр Флори,
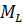
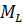 - масса единицы длины полимерной
цепи,
- масса единицы длины полимерной
цепи, 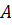
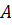 - длина статистического сегмента,
- длина статистического сегмента, 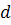
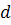 - гидродинамический диаметр,
- гидродинамический диаметр, 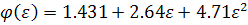
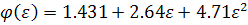 .
.
Построение, соответствующее
соотношению (63) представлено на рис.15 и 16 (для 4.17M NaCl и H2O ε=0), где
точки укладываются на прямую зависимость с достаточно хорошим уровнем линейной
корреляции. Используя величину массы единицы длины цепи 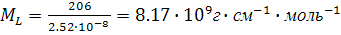
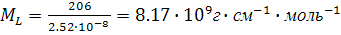 , получаем из наклона оценку длины
статистического сегмента
, получаем из наклона оценку длины
статистического сегмента 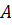
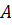 , а из отсекаемого на оси ординат
отрезка можно оценить гидродинамический диаметр d. Результаты
этих оценок представлены в табл.4.
, а из отсекаемого на оси ординат
отрезка можно оценить гидродинамический диаметр d. Результаты
этих оценок представлены в табл.4.
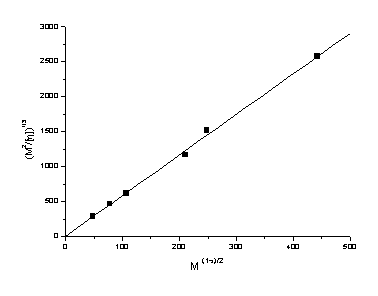
Рис.15. Построение (M2/[η])1/3 - M(1-ε)/2 при ε=0,186, используемое
для оценки длины сегмента Куна A и гидродинамического диаметра d молекул
полистирол сульфоната (растворитель - 0.2M NaCl).
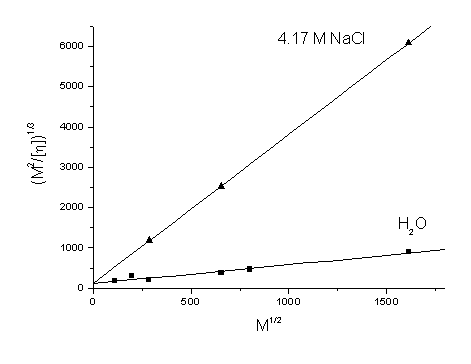
Рис.16. Построение (M2/[η])1/3 - M1/2,
используемое для оценки длины сегмента Куна A и
гидродинамического диаметра d молекул полистирол сульфоната
(растворители - 4.17M NaCl и H2O).
Табл. 4. Оценки Длины сегмента Куна
и диаметра
|
Построения
|
Растворитель
|
Наклон
|
Отсек.отрезок
|
A нм
|
d нм
|
|
(M2/[])1/3
|
H2O
|
0.47±0.05
|
120±40
|
85
± 20
|
3
± 3
|
|
s0
|
0.2M
NaCl
|
5.8±0.1
|
5±30
|
3.9
± 0.2
|
0.5±0.2
|
|
(M2/[])1/3
|
4.17M
NaCl
|
3.70±0.02
|
120±20
|
1.4 ± 0.02
|
0.06 ± 0.02
|
ВЫВОДЫ
. Растворы полистиролсульфонатов изучены
методом вискозиметрии в водных растворах при различных ионных силах.
. Проведен седиментационный анализ
образцов в 0.2 М NaCl.
. По экспериментальным значениям
коэффициентов седиментации, характеристической вязкости, концентрационного
коэффициента седиментации с использованием гидродинамического инварианта А0 и
седиментационного параметра s
были рассчитаны молекулярные массы Msи
Mkss образцов, которые
удовлетворительно коррелируют между собой.
. Получены соотношения
Куна-Марка-Хаувинка-Сакурады для образцов полистиролсульфонатов при различных
ионных силах.
. На основе теории Грея-Блюмфельда-Хирста
проведены оценки длины статистического сегмента Куна и гидродинамического
диаметра молекул полистиролсульфонатов в растворах. Проведено сравнение с
литературными данными.
СПИСОК
ЛИТЕРАТУРЫ
1. Цветков
В.Н. Жесткоцепные полимеры. М.: Наука, 1986.
2. Павлов
Г.М., Зайцева И.И., Губарев А.А., Гаврилова И.И., Панарин, Е.Ф.// Журнал
прикладной химии. 2006. т. 79. вып. 9, С. 1506-1509.
3. Павлов
Г.М., Губарев А.А., Зайцева И.И., Сибилева М.А. // Журнал прикладной химии.
2006. т. 79. вып. 9, С. 1423-1428
4. Павлов
Г.М., Зайцева И.И., Губарев А.С., Корнеева Е.В., Гаврилова И.И., Панарин,
Е.Ф.// ДАН РАН 2008. т. 419, N6
5. Цветков
В.Н., Эскин В.Е., Френкель С.Я. Структура макромолекул в растворах. М.: Наука,
1964.
6. Gray
G., Bloomfield V., Hearst J.// J. Chem. Phys. 1967. V. 46
7. Fedors
R.F. //Polymer. 1979. V.20. P. 225-228.
. Flory
P. J. Chem. Phys. 21. 162. (1953).
.
Птицын О.Б., Высокомол. соед. 3, 1084, 1252, 1401 (1961).
10.
Katchalsky A., S.Lifson, J.Polymer Sci 5, 283 (1950).
.
Katchalsky A., O.Künzle, W.Kuhn, J. Polymer Sci.
5, 283 (1950)
.
Schuck
P. // Biophys. J. 2000. V.78. P.606-619.
.
Cantor C.R., Schimmel P.R. Biophysical chemistry. San Francisco: Freeman, 1980.
V. 2.
14. Schuck P.//
<http://www.analyticalultracentrifugation.com/images/sedfit.exe>
15. Смирнов
А.М., Зайцева И.И., Павлов Г.М. //Конференция ИВС 2008.
16. Смирнов
А.М., Зайцева И.И., Губарев А.С.//Конференция Физика и прогресс 2008.