Термодинамический анализ технической системы
КУРСОВАЯ РАБОТА
Термодинамический анализ
технической системы
Введение
эксергетический топливо выхлопной термодинамический
Сушкой называется термический процесс удаления из твердых
материалов или растворов содержащейся в них влаги путём её испарения.
Изделие или материал приходится сушить в зависимости от их
назначения для разных целей. Твёрдое топливо, например, подсушивают для
повышения теплоты сгорания, улучшения процесса горения, древесину - для
увеличения прочности, предохранение от гниения и плесени, различные другие
изделия - для облегчения обработки, увеличения долговечности, предотвращения
сжатия, искривления и растрескивания. Ряд материалов подвергается сушке для
уменьшения их веса и тем самым удешевления транспортировки, изменение физических
свойств (например, уменьшения теплопроводности).
Перечень материалов, подвергающихся в процессе их обработки
также и сушке, чрезвычайно велик. Глубина обезвоживания материала в каждом
отдельном случае определяется многими причинами.
В некоторых случаях перед сушкой материалов целесообразно
предварительное обезвоживания их механическим или физико-химическим способом.
Механическое обезвоживание материалов более экономно, чем
тепловая сушка, однако оно применимо только для материалов допуска, допускающих
деформация (торфяная масса, текстиль, шерсть и т.п.) При этом одно механическое
обезвоживание материала в большинстве случаев является недостаточным, так как
оно обеспечивает только частичное удаление свободной влаги. Поэтому часто
комбинируются различные способы удаления влаги.
Сушка материалов имеет большое распространение в различных
производствах. Назначение сушки может быть различным в зависимости от того,
какой материал подвергается этому процессу. В некоторых случаях она является
завершающей фазой технологического процесса, придает материалу свойства,
необходимые для его использования. Иногда сушка является промежуточной стадией
технологического процесса.
Сушка материала - это процесс удаления из него жидкости,
природа которой отлична от природы самого материала. В подавляющем большинстве
случаев удалению подлежит вода. Однако иногда из высушиваемого материала
удаляются другие жидкости.
Сушилки, работающие на смеси топочных газов с воздухом,
получили в настоящее время большое распространение. Топочные газы в большинстве
случаев получаются в специальных топках, и если они имеют высокую температуру,
то для получения сушильного агента с требуемой температурой их разбавляют
воздухом.
При полном сгорании (с избытком воздуха) горючей части
твердого или жидкого топлива, состоящей из углерода С, водорода Н и серы S,
продукты сгорания будут состоять из СО2, Н2О, SO3,
N2 и О2. В случае, если топливо не содержит серы,
продукты сгорания отличаются от чистого воздуха только некоторым содержанием
углекислоты и повышенным содержанием азота и водяных паров. Положение
значительно усложняется, если происходит неполное сгорание, так как в этом
случае продукты сгорания засорены не только сажей, т.е. частицами несгоревшего
углерода, но и продуктами сухой перегонки в виде СО и ряда углеводородов,
которые, как правило, химически активны, обладают специфическим запахом,
сравнительно низкой точкой кипения и т.д. Таким образом, одним из основных
требований применения сушки топочными газами является осуществление полного
сгорания.
Воздух и дымовые газы поступают в топку. Некоторое количество
дымовых газов поступает в камеру смешения. Основным отличием топок сушильных
установок от топок паровых котлов является то, что в них может иметь место
более низкая температура горения топлива. С целью защитить стенки топки от
действия высоких температур и улучшить горение коэффициент избытка воздуха при
сжигании твердого топлива принимают равным 2 - 2,5, а затем топочные газы
разбавляют воздухом или циркулирующей в сушилке смесью до требуемой
температуры.
Основное требование, предъявляемое к топочным устройствам
сушильных установок, состоит в том, чтобы в топке происходило полное сгорание
топлива без наличия сажи, а продукты сгорания содержали минимальное количество
частичек золы.
1.
Описание энергетического расчета системы
1.1 Расчет
горения топлива в воздухе. Расчет состава и удельного объема выхлопных газов
Природный газ является высокоэффективным энергоносителем и
ценным химическим сырьем. Он имеет ряд преимуществ по сравнению с другими
видами топлива и сырья:
стоимость добычи природного газа значительно ниже, чем других
видов топлива; производительность труда при его добыче выше, чем при добыче
нефти и угля;
отсутствие в природных газах оксида углерода предотвращает
возможность отравления людей при утечках газа;
при газовом отоплении городов и населенных пунктов гораздо
меньше загрязняется воздушный бассейн;
при работе на природном газе обеспечивается возможность
автоматизации процессов горения, достигаются высокие КПД;
высокие температуры в процессе горения (более 2000°С) и
удельная теплота сгорания позволяют эффективно применять природный газ в
качестве энергетического и технологического топлива.
Целью расчета горения топлива в воздухе является нахождение
состава дымовых газов, действительного объема и средней объемной изобарной
теплоемкости газов (температура выходных газов задана).
Целью расчета горения топлива в воздухе является нахождение
состава дымовых газов, его температуры и средней объемной изобарной
теплоемкости газов.
Объемный состав природного газа:
Плотность компонентов при нормальных условиях вычисляется по
следующей формуле [1, с. 36, формула (1.4)]:

где 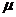 ,
,  - молярная масса компонента.
- молярная масса компонента.
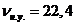
 - объем при нормальных условиях
- объем при нормальных условиях
 :
:

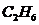 :
:

 :
:
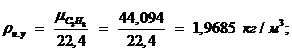
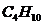 :
:
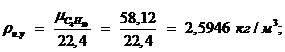
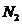 :
:
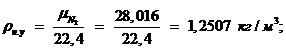
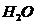 :
:

Теплоемкости компонентов топлива [1, с. 64]:

где 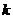 - показатель адиабаты;,
- показатель адиабаты;,  - универсальная газовая постоянная;-
объемная концентрация вещества.
- универсальная газовая постоянная;-
объемная концентрация вещества.
Таблица 1.1 - Объемный состав природного газа
|
Элемент
|
CH4
|
C 2H6
|
C3 H8
|
C 4H10
|
N2
|
H2O
|
|
Объёмное содержание r, %
|
80,4
|
9,0
|
5,0
|
3,7
|
1,2
|
0,7
|
|
Показатель адиабаты k
|
1,33
|
1,33
|
1,33
|
1,33
|
1,4
|
1,33
|
 :
:

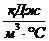 ;
;
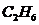 :
:
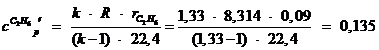
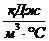 ;
;
 :
:

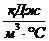 ;
;
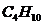 :
:
 ;
;
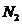 :
:

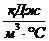 ;
;
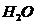 :
:

Общая теплоемкость топлива, кДж/(м К) [1, с. 179, формула (7.57)]:
К) [1, с. 179, формула (7.57)]:
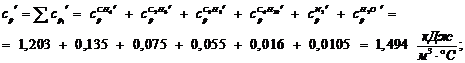
Физическая энтальпия топлива, кДж/м :
:

где tт - температура топлива.
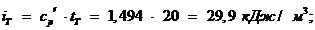
Состав сухого воздуха:
Таблица 1.2 - Объемный состав сухого воздуха
|
Элемент
|
N2
|
CO2
|
O2
|
Ar
|
|
Объёмное содержание r, %
|
78,09
|
0,03
|
20,95
|
0,93
|
|
Молярная масса µ, кг/кмоль
|
28
|
44
|
32
|
40
|
Молярная масса компонента рассчитывается по следующей
формуле, кг/ кмоль [1, с. 177, формула (7.45)]:
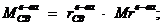
Содержание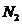 :
:

Содержание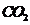 :
:

Содержание :
:

Содержание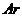 :
:

Содержание 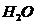 , соответствующее влагосодержанию 20 г./кг
[1, с. 314, формула 11.99]:
, соответствующее влагосодержанию 20 г./кг
[1, с. 314, формула 11.99]:


Влажный воздух содержит сухого воздухах [1, с. 309, формула
11.43]:
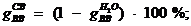
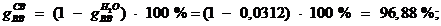
Молярная масса сухого воздуха, кг/кмоль [1, c. 177, формула 7.46]:

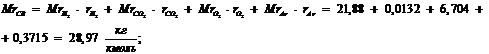
Состав влажного воздуха рассчитывается по следующим формулам [1,
с. 178, формула 7.50]:
Содержание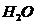 :
:


Содержание компонентов во влажном воздухе [1, с. 309, формула
11.49]:

Содержание
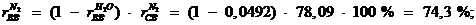
Содержание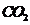 :
:

Содержание :
:

Содержание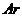 :
:

Теплоемкость влажного воздуха рассчитывается по следующей
формуле, кДж/ (м3 ˙ гр):

где 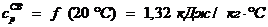 ;
;
 ;
;
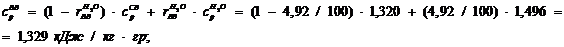
Энтальпия ВВ, кДж/м :
:
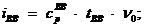
где  - действительный объем воздуха, м3/м3;
(формула );
- действительный объем воздуха, м3/м3;
(формула );

Теплота сгорания, кДж/м3 [4, c. 10, формула 2.10]
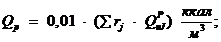

где  - объемный состав;
- объемный состав;
 - низшая теплота сгорания каждого компонента, ккал/м3
[4, с. 10]
- низшая теплота сгорания каждого компонента, ккал/м3
[4, с. 10]
 - низшая теплота сгорания метана;
- низшая теплота сгорания метана;
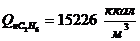 - низшая теплота сгорания этана;
- низшая теплота сгорания этана;
 - низшая теплота сгорания пропана;
- низшая теплота сгорания пропана;
 - низшая теплота сгорания бутана;
- низшая теплота сгорания бутана;

Коэффициент избытка воздуха  подбирается под содержание кислорода в сухих отходящих газах
(10%) -
подбирается под содержание кислорода в сухих отходящих газах
(10%) - 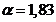 .
.
Теоретическое количество ВВ,  :
:
Теоретически необходимый объём
воздуха для полного сгорания 1 м3 топлива [4, с. 16, формула 4.13]:

где  - элемент состава природного газа;
- элемент состава природного газа;
m и n - количество атомов углерода и водорода
соответственно в молекулах углеводорода природного газа;
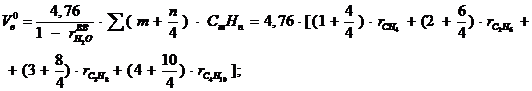
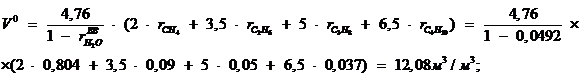
Теоретический объём 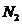 ,
,  , [4, с. 16,
формула 4.14]:
, [4, с. 16,
формула 4.14]:

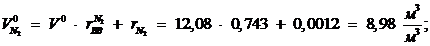
Теоретический объём  ,
,  [4, с. 16,
формула 4.15]:
[4, с. 16,
формула 4.15]:


Теоретический объём 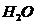 ,
,  : [4, с. 16, формула 4.16]:
: [4, с. 16, формула 4.16]:


Теоретический объём Ar,  : [4, с. 16, формула
4.9]:
: [4, с. 16, формула
4.9]:



Теоретический объём дымовых газов,  :
:

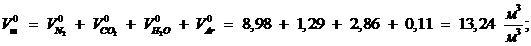
Действительный объем воздуха,  :
:
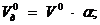

Действительный объём 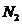 ,
,  :
:


Действительный объём 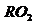 ,
,  :
:
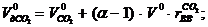


Действительный объём 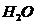 ,
,  :
:


Действительный объём  ,
,  :
:


Действительный объём 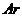 ,
,  :
:
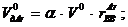


Теперь рассчитываем объем дымовых газов,  :
:


Содержание  в ДГ будет [1, с. 16, формула 4.9]:
в ДГ будет [1, с. 16, формула 4.9]:


Состав сухих дымовых газов действительного потока:






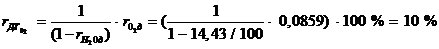


Смешение выхлопных газов с воздухом:

Рисунок 1.1 - Смешение потоков выхлопных газов и влажного воздуха
в T-s диаграмме

Рисунок 1.2 - Смешение потоков выхлопных газов и влажного воздуха
в p-v
диаграмме
Расход выхлопных газов определен выше (формула).

Состав выхлопных газов, который поступает на смешение с воздухом
[1, с. 176, формула (7.37)]:

Содержание азота:

Содержание трехатомных газов:

Содержание водяных паров:

Содержание кислорода рассчитано выше (формула).

Содержание аргона:

Температура выхлопных газов (задано) - 460˚С.
Средние объемные изобарные теплоемкости компонентов рассчитываются
по следующим формулам [1, с. 179, формула 7.57]:

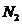 :
:

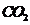 :
:

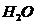 :
:

 :
:
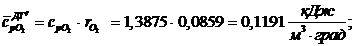
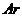 :
:

Объемные изобарные теплоемкости
веществ находятся как функции от температуры.
Общая объёмная изобарная теплоемкость ДГ, кДж/(м К):
К):


Находим расход воздуха на м3 ВГ:
Чтобы обеспечить сгорание топлива в топке с 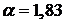 необходимо получить поток (смесь дымовых
газов с воздухом), в котором объемный процент кислорода
необходимо получить поток (смесь дымовых
газов с воздухом), в котором объемный процент кислорода  .
.
Если 13% >  , то
, то

иначе 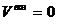 .
.
где 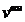 - удельный расход воздуха на 1 м³
топлива, м³/м³;
- удельный расход воздуха на 1 м³
топлива, м³/м³;
 - удельный расход ВГ на 1 м³, поступающего в ГТД, м³/м³ (формула);
- удельный расход ВГ на 1 м³, поступающего в ГТД, м³/м³ (формула);
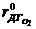 - объемное содержание кислорода в действительных дымовых
газах(формула);
- объемное содержание кислорода в действительных дымовых
газах(формула);
 - объемное содержание кислорода в поступающем воздухе (формула);
- объемное содержание кислорода в поступающем воздухе (формула);

Состав воздуха, поступающего на смешение, рассчитан выше
(формула).
Теплоемкость сухой компоненты и теплоемкость водяных паров
находятся в зависимости от температуры воздуха.
Теплоемкость влажного воздуха рассчитывается выше (формула ):
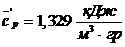 ;
;
Смесь дымовых газов с воздухом:
Расход смеси:
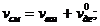
 ;
;
где  , м3/ м3 - расход воздуха;
, м3/ м3 - расход воздуха;
 , м3/ м3 - расход выхлопных газов.
, м3/ м3 - расход выхлопных газов.
Определяем объемный процент каждого компонента в смеси, иначе
говоря, находим ее состав [1, с. 177, формула 7.37]:

где  - процентное содержание i - го компонента
смеси, %;
- процентное содержание i - го компонента
смеси, %;
 - объем i - го компонента в дымовых газах, м³/м³;
- объем i - го компонента в дымовых газах, м³/м³;
 - объемный процент i - го компонента смеси, %;
- объемный процент i - го компонента смеси, %;
 - объем i - го компонента во влажном воздухе, м³/м³;
- объем i - го компонента во влажном воздухе, м³/м³;
Изобарная удельная теплоемкость смеси определяется как [1, с.
179, формула 7.57]:
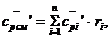
где  - средняя изобарная удельная объемная теплоемкость i-го компонента
в смеси, кДж/м3;
- средняя изобарная удельная объемная теплоемкость i-го компонента
в смеси, кДж/м3;
 - объемная доля i - го компонента в смеси, %.
- объемная доля i - го компонента в смеси, %.
Расчет смеси покажем на примере одного компонента смеси - N2:
Процентное содержание N2 в смеси:
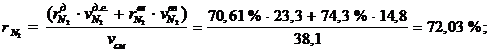
Средняя удельная теплоемкость компонента в смеси:
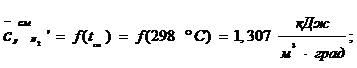
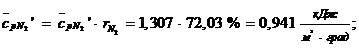
Результат расчета смеси дымовых газов дан в таблице 1.3.
Таблица 1.3 - Состав смеси дымовых газов с воздухом
|
Элемент
|
N2
|
RO2
|
H2O
|
Ar
|
O2
|
смесь
|
|
Объёмное содержание r, %
|
72,03
|
3,39
|
10,72
|
0,86
|
13
|
100
|
|
Удельная теплоемкость компонента в смеси,  0,9413 0,9413
|
0,0631
|
0,1654
|
0,0080
|
0,1766
|
1,354
|
|
|
Объём элемента Vi в смеси, м3/м3
|
27,5
|
1,3
|
4,1
|
0,3
|
5
|
38,1
|
Энтальпия выхлопных газов действительного состава на 1 м3
выхлопных газов:
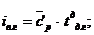
где 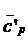 - средняя объёмная изобарная теплоемкость
дымовых газов (формула ).
- средняя объёмная изобарная теплоемкость
дымовых газов (формула ).
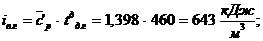
Энтальпия выхлопных газов действительного состава на 1 м3
природного газа:

Энтальпия вносимого влажного воздуха на метр воздуха:
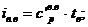
где  - теплоемкость влажного воздуха,
- теплоемкость влажного воздуха,  (формула);
(формула);
 - температура влажного воздуха.
- температура влажного воздуха.

Найдем температуру смеси:
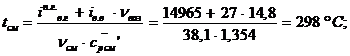
Находим энтальпию смеси:

 ;
;
1.2 Расчет
горения природного газа в атмосфере ВГ по схеме «воздух - модифицированное
топливо»
Для расчёта топки используем условную схему разделения потока
окислителя на балласт и воздух. Состав МТ представлен в Таблица 1.4.

ПГ - природный газ; окислитель - дымовые газы из ГТУ; ДГ -
дымовые газы после топки; РГ - реакция горения; балласт - негорючие элементы
окислителя.
Рисунок 1.3 - Расчётная схема горения топлива в окислителе для
топки
Состав модифицированного топлива определяем смешением
балласта и природного газа. Доля каждого компонента в модифицированном топливе
рассчитывается по формуле [1, стр. 309]:

где  - объёмная доля компонента в
модифицированном топливе;
- объёмная доля компонента в
модифицированном топливе;
 и
и  - соответственно объёмные доли компонента
в природном газе и в балласте;
- соответственно объёмные доли компонента
в природном газе и в балласте;
Таблица 1.4 - Состав модифицированного топлива
|
Состав модифицированного топлива
|
ПГ
|
Балласт
|
МТ
|
|
1
|
2
|
3
|
4
|
|
СО
|
0,0%
|
0%
|
0,0%
|
|
Н2
|
0,0%
|
0%
|
0,0%
|
|
СН4
|
79,3%
|
0%
|
9,5%
|
|
С2Н4
|
0,0%
|
0%
|
0,0%
|
|
С2Н6
|
8,9%
|
0%
|
1,1%
|
|
С3Н8
|
4,9%
|
0%
|
0,6%
|
|
С4Н10
|
3,7%
|
0%
|
0,4%
|
|
С5Н12
|
0,0%
|
0%
|
0,0%
|
|
СmНn*
|
0,0%
|
0%
|
0,0%
|
|
СО2
|
0,0%
|
9,7%
|
8,5%
|
|
О2
|
0,0%
|
0%
|
0,0%
|
|
N2
|
1,2%
|
67,9%
|
59,8%
|
|
Н2О
|
2,0%
|
21,6%
|
19,3%
|
|
H2S
|
0,0%
|
0%
|
0,0%
|
|
Ar
|
0%
|
0,81%
|
0,7%
|
|
|
|
|
|
|
|
Таблица 1.5 - Рабочая масса компонентов
|
Компонент природного газа
|
Молярная масса
|
Низшая теплота сгорания
|
Плотность при нормальных условиях
|
В расчет
|
|
|
Нормативный метод
|
Тымчак
|
|
|
|
кг/ кмоль
|
ккал/ м3
|
ккал/ м3
|
кг/ м3
|
%
|
|
СО
|
28,011
|
3018
|
3016
|
1,2505
|
0,0%
|
|
Н2
|
2,016
|
2579
|
2577
|
0,0900
|
0,0%
|
|
СН4
|
16,042
|
8555
|
8558
|
0,7162
|
9,5%
|
|
С2Н4
|
28,052
|
14107
|
14105
|
1,2523
|
0,0%
|
|
С2Н6
|
30,068
|
15226
|
15235
|
1,3423
|
1,1%
|
|
С3Н8
|
44,094
|
21795
|
21802
|
1,9685
|
0,6%
|
|
С4Н10
|
58,12
|
28338
|
28345
|
2,5946
|
0,4%
|
|
С5Н12
|
72,151
|
34890
|
34900
|
3,2210
|
0,0%
|
|
СmНn*
|
114,22
|
14107
|
17000
|
5,0991
|
0,0%
|
|
СО2
|
44,011
|
0
|
0
|
1,9648
|
8,5%
|
|
О2
|
32
|
0
|
0
|
1,4286
|
0,0%
|
|
N2
|
28,016
|
0
|
0
|
1,2507
|
59,8%
|
|
Н2О
|
18,016
|
0
|
0
|
0,8043
|
19,3%
|
|
H2S
|
34,082
|
5585
|
5534
|
1,5215
|
0,0%
|
|
Ar
|
39,948
|
0
|
0
|
1,7834
|
0,7%
|
|
Проверка материального состава топлива по
балансу
|
100%
|
Теплоемкость топлива, не зависящая от температуры:
Ср=1,374 кДж/ (м3 ˑ К);
Физическая энтальпия топлива, кДж/м3:
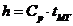
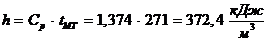 ;
;
где температура модифицированного топлива:
 0С;
0С;
где 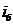 - энтальпия балласта, которая
рассчитывается следующим образом
- энтальпия балласта, которая
рассчитывается следующим образом
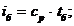
 - средняя объёмная изобарная теплоемкость газов;
- средняя объёмная изобарная теплоемкость газов;
 - температура балласта;
- температура балласта;
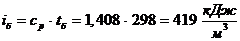 ;
;
Определяем коэффициент избытка воздуха модифицированного топлива α=1,155,
подбирается под заданный
кислород сухих отходящих газов.
Температура воздуха tв=298 0С, она совпадает
с температурой окислителя.
Температура топлива tт=271 0С, совпадает с
температурой модифицированного топлива, которая рассчитывалась выше.
Состав сухого воздуха задан выше (Таблица 1.2).
Состав влажного воздуха рассчитан выше (формула).
Исходя из этих данных, можем найти теплоемкость влажного воздуха:

где  = 1,542 кДж/ (м3ˑ 0С)
при t = 298 0С.
= 1,542 кДж/ (м3ˑ 0С)
при t = 298 0С.
 кДж/ (м3˙ 0С); ё
кДж/ (м3˙ 0С); ё
Энтальпия вносимого воздуха  кДж/м3;
кДж/м3;
Теплота сгорания топлива модифицированного топлива рассчитывается
аналогично теплоте сгорания природного газа (формула .
Результат расчета приведен в таблице 1.6:
Таблица 1.6 - Теплота сгорания модифицированного топлива
|
Теплота сгорания (Рассчитывается по составу)
|
Далее в расчетах используется
|
|
топлива: (теплота сгорания из норм. метода)
|
0
|
эта величина
|
|
влажного
|
ккал/м3
|
1115
|
кДж/м3
|
4667
|
|
|
|
сухого
|
ккал/м3
|
1524
|
кДж/м3
|
4667
|
|
|
|
Теплота сгорания высшая на рабочую массу
|
|
ккал/м3
|
1471,4721
|
|
Теплота сгорания высшая на рабочую массу
|
|
кДж/м3
|
6161,0535
|
|
Объем водяных паров при сжигании в сухом
воздухе
|
м3/м3
|
0,460824
|
|
Теплота парообразования водяных паров в д.г.
|
|
ккал/кг
|
600
|
Расчет количества воздуха, необходимого для горения
модифицированного топлива (формула ):
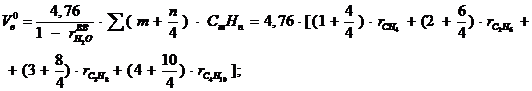

где состав задан в таблице 1.5.
Теоретические расходы газов рассчитываются аналогично, как при
горении природного газа (формулы , , , , ).
Расход воздуха и выход газов при горении топлива приведен в
(Таблице 1.7):
Таблица 1.7 - Расход воздуха и выход газов при горении топлива
|
Расход воздуха и выход газов при горении
топлива:
|
|
При сжигании 1 м3 газообразного
топлива:
|
Размерность
|
Значение
|
|
теоретическое количество влажного воздуха, V0
|
м3/м3
|
1,43
|
|
теоретический объём азота, VN20
объём трёхатомных газов, VRO2
|
м3/м3
|
1,66
|
|
м3/м3
|
0,24
|
|
теоретический объём водяных паров, VH2O0*)
|
м3/м3
|
0,53
|
|
теоретический объём аргона, VAr0*)
|
м3/м3
|
0,02
|
|
теоретический объём дым. газов, V0д
|
м3/м3
|
2,45
|
|
теоретическая масса воздуха, V0
теоретическая масса азота, VN20
|
кг/м3
|
1,816
|
|
кг/м3
|
2,078
|
|
теоретическая масса трёхатомных газов, VRO2
|
кг/м3
|
0,47
|
|
теоретическая масса водяных паров, VH2O0*)
|
кг/м3
|
0,43
|
|
теоретическая масса аргона, VAr0*)
|
кг/м3
|
0,04
|
|
теоретическая масса дымовых газов, V0д
|
кг/м3
|
3,01
|
|
плотность теоретических дымовых газов
|
кг/м3
|
1,228
|
|
содержание азота в теорет. прод. сгорания, VN20
|
% по объему
|
67,81%
|
|
содержание трёхатомных газов в - «-, VRO2
|
% по объему
|
9,70%
|
|
содержание водяных паров в - «-, VH2O0*)
|
% по объему
|
21,68%
|
|
содержание аргона в - «-, VH2O0*)
|
% по объему
|
0,81%
|
Действительные расходы газов рассчитываются аналогично, как при
горении природного газа (формулы , , , , , ).
Расчет дымовых газов приведен в (Таблица 1.8):
Таблица 1.8 - Расчет действительных дымовых газов
|
Действительные дымовые газы
|
|
При сжигании 1 м3 газообразного
топлива:
|
Размерность
|
Значение
|
|
действительный объем воздуха, Vвз
|
м3/м3
|
1,7
|
|
действительная масса воздуха, Gвз
|
кг/м3
|
2,1
|
|
избыточный объем воздуха, (альфа-1)*V0
|
м3/м3
|
0,2
|
|
избыточная масса воздуха, (альфа-1)*Gвз
|
кг/м3
|
0,3
|
|
действительный объём дымовых газов, Vг
|
м3/м3
|
2,672
|
|
действительная масса дымовых газов, Gг
|
кг/м3
|
3,3
|
|
плотность действительных дым. газов
|
кг/м3
|
1,231
|
|
объём азота в действительных д.г., VN2
|
м3/м3
|
1,83
|
|
объём трёхатомных газов в действ. д.г., VRO2
|
м3/м3
|
0,2378
|
|
объём водяных паров в действ. д.г., VH2O
|
м3/м3
|
0,5421
|
|
объём кислорода в действительных д.г., VO2
|
м3/м3
|
0,0442
|
|
объём аргона в действительных д.г., VAr
|
м3/м3
|
0,0146
|
|
Объем д. г.
|
м3/м3
|
2,665
|
|
азота, VN2
|
% объемн.
|
68,53%
|
|
трёхатомных газов, VRO2
|
% объемн.
|
8,92%
|
|
водяных паров, VH2O
|
% объемн.
|
20,34%
|
|
кислорода, VO2
|
% объемн.
|
1,66%
|
|
аргона VAr
|
% объемн.
|
0,55%
|
|
Баланс
|
% объемн.
|
100,0%
|
|
Состав сухих д.г. действительного потока
|
Процентное содержание
|
|
азота, VN2
|
% объемн.
|
86,0%
|
|
трёхатомных газов, VRO2
|
% объемн.
|
11,2%
|
|
водяных паров, VH2O
|
% объемн.
|
0,0%
|
|
кислорода, VO2
|
% объемн.
|
2,1%
|
|
аргона VAr
|
% объемн.
|
0,7%
|
|
Баланс 100,0%
|
Расчет адиабатной температуры горения:
Энтальпия дымовых газов на м3 топлива по низшей
теплоте сгорания:

где  - энтальпия вносимого воздуха;,
- энтальпия вносимого воздуха;,  - физическая энтальпия топлива в КУ;
- физическая энтальпия топлива в КУ;
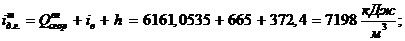
Энтальпия дымовых газов на м3 топлива на м3
воздуха:



Температура действительных дымовых газов:
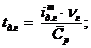
где 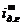 ,
, - энтальпия дымовых газов на м3
топлива по высшей теплоте сгорания;
- энтальпия дымовых газов на м3
топлива по высшей теплоте сгорания;
 ,
, - средняя объёмная изобарная теплоемкость газов;
- средняя объёмная изобарная теплоемкость газов;
 ˚С;
˚С;
Адиабатная температура горения:
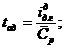
 ˚С;
˚С;
Результат расчета адиабатной температуры горения приведен в
(Таблица 1.9).
Таблица 1.9 - Расчет адиабатной температуры горения
|
Расчет адиабатной температуры горения
|
|
Расчетная температура горения (адиабатная)
|
|
1350
|
|
Теоретическая температура горения (адиабатная)
|
˚С
|
приближенная
|
1351
|
|
Средние объёмные изобарные теплоемкости газов:
|
кДж/ (м3ˑ гр)
|
1,5853
|
|
N2
|
0,9802012
|
кДж/ (м3ˑ гр)
|
1,4304
|
|
CO2
|
0,2054131
|
кДж/ (м3ˑ гр)
|
2,3020
|
|
H2O
|
0,3694135
|
кДж/ (м3ˑ гр)
|
1,8158
|
|
O2
|
0,0251337
|
кДж/ (м3ˑ гр)
|
1,5155
|
|
Ar
|
0,0051213
|
кДж/ (м3ˑ гр)
|
0,9335
|
|
по низшей теплоте сгорания
|
|
Энтальпия дымовых газов на м3
топлива
|
кДж/ м3
|
5705
|
|
Энтальпия дымовых газов на м3 дыма
|
кДж/ м3
|
2140,9
|
|
по высшей теплоте сгорания
|
|
Энтальпия дымовых газов на м3
топлива
|
кДж/ м3
|
7198
|
|
Температура дествительных дымовых газов
|
оС
|
1700
|
|
|
|
|
|
Расчет требуемого количества окислителя:
Требуемый расход окислителя:

где  - требуемый расход воздуха в окислителе
- требуемый расход воздуха в окислителе
 = 0,653 - количество воздуха ВГ в% от расхода смеси.
= 0,653 - количество воздуха ВГ в% от расхода смеси.
Требуемый расход воздуха в окислителе:
 ,
,
где  - расход ПГ на топку КУ (задаемся
расходом природного газа на топку 1 м3;
- расход ПГ на топку КУ (задаемся
расходом природного газа на топку 1 м3;
 - коэффициент избытка воздуха модифицированного топлива;
- коэффициент избытка воздуха модифицированного топлива;
 - теоретическое количество влажного воздуха в КУ;
- теоретическое количество влажного воздуха в КУ;

Минимальный расход окислителя, при котором обеспечивается заданная
концентрация кислорода на выходе топки, такая же, что и при горении ПГ с
коэффициентом избытка воздуха равном 1,155 определяется: расходом топлива в
топку КУ, требуемым коэффициентом избытка воздуха, теоретическим количеством воздуха
в окислителе, равном 65,3%, количеством балласта в окислителе, равном 34,7%.
Расчет требуемого расхода окислителя приведен в таблице (1.10)
Таблица 1.10 - Расчет требуемого расхода окислителя
|
Требуемый расход окислителя, обеспечивающий
концентрацию
|
м3/час
|
21
|
|
Заданный для репера коэффициент избытка воздуха
при горении ПГ
|
1,100
|
|
Заданная концентрация кислорода на выходе топки
с ПГ равна
|
1,67%
|
|
Коэффициент избытка воздуха модифицированного
топлива (подбирается)
|
1,155
|
|
с той концентрацией кислорода на выходе топки,
равной
|
1,66%
|
2. Расчет
элементов системы
2.1 Расчет камеры смешения
Так как при горении топлива весь расчет мы производили на 1 м3
модифицированного топлива, то реальный выход дымовых газов на 1м3
природного газа мы найдем как:
 ,
,
где 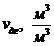 - объем действительных дымовых газов на 1
м3 модифицированного топлива (Таблица 1.8);
- объем действительных дымовых газов на 1
м3 модифицированного топлива (Таблица 1.8);
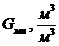 - расход МТ на 1м3 ПГ;
- расход МТ на 1м3 ПГ;
 ;
;
Составим материальный баланс и энергетический баланс, для
нахождения расхода в точках ДГ3 и gДГ1:

где  - присос воздуха в камеру смешения (7% от
- присос воздуха в камеру смешения (7% от
 ).
).
Решая систему, получим:
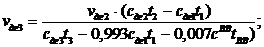
Для определения состава точки ДГ 3 смешиваем потоки дымовых
газов gДГ 1, при температуре 460 ˚С, и ДГ 2, при температуре 1350 ˚С,
на выходе получаем поток с новым составом и температурой 700 ˚С.
Составы точек ДГ 1 и Д Г2 рассчитаны выше.
Расчет состава точки ДГ 3 приведем на примере расчета одного
компонента смеси - N2:
Процентное содержание N2 в смеси:
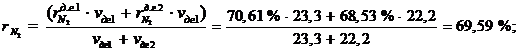
где 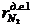 - содержание азота в потоке ДГ 1;
- содержание азота в потоке ДГ 1;
 - содержание азота в потоке ДГ 2;
- содержание азота в потоке ДГ 2;
Средняя удельная теплоемкость компонента в смеси:
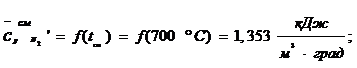

Результат расчета состава точки ДГ 3 приведен в таблице 2.1:
Таблица 2.1 - Состав и теплоемкость точки ДГ 3
|
Состав действительных д. г.
|
Доля
|
Процентное содержание
|
|
азота, VN2
|
% объемн.
|
69,59%
|
|
трёхатомных газов, VRO2
|
% объемн.
|
7,19%
|
|
водяных паров, VH2O
|
% объемн.
|
17,32%
|
|
кислорода, VO2
|
% объемн.
|
5,2%
|
|
Аргона VAr
|
% объемн.
|
0,8%
|
|
Баланс
|
% объемн.
|
100,00%
|
|
t=700˚С
|
|
|
|
Средние объёмные изобарные теплоемкости
газов:
|
кДж/ (м3 ˑ гр)
|
1,45727
|
|
N2
|
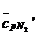 0,941861кДж/ (м3 ˑ
гр)1,3534 0,941861кДж/ (м3 ˑ
гр)1,3534
|
|
|
|
|
CO2
|
 0,150209кДж/ (м3 ˑ
гр)2,0890 0,150209кДж/ (м3 ˑ
гр)2,0890
|
|
|
|
|
H2O
|
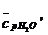 0,284219кДж/ (м3 ˑ
гр)1,6414 0,284219кДж/ (м3 ˑ
гр)1,6414
|
|
|
|
|
O2
|
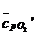 0,074468кДж/ (м3 ˑ
гр)1,4311 0,074468кДж/ (м3 ˑ
гр)1,4311
|
|
|
|
|
Ar
|
 0,006514кДж/ (м3 ˑ
гр)0,9335 0,006514кДж/ (м3 ˑ
гр)0,9335
|
|
|
|
|
|
|
|
|
|
Подставляя значения в формулу, получаем  = 87,21
= 87,21  ;
;
Из материального баланса имеем:
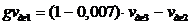 ;
;

 ;
;
Т.к. на 1 м3 природного газа приходится 23,27 м3/м3
дымовых газов (формула ), то удельный расход топлива на генерацию gДГ1:

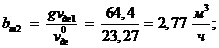
Аналогично находим удельный расход топлива на генерацию ДГ1:

Удельный расход топлива, подаваемый в топку приняли равным 1м3/ч.
2.2 Расчет
сушильной камеры
Материал - калийная соль;
Соль на входе:
Точка на схеме (Рисунок 2.2) - СМ1;
Температура t=140C;
Влажность на общую массу w1=6,1%;
Расход G=22 т/час;
Соль на выходе:
Точка на схеме (Рисунок 2.2) - СМ2;
Влажность на общую массу w2=0,1%;
Температура t=1350C;
Теплоемкость изобарная, удельная массовая (не зависит от
температуры) - Ср=0,693кДж/кг•0С;
Тракт сушильного агента:
Точка на схеме (Рисунок 2.2) - ДГ5;
Температура СА t=1500C;
Присосы воздуха:
ПВСК =1%;
Рассеяние энергии через ограждающие конструкции - 2%;
В первую очередь рассмотрим поток сушильного материала (калийная
соль).
Найдем количество влаги содержащейся в точке СМ1 [3, с. 11,
формула 1.6]:


где 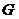 - расход до сушильной камеры, кг/час;
- расход до сушильной камеры, кг/час;
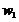 - влажность на общую массу (перед СК);
- влажность на общую массу (перед СК);
 - влажность на общую массу (после СК).
- влажность на общую массу (после СК).
Или в пересчете на объемный расход:
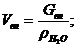

Количество калийной соли выходящее из сушильной камеры вычислим из
разности [3, с. 10, формула 1.5]:


Предположим, что на рециркуляцию поступает 56,6% от расхода после
сушильной камеры. Можно сказать, что состав дымовых газов в точках ДГ 4 и ДГ 5
будет одинаков в связи с тем, что состав в точках ДГ 4 и ДГ 5’ изменяется исключительно
из-за поступления влаги из калийной соли. Эта же влага удаляется в точке
раздела потока ДГ 5, так как она не может поступать на рециркуляцию. Влага
удаляется вместе с потоком дымовых газов ДГ 5’. Состав точки ДГ 4 приведен в
таблице (2.3). Состав точки ДГ 5 приведен в таблице (2.2)
Выше указанные предположения, знание состава дымовых газов в точке
ДГ 3 (состав дан в таблице (2.1)) и количества выделившейся влаги из калийной
соли позволяют нам найти средние объемные изобарные теплоемкости всех потоков
участвующих в рассматриваемой системе потоков сушильной камеры.
Для определения состава точки ДГ 4 смешиваем потоки дымовых газов
ДГ 5, при температуре 150 ˚С, и ДГ 3, при температуре 700 ˚С, на
выходе получаем поток с новым составом и температурой 510 ˚С.
Расчет состава точки ДГ 5 приведем на примере расчета одного
компонента смеси - N2:
Процентное содержание N2 в смеси:

Процентное содержание Н2O в смеси:

где  - содержание азота в потоке ДГ 3;
- содержание азота в потоке ДГ 3;
 , м3 - объем влаги,
выделившийся при сушке соли.
, м3 - объем влаги,
выделившийся при сушке соли.
Средняя удельная теплоемкость компонента в смеси:
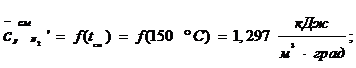

Таблица 2.2 - Результаты расчета состава и теплоёмкости для ДГ 5
|
Состав действительных дымовых газов
|
Доля
|
Процентное содержание
|
|
азота, VN2
|
% объемн.
|
69,55%
|
|
трёхатомных газов, VRO2
|
% объемн.
|
7,19%
|
|
водяных паров, VH2O
|
% объемн.
|
17,37%
|
|
кислорода, VO2
|
% объемн.
|
5,20%
|
|
аргона VAr
|
% объемн.
|
0,7%
|
|
Баланс
|
% объемн.
|
100,00%
|
|
t = 150 ˚С
|
|
|
|
Средние объёмные изобарные теплоемкости
газов:
|
кДж/ (м3 ˑ гр)
|
1,36601
|
|
N2
|
0,901972
|
кДж/ (м3 ˑ гр)
|
1,2969
|
|
CO2
|
0,125354
|
кДж/ (м3 ˑ гр)
|
1,7444
|
|
H2O
|
0,262954
|
кДж/ (м3 ˑ гр)
|
1,5141
|
|
O2
|
0,069223
|
кДж/ (м3 ˑ гр)
|
1,3312
|
|
Ar
|
0,006511
|
кДж/ (м3 ˑ гр)
|
0,9335
|
Зная состав точки ДГ 5, определяем состав точки ДГ 4:
Расчет состава точки ДГ 4 приведем на примере расчета одного
компонента смеси - N2:
Процентное содержание N2 в смеси:
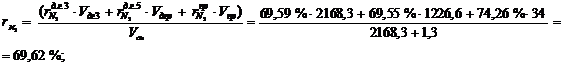
где  - содержание азота в потоке влажного
воздуха;
- содержание азота в потоке влажного
воздуха;
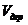 , м3 - объем дымовых газов,
идущих на рециркуляцию.
, м3 - объем дымовых газов,
идущих на рециркуляцию.
Средняя удельная теплоемкость компонента в смеси:
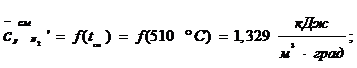
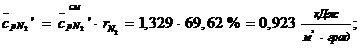
Таблица 2.3 - Результаты расчета теплоёмкости и состава для ДГ 4
|
Состав действительных
дымовых газов
|
Доля
|
Процентное содержание
|
|
азота, VN2
|
% объемн.
|
69,62%
|
|
трёхатомных газов, VRO
|
% объемн.
|
7,12%
|
|
водяных паров, VH2O
|
% объемн.
|
17,21%
|
|
кислорода, VO2
|
% объемн.
|
5,35%
|
|
аргона VAr
|
% объемн.
|
0,7%
|
|
Баланс
|
% объемн.
|
100,00%
|
|
t=510 ˚C
|
|
|
|
Средние объёмные изобарные теплоемкости
газов:
|
кДж/ (м3 ˑ гр)
|
1,42268
|
|
N2
|
0,925516
|
кДж/ (м3 ˑ гр)
|
1,3293
|
|
CO2
|
0,141990
|
кДж/ (м3 ˑ гр)
|
1,9948
|
|
H2O
|
0,273948
|
кДж/ (м3 ˑ гр)
|
1,5916
|
|
O2
|
0,074696
|
кДж/ (м3 ˑ гр)
|
1,3966
|
|
Ar
|
0,006528
|
кДж/ (м3 ˑ гр)
|
0,9335
|
Энергетический баланс сушильной камеры будет иметь вид:
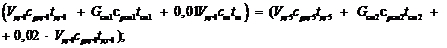
Приняв, ранее оговоренное 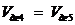 , выражаем из
, выражаем из  :
:
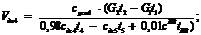

Запишем энергетический и материальный баланс для точки смешения
ДГ4, ДГ3 и ДГр (Рисунок 2.2):


Отсюда имеем:

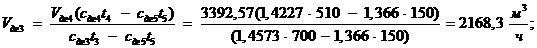
Подставляя 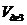 в материальный баланс, получаем:
в материальный баланс, получаем:


Найдя из расчета камеры смешения абсолютные величины объёмов можем
найти суммарный расход топлива:

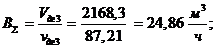
Расход топлива, поступающий на ДГ1:
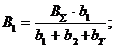
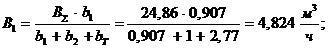
Расход топлива, поступающий на gДГ1:


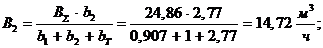
Расход топлива в топку:


Зная расход топлива можно определить абсолютные величины расходов:
2.3 Расчет
топки
Поскольку, расчет топки, выполненный в «Excel», мы выполняли
без учета присоса воздуха (0,4% от расхода окислителя) и рассеяния, через
ограждающие стенки топки (3,1%), необходимо пересчитать абсолютные величины
объёмов. Для этого составим энергетический баланс топки:

где Q, 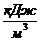 - теплота сгорания влажного топлива;
- теплота сгорания влажного топлива;
 - физическая энтальпия топлива;
- физическая энтальпия топлива;
 - присос воздуха в топку;
- присос воздуха в топку;
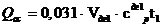 , м3 - рассеяние энергии через стенки.
, м3 - рассеяние энергии через стенки.
Откуда получим:
 = 535,3
= 535,3  ;
;
Из баланса камеры смешения , по пересчитанному  , находим
, находим  = 2168,32
= 2168,32  и
и  = 1656
= 1656  .
.
3. Балансы энергий
3.1 Баланс энергии топки
Баланс энергии для топки был расписан выше . Согласно рисунку 2.3
распишем потоки, входящие в топку и выходящие из неё.
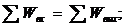
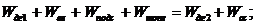
Распишем потоки энергий:
Входная энергия:


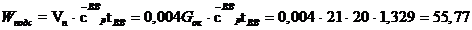

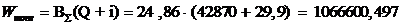

Выходная энергия:


Входная энергия:

Выходная энергия:

Дисбаланс 0%.
3.2 Баланс энергии камеры смешения
Баланс энергии для камеры смешения был расписан выше . Согласно
рисунку 2.1 распишем потоки, входящие в топку и выходящие из неё.
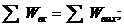

Распишем потоки энергий:
Входная энергия:
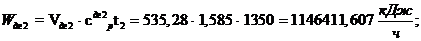


Выходная энергия:
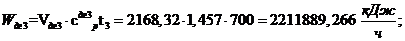
Входная энергия:
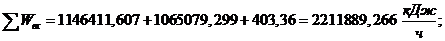
Выходная энергия:

Дисбаланс 0%.
3.3 Баланс сушильной камеры
Баланс энергии для сушильной камеры был расписан выше . Согласно
рисунку 2.2 распишем потоки, входящие в топку и выходящие из неё.

Распишем потоки энергий:
Входная энергия:



 ;
;
Выходная энергия:
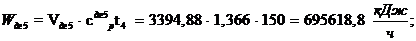


Входная энергия:

Выходная энергия:

Дисбаланс 0%.
3.4 Баланс всей системы
Для составления баланса всей системы распишем все потоки
энергий, входящие в систему и выходящие из неё, с учетом присосов энергии и
рассеяния энергии через ограждающие стенки всех элементов, входящих в систему.
Составим баланс энергии для всей системы:

Входная энергия:
 ,04
,04

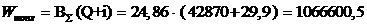

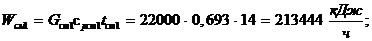
 ;
;
Выходная энергия:



 ;
;
Входная энергия:

Выходная энергия:

Дисбаланс 0,04%, что допустимо.
4. Эксергетический баланс системы
Эксергия - часть энергии, равная максимальной полезной
работе, которую может совершить термодинамическая система при переходе из
данного состояния в состояние равновесия с окружающей средой. Эксергией иногда
называется работоспособность системы. Использование понятия эксергии даёт
возможность количественно определить влияние неравновесия термодинамических
процессов на эффективность преобразования энергии, то есть позволяет вычислять
особенности второго начала термодинамики: выделить ту часть энергии, которая не
может быть использована из-за газодинамических явлений, трения, теплообмена.
Такой подход даёт возможность анализировать степень термодинамической
доскональности того или другого элемента установки и не требует предварительной
оценки работоспособности всей установки в целом.
4.1 Методика эксергетического расчета
Эксергия топлива,  , [2, с. 220, формула 18.101]
, [2, с. 220, формула 18.101]

где  , кДж/м3 - высшая теплота
сгорания топлива;
, кДж/м3 - высшая теплота
сгорания топлива;
Эксергия дымовых газов:
Концентрационная составляющая эксергии дымовых газов [2, с.
210, формула 18.57]

где T0, К - температура окружающей среды;
 - содержание i - го элемента
в дымовых газах;
- содержание i - го элемента
в дымовых газах;
Ri - универсальная газовая постоянная;
Термомеханическая составляющая эксергии дымовых газов [2, с.
210, формула 18.57]

где T0, К - температура окружающей среды;
 - энтропия дымовых газов, при температуре потока;
- энтропия дымовых газов, при температуре потока;
 - энтропия дымовых газов, при температуре окружающей среды;
- энтропия дымовых газов, при температуре окружающей среды;
R - универсальная газовая постоянная;
Полная эксергия дымовых газов,  :
:

Потери эксергии,  :
:

где 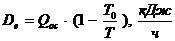 - внешние потери эксергии [2, с. 282,
формула 8.260];
- внешние потери эксергии [2, с. 282,
формула 8.260];
 - внутренние потери эксергии;
- внутренние потери эксергии;
4.2 Эксергетический расчет топки
Аналогично тому, как расписывались потоки, при составлении
энергетического баланса топки, рассчитаем эксергии потоков входящих и выходящих
из топки, согласно рисунку (2.3).
Эксергия топлива:

Термомеханическая составляющая:
Эксергия в точке ДГ 1:

Эксергия в точке ДГ 2:

Термомеханическая составляющая эксергии рассеяния в окружающую
среду:

Концентрационная составляющая:
Эксергия в точке ДГ 1:
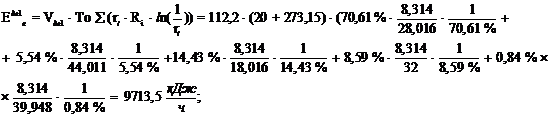
Эксергия в точке ДГ 2:

Эксергия рассеяния в окружающую среду:

Полная эксергия потока ДГ 1:

Полная эксергия потока ДГ 2:
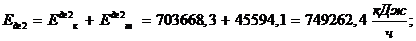
Полная эксергия потока рассеяния:

Потери эксергии:

Внешние потери эксергии:
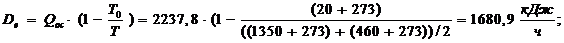
Внутренние потери эксергии:

Результаты расчета приведены в таблице (4.1):
Таблица 4.1 - Результат расчета эксергии топки
|
Составляющая эксергии
|
EТВ, МДж/ч
|
ЕДГ1, МДж/ч
|
ЕВЗ, МДж/ч
|
EДГ2, МДж/ч
|
EП, МДж/ч
|
Eос, МДж/ч
|
|
Термомеханическая
|
-
|
26,9
|
0
|
703,7
|
0
|
0,83
|
|
Концентрационная
|
-
|
9,6
|
0
|
45,6
|
0
|
1,24
|
|
Полная
|
1297,3
|
36,5
|
0
|
749,3
|
0
|
2,07
|
|
Потери
|
 =1,68 МДж/ч =1,68 МДж/ч =581 Дж/ч =581 Дж/ч
|
|
.3 Эксергетический расчет камеры смешения
Аналогично тому, как расписывались потоки, при составлении
энергетического баланса камеры смешения, рассчитаем эксергии потоков входящих и
выходящих из элемента, согласно рисунку (2.1). Результаты расчета приведены в
таблице (4.2):
Таблица 4.2 - Результат расчета эксергии камеры смешения
|
Составляющая эксергии
|
ЕДГ2, МДж/ ч
|
ЕgДГ1, МДж/ ч
|
EДГ3, МДж/ ч
|
EП, МДж/ ч
|
Eос, МДж/ ч
|
|
Термомеханическая
|
703,7
|
396,7
|
1037,5
|
0
|
0,02
|
|
Концентрационная
|
45,6
|
143,2
|
214,6
|
0
|
0,08
|
|
Полная
|
749,3
|
539,9
|
1251,1
|
0
|
1
|
|
Потери
|
 =0,1 МДж/ ч =0,1 МДж/ ч =38 Дж/ ч =38 Дж/ ч
|
|
|
|
|
|
|
|
|
4.4 Эксергетический расчет сушильной камеры
Аналогично тому, как расписывались потоки, при составлении
энергетического баланса камеры сушильной камеры, рассчитаем эксергии потоков
входящих и выходящих из элемента, согласно рисунку (2.2). Результаты расчета
приведены в таблице (4.3):
Таблица 4.3 - Результат расчета эксергии сушильной камеры
|
Составляющая эксергии
|
Eдг4, МДж/ ч
|
Едг5, МДж/ ч
|
Есм1, МДж/ ч
|
Eсм2, МДж/ ч
|
EП, МДж/ч
|
Eос, МДж/ ч
|
|
Термомеханическая
|
975,60
|
103,90
|
-
|
-
|
0
|
2,08
|
|
Концентрационная
|
275,80
|
336,60
|
-
|
-
|
0
|
6,70
|
|
Полная
|
1251,40
|
440,50
|
4426,40
|
4156,40
|
0
|
8,78
|
|
Потери
|
 =28,8 МДж/ ч =28,8 МДж/ ч =1045,0 МДж/ ч =1045,0 МДж/ ч
|
|
Эксергию калийной соли принимаем постоянной, равной 201,2  , [2, с. 517]
, [2, с. 517]
4.5 Эксергетический КПД системы
Эксергетический КПД [2, с. 232, формула (18.134)]:


Заключение
В данной курсовой работе были рассчитаны все основные
характеристики сушильной установки с дымовыми газами в качестве сушильного
агента. Установлены параметры рабочего тела в характерных точках системы, его
физические характеристики и составы. Рассчитаны параметры элементов технической
системы. Также построены полосовые диаграммы Сэнки и Грассмана.
Были рассчитаны расходы дымовых газов. Это позволило
составить энергетические балансы, как всей системы, так и каждого элемента в
частности. Рассчитать потери энергии в окружающею среду через ограждающие
конструкции. В итоге найден общий расход топлива, который составил Bт=24,86 м3/ч.
Были составлены эксергетические балансы системы, отдельных
элементов. Вычислены потери эксергии каждого компонента. В итоге
эксергетический КПД сушильной установки 
Список
использованных источников
1. Хрусталев,
Б.М. Техническая термодинамика: учеб.: в 2 ч. / Б.М. Хрусталев, А.П. Несенчук,
В.Н Романюк. - Минск: УП «Технопринт», 2004. -
Ч. 1. - 487 с.
. Хрусталев,
Б.М. Техническая термодинамика: учеб.: в 2 ч. / Б.М. Хрусталев, А.П. Несенчук,
В.Н Романюк. - Минск: УП «Технопринт», 2004. - Ч. 2. - 560 с.
3. Филоненко
Г.К., Лебедев П.Д. Сушильные установки. - Москва: «Госэнергоиздат», 1952. - 296
с.
. Кузнецов,
Н.В. Тепловой расчет котельных аппаратов. - Москва: «Энергия», 1973. - 265 с.