Индустриализация применения методов неразрушающего контроля
ОГЛАВЛЕНИЕ
СПИСОК СОКРАЩЕНИЙ.. 3
ВВЕДЕНИЕ. 4
ОБЗОР ЛИТЕРАТУРЫ.. 5
1.1 Классификация гастритов. 5
1.2Определение атрофического гастрита. 5
1.3 Классификация и этиология
атрофического гастрита. 6
1.4 Клинические проявления. 9
1.5 Методы исследования. 10
1.6 Лабораторные маркеры
атрофического гастрита. 11
1.6.1 Диагностика инфекции
Helicobacter pylori 12
1.7 Диагностика. 13
2.1 Нейтрофильные гранулоциты.. 14
2.1 Функции нейтрофилов. 15
3.1 Хемилюминесцентный анализ оценки
активности нейтрофильных гранулоцитов 17
3.2 Основные стадии
хемилюминесцентного анализа. 18
3.3 Свободные радикалы
хемилюминесценции клеток. 19
3.4 Применение хемилюминесцентного
анализа. 20
МАТЕРИАЛЫ И МЕТОДЫ.. 21
4.1 Объект исследования. 21
4.2 Хемилюминесцентный анализ. 21
4.2.1Реактивы.. 21
4.2.2 Принцип действия
хемилюминесцентного анализа. 21
4.2.3Методика определения
хемилюминесценции. 22
4.2.4 Расчеты.. 23
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ. 24
ЗАКЛЮЧЕНИЕ. 25
РЕФЕРАТ(SUMMARY) 26
АГ – Атрофический гастрит
ХЛ – Хемилюминесценция
СР – Свободный радикал
ХЛсп – Спонтанная
хемилюминесценция
ХЛакт – Активированная
хемилюминесценция
Ихл – Индекс
хемилюминесценции
АФК – Активные формы
кислорода
СОЖ – Слизистая оболочка
желудка
Н.Р.- Helicobacterpylori
В настоящее время проблема заболевания раком желудка во
всем мире остается очень актуальной. Из анализа международных данных видно, что
сохраняется тенденция к росту числа онкологических заболеваний желудочно-кишечного
тракта. Ежегодно в мире регистрируется 1,1 млн случаев рака желудка.[[1]]
Среди предполагаемых предраковых заболеваний наибольшее
значение имеет длительно существующий хронический атрофический гастрит (АГ).
После принятия Сиднейской системы различают два варианта атрофического
гастрита: инфекционный (ассоциированный с Helicobacter pylori – (Н.Р.)),
развивающийся в антральном отделе желудка, и аутоиммунный, развивающийся
исключительно в теле желудка.[1]
Диагностика и лечение атрофического гастрита до сих
пор представляется большинству врачей банальным процессом, не имеющим новизны и
проблем. Однако именно проблема ранней и точной диагностики атрофического
гастрита, является краеугольным камнем проблемы профилактики рака желудка.[[2]]
Самая исследуемая и
самая информативная из сред организма является кровь. Современная лабораторная
диагностика показателей крови даёт более 60% информации о пациенте. В первую
очередь, любая патология отражается на обменных процессах в организме вообще и
на состоянии иммунного (антигенного) статуса в частности.[[3]]
Центральная роль в
иммунном ответе всегда принадлежит лейкоцитам, в том числе нейтрофилам.
Нейтрофильный ответ - самый первый ответ на бактериальные и многие другие
инфекции. Нейтрофильный ответ при острых воспалениях и инфекциях всегда
предшествует более специфическому лимфоцитарному ответу.[[4]]
Целью моей работы
является определение особенностей хемилюминесцентной активности нейтрофильных
гранулоцитов у больных атрофическим гастритом.
На основании
поставленной цели были определены следующие задачи:
1.
Составить обзор литературы по данной проблеме.
2.
Определить хемилюминесцентную активность нейтрофилов в группе у больных
атрофических гастритом
«В 1990 г. в Сиднее (Австралия)
была принята новая классификация гастритов, получившая названия Сиднейской
системы, согласно которой диагноз гастрита должен формулироваться на основании
4–х признаков заболевания:
1. Локализация
патологического процесса.
2. Гистологические
признаки, выявленные при исследовании биоптатов.
3. Макроскопические
признаки, выявленные при эндоскопии.
4. Вероятные
этиологические факторы.
Более поздняя Хьюстоновская
классификация внесла в Сиднейскую систему важные дополнения, в соответствии с
которыми различают:
•
Хронический неатрофический гастрит (прежде всего вызванный H. Р.)
•
Хронический атрофический гастрит
•
Мультифокальный гастрит (как исход длительно текущего гастрита,
ассоциированного с H.Р.)
•
Аутоиммунный гастрит
•
Особые формы гастрита.» [[5]]
Таблица 1 - "Сиднейская
система" классификация хронических гастритов[5]
|
Тип
|
Топография
|
Эндоскопические категории
|
Этиология
|
|
Острый
Хронический
|
Антральный
Фундальный
Пангастрит
|
Эритематозный
Эрозивный
Геморрагический
Гиперплазия складок
|
Аутоимунный – тип А
Ассоциированный с НР – тип В
Реактивный – тип С
Особые формы
|
|
Кроме того, выделяют фазы: ремиссии и обострения, стадии –
компенсации и декомпенсации
|
1.2Определение атрофического гастрита
Атрофический гастрит представляет собой
заболевание, протекающее бессимптомно или проявляющееся неспецифической
симптоматикой в течение многих лет и часто остающееся не
диагностированным. Многочисленные исследования показали, что риск развития
рака желудка повышается параллельно тяжести атрофического гастрита,
а вероятность развития рака желудка прямо пропорциональна степени
атрофических изменений, выявляемых одновременно в антральном отделе
и в теле желудка.[[6]]
Атрофический гастрит (также известный как гастрит
типа А или В) – хронический воспалительный процесс в слизистой желудка, который
ведет к потере железистых клеток желудка и их замещению интерстициальной и
фиброзной тканью. В результате этих изменений желудочная секреция таких
веществ, как соляная кислота, пепсин и др. исчезает, что способствует
расстройствам пищеварения, недостаточности витамина В12. Данные изменения, в
свою очередь, могут привести к возникновению мегалобластической и
железодефицитной анемии. Кроме аутоиммунных процессов в возникновении
атрофического гастрита большую роль играет инфекция Helicobacter pylori.
Доказано, что атрофический гастрит является причиной развития желудочной карциномы.
Гастрит типа А, как правило, первично локализуется в теле желудка, и при данном
виде заболевания прослеживается четкая взаимосвязь с развитием пернициозной
анемии. Гастрит типа В наиболее часто локализуется в привратниковой области
желудка и в большинстве случаев связан с инфекцией H. Р. [[7]]
Условно в желудке различают 4 отдела:
1. Кардиальный
отдел – самый начальный отдел, в который переходит пищевод.
2. Свод (дно,
фундальный отдел) – куполообразная часть желудка, расположенная в самом верху.
3. Тело
желудка – отдел, где пища находится во время переваривания.
4. Пилорическая
(привратниковая) часть, она заканчивается пилорическим сфинктером,
ограничивающим полость желудка от полости двенадцатиперстной кишки.
Атрофия может затрагивать все отделы желудка или каждый из них в
отдельности. В этой связи патоморфологи
выделяют «диффузный» (фундальный, антральный или тотальный), а также
«мультифокальный» атрофический гастрит. Физиологические и клинические
проявления атрофии в разных отделах желудка могут быть совершенно разными [[8]]; СОЖ
фундального отдела желудка, как его основная функциональная составляющая часть,
представлена тремя основными популяциями клеток: добавочными –
слизеобразующими, вырабатывающими муцин, париетальными, секретирующими соляную
кислоту и главными – продуцирующими пепсины [5].
Атрофический процесс может захватывать как все железы, так и
избирательно поражать те или иные клетки. Так, описаны формы аутоиммунного
гастрита, поражающего только париетальные клетки. Атрофия желез заключается в
уменьшении численности клеток, продуцирующих пепсины, и париетальных клеток,
выделяющих соляную кислоту. Атрофия может затрагивать одну или обе популяции
клеток, число которых меняется независимо друг от друга. Атрофия желез тела
желудка может быть компенсирована за счет увеличения его объема, увеличения
высоты складок, гипертрофии СОЖ антрального отдела и появления в составе
антральных желез париетальных клеток. Однако такой компенсации может и не быть,
и атрофия СОЖ может охватывать весь желудок. [5]
Таким образом, на фоне существования десятков причин и
морфофункциональных вариантов атрофии, Диагноз «хронический атрофический
гастрит» является лишь собирательным понятием, который совершенно не отражает
реальную картину структурной организации желудка и физиологию желудочной
секреции.[5]
Атрофический гастрит – мультифакторное
состояние. Существует более десятка причин, каждая из которых способна
приводить к атрофии слизистой оболочки и, соответственно, к развитию
функциональной недостаточности желудка. Развитие атрофических изменений в слизистой
оболочки (СОЖ) может быть результатом патологического процесса или возрастных
инволюционных изменений, также возможна генетически обусловленная гипо– или
атрофия СОЖ.[5]
Наиболее частыми этиологическими факторами, вызывающими атрофический
гастрит, признаны инфекция Helicobacter pylori и аутоиммунный гастрит, который
встречается реже чем Н.Р. [[9]].
•
Атрофический гастрит, ассоциированный с Helicobacter pylori
С Н. Р. связывают возникновение
подавляющего большинства атрофических гастритов. Бактерии Н. Р, персистируя на
желудочном эпителии, вызывают хронический хеликобактерный поверхностный
гастрит. Длительно существующий поверхностный хеликобактерный гастрит без
соответствующего лечения трансформируется в атрофический. Мультифокальный
атрофический гастрит характеризуется вовлечением тела и антрального отдела
желудка с прогрессирующим развитием атрофических изменений слизистой –
уменьшением количества желез и их частичным замещением кишечным эпителием
(кишечная метаплазия). Пациенты с данным видом хронического гастрита имеют
повышенный риск развития карциномы желудка.[5]
•
Аутоиммунный хронический атрофический гастрит.
Данный тип хронического гастрита связан с образованием аутоантител (к
париеталным клеткам и внутреннему фактору Касла). Антитела связываются с
микроворсинками париетальных клеток и делают невозможным соединение витамина
В12с внутренним фактором Касла. Считается, что выработка антител к H+K+–АТФазе
париетальных клеток является одной из причин ахлоргидрии. Повреждение
антителами собственных (фундальных) желез приводит к их потере. При этом в теле
и дне желудка развивается прогрессивная атрофия главных и париетальных клеток с
недостаточностью внутреннего фактора Кастла, что может приводить к пернициозной
анемии.[5]
Аутоиммунный гастрит часто сочетается с другой аутоиммунной патологией
и нередко развивается в рамках так называемого аутоиммунного полигландулярного
синдрома [5].
Гистологические изменения при аутоиммунном атрофическом гастрите
зависят от фазы заболевания:
а) в раннюю фазу отмечается многоочаговая диффузная инфильтрация собственной пластинки мононуклеарными
клетками и эозинофилами, а также очаговая Т–клеточная инфильтрация собственных
желез желудка с их разрушением. Наблюдают очаговую гиперплазию мукоидных клеток
(псевдопилорическая метаплазия), а также гипертрофические изменения
париетальных клеток;[5]
б) в более позднюю фазу заболевания усиливается лимфоцитарное
воспаление, атрофия собственных желез желудка и очаговая кишечная метаплазия.[5]
Последняя стадия характеризуется диффузным атрофическим гастритом с
вовлечением тела и дна желудка с небольшими явлениями кишечной метаплазии.
Антральный отдел не поражен.[5]
Клинические проявления формируются как местными, так и общими
расстройствами, развивающимися в периоды обострений. Местные проявления
связаны, как правило, с нарушением эвакуации из желудка (тяжесть, давление,
полнота в эпигастральной области, появляющиеся или усиливающиеся во время или
вскоре после еды; отрыжка, срыгивание, тошнота, изжога — при повышении
внутрижелудочного давления). Они, как правило, характерны либо для гастрита
выходного отдела желудка, либо для диффузных форм. У больных с H.Р.-ассоциированным
гастритом в фазу повышенной желудочной секреции выделяют другие варианты
клинического течения.[[10]]
«Из–за выраженного снижения функциональной активности желудка, при
атрофическом гастрите ведущим является синдром диспепсии, в отличие от
гиперацидного гастрита, где преобладает болевой синдром.
1. Синдром диспепсии: ухудшение аппетита, отрыжка воздухом или тухлой
пищей, тошнота. Характерно чувство тяжести, переполнения желудка, кокосмия
(плохой запах изо рта), слюнотечение, неприятный привкус во рту.
2. Синдром избыточного бактериального роста также часто лидирует в
клинической картине. Его развитие связано с нарушением бактерицидной функции
соляной кислоты. Проявляется он урчанием, вздутием в животе, непереносимостью
молочных продуктов, неустойчивым стулом. При частых поносах может наступить
похудание, анемия.
3. Анемический синдром связан:
а) с нарушением всасывания витамина В12 из–за снижения выработки
внутреннего фактора Касла;
б) и/или железа (нарушение процесса восстановления трехвалентного
железа в двухвалентное под действием соляной кислоты);
в) фолиеводефицитная анемия может развиваться из–за нарушений кишечной
микрофлоры.
4. Также имеет место болевой синдром, но связанный не со спазмом
гладкой мускулатуры, а с растяжением желудка из–за нарушения эвакуаторной
функции желудка. Боли, как правило, тупые, ноющие, усиливающиеся после приема
пищи, без четкой локализации (т.е. носят не спастический, как при гиперацидном
гастрите, а дистензионный характер).
5. Дистрофический синдром, обусловленный полигиповитаминозами
(Р,С,А,Д), белковой недостаточностью, вследствие нарушения переваривания
белков.
При осмотре: атрофичный «полированный язык», при обострениях – язык
обложен густым белым налетом. При пальпации болезненность обычно отсутствует.
Секреция прогрессивно снижается вплоть до ахлоргидрии. Часто
присоединяется сопутствующая патология: панкреатит, холецистит, энтероколит.»[5]
«Неизменным следствием атрофии СОЖ является функциональная
недостаточность желудка, что определяет довольно широкую гамму клинических
проявлений.
Основными
функциями желудка являются:
1.
Депонирование пищи.
2.
Частичное переваривание. В желудке начинается переваривание белков и
клетчатки.
• Под действием
соляной кислоты денатурируются белки и набухает растительная клетчатка.
• Под
действием пепсина и гастриксина белки расщепляются до пептидов и аминокислот.
Пепсин вырабатывается главными клетками в виде пепсиногена, который под
воздействием соляной кислоты переходит в активную форму.
3.
Частичное всасывание. В желудке могут всасываться некоторые лекарства
(ацетилсалициловая кислота) и алкоголь.
4.
Проведение пищи до кишечника. Пища в среднем находится в желудка 3–10
часов. Причем жидкость эвакуируется незамедлительно, дольше всего задерживается
жирная пища. Блуждающие нервы усиливают мышечную активность, а симпатические
уменьшают.
5.
Бактерицидная функция реализуется за счет действия соляной кислоты.
Поэтому неизменным спутником гипоацидных состояний, а также длительного приема ингибиторов
протонной помпы (омепразол) является дисбактериоз.
6.
Кроветворная функция (синтез внутреннего фактора Кастла).»[5]
В начале 1980-х годов американский гастроэнтеролог M. Samloff предложил
серологическое определение пепсиногена, проэнзима пепсинов, как простой неинвазивный
метод оценки желудочной секреции. Им была показана тесная корреляция между
уровнем сывороточного пепсиногена и тяжестью поражения слизистой оболочки
желудка (СОЖ), подтвержденной морфологически, что позволило рассматривать
сывороточный пепсиноген в качестве маркѐра атрофии СОЖ [[11]].
Пепсиноген, секретируемый в желудке, можно подразделить на 2 группы в
соответствии с иммунологическими свойствами: пепсиноген-1 (ПГ1) и пепсиноген-2
(ПГ2). ПГ1 вырабатывается исключительно главными клетками дна и тела желудка, в
то время как ПГ2 секретируется муцинообразующими клетками желез всех отделов
желудка, а также дуоденальных Бруннеровых желез. Поэтому исследование уровня
ПГ1 дает информацию о состоянии желез тела и фундального отдела желудка, а ПГ2
всех отделов желудка, их соотношение ПГ1/ПГ2 также может отражать
функциональный статус желудка.[1]
Гастрин по сути неоднороден и
включает карбоксиамидированные гастрины-71, −52, −34,−17,
−14 и −6. Они циркулируют в крови в сульфатированной и
несульфатированной формах. Основными циркулирующими формами являются гастрин-17
(Г-17) и гастрин-34 (состоящие соответственно из 17-ти и 34-х аминокислот). В
СОЖ антрального отдела гастрин представлен на 90 % в виде Г-17. Именно Г-17,
являясь основным регулирующим продукцию НСl гормоном, с одной стороны, может
меняться в зависимости от уровня желудочной секреции (повышаться при ее
снижении и снижаться при повышении),с другой — косвенно отражает функциональные
возможности антрального отдела [[12]].
Основываясь на вышеизложенных функциональных особенностях СОЖ,
финскими учеными была создана тестовая система «GastroPanel». С помощью
«GastroPanel» по анализу крови можно определить состояние и функциональную
активность всей СОЖ. Этот метод исследования является неинвазивным, безопасным
и удобным для пациента.[1]
1. В последние годы все большую популярность получает метод
исследования содержания в сыворотке крови пепсиногена I, пепсиногена II и
гастрина–17 в качестве маркеров атрофии СОЖ фундального и антрального отделов
желудка. Этот малоинвазивный метод позволил выделить несколько разновидностей
атрофического гастрита в теле желудка и в антральном отделе. Пепсиноген I и II
синтезируются и секретируются главными клетками желудка. После попадания в
просвет желудка они превращаются в протеолитический фермент пепсин. Снижение
уровня пепсиногена I коррелирует со снижением количества главных клеток при
атрофии слизистой желудка. Измерение уровней пепсиногена I и пепсиногена II, а
также их соотношения в сыворотке крови используется в качестве скринингового
метода для выявления атрофического гастрита и рака желудка. Чувствительность и
специфичность данного метода относительно невелика (84,6 и 73,5%
соответственно) [[13]].
2. Определение антипариетальных антител и антител к внутреннему
фактору Кастла в сыворотке крови.[13]
Антипариетальные антитела направлены против микросомальных компонентов
париетальных клеток желудка. Тест положителен у 95% пациентов с пернициозной
анемией, хотя специфичность теста низкая. Антитела к париетальным клеткам
присутствуют у 25–30% пациентов с аутоиммунным тиреоидитом.[13]
При определении антител к внутреннему фактору следует не допускать
введения витамина В12 в течение 48 часов перед взятием образца. Антитела к
внутреннему фактору могут присутствовать у 3–6% людей с гипертироидизмом или
инсулинозависимым диабетом.[13]
3. Определение уровня гастрина в сыворотке крови.
Для аутоиммунного хронического гастрита характерно повышение уровня
гастрина. Необходимо проведение дифференциальной диагностики с гастриномой
(синдром Золлингера–Эллисона).[13]
Диагностика Helicobacter pylori необходима при любом гастрите. Она
помогает выявить причину поражения желудка, т.к. в большинстве случаев
этиологическим фактором атрофии признанна длительно текущая инфекция
Helicobacter pylori. Существуют 2 группы методов – прямые и косвенные.[[14]] Следует
помнить, что достоверность тестов зависит от выбранного метода и используемых
методик и реактивов.[13]
«Золотым стандартом» достоверности признано морфологическое
исследование биоптатов.[13]
Принципиальное значение для практики имеет проведение диагностики Н.
pylori–инфекции до лечения – первичная диагностика, и после проведения
противохеликобактерной терапии – контроль эффективности выбранной схемы
лечения.[13]
Анализ кала – дешевый и простой метод, который позволяет выявить
косвенные признаки секреторной недостаточности желудка. Так, при атрофическом
гастрите в кале появляется большое количество (+++) неизмененных мышечных
волокон, соединительной ткани, перевариваемой клетчатки и внутриклеточного
крахмала, а также признаки, свидетельствующие о сопутствующем дисбактериозе.[13]
1.7 Диагностика
Диагностика гастрита включает:
•
анализ клинической картины;
•
эндоскопию (пищевода, желудка, двенадцатиперстной кишки) с взятием
диагностических биопсий;
•
морфологические методы: с окраской гематоксилином и эозином, гистохимические
окраски, окраска по Гимзе без дифференцировки на H.p., иммуноморфологический с
окраской антисыворотками к гастриту, соматостатину и гистамину;
•
методы, направленные на выявление H.p.: морфологический, уреазный
(кло-тест, дыхательный), иммуноморфологический, бактериологический с посевами
на среды;
•
радиоиммунологический метод с определением в крови гастрина и
пепсиногена 1; иммунологический метод с применением иммуносорбентов: АТ к
париетальным клеткам, АТ к ферменту K/Na-АТФазы в париетальных клетках, АТ к
внутреннему фактору Кастла, АТ к H.p.;
•
лабораторные исследования: общий анализ крови, определение уровня
уропепсина в моче;
•
консультация невролога при установлении атрофии слизистой тела желудка и
наличии В12-фолиевой анемии.
«Лейкоциты, или белые кровяные клетки, периферической крови
позвоночных и человека разнородны по морфологическим признакам и биологической
роли. Все лейкоциты подразделяются на две большие группы : зернистые лейкоциты
(или гранулоциты) и не зернистые лейкоциты (агранулоциты). Группа зернистых
лейкоцитов характеризуется наличием в цитоплазме специфической зернистости и
сегментированными ядрами. При окраске смесью кислого (эозин) и основного (азур)
красителей по методу Романовского-Гимзы зернистость в одних лейкоцитах
обнаруживает сродство к кислым красителям, и такие лейкоциты называются
эозинофильными, или ацидофильными, в других — к основным красителям —
базофильные лейкоциты; зернистость третьих обнаруживает сродство к кислым и
основным красителям, такие лейкоциты называются нейтрофилъными, или
гетерофильными. Группа незернистых лейкоцитов отличается отсутствием
специфической зернистости в цитоплазме и несегментированными ядрами. Они
подразделяются на лимфоциты и моноциты, имеющие разные морфологические и
функциональные показатели.
Нейтрофильные гранулоциты (granulocytus neutrophilicus) —
нейтрофильные лейкоциты, или нейтрофилы, имеют округлую форму, их диаметр в
капле свежей крови около 7—9 мкм. На стекле при изготовлении мазка они
несколько распластываются, и их диаметр составляет 10—12 мкм. В крови взрослого
человека нейтрофилов содержится больше, чем других лейкоцитов; их относительное
количество достигает 65—75% от общего числа лейкоцитов.
Цитоплазма нейтрофилов слабо оксифильна, в ней содержится мелкая
зернистость, плохо заметная не только на свежих, но и на фиксированных,
окрашенных препаратах. Количество гранул в каждой клетке может быть от 50 до 200.
При окраске по методу Романовского-Гимзы зернистость принимает
розово-фиолетовый цвет. Зернистостью занята не вся цитоплазма — поверхностный
слой ее в виде узкой каемки остается гомогенным, содержит тонкие филаменты.
Этот слой играет главную роль при амебоидном движении клетки, участвуя в
образовании псевдоподии.
В зависимости от строения и химического состава различают два основных
типа зернистости: специфическую (вторичные гранулы) и азурофильную (первичные
гранулы). Специфическая зернистость преобладает и составляет около 80-90% всех
гранул. В ней выявляется щелочная фосфатаза, пероксидаза, цитохромоксидаза,
мурамидаза, аминопептидаза, а также гликоген, липиды и др. Количество
азурофильных гранул составляет 10-20%, они представляют собой лизосомы с характерным
набором гидролитических ферментов.
Ядра нейтрофилов содержат довольно плотный хроматин, особенно по
периферии, в котором трудно различить ядрышки. Зрелые нейтрофилы имеют
сегментированное ядро, состоящие из 2-3 долек, связанных очень тонкими перемычками.
Они составляют 60-65% лейкоцитов. 3-5% нейтрофилов содержат ядро в виде палочки
или подковы. 0-0,5% в периферической крови юных форм нейтрофилов, имеющих
бобовидное ядро.
Нейтрофилы обладают высокой подвижностью и фагоцитарной способностью,
способны к хемотаксису. Они захватывают бактерии и другие частицы, которые
разрушаются (перевариваются) под действием гидролитических ферментов. Живут
нейтрофильные гранулоциты до 8 сут. В кровеносном русле они находятся 8-12 ч,
а затем выходят в соединительную ткань, где осуществляют свои функции.» [[15]]
Функцией зрелых нейтрофильных лейкоцитов является уничтожение,
проникших в организм инфекционных агентов. Осуществляя ее они тесно
взаимодействуют с макрофагами, Т- и В-лимфоцитами. На важность функционального
вклада нейтрофилов и защиту организма от инфекции указывает, например, тяжесть
течения инфекционных заболеваний у больных, страдающих сниженной продукцией или
качественными нарушениями этих клеток. Нейтрофилы секретируют вещества,
обладающие бактерицидными эффектами, способствуют регенерации тканей, удаляя из
них поврежденные клетки, а также секретируя стимулирующие регенерацию вещества.
Часть нейтрофильных гранул, дают положительную окраску на фермент миелопероксидазу,
представлены лизосомами, содержащими многочисленные энзимы: лизоцим,
повреждающий стенку бактерий; катионные белки, нарушающие дыхание и рост
микроорганизмов; нейтрофильные протеазы и кислые гидролазы, позволяющие
нейтрофилам легко переваривать фагоцитированные объекты.[[16]]
Гранулы нейтрофилов, не окрашивающиеся на миелопероксидазу, содержат
лактоферрин, оказывающий бактериостатическое действие, транскобаламины I и III
— переносчики витамина В12 в крови, лизоцим. В гранулах третьего типа
содержатся кислые глюкозаминогликаны, участвующие в процессах размножения,
роста и регенерации тканей. Гранулы 2-го и 3-го типов — это секреторные
органеллы, выделяющие секрет и вне фагоцитоза, что позволяет отнести нейтрофилы
к клеткам, постоянно секретирующим биологически активные вещества.[16 ]
Нейтрофилы осуществляют свои функции, благодаря способности быстро
мигрировать и накапливаться в инфицированном или поврежденном участках
организма, фагоцитировать, т.е. захватывать и разрушать в фагоцитарных вакуолях
внутри клетки поглощенные бактерии и поврежденные клетки. Их способность к
миграции связана с хорошо развитым аппаратом движения. Выбор направления их
движения к воспаленным или инфицированным тканям обусловлен появлением в этих
тканях вазоактивных и хемотаксических факторов. Вазоактивные факторы повышают
проницаемость капилляров, что способствует миграции нейтрофилов в ткань.
Хемотаксические факторы взаимодействуют с рецепторами на поверхности
гранулоцитов, образуя лигандрецепторный комплекс, определяющий движение
нейтрофилов к воспаленному участку. Самым мощным хемотаксическим эффектом
обладают лейкотриены, производные метаболизма арахидоновой кислоты в мембране
клеток. Они секретируются активированными Т-лимфоцитами и макрофагами после
воздействия на них бактериальных веществ. Помимо лейкотриенов эти клетки
секретируют другие хемоатрактанты — эндотоксины. Важными хемотаксическими
факторами являются продукты активации комплемента — фрагменты его молекул С2а и
С5а. Некоторые из этих факторов, особенно С, функционируют как опсонины, т.е.
вещества, облегчающие фагоцитоз бактерий (от греческого opsonein — делать
съедобным).[[17]]
Большинство реакций, в которых участвуют нейтрофилы, совершается в
тканях. Поэтому адгезивность, характеризующая способность клеток прикрепляться
и задерживаться на определенных субстратах, имеет важное значение при оценке
функционального потенциала нейтрофильного гранулоцита.[ 17]
Нейтрофильные гранулоциты способны осуществлять киллинг
микроорганизмов с помощью двух принципиально различных механизмов:
кислородозависимого и кислороднезависимого.[17]
К кислородзависимому пути относят «респираторный взрыв», который
развивается при взаимодействии нейтрофилов с объектами фагоцитоза.
Кислородзависимый механизм не является системой жизнеобеспечения нейтрофила,
который хорошо переносит гипоксию и нормально выполняет ряд функций (например,
поглощение) в условиях анаэробиоза. «Респираторный взрыв» относится к серии
метаболических процессов, имеющих место при стимуляции нейтрофилов: увеличение
потребления кислорода и усиление окисления глюкозы в пентозофосфатном цикле
(ПФП), и как результат этого – продукция активных форм кислорода, обладающих
бактерицидным действием и обеспечивающих цитотоксический эффект в отношении
опухолевых клеток. Именно на регистрации интенсивности «респираторного взрыва»
основаны многие клинико-диагностические методы оценки состояния организма, в
частности и хемилюминесцентный анализ.[17]
Одним из наиболее перспективных методов, позволяющих оценить
функциональную активность нейтрофильных гранулоцитов, является
хемилюминесцентный анализ.[[18]]
Хемилюминесцентный анализ позволяет получать информацию о нативном
состоянии и функциональной активности клеток. Установлена возможность
непосредственного исследования клеточного ответа при воздействии
физиологических и патологических агентов. Доказан высокий уровень корреляции
между уровнем хемилюминесценции фагоцитов и киллингом.[18]
В связи с этим, определение хемилюминесценции нейтрофилов может
использоваться как один из критериев их способности к завершенному фагоцитозу.
Уровень хемилюминесценции нейтрофилов характеризует интенсивность
«респираторного взрыва» в клетках с продукцией активных форм кислорода,
оказывающих бактерицидное действие (супероксидный анион-радикал, перекись
водорода, гидроксильный радикал, синглетный кислород и др.).[18]
Метод регистрации ХЛ клеток крови позволяет проводить изучение и отбор
иммуномодулирующих фармакологических препаратов на основании сравнения
люминолзависимой стимулированной хемилюминесценции до и после введения в пробу
с лейкоцитарной взвесью исследуемых препаратов.[18]
Хемилюминесцентный тест является высокочувствительным и безопасным
методом диагностики непереносимости лекарственных средств. В случае
непереносимости инкубация цельной крови с раствором этих препаратов в
терапевтических концентрациях сопровождается достоверным снижением генерации
активных форм кислорода нейтрофилами, стимулированными неспецифическими
активаторами. Снижение люминолзависимой хемилюминесценции цельной крови при
непереносимости лекарственного препарата отмечается независимо от химических
свойств и принадлежности медикаментов к фармакологическим группам.[18]
Явление хемилюминесценции - свечения, сопровождающего химические
реакции, – все более широко используется в практических целях, поскольку
позволяет создать ультра чувствительные и специфические методы анализа
различных биологических субстратов. Хемилюминесценция (ХЛ) обусловлена,
реакциями экзотермического типа и протекает, как правило, в три стадии :[[19]]
1. Восстановление одного из участников реакции (присоединение
электрона) и окисление второго (отрыв электрона), что приводит к запасанию
химической энергии в системе, которая позднее выделится в виде фотона.[19]
2. Перенос электрона (окислительно-восстановительная реакция) на
один из более высоких энергетических уровней и образование продукта реакции в
электронно- возбужденном состоянии.[19]
3. Высвечивание фотона при переходе молекулы из
электронно-возбужденного в основное состояние (люминесценция). Обычно
химические реакции, сопровождающиеся свечением, протекают через целый ряд
промежуточных стадий, но основные этапы образования и испускания энергии
сходны.[19]
Хемилюминесцентный метод позволяет регистрировать короткоживущие
свободные радикалы, которые можно разделить на четыре группы: а) свободные
радикалы (CР) активных форм кислорода, б) СР липидов, в) СР, осуществляющие
ферментативное дыхание в митохондриях, г) СР естественных антиоксидантов. [19]
Живые клетки - фагоциты (к которым относятся гранулоциты и моноциты
крови, а также тканевые макрофаги) сами образуют активные формы кислорода при
их стимулировании. При этом наблюдается хемилюминесценция, особенно яркая в
присутствии люминола (или люцигенина). В качестве примера показана
хемилюминесценция клеток крови при действии на кровь кратковременных
электрических импульсов, вызывающих увеличение проницаемости клеточных мембран
и стимуляцию выделения клетками активных форм кислорода. Такие же
"хемилюминесцентные ответы" можно получить, если добавить к
лейкоцитам крови суспензию бактерий, изолированные оболочки дрожжевых клеток,
кристаллы кварца или сульфата бария, а также определенные химические
соединения; все эти агенты получили собирательное название
"стимулов". Стимулированная ХЛ клеток в присутствии люминола - ценный
показатель функционального состояния фагоцитов крови и тканей, их способности
производить при необходимости активные формы кислорода, т.е. выполнять свою
защитную функцию. Эта способность обычно усиливается про возникновении в
организме очагов воспаления (например, после инфаркта миокарда) и в ряде других
случаев. Наоборот, при длительном недостатке кислорода, связанном с общим
ослаблением организма, активность фагоцитов и ХЛ-ответы снижаются.[[20]]
Уровень хемилюминесценции при фагоцитозе характеризует интенсивность
"респираторного взрыва" в клетках с продукцией активных форм
кислорода, оказывающих бактерицидное действие. Первичными метаболитами
активированного кислорода являются супероксидный анион-радикал (О2•), перекись
водорода (Н2О2), гидроксильный радикал (ОН•), синглетный кислород (1О2). В
качестве основных вторичных метаболитов необходимо отметить гипохлорную кислоту
(HOCl), хлорамины и продукты перекисного окисления липидов. Взаимопревращения
первичных и вторичных оксидантов с мощным энергетическим потенциалом создают
динамический спектр молекул, которые прямо или косвенно вовлекаются в реакции
фагоцитов. При этом, взаимодействие высокоэнергетических оксидантов с
люминесцирующими посредниками (люминол, люцигенин и др.) приводит к переходу
последних в электронно-возбужденное состояние, выход из которого сопровождается
испусканием кванта света. Регистрация светоизлучения хемилюминесцентной реакции
производится на хемилюминометрах отечественного или зарубежного производства.[[21]]
В целом, о каком бы разнообразии конечных и промежуточных эффекторов
не шла бы речь, в основе реактивной хемилюминесценции лежит прямое или
опосредованное вовлечение кислорода в образование высоко реактогенных молекул,
излучающих свет. Главное содержание таких реакций - мобилизация кислорода
активированными клетками - сближает хемилюминесценцию с реакцией восстановления
нитросинего тетразолия (НСТ). Следовательно, отмечая объективные преимущества
хемилюминесцентного анализа, необходимо помнить о базисной информации
накопленной при использовании в клинической практике НСТ-теста.[20 ]
В патогенезе многих болезней и патологических процессов играет важную
роль оксидативный стресс. Метод ХЛ оказывается полезным при изучении таких
патологий, поскольку дает возможность измерять уровень свободных радикалов (АФК,
NO), оценивать параметры антиоксидантной защиты и влияние антиоксидантов.
Хемилюминесценцию успешно применяют при изучении иммунных нарушений, нарушений
метаболизма, дисфункции эндотелия, ишемии/реперфузии миокарда и мозга,
онкологических и воспалительных заболеваний, а также многих других болезней,
патогенез которых связан с оксидативным стрессом.[[22]]
Свободные радикалы – важные участники регуляторных процессов в живых
клетках, но одновременно – причина повреждения клеточных структур и триггер,
запускающий каскад реакций самоуничтожения. Их ведущая роль в развитии
практически всех болезней пожилого возраста и старении организма общепризнана и
является объектом многочисленных исследований. Однако средняя по времени
(стационарная) концентрация этих активных частиц в живой клетке очень мала, и
их прямое обнаружение обычными биохимическими методами практически невозможно.
Метод хемилюминесценции основан не на анализе веществ, а на измерении скорости
реакций, сопровождающихся свечением, а именно такие реакции характерны для
свободных радикалов.[22]
Наиболее известные хемилюминесцентные реакции в биохимических системах
– собственное (сверхслабое) свечение при цепном окислении липидов, реакции
люминола с АФК (гидроксильным радикалом и супероксидом) и органическими
радикалами, реакции люцигенина и ряда производных люциферинов с супероксидным
радикалом. Все они включают в себя на определенном этапе взаимодействие двух
радикалов, которое позволяет образовавшейся молекуле накопить такое количество
энергии, что ее оказывается достаточно для излучения фотона конечных продуктов.
[22]
Метод ХЛ стал одним из основных методов изучения свободнорадикальных
процессов в научных и клинических исследованиях.[22]
Во время проведения анализов мы
использовали кровь атрофическим гастритом. Кровь взята из локтевой вены на
голодный желудок. Медицинское учреждение, в котором брали кровь – Клиника ФБГУ
НИИ Медицинских проблем Севера СО РАМН.
В методе хемилюминесцентного анализа используют такие
реактивы как:
·
Раствор Хенкса
·
Уксусная кислота
·
Люминол или люцигенин в концентрации 100 мкг/мл
·
Зимозан или бактериальная суспензия Staphylococcus epidermidis
или Staphylococcus aureus в концентрации (0,4 ОП)
·
Физиологический раствор.
Метод хемолюминесцентного анализа основан на регистрации квантового потока,
образующегося при переходе вещества из электронно-возбужденного в основное
состояние. Наибольшее значение этот метод приобрел в исследовании
воспалительных процессов, сопровождающихся образованием клетками активных форм
кислорода (супероксидного анион-радикала, гидропероксидного и гидроксильного
радикалов, пероксида водорода, синглетного кислорода). Вследствие низкой
интенсивности собственного свечения исследуемых образцов при хемилюминесцентном
исследовании используются вещества, в частности люминол (5-амино-2,3-дигидро-1,4
фталазидинедион), способные многократно усиливать световой поток, который затем
регистрируется датчиком и отображается в виде графика. По оси Х откладывается
время, по оси Y - интенсивность излучения, характеризующая число квантов света,
попадающих на единицу поверхности датчика. Кривая ХЛ исследуемых клеток
характеризуется уровнем спонтанной (ХЛсп) и активированной (ХЛакт)
люминесценции (рис. 2). Для активации клетки использовался зимозан.[23]
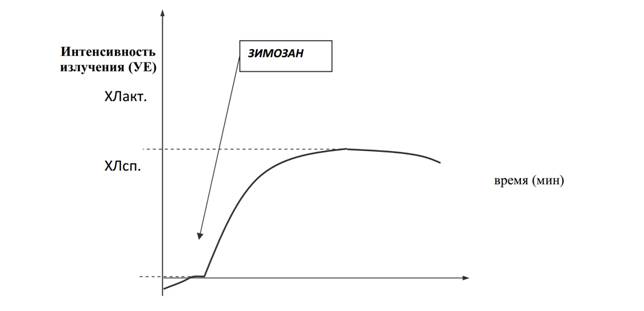
Рисунок 1 - График ХЛ фагоцитирующих клеток. Стрелкой на
шкале времени показан момент активациии клеток зимозаном
«1.Лейкоцитарный супернатант дважды отмывают в растворе Хенкса без
фенолового красного по 10 мин при 500g. Супернатан сливают, оставшиеся
нейтрофильные гранулоциты разводят в 1 мл Хенкса и получают взвесь.
2. Для подсчета клеток в планшет добавляют 40 мкл уксусной кислоты и
10 мкл лейковзвеси и подсчитывают количество нейтрофильных гранулоцитов в
камере Горяева в 5 больших квадратах по диагонали. Количество клеток определяют
по формуле (Х1*11*1000)/0,02=(Х2/2000000)-1 количество Хенкса необходимое
добавить к 1 мл лейкоцитарной суспензии, где Х1 – суммарное количество клеток в
5 квадратах , Х2- количество нейтрофилов в1 мл суспензии (необходимое
количество клеток 2*10 в 6 степени).
3.Для проведения хемилюминесцентного анализа используют следующие
реактивы : донорскую сыворотку (группа крови АВ резус-фактор отрицательный),
раствор Хенкса (без фенолового красного), люминол или люцигенин в концентрации
100 мкг/мл.
·
Готовят пробу : 200 мкл взвеси нейтрофильных гранулоцитов, 20 мкл
донорской сыворотки, 240 мкл раствора Хенкса, 50 мкл люминола или люцигенина и
40 мкл зимозана или бактериальной суспензии Staphylococcus epidermidis или
Staphylococcus aureus в концентрации (0,4 ОП).
·
Бактериальную взвесь делают из суточной бактериальной культуры,
которую разводят в 3 мл физиологического раствора.
·
Концентрацию клеток измеряют на приборе КФК-2 при λ=590 им
относительно физ.раствора, затем доводят физиологическим раствором
концентрацию бактериальной суспензии до 0,4 ОП.
4.Хемилюминесцентный анализ проводят в 8 кюветах ( в первых 4
используем люминол; во вторые 4 добавляем люцигенин). Спонтанная
хемилюминесценция осуществляется без добавления индуктора, во вторую кювету
добавляют зимозан, в третью бактериальную суспензию Staphylococcus epidermidis,
в четвертую Staphylococcus aureus при помощи хемилюминесцентного анализатора,
например « CL.3604» в течение 90 мин. Регистрация результатов и управление
хемилюминесцентным анализатором осуществляется через компьютер. Получают кривую
хемилюминесценция. Определяют величину Tmax Imax Smax для каждого показателя
(спонтанная хемилюминесценция, зимозан-зависимая хемилюминесценция и
стафилококк-зависимая хемилюминесценция).»[[23]]
О функциональном состоянии нейтрофилов судили по величине спонтанной
ХЛ, активированной ХЛ и хемилюминесцентному индексу – Ихл, отражающему
резервные возможности клеток:
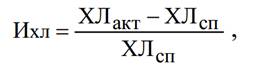
где ХЛсп – максимальный показатель спонтанного
теста, ХЛакт – максимальный показатель стимулированного теста
хемилюминесценции.[23]
Группа исследуемых больных состояли из 30 человек.
Соотношение по половому признаку – 7 мужчин и 23 женщины. Возрастная категория
в диапазоне от 25 до 65 лет.
Таблица 2 -
Хемилюминесцентная активность нейтрофильных гранулоцитов в группе больных
атрофическим гастритом
|
Параметры
|
Хемилюминесцентная активность нейтрофилов
|
|
Спонтанная хемилюминесценция
|
Индуцированная хемилюминесценция
|
|
Контроль N=50
|
Больные N=28
|
Контроль N=50
|
Больные N=28
|
|
T max (сек)
|
1183,5
|
1371,5
|
1074,5
|
1349
|
|
I max (о.е)
|
13647,5
|
14757,5
|
38098,5
|
|
S qur (о.е)
|
1100000
|
1440000
|
2520000
|
3975000
|
|
Идекс активации (iSmax/sSmax)
|
Контроль
|
Больные
|
|
2,013267275
|
1,572403607
|
Параметры хемилюминесцентной активности нейтрофильных гранулоцитов:
время выхода на максимум (T max), интенсивность свечения (I max), площадь под
кривой (S qur) и индекс активации (iSmax/sSmax) группы больных атрофическим
гастритом не имеют статистически значимых отличий в сравнении с группой
практически здоровых людей.
Нейтрофильные гранулоциты ответственны за неспецифический клеточный
иммунитет. Он является первым ответом на инфекцию. Нейтрофилы наиболее активны
в начале такой иммунной реакции, как воспаление. В данном случае атрофический
гастрит является не острым воспалительным процессом, а хронической болезнью. Таким
образом, нейтрофильный ответ менее эффективен, и поэтому различий между
контрольной группой и группой больных атрофическим гастритом не наблюдается.
1. Проанализирована научная литература.
2. Данные хемилюминесценции нейтрофильных гранулоцитов
группы больных атрофическим гастритом свидетельствуют о хронической стадии
воспаления
РЕФЕРАТ(SUMMARY)
Neutrophilic response - the first response
to bacterial infection and many others. Neutrophilic response in acute
inflammation and infection is always preceded by a specific lymphocytic
Neutrophilic granulocytes are responsible
for non-specific cellular immunity. He is the first response to infection.
Neutrophils are the most active in the beginning of such immune responses such
as inflammation. In this case, atrophic gastritis is not acute inflammation and
chronic disease. Thus, neutrophil response less effective, and therefore
differences between the control group and the group of patients with atrophic
gastritis is not observed.
[1]
Дорн О.Ю. Песков С.А. Степанова Е.Г. Клинова Т.В. Паламарчук М.В. Цикаленко
Е.А. Аникина Т.В. Использование методов неинвазивной диагностики заболевания
желудка в современной клинической практике / О.Ю. Дорн С.А. Песков Е.Г.
Степанова Т.В. Клинова М.В. Паламарчук Е.А. Цикаленко Т.В. Аникина // 14.00.00
медицинские и фармацевтические науки – 2013. -№1.
[2]
Бабак О.Я. Протас Ю.В. Хронический атрофический гастрит – точка отсчета начала
канцерогенеза / О.Я. Бабак Ю.В. Протас // Сучасна гастроентерологія, - 2005. -
№ 5 (25). – С. 9-14
[3]Ингерлейб
М.Б. Медицинские Анализы : диагностический справочник / М.Б. Ингерлейб –
Москва 2011. С.13.
[4]Земсков
А.М. Клиническая иммунология: учебное пособие для студентов медицинских
вузов/Под ред.А.М.Земскова. М.: ГЭОТАР-Медиа, 2005.С 20.
[5]
Костюкевич О.И. Атрофический гастрит: что мы поднимаем под этим состоянием.
Современные подходы к диагностике и лечению / О.И. Костюкевич // Болезни
органов пищеварения – 2010. – Том 18, №28. – С. 1717-1722
[6]
Пасечников В.Д. Балабеков А.В. Чуков С.З. Процессы клеточного обновления при H.Pyloriассоциированном хроническом
атрофическом гастрите/ В.Д. Пасечников А.В. Балабеков С.З. Чуков // Клиническая
гастроэнтерология – 2010. – С.8
[7]
Волкова Н.Н. Факторы риска развития хронического атрофического
гастрита(литературный обзор)/ Н.Н. Волкова // Гастроэнтерология – 2013. - №31.
С. 1617 - 1620
[8]
Лысиков Ю.А., Малицына Т.А., Рославцева Е.А. .Трудности в диагностике
атрофических
гастритов у детей/ Ю.А. Лысиков Т.А. Малицына Е.А.
Рославцева// Журнал «Трудный пациент»-2006. - №6
[9]
Богданов И.В., Гриневич В.Б., Першко А.М. и др. Хронический гастрит/ И.В.
Богданов В.Б. Гриневич А.М. Першко и др.// НовыеСанкт–Петербург, врачеб.
ведомости (Приложение).– 2001.–№ 3.– С. 4–13
[10]
Минушкин О.Н. Хронический гастрит: представления, диагностика, лечебные подходы
/ О.Н, Минушкин // Медицинский совет – 2007. - №3. С. – 71 - 76
[11] Kokkola A. Rautelin H. Puolakkainen P. Diagnosis of Helicobacter
pylori infection in patients with atrophic gastritis: comparison of histology,
13C-urea breath test, and serology / А. Kokkola, Н. Rautelin, Р. Puolakkainen //
Scand. J. Gastroenterol. — 2000. — Vol. 35. — Р. 138–141
[12] Sipponen Р. Ranta P. Kaariainen I. Serum levels of amidated
gastrin-17 and pepsinogen I in atrophic gastritis: an observational
case-control study / Р. Sipponen, Р. Ranta, I. Kaariainen // Scand. J. Gastroenterol.
— 2002. — Vol. 37. — Р. 785–791.
[13]
Костюкевич О.И. Атрофический гастрит: что мы понимаем под этим состоянием.
Современные подходы к диагностике и лечению. [Электронный ресурс]. Режим
доступа: #"#_ednref14" name="_edn14" title="">[14]
Шептулин А.А. Киприанис В.А. /Диагностика и лечение инфекции Helicobacter
pylori: основные положения согласительного совещания «Маастрихт–3»/А.А.
Шептулин В.А. Киприанис //Российский журнал гастроэнтерологии, гепатологии,
колопроктологии, 2006, № 2, с. 88–91
[15]ЕлисеевВ.Г.
Гистология : подредакцией / В.Г. Елисеев, Ю.И. Афанасьев, Н.А. Юрина. – Москва
: Медицина, 1983.- 146 с.
[16]Пинегин
Б.В., Маянский А.Н. Нейтрофилы: структура и
функции//Иммунология.-2007.-№6.-С.374-381.
[17]Ткаченко
Б.И. Основы физиологии человека. Учебник для высших учебных заведений, в 2-х
томах, под редакцией акад. РАМН 1994. Т.1 — 567с, т.2 C 413.
[18]Борисов
А. Разработка хемилюминесцентного метода подбора иммуноактивных препаратов для
персонифицированного лечения пациентов с инфекционно-воспалительными
заболеваниями [Электронный ресурс]. Режим доступа:
#"#_ednref19" name="_edn19" title="">[19]Винник
Ю.С. Савченко А.А. Клинические аспекты применения хемилюминесцентного
анализа/Ю.С. Винник А.А. Савченко //Сибирское медицинское обозрение -2006 №3
-С 42-44
[20]Грачева
Т.А. Совершенствование хемилюминесцентного метода исследования функциональной
активности фагоцитирующих клеток//Клиническая лабораторная
диагностика.-2008.-№2.-С54-55.
[21]
Blazheevskly M. Ye., Bondarenco N. Yu. Chemiluminescence-based
kinetic determination of drug / M. Ye. Blazheevskly N. Yu. Bondarenco
// Методы химического анализа, 2011, т6, №3. С124-142.
[22]Владимиров
Ю.А. Проскурнина Е.В. Свободные радикалы и клеточная хемилюминесценция : под
редакцией / Ю.А. Владимиров Е.В. Проскурина – Москва : Факультет
фундаментальной медицины МГУ им. М.В. Ломоносова, 2009, С.341-388.
[23]ДмитриеваН.Ю.
СавченкоА.А. Вычислительноемоделированиединамикихемилюминесценциинейтрофильныхгранулоцитов
/ Н.Ю. ДмитриеваА.А. Савченко // JournalofSiberianFederalUniversity.
Mathematics & Physics 2008, 1(4). С 435-442.