Современная онкология
Содержание
Введение
. Современная онкология
. Химиотерапия пожилого
возраста
Заключение
Литература
Введение
Заболеваемость злокачественными
новообразованиями
В 2014 г. в Российской Федерации (здесь и далее
сводные данные представлены с Крымским ФО) впервые в жизни выявлено 566970
случаев злокачественных новообразований (54,2% у женщин, 45,8% у мужчин), что
на 21,% больше по сравнению с 2004г. (468029).
На конец 2014г. в территориальных онкологических
учреждениях России состояли на учете 3291035 больных (2013г. - 3098855).
Совокупный показатель распространенности составил 2252,4 на 100000 населения.
Диагноз злокачественного новообразования был
подтвержден морфологически в 88,8% случаев (2004 г. - 80,0%), наиболее низкий
удельный вес морфологической верификации диагноза наблюдается при опухолях
поджелудочной железы (51,8%), печени (56,4%), трахеи, бронхов, легкого (70,7%),
почки (78,6%), костей и суставных хрящей (84,2%). Распределение впервые
выявленных злокачественных новообразований по стадиях: I стадия - 26,7%, II -
25,3%, III - 20,6%, IV - 20,7% (в 2004 г. - 23,3%).
Максимальное число заболеваний приходится на
возрастную группу 60-64 года (16,2%)6 у мужчин - 18,3%, у женщин - 14,6%.
Структура заболеваемости
злокачественными новообразованиями.
Ведущими локализациями в общей (оба пола)
структуре онкологической заболеваемости являются: кожа (12,6%, с меланомой -
14,2%), молочная железа (11,6%), трахея, бронхи, легкое (10,2%), желудок
(6,7%), ободочная кишка (6,6%), предстательная железа (6,6%), прямая кишка,
ректосигмоидное соединение, анус (4,9%), лимфатическая и кроветворная ткань
(4,6%), тело матки (4,2%), почка (3,9%), поджелудочная железа (3,0%), шейка
матки (2,8%), мочевой пузырь (2,6%), яичник (2,4%).
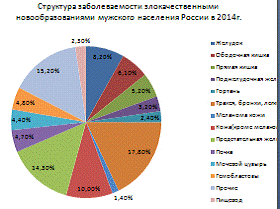
Первые места в структуре заболеваемости
злокачественными новообразованиями мужского населения России распределены
следующим образом: опухоли трахеи, бронхов, легкого (17,8%), предстательной
железы (14,3%), кожи (10,1%, с меланомой - 11,5%), желудка (8,2%), оболочной
кишки (6,1%>). Значителен удельный вес злокачественных новообразований
прямой кишки, ректосигмоидного соединения, ануса (5,2%), лимфатической и
кроветворной ткани (4,8%), почки (4,7%), мочевого пузыря (4,4%), поджелудочной
железы (3,2%), гортани (2,4%). Значимую по удельному весу группу у мужчин
формируют злокачественные опухоли органов мочеполовой системы, составляя 24,2%
всех злокачественных новообразований (рис. 1).
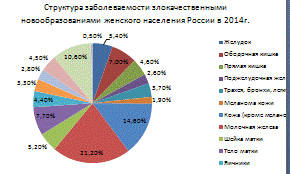
Рак молочной железы (21,2%) является ведущей
онкологической патологией у женского населения, далее следуют новообразования
кожи (14,6%, с меланомой - 16,6%), тела матки (7,7%), ободочной кишки (7,0%),
желудка (5,4%), шейки матки (5,2%), прямой кишки, ректосигмоидного соединения,
ануса (4,6%), яичника (4,4%), лимфатической и кроветворной ткани (4,5%),
трахеи, бронхов, легкого (3,7%). Таким образом, наибольший удельный вес в
структуре онкологической заболеваемости женщин имеют
злокачественные новообразования органов
репродуктивной системы (39,4%), при этом опухоли половых органов составляют
18,2% всех злокачественных новообразований у женщин (рис. 2).
1. Современная
онкология
Современная онкология является тем разделом
медицины, где в последние десятилетия достигнуты большие успехи - от
распознавания механизмов канцерогенеза до совершенствования диагностических и лечебных
подходов. Наибольшие надежды в клинической онкологии возлагаются на
лекарственную терапию. Это то лечебное направление, которое развивается и
совершенствуется столь быстро и успешно, что стало основным видом терапии у
большого числа онкологических больных. Прошло всего несколько десятилетий с
момента использования первого противоопухолевого препарата эмбихин (1946г.), а
в «портфеле» химиотерапевтов имеется большой арсенал противоопухолевых агентов
с различным механизмом действия (алкилаты, антиметаболиты, ингибиторы разных
ферментов и т.д.). Именно это терапевтическое направление уже демонстрирует
бесспорные успехи в лечении больных с диссеминированным опухолевым процессом.
Химиотерапия разрабатывалась в первую очередь
как системное лечение злокачественного процесса. Обладающего способностью с
током крови проникать во все части организма и повреждать или уничтожать
опухолевые клетки. Впервые внутривенное введение химиопрепарата было
произведено в 1943 году в Йельском университете при лечении лимфомы.
Но сегодня противоопухолевые препараты можно
вводить не только системно, но и практически в любой участок тела, в конкретный
орган, в естественные полости и анатомические отделы.
Принципиально новые возможности химиотерапии
открываются при использовании высокодозной химиотерапии. Увеличение спектра
химиопрепаратов и доз противоопухолевых агентов позволяет преодолеть их
фазовоспецифичность и множественную лекарственную устойчивость опухоли, что
приводит к повышению результативности лечения.
2. Химиотерапия
пожилого возраста
По данным мировой статистики, одной из стойких
демографических тенденций является увеличение средней продолжительности жизни
населения планеты и рост удельного веса лиц пожилого (65 лет и старше)
возраста.
Наблюдаемые демографические сдвиги заставляют
уделять особое внимание разработке адекватных методов лечения заболеваний,
характерных для данной возрастной группы, в число которых входят и
онкологические.
Как известно, лица пожилого возраста (65 лет и
старше) составляют значительную часть больных раком.
Рост заболеваемости злокачественными
новообразованиями с увеличением возраста является закономерным и обусловлен
рядом факторов:
Ø накопление соматических мутаций;
Ø более длительный период экспозиции
канцерогенов в организме;
Ø повышение чувствительности организма
к воздействию внешних канцерогенов;
Ø уменьшение способности ДНК к
репарации;
Ø активация онкогенов или амплификация
или потеря генов-супрессоров развития опухоли;
Ø снижение иммунной защиты;
Ø повышение восприимчивости к онкогенным
вирусам;
Ø нарушение гормонального баланса.
Таким образом, предрасположенность к заболеванию
злокачественными опухолями значительно увеличивается с возрастом.
Демографические и эпидемиологические тенденции
заставили активизировать поиск оптимальных тактических подходов к лечению рака
у пожилых больных. В 1990 г. Fentiman
был одним из первых, поставивших вопрос о лечении рака у пожилых больных как
проблему, нуждающуюся в пристальном внимании медицины. Среди причин,
препятствующих разработке адекватного лечения данной категории больных, были
названы следующие:
· консерватизм большей части
онкологов, считающих пожилой возраст противопоказанием для активного лечения;
· недостаток внимания к лечению рака у
пожилых больных при проведении большинства онкологических конференций;
· исключение из клинических испытаний
лиц 70 лет и старше;
· недостаток фармакокинетических
исследований лекарственной активности у пожилых;
· недооценка значения
продолжительности жизни;
· неправильная точка зрения о том, что
пожилые люди плохо переносят химиотерапию и лучевую терапию;
· общераспространенное мнение о том,
что рак у пожилых более индолентен;
· отсутствие четко обоснованных
показаний и оптимальной лечебной тактики, специфичной для лечения пожилых
больных;
· недоучет психологии пожилых больных
в отношении рака;
· отсутствие возможности у пожилых
пациентов самостоятельно высказать свою собственную точку зрения о заболевании
и самостоятельно выбрать лечение.
Monfardini
и Yancik в 1993 г.
дополнили этот список следующими причинами:
· неправильная
интерпретация жалоб больных вследствие наличия у них различных сопутствующих
заболеваний;
· типичность
наличия скрытых симптомов рака;
· поздняя
обращаемость пожилых больных к врачу;
· частое
незнание пациентами симптомов рака.
Следствием этих причин является то, что, с одной
стороны, пожилые больные на момент установления диагноза часто имеют
распространенные формы злокачественных новообразований и, с другой стороны, не
подвергаются адекватному лечению.
Каково же значение лиц пожилого возраста для
общества?
Пожилой возраст - это:
· концентрация
исторического, социального, нравственного, духовного и профессионального опыта
целого поколения - своеобразный Форт Нокс человечества;
· живая
связь поколений;
· наш
последний барьер перед небытием.
Далеко не случайно показателем уровня
социального развития общества является не только положение женщин и детей, но и
стариков. Именно в отношении к старикам человек реализует себя как Homo
sapiens. Современные
пожилые в большинстве своем профессионально и социально активны, обладая
колоссальным опытом и знаниями, они давно уже перестали быть в тягость
человечеству, а мудрость, присущая людям пожилого возраста, позволяет им стать
залогом успешного прогресса всего человечества.
Поэтому не только увеличение общей
продолжительности жизни, но и возросшая социальная значимость пожилого возраста
делает актуальной проблему оказания адекватной медицинской помощи лицам данной
возрастной группы.
На современном этапе развития общества решение
этой задачи вполне реально и обусловлено:
■ уровнем социально-экономического
развития общества (высокий уровень развития производительных сил позволяет
современному обществу обеспечить достойную старость);
■ состоянием современной противоопухолевой
терапии, которое включает:
- широкий спектр эффективных противоопухолевых
препаратов;
постоянный синтез и внедрение в клиническую
практику новых лекарственных средств;
цитостатики последней генерации и таргетные
препараты: предсказуемая и управляемая токсичность;
развитие сопроводительной/поддерживающей
терапии.
Таким образом, в настоящее время имеется
возможность индивидуального подбора эффективного и безопасного лечения.
Ø 60-74 года - пожилой;
Ø 75-89 лет - старческий;
Ø 90 лет и старше - долгожители.
Классификация пожилого возраста - Yancik,
1991 г.:
Ø 65-74 года - ранний пожилой возраст
(young old);
Ø 75-84 года - средний пожилой возраст
(older old);
Ø 85 лет и старше - поздний пожилой
возраст (oldest
old). Классификация
пожилого возраста - Garanasos,
1993 г.:
Ø 65-74 года - ранний пожилой возраст (young-old;
early old age);
Ø 75-84 года - средний пожилой возраст
(middle-old; middle old age);
Ø 85 лет и старше - поздний пожилой
возраст (oldest-old;
late old
age);
Ø 95 лет и старше - элитный пожилой
возраст (elite-old
);
Ø 100 лет и старше - столетние (centernarians).
По определению Balducci
и Extermann, старение - это
прогрессивное полиорганное снижение функциональных резервов организма с
соответствующим снижением толерантности к стрессам, в том числе и к
химиотерапии. Клинические проявления процесса старения, как правило,
наблюдаются после 70 лет.
Однако возрастные изменения индивидуальны.
Изучение больных пожилого возраста показывает, что они являются неоднородной
группой и значительно различаются по физическому, психическому и
интеллектуальному статусу. Это обстоятельство свидетельствует о том, что выбор
лечебной тактики в большей степени должен основываться не на хронологическом, а
на биологическом возрасте, более точно отражающем индивидуальные особенности
пациента. Ключевыми вопросами при выборе лечебной тактики являются следующие:
· Является
ли онкологическое заболевание доминирующим заболеванием, определяющим
продолжительность и качество жизни конкретного пациента?
· Способен
ли данный больной перенести химиотерапию?
· Каково
соотношение пользы и вреда для данного больного?
К сожалению, в настоящее время не существует
единых стандартизованных критериев отбора пожилых онкологических больных для
химиотерапии. Шкалы, традиционно используемые в гериатрии, не адаптированы для
онкологических заболеваний, а шкалы оценки функционального состояния больного,
применяемые в онкологии, не учитывают возрастные изменения. Отсутствие четких
критериев отбора при назначении химиотерапии пожилым больным заставляет врачей
в большей степени ориентироваться на собственный опыт и немногочисленные данные
международных исследований.
Попыткой решить эту проблему является инициированная
Balducci и Extrmann
Гериартрическая онкологическая программа, предлагающая использовать
многофакторную гериатрическую шкалу оценки, - CGA
(comprehensive
geriatric
assessment) - для решения
вопроса о назначении химиотерапии онкологическому больному пожилого возраста.
Шкала скрининга включает следующие параметры:
1)стадия
и прогноз онкологического заболевания;
2)функциональное
состояние больного: оценка функционального статуса по шкале ВОЗ или
Карнофского, а также по мультипараметрическим шкалам ADL
(Activities
Daily Living,
Katz) и IADL
(Instrumental
Activities
of Daily
Living, Lawton);
3)оценка
количества и тяжести сопутствующих заболеваний;
4)когнитивный
статус (оценка миниментального статуса по Folstein);
5)эмоциональное
состояние (гериатрическая шкала депрессий);
6)социальный
статус (помощь родственников и друзей, возможность организации наблюдения в
целях своевременного выявления побочных эффектов химиотерапии, обеспечение
постоянного контакта с врачом, возможность транспортировки больного в
экстренных случаях);
7)препараты
сопутствующей терапии, их количество, показания к назначению, возможное
взаимодействие с цитостатиками;
8)питание
больного (диета, соответствие веса и роста, динамика веса, уровень альбумина в
сыворотке крови);
9)наличие
гериатрических синдромов (делириозный, депрессии, деменции, остеопороза,
«падений», «недержания», «неряшливости», когнитивных расстройств).
Шкала ADL
позволяет оценить возможность пациента самостоятельно, без посторонней помощи
обслуживать себя: принимать ванну, соблюдать личную гигиену, одеваться,
ложиться в кровать и вставать, перемещаться (выходить из дома, подниматься по
лестнице), принимать пищу.
Шкала IADL
оценивает уровень бытовой активности: способность самостоятельно или с
небольшой посторонней помощью пользоваться общественным или личным транспортом,
делать покупки, готовить пищу, наводить порядок в доме, выполнять мелкую
домашнюю работу, пользоваться телефоном, принимать лекарства, вести финансовые
расчеты. Неспособность пациента самостоятельно пользоваться телефоном, делать
покупки, расплачиваться по счетам может явиться предвестником развивающейся
деменции и свидетельствовать о снижении толерантности к химиотерапии.
Использование этих шкал позволяет получить более
полное представление не только о функциональном состоянии пациента, но и о
возможной продолжительности жизни. Показана корреляция между функциональной
зависимостью больного от посторонней помощи и продолжительностью жизни. Так,
средняя продолжительность жизни больных, нуждающихся в постоянной посторонней
помощи хотя бы по одному из пунктов шкалы ADL,
не превышала 3 лет.
По данным Siu,
2-летняя смертность в группе больных 70 лет и старше составила: 8% - для лиц,
полностью обслуживающих себя, 17% - для лиц, нуждающихся в посторонней помощи
по двум и более параметрам шкал ADL
или IADL, и 40% -
для лиц, нуждающихся в полном постороннем уходе.
Сопутствующие заболевания, так же как и
функциональный статус, являются независимым неблагоприятным прогностическим
фактором, отрицательно влияющим на общее состояние и продолжительность жизни
пожилых больных. Кроме того, сопутствующие заболевания снижают толерантность к
химиотерапии. Наиболее значимыми являются коронарная болезнь сердца, сердечная
недостаточность, хроническая обструктивная болезнь легких, почечная
недостаточность, цереброваскулярные заболевания, сосудистые осложнения
сахарного диабета, артриты, анемии.
Оценка когнитивного и эмоционального статуса
больного необходима для выявления нарушений памяти и скрытой депрессии,
затрудняющих планомерное проведение лечения, своевременное выявление и
коррекцию побочных эффектов. Нарушения памяти можно выявить уже при опросе
пациента: попросить назвать дату и место рождения, возраст, сегодняшнее число и
год, возраст детей, их профессию; перечислить больному 3 предмета и попросить
сразу и спустя 15-20 мин повторить их названия. Для оценки эмоционального
статуса необходимо выяснить настроение пациента, часто ли он испытывает чувство
тревоги, уныния, безысходности. При положительном ответе необходимо более
тщательное обследование у психоневролога и последующее лечение депрессии и
тревоги.
Значение социальной поддержки пожилого пациента
трудно переоценить. Именно она зачастую является залогом безопасности лечения.
Оценка нутритивного статуса пациента направлена
на выявление нарушения питания и его коррекцию. Сниженный нутритивный статус
связан с повышением риска развития осложнений химиотерапии.
Гериатрические синдромы, как правило,
свидетельствуют об истощении функциональных резервов организма и являются противопоказанием
для химиотерапии.
В соответствии с полученными результатами Balducci
и Extrmann предлагают
подразделять больных на три группы. На соответствии пациента критериям той или
иной группы базируется выбор лечебной тактики:. Пожилые больные:
· ведущие
активный образ жизни;
· самостоятельно
обслуживающие себя;
· имеющие
адекватный интеллектуальный уровень;
· без
тяжелых сопутствующих заболеваний, гериатрических синдромов и полипрагмазии.
Лечебная тактика: возможны стандартные режимы
химиотерапии. П. II. Пожилые
больные:
· частично
нуждающиеся в посторонней помощи;
· страдающие
двумя и более сопутствующими заболеваниями. Лечебная тактика:
· злокачественная
опухоль не сокращает продолжительность жизни больного или имеет место низкая
толерантность к лекарственной терапии - активная симптоматическая терапия;
· злокачественная
опухоль является основным заболеванием, определяющим продолжительность жизни, -
химиотерапия с исходной редукцией доз вводимых препаратов и последующей их
коррекцией в зависимости от переносимости, часто используется монотерапия.
III. Химиотерапия противопоказана при
соответствии хотя бы одному из следующих пунктов:
· возраст
85 лет и старше;
· нуждаемость
в постоянной посторонней помощи хотя бы по одному из пунктов шкалы ADL;
· наличие
трех и более сопутствующих заболеваний;
■ наличие хотя бы одного гериатрического
синдрома (истощение резервов!).
Лечебная тактика: классифицируются как
ослабленные, «дряхлость» - активная симптоматическая терапия (Принцип
Гиппократа: «Не навреди!» ).
Таким образом, авторы предлагают методику
комплексной оценки функционального состояния пожилых онкологических больных,
которая позволяет более точно оценить индивидуальные функциональные резервы
организма, предполагаемую продолжительность жизни, толерантность к
химиотерапии.
Полученные результаты и являются основой
алгоритма лечения.
Существуют объективные предпосылки, связанные с
возрастными физиологическими процессами, повышающими риск развития побочных
эффектов химиотерапии у пожилых больных.
1. Изменения в объеме распределения.
Объем распределения зависит от содержания
жировой ткани и жидкости в организме, уровня сывороточного альбумина и
количества эритроцитов. С возрастом происходит увеличение процентного
содержания жировой ткани (с 15 до 30% от веса тела), уменьшение объема общей и
внутриклеточной жидкости.
Наблюдается также снижение уровня альбумина и
гемоглобина. В этих условиях возможно увеличение токсичности цитостатиков,
связывающихся с белками или эритроцитами. К ним относятся таксаны,
эпиподофилотоксины, кампто-тецин, антрациклины и антрацендионы. Анемия может
явиться причиной снижения эффективности препаратов, транспорт которых
осуществляется эритроцитами (антрациклины, камптотецин). Кроме того, анемия
может привести к декомпенсации сердечно-сосудистых заболеваний, столь часто
встречающихся у пожилых больных и снижению толерантности к химиотерапии.
Известно, что анемия способствует развитию резистентности злокачественной
опухоли к лекарственной и лучевой терапии и повышению агрессивности опухоли.
Учитывая негативное влияние анемии на
функциональный статус, эффективность и переносимость химиотерапии коррекция
уровня гемоглобина у пациентов преклонного возраста является обязательной.
Показано, что оптимальным для пожилых является уровень гемоглобина 12 г/дл и
выше.
злокачественный новообразование заболеваемость
2. Изменение метаболической функции
печени.
Как известно, возраст влияет на печеночный
метаболизм лекарственных препаратов. Метаболическая функция печени зависит от
массы печени, печеночного кровотока, скорости экскреции лекарственных
препаратов гепатоци-тами, внутриклеточной концентрации и активности ферментов.
Метаболизм лекарственных препаратов в печени включает в себя две основные фазы
реакций - окислительные реакции с участием системы цитохрома Р450 (I фаза) и
реакции конъюгации (II фаза), которые дают возможность водорастворимым
компонентам экскретироваться с желчью и мочой. На активность этих реакций
влияют как возраст, так и различные лекарственные препарата. С возрастом уменьшаются
размеры печени, снижаются печеночный кровоток, белково-син-тетические функции и
активность ферментных систем цитохрома Р450. Изменения в реакциях I фазы могут
повлиять на активность и токсичность препаратов, метаболизирующихся посредством
данного механизма (циклофосфан, ифосфамид, идарубицин). Полипрагмазия,
характерная для пациентов пожилого возраста, может явиться причиной изменения
активности цитохрома Р450.
Нарушения функции печени при нормальной функции
почек не требуют коррекции доз эпиподофилотоксинов и большинства алкилирующих
агентов. Дозы винбластина, доксорубицина и митоксантрона должны быть снижены на
50% при повышении уровня билирубина более 1,5 мг/дл и на 75%, если уровень
билирубина превышает 3,0 мг/дл.
Введение паклитаксела при нарушении функции
печени не желательно, поскольку сопровождается значительным увеличением AUC
(площадь под фарма-кокинетической кривой) и соответствующим ростом токсичности,
главным образом нейтропении. В настоящее время у пожилых больных раком легкого
и раком молочной железы изучаются режимы еженедельного введения паклитаксела,
которые обладают меньшей токсичностью, особенно гематологической, без снижения
эффективности. Согласно существующим рекомендациям, при лечении доцетакселом
одновременное повышение уровня трансаминаз и щелочной фосфатазы требует 25%
редукции дозы даже при нормальном уровне билирубина. По результатам
предварительных исследований, еженедельное введение доцетаксела пациентам
пожилого возраста приводит к существенному снижению миелотоксичности препарата
без снижения его эффективности.
Согласно данным большинства исследований,
возраст не оказывает существенного влияния на фармакокинетику и токсичность
иринотекана.
Тем не менее в первых клинических исследованиях
иринотекана пожилой возраст выделяли как потенциальный фактор увеличения
токсичности. На этом основании была рекомендована редукция стартовой дозы
иринотекана (Кампто) с 350 до 300 мг/м2 в режиме инфузионного
введения 1 раз в 3 недели у больных старше 70 лет.
Результаты дальнейших исследований не
поддерживают эту рекомендацию. Согласно данным Freyer,
Chau, пожилой возраст
не влияет на частоту побочных эффектов III-IV
степени (нейтропения, диарея) при лечении иринотека-ном (Кампто).
. Снижение клубочковой фильтрации
Одним из наиболее стойких функциональных
изменений, присущих пожилому возрасту, является снижение скорости клубочковой
фильтрации. Рутинное определение уровня сывороточного креатинина не дает
адекватной оценки функции почек: возрастная потеря мышечной массы приводит к
уменьшению продукции креатинина и ложной нормализации его уровня. Более точно
функцию почек отражает клиренс креатинина, рассчитанный по формуле Коккрофта:
Снижение гломерулярной фильтрации приводит к
увеличению токсичности химиопрепаратов, основным путем выведения которых
являются почки (блеомицин, метотрексат, цисплатин), а также противоопухолевых
агентов, метаболиты которых выводятся с мочой. В связи с этим до начала любой
химиотерапии у пожилых пациентов необходимо определять КК (клиренс креатинина)
и проводить соответствующую коррекцию доз вводимых цитостатиков.
4. Снижение резервов костного мозга.
Возрастное снижение резервов костного мозга у
пожилых приводит к повышению частоты глубокой гематологической токсичности,
развитию непредсказуемой миелотоксичности, повышению летальности от
инфекционных осложнений. Это касается даже режимов с относительно низкой
гематологической токсичностью, таких как режим CMF,
не говоря уже о режимах, содержащих антрациклины, иринотекан, таксаны,
гемцитабин (Гемзар), этопозид (Вепе-зид), карбоплатин, режима FOLFOX4
(оксалиплатин + инфузия 5-ФУ/Лв).
Однако химиотерапия оксалиплатином в комбинации
с капецитабином (режим XELOX)
не сопровождается повышением токсичности у пожилых. Причиной является низкая
гематологическая токсичность данного режима: нейтропения III-IV
степени развивается только у 8% больных, при использовании режима FOLFOX4
- у 41%.
Опыт лечения пожилых больных неходжкинскими
лимфомами по схеме CHOP
показал, что риск развития жизнеугрожающей нейтропении у больных старше 70 лет,
по данным всех исследований, составляет более 40%, риск инфекционных осложнений
- 21-47%, летальность - 5-30%. Применение КСФ снижает риск развития нейтропении
и инфекционных осложнений на 32-83%. В связи с этим NCCN
и ASCO рекомендуют
первичную профилактику КСФ у всех больных старше 70 лет, получающих
химиотерапию в режимах, интенсивность которых подобна CHOP.
При тромбоцитопении вместо карбоплатина может
быть использован цис-платин при отсутствии противопоказаний к гидратации.
В литературных источниках имеются указания на
то, что редукция дозы цисплатина не снижает эффективности лечения у пожилых
больных. Так, при немелкоклеточном раке легкого изучение цисплатина в диапазоне
доз 60- 90 мг/м2 в комбинации с невельбином у пациентов старше 70
лет показало, что доза цисплатина не влияла на непосредственный эффект.
Представленный Chiara
анализ результатов химиотерапии цисплатином (в разовой дозе, преимущественно,
50 мг/м2) в комбинации с циклофосфаном или с циклофосфаном и
антрациклинами не выявил существенных отличий в эффективности и токсичности
этих режимов у больных раком яичников старше и моложе 65 лет.
5. Возрастная кардиомиопатия.
Атрофические и дистрофические процессы,
приводящие к кардиосклерозу и фиброзу миокарда, негативно сказываются на
функциональных и компенсаторных возможностях миокарда. В этих условиях возможно
повышение кардио-токсичности антрациклинов. Однако при отсутствии тяжелых
сердечно-сосудистых заболеваний риск развития кардиотоксичности повышается
после достижения определенной кумулятивной дозы препаратов. Для пожилых
кумулятивная доза доксорубицина не должна превышать 400 мг/м2.
В целях профилактики кардиотоксичности может
быть рекомендован кар-диоксан. Однако препарат не исследовался у пожилых
больных, имеются литературные данные о том, что он может способствовать
повышению гематологической токсичности и снижению противоопухолевой активности
доксорубицина.
В настоящее время существует липосомальная
пегилированная форма доксорубицина (Келикс), практически не обладающая
кардиотоксичностью.
. Возрастные изменения нервной системы.
Возрастные изменения центральной и
периферической нервной системы повышают риск развития как периферической, так и
центральной нейроток-сичности противоопухолевых препаратов (винкаалкалоидов,
эпиподофилоток-синов, таксанов, производных платины). Авторы исследования TAX
326 отметили, что химиотерапия цисплатином в комбинации с доцетакселом или
вино-рельбином сопровождается увеличением частоты периферических нейропатий III-IV
степени у лиц старше 64 лет. По данным Langer
и соавт., на фоне химиотерапии цисплатином в комбинации с этопозидом или
пакситакселом проявления центральной нейротоксичности чаще встречались у
больных 70 лет и старше, чем у пациентов моложе 70 лет.
Таким образом, процесс старения характеризуется
снижением толерантности организма к цитостатикам. Однако хронологический
возраст как таковой не является противопоказанием к химиотерапии. Адекватная
оценка общего состояния способствует выработке оптимальной лечебной тактики с
учетом индивидуальных особенностей гериатрического больного. Выбор оптимальных
лечебных режимов, адаптация доз вводимых препаратов в соответствии с физиологическими
особенностями организма, использование всего арсенала средств сопроводительной
терапии являются залогом эффективности и безопасности химиотерапии
онкологических больных пожилого возраста.
Принципы химиотерапии пожилого возраста:
· адекватная
оценка функциональных резервов организма;
· адекватная
коррекция сопутствующих заболеваний;
· активное
включение в лечебный процесс не только больного, но и его близких (постоянный
мониторинг);
· выбор
оптимальной лечебной тактики;
· выбор
оптимального цитостатика или режима лечения:
- цисплатин - карбоплатин - оксалиплатин;
- доксо/эпирубицин - Келикс (Доксил);
- CMF
- капецитабин;
- плановая последовательная XT
в монорежиме (метастатический рак молочной железы);
· оптимизация
доз - редукция, исходная редукция с последующей эскалацией; редукция доз у
пожилых не снижает эффективность лечения;
· оптимизация
режимов: выбор наименее токсичного режима (XELOX,
XELIRI, САРОХ, CAPIRI,
режимы еженедельного введения таксанов);
· обязательная
коррекция анемии;
· активное
использование всего арсенала средств сопроводительной терапии.
Заключение
Постоянный поиск путей решения проблемы
лекарственной терапии рака, достижения медицинской промышленности в создании
новых материалов и инструментов определяют настоятельную необходимость
постоянного совершенствования знаний не только врачами, но и медицинскими
сестрами. Оружие онколога - химиопрепараты, без знания предмета оно может быть
либо опасным, либо бесполезным. Медсестра должна хорошо представлять возможности
химиопрепаратов, достоинства и недостатки.
Литература
1. «Организация
специализированного сестринского ухода» под редакцией З. Е. Сопиной Москва
2013г.
. «Сестринская помощь
онкологическим больным» Санкт Петербург 2016г.
. «Пособие по онкологии для
медицинских сестер» под редакцией В. А. Горбуновой Москва 2009г.