Получение хлорида калия
Оглавление
Введение
. Назначение процесса. Характеристика исходных веществ и
продуктов. Условия проведения процесса
. Физико-химические основы процесса
. Технологическая схема
.1 Описание работы основного и вспомогательного оборудования
Список литературы
Введение
Хлорид калия - химическое соединение, формула KCl или калиевая соль соляной кислоты, образует белое
кристаллического вещество без запаха. В природе встречается в виде минералов
сильвина и карналлита, а также входит в состав сильвинита.
В настоящее время существует два метода получения хлорида калия:
. Галургия;
2. Флотация.
Галургический метод основан на различной растворимости KCl и NaCl в воде при повышенных температурах. При нормальной
температуре растворимость хлоридов калия и натрия почти одинакова. С повышением
температуры растворимость хлорида натрия почти не меняется, а растворимость
хлорида калия резко возрастает. На холоде готовится насыщенный раствор обеих
солей, затем он нагревается, и сильвинит обрабатывается полученным раствором. В
процессе обработки раствор дополнительно насыщается хлоридом калия, а часть
хлорида натрия вытесняется из раствора, выпадает осадок и отделяется
фильтрованием. Кристаллы отделяются на центрифугах и сушатся, а маточный
раствор идет на обработку новой порции сильвинита.
Наглядно этот процесс представлен на блок-схеме:
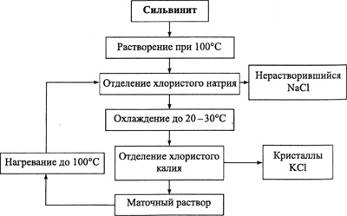
Рис.1. - Блок-схема получения хлорида калия методом галургии.
Флотационный метод заключается в разделении минералов измельченной руды
на основе различной их способности удерживаться на границе раздела фаз в жидкой
среде.
1.
Назначение процесса. Характеристика исходных веществ и продуктов. Условия
проведения процесса
Назначение процесса: получение хлорида калия.
Исходное вещество: основное сырье для калийной промышленности в настоящее
время являются сильвинитовые руды Верхнекамского и Старобинского
местонахождений. Минералогическую основу этих руд составляют сильвинит и галит,
в качестве примесей присутствуют карналлит, глинистый и нерастворимый в воде
остаток, а также бром, йод, рубидий, медь, цинк и другие.
Из всех известных методов обогащения в производстве хлорида калия из
сильвинитовых руд наиболее широкое распространение у нас в стране и за рубежом
получил метод флотации (от англ. flotation - всплывание). Основываясь на внешних признаках, процесс флотации можно
было бы определить как способ разделения, при котором один минерал всплывает на
поверхность пульпы и плавает на этой поверхности, а другой тонет и остается
внутри пульпы. Однако такое определение исходит только из внешней стороны
процесса и не отражает сущности явлений, происходящих при флотации. Кроме того,
известные такие флотационные процессы, при которых никакого всплывания или
плавания частиц нет. Между тем они обусловлены теми же причинами, что и обычная
флотация. Поэтому их совершенно правильно относят к группе флотационных
процессов. Поскольку в любом случае процесс связан с наличием поверхностей
раздела фаз, то наиболее правильным будет следующее определение понятия
"флотация": флотация - метод обогащения, заключающийся в разделении
минералов измельченной руды на основе различной их способности удерживаться на
границе раздела фаз в жидкой среде.
Продукты:
. Сильвинитовые руды;
2. Галит.
2.
Физико-химические основы процесса
хлорид калий галургия сильвинит
Сущность этого метода состоит в том, что хлористый калий выщелачивают из
сильвинита горячим оборотным щелоком, а оставшийся нерастворенным галит (хлорид
натрия) направляют в отвал. Полученный горячий насыщенный щелок проходит
очистку от солевого и глинистого шламов путем отстаивания, затем осветленный
горячий щелок охлаждают. Происходящая при этом кристаллизация КСl связана с ярко выраженным изменением
растворимости этой соли в воде и в насыщенных растворах NaCl.
|
Совместная растворимость
хлоридов натрия и калия в воде при различных температурах
|
|
t° С
|
0
|
25
|
50
|
75
|
100
|
125
|
|
КСl, вес. %
|
7,35
|
11,15
|
14,7
|
18,35
|
21,7
|
24,9
|
|
NaСl, вес. %
|
22,35
|
20,4
|
19,1
|
17,75
|
16,8
|
16,3
|
Диаграмма зависимости совместной растворимости хлоридов натрия и калия от
температуры:
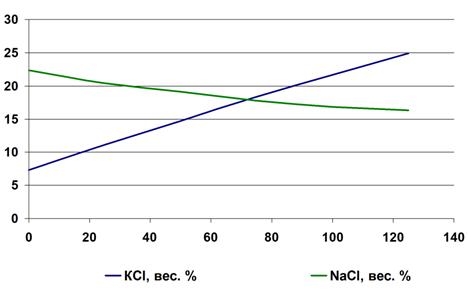
Растворимость (мера растворимости) - это количество вещества, которое при
растворении в 100 г растворителя при данной температуре приводит к образованию
насыщенного раствора. Насыщенный раствор - это раствор такой концентрации,
когда соль при данной температуре больше уже не растворяется.
Любой процесс растворения твердого тела в жидкости можно рассматривать
как химическую реакцию. Однако существует следующее условное разграничение. В
тех случаях, когда под действием жидкой фазы происходит лишь разрушение
кристаллической решетки, т.е. отщепление частиц твердого вещества и переход их
в раствор, процесс носит название физического растворения. Растворение,
происходящее при химическом взаимодействии растворителя с растворимым
веществом, принято называть химическим. Их принципиальное различие состоит в
том, что процесс физического растворения является обратимым (поскольку возможна
обратная кристаллизация твердого вещества из раствора), а процесс химического
растворения необратим. На свойстве обратимости процесса физического растворения
и основано получения хлористого калия из сильвинита.
Сильвинитовую руду, содержащую галит, сильвин и глинисто-карбонатный
материал (н.о.), растворяют в горячих маточных (после кристаллизации КСl) щелоках. Состав этих щелоков
изменяется во времени в зависимости от:
. температуры щелоков
2. состава исходных маточных щелоков и руды
. количественного соотношения руды и щелока
. степени измельчения руды
. условий растворения (форма аппаратов растворителей, направление
потоков жидкости и твердой фаз, скорости перемешивания).
Повышение температуры сказывается не только на относительном увеличении
растворимости хлорида калия в растворах, но так же на росте коэффициентов
скорости растворения К сильвина и галита. Так при растворении сильвина и галита
в собственных растворах К (см/мин) для сильвина имеет значения 1,09 при 50°С,
1,52 при 75°С и 2,04 при 100°С;
Для галита - 0,82 при 50°С, 1,22 при 75°С и 1,65 при 100°С.
Следовательно, температурный фактор имеет большое значение в кинетике
растворения сильвинита.
Так как исходная сильвинитовая руда содержит хлорида натрия в 2-2,5 раза
больше, чем хлорида калия, то NaCl
переходит в раствор с большей скоростью. В результате этого в растворе вначале
достигается концентрация хлорида натрия более высокая, чем равновесная. Однако
по мере дальнейшего растворения хлорида калия избыток хлористого натрия
выпадает в виде мелкого солевого шлама. Высаливание - уменьшение растворимости
одного вещества при увеличении концентрации другого в одном и том же растворе.
КСl и NaCl являются высаливателями по отношению друг к другу.
Следует отметить, что на процесс растворения оказывает влияние наличие
хлористого магния и шламов в исходном сырье. Так при содержании в растворе
хлорида магния свыше 100 г/л Н2О возрастание растворимости КСl при повышении температуры
уменьшается. Влияние шламов на скорость растворения КСl и NaCl
заметно увеличивается при содержании их в руде свыше 10%.
В основе получения хлористого калия галургическим методом лежат свойства
системы КСl- NaCl- Н2О.
Диаграммы используются при расчетах процессов, строятся по имеющимся в
справочниках таблицам растворимости на миллиметровой бумаге.
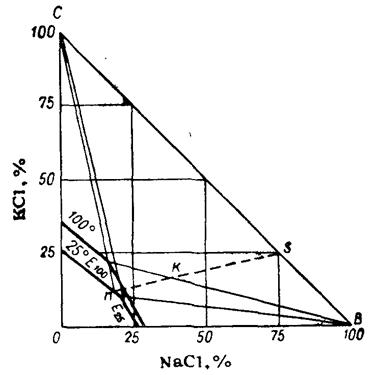
Рис.2 - Растворимость в системе КСl- NaCl- Н2О
при 25 и 100ºС
Количество сильвинита должно соответствовать количеству подаваемого
раствора. Если имеется избыток маточного раствора, то получается раствор не
насыщенный по хлористому калию и насыщенный по хлористому натрию; при
охлаждении такого раствора выпадающий вначале хлористый натрий будет загрязнять
готовый продукт, т.е. снижать качество. При недостатке маточного щелока из
сильвинита растворится не весь хлористый калий, и, следовательно, извлечение
полезного компонента из исходного сырья уменьшится.
Рассмотренные процессы совместной растворимости и кристаллизации солей
при понижении температуры и послужили основанием для выбора принципиальной
технологической схемы переработки сильвинита.
3.
Технологическая схема
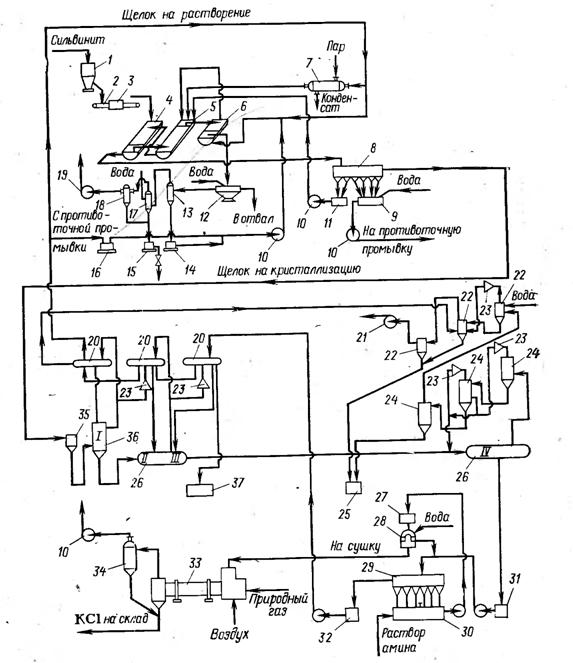
Рис.3 - Схема производства хлористого калия галургическим методом
Перед выщелачиванием сырую руду подвергают дроблению. На выщелачивание
поступает сильвинитовая руда с размерами частиц 1-4 мм. Хлористый калий
извлекают из сильвинита горячим (105-115ºС) щелоком в двух шнековых
растворителях 4 и 5. В первом из них руда и раствор движутся прямотоком, во
втором - противотоком. Отвал, выходящий из растворителя 5, дополнительно
обрабатывают в шнековой мешалке 6 щелоком при температуре 70ºС для более полного извлечения из
него хлористого калия и рекуперации тепла отвала. Маточный раствор,
содержащийся в отвале после шнековой мешалки, удаляют. Для этого отвал
промывают горячей водой на вакуум-фильтре 12. Промытый отвал с содержанием 5-6%
влаги и 2,5% KCl удаляют на солеотвал системой
конвейеров.
Насыщенный горячий (97-107ºС) щелок, полученный в отделении
растворения, содержит 245-265 г/л KCl, 270 г/л NaCl и взвешенные
солевые и глинистые частицы. Осветление щелока проводится в
отстойнике-сгустителе 8. С целью ускорения осаждения добавляются реагенты
(водный раствор полиакриламида). Солевой шлам непрерывно возвращается во второй
растворитель 5, а глинистый шлам направляют в мешалку 9, а после обработки и
промывки отправляют на шламохранилище.
Сгущенную пульпу направляют на центрифуги 28, влажность после центрифуг
5-7%. Далее кристаллы сушат до содержания влаги 0,5-1%.
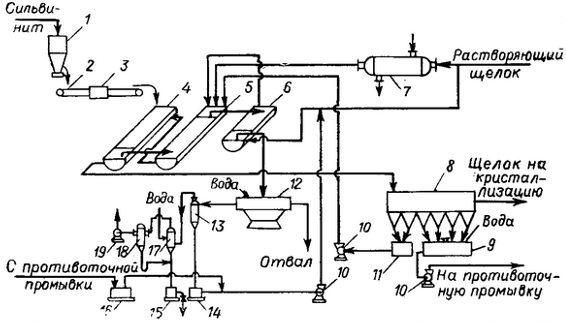
Рис. 4. - Схема получения хлорида калия из сильвинита (операции
выщелачивания, промывки отвала и осветления насыщенного раствора): 1 - бункер с
питателем; 2 - ленточный транспортер; 3 - автоматические весы; 4 - первый
шнековый растворитель; 5 - второй шнековый растворитель; 6 - шнековая мешалка;
7 - трубчатый подогреватель; 8 - отстойник-сгуститель; 9 - мешалки для
глинистого шлама; 10 - центробежные насосы; 11 - сборник солевого шлама; 12 -
план-фильтр; 13 - вакуум-котел; 14,16 - бак для промывной волы; 15 -
барометрический бак; 17 - барометрический конденсатор смещения; 18 -
брызгоуловитель; 19 - вакуум-насос.
.1
Описание работы основного и вспомогательного оборудования
Оборудование, применяемое для выщелачивания
Одним из распространённых аппаратов этой группы является горизонтальный
корытный растворитель с комбинированной шнеково-ленточной мешалкой, известный
под названием шнековый растворитель. Он состоит из сварного корпуса корытообразной
формы с мешалкой и наклонным ковшовым элеватором для выгрузки нерастворившейся
твёрдой фазы. Корпус снабжён герметичной крышкой, на которой расположены
люки-лазы, и поперечными перегородками, достигающими окружности, описываемой
элементами мешалки. Перегородки, предназначенные для продольного перемешивания,
делят объём растворителя на шесть секций. Корпус растворителя и наклонного
элеватора опирается на строительные конструкции лапами, которые могут
перемещаться по роликам при температурных деформациях корпуса.
Мешалка представляет собой горизонтальный вал, вращающийся в подшипниках
скольжения. Она имеет пять секций перемешивающих элементов: лопасти, образующие
прерывистую спираль для перемещения твёрдого материала вдоль корпуса, и
скребки, установленные параллельно валу для перемешивания в пределах каждой
секции. Первая по ходу твёрдой фазы секция предназначена для получения
суспензии и её транспортирования, поэтому она состоит из шнековой и ленточной
полусекций. Вал снабжён сальниковыми уплотнениями и приводится во вращение
электродвигателем через редуктор и дополнительную зубчатую передачу.
Твёрдый материал и растворяющая жидкость непрерывно поступают в корпус
аппарата через штуцеры, а раствор отводится через сливной желоб с
противоположного конца корпуса растворителя. Твёрдый материал перемещается
вдоль корпуса аппарата спиральными лопастями, а жидкость движется в том же
направлении самотёком. Нерастворившийся остаток перегружается в приёмный карман
наклонного элеватора, откуда перфорированными стальными ковшами, укреплёнными
на цепи, выгружается через лоток приводной головки элеватора. Во время
транспортирования твёрдая фаза промывается в ковшах водой. Для опорожнения
аппарата в случае аварийной остановки предусмотрены штуцеры. Температура
регулируется подачей в суспензию острого пара через дюзы.
Недостатком описанной конструкции шнекового растворителя является большой
унос мелких фракций соли (солевого шлама). Это связано с большой скоростью
движения жидкости в зоне отвода раствора и интенсивным перемешиванием лопастями
мешалки.
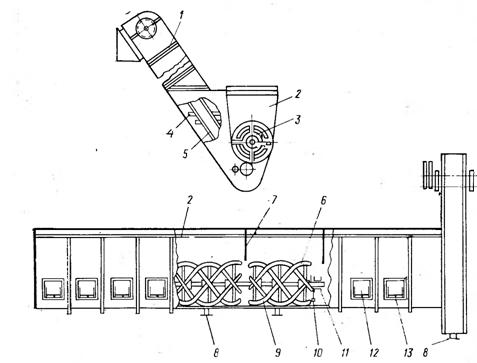
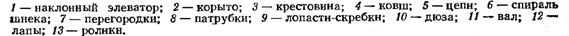
Рис.5 - Растворитель шнековый
Оборудование, применяемое для отстаивания
Для осветления горячего насыщенного щелока используются отстойники типа
"Брандес" и "Дорр", а также многоконусные. В процессе
осветления выделяются солевые и глинистые частицы, оставшиеся в щелоке после
проведения процесса растворения.
Отстойник непрерывного действия с гребковой мешалкой типа
"Дорр" представляет собой невысокий цилиндрический резервуар с
плоским слегка коническим днищем и внутренним кольцевым желобом, расположенного
вдоль верхнего края аппарата. В резервуаре установлена мешалка с наклонными
лопастями, на которых имеются гребки для непрерывного перемешивания, осаждающегося
глинистого шлама к разгрузочному отверстию. Одновременно гребки слегка
взбалтывают осадок, способствуя этим более эффективному его обезвоживанию.
Мешалка делает от 0,015 до 0,5 об/мин., т.е. вращается настолько медленно, что
не нарушает процесса осаждения. Насыщенный щелок непрерывно подается через
трубу в середину резервуара. Осветленный щелок переливается в кольцевой желоб и
удаляется через штуцер. Глинистый шлам удаляется из резервуара при помощи
центробежного насоса. Вал мешалки приводится во вращение от электродвигателя
через редуктор. Вместе с удаляемым осадком теряется значительное количество
хлористого калия, поэтому для уменьшения его потерь и выделения хлорида калия
из суспензии глинистого шлама, осадок из отстойников "Дорр" направляют
в отстойник сточных вод.
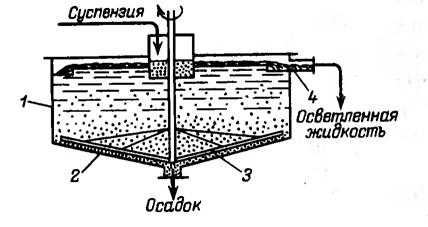

Рис.6 - Отстойник
Оборудование для проведения процесса кристаллизации
Процесс протекает в вакуум-кристаллизаторах. В обычных
вакуум-кристаллизаторах нет подвода тепла извне, кроме теплоты питающего
раствора.
Вертикальный вакуум-кристаллизатор представляет собой полый стальной
цилиндрический барабан, имеющий сферическую крышку и днище в виде усеченного
конуса. Насыщенный раствор поступает через штуцер на зеркало испарения, а
паровоздушная смесь направляется в поверхностные конденсаторы через ловушку.
Ловушка задерживает капли раствора, увлеченные потоком воздуха; через
коническое дно ловушки они падают обратно в жидкость. В нижней части аппарата
имеется штуцер для вывода осветленного раствора и выпавших кристаллов соли. Аппарат
гуммируется листовой резиной.
Горизонтальный вакуум-кристаллизатор представляет собой стальной
горизонтальный цилиндр с торцевыми сферическими стенками. Внутри аппарата
имеется горизонтальная рамная мешалка, приводимая в движение двигателем через
редуктор. Скорость вращения мешалки 16/ об/мин. Для герметизации корпуса вал
мешалки снабжен сальником с водяным затвором.
Горизонтальные вакуум-кристаллизаторы могут состоять из одной, двух или
трех ступеней. В последних случаях цилиндрический барабан разделяется на
ступени вертикальными перегородками, в которых имеются отверстия.
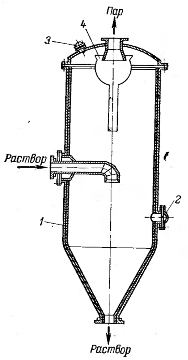
Рис.7 - Вертикальный вакуум-кристаллизатор
Щелок поступает в кристаллизатор через штуцер, а охлаждаемый раствор с
кристаллами соли (суспензия) через отверстия в перегородках перетекает из одной
ступени в другую. Из корпуса суспензия выводится через штуцер. Пары воды и
воздух отводят в поверхностный конденсатор через штуцер каждой ступени.
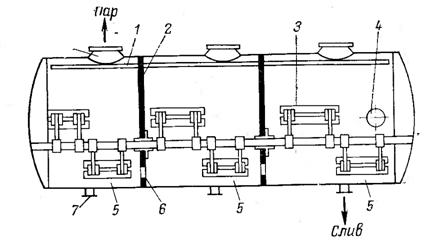
Рис.8 - Горизонтальный вакуум-кристаллизатор
Список
литературы
. Печковский В.В. Технология калийных удобрений. -
Минск.: Высш. школа, 1982
2. Белов В.Н., Соколов А.В. Добыча и переработка
калийных солей. - Л.: Химия, 1971
. Мельников Е.Я. и др. Технология неорганических
веществ и минеральных удобрений. - М.: Химия, 1983
. Позин М.Е. Технология минеральных солей (удобрений,
пестицидов, промышленных солей, окислов и кислот). - Л.: Химия, 1974
. Росприбор [Интернет - ресурс].
URL:http://www.rospribor.com