Определение аутоиммунных антител к ДНК с помощью потенциометрического ДНК-сенсора
КАЗАНСКИЙ
ГОСУДАРТВЕННЫЙ УНИВЕРСИТЕТ
Химический
институт им. А.М. Бутлерова
Кафедра
аналитической химии
Курсовая
работа
Определение
аутоиммунных антител к ДНК с помощью потенциометрического ДНК-сенсора
Содержание
Введение
. Методы получения и свойства
полианилина
(Литературный обзор)
.1 Строение и электрохимические
свойства полианилина
.2 Влияние условий
электрохимического получения полианилина на его свойства
.3 Влияние минеральных кислот,
используемых для получения полианилина на его свойства
.4 Определение антител к ДНК
. Экспериментальная часть
.1 Материалы и реагенты
.2 Приборы и методы эксперимента
. Определение аутоиммунных антител к
ДНК с помощью потенциометрического ДНК-сенсора
ВЫВОДЫ
Список использованных
библиографических источников
Введение
Одной из проблем современной медицины является
своевременная диагностика аутоиммунных заболеваний. Они поражают до 7%
населения земного шара, причем, как правило, в молодом возрасте. Причины
возникновения аутоиммунных заболеваний до конца не выяснены. Это могут быть
иммунологические, генетические, вирусные, лекарственные и гормональные факторы
или их комбинации. Одним из способов объективной оценки аутоиммунного статуса
организма является обнаружение в крови больного аутоантител к нативной ДНК. У
здоровых доноров такие аутоантитела, как правило, отсутствуют или же их
количество чрезвычайно мало. В аутоиммунном процессе массовая гибель клеток в
результате апопоптоза приводит к увеличению титра внеклеточной ДНК в кровотоке,
что и продуцирует антитела, способствующие выведению избытка нуклеиновых
кислот. Единственным способом клинического определения аутоиммунных антител
является твердофазный иммуноферментный анализ. В нем образование комплекса ДНК
- антитело регистрируется с помощью коньюгата, включающего видоспецифичные
антитела и индикаторный фермент, обычно пероксидазу. Активность фермента,
измеренная спектрофотометрически, является мерой содержания антител в сыворотке
крови. Метод отличается многостадийностью, большой длительностью, требует дорогостоящих
реактивов, специального оборудования и квалифицированного персонала. В этой
связи большое внимание уделяется развитию альтернативных методов контроля,
предназначенных на индикации присутствия антител к ДНК в крови больного. Это
может быть достигнуто путем использования биосенсорных технологий. Целью данной
работы было изучение влияний условий получения полианилина и измерения сигнала
сенсора на основе электрода, модифицированного полианилином, на характеристики
детектирования антител к ДНК.
В работе использовали антитела и сыворотки крови
больных, предоставленные кафедрой эндокринологии Казанской государственной
медицинской академией (зав.каф. проф.Анчикова Л.И.).
1. Методы получения и свойства полианилина
(Литературный обзор)
.1 Щтроение и электрохимические свойства
полианилина
аутоиммунный
антитела полианилин
Возрастающий интерес к полианилину в областях
науки и технологии может быть проиллюстрирован статистикой по публикациям.
Например, в журналах такого известного и широко распространенного издательства
как Elsevier: в период с 1985 года по 1995 было опубликовано порядка 900
статей, а за последнее десятилетие уже около двух тысяч. Такой интерес к этому
полимеру вызван как разнообразием, так и уникальностью некоторых свойств
полианилина, делающих возможным его использование в различных областях науки и
техники. Это хранение и преобразование энергии, нелинейная оптика,
электромагнитная защита, а также, катализаторы, индикаторы, сенсоры, мембраны с
контролируемой морфологией и т.д. Хотя полианилин уже достаточно изучен и
используется в большом числе промышленных товаров, все же остается множество
вопросов относительно о его структуре и свойствах, наблюдаемых при
использовании модификаторов, способных влиять на процесс полимеризации и
формирования полимера.
Основные результаты, полученные при изучении
полианилина и подробно представленные в обзорных работах [1-4], можно
резюмировать в виде рис.1.
Как видно, полианилин может существовать в трех
основных окислительно-восстановительных формах в виде оснований и их солей
(допированные формы). При изменении pH
и окислительно-восстановительного состояния между ними происходит перенос как
электронов, так и ионных зарядов [4-8]. Происходит также и перенос молекул
растворителя, но этот процесс не изучен в полной мере, что не позволяет
отобразить его в данной модели.
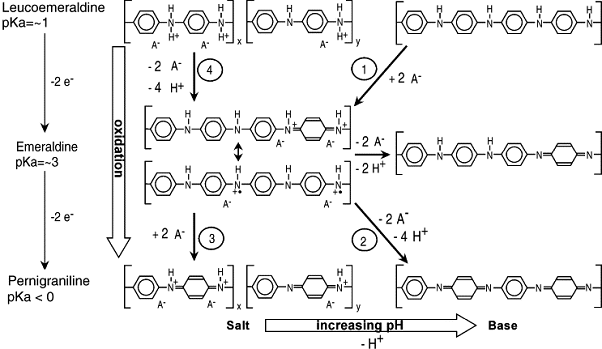
Рисунок 1. Формы полианилина, образующиеся при
электрохимическом окислении полианилина при различных рН раствора
Полианилин электропроводен при рН ниже 3-4, при этом
он способен подвергаться электрохимическому окислению и восстановлению и
находиться в трех редокс-формах: лейкоэмералдин, соль эмералдина,
пернигранилин, но электропроводной формой является только соль эмералдина. В
соответствии с этим, на циклических вольтамперограммах наблюдаются две пары
редокс-пиков, соотносящихся к переходам между этими формами.
В водных растворах степень протонирования всех
трех форм зависит от рН среды, на рисунке переход показан слева направо. В
случае эмералдина значение pKa
находится между 0 и 1 [4]: протонирование начинается при рН 2 и практически
полностью завершается при рН -1 [8-9]. Однако следует отметить, что степень
протонирования зависит также от природы кислоты, участвующей в данной реакции
[10]. Так в случае нафталинсульфоновой кислоты лейкоэмералдин находится в
полностью протонированной форме даже при рН 2 [8]. Для эмералдина характерное
значение pKa
приблизительно равно 3 [4], в то время как для пернигранилина это значение
меньше 0. На рис.1 полностью протонированные звенья имеют индекс Х, но в
большинстве кислот полимерные цепи являются смесью фрагментов, состоящих из X-
и Y-участков,
соотношение которых зависит от рН раствора. В левой части рис.1 показана только
полностью протонированная форма основания эмералдина. Именно она является
единственным электропроводящим состоянием полианилина из всех шести,
отображенных на этом рисунке [11]. Две эквивалентные резонансные структуры
данной соли называют биполяронной и поляронной формами соли эмералдина.
Рис. 1 иллюстрирует также процессы, при которых
в зависимости от рН раствора и от редокс-состояния полианилин изменяет свой
объем. Они обусловлены транспортом ионов внутрь полимера и обратно вовне,
необходимым для поддержания его электронейтральности. Полианилин, будучи в форме
соли эмералдина, сжимается при погружении в раствор основания (переход слева
направо в центральной части рисунка), при этом происходит отток анионов из
структуры полианилина [12]. Изменение объема полимера происходит также при
электрохимическом воздействии, а именно, при окислении соли эмералдина до
пернигранилина и при восстановлении до лейкоэмералдина. Этот процесс обусловлен
тем, что наряду с изменением степени окисления полимерной цепи (вертикальная
ось на рисунке), происходит транспорт ионов. Он сопровождается также переносом
протонов, вызванным различием величин pKa
соответствующих редокс-форм полианилина [13].
Поскольку величины рН сред, используемых
совместно с полианилином, часто находятся в пределах от 0 до 2,
окислительно-восстановительные реакции протекают по схемам 1 и 2 рис.1, т.е.
основание лейкоэмералдина - соль эмералдина - основание пернигранилина. При
этом во время окисления лейкоэмералдина до эмералдина полианилин расширяется за
счет включения анионов из раствора [14], и увеличивается его масса [4].
Напротив, при переходе от эмералдина до пернигранилина по схеме (2) полимер,
обычно, сжимается, а масса уменьшается. При многократном изменении
окислительно-восстановительного состояния полианилина рекомендуется
придерживаться перехода между формами лейкоэмералдина и эмералдина, так как
пернигранилин неустойчив в водных растворах большинства кислот. В апротонных
растворителях перенос протонов между полимером и растворителем во время
редокс-реакций происходить не может, поэтому они протекают по схемам 1 и 3
рис.1 с включением анионов во время обеих реакций [9], расширяя, таким образом,
полимер на протяжении всего процесса окисления. Поскольку в растворах ионы
имеют сольватную оболочку, из-за изменений во взаимодействии полимер - раствор
и осмотического давления при протекании редокс-реакций возможно также наличие
отдельных потоков раствора внутрь и наружу полимера [15]. Встречный поток
молекул воды при включении в состав полимера ионов может быть достаточно
большим - до 10 молекул воды на один анион [15]. Эти потоки могут зависеть как
от природы кислоты, так и от рН раствора [9]. Изменения в массе полимера могут
быть вызваны и другими факторами, например, такими как изменение геометрии
полимерной цепи. Так, для окисленной формы сопряженной полианилиновой цепи
характерно более линейное и малоподвижное состояние, вызванное усилением
взаимодействий p-орбиталей (на схемах рисунка 1 не
показано).
.2 Влияние условий электрохимического получения
полианилина на его свойства
Процесс электрохимической полимеризации с
окислением анилина может быть описан с помощью формального стехиометрического
уравнения (1):
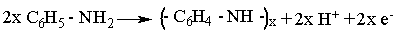
Электрохимические свойства
полианилина и способы его получения с достаточной полнотой рассматриваются в
[16-18]. Электрохимический синтез осуществляется в следующих основных режимах
на поверхности твердотельных электродов:
1. В гальваностатическом, при постоянном
токе во время электролиза в диапазоне 1-10 мА.
2. В потенциостатическом, при потенциалах
рабочего электрода от 0.7 до 1.1 В относительно НКЭ.
. В потенциодинамическом режиме в
интервале от -0.2 до +1.0 В относительно нас.к.э., используя импульсное или
циклическое изменение потенциала.
В ранних работах, связанных с получением
электрополимеризованного анилина, сообщается, что потенциодинамические методы
позволяют получить полимер с лучшей адгезий, гладкостью и оптическими
свойствами, но причины этого выявлены не были [16]. В другом случае достоверной
разницы в свойствах получаемого полимера обнаружено не было [16].
Подробное исследование этих методик было
проведено в работах опубликованных много позже. Так было выявлено, что
использование импульсного потенциостатического режима позволяет десятикратно
увеличить токи окисления-восстановления получаемой пленки полимера по сравнению
с потенциостатическим и потенциодинамическим режимом [19]. Отмечено также, что
пленки полианилина, полученные импульсным и статическим потенциостатическими
методами, обладали сходным электрохимическим поведением. Последующее изучение показало
, что импульсный метод влияет не на процесс формирования первоначальных ядер -
центров олигомеризации - на поверхности электрода, а на дальнейший их рост,
когда происходят реакции образования полимерной пленки. Было высказано мнение,
что преимущества этого метода связаны не с воздействием импульсной методики на
процесс чрезмерного окисления анилина и полианилина, а с постоянным
перераспределением редокс-центров в растущем полимере и с периодическим
растягиванием и сжатием полимерных цепей.
В работах [20,21] авторы предположили, что
причины различий, наблюдаемых при использовании потенциостатического и
потенциодинамического режима получения полианилина, связаны с накоплением
значительного количества продуктов деградации в матрице полимера при использовании
потенциостатического режима. В этом случае присутствие продуктов гидролиза
(таких как гидрохинон и п-аминофенол), появляющихся в процессе
неконтролируемого окисления полианилина во время продолжительного
потенциостатического импульса, приводит к ингибированию роста волокнистого
полимера и способствует образованию продукта порошкообразной морфологии.
Сообщалось также, что пленки полианилина, получаемые в потенциодинамическом
режиме с большими скоростями развертки потенциала, обладают большей однородностью
и компактностью по сравнению с получаемыми при малых скоростях .
Подробное изучение электрохимического
сопротивления полианилиновых пленок, полученных на электродах из нержавеющей
стали в гальваностатическом, потенциостатическом и потенциодинамическом режимах,
было проведено в работе [22]. Проводился анализ спектров электрохимического
сопротивления на основе модели электрохимической ячейки с двумя полными
контурами сопротивления. Было показано, что спектры импеданса для электродов с
полианилином, приготовленных в гальваностатическом и потенциостатическом
режимах, весьма сходны. Выяснено также, что сопротивление пор, содержащих
раствор (Raq),
вызываемое процессами допирования - дедопирования, намного превышает
сопротивление переноса заряда (Rp)
самих полимерных цепей. Значения этих величин возрастают с увеличением толщины
полимерной пленки c
одновременным уменьшением внутренней пористости полимера и его разрядной
емкости, что согласуется с теорией. Однако в случае потенциодинамического
режима полимеризации спектры сопротивления имеют другой вид, а Raq
< Rp. При этом
сопротивление получаемых пленок зависит от скорости развертки потенциала,
уменьшаясь с ее увеличением. На основе полученных сканирующим электронным
микроскопом снимков можно сделать вывод о зависимости морфологии полианилина от
скорости развертки. При малых скоростях (10 мВ/с) превалируют кластерные
структуры с большими порами между элементами структуры. Напротив, при больших
скоростях (200 мВ/с) пленка получается более однородной с преобладанием тонкопористой
структуры. Следует отметить также обратную зависимость между массой получаемого
полимера и Rp ,
наблюдаемую для потенциодинамического режима. В этом случае Rp
уменьшается с увеличением массы покрытия, а Raq
остается практически неизменным. Исследование влияния концентрации анилина на
получаемую пленку показало практически линейную зависимость падения разрядной
емкости и существенное увеличение Rp
при концентрации анилина 0.5 М. Как отмечается в работе, данные электрической
емкости, полученные в электрохимической импедансометрии, хорошо согласуются с
результатами аналогичных исследований, проведенных методом циклической
вольтамперометрии.
.3 Влияние минеральных кислот, используемых для
получения полианилина, на его свойства
На данный момент известны работы по
электрохимическому синтезу полианилина из водных сред, содержащих различные
кислотные электролиты.
Электрохимическое окисление анилина обычно
проводят в 1 М HCl,
0.1 M
H2SO4
или 1 М H2SO4.
Кроме того, успешно использовали для синтеза полианилина HClO4,
HCl, CF3COOH
и HBF4. Полимер осаждали
на различных подложках, начиная с металлов (золото, платина, титан, покрытый
платиной, нержавеющая сталь) и заканчивая оксидом олова и углеродными
материалами.
В [23] полианилин осаждали потенциодинамически
на платиновом электроде из растворов 1 М HClO4,
0.5 М H2SO4,
1 М HCl и 1 М
водного раствора п-толуенсульфоновой кислоты циклированием потенциала (100
циклов) в диапазоне потенциалов от -0.2 до 1 В отн. Ag/AgCl
при скорости развертки 100 мВ/с. Было показано, что наилучшими свойствами
обладает полианилин, синтезированный из раствора хлорной кислоты. Наиболее
часто встречающиеся проблемы, связанные с кислотными электролитами - это
выделение водорода при высоких потенциалах (>1В), высокое сопротивление электролитов
и их испарение в течение синтеза. Для преодоления этих проблем в предлагалось
использовать уникальный электролит - AlCl3:H2O
(1:2.75, 1:5), насыщенный AgCl.
Циклирование проводилось в диапазоне потенциала от -0.2 до 1.2 В при скорости
развертки 20 мВ/с. На циклических вольтамперограммах наблюдались 2
окислительно-восстановительных пика . Деградация полианилина, полученного после
100 циклов сканирования, в течение 15 дней была незначительна, а его
электрохромные свойства были такими же, как у полимера, полученного в кислотных
электролитах.
В последнее время исследователи уделяют внимание
электрополимеризации анилина в органических растворителях, таких как
ацетонитрил или дихлорэтан, с использованием LiClO4
или солей четвертичных аммониевых оснований для повышения электропроводности
растворов. Однако проводящие полимеры, полученные из этих сред, часто были
нерастворимы в обычных органических растворителях из-за жесткости полимерного
скелета и кросс-сшивок во время полимеризации [24].
Исключающий эти недостатки способ полимеризации
анилина приведен в [24]. В этом случае анилин полимеризовали в уксусной кислоте
при контролируемом потенциале 1.1 В отн. нас.к.э. (рабочий и вспомогательный
электроды - никелевая фольга). Полимер, полученный таким образом, был дедопированным
и растворялся во многих органических растворителях, таких как уксусная кислота,
N-метил-2-пирролидон,
ацетонитрил, тетрагидрофуран, метанол, спирт и ацетон. Его электрохимическое
поведение и структура были определены с помощью циклической вольтамперометрии,
спектрофотометрии в УФ и видимой областях и ИК-спектроскопии. Экспериментальные
результаты показали, что полимер имел короткую и разветвленную структуру.
Получаемый продукт в растворе менял цвет до темно-коричневого в процессе
полимеризации. После полимеризации в УФ-спектрах реакционной смеси появилась
новая полоса при 415 нм, что соответствует дедопированному состоянию
водорастворимого полианилина в щелочном (рН 8-12) буферном растворе фосфата
натрия. Это может быть объяснено тем, что чистая уксусная кислота обладает
очень низким содержанием ионов водорода.
После полимеризации на циклических
вольтамперограммах наблюдались две волны окисления при 0.13 В и -0.21 В. Волна
восстановления появлялась при -0.26 В, сигнал восстановления при 0.2 В был
довольно сглаженным. В целом вольтамперограмма была подобна полученным для
тонких пленок полианилина в неводных средах, таких как ацетонитрил. ИК-спектры
раствора были аналогичны спектрам, полученным для пленок полианилина,
образующихся при электрополимеризации анилина из ацетатных буферных растворов .
Однако было показано, что полианилин, синтезированный потенциостатически из
уксусной кислоты, имеет разветвленную или привитую структуры. Средняя молярная
масса полимера была менее 2000 г/моль. Электропроводность полианилина была
близка к значению, полученному для традиционного дедопированного полимера. При
обработке полианилина, синтезированного потенциостатически из уксусной кислоты
водным раствором HCl,
он терял растворимость в уксусной кислоте и многих других органических
растворителях.
В [25] проведено сравнение полианилина,
допированного двумя органическими кислотами (хлоруксусной и трихлоруксусной), с
полианилином, полимеризованным из хлорной кислоты. Было показано, что
окислительно- восстановительные свойства осажденного полианилина сильно зависят
от допирующей кислоты. Потенциалы окисления и восстановления были различны для
каждой из кислот, и этот факт может быть объяснен электростатическим
взаимодействием допанта с химически гибкими >NH-группами
полимера. Значения различных кинетических параметров также зависели от типа
кислоты, используемой в процессе полимеризации. УФ-спектрофотометрия осадков
полианилина различной толщины в N-метилпирролидине
показала ингибирование деградации в толстых пленках. Это было характерно для
всех трех допирующих кислот.
Также в литературе было описано получение
полианилина из щавелевой кислоты на подложке из стали [26]. Интересно, что
прямое окисление анилина в полианилин на стали не наблюдается, а первым этапом
является формирование пленки оксалата железа. Этот пассивирующий слой состоит в
основном из оксалата железа (II)
с включенными оксидами. Анилин полимеризуется на пленке оксалата Fe(II),
образуя эмералдиновую соль зеленого цвета. Предварительно пассивированная сталь
позволяет прямое осаждение полианилина на эту оксалатную пленку.
Таким образом, варьирование условий
полимеризации анилина, подложек и минеральных кислот, из которых идет осаждение
полимера, в значительной степени влияют на его окислительно -восстановительные
и электрохромные свойства, электропроводность и структуру.
.4 Определение антител к ДНК
Антитела к ДНК являются объектом интереса
широкого круга физиологов и иммунологов. Присутствие больших количеств
сывороточных антител к двухцепочечной ДНК является специфичным признаком
системной красной волчанки и других аутоиммунных заболеваний, таких как
ревматоидный артрит, аутоиммунный тиреоидит и др.
У большинства здоровых людей в сыворотке крови
имеются антитела IgM
к одноцепочечной ДНК. Эти антитела являются естественными антителами, они имеют
низкое сродство к ДНК, тироглобулину и миозину. Напротив, антитела IgG
к двухцепочеченой ДНК менее распространены среди здоровых людей и, видимо,
включают в себя подгруппы с высоким сродством и ограниченной перекрестной
реактивностью [27].
Для определения аутоантител к нативной ДНК
используют различные по чувствительности методы, зачастую трудоемкие и не
поддающиеся автоматизации.
Наиболее часто используют варианты
иммуноферментного анализа, в которых сначала на поверхность полистирольных
планшетов для иммуноанализа наносят препарат антигена (нативной или
денатурированной ДНК), после чего добавляют сыворотку крови больного и далее -
препарат коньюгата специфического антитела и индикаторного фермента
(пероксидазы), после чего в реакционную смесь вносят субстрат фермента, дающий
в реакции с ферментом окрашенные продукты. Положительным результатом (наличие
антител к ДНК в сыворотке крови) служит появление окраски, интенсивность
которой зависит от концентрации антител в крови больного. Метод отличается
высокой чувствительностью (определение антител в сыворотках с оптимальных
рабочим разведением 1:100), но имеет следующие недостатки: (1) длительность
стадий инкубирования (общая продолжительность анализа более двух часов); (2) многостадийность
определения (три стадии с промежуточными отмывками), (3) необходимость
применения коньюгата индикаторного фермента со специфичными антителами [28].
В работе [29] приведен пример амперометрического
ДНК - биосенсора для определения антител к ДНК, используя взаимодействие ДНК с
комплексами Pt(II).
Денатурированную ДНК иммобилизовали на пленке из нитрата целлюлозы.
Модифицированная пленка использовалась как биочувствительная часть
амперометрического ДНК-сенсора, основанного на стационарном серебряном
электроде, покрытом ртутной пленкой. Биосенсор использовали как новый вариант
твердофазного иммуноанализа для определения антител к ДНК в сыворотке крови без
предварительного разделения компонентов. Содержание антител контролировали по
величине тока каталитического выделения водорода при -1.2 ... -1.4 В,
наблюдаемого при комплексообразовании соединений платины с ДНК или антителами,
соответственно. Метод и ДНК-сенсор использовали в диагностике алеутской болезни
норок, при которой в крови животных образуются антитела к ДНК.
В [30] приведен пример вольтамперометрического
определения антител к ДНК с использованием золотого электрода,
модифицированного ДНК, выступающей в качестве хеморецепторного лиганда. Для
иммобилизации ДНК ее молекулу сначала модифицировали дисульфидом, ковалентно
связанным с 5'- терминальными группами биополимера. Модифицированная таким
образом ДНК образовывала прочные тиольные связи с материалом электрода.
Исследования методом циклической вольтамперометрии показали, что обратимая электродная
реакция окислительно - восстановительной пары ферроцианид/феррицианид в
присутствии ДНК подавляется за счет электростатического отталкивания между
иммобилизованной ДНК и ионами маркера. Добавка антител, которые не реагируют с
ДНК, не влияет на токи регистрируемые токи феррицианида. Антитела к ДНК,
неселективно связывающиеся с с одно - и двухцепочечной ДНК, значительно снижают
регистрируемый ток ионов маркера. Эти результаты подтверждают, что связанная с
поверхностью электрода ДНК успешно выступает в качестве распознающего элемента
для диагностики антител к ДНК в сыворотке крови пациентов.
2. Экспериментальная часть
.1 Материалы и реагенты
В работе использовали дезоксирибонуклеиновую
кислоту (ДНК) из эритроцитов цыплят, глутаровый альдегид (Ланкастер, Eastgate,
Англия), анилин (Россия, ООО "Экофарм"). Сыворотки крови больных
аутоиммунным тиреоидитом, предоставленные кафедрой эндокринологии КГМА ,
хранили в морозильной камере и размораживали однократно перед приготовлением их
разбавленных растворов. Для приготовления растворов ДНК и сывороток
использовали 0.001 М фосфатный буферный раствор, рН 7.5. Измерения проводили в
четырех буферных растворах:0.001М фосфатном буферном растворе, содержащем 0.03
М Na2SO4;
0.001 М фосфатном буферном растворе, содержащем 0.03 М NaBF4;
0.001М фосфатном буферном растворе, содержащем 0.03 М NaCl;
0.001 М фосфатном буферном растворе, содержащем 0.03 М Na2C2O4.
Растворы готовили путем растворения точных навесок солей в дистиллированной
воде с последующим доведения объема раствора до 100 мл. Величину pH
полученных растворов корректировали с помощью 10%-ных растворов NaOH
и HCl.
Полимеризацию анилина производили в следующих
кислотах: 0.4 М НСl
(ОАО"Уральский завод химреактивов"), 1.0 M
HBF4 (Михайловский
завод химреактивов), 1.0 M
H2C2O4
(Черкасский завод химических реактивов), 0.2 М Н2SO4
(ОАО"Уральский завод химреактивов"). Растворы кислот были
приготовлены из фиксаналов разбавлением дистиллированной водой.
.2 Приборы и методы эксперимента
Измерения проводили с помощью вольтамперометрического
анализатора "Экотест-ВА" в циклическом режиме линейной
вольтамперометрии. В качестве рабочего электрода использовали стеклоуглеродный
электрод, с площадью поверхности 0.01767 см2. Противоэлектродом служила
никелевая фольга площадью поверхности 1 см2, электродом сравнения -
хлоридсеребряный электрод (Ag/AgCl).
Контроль величины pH
рабочих растворов проводили с помощью pH-метра
"Эксперт-001" (рН-метрический электрод ЭВЛ-1М3.1,
ЗАО"Эконикс-Эксперт", Москва, Россия).
Дозирование реагентов при приготовлении
растворов и проведении измерений производили с помощью микродозаторов Unipipette
2010 и Vari (“Plastomed”,
Польша).
.2.1 Полимеризация анилина в соляной кислоте.
В ячейку добавляли 5 мл 0.4 М HCl
и проводили электрохимическую очистку электрода при следующих условиях.
Накладывали потенциал 800 мВ на 3 мин., затем проводили девятикратное
циклирование в диапазоне потенциала от -300 до 800 мВ при скорости развертки 40
мВ/с. Затем в ячейку добавляли 33.3 мкл анилина, перемешивали в течение 10 мин.
и проводили электрополимеризацию анилина десятикратным циклированием потенциала
от -200 до 1000 мВ при скорости развертки 50 мВ/с. Электрод сушили при
комнатной температуре под вентилятором.
.2.2 Полимеризация анилина в серной кислоте
В ячейку добавляли 5 мл 0.2 М H2SO4
и проводили электрохимическую очистку электрода при следующих условиях.
Накладывали потенциал 800 мВ на 3 мин., затем проводили девятикратное
циклирование в диапазоне потенциала от -300 до 800 мВ при скорости развертки 40
мВ/с, затем в ячейку добавляли 33.3 мкл анилина, перемешивали в течение 10 мин.
и проводили электрополимеризацию анилина десятикратным циклированием потенциала
от -300 до 800 мВ при скорости развертки 50 мВ/с. Электрод сушили при комнатной
температуре под вентилятором.
.2.3 Полимеризация анилина в
тетрафторбористоводородной кислоте
В ячейку добавляли 5 мл 1 М HBF4
и проводили электрохимическую очистку электрода при следующих условиях.
Накладывали потенциал 800 мВ на 3 мин., затем проводили девятикратное
циклирование в диапазоне потенциала от -300 до 800 мВ при скорости развертки 40
мВ/с, в ячейку добавляли 33.3 мкл анилина, перемешивали в течение 10 мин. и
проводили электрополимеризацию анилина десятикратным циклированием потенциала
от -300 до 800 мВ при скорости развертки 50 мВ/с. Электрод сушили при комнатной
температуре под вентилятором.
.2.4 Методика полимеризации анилина в щавелевой
кислоте
В ячейку добавляли 5 мл 1 М H2C2O4
и проводили электрохимическую очистку при следующих условиях: накладывали
потенциал 800 мВ на 3 мин., затем проводили девятикратное циклирование в
диапазоне потенциала от -300 до 800 мВ при скорости развертки 40 мВ/с. Затем в
ячейку добавляли 33.3 мкл анилина, перемешивали в течение 10 мин. и проводили
электрополимеризацию анилина десятикратным циклированием потенциала от -700 до
800 мВ при скорости развертки 50 мВ/с. Электрод сушили при комнатной
температуре под вентилятором.
.2.5 Измерение сигнала ДНК-сенсора в фосфатном
буфере с хлоридом натрия
На электрод наносили 2 мкл смеси из 0.025мг/мл
раствора ДНК и 3% глутарового альдегида ( 2 мкл глутарового альдегида смешивали
с 10 мкл ДНК). Высушивали под вентилятором. Снимали на рН-метре-иономере зависимость
потенциала от времени в течении 20 мин. в 0.001 М фосфатном буферном растворе,
содержащем 0.03 М NaCl.
Электрод вынимали из электрохимической ячейки, промывали дистиллированной
водой, высушивали, наносили 5 мкл разбавленной сыворотки крови человека,
накрывали пластиковой пипеткой Эппендорфа для предотвращения высыхания, каплю
сыворотки смывали рабочим буферным раствором. Затем опять снимали зависимость
потенциала от времени. Сигнал обрабатывали по методу вычета базовой кривой и по
разнице потенциала в минимумах. Аналогичным образом проводили измерение в 0.001
М фосфатном буферном растворе, содержащем 0.03 М Na2SO4
, 0.03 М NaBF4. или 0.03
М оксалата натрия.
3. Определение аутоиммунных антител к ДНК с
помощью потенциометрического ДНК-сенсора
Для регистрации взаимодействия ДНК-белок нами
предложено использовать изменение электростатических характеристик полиионного
комплекса, образуемого ДНК и полианилином. Данный полимер в обычных условиях
получения несет положительный заряд и способен электростатически связываться с
отрицательно заряженной ДНК. Такое связывание влияет на электрохимические
характеристики полианилина, обусловленные обратимыми процессами переноса ионов
водорода и противоанионов электролита. Как следует из рис.1 литературного
обзора, окислительно-восстановительные реакции полианилина сопровождаются
процессами протонирования и депротонирования, а также синхронным переносом
анионов в слой полимера из раствора и обратно. Присутствие на поверхности
полианилина ДНК и белка может менять как область протонирования и
окислительно-восстановительный потенциал полимера, так и скорость переноса
анионов в области допирования полианилина.
Для регистрации взаимодействия ДНК - белок
стеклоуглеродный электрод после механической и электрохимической очистки
покрывали слоем полианилина. После этого на электрод наносили раствор нативной
высокополимерной ДНК эритроцитов крови цыпленка. Для уменьшения десорбции ДНК с
электрода в раствор добавляли сшивающий реагент - глутаровый альдегид. После
промывки электрод опускали в рабочий буферный раствор и регистрировали
изменение потенциала, обусловленное установлением равновесия допирования в
результате изменения рН раствора. После этого на рабочую поверхность электрода
наносили разбавленную сыворотку крови, содержащую антитела к ДНК, и через 10
мин. измерение потенциала повторяли. Типичное изменение потенциала электрода
представлено на рис.2.
Как видно, форма кривой после контакта
биосенсора с антителами к ДНК сохраняется, однако она смещается в зависимости
от содержания антител в сыворотке или от ее разбавления.
Количественную характеристику изменения
потенциала после инкубирования сыворотки крови и ДНК на электроде определяли
двумя способами:
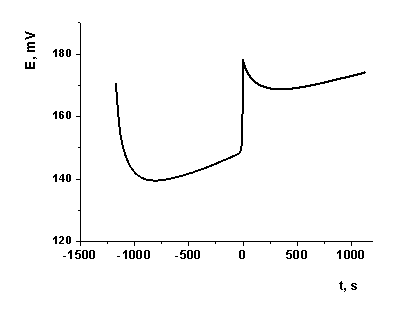
Рисунок 2. Изменение потенциала
электрода, модифицированного полианилином и ДНК, до и после его инкубирования с
сывороткой крови, содержащей антитела к ДНК
) по положению минимума на кривых
изменения э.д.с. во времени (метод минимумов); расчет производится по формуле:
DЕ
= Е2-Е1,
где DЕ, мВ, - изменение э.д.с., характеризующее
присутствие антител в сыворотке крови, Е1, мВ, и Е2, мВ, - значения э.д.с,
соответствующие минимумам, наблюдаемым на временных зависимостях э.д.с.,
регистрируемых до и после контакта электрода с сывороткой крови, соответственно.
Способ расчета представлен на рис.3а.
) по смещению кривой изменения
э.д.с. после прохождения минимума, аппроксимируемому линейной функцией (метод
вычета базовой линии). Расчет производится следующим образом. Сначала строят
линейную регрессию Е = а + b´t на участке
кривой изменения э.д.с. E, мВ, во времени t, с,
регистрируемой до контакта электрода с сывороткой крови. Находят по уравнению
значение Е1, соответствующее величине э.д.с. при времени t’. Значение t’
рассчитывают следующим образом:
t’ = 1200 + t2
где 1200 с - время измерения э.д.с.
до контакта электрода с сывороткой крови, t2 - время
появления минимума на временной зависимости э.д.с., регистрируемой после
контакта электрода с сывороткой крови. После этого рассчитывают изменение
э.д.с. Е, мВ, характеризующее содержание антител в сыворотке крови:
Е = Е2 - Е1
где Е2 - э.д.с. минимума на
временной зависимости э.д.с., регистрируемой после контакта электрода с
сывороткой крови, Е1 - аппроксимированное значение э.д.с. до контакта электрода
с сывороткой крови, которое наблюдалось бы во время t2 появления
минимума. Способ расчета представлен на рис.3б.
На рис.5 показана характерная кривая
изменения сигнала биосенсора, полученная при различных разбавлениях сыворотки
крови больного системной красной волчанкой и аутоиммунным тиреоидитом. Максимум
изменения сигнала приходится на разведение 1:20 - 1:50. Напротив, при
тестировании сыворотки крови здорового донора изменения либо статически
незначимы, или происходят в сторону уменьшения потенциала биосенсора (рис.6).
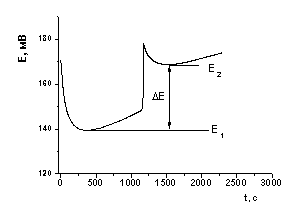
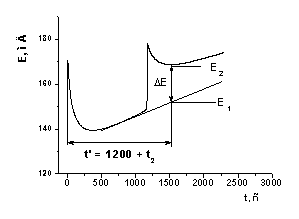
Рисунок 3. Способ расчета количественных
характеристик взаимодействия ДНК-антитело по динамических кривым изменения
потенциала ДНК-сенсора
Для изучения условия генерирования
аналитического сигнала биосенсора, нами было проведено исследование влияния
условий полимеризации анилина и природы противоиона фонового электролита.
На рис.7 представлены вольтамперные кривые,
полученные в процессе электрополимеризации в соляной кислоте. Как видно,
наибольший рост пиков полианилина происходит в интервале сканирования
потенциала от -200 до + 1000 мВ при скорости развертки потенциала 100 мВ/с.
Снижение максимального значения потенциала до +800 мВ полностью прекращало
процесс полимеризации. То же самое происходило при уменьшении объемной
концентрации соляной кислоты с 0.4 до 0.2 моль/л.
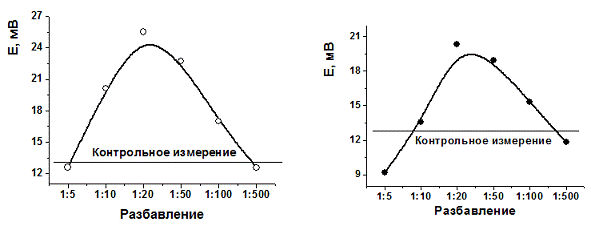
Рисунок 5. Зависимость сигнала сенсора от
разбавления сыворотки больных системной красной волчанкой и аутоиммунным
тиреоидитом. Полианилин получали из серной кислоты, рабочий буферный раствор
содержал сульфат натрия
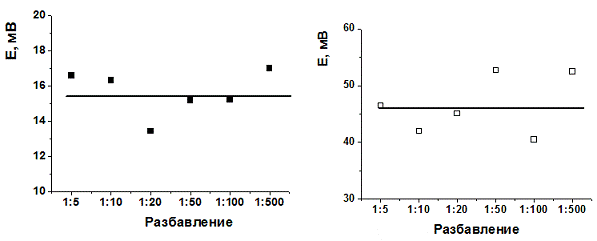
Рисунок 6. Зависимость сигнала сенсора от
разбавления сыворотки здорового донора. Полианилин получали из серной кислоты,
рабочий буферный раствор содержал сульфат натрия
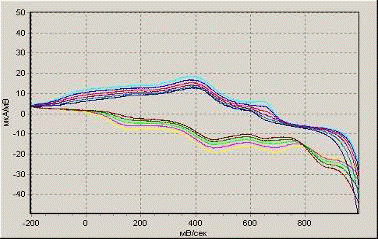

100 мВ/с, -200…+1000 мВ
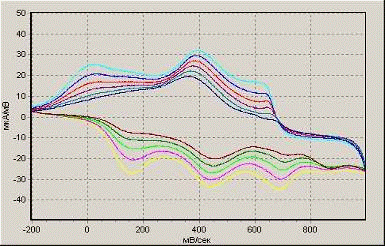

50 мВ/с, -200…+1000 мВ
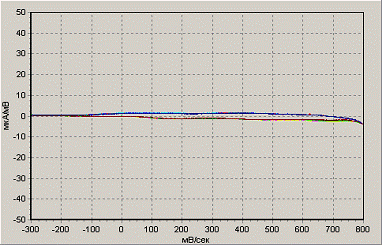

50 мВ/с, -300…+800 мВ
Рисунок 7. Влияние условий полимеризации в
соляной кислоте на рост пленки полианилина на поверхности электрода.
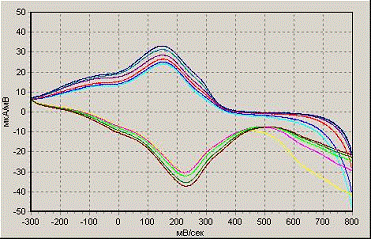

0.2 М HBF4 50
мВ/с, -300…+800 мВ
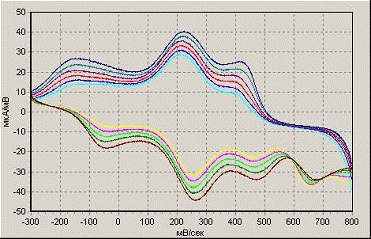

1 М HBF4
50
мВ/с, -300…+800 мВ
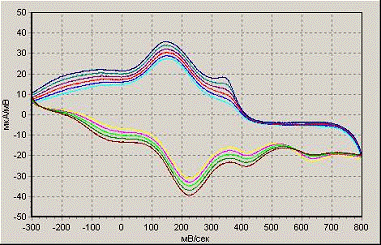

0.4 М HBF4
+ 0.2 М H2SO4
100 мВ/с, -300…+800 мВ
Рисунок 8. Влияние условий полимеризации в
тетрафторбористоводородной кислоте на рост пленки полианилина на поверхности
электрода
В том же диапазоне концентраций в
тетрафторбористоводородной кислоте полимеризация анилина практически не
протекает. На всех вольтамперограммах наблюдается только один квази-обратимый
пик окисления-восстановления, высота которого незначительно меняется в процессе
циклирования потенциала (рис.8). Раздвоение пика и формирование растущей пленки
полимера происходит только при увеличении концентрации кислоты с 0.4 до 1
моль/л. К аналогичному эффекту приводит проведение электролиза в смеси серной и
тетрафторбористоводородной кислот.Полученные таким образом полианилиновые
покрытия были использованы для иммобилизации ДНК и получения
потенциометрического отклика на антитела к ДНК. Наилучшие результаты по
тестированию сыворотки крови дольных и здоровых доноров были получены при
совпадении аниона минеральной кислоты, используемой для полимеризации анилина,
и включенной в состав буферного раствора как фонового электролита.
На рис.9 приведены кривые разведения, полученные
на полианилине и в буферном растворе, содержащих только хлорид-ионы.
Как видно, по внешнему виду кривых разведения
сыворотки можно вполне отчетливо провести разделение сывороток крови больных и
здоровых пациентов. По сравнению с результатами, полученными в серной кислоте,
абсолютные изменения потенциала в пике еще выше. Разведение сыворотки,
отвечающее максимуму кривой разведения, для всех способов расчета и способов
проведения полимеризации практически совпадают. Наиболее удобен в работе метод
минимумов. Но при нем несколько хуже различение сигнала, получаемого с
сывороткой крови больного и здорового донора. В целом же метод минимумов и
метод вычитания базовой дает одну и ту же картину изменения параметров
биосенсора.
На рис.10 представлены аналогичные зависимости,
полученные с полианилином, синтезированном в тетрафторбористоводородной
кислоте.
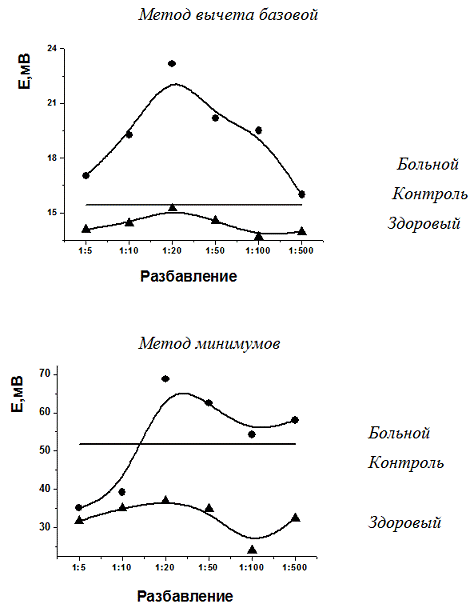
Рисунок 9. Зависимость сигнала сенсора от
разбавления сыворотки больного аутоиммунным тиреоидитом. Полианилин получали из
соляной кислоты, рабочий буферный раствор содержал хлорид натрия в качестве
фонового электролита.
И здесь различие кривых разведения сыворотки
крови больного и здорового донора максимально и позволяет достоверно проводить
диагностику присутствия антител. Для математической обработки результатов
использовался метод фиксированного времени, поскольку минимум на кривой
изменения потенциала выражен слабо.

Рисунок 10. Зависимость сигнала сенсора от
разбавления сыворотки больного аутоиммунным тиреоидитом. Полианилин получали из
тетрафторбористоводородной кислоты, рабочий буферный раствор содержал
тетрафторборат натрия в качестве фонового электролита.
Если же полимеризацию проводить в соляной
кислоте, а измерение - на фоне сульфата натрия, то влияние разбавления
сыворотки на сигнал меняются (рис.11). И для здорового, и для больного донора
изменение менее выражено и меньше отличается друг от друга.
На наш взгляд, это связано с тем, что при замене
аниона фонового электролита затрудняется обмен анионами при обратимых
окислительно-восстановительных реакциях с участием полианилина, участвующих в
генерировании сигнала биосенсора. Это согласуется с литературными данными,
согласно которым анионы кислоты, участвующей в реакции полимеризации анилина,
оказывают своеобразный темплатный эффект, задавая особенности микроструктуры
образующейся полимерной пленки.
На рис.12 приведен подбор условий полимеризации
полианилина в щавелевой кислоте. Полимеризация протекает в более катодной
области потенциалов. Продукт полимеризации - полианилин - получается в восстановленной
форме, имеющей желтую окраску.
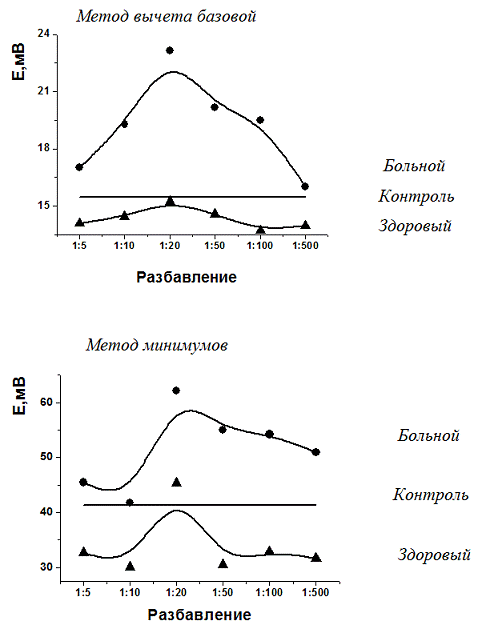
Рисунок 11. Зависимость сигнала сенсора от
разбавления сыворотки больного аутоиммунным тиреоидитом. Полианилин получали из
соляной кислоты, рабочий буферный раствор содержал сульфат натрия в качестве
фонового электролита.
Поскольку при работе с восстановленным
полианилином мы получили характерную кривую зависимости сигнала сенсора от
разбавления сыворотки крови (рис.13), аналогичную зависимостям, полученным
ранее ( хотя максимум на кривой разбавления сместился к разбавлениям 1:5-1:10),
можно предположить, что механизм формирования сигнала связан не с
окислительно-восстановительным потенциалом полианилина, а с числом зарядов на
его поверхности.
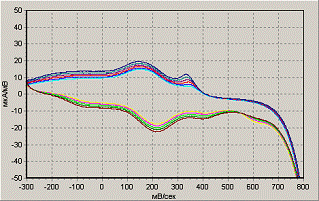
50 мВ/с -300…+800 мВ
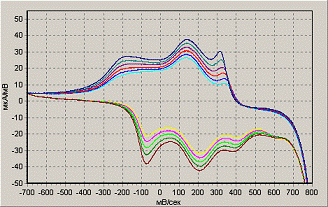

50 мВ/с -700…+800 мВ
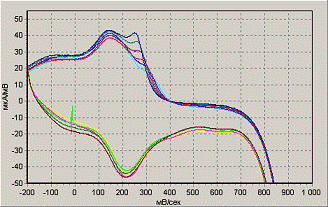

100 мВ/с -200…+1000 мВ
Рисунок 12. Влияние условий полимеризации на
рост пленки полианилина из щавелевой кислоты.
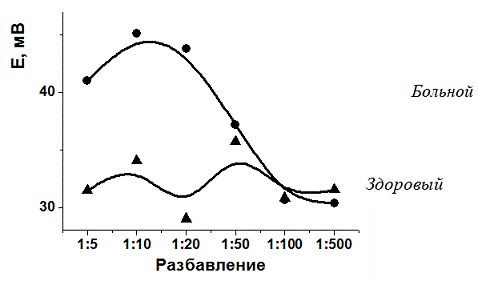
Рис.13. Зависимость сигнала сенсора от
разбавления сыворотки больного аутоиммунным тиреоидитом. Полианилин получали из
щавелевой кислоты, рабочий буферный раствор содержал оксалат натрия в качестве
фонового электролита.
Выводы
. Потенциал стеклоуглеродного электрода,
модифицированного полианилином и нативной двунитевой ДНК, зависит от
присутствия в растворе нативных антител к ДНК, взаимодействие которых с ДНК
меняет окислительно-восстановительные характеристики и равновесия допирования
слоя полианилина.
. Предложены способы количественного выражения
влияния антител на динамическую кривую потенциала сенсора, позволившие
установить различие в поведении ДНК-сенсора при контакте с сывороткой крови
здорового донора и больного аутоиммунным тиреоидитом.
. Способ получения полианилина, в том числе,
природа минеральной кислоты в электролите для полимеризации и природа
допирующего иона буферного раствора, влияют на количественные характеристики
отклика при сохранении общего вида кривой разбавления сыворотки крови больного.
. Проведена апробация сенсора на 10 сыворотках
крови больных системной красной волчанкой и аутоиммунным тиреоидитом , во всех
случаях найдено соответствие между результатами иммуноферментного анализа
данных сывороток и результатами, полученными на разработанном ДНК-сенсоре.
Список использованных
библиографических
источников
1.
MacDiarmid A. G. Polyaniline: synthesis and characterization of the emeraldine
oxidation state by elemental analysis / A. G. MacDiarmid, J. C. Chian, A. F.
Richter, N. L. D. Somasiri, A. J. Epstein // Conducting Polymers. 1987. - P.
105-120
.
MacDiarmid A. G. Polyanilines: a novel class of conducting polymers / A. G.
MacDiarmid, A. J. Epstein // Faraday Discuss. Chem. Soc. 1989. - V.88. - P.
317-332.
.
Travers J.-P. Polyaniline: A material still under discussion / J.-P. Travers,
F. Genoud, C. Menardo, M. Nechtschein // Synth. Met. 1990. - V.35. - P. 159-168
.
Orata D. Determination of ion populations and solvent content as functions of
redox state and pH in polyaniline / D. Orata, D.A. Buttry // J. Am. Chem. Soc.
1987. - V.109. - P. 3574-3581
.
MacDiarmid A.G. Secondary doping in polyaniline / A.G. MacDiarmid, A.J. Epstein
// Synth. Met. 1995. - V.69. - P. 85-92.
.
Barisci J.N. Conducting Polymer Sensors - A Review / J.N. Barisci, C. Conn,
G.G. Wallace // Trends in Polymer Science. 1996.- V.4. - P.307-311
7.
Magnuson M. The electronic structure of polyaniline and doped phases studied by
soft X-ray absorption and emission spectroscopies / M. Magnuson, J.-H. Guo,
S.M. Butorin, A. Agui, C. Såthe, J. Nordgren, A.P. Monkman // J. Chem.
Phys. 1999. - V.111. - P. 4756-4761
.
Tawde S. Redox behavior of polyaniline as influenced by aromatic sulphonate
anions: cyclic voltammetry and molecular modeling / S. Tawde, D. Mukesh, J.V.
Yakhmi // Synth. Met. 2001. - V.125. - P. 401-413
.
Desilvestro J. In situ determination of gravimetric and volumetric charge
densities of battery electrodes. Polyaniline in aqueous and nonaqueous
electrolytes / J. Desilvestro, W. Scheifele, O. Haas // J. Electrochem. Soc.
1992. - V.139. - P. 2727-2736
.
Barbero C. Direct in situ evidence for proton/anion
exchange in polyaniline films by means of probe beam deflection / C. Barbero,
M.C. Miras, O. Haas, R. Kötz // J. Electrochem.
Soc. 1991. - V.138. - P. 669-672
11.
Geniès E.M. Polyaniline: A historical survey / E.M. Geniès, A.
Boyle, M. Lapkowski, C. Tsintavis // Synth. Met. 1990. - V.36. - P. 139-182.
.
Herod T.E. Doping-induced strain in polyaniline: stretchoelectrochemistry /
T.E. Herod, J.B. Schlenoff // Chem. Mater. 1993. - V.5. - P. 951-955
.
Takashima W. The electrochemical actuator using electrochemically-deposited
poly-aniline film / W. Takashima, M. Kaucko, K. Kaneto, A.G. MacDiarmid //
Synth. Met. 1995.- V.71.- P. 2265-2266
.
Varela H. Ionic Exchange Phenomena Related with the Redox Process of
Polyaniline in Nonaqueous Media / H. Varela, R.M. Torresi // J. Electrochem.
Soc. 2000.- V.147.- P. 665-670.
.
Pruneanu S. Electrochemical quartz crystal microbalance study of the influence
of the solution composition on the behaviour
of poly(aniline) electrodes / S. Pruneanu, E. Csahók, V. Kertész,
G. Inzelt // Electrochim. Acta. 1998.- V.43.- P.
2305-2323
.
Park S.M. Handbook of Organic Conductive Molecules and Polymer vol. 3 / S.M.
Park H.S. Nalwa // Wiley 1997.- P. 429
.
Kang E.T. Polyaniline: A polymer with many interesting intrinsic redox states /
E.T. Kang, K.G. Neoh, K.L. Tan // Prog. Polym. Sci. 1998.- V.23.- P. 277.
.
Syed A.A. Review: Polyaniline-A novel polymeric material / A.A. Syed, M.K.
Dinesan // Talanta 1991.- V.38.- P. 815
.
Taskova V. Electrochemical formation and stability of polyaniline films / V.
Taskova, A. Milchev // Electrochim. Acta. 1991.- V.36.- P.1579
.
Cui C.Q. Origin of the difference between potentiostatic and cyclic potential
sweep depositions of polyaniline / C.Q. Cui, L.H. Ong, T.C. Tan, J.Y. Lee // J.
Electroanal. Chem. 1993.- V.346.- P. 477
.
Cui C.Q. Extent of incorporation of hydrolysis products in polyaniline films
deposited by cyclic potential sweep / C.Q. Cui, L.H. Ong, T.C. Tan, J.Y. //
Electrochim. Acta 1993.- V.38.- P.1395
.
Mondal S. Analysis of electrochemical impedance of polyaniline films prepared
by galvanostatic, potentiostatic and potentiodynamic methods / S. Mondal, K.
Prasad, N. Munichandraiah // Synth. Met. 2005.- V.148.- P.3
.
Prakash R.Electrochemistry of polyaniline: study of the pH effect and
electrochromism/ R.Prakash //J.Appl.Polymer Sci. 2002 - V. 83. - P. 378-385.
.Guo
L. Electrosynthesis of soluble polyaniline in acetic acid / L.Guo, G. Shi, Y.
Liang // Polymer Bulletin 1998 .- V. 41. -P.681-686
.Pruneau
S. Characterization of polyaniline by cyclic voltammetry and UV - vis
absorption spectroscopy / S. Pruneau, E. Veress, I. Marian, L. Oniciu.//J.
Mater.Sci 1999. - V. 34 . - P. 2733-2739
.
Martyak N.M. Chronoamperometric studies during the polymerization of aniline
from an oxalic acid solution / N.M. Martyak //Mater. Chem. Phys. 2003. - V. 81.
- P. 143-151
.
Hann B.H. Antibodies to DNA/B.H.Hann // New England J. Med. 1998. - V.338. - P.
1359-1368
.
Патент
РФ
№ 2059245, G01N33/53, 1996 г.
.Babkina
S.S. Amperometric DNA biosensor for the determination of auto - antibodies
using DNA interaction with Pt(II) complex / S.S Babkina, N.A. Ulakhovich, Yu.I.
Zyavkina // Anal. Chim. Acta 2004. - V.502. - P.23-30
.Katayama
Y. Bioaffinity sensor to Antibodies Using DNA Modified Au Electrode/ Y.
Katayama, M. Nakayama, H. Irie, K. Nakano, M. Maeda // Chem. Lett. 1998. -
P.1181-1182