Ионохроматографическое определение неорганических анионов в нефти
Федеральное государственное
автономное
образовательное учреждение
высшего образования
«СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ
УНИВЕРСИТЕТ»
Институт нефти и газа
Кафедра химии и химической
технологии природных энергоносителей и углеводородных материалов
КУРСОВАЯ
РАБОТА
Ионохроматографическое
определение неорганических анионов в нефти
СОДЕРЖАНИЕ
ионный хроматография нефть потенциометрический
Введение
Литературная
часть
.1
Основы метода ионной хроматографии
1.1.1 Двухколоночная ионная хроматография
.2 Коррозионное действие солей, содержащихся в
нефти
.3 Обессоливание и обезвоживание нефти
.4 Потенциометрическое титрование
Экспериментальная часть
.1 Реактивы, приборы и оборудование
.2 Методика эксперимента
.3 Объекты исследования
.4 Пробоподготовка
.5 Обсуждение результатов
Выводы
Список использованных источников
ВВЕДЕНИЕ
В транспортировке нефти и ее переработке
основные проблемы коррозионного износа связаны с наличием сероводорода,
неорганических солей, механических примесей в виде песка, глины и других пород,
а так же воды. При перегонке нефти примеси могут частично оседать на стенках
труб, что приводит к ускорению износа аппаратуры. Перегонка нефти, содержащей
соли, становится невозможной из-за интенсивной коррозии аппаратуры, а так же
отложения солей в трубах печей и теплообменниках. В частности, ионы хлора
оказывают большое влияние на внутренние стенки трубопровода, вызывая наиболее
опасную локальную коррозию, которая развивается с высокой скоростью и
вследствие малых размеров обнаруживается только в момент выхода оборудования из
строя. Поэтому коррозия часто является причиной возникновения пожароопасных и
взрывоопасных ситуаций.
В связи с вышеперечисленным, перед химиками
стоит важная практическая задача определения неорганических анионов в сырой
нефти.
Современным чувствительным, селективным,
экспрессным и универсальным методом анализа неорганических ионов является
ионная хроматография, поэтому именно этот физико-химический метод анализа был
выбран мной для исследования образцов нефти.
Целью данной работы является определение
неорганических анионов в образцах нефти методом двухколоночной ионной
хроматографии.
Объектами исследования являются образцы нефти из
северных месторождений.
Задачами данной работы являются:
) Освоить метод ионной хроматографии и
способы пробоподготовки нефти
) Провести сравнительное исследование
концентраций неорганических анионов в образцах.
) Провести сравнительное исследование
между методом потенциометрического титрования и методом двухколоночной ионной
хроматографии.
1 ЛИТЕРАТУРНАЯ
ЧАСТЬ
.1 Основы
метода ионной хроматографии
Ионная хроматография - метод разделения
органических и неорганических ионов, высокоэффективный вариант ионообменной
хроматографии с применением кондуктометрического детектирования
разделенныхионов.
В основе метода ионной хроматографии лежит
процесс ионного обмена между ионообменником и анализируемым раствором.
Ионная хроматография представляет собой вариант
колоночной элюентной ионообменной хроматографии. Подвижная фаза (элюент) служит
для перемещения веществ через хроматографическую систему. Разделение в этом
случае происходит благодаря разному сродству компонентов определяемой смеси к
неподвижной фазе и, следовательно, разным скоростям перемещения по колонке.
Неподвижной фазой в ионообменной хроматографии является ионообменник.
Ионный обмен заключается в том, что некоторые
вещества (ионообменники) при погружении в раствор электролита поглощают из него
катионы или анионы, выделяя в раствор эквивалентное число других ионов с
зарядом того же знака.
Разделение анионов производится на
анионообменниках, содержащих фиксированные группы -NR3, -NHR2,
-NH2R и анионы как противоионы. Наиболее распространенными элюентами
при определении анионов являются (1-5)'10~3 М растворы карбоната,
гидрокарбоната или гидроксида натрия.
Время и порядок элюирования анионов определяется
их зарядом и размером гидратированного иона. Ионы удерживаются тем сильнее, чем
больше их заряд и размер гидратированного иона. Элюирующая способность
подвижной фазы возрастает с увеличением концентрации ионов, содержащихся в ней,
и их сродства к ионообменнику.
Результатом ионхроматографического исследования
является хроматограмма - график зависимости электропроводности исследуемого
раствора от времени анализа, т.е. каждый пик на хроматограмме [1] .
С помощью метода ионной хроматографии можно
определить ионный состав практически любого жидкого объекта.
Особенности метода ионной хроматографии:
· возможность определения требуемых
ионов за один анализ в пробах с мешающими ионами и/или органическими
соединениями;
· универсальность - определение
катионов и анионов (в том числе органических);
· широкий выбор проверенных методик по
различным областям применения от экологического контроля до анализа напитков и
технических продуктов.
Преимущества метода:
· низкий предел обнаружения метода с
химическим подавлением фона до 2-4 мкг/л (для анионов);
· широкий линейный диапазон
определения с электронным подавлением фона 5-25000 мкг/л (для хлорид-аниона);
· минимальная величина пробы 200-500
мкл;
· возможность автоматизации всех стадий
процесса от пробоподготовки до детектирования;
· относительно высокая
производительность при использования автосамплера.
Ограничения метода:
· ограниченно используется для анализа
органических соединений;
· ограниченно используется для анализа
металлов;
· ограниченно используется для анализа
полимеров;
· не используется для анализа газов
Широкое распространение ионной хроматографии в
геологии, биохимии, фармацевтике и медицине, а также для контроля объектов
окружающей среды и пищевых продуктов обусловлено рядом ее несомненных
достоинств:
возможностью одновременного определения
большого спектра неорганических и органических катионов или анионов;
высокой чувствительностью определения
без предварительного концентрирования, селективностью и экспрессностью;
малым объемом анализируемой пробы;
широким диапазоном определяемых
концентраций;
возможностью использования различных
детекторов и их комбинаций, что позволяет обеспечить селективность и малое
время определения;
отсутствием предварительной пробоподготовки во
многих случаях [2].
1.1.1 Двухколоночная
ионная хроматография
Этот вариант ИХ основан на подавлении фоновой
электропроводности электролита (подвижной фазы), содержащегося в элюенте для
разделения смеси ионов на колонке, с помощью второй ионнообменной колонки,
расположенной между разделительной колонкой и детектором. Блок-схема
хроматографа представлена на рисунке 1 [3].
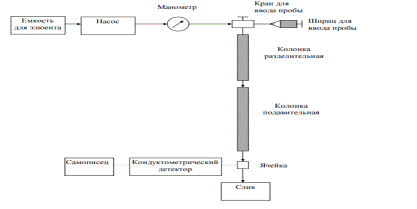
Рисунок 1 - Блок-схема ионного
хроматографа
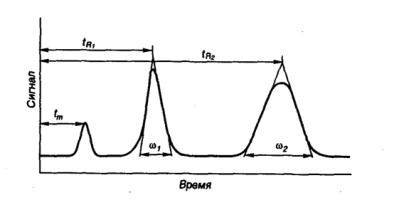
Рисунок 2 - Хроматограмма смеси двух веществ
Существуют два способа детектирования - прямой и
косвенный. В первом способе элюент переводят в соединение с низкой
электропроводностью, а определяемый ион - в высокопроводящее соединение и
детектирование проводят по положительным, пикам. Во втором - наоборот.
В двухколоночном методе используются две
последовательно соединенные хроматографические колонки. В первой колонке ионы
разделяются с помощью ионообменной смолы низкой емкости, в качестве элюентов
используются сильно разбавленные растворы электролитов. Во второй колонке
высокой емкости происходит подавление фоновой активности элюента за счет его
химической модификации [5].
Элюенты, предназначенные для двухколоночной
системы, должны отвечать двум основным требованиям: вытеснять ионы из
разделительной колонки и вступать в реакции обмена в подавительной системе с
образованием слабо диссоциирующих соединений, обладающих низкой проводимостью.
Наиболее распространенными элюентами для определения анионов являются
разбавленные растворы солей угольной кислоты (NaHCO3). Анионит в
разделяющей колонке находится в НСОз-- форме. Подавляющей
системой служит колонка, заполненная катионообменником высокой емкости в Н+
- форме. В этом случае, в разделяющей и подавляющей колонках имеют место
следующие равновесия:
разделяющая колонка:
R-HCO3
+ Na+
+ (Cl-,
NO3-)
↔ R-Na
+ H2CO3, (1)
подавляющая колонка:
R-H
+ Na+
+ HCO3-
↔ R-Na
+ H2CO3,
(2)
R-H + Na+ + (Cl-,
NO3-) ↔ R-Na + H+ + (Cl-, NO3-). (3)
Определяемые анионы попадают в
кондуктометрический детектор в виде сильных кислот (HCI, HNO3),
имеющих высокую электропроводность на фоне слабой угольной кислоты Н2СО3.
Эквивалентная электропроводность Н+ выше электропроводности
катионов. Такая система детектирования обеспечивает максимальную
чувствительность определения.
Пределы детектирования анионов лежат в интервале
0,1 - 1,0 мг/дм3. Метод прост и пригоден для разделения
неорганических и органических анионов как при анализе загрязнений окружающей
среды - воздуха и воды, так и при анализе сложных образцов различного ионного
состава, в том числе пищевых продуктов и медикаментов [4].
Важным достоинством двухколоночного варианта
ионной хроматографии являются низкие пределы обнаружения ионов и линейность
градуировочного графика в широком интервале их концентрации. Это дает возможность
использовать метод стандартов в количественном анализе без обязательного
построения градуировочного графика [6].
1.2 Коррозионное
действие солей, содержащихся в нефти
Нефть представляет собой многокомпонентную
смесь, в основном углеводородов разного строения с различной молекулярной
массой и с небольшой примесью минеральных соединений. При добыче,
транспортировании и переработке нефти коррозионное действие на оборудование и
трубопроводы оказывают, главным образом, примеси нефти (сероводород, соленая
вода, кислород). В нефти разных месторождений они содержатся в различных
количествах.
Все примеси нефти, оказывающие коррозионное
воздействие, можно разделить на две группы: олеофобные и олеофильные. К
олеофобным относятся те, которые по своей природе не растворимы в нефти - это
вода и растворенные в ней неорганические соли, а также твердые соли,
механические примеси (песок, глина), свободный сероводород и др. Эти примеси
находятся в другой фазе, диспергированной в нефти [7].
Как известно, нефть вместе с сопутствующей ей
пластовой водой залегает в геологических формациях, состоящих из таких пород,
как песчаники, известняки, доломит и др. Породы, в которых залегает нефть и с
которыми контактирует пластовая вода (хлориды, сульфиды, карбонаты и др.), определяют
состав и концентрацию минеральных солей, содержащихся в ней. В процессе добычи
нефти обычно сопутствующая пластовая вода своим напором вытесняет нефть из
пористых пород пласта к скважинам. В зависимости от структурных свойств пласта,
скорости отбора нефти, ее вязкости и по другим причинам приток воды к скважине
вместе с нефтью может быть разным. В начальный период добычи на новом
месторождении из скважин часто получают безводную или малообводненную нефть.
Однако со временем обводненность добываемой нефти увеличивается с различной
скоростью и на старых промыслах иногда достигает 80-90%. Средняяобводненность
добываемой в нашей стране нефти в настоящее время превышает 50% [8].
В процессе добычи и совместного движения нефти и
пластовой воды при транспорте образуется эмульсия воды в нефти. Устойчивость
эмульсии зависит от состава нефти и условий ее смешения с пластовой водой.
Часть пластовой воды отделяется в резервуарах сборных парков. Для более полного
отделения пластовой воды, а вместе с ней и растворенных солей, требуется
максимальное разрушение водонефтяной эмульсии, что обусловливает применение
специальной обработки сырой нефти реагентами - деэмульгаторами на промысловых
установках подготовки нефти [7].
На промыслах для обезвоживания нефти широко используют
так называемый внутритрубный способ деэмульгировання как наиболее эффективный.
Состав и содержание после промысловой подготовки олеофобных примесей в нефти,
поступающей на нефтеперерабатывающие предприятия, представлен в таблице
Таблица 1- Состав и содержание олеофобных
примесей в нефти
|
Вода,
%
|
0,1-2,0
|
|
Хлориды,
мг/л
|
20-3000
|
|
Механические
примеси, ррm
|
2,5-1500
|
|
Сероводород
(нерастворенный), %
|
0-0,5
|
Таким образом, в сырой нефти остается
относительно небольшое количество олеофобных загрязнений. Однако даже в таком
количестве олеофобные примеси в нефти, поступающей на переработку, приносят
большой вред, поскольку вызывают хлористоводородную и сероводородную коррозию
всего нефтеперегонного оборудования. Кроме того, при подогреве нефти выпадающие
из пластовой воды соли забивают трубы теплообменников, печей и нарушают
нормальный технологический режим установок, что приводит к ухудшению качества
нефтепродуктов и сокращению сроков работы оборудования. Содержание воды в
нефти, поступающей на перегонку, не должно превышать 0,1-0,2%, так как сама
вода является наиболее нежелательной олеофобной примесью, так как приводит к
повышению давления в аппаратуре установок перегонки нефти. Уже на испарение
воды при перегонке затрачивается в восемь раз больше тепла, чем на испарение
такого же количества углеводородов нефти. В присутствии воды при подогреве
нефти происходит гидролиз хлоридов и образуется соляная кислота, оказывающая
сильное коррозионное действие на оборудование [9].
При транспортировании и хранении нефти, содержащей
даже небольшое количество воды, образуется смесь водонефтяной эмульсии с
механическими примесями, так называемый донный осадок, который скапливается в
емкостях, резервуарах и трубах. Донный осадок нельзя сбрасывать вместе со
сточной водой, так как в нем содержится много нефти. Кроме эмульсии пластовой
воды в некоторых нефтях иногда содержатся кристаллические хлориды, что еще
более усложняет подготовку нефти к переработке, кристаллические соли в нефти
могут быть и результатом испарения воды при местных перегревах в процессе
сепарации и подготовки нефти, когда вода частично испаряется, а соли выпадают в
виде кристаллов. Вымывание кристаллов солей водой из нефти связано с большими
трудностями, так как кристаллы обволакиваются гидрофобной пленкой асфальтенов и
смолистых веществ, препятствующих смачиванию их водой.
Наибольшее коррозионное действие на оборудование
в процессе перегонки нефти оказывают хлориды, попадающие в нефть вместе с
эмульгированной пластовой соленой водой. В пластовой воде в растворенном виде
содержатся преимущественно хлориды натрия, магния и кальция. При подогреве
нефти до 120°С и выше наиболее легко гидролизуются хлориды магния и кальция.
Гидролиз хлорида магния идет по следующим уравнениям:
MgCl2
+ H2O
= MgOHCl + HCl
(4)
MgCl2 + 2H2O =
Mg(OH)2 + 2HCl (5)
Скорость гидролиза сильно увеличивается с
повышением температуры. Так, по литературным данным, хлорид магния,
содержащийся в нефти, при подогреве до 343°Сгидролизуется на 90%.
По степени гидролиза хлориды можно расположить в
следующий ряд:
3
и AlCl3> MgCl2> СаСl2>NaCl
В условиях перегонки нефти хлорид натрия
теоретически не должен гидролизоваться, однако в присутствии других солей он
может способствовать значительному увеличению хлористоводородной коррозии,
например MgSO4. В процессе подогрева нефти MgSO4
реагирует с NaCl с образованием легко гидролизующегося MgCl2 [10].
1.3 Обессоливание
и обезвоживание нефти
Обезвоживание нефти проводят путем разрушения
(расслоения) водно-нефтяной эмульсии с применением деэмульгаторовразличных ПАВ,
которые, адсорбируясь на границе раздела фаз, способствуют разрушению капель
(глобул) диспергированной в нефти воды. Однако даже при глубоком обезвоживании
нефти до содержания пластовой воды 0,1-0,3% (содержание хлоридов: 100-300
мг/л).
Поэтому одного только обезвоживания для
подготовки к переработке нефтей большинства месторождений недостаточно.
Оставшиеся в нефти соли и воду удаляют с помощью принципиально мало
отличающейся от обезвоживания операции, называется обессоливанием. Последнее заключается
в смешении нефти со свежей пресной водой, разрушении образовавшейся эмульсии и
последующем отделении от нефти промывной воды с перешедшими в нее солями и
механическими примесями.
Эмульсия - это гетерогенная система, состоящая
из двух несмешивающихся или малосмешивающихся жидкостей, одна из которых
диспергирована в другой в виде мелких капель (глобул) диаметром, превышающим
0,1 мкм.
Образование эмульсий связано с поверхностными
явлениями на границе раздела фаз дисперсной системы, прежде всего поверхностным
натяжением-силой, с которой жидкость сопротивляется увеличению своей
поверхности.
На НПЗ поступают эмульсии воды в нефти. Они
являются весьма стойкими и в большинстве случаев не расслаиваются под действием
одной только силы тяжести. Поэтому необходимо создать условия, при которых
возможно укрупнение, слияние глобул воды при их столкновении и выделение из
нефтяной среды. Чем благоприятнее условия для передвижения капель, тем легче
разрушаются эмульсии [10].
Различные нефти обладают разной склонностью к
образованию эмульсии (эмульсионность) и по этому показателю, измеряемому в
процентах, они разделяются на три группы: высокоэмульсионная (эмульсионность от
80 до 100 %), промежуточная (эмульсионность 40 %), низкоэмульсионная
(эмульсионность 1,3-8,0%). Оценка эмульсионностинефтей позволяет выбирать
оптимальный режим и схему процесса их обезвоживания и обессоливания [11].
Методы разрушения водонефтяных эмульсий.
Эмульсии подвергают различным воздействиям,
направленным на укрупнение капель воды, увеличение разности плотностей
(движущая сила расслоения), снижение вязкости нефти.
Для обезвоживания и обессоливания нефти
используют следующие технологические процессы:
) гравитационный отстой нефти;
) горячий отстой нефти;
) подогрев эмульсии (термообработка);
) применение электрического поля
(электрообработка).
На практике в основном применяется сочетание
термодинамического и электрического способов разрушения эмульсии [12].
Обессоливание нефтей.
Наряду с обезвоживанием необходимо глубокое
обессоливание нефти. Все упомянутые выше факторы способствуют интенсификации
выделения воды из эмульсии, но не влияют на засоленность остающихся после
обезвоживания капель воды в нефти. С целью достижения не только глубокого
обезвоживания, но и обессоливания нефти используют промывку нефти свежей
пресной водой. Роль этой промывной воды двояка. С одной стороны, смешиваясь с
солёными каплями воды эмульсии, она разбавляет их и уменьшает концентрацию
солей в них, а с другой стороны, турбулизирует поток нефтяной эмульсии,
способствуя также коалесценции капель, т.е. оказывает гидромеханическое
воздействие на эмульсию [13].
Количество оставшихся в нефтях солей зависит как
от содержания остаточной воды, так и от ее засоленности. Поэтому с целью
достижения глубокого обессоливания осуществляют промывку солей подачей в нефть
оптимального количества промывной (пресной) воды. При подаче промывной воды
только 1 % участвует в разбавлении капель солёной воды, находящейся в эмульсии,
а остальное количество промывной воды является только турбулизатором, поэтому
подаётся до 1 % пресной воды и от 4 до 5% рециркулирующей, уже использованной
от массы нефти, что позволяет в 5-6 раз снизить количество сбрасываемой сточной
солёной и загрязнённой воды и уменьшить мощности по её обезвоживанию. При
чрезмерном увеличении количества промывной воды растут затраты на обессоливание
нефти и количество образующихся стоков. В этой связи с целью экономии пресной
воды на ЭЛОУ многих НПЗ успешно применяют двухступенчатые схемы с противоточной
подачей промывной воды: свежая вода поступает на вход последней ступени, а
дренажная выводится из первой. Число ступеней (1, 2 или 3) обессоливания нефти
определяется свойствами исходной эмульсии и содержанием в ней солей [14].
1.4 Потенциометрическое
титрование
Метод потенциометрического титрования основанна
измерении равновесной разности потенциалов между двумя электродами, один из
которых является индикаторным (или рабочим), другой - электродом сравнения.
Равновесный потенциал индикаторного электрода зависит от концентрации (точнее -
активности) анализируемого компонента в растворе. Для измерения разности
потенциалов (ЭДС) собирают электрохимическую ячейку, включающую гальваническую
цепь из двух полуэлементов:
электрод сравнения || анализируемый раствор |
индикаторный электрод Например:
, H2 | H+ || Cu2+
| Cu (6)|
Hg2Cl2, KCl || Fe3+, Fe2+ | Pt (7)
При погружении двух электродов в анализируемый
раствор возникающая разность потенциалов составляет электродвижущую силу
гальванической цепи, которая измеряется практически в отсутствие тока:
ЭДС. = |Eср. - Eинд. | (8)
Измерительными устройствами в данном методе
анализа служат потенциометры разных типов.
В потенциометрическом титровании индикация точки
эквивалентности проводится по резкому скачку величины измеряемой ЭДС, которая
изменяется благодаря изменению равновесного потенциала индикаторного электрода
(Eинд.) в результате химической реакции с участием потенциалопределяющего
компонента. Величина скачка связана с заменой одной потенциалопределяющей
реакции, протекающей до точки эквивалентности, на другую после ее достижения.
Кривые титрования, построенные в координатах ЭДС (мВ) - объем титранта (мл),
аналогичны расчетным кривым титрования в разных методах титриметрии с
использованием индикаторов. Метод потенциометрического установления точки
эквивалентности по своим возможностям превосходит титриметрические методы с
применением цветных индикаторов. Он обладает большей точностью,
чувствительностью, позволяет анализировать окрашенные и мутные растворы,
допускает возможность дифференцированного определения веществ в одном растворе
и позволяет автоматизировать процесс титрования. Как и в обычном
титриметрическом анализе, в потенциометрическом титровании используются реакции
нейтрализации, осаждения, комплексообразования, окисления-восстановления.
Требования к реакциям титрования те же, что и при химической индикации: высокая
скорость прямой реакции; строгая стехиометричность и практическая
необратимость, отсутствие побочных реакций.
Методика определения концентраций хлорид ионов в
нефти методом потенциометрического титрования описана в ГОСТ 21534[17].
Два
результата определений, полученные одним исполнителем, признаются достоверными
(с 95%-ной доверительной вероятностью), если расхождение между ними не
превышает значений, приведенных в таблице 2.
Таблица 2
|
Массовая
концентрация хлористых солей, мг/дм Сходимость,
мг/дм Сходимость,
мг/дм
|
|
|
50
|
3
|
|
от
50 до 100
|
|
от
100 до 200
|
12
|
|
от
200 до 500
|
27
|
|
от
500 до 1000
|
50
|
|
от1000
до 2000
|
100
|
|
более
2000
|
6%
значения меньшего результата
|
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1 Реактивы, приборы и
оборудование
При выполнении работы использовались следующие
реактивы:
ГСО 7262-96 состава раствора хлорид-ионов, ОАО
«Уральский завод химических реактивов»;
ГСО 7258-96 состава раствора нитрат-ионов, ОАО
«Уральский завод химических реактивов»;
ГСО 7789-2000 состава раствора фторид-ионов, ОАО
«Уральский завод химических реактивов»;
ГСО 7253-96 состава раствора сульфат-ионов, ОАО
«Уральский завод химических реактивов»;
карбонат натрия, х.ч.;
гидрокарбонат натрия, х.ч.;
н-гексан, х.ч.;
азотная кислота, х.ч.;
вода деионизованная;
образца нефти северных месторождений
Красноярского края.
В работе были использованы следующие приборы и
посуда: колбы мерные объемом 25, 50, 100, 500 мл, ГОСТ 1770-74; мерные пипетки
объемом 1, 5, 10 мл; воронки стеклянные ГОСТ 8613-75; мерный цилиндр объемом
100 мл, ГОСТ 1770-74; химические стаканы объемом 50, 100, 200 мл, ГОСТ 1770-74;
бумажные фильтры «Синяя лента» диаметром 9 см; весы лабораторные MettlerToledoXP603S,
микрошприцHamilton.
Работу выполняли на высокоэффективном жидкостном
хроматографе LC-20Prominence с кондуктометрическим детектором в варианте
двухколоночной (разделяющая колонка120×5 мм
КанК-АСт, 14 мкм;подавительная колонка СПС-SAC, 50 мкм, 200×6
мм
с катионитом в H+-форме). В качестве элюента применяли карбонатный
буферный раствор (1,9 мМNa2CO3+ 2,4мМ NaHCO3).
Объем вводимой пробы 20мкл. Скорость потока элюента составляла 1,0 мл/мин.
Температура термостата колонки 33 °С.
Внешний вид хроматографа LC-20Prominence
представлен на рисунке 3:

Рисунок 3 - Высокоэффективный жидкостной
хроматографLC-20 Prominence
2.2 Методика эксперимента
Предварительно готовили исходные растворы для приготовления
элюентов 0,1 М Na2CO3
и 0,1 М NaHCO3.
Для этого в колбы вместимостью 500 мл помещали 5,3 г Na2CO3
и
4,2 г NaHCO3
и, перемешивая, доводили деионизованной водой до метки.
Элюент готовили следующим образом: в колбу
вместимостью 500 мл добавляли 9,5 мл 0,1 М Na2CO3
и 12,0 мл 0,1 М NaHCO3
и, перемешивая, доводили деионизованной водой до метки. Получали раствор
рабочего элюента 2,4 мМNaHCO3
и 1,9 мМNa2CO3.
2.3 Объекты исследования
Объектом исследования были образцы нефти
северных месторождений Красноярского края. Образцы были предоставлены ИНиГ СФУ.
2.4 Пробоподготовка
В ходе изучения дипломной работы известно, что
оптимальная область определения концентрации неорганических анионов в экстракте
нефти при объемном соотношении нефти и экстрагента 1:10, температуре
экстрагента 90°С и времени экстрагирования 20 мин [15].
Способ «горячей экстракции»
Для определения неорганических анионов в нефти
пробу экстрагировали деионизованной водой, нагретой до температуры 90 ºC.
в соотношении 1 мл нефти к 10 мл деионизированной воды.
Перед введением в хроматограф полученные
экстракты помещали в делительную воронку вместимостью 50 мл, добавляли 2,5 мл
гексана и экстрагировали в течение 10 мин, периодически открывая пробку.
После расслоения смеси нижний водный слой
фильтровали через шприцевой фильтр. В делительной воронке оставляли немного
водного слоя, чтобы избежать попадания в колбу гексанового экстракта.
2.5 Обсуждение результатов
Ранее было установлено [16], что наилучшее
разделение F-,
CI-,
NO3-,
SO42-
- ионов на применяемой хроматографической системе наблюдается при использовании
элюента состава 2.4 мМNaHCO3
и 1,9 мМNa2CO3
при скорости элюента 1,0 мл/мин. Поэтому в данных оптимальных условиях
проводили разделение смеси неорганических анионов.
Результаты анализа стандартного раствора
представлены на рисунке 4 и в таблице 3:
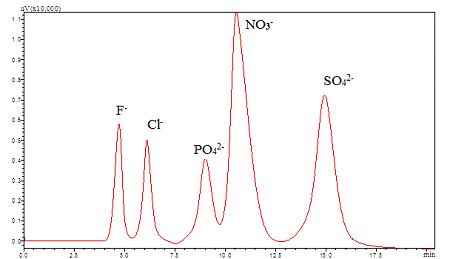
Ионный хроматограф LC-20
Prominence. Разделяющая
колонка 120×5 мМКанК-АСт 14 мкм,
ν=1,0 мл/мин.Составэлюента:
1,9 мМNa2CO3+2,4
мМNaHCO3
Рисунок 4 - Результаты анализа стандартной смеси
анионов
Таблица 3 -
Результаты анализа стандартного раствора
|
Ион
|
Время
удержания, мин
|
Площадь
пика
|
|
Cl-
|
6,119
|
133496
|
|
SO42-
|
14,928
|
483156
|
|
NO3-
|
10,585
|
622817
|
|
|
|
|
|
|
На рисунках 5 и 6 приведены хроматограммы
вытяжки из нефти при экстракции горячей водой, результаты определения
неорганических анионов в образцах нефти - в таблице 4.
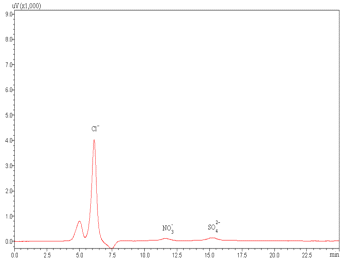
Ионный хроматограф LC-20
Prominence. Разделяющая
колонка 120×5 мм КанК-АСт 14 мкм,
ν=1,0 мл/мин.Состав
элюента: 1,9 мМNa2CO3+2,4
мМNaHCO3
Рисунок 5 - Хроматограмма вытяжки из нефти.
Экстрагент - бидистиллированная вода (T=90±2°C)
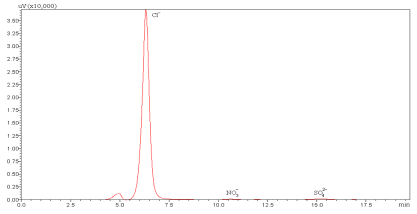
Ионный хроматограф LC-20
Prominence. Разделяющая
колонка 120×5 мм КанК-АСт 14 мкм,
ν=1,0 мл/мин.Состав
элюента: 1,9 мМNa2CO3+2,4
мМNaHCO3
Рисунок 6 - Хроматограмма вытяжки из нефти.
Экстрагент - бидистиллированная вода (T=90±2°C)
Таблица 4 - Содержание неорганических анионов в
образцах нефти северных месторождений Красноярского края (экстрагент - бидистиллированная
вода (T=90±2°C)),
n=3, P=0,95
|
Номер
пробы
|
Анион
|
Время
удерживания, мин
|
С,
мг/л
|
Cl-
|
6,072
|
6,09±0,04
|
|
NO3-
|
10,29
|
0,42±0,02
|
|
SO42-
|
15,01
|
0,52±0,02
|
|
2
|
Cl-
|
6,087
|
103±4
|
|
NO3-
|
10,31
|
0,71±0,02
|
|
SO42-
|
15,03
|
0,54±0,02
|
|
3
|
Cl-
|
6,075
|
2,51±0,02
|
|
NO3-
|
10,32
|
0,62±0,02
|
|
SO42-
|
15,02
|
0,31±0,02
|
|
4
|
Cl-
|
6,141
|
3,91±0,02
|
|
SO42-
|
15,162
|
0,06±0,01
|
ВЫВОДЫ
1. Методом ионной хроматографии были
определены неорганические анионы в различных образцах нефти.
2. В пробах нефти были обнаружены хлорид-,
нитрат- и сульфат- ионы. Концентрации анионов составили:
Хлорид-ион:от 3,91±0,02мг/л до103±4мг/л
Нитрат-ион:от 0,42±0,02мг/л до0,71±0,02мг/л
Сульфат-ион:от 0,06±0,01мг/л до0,54±0,02мг/л
Так же было обнаружено, что проба №4 не содержит
нитрат-ион.
. Был проведен сравнительный анализ
характеристик потенциометрического и ионохроматографического методов, из
которого следует вывод, что метод ионной хроматографии является более
экспрессным и чувствительным методом, что делает его более предпочтительным при
проведении анализа.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Хроматография.
Основные понятия. Терминология / под ред. С.А. Волков. -М.: Химия, 1997. - 48с.
. Золотов,
Ю.А. Основы аналитической химии: в 2 т. Т. 2 / Ю.А. Золотов. - Высшая школа,
2000. - 494 с.
. Айвазов,
Б.Н. Введение в хроматографию / Б.В. Айвазов. - М.: Высшая школа, 1984. - 384
с.
. Отто,
М. Современные методы аналитической химии: в 2 т. Т. 2 / М. Отто. - М.:
Техносфера, 2004. - 288 с.
5. Фритц,
Дж. Ионная хроматография / Дж. Фритц, Д. Гьертде, К. Поланд. - М.: Мир, 1995. -
221с.
. Шпигун,
О.А. Ионная хроматография и ее применение в анализе вод/О.А. Шпигун, Ю.А.
Золотов. - М.: МГУ, 1990. - 199 с.
7. Батуева,
И.Ю. Химия нефти / И.Ю. Батуева. - Л.: Химия, 1984. - 360с.
8. Егоров,
Н.И.Химия нефти и газа /Н.И. Егоров, А.И.Богомолов; В.А. Проскурякова, А.Е.
Драбкина.- М.: Наука, 1962. - 293с.
. Бакиров,
А.А. Теоретические основы поисков и разведки нефти газа / А.А. Бакиров, Э.А.
Бакиров, Г.А. Габриэлянц, В.Ю. Керимов, Л.П. Мстиславская - М.: Недра, 2012 -
9с.
. Вержичинская
С.В. Химия и технология нефти и газа / С.В. Вержичинская, Н.Г. Дигуров, С.А.
Синицин. - М.: Форум, 2013. - 124 с.
. Эрих,
В.Н. Химия и технология нефти и газа / В.Н. Эрих, М.Г. Расина, М.Г. Рудин. -
Л.: Наука, 1992. - 96 с.
. Филимонова,
Е.И. Основы технологии переработки нефти: Учебное пособие / Е.И. Филимонова. -
Ярославль: ЯГТУ, 2010. - 171 с.
. Баннов,
П.Г. Процессы переработки нефти / П.Г.Баннов. - М.: ЦНИИТЭ, 2000. - 224 с.
. Логинов,
В.И. Обезвоживание и обессоливание нефтей/ В.И.Логинов. -М.: Химия, 1979. -
216с.
. Иванова,
А.А. Ионохроматографическое определение хлорид-ионов в нефти: диплом.работа /
А.А. Иванова, О.П. Калякина. - 2015. - 46 с.
16. Юсенко,
Е.В. Определение щавелевой кислоты методом ионной хроматографии с
кондуктометрическим детектированием на ионитах различного типа / Е.В. Юсенко,
О.П. Калякина, А.И. Лыжова, Е.А. Полынцева// Сорбционные и хроматографические
процессы. - 2013. - Т.13.№3. - С.379 - 386.
17. ГОСТ21534
Нефть. Методы определения содержания хлористых солей (с изменениями N1,
2)-Введ. 01.01.1977. - Москва :Стандартинформ, 1977. -78 с.