|
Период
|
Характеристика
|
|
Допастеровекая
эра (1865)
|
Использование
спиртового и молочнокислого брожения при получении пива, вина, хлебопекарных
и пивных дрожжей, сыра. Получение ферментированных продуктов и уксуса.
|
Производство
этанола, бутанола, ацетона, глицерина, органических кислот, вакцин. Аэробная
очистка канализационных вод. Производство кормовых дрожжей из углеводов.
|
|
Период
антибиотиков (1940-1960 гг.)
|
Производство
пенициллина и других антибиотиков путем глубинной ферментации.
Культивирование растительных клеток и получение вирусных вакцин.
Микробиологическая трансформация стероидов.
|
|
Период
управляемого биосинтеза (1961-1975гг.)
|
Производство
аминокислот с помощью микробных мутантов. Получение очищенных ферментных
препаратов. Промышленное использование иммобилизованных ферментов и клеток.
Анаэробная очистка канализационных вод и получение биогаза. Производство
бактериальных полисахаридов.
|
|
Эра новой
биотехнологии (с 1973 г.)
|
Использование
клеточной и генетической инженерии в целях получения агентов биосинтеза.
Получение гибридов, продуцирующих моноклональных антител, трансплантация
эмбрионов.
|
Принципиальной основой деления истории биотехнологии на 5
периодов явились использовавшиеся технологии, их совершенствование с получением
все более качественных биопродуктов.
Основные цели и задачи биотехнологии [7]
Во-первых, активация и поддержание путей обмена клеток,
ведущих к накоплению заданных продуктов при доминировании над другими реакциями
обмена у культивируемого организма;
Во-вторых, получение клеток или их составных частей
(преимущественно ферментов) для направленного изменения сложных молекул;
В-третьих, создание безотходных и экологически безопасных
биотехнологических процессов;
В-четвертых, совершенствование и оптимизация аппаратурного
оформления биотехнологических процессов с целью достижения максимального выхода
конечных продуктов при культивировании естественных видов методами генной и
клеточной инженерии;
В-пятых, повышение технико-экономических показателей
биотехнологических процессов по сравнению с существующими.
Также в задачи биотехнологии входит создание и широкое
освоение:
) новых биологически активных веществ (БАВ) и лекарственных
препаратов для медицины (инсулина, гормонов и др.), позволяющих осуществить
раннюю диагностику и лечение тяжелых заболеваний;
) микробиологических средств защиты растений от болезней и
вредителей, бактериальных удобрений и регуляторов роста культур; новых
высокопродуктивных и устойчивых к неблагоприятным факторам внешней среды сортов
и гибридов;
) ценных кормовых добавок и БАВ для повышения продуктивности
животноводства; новых методов биоинженерии для эффективной профилактики,
диагностики и терапии основных болезней с/х животных;
) новых технологий получения ценных продуктов для
использования в пищевой, химической, микробиологической и других отраслях
промышленности;
) технологий глубокой и эффективной переработки с/х,
промышленных и бытовых отходов, использования сточных вод для производства
биогаза и высококачественных удобрений.
биотехнология наука биообъект
2.
Основные направления биотехнологии
В зависимости от того какой признак положен в основу
существует различная классификация направлений биотехнологии. Например, по
биологическому объекту, используемому в биотехнологическом производстве -
микроорганизмам, растениям и животным, выделяют 3 типа - микробиотехнологию,
фитобиотехнологию и зообиотехнологию соответственно (рис. 3) [2,6].
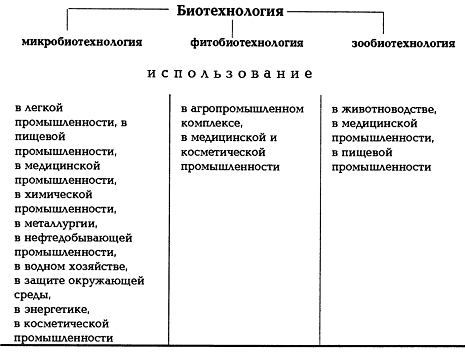
Рис. 3. Направления биотехнологии (Н.П. Еленов, 1995)
Биотехнология как современная отрасль высоких технологий,
основой которой является биология, биологические процессы с живыми организмами
развивается по различным самостоятельным научным направлениям:
сельскохозяйственная, фармацевтическая, промышленная, экологическая,
молекулярная биотехнология, иммунобиотехнология и др [9].
2.1
Сельскохозяйственная биотехнология
Это направление охватывает растениеводство, животноводство и
ветеринарию. Использование биотехнологии в с/х ориентировано на [8]:
· стабильное развитие с/х производства;
· решение
проблемы продовольственной безопасности;
· получение высококачественных, экологически
чистых продуктов питания;
· переработку отходов с/х производства;
· восстановление
плодородия почв.
В данном направлении наиболее приоритетным является:
· создание новых сортов с/х растений и
животных с использованием современных постгеномных и биотехнологических
методов;
· разработка и внедрение методов геномной
паспортизации для повышения эффективности селекционно-племеной работы,
технологий клонирования животных-производителей;
· производство биопрепаратов для
растениеводства и ветеринарии;
· производство кормовых добавок для с/х
животных.
Актуальна задача уменьшения применения в сельском хозяйстве
средств химизации, пестицидов и расширение использования бактериальных удобрений,
инсектицидов микробного происхождения; разработка генно-инженерных вакцин и
диагностикумов на основе моноклональных антител [2].
2.2
Медицинская биотехнология
В литературе [8] выделяют 2 типа медицинских биотехнологий:
диагностические и лечебные. Современная биотехнология изучает процессы на
молекулярном и клеточном уровнях. И прежде всего, биотехнологии нашли широкое
применение в диагностике заболеваний. В мире уже разработано более 1 000
биотехнологических тест-систем, основанных на ДНК. В 1983 г. американский
ученый Кэри Мюллис получил Нобелевскую премию за революцию в диагностике - он
изобрел генетический анализ полимерной цепной реакции (ПЦР). ПЦР позволяет
обнаружить участки ДНК вирусов и бактерий в любом биологическом материале
(слюне, крови, моче и т.д.), даже если инфекции протекают в скрытой форме.
Сегодня с помощью ПЦР диагностируют гепатит С, туберкулез, ВИЧ и др.
Одно из последних достижений биотехнологической диагностики -
метод биосенсоров, которые "отлавливают" связанные с
болезнями молекулы и подают сигналы на датчики. Биосенсорную диагностику часто
применяют в скорой помощи (например, для определения глюкозы в крови больных
диабетом).
Передовой технологией в диагностике считают микрочипы.
Их применяют для диагностики инфекционных, онко - и генетических заболеваний,
аллергенов, а также при исследовании новых лекарств [8].
Один из основных периодов истории развития биотехнологии -
это период открытия антибиотиков, их получение в лабораторных условиях и
производство в промышленных масштабах. Разработка новых антибиотиков, особенно
природного происхождения и сегодня остается первостепенной задачей для
практического здравоохранения, а также для ветеринарной и пищевой
промышленности [2].
2.3
Экологическая биотехнология
Экологическое состояние окружающей среды - это постоянно
нарастающая проблема для человеческого общества в целом. Темпы загрязнения
почвы, воды и воздуха ксенобиотиками, химическими веществами, в том числе
токсическими соединениями, тяжелыми металлами, пестицидами, коммунальными
отходами возможно приостановить, используя биологические технологии их
утилизации [2].
Отходы и побочные продукты деятельности в области с/х, лесной
и пищевой промышленности можно использовать в различных целях, в частности для
получения энергии с одновременным увеличением биомассы и уменьшением
загрязнения окружающей среды. Их также можно при помощи микроорганизмов
разлагать до сбраживаемых соединений [7].
Гипотеза о "микробиологической надежности",
предполагающая, что из-за повсеместного присутствия микроорганизмов в
окружающей среде и их большого катаболического потенциала, любое соединение,
попавшее в биосферу будет полностью минерализовано, вытекает из
основополагающей роли микроорганизмов в круговороте веществ в природе. К
сожалению, в реальности динамика антропогенного загрязнения окружающей среды
превалирует над утилизирующими "мощностями" микроорганизмов. Если
образование огромного количества жидких и твердых отходов, загазованность
крупных мегаполисов, загрязнение водоемов и почв просто очевидно, то уменьшение
вследствие этого биологического многообразия, оскудение генофонда в природе
менее заметно, но более фундаментально по актуальности.
Поэтому основными направлениями экологической биотехнологии
следует считать [2]:
· расширение спектра и объема применяемых в
растениеводстве, животноводстве и других отраслях биопрепаратов вместо
синтетических;
· ремедиация окружающей среды путем
активного извлечения и деструкции загрязняющих элементов (пестициды, тяжелые
металлы, нефть и нефтепродукты);
· утилизация ила сточных вод, твердых
коммунальных отходов;
· нитрификация, восстановление структуры,
гумуса почв путем разработки и промышленного применения безопасных для здоровья
людей, животных и растений биологических технологий.
2.4
Промышленная биотехнология
Охватывает различные отрасли народного хозяйства. Ведущим
звеном промышленный технологии (ПБ) является промышленная микробиология, так
как в основе крупных биотехнологических производств лежат микробиологические
процессы. Это получение в промышленных масштабах ферментов, антибиотиков,
аминокислот микробного происхождения, производство в качестве инсектицидов и
удобрений микробной биомассы, производство кормового белка, этанола, биогаза,
витаминов, органических кислот, полисахаридов, получение белков человека,
гормонов, биологически активных веществ на основе технологии рекомбинантных ДНК
[2].
В пищевой промышленности, применяя обычные технологические
линии по производству синтетических волокон, можно получать из искусственных
белков длинные нити, которые после пропитки их формообразующимн веществами,
придания им соответствующего вкуса, цвета и запаха могут имитировать любой
белковый продукт. Таким способом уже получены искусственное мясо (говядина,
свинина, различные виды птиц), молоко, сыры и другие продукты [10].
Собственно ПБ имеет место в горной металлургии. Это биогеотехнология
металлов [7] - наука об извлечении металлов из руд, концентратов,
горных пород и растворов под воздействием микроорганизмов или их метаболитов
при нормальном давлении и температуре. Составными ее частями являются:
) биогидрометаллургия (бактериальное выщелачивание металлов);
) обогащение руд;
) биосорбция металлов.
В нефтедобывающей отрасли находят применение микроорганизмы,
расщепляющие балластный углеводород - парафин, разжижающие нефть и облегчающие
ее извлечение на поверхность. Микроорганизмы - нефтедеструкторы используются
для очистки загрязненных нефтепродуктами почв и водоемов.
Получение биогаза (метана) также имеет реальные перспективы
развития. В процессах получения биогаза можно переработать самое разнообразное
сырье - различную растительную биомассу, включая отходы древесины, несъедобные
части сельскохозяйственных растений, отходы перерабатывающей промышленности,
специально выращенные культуры (водяной гиацинт, гигантские бурые водоросли),
жидкие отходы сельскохозяйственных ферм, промышленные и бытовые стоки, ил
очистных сооружений, а также мусор городских свалок. Важно, что сырье с высоким
содержанием целлюлозы, трудно поддающееся методам переработки, также эффективно
сбраживается и трансформируется в биогаз [11].
Биоэлектроника - это использование
биологических систем в качестве сенсоров, измерительно-контролирующих датчиков
в сфере информационных технологий.
Наряду с инженерной энзимологией (получение и
использование ферментов в биотехнологии) интенсивно развивается протоинженерия
(технологии изменения свойств природных белков на генетическом уровне,
получение новых белков) [2].
2.5 Иммунная
биотехнология
Иммунобиотехнология объединяет производства вакцин, иммуноглобулинов
крови, иммуномодуляторов, иммуномедиаторов, моноклональных антител и некоторых
других.
Она представляется частным случаем медицинской биотехнологии.
Однако, вычленение иммунобиотехнологии в качестве самостоятельной научной
субдисциплины является обоснованным, и производственные процессы здесь четко
ограничены использованием иммунной системы того или иного макроорганизма или
отдельных компонентов ее (макрофаги, лимфоциты, различные иммуноглобулины) [6].
Развитие иммунной биотехнологии было вызвано практической
необходимостью получения большого количества иммунопрепаратов для профилактики,
диагностики и лечения как инфекционных, так и неинфекционных заболеваний.
Иммунная биотехнология призвана на основе достижений иммунологии,
микробиологии, генетической инженерии создавать и производить широкий спектр
иммунных препаратов: вакцины, диагностикумы, иммунные сывортки и моноклональные
антитела (МАТ) [2].
Вакцины применяются для иммунопрофилактики, реже для лечения,
поскольку они создают активный приобретенный иммунитет. Диагностикумы
необходимы для серологической диагностики заболеваний в иммуноферментном
анализе, реакции связывания комплемента и других иммунологических реакциях.
Иммунные сыворотки востребованы при диагностике инфекционных заболеваний. А также
они применяются с лечебной целью для создания приобретенного пассивного
иммунитета.
В настоящее время МАТ используют для [1]:
· обнаружения
загрязнителей окружающей среды;
· проверки пищевых продуктов на наличие
опасных микроорганизмов;
· распознавания злокачественных клеток среди
нормальных;
· аналитических целей - как
"иммунологический микроскоп" с чрезвычайно высоким разрешением;
· диагностики инфекционных заболеваний
человека, животных и растений, а также в биотехнологии в качестве лигандов для
аффинной хроматографии.
Рис. 4. Использование достижений биотехнологии в различных
отраслях народного хозяйства (по Д. Тейлор и др., 2002).
Поскольку биотехнология используется в различных отраслях
промышленности и затрагивает многие сферы жизни человека (рис. 3,4) [1], в мире
принята следующая "цветовая" классификация биотехнологии [12]: это
"белая", "зеленая", "красная", "серая"
и "синяя" биотехнология.
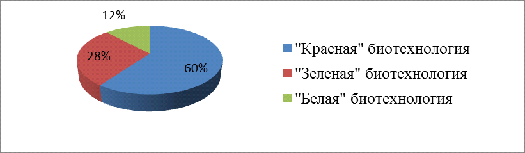
К белой биотехнологии относят промышленную
биотехнологию, ориентированную на производство продуктов, ранее производимых
химической промышленностью, - спирта, витаминов, аминокислот и др. (с учетом
требований сохранения ресурсов и охраны окружающей среды).
Зеленая биотехнология охватывает область,
значимую для сельского хозяйства. Это исследования и технологии, направленные
на создание биотехнологических методов и препаратов для борьбы с вредителями и
возбудителями болезней культурных растений и домашних животных, создание
биоудобрений, повышение продуктивности растений, в том числе с использованием
методов генетической инженерии.
Красная (медицинская) биотехнология - наиболее значимая
область современной биотехнологии. Это производство биотехнологическими
методами диагностикумов и лекарственных препаратов с использованием технологий
клеточной и генетической инженерии (зеленые вакцины, генные диагностикумы,
моноклональные антитела, конструкции и продукты тканевой инженерии и др.).
Серая биотехнология занимается разработкой
технологий и препаратов для защиты окружающей среды; это рекультивация почв,
очистка стоков и газовоздушных выбросов, утилизация промышленных отходов и
деградация токсикантов с использованием биологических агентов и биологических
процессов.
Синяя биотехнология в основном ориентирована
на эффективное использование ресурсов Мирового океана. Прежде всего, это
использование морской биоты для получения пищевых, технических, биологически
активных и лекарственных веществ.
3. Основные
методы биотехнологии
В литературе [8] выделяют 3 основных метода биотехнологии:
· Генная инженерия;
· Клеточная инженерия;
· Клонирование.
С помощью методов клеточной и генной инженерии возможно
получение новых высокопродуктивных продуцентов белков и пептидов человека,
антигенов, вирусов и др. Развитие генетической и клеточной инженерии приводит к
тому, что биотехнологическая промышленность все шире завоевывает новые области
производства. Фундаментом для возникновения новейших методов биотехнологии
послужили открытия в генетике, молекулярной биологии, генетической энзимологии,
вирусологии, микробиологии и других дисциплинах [11].
Клеточная инженерия [8] использует методы
(клеточная селекция и соматическая гибридизация) введения культур и клеток и их
практического использования.
Клеточная селекция основана на выращивании клеток (как
растительных, так и животных) вне организма на специально подобранных средах в
регулируемых условиях.
Соматическая гибридизация - это слияние двух различных клеток
в культуре тканей.
Генная инженерия - совокупность методов,
позволяющих осуществить генетическую информацию, перенос (трансгенез)
чужеродных генов из одного организма в другой [8].
По Э.С. Пирузян генетическая инженерия - система
экспериментальных приемов, позволяющих конструировать лабораторным путем (в
пробирке) искусственные генетические структуры в виде так называемых
рекомбинантных или гибридных молекул ДНК.
Цель прикладной генетической инженерии заключается в
конструировании таких рекомбинантных молекул ДНК, которые при внедрении в
генетический аппарат придавали бы организму свойства, полезные для человека.
Например, получение "биологических реакторов" - микроорганизмов,
растений и животных, продуцирующих фармакологически значимые для человека вещества,
создание сортов растений и пород животных с определёнными ценными для человека
признаками. Методы генной инженерии позволяют провести генетическую
паспортизацию, диагностировать генетические заболевания, создавать ДНК-вакцины,
проводить генотерапию различных заболеваний [10].
Технология рекомбинантных ДНК использует следующие методы
[10]:
· специфическое расщепление ДНК
рестрицирующими нуклеазами, ускоряющее выделение и манипуляции с отдельными
генами;
· быстрое секвенирование всех нуклеотидов
очищенном фрагменте ДНК, что позволяет определить границы гена и аминокислотную
последовательность, кодируемую им;
· конструирование
рекомбинантной ДНК;
· гибридизация нуклеиновых кислот,
позволяющая выявлять специфические последовательности РНК или ДНК с большей
точностью и чувствительностью, основанную на их способности связывать
комплементарные последовательности нуклеиновых кислот;
· клонирование ДНК: амплификация in vitro с помощью цепной
полимеразной реакции или введение фрагмента ДНК в бактериальную клетку, которая
после такой трансформации воспроизводит этот фрагмент в миллионах копий;
· введение рекомбинантной ДНК в клетки или
организмы.
Клонирование - получение нескольких генетически
идентичных организмов естественным путем или путем бесполого размножения.
В [3] выделяют другую классификацию методов биотехнологии:
I. Методы, которые используются при
исследовании фундаментальных механизмов функционирования биологических систем. Это современные методы
биохимии, генетики, молекулярной биологии, иммунологии и других биологических
наук. Используя арсенал этих методов, биотехнологи решают такие фундаментальные
задачи как механизмы структурно-функциональной организации продуцентов.
II. Методы, которые позволяют осуществить
реконструкцию биологических объектов, использующихся в биотехнологии (методы
молекулярной биотехнологии). Эти методы, в свою очередь, можно разбить на 2
группы:
1) конструирование векторов и рекомбинантных ДНК, т.е.
молекулярные манипуляции;
) гибридизация клеток, т.е. клеточный уровень.
III. Специфические методы крупномасштабного
(промышленного) культивирования биообъектов, которые позволяют получать целевой
продукт в промышленном объеме. Особенность методов биотехнологии связана с
тем, что все продуценты осуществляются в асептических (стерильных) условиях,
т.е. в условиях, исключающих возможность попадания в среду культивирования
биообъектов болезнетворных (патогенных) и не болезнетворных (сапрофитных)
микроорганизмов.
4.
Нанобиотехнологии
Нанобиотехнология - область нанонауки и наноинженерии,
применяющей методы и подходы нанотехнологии для создания устройств с целью
изучения биологических систем. В рамках нанобиотехнологии также изучаются
возможности использования живых систем для создания наноустройств.
Нанобиотехнология объединяет в себе достижения нанотехнологии
и молекулярной биологии. Молекулярные биологи помогают нанотехнологам научиться
понять и использовать наноструктуры и наномеханизмы, созданные в результате
процесса эволюции, длившегося 4 миллиарда лет, - клеточные структуры и биологические
молекулы. Использование особых свойств биологических молекул и клеточных
процессов помогает биотехнологам в достижении целей, перед которыми бессильны
другие методы.
К практическим применениям нанобиотехнологии относятся:
увеличение скорости и точности диагностики заболеваний;
создание наноструктур для доставки функциональных молекул в
клетки-мишени;
повышение специфичности и скорости доставки лекарств;
миниатюризация биосенсоров путем объединения биологического и
электронного компонентов в один мельчайший прибор;
способствование развитию экологически чистых производственных
процессов и др.
Получены данные о возможности использования наночастиц для
создания нанолекарств, эффективных вакцин. Разработаны новые транспортные
наносистемы (контейнеры) для доставки лекарств в органы-мишени и т.д. Эти
разработки позволяют повысить растворимость, биодоступность, терапевтические
возможности препаратов, снизить дозы и побочные эффекты, значительно уменьшив
лекарственные нагрузки на организм [13].
4.1 Нанобиотехнологии
в медицине
В настоящее время уже появились наноматериалы из которых
делают нанолекарства - препараты нового поколения. Развитие нанотехнологий c применением белковых,
липидных молекул, нуклеиновых кислот или их cинтетических миметиков в
медицине дает возможность создавать новые высокочувствительные и дешевые
системы для ранней диагностики, лечения, а также доставки лекарств к
клеткам-мишеням или органам. В период 1998-2005 годов опубликовано более 200
научных работ, демонстрирующих эффективность применения фуллеренов (фуллере́ны - молекулярные со-единения, представляющие собой выпуклые
замкнутые многогранники, составленные из четного числа трехкоординированных
атомов углерода) при лечении целого ряда заболеваний, включая рак, склероз,
вирусные и бактериальные инфекции (менингит и ВИЧ). Создаются лекарства для
клеток-мишеней и клеточных наноструктур, включая генотерапию, новые
противоопухолевые, кардиотропные и психотропные средства, новые антибиотики,
иммуномодуляторы, аллерготропины и наноантитела для лечения иммунодефицитов,
аллергии, опухолей и аутоиммунных заболеваний. Ученые работают над адресным
преодолением клеточных мембран, различных биологических барьеров для адресной
доставки лекарств. В России ведутся работы и получены положительные результаты,
подтвержденные публикациями и патентами, в области применения фуллеренов и их
модификаций для лечения гриппа, онкологических заболеваний и бактериальных
инфекций (туберкулез).
Одним из способов создания лекарственных средств нового
поколения стало снабжение их системами доставки, обеспечивающими
пролонгированное поступление лекарственных веществ в определенные органы и
клетки-мишени, а также улучшение фармакологических свойств препарата.
Разработанные системы доставки лекарств используются практически во всех
областях медицины. При этом существенное внимание уделяется фосфолипидным
наночастицам - переносчикам лекарственных средств, эффективность действия
которых обеспечивается не только их биологическими свойствами, но и малыми
размерами. Адресная доставка лекарств к больным клеткам позволяет медикаментам
попадать только в больные органы, избегая здоровые, которым эти лекарства могут
нанести вред.
Нановакцины. С помощью нанотехнологий
становятся возможными противоопухолевая защита организма, адресное
стимулирование или подавление его иммунитета. В первую очередь, речь идет о
создании вакцин нового типа против туберкулеза, СПИДа, гепатитов, гриппа и
других новых и возвращающихся социально значимых инфекций. Исследователи
синтезируют белки, способные связываться с вирусами и мутантными генами,
вызывающими опухоли, и обезвреживать их; создают высокоэффективные вакцины и
изучают белки-рецепторы клеточной поверхности, которые часто являются мишенями
для фармацевтических препаратов. Получены данные о возможности использования
наночастиц для производства эффективных вакцин.
Нановакцины имеют следующие преимущества [1]:
· они практически безопасны, поскольку
содержат только вакцинные компоненты;
· они нетоксичны, биосовместимы и
биоразлагаемы в организме;
· самосборка компонентов нановакцины решает
проблему очистки, иммобилизации и концентрирования компонентов, обеспечивает
стандартность получаемого продукта;
· технология нановакцин позволяет получать
многокомпонентные препараты, защищающие одновременно от широкого спектра
социально-значимых или особо опасных заболеваний.
Наноантитела. В 70-х годах прошлого
века в разработке противораковых препаратов наступил переломный момент - были
созданы так называемые моноклональные антитела (МАТ - это антитела, вырабатываемые
иммунными клетками, принадлежащими к одному клеточному клону, т.е.
произошедшими из одной клетки-предшественнищы). За счет того, что эти белковые
молекулы обладают свойствами специфически узнавать определенный антиген или
белок какой-то определенной структуры, они могут существенно более
избирательно, чем традиционные химиопрепараты, воздействовать именно на целевые
клетки злокачественной опухоли, заметно меньше повреждая при этом нормальные
клетки организма. У этой технологии есть свои минусы:
Во-первых, МАТ - молекулы довольно крупные и проникать внутрь
клетки или глубоко в ткани они не способны.
Во-вторых, для достижения необходимого результата их
концентрация должна быть в 5-10 тысяч раз выше, чем концентрация
молекул-мишеней.
В-третьих, МАТ вырабатываются исключительно на клеточных
культурах, что делает их производство недешевым.
Как и обычные антитела, например, те же МАТ, наноантитела
обладают высокой специфичностью и низкой токсичностью, но наряду с этим у них
есть сразу несколько потенциальных преимуществ:
) они имеют гораздо меньший размер (2×4 нанометра) и новые структурные особенности - лучшее проникновение
внутрь ткани и узнавание того, что до сих пор не узнавалось;
) наноантитела намного проще и дешевле производить в больших
количествах;
) наноантитела по сравнению с узнающими доменами традиционных
антител намного лучше растворяются в организме человека и гораздо более
устойчивы к значительным колебаниям температуры и кислотности (рН);
) с наноантителами довольно просто проводить всевозможные ген-но-инженерные
манипуляции (например, создавать более эффективные комбинированные конструкции,
включающие два или несколько наноантител, а также другие белковые домены или
функциональные группы).
Все эти преимущества открывают широкое поле применения наноантител
в качестве основы лекарственных препаратов нового поколения для широкого
спектра заболеваний.
4.2
Нанотрансгенез или трансгенное наноконструирование [13]
Трансгенными могут называться те организмы, в которых успешно
функционирует ген (или гены) пересаженные из других организмов (растений,
животных или микроорганизмов). Осуществляется трансгенез бактерий, вирусов,
происходит создание различных векторных наноконструктов; трансгенез растений,
животных.
Делается это для того, чтобы организм, например, растение
реципиент получило новые удобные для человека свойства, повышенную устойчивость
к вирусам, к гербицидам, к вредителям и болезням растений. Пищевые продукты,
полученные из таких генно-измененных культур, могут иметь улучшенные вкусовые
качества, лучше выглядеть и дольше храниться. Также часто такие растения дают
более богатый и стабильный урожай, чем их природные аналоги. Создание,
например, трансгенных растений в настоящее время развиваются по следующим
направлениям:
· получение сортов с/х культур с более
высокой урожайностью;
· получение с/х культур, дающих несколько
урожаев в год (в России существуют ремантантные сорта клубники, дающие два
урожая за лето);
· создание сортов с/х культур, токсичных для
некоторых видов вредителей (в России ведутся разработки, направленные на
получение сортов картофеля, листья которого являются остро токсичными для
колорадского жука и его личинок);
· создание сортов с/х культур, устойчивых к
неблагоприятным климатическим условиям (например, были получены устойчивые к
засухе трансгенные растения, имеющие в своем геноме ген скорпиона);
· создание сортов растений, способных
синтезировать некоторые белки животного происхождения (например, в Китае
получен сорт табака, синтезирующий лактоферрин человека).
Заключение
Биотехнология стремительно выдвинулась на передовые рубежи
научно-технического прогресса благодаря бурному развитию различных областей
науки, на которые она опирается, что позволяет использовать потенциал живых
организмов в интересах человека. С другой стороны, человечество испытывает
потребность в новых технологиях, способных ликвидировать нехватку
продовольствия, энергетики, минеральных ресурсов, экологическую ситуацию.
Решению этих задач может способствовать развитие новых технологий с
использованием биообъектов - биотехнологий.
Список
использованных источников
1.
Загоскина Н.В. Биотехнология: теория и практика: учеб. пособие для вузов. / М.:
Оникс, 2009.496с., 8с. цв. вкл.: ил.
.
Божков А.И. Биотехнология. Фундаментальные и промышленные аспекты. Харьков:
2005.364 с.
.
Россихин В.В. Биотехнология: введение в науку будущего. Харьков:
"Колорит", 2005.288с.
.
Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. Пер.
с англ. М.: Мир, 2002.589 с.
.
Елинов Н.П. Основы биотехнологии.С. - Пб.: "Наука", 1995.601 с.
.
Ревин В.В. Введение в биотехнологию: от пробирки до биореактора: учеб. пособие.
/ Саранск: Изд-во Мордовского ун-та, 2006.256 с.
.
Тихомирова Л.И. Основы биотехнологии: опорный конспект лекций: учеб. пособие. /
Барнаул: Изд-во Алт. ун-та, 2013.79 с.
.
Шмид Р. Наглядная биотехнология и генетическая инженерия. / Р. Шмид; пер. с
нем.2-е изд. М.: БИНОМ. Лаборатория знаний, 2014.324 с.: ил.
10. http://www.biotechnolog.ru/
. Волова Т.Г.
Биотехнология. Новосибирск: Изд-во СО РАН, 1999.252с.
. Войнов Н.А.,
Волова Т.Г., Зобова Н.В. Современные проблемы и методы биотехнологии: эл. учеб.
пос. / Н.А. Войнов, Т.Г. Волова, Н.В. Зобова и др.; под ред. Т.Г. Воловой.
Красноярск: ИПК СФУ, 2009.418 с.
. Карпунина Л.В.,
Щербаков А.А., Ларионова О.С. Биотехнология (в том числе бионанотехнологии).
Саратов: ФГБОУ ВПО "Саратовский ГАУ", 2014.82 с.