Оценка уровня благополучия гепардов в условиях неволи с помощью неинвазивных методов на протяжении года
Оглавление
Введение
Глава 1. Обзор литературы
.1 Стероидные гормоны как отражение благополучия животного
1.2 Инвазивный и неинвазивный методы оценки гормонального
статуса животного
1.3 Гепард как объект исследования
Глава 2. Материалы и методы исследований
Глава 3. Результаты и обсуждение
Выводы
Список литературы
Введение
гормон гепард глюкокортикоид стероидный
Гепард (Acinonyx jubatus) - один из самых крупных предствителей подсемейства Малые кошки (Felinae) семейства Кошачьи (Felidae). В конце
века численность гепардов составляла около 100 000 особей. До настоящего
времени сохранилось около 7100 гепардов, которые населяют 9% территории от их
исторического ареала. В дикой природе Азии гепарды сохранились только в Иране.
Гепарды включены в категорию «уязвимых» видов Красного списка Международного
союза охраны природы и природных ресурсов (МСОП). Для проведения программ по
сохранению данного вида. требуется выявить, на сколько благополучно состояние
животных при вольерном содержании гепардов. Для этого использовался
неинвазивный метод оценки концентрации метаболитов глюкокортикоидов в
экскрементах животных, потому что не требует непосредственного контакта с
животным.
Цель работы. Оценить
уровень благополучия гепардов в условиях неволи с помощью неинвазивных методов
на протяжении года.
Для достижения цели работы поставлены следующие задачи.
1. Оценить сезонную динамику уровня глюкокортикоидов у гепардов.
2. Сопоставить уровень глюкокортикоидов у самцов и самок в
течение года.
3. Выявить отличия гормонального статуса у отдельных особей
гепардов.
В работе впервые была проанализирована годовая динамика уровня
метаболитов глюкокортикоидов с использованием неинвазивных методов у гепардов
африканских подвидов зоопитомника Московского зоопарка, расположенного под г. Волоколамск
в Московской области.
Данные методы оценки гормонального статуса животных позволяют понять
процессы, протекающие в организме под действие различных факторов.
Представления об уровне стрессированности и гормональное состояние
животных, содержащихся в условиях неволи, имеют большое практическое значение
для оценки благополучия редких видов животных и дальнейшего выбора необходимых
мер для сохранения вида.
Автор выражает глубокую и искреннюю благодарность д.б.н. Жигареву И.А. за
научное руководство при написании работы и д.б.н. Найденко С.В. за неоценимую
помощь в освоении методов, предоставление научной литературы и за возможность
работать с таким редким видом, как гепард.
Глава 1.
Обзор литературы
1.1
Стероидные гормоны как отражение благополучия животного
Стероидные гормоны - производные полициклических спиртов - стеролов, у
которых укорочена (окислена) боковая цепь (Филлипович, 1999). Они синтезируются
из общего субстрата - ацетил-КоА, путем превращения его в холестерол. Синтез
стероидов происходит непосредственно в железах внутренней секреции: в коре
надпочечников, семенниках, яичниках и желтых телах (Филлипович, 1999).
Промежуточным звеном биосинтеза стероидных гормонов из холестерола является
прегненолон, который в семенниках и яичниках превращается в андрогены и
эстрогены соответственно. В синтезе эстрогенов этап образования андрогенов, как
промежуточного звена, обязателен, поэтому у самок всегда присутствуют и мужские
половые гормоны. Половые гормоны играют важную роль в способности выполнения
репродуктивной функции. Они отвечают не только за развитие и функционирование
половой системы, начиная с гонад в онтогенезе, но и обеспечивают нормальное
протекание беременности. Наиболее активные мужские стероидные гормоны
(тестостерон, андростерон и др.) ответственны как за формирование половых
признаков, так и за сперматогенез. Основными женскими гормонами являются
прогестерон и эстрадиол. Благодаря действию эстрадиола происходит формирование
половых признаков и регуляция работы яичников. При наступлении эструса уровень
эстрадиола значительно повышается. Беременность проходит без осложнений
благодаря действию прогестерона, синтезируясь сначала яичниками и желтыми
телами. Во время беременности прогестерон начинает синтезироваться так же
плацентой. Андрогены и эстрогены образуются не только в половых железах, но и в
коре надпочечников, только в меньших количествах.
В коре надпочечников синтезируются такие жизненно важные гормоны, как
глюкокортикоиды. Наиболее активными глюкокортикоидами являются кортизол
(гидрокортизон) и кортикостерон. Они оказывают непосредственное влияние на
углеводный, белковый и жировой обмен в организме. Свое название глюкокортикоиды
получили благодаря их главному метаболическому эффекту - стимуляции
глюконеогенеза в печени (Barcellos et al., 2010). Под действие высокого
уровня кортизола в крови аминокислоты метаболизируются с образованием глюкозы.
Этот процесс рассматривают как катаболический, потому что высвобождение
аминокислот происходит в результате расщепления мышечных белков. Так же
глюкокортикоиды могут подавлять использование глюкозы всеми клетками тела,
повышая образование глюкозы в крови и таким образом противодействуя эффекту
инсулина (Lansang, Hustak, 2011). Так же глюкокортикоиды обладают
антианаболическим действием (снижают синтез мышечных белков) и участвуют в
обмене липидов.
Селье дал определение стрессу, как общему адаптационному синдрому (Селье,
1960). Ключевым звеном являются глюкокортикоидные гормоны. Стресс приводит к
повышению уровня глюкокортикоидов. Это и является эндокринным механизмом,
который защищает организм от стрессовых условий. Однако, не все изменения
концентрации глюкокортикоидов связаны со стрессом. Секреция глюкокортикоидов
находится под контролем гипоталамо-гипофизарно-надпочечниковой системы, а именно
адренокортикотропного гормона (АКТГ), который стимулирует синтез кортизола в
клетках коры надпочечников. Глюкокорикоиды поступают в кровь эпизодически,
подчиняясь циркадному ритму, поскольку секреция АКТГ тоже имеет эпизодический
характер. Этот процесс свободен от внешних факторов. Но циркадные и сезонные
ритмы не
соотносятся с понятием стресса. Так же в различных ситуациях одно и то же
воздействие не всегда вопринимается как стрессор, что говорит о значительном
влиянии ЦНС на развитие стрессовой реакции (Herman, Cullinan, 1997). Таким образом, нельзя определить, стрессировано ли животное,
только по одному уровню глюкокортикоидов. Необходимо знать о всех
воздействующих факторах.
В настоящее время регулярные циркадные и сезонные изменения уровня
глюкокортикоидов рассматривают, как приспособление к постепенным, предсказуемым
изменениям окружающей среды. Стресс, напротив, считают «экстренным»
приспособлением к воздействию сильных стрессоров (неконтролируемых и
непредсказуемых факторов). Благодаря действию стресса организм способен
максимально мобилизовать свои ресурсы, чтобы справиться с возникшей ситуацией.
Но если организм не может адаптироваться к изменениям внешних условий, то
это может привести к различным негативным последствиям: от снижения репродуктивного
успеха, вплоть до истощения и гибели животного. Это является результатом
негативного продолжительного влияния глюкокортикоидов на иммунную и
репродуктивную системы, когнитивные способности организма. Однако, чтобы
избежать таких последствий, существуют специальные механизмы, которые помогают
организму приспосабливаться к влиянию высокого уровня глюкокортикоидов.
Таким образом, повышение уровня глюкокортикоидов в организме -
необходимое условие для адаптации к изменениям окружающей среды и повышенным энергозатратам
организма. По уровню глюкокортикоидов можно определить состояние особи, и
насколько благоприятны данные условия обитания для животного.
В настоящее время оценка благополучия животных по уровню глюкокортикоидов
широко используется при проведении исследований в природе, потому что позволяет
определить конкретные факторы, которые негативно влияют на организм. Во многих
работах доказано, что антропогенные факторы отрицательно влияют на уровень
глюкокортикоидов и благополучие животных в целом, например, близость дорог и
населённых пунктов.
Так же на уровень глюкокортикоидов влияют и биотические факторы. Один из
них - это присутствие хищника. Например, уровень глюкокортикоидов у
европейского кролика (Oryctolagus cuniculus) в
природе напрямую зависит от плотности хищников. Увеличение численности
канадской рыси (Lunx canadensis) влияет на увеличение уровня
глюкокортикоидов у американского зайца-беляка (Lepus americanus). В результате происходит снижение
репродуктивной активности зайца (Sheriff et al., 2009). Но подобная зависимость
прослеживается не всегда. Так, уровень глюкокортикоидов у оленей (Cervus elaphus) в Йелоустоунском национальном парке
не зависит от численности волков (Canis lupus) (Creel et al., 2009). Также уровень глюкокортикоидов может зависеть от
достатка пищевых ресурсов (Роговин и др., 2006).
Важным фактором, влияющим на уровень глюкокортикоидов, является тип
социальной организации вида и социальное поведение особей. Социальный статус
влияет как на базальный уровень глюкокортикоидов, так и на стресс-ответ
организма ( Creel, 2005). Так же увеличение уровня
глюкокортикоидов может свидетельствовать о высокой плотности популяции, что
отрицательно сказывается на половом созревании особей (Novikov, Moshkin,
1998). У кошачьих, которые в основном ведут одиночный образ жизни, повышение
концентрации глюкокортикоидов может происходить при встрече особи своего вида
вне сезона размножения (Павлова, 2010), в результате чего возможно снижение
половой активности.
У видов, размножение которых приурочено к сезонам, во время гона
концентрация глюкокортикоидов может быть как как низкой, так и высокой.
Например, это связано с такими особенностями вида, как длительность
периода размножения. Так как во время беременности у самок повышаются
энергозатраты организма для вынашивания плода, то, соответственно,
увеличивается и концентрация глюкокортикоидов (Hunt et al., 2006).
Изменение погодных условий могут приводить к повышению уровня
глюкокортикоидов, например, низкие температуры, глубокий снег, повышенное атмосферное
давление (Frigerio et al., 2004).
Также благодаря изменениям уровня глюкокортикоидов можно определить, на
сколько благоприятны условия содержания особей в неволе. Например, было
доказано, что у дымчатых леопардов (Neofelis nebulosa), которые содержались в 12 различных
зоопарках и исследовательских центрах США, уровень глюкокортикоидов был
повышенным у животных, содержавшихся рядом с крупными хищниками и на экспозиции
посетителям, а также у животных, содержавшихся в более низких вольерах. Высота
вольера - фактор, связанный с древесным образом жизни этого вида (Wielebnowski et al., 2002). Для многих видов было отмечено отрицательное
воздействие большого количества посетителей и хищников.
В настоящее время широко используется метод оценки благополучия животных
разных видов с помощью изменения уровня глюкокортикоидов, поэтому количество
подобных работ активно растет. Но работы на кошачьих достаточно редки. Это
связано со скрытным образом жизни, что в принципе затрудняет их изучение. Так
же отлов крупных представителей семейства - это достаточно трудоемкая и опасная
задача. К тому же отлов не позволяет достоверно определить уровень
глюкокортикоидов, так как сам по себе является стрессирующим фактором. Поэтому
необходимо тщательно подобрать методику для оценки уровня глюкокортикоидов.
На данный момент в научной сфере не достиги согласия в выявлении единой
концепции, которая могла бы объяснить зависимость организма от
условий среды. Поэтому происходит путаница, при которой одни и те же
явления описываются с использованием разной терминологии.
В данной работе речь пойдет об оценке благополучия животных по уровню
глюкокортикоидов. Показателем благополучия животных является умения организма
приспосабливаться не только к влиянию стрессоров, но и многим другим внешним
условиям (Mcewen, Wingfield, 2003).
1.2
Инвазивный и неинвазивный методы оценки гормонального статуса животного
В настоящее время для изучения уровня гормонов у животных используются
различные методы, которые имеют свои плюсы и минусы.
Инвазивные методы заключаются в сборе крови из вены животного для
последующего измерения концентрации глюкокортикоидов в сыворотке или плазме.
Измерение глюкокортикоидов в крови показывает состояние животного в конкретный
момент времени. Так же сбор крови сам по себе является стрессирующим фактором,
потому что животное необходимо отловить, а иногда и обездвижить. При отлове в
течении нескольких минут происходят значительные изменения уровня
глюкокортикоидов. Поэтому получить базальную концентрацию глюкокортикоидов (концентрация
глюкокортикоидов в течении 3 минут после отлова (Romero et al., 2008)) достаточно трудно. Кроме того, фактор отлова влияет
и на секрецию половых гормонов (Chichinadze, Chichinadze, 2008). На уровень глюкокортикоидов
так же влияют такие факторы, как пол и сезон года (Romero et al., 2008), поэтому полученные данные не всегда будут
достоверны. Таким образом, базальный уровень гормонов нельзя определить путем
отлова животного.
Альтернативный способ измерения уровня глюкокортикоидов заключается в
использовании неинвазивных методов,с помощью которых
гормоны и их метаболиты можно измерять в моче, экскрементах, слюне,
шерсти и перьях (Sheriff
et al., 2011). Разные субстраты дают информацию о различных
периодах активности эндокринной системы. Так уровень метаболитов в экскрементах
показывает усредненное значение за час/сутки, а шерсть и перья - за
неделю/месяц. их даст среднее значение за период от часа до суток, в
зависимости от частоты дефекации у животного; шерсть и перья дадут усреднённую
картину для периода от нескольких недель до нескольких месяцев. При
долгосрочных исследованиях нет необходимости в частом сборе материалов, так как
это не добавит точности результатам. Слюну и шерсть у диких животных сложно
собрать, не влияя на уровень глюкокортикоидов. Однако, пробы мочи можно собрать
не тревожа животное, но это требует специальных условий содержания. В природе
этот процесс сильно затруднён, за исключением отдельных случаев. Для животных с
низкой скоростью метаболизма, которая не позволяет собирать экскременты
регулярно, использование мочи является удобным, например, у амфибий.
При изучении долговременных изменений уровня глюкокортикоидов необходимо
регулярно собирать образцы, не причиняя стресса животным, так как это может
повлиять на достоверность результатов. Из-за того, что кошачьи ведут одиночный
и скрытный образ жизни, это делает отлов затруднительным, или даже невозможным,
если необходимо получить большое количество проб от одного и того же животного.
Использование экскрементов позволяет, не причиняя стресса животным, получить
необходимое количество образцов. Таким образом, наиболее целесообразным, на наш
взгляд, является использование методов оценки гормонального статуса по
концентрации гормонов и их метаболитов в экскрементах животных.
.3 Гепард
как объект исследования
Гепард (Acinonyx jubatus) - один из самых крупных предствителей подсемейства Малые кошки (Felinae). В настоящее время выделяют 5
нынеживущих подвидов: A j. hecki, A j. fearsoni, A.j. jubatus, A.j. soemmerringi,
A.j. venaticus, которые по внешним признакам
незначительно отличаются друг от друга. Acinonyx jubatus venaticus (азиатский подвид гепарда) сейчас
встречается только на территории Ирана. Остальные 4 подвида распространены в
Африке. Гепарды включены в категорию «уязвимых» видов Красного списка
Международного союза охраны природы и природных ресурсов (МСОП). В Конвенции по
международной торговле видами дикой флоры и фауны, находящимися под угрозой
исчезновения (CITES) гепард помещен в Приложение I.
В конце 19 века численность гепардов составляла около 100 000 особей. За
последние пару десятилетий их численность резко уменьшилась из-за сокращения
естественных мест обитания (пустынь и саванн с одиночными деревьями и густой
травой), конфликта с местным населением, конкуренции с более крупными и
агрессивными хищниками (львами, гиенами), высокого уровня браконьерства, так
как сейчас считается очень модным, держать экзотическое животное дома. Особенно
это популярно в странах Ближнего Востока.
На долю антропогенных факторов приходится наибольшее количество известных
смертей гепардов. Главная причина - местное население, которое считает, что
гепарды наносят значительный вред животноводству. Однако иранские власти
налагают высокие штрафы за убийство гепарда, пытаясь сократить количество инцедентов
(Farhadinia et al., 2016).
Исторический ареал гепарда охватывает практически всю Африку, кроме
бассейна реки Конго, и значительную часть Азии до Восточной Индии. Но за
последние сто лет ареал гепардов значительно сократился. По
последним данным 2016 года численность гепардов составляет не более 7100
особей, которые населяют 9% территории от их исторического ареала (рис.1) (Durant, 2016). Причем гепарды чрезвычайно
быстро исчезли из дикой природы Азии, за исключением Ирана, где обитают около
60 особей. Наибольшей численности гепарды достигают в Южной Африке (Намибия,
Ботсвана) и Западной Африке (Кения, Танзания).
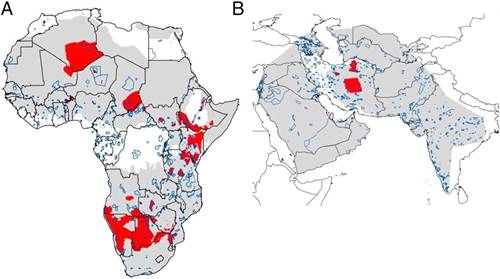
Рисунок 1. Распространение гепарда в Африке (А) и Азии (В). Серым цветом
обозначен исторический ареал, красным - современный. Синим цветов обозначены
границы ООПТ по категориям I-IV МСОП (Durant, 2016).
Было выявлено, что около 33% особей обитают на территории ООПТ, где
находятся под защитой, а остальные особи населяют неохраняемые районы. Так же
прирост численности гепардов на охраняемых территориях на 10% выше, чем за их
пределами (Durant, 2016).Но миграции гепардов
ослабляют их защиту и значительно усиливают их уязвимость. Сейчас широко
применяется метод фотоловушки и ошейники для того, что отследить перемещения
гепардов и их точное количество.
За последние 10 лет из Африки было вывезено около 1200 котят, из которых
около 85% погибли при транспортировке. До сих пор известны случаи незаконного
отлова и продажи детенышей гепардов. Этой проблемой занялся секретариат Cites. В 2016 году на конференции было
решено, что просвещение населения, использование соцсетей и тесное
сотрудничество стран, где обитает гепард, являются важными методами для
сохранения этого вида.
Одним из наиболее важных показателей благополучия животного является его
успешное размножение (Wielebnowski, 2003). Так как в природе отмечена высокая смертность молодняка из-за
пресса других хищников. Поэтому требуется их изучение и разведение в неволе,
чтобы в дальнейшем сохранить природные популяции. При этом необходимо учитывать
особенности поведения гепардов и их местообитания, чтобы максимально точно
смоделировать параметры естественной среды (Челышева, 2006).
Было доказано, что благополучие кошачьих в неволе напрямую зависит от
взаимоотношений с киперами, но не всегда эта зависимость отрицательная, так как
не все животные агрессивно реагируют на присутствие сотрудника (Непринцева,
2004). Так же необходимо учитывать особенности кормления.
На благополучие гепардов так же влияет и организация пространства
вольеров. Так как гепарды приспособлены к быстрому бегу, им необходима
территория, на которой возможно активно «охотиться» и оставлять метки. Гепарды
предпочитают возвышенные участки для обзора окрестностей (Eaton, 1971). Оптимальный размер вольера для
одной особи должен быть не менее 0,5 га и иметь предпочтительно вытянутую форму
согласно Фонду по сохранению гепарда в Намибии (Cheetah Conservation Fund, CCF).
Так как гепарды в основном ведут одиночный образ жизни, необходимо
обеспечить комфортные условия для их существования.
Некоторыми исследователями было показано, что социальные факторы являются
более важными, чем пространственные для обеспечения животным психологически
комфортных условий существования в неволе. Совместное содержание особей, особенно
самцов, является стрессирующим фактором, который может приводить к гормональным
нарушениям и снижению репродуктивной функции (Terio, Munson,
2000). Таким образом, обеспечение благоприятного содержания гепардов в неволе
достаточно сложный и требующий внимания процесс.
Течка у самок гепардов впервые наступает в возрасте 16 месяцев.
Беременность длится в среднем около 95 дней, средний размер помета составляет
4-5 детенышей. Самцы не принимают участия в воспитании котят. Было обнаружено,
что генетическое разнообразие диких популяций гепардов в Намибии значительно
сокращается с конца 1970-х годов, особенно у самцов. Возможно, это связано с
чрезвычайно высоким процентом морфологически аномальных сперматозоидов в
эякуляте, однако зависимости между инбридингом и качеством спермы самцов не
обнаружена (Terrell et al., 2016). Таким образом, генетические факторы сами по себе
вряд ли будут причиной плохой рождаемости в неволе. Скорее, главной причиной
могут быть проблемы социального поведения (Caro, 1993) В настоящее время, очень важно сохранение
генетического разнообразия в популяциях гепарда.
В настоящее время опубликовано достаточное количество работ, связанных с
изучением гормонального статуса гепардов в неволе (Wells et al. 2004). Метод оценки концентрации глюкокортикоидов в
экскрементах является достаточно удобным для выявления благополучия гепардов,
потому что не требует непосредственного контакта с животными.
Глава 2.
Материалы и методы исследований
Исследования по изучению гормонального статуса гепардов, содержащихся в
зоопитомнике Московского зоопарка, расположенного под г. Волоколамск в
Московской области, проводили в период с октября 2014 года по октябрь 2015 года
в условиях вольерного содержания животных.
Экстракцию образцов проводили в лаборатории ИПЭЭ РАН по описанной ранее
методике (Jewgenow et al., 2006; Павлова, Найденко, 2008). От каждого образца
экскрементов отбирали навеску 0.1 г. в пробирку Эппендорфа, добавляли 0.1г
трехвалентного оксида алюминия и 0.9 мл 90% метанола для начала экстракции.
Пробирки встряхивали в течение 30 минут с помощью перемешивающего устройства
«Экрос». После этого пробирки центрифугировали на протяжении 10 минут со
скоростью 4000 об/минуту, затем 400 мкл супернатанта отбирали в новую пробирку
и разводили равным объёмом дистиллированной воды. Полученный экстракт хранили
при температуре -18°С до проведения анализа. Так же навески экскрементов массой
0,5-1 г взвешивали с точностью до сотых на весах Ohaus (Scout Pro, Ohaus Corporation, США), после этого высушивали при
температуре 80°С до достижения постоянной массы. Благодаря этому рассчитывали
влажность каждого образца и пересчитывали концентрацию метаболитов кортизола на
1 г сухих экскрементов.
Концентрацию метаболитов глюкокортикоидов в экскрементах измеряли методом
гетерогенного иммуноферментного анализа с использованием наборов компании
«Иммунотех» (Москва, Россия). Измерения концентрации метаболитов
глюкокортикоидов проводились с помощью планшетного спектрофотометра Multiskan EX (Thermo Electron Corporation, США). Данная методика измерения
концентрации метаболитов глюкокортикоидов была валидирована в лаборатории ИПЭЭ
РАН для амурского тигра (Найденко и др., 2011) и дальневосточного леопарда
(Иванов и др., 2014), а с использованием немецких коллег - и для гепарда (Ludwig et al, 2013). Статистическую обработку данных проводили с помощью
программы Statistica 10 (StatSoft, США).
Глава 3.
Результаты и обсуждение
Динамика среднемесячных показателей уровня глюкокортикоидов имеет
определенную специфику. На графике (рис.2) заметно непостоянство уровня
гормонов у пяти исследованных гепардов в течение года с октября 2014 по октябрь
2015. Размах колебаний среднемесячного показателя составляет более чем
двукратные отличия. Наиболее выражено увеличение уровня глюкокортикоидов в
апреле, когда средняя концентрация метаболитов составила максимальную величину
- 4481 нг/г. Минимальное значение концентрации метаболитов глюкокортокоидов
наблюдалось в октябре 2014 года (2046,4 нг/г).
Рисунок 2. Изменения средней концентрации метаболитов глюкокортикоидов в
экскрементах гепардов с октября 2015 по октябрь 2016 (отрезком обозначена
ошибка средней, при p=0,05)
Так же снижение уровня глюкокортикоидов происходит в феврале и мае.
Средняя концентрация исследуемых метаболитов у пяти гепардов за год составила
2754,58 нг/г. Пики среднемесячной концентрации глюкокортикоидов в течение года
выявлены в декабре (3391,2 нг/г), апреле (4481 нг/г) и июле (3913,6 нг/г).
Кроме существенных подъемов уровня глюкокортикоидов в декабре, апреле и
июле так же прослеживаются и значительные колебания на протяжении всего года
(рис.3).

Рисунок 3. Изменение уровня концентрации метаболитов глюкокортикоидов в
экскрементах гепардов в процентах от средней с октября 2014 по октябрь 2015. На
оси абсцисс: дата; на оси ординат: уровень метаболитов глюкокортикоидов в
процентах от средней; отрезком обозначена ошибка средней, при p=0,05.
Наибольшее увеличение концентрации метаболитов глюкокортикоидов
происходит в апреле и июле, тогда как с января по февраль они относительно
невысокие. Это свидетельствует о том, что температура окружающей среды не
влияет на уровень глюкокортикоидов.
Для понимания зависимости средних показателей от сезона года мы решили
исследовать эти показатели у самцов и самок отдельно. Выяснилось, что
совпадение пиков происходит только в теплое время года - в апреле и июле. В
декабре у самцов, в отличие от самок, пика нет. Так, у самцов концентрация
метаболитов глюкокортикоидов приходится на апрель (4212,9 нг/г) и июль (3062,1
нг/г). У самок отмечается 3 пика: в декабре (5647,2 нг/г), апреле (4883,2 нг/г)
и июле (3062,1 нг/г). В декабре у самцов прослеживается незначительное
повышение уровня метаболитов глюкокортикоидов (1887,1 нг/г). Кроме этого,
средняя концентрация исследуемых метаболитов у самцов в течение года
существенно ниже, чем у самок (рис. 4). Таким образом, при объединении данных
по самцам и самкам пик концентраций в декабре обусловлен исключительно данными
самок.
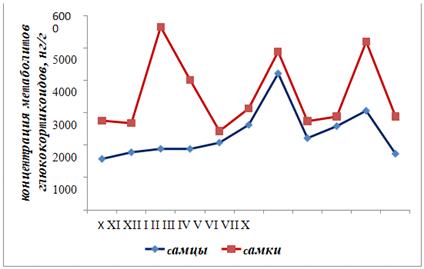
Рисунок 4. Изменения среднемесячной концентрации метаболитов
глюкокортикоидов в экскрементах у самцов и самок с октября 2014 по октябрь 2015
С помощью дисперсионного анализа выявлено, что фактор пола оказывает
достоверное влияние на уровень метаболитов
глюкокортикоидо (DF=1, F=12.34, p=0,01). Интересно, что у самок и самцов апрельский и июльский
пики совпадают. Фактор месяца достоверно влияет на концентрацию
глюкокортикоидов (DF=11, F=2.26, p=0,032). Значит небольшой подъем уровня исследуемых
метаболитов у самцов в декабре оказывает существенное влияние. Совместное
влияние этих двух факторов (пол и месяц) является недостоверным (DF=11, F=1, p=0,46).
Это объясняется значительно различающейся концентрацией метаболитов
глюкокортикоидов у самцов и самок в течение большей части года. Таким образом,
пики концентраций глюкокортикоидов не связаны с сезонными изменениями, в том
числе, как было сказано ранее, и с температурой.
Интересно посмотреть и сравнить индивидуальную динамику изучаемых
метаболитов у гепардов. В работе было задействовано 5 гепардов африканских
подвидов: 3 самца (Кай, Кими, Сева) и 2 самки (Ева и Синди). Сева привезен из
европейского зоопарка, а Кай и Кими - из африканского. Ева и Синди являются
сестрами.
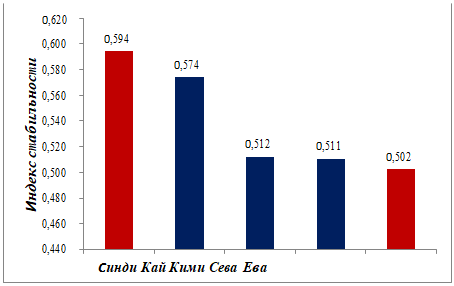
Рисунок 5. Индекс стабильности (IS) динамики уровня метаболитов глюкокортикоидов в течение года у пяти
особей гепардов. Если IS =
0, то динамика уровня метаболитов глюкокортикоидов нестабильна, если IS = 1, то стабильна.
Характер и размах колебаний концентраций метаболитов глюкокортикоидов у
отдельных особей показывают уровень их стабильности (Жигарев, 2005). Для этого
использовали индекс стабильности (IS). Если IS = 0, то динамика уровня метаболитов
глюкокортикоидов абсолютно нестабильна, если IS = 1, то стабильна. Из пяти гепардов динамика исследуемых
метаболитов наиболее стабильна у Синди ( IS = 0,594) (рис.5). Так же достаточно высокой стабильностью
обладает Кай ( IS = 0,574). Для
остальных 3 гепардов ( Кими, Сева, Ева) характерна нестабильная динамика уровня
глюкокортикоидов. Кроме того, самая нестабильная динамика выявлена у Евы ( IS = 0,502).
У Синди отмечена самая высокая концентрации метаболитов глюкокортикоидов,
по сравнению с другими гепардами, которая приходится на декабрь (15,6102 мг/г)
(рис.6). Так же увеличение уровня исследуемых метаболитов происходит в апреле
(8,2695 мг/г), мае (8,8585 мг/г) и июне (7,6855). Кроме того, среднее значение
концентрации глюкокортикоидов равно 3,5420 мг/г из-за низких показателей в
течение года.
Рисунок 6. Изменения концентрации метаболитов глюкокортикоидов в
экскрементах Синди в течение года (октябрь 2014 - октябрь 2015)
В мае уровень исследуемых метаболитов у Синди достигал минимального
значения - 1,1191 мг/г. Несмотря на огромную разницу между максимальной и
минимальной концентрациями глюкокортикоидов, Синди имеет самую стабильную
динамику исследуемых метаболитов ( IS = 0,594) (рис.5).
У Кая пик концентрации метаболитов глюкокортикоидов приходится на конец
июля (9,9230 мг/г) (рис.7). Колебания уровня глюкокортикоидов в течение всего
года прослеживаются в более низких концентрациях. Поэтому средняя концентрация
исследуемых метаболитов равна 1,9855 мг/г. Динамика исследуемых метаболитов у
Кая имеет достаточно высокую стабильность ( IS =0,574) (рис.5).
Рисунок 7. Изменения концентрации метаболитов глюкокортикоидов в
экскрементах Кая в течение года (октябрь 2014 - октябрь 2015)
У Кими выявлены 3 пика уровня метаболитов глюкокортикоидов (рис.8).
Наибольшую концентрацию исследуемых метаболитов наблюдаем в апреле (12,7374
мг/г). Менее выраженные пики отмечены в июле (8,0209 мг/г) и сентябре (6,8132
мг/г). В остальные месяцы так же прослеживаются значительные колебания уровня
исследуемых метаболитов. В отличие от Синди и Кая динамика уровня метаболитов
глюкокортикоидов у Кими имеет более низкую стабильность ( IS =0,512) (рис.5).
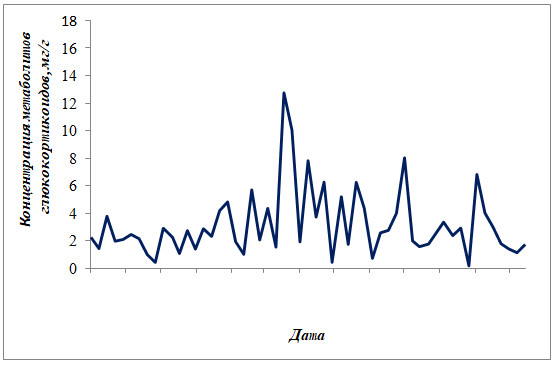
Рисунок 8. Изменения концентрации метаболитов глюкокортикоидов в
экскрементах Кими в течение года (октябрь 2014 - октябрь 2015)
У Севы уровень колебаний концентрации метаболитов глюкокортикоидов более
низкий, чем у других гепардов (Рис.9). Установлены 3 больших пика концентрации
исследуемых метаболитов: в декабре (4,635 мг/г), июне (4,958 мг/г) и июле
(5,7652 мг/г). В остальные месяцы прослеживаются пики и спады метаболитов
глюкокортикоидов в еще меньших концентрациях. Тем не менее, динамика уровня
исследуемых метаболитов у Севы, как и у Кими, достаточно низкая ( IS =0,511) .
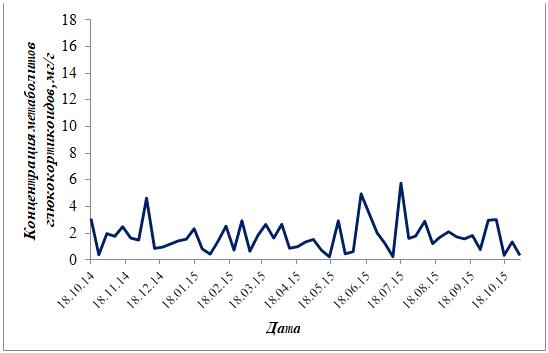
Рисунок 9. Изменения концентрации метаболитов глюкокортикоидов в
экскрементах Севы в течение года (октябрь 2014 - октябрь 2015)
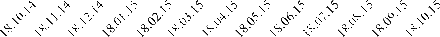
Рисунок 10. Изменения концентрации метаболитов глюкокортикоидов в
экскрементах Евы в течение года (октябрь 2014 - октябрь 2015)
У Евы прослеживаются значительные колебания концентрации метаболитов
глюкокортикоидов между максимальными и минимальными значениями (max=14,1291 мг/г, min=0,1680 мг/г) (рис.10). Максимальная
концентрация уровня метаболитов глюкокортикоидов приходится на июль. Еще два
пика выявлены в конце декабря (10,7828 мг/г) и апреле (10,0181 мг/г). В
сравнении с другими особями гепардов Ева имела самую нестабильную динамику
уровня метаболитов глюкокортикоидов (рис.5).
Выявлена достоверность различий концентраций метаболитов глюкокортикоидов
между особями (табл.1). Значения уровня концентрации метаболитов
глюкокортикоидов достоверно различаются у Евы и Кая (критерий Манна-Уитни: U=1029; Z=3,25; n1=57;
n2=56; p=0,0011), у Евы и Севы (критерий Манна-Уитни: U=864; Z=3,86; n1=57;
n2=53; p=0,0001), у Кая и Кими (критерий Манна-Уитни: U=974; Z=3,21; n1=56;
n2=54; p=0,0013), у Кая и Синди (критерий Манна-Уитни: U=664; Z=5,16; n1=56;
n2=55; p=0,0000), у Кими и Севы (критерий Манна-Уитни: U=839; Z=3,69; n1=54;
n2=53; p=0,0002), у Севы и Синди (критерий Манна-Уитни: U=548; Z=5,59; n1=53;
n2=55; p=0,0000). Различия концентрации метаболитов глюкокортикоидов
недостоверны у Евы и Кими (критерий Манна-Уитни: U=1537; Z=0,0088;
n1=57; n2=54; p=0,99),
у Евы и Синди (критерий Манна- Уитни: U=1295; Z=1,58; n1=57; n2=55;
p=0,11), у Кая и Севы (критерий
Манна-Уитни: U=1339; Z=0,88; n1=56;
n2=53; p=0,38), у Кими и Синди (критерий Манна-Уитни: U=1242; Z=1,47; n1=54;
n2=55; p=0,14).
Таблица 1. Достоверность различий концентраций метаболитов
глюкокортикоидов у гепардов («+» - достоверно, «-» - недостоверно)
|
Синди
|
Кай
|
Кими
|
Сева
|
Ева
|
|
Синди
|
|
+
|
-
|
+
|
-
|
|
Кай
|
|
|
+
|
-
|
+
|
|
Кими
|
|
|
|
+
|
-
|
|
Сева
|
|
|
|
|
+
|
|
Ева
|
|
|
|
|
|
Средняя концентрация метаболитов глюкокортикоидов у Синди составила
3,5420 мг/г, у Евы - 3,3248 мг/г, у Кими - 3,1752 мг/г, у Кая - 1,9855 мг/г, у
Севы - 1,7451 мг/г (Рис. 11). У Синди и Евы уровень метаболитов
глюкокортикоидов выше, чем у других гепардов. Это подтверждает их родство. Но
Синди отличается очень большим разбросом значений. Это демонстрирует достаточно
чувствительную реакцию на разные факторы. Наибольшая средняя концентрация
метаболитов глюкокортикоидов у самцов выявлена у Кими. Хотя у Кая и Севы
отмечаются меньшие значения концентрации уровня глюкокортикоидов. Это не
подтверждает общее африканское происхождение Кая и Кими, так как показатели
концентрации метаболитов глюкокортикоидов различаются. Таким образом, выявлены
достоверные индивидуальные различия в уровне метеболитов глюкокортикоидов.
Рисунок 11. Средняя концентрация метаболитов глюкокортикоидов у отдельных
особей гепардов за год (октябрь 2014 - октябрь 2015). Отрезком обозначена ошибка средней.
Выводы
1. Выраженной сезонной динамики уровня глюкокортикоидов у гепардов,
содержащихся в условиях вольерного содержания в течение года не выявлено.
Отмечены общие пики концентрации метаболитов глюкокортикоидов в апреле и июле,
при этом не выявлено реакций гипоталамо-гипофизарно-надпочечниковой системы на
низкие температуры воздуха.
2. Средний уровень глюкокортикоидов в течение года у самок
исследуемых гепардов выше, чем у самцов. Повышенный уровень глюкокортикоидов у
самок отмечен в декабре, апреле и июле, тогда как у самцов лишь в апреле и в
июле.
3. Выявлены достоверные индивидуальные различия в уровне
глюкокортикоидов у пяти гепардов. Эти различия могут быть связаны с
генетическими особенностями животных и наследственно детерминированы реакцией
гипоталамо-гипофизарно-надпочечниковой системы.
Список
литературы
1. Жигарев И.А. 2005. Оценка стабильности численности
популяций мелких млекопитающих // Доклады академии наук 6: 843-846.
3. Найденко С.В., Иванов Е.А., Лукаревский В.С., Эрнандес
Бланко Х.А., Сорокин П.А., Литвинов М.Н., Котляр А.К., Рожнов В.В. 2011.
Активность системы гипоталамус-гипофиз-надпочечники у амурских тигров (Panthera tigris altaica) в неволе и в природе и ее изменение в течение года
// Известия РАН Сер биология 3: 358 - 363.
4. Непринцева Е.С. 2004. Служители зоопарка, как
средообразующий фактор для приматов // Вопросы прикладной приматологии. М: 47-63.
5. Павлова Е.В. 2010. Взаимосвязь социального поведения и
гормонального статуса у дальневосточного лесного кота (Prionailurus bengalensis euptilura) // Дис Канд Биол Наук М: ИПЭЭ РАН:
164 с.
6. Павлова Е.В., Найденко С.В. 2008. Неинвазивный
мониторинг глюкокортикоидов в экскрементах дальневосточного лесного кота (Prionailurus bengalensis euptilura) // Зоологический журнал: 1375-1381.
7. Роговин К.А., Тупикин А.А., Рандалл Д.А., Колосова
И.Е., Мошкин М.П. 2006. Многолетняя динамика уровня кортикостерона и его
корреляты у самцов большой песчанки (Rhombomys opimus licht.) в природе.
Неинвазивные
методы в исследованиях стресса // Журнал общей биологии 67: 37-52.
8. Селье Г. 1960. Очерки об адаптационном синдроме //. М: Медгиз, 253 с.
9. Филлипович Ю.Б. 1999. Основы биохимии: Учебник для
химических и биологических специальностей педагогических университетовтов и
институтов. //. 4-е издание, переработанное и дополненное ed, М: Агар, 516.
10. Челышева Е.В. 2006. Особенности социального поведения
гепарда (Acinonyx jubatus) в природе и в неволе: к вопросу об оптимизации
условий содержания // Хищные и морские млекопитающие в искусственной среде
обитания. М:
32-62.
11. Barcellos
L.J.G., Marqueze A., Trapp M., Quevedo R.M., Ferreira D. 2010. The effects of
fasting on cortisol, blood glucose and liver and muscle glycogen in adult
jundiá Rhamdia quelen // Aquaculture 300: 231-236.
12. Caro T.M. 1993. Behavioral solutions
to breeding cheetahs in captivity: insights from the wild // Zoo Biology 12: 19
- 30.
13. Chichinadze K., Chichinadze N. 2008.
Stress-induced increase of testosterone: contributions of social status and
sympathetic reactivity // Physiology & behavior 94: 595-603.
14. Creel S. 2005. Dominance, Aggression,
and Glucocorticoid Levels in Social Carnivores // Journal of Mammalogy 86:
255-264.
15. Creel S., Winnie J.A., Christianson
D. 2009. Glucocorticoid stress hormones and the effect of predation risk on elk
reproduction // Proceedings of the National Academy of Sciences 106: 12388-12393.
16. Durant S.M. 2016. The global decline
of cheetah Acinonyx jubatus and what it means for conservation // PNAS 3:
528-533.
17. Eaton R.L. 1971. The World’s Cats
//Ecology and Conservation. Vol.1:239-263.
18. Farhadinia M.S, Akbari H., Eslami M.,
Adibi M.A., 2016. A review of ecology and conservation status of Asiatic
cheetah in Iran. Cat News 10: 18- 26
19. Frigerio
D., Dittami J., Möstl E., Kotrschal K. 2004. Excreted corticosterone
metabolites co-vary with ambient temperature and air pressure in male
Greylag geese (Anser anser) // General and
comparative endocrinology 137: 29-36.
20. Herman J.P., Cullinan W.E. 1997.
Neurocircuitry of stress: central control of the
hypothalamo-pituitary-adrenocortical axis // Trends in Neurosciences 20: 78-84.
21. Hunt K.E., Rolland R.M., Kraus S.D.,
Wasser S.K. 2006. Analysis of fecal glucocorticoids in the North Atlantic right
whale (Eubalaena glacialis) // General and comparative endocrinology 148:
260-272.
22. Jewgenow K., Naidenko S.V., Goeritz
F., Vargas A., Dehnhard M. 2006. Monitoring testicular activity of male
Eurasian (Lynx lynx) and Iberian (Lynx pardinus) lynx by fecal testosterone
metabolite measurement // General and comparative endocrinology 149: 151-158.
23. Lansang M.C., Hustak L.K. 2011.
Glucocorticoid-induced diabetes and adrenal suppression: How to detect and
manage them // Cleveland Clinic Journal of Medicine 78: 748-756.
24. Ludwig C., Wachter B., Silinski-Mehr
S., Ganswindt A., Bertschinger H., Hofer H., Dehnhard M. 2013. Characterisation
and validation of an enzyme- immunoassay for the non-invasive assessment of
faecal glucocorticoid metabolites in cheetahs (Acinonyx jubatus) // General and
comparative endocrinology 180: 15-23.
25. Ludwig C., Wachter B., Silinski-Mehr
S., Ganswindt A., Bertschinger H., Hofer H., Dehnhard M. 2013. Characterisation
and validation of an enzyme- immunoassay for the non-invasive assessment of
faecal glucocorticoid metabolites in cheetahs (Acinonyx jubatus) // General and
Comparative Endocrinology 180: 15-23.
26. Mccarty R. 2007. Fight-or-Flight
Response. // Editor-in-Chief: george Finkassociate Editors:Bruce, M., Kloet,
E.R.D., Robert, R., George, C., Andrew, S., Noel, R., Ian, C., Giora
Feuersteina2 - Editor-in-Chief: george Finkassociate Editors:Bruce Mcewen,
E.R.D.K.R.R.G.C.a.S.N.R.I.C.G.F.
(Eds.) Encyclopedia of Stress (Second Edition), New
York: Academic Press: 62-64.
27. Novikov E., Moshkin M. 1998. Sexual
maturation, adrenocortical function and population density of red-backed vole,
Clethrionomys rutilus (Pall.) // Mammalia 62: 482-631.
28. Palme
R., Rettenbacher S., Touma C., El-Bahr S.M., Möstl E. 2005. Stress
hormones in
mammals and birds: comparative aspects regarding metabolism, excretion, and
noninvasive measurement in fecal samples // Annals of the New York Academy of
Sciences 1040: 162-171.
29. Romero L.M., Meister C.J., Cyr N.E.,
Kenagy G.J., Wingfield J.C. 2008. Seasonal glucocorticoid responses to capture
in wild free-living mammals // American Journal of Physiology - Regulatory,
Integrative and Comparative Physiology 294: 614-622.
30. Sheriff M.J., Dantzer B., Delehanty
B., Palme R., Boonstra R. 2011. Measuring stress in wildlife: techniques for
quantifying glucocorticoids // Oecologia 166: 869-887.
31. Sheriff M.J., Krebs C.J., Boonstra R.
2009. The sensitive hare: sublethal effects of predator stress on reproduction
in snowshoe hares // The Journal of animal ecology 78: 1249-1258.
32. Shutt K., Setchell J.M., Heistermann
M. 2012. Non-invasive monitoring of physiological stress in the Western lowland
gorilla (Gorilla gorilla gorilla): Validation of a fecal glucocorticoid assay
and methods for practical application in the field // General and comparative
endocrinology 179:167-177.
33. Terio K.S., Munson L. 2000. Gastritis
in cheetahs and relatedness to adrenal function. In: Pukazhenthi B, Wildt D,
Mellen J, eds. Felid taxon advisory group action plan. Report. Columbia, SC:
American Zoo and Aquarium Association: 35-36.
34. Terrell K.A., Crosier A.E., Wildt D.E.,
O'Brien S.J., Anthony N,M., Marker L., Johnson W.E. 2016.Continued decline in
genetic diversity among wild cheetahs (Acinonyx jubatus) without further loss
of semen quality // Biological Conservation 200: 192-199.
35. Wells, A; KA Terio; MH Ziccardi; L
Munson. 2004.The stress response to environmental change in captive cheetahs
(Acinonyx Jubatus) // Journal of Zoo and Wildlife Medicine 35(1): 8-14.
36. Wielebnowski N. 2003. Stress and
distress: evaluating their impact for the well-being of zoo animals.
//JAVMA,Vol. 223: 973-977.
37. Wielebnowski N.C., Fletchall N.,
Carlstead K., Busso J.M., Brown J.L. 2002. Noninvasive assessment of adrenal
activity associated with husbandry and behavioral factors in the North American
clouded leopard population // Zoo Biology 21: 77-98.