Оксидативний стрес
ДЕРЖАВНИЙ ВИЩИЙ НАВЧАЛЬНИЙ ЗАКЛАД
"ЗАПОРІЗЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ" МІНІСТЕРСТВО ОСВІТИ І НАУКИ
УКРАЇНИ
Оксидативний стрес
Запоріжжя 2015 р.
Содержание
Оксидативний стрес
Механізм дії природних, синтетичних антиоксидантів і ліків
Окиснення ліпідів, білків і вуглеводів
Шляхи подолання оксидативного стресу
Список літератури
Оксидативний
стрес
Стрес - це природний фізіологічний стан,
необхідний для нормальної життєдіяльності людини, що виникає в процесі
реалізації її бажань і потреб, а також під впливом зовнішніх факторів
природного і соціального середовища. Стрес супроводжує людину все життя. На
фізіологічному рівні розрізняють евстрес, тобто нормальний, помірний, і дистрес
- такий, що виходить за межі адаптації, порушує гомеостаз і може стати причиною
захворювань. На відміну від тварин для людини головне джерело стресів - не
фізичні фактори середовища, а психосоціальні конфлікти [1].
Канадський учений Ганс Сельє (Hans Selye) свого
часу звернув увагу на стереотипність відповіді організму на стресові стимули
незалежно від їхньої природи (фізичне напруження, негативні емоції, радіація,
інтоксикація тощо). Головну роль при цьому відіграє нейрогормональна система
організму.
Основних стрес-реалізуючих систем дві:
симпато-адреномедулярна і гіпоталамо-гіпофізо-кортикоадреналова (ГГКАС). Перша
є системою аварійної відповіді, як її назвав американський учений Уолтер Кенон
(Walter Cannon). Основною ознакою її є викид у кров адреналіну з мозкової
речовини надниркових залоз. Одразу після цього активується ГГКАС, що при
зводить до посилення в корі надниркових залоз секреції кортизолу -
глюкокортикоїдного гормону. Він здійснює головну захисну функцію і підвищує
неспецифічну резистентність організму, тобто здатність виявляти опір
різноманітним хвороботворним чинникам [1, 2].
Початковою ланкою реакції ГГКАС на стресогенні
фактори є особлива ділянка головного мозку - гіпоталамус. Він синтезує і
вивільнює кортиколіберин - пептид, який надходить із кровотоком венозної
портальної системи гіпофіза до його передньої частки (аденогіпофіза) і посилює
там утворення і вивільнення у кров адренокортикотропного гормону (АКТГ) -
стимулятора секреції кортизолу. Секрецію АКТГ посилює також гіпоталамічний
олігопептид вазопресин. Він надходить по довгих аксонах до задньої частки
гіпофіза, де й депонується. Переносниками вазопресину по аксону є спеціальні
білки - нейрофізини. Під час стресової активації ГГКАС вазопресин проникає
короткими судинами до аденогіпофіза і стимулює вивільнення АКТГ.
Поряд із стрес-реалізуючими існують стрес -
лімітуючі системи, які обмежують надмірні прояви стресу, що можуть посилити
його негативні наслідки. Гормональні та інші реакції стресу здатні обмежувати
аміномасляна кислота (головний гальмівний нейромедіатор мозку), гормон
шишкоподібного тіла мелатонін, пептид сну тощо [1, 2].
Невід’ємним супутником дистресу є зсув
редокс-рівноваги в організмі в бік вільнорадикального окиснення і утворення
пероксидів ліпідів, що в сучасній науці дістало назву "оксидативний
стрес" [3, 4]. У біологічних системах найактивнішими є вільні радикали та
іон - радикали, що містять неспарені електрони в атомах O, N, S чи Сl і
утворюють так звані активні форми кисню (АФК), азоту (АФА), сірки (АФС) і хлору
(АФХ).
З одного боку, кисень абсолютно необхідний для
дихання і процесів окиснення вуглеводів, білків і жирів, що супроводжується
вивільненням великої кількості енергії, потрібної для нормального
функціонування організму; з іншого - активні форми кисню викликають деструкцію
клітинних структур, загибель мембран і органел. Утворенню радикалів сприяють
куріння, пестициди, озон, токсичні відходи тощо.
Активні форми азоту утворюються при взаємодії NO
з АФК, найбільш реакційноздатним і небезпечним з них є пероксинітрит ONOO-.
Активні форми сірки утворюються при дії АФК на тіольні сполуки. Вони містять
дисульфід-S - оксиди, сульфенові кислоти, тіольні радикали, які модулюють
редокс-статус біологічних тіолів і дисульфідів. АФХ включають гіпохлоритну
кислоту, нітрил гіпохлорит, атомарний хлор.
Найзагальніша і найдавніша реакція клітини на
стресові події - це посилення продукуван - ня енергії електрон-транспортними
системами мітохондрій і мікросом (ендоплазматичного ретикулуму) зі збільшенням
споживання кисню. Внаслідок бурхливого посилення окисних реакцій утворюється
велика кількість АФК. Вони виникають і в разі прямого пошкодження клітинних
мембран і стінок. Активація вільнорадикального окиснення і ліпідної
пероксидації є незмінним і обов’язковим компонентом клітинної відповіді на дію
стресорів. Мабуть, це і є та загальна ланка механізму індукції стресу, в якій
поєднуються ефекти різних стресогенних чинників. У відповідь зростає активність
системи антиоксидативного захисту.
Надлишок активних форм кисню порушує транспорт
електронів і знижує вироблення енергії, утворення макроергів. Це спричинює
різке обмеження і пригнічення всіх процесів у клітині, які потребують енергії:
синтезу ДНК, РНК і білків, поділу клітин, роботи іонних каналів і насосів,
обміну речовин (рис.1). Ступінь пригнічення продукування енергії має вирішальне
значення для виживання або загибелі клітин при тяжких і тривалих стресах. З
іншого боку, АФК, АФА, АФС, АФХ є необхідними посередниками багатьох процесів
нормального функціонування клітин [5, 6]. Так, перекисне окиснення ліпідів
важливе для біосинтезу простагландинів, лейкотрієнів, інших біологічно активних
речовин тощо.
Усі джерела активних форм кисню потребують
антиоксидантного обмеження.
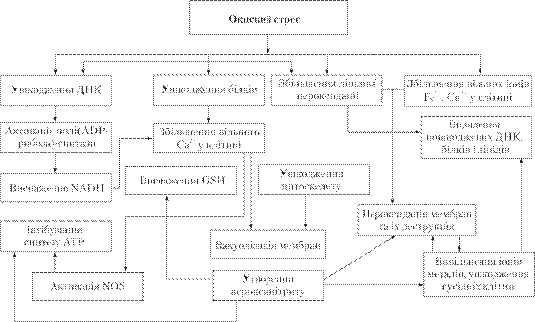
Рис. 1. Механізм дії
оксидативного стресу (GSH - глутатіон відновлений; NOS - NO-синтаза; NADH -
нікотинаденіндинуклеотид відновлений; АТР - аденозинтрифосфат)
Якщо активація вільнорадикального окиснення
відіграє таку важливу роль у механізмі стресу, то системи антиоксидантного
захисту, які є на всіх рівнях структури організму, виступають як найважливіша
внутрішня сила протидії стресовим ушкодженням і порушенням. Разом з тим
антиоксидантні механізми безпосередньо задіяні у стрес-реакції, є її
невід’ємною частиною, завдяки чому стрес власне і є адаптивною реакцією.
Введення антиоксидантів ззовні, з харчовими продуктами та фармпрепаратами,
поповнює їх ендогенні резерви, збільшує захис - ну активність системи,
забезпечує утримання стресу у фізіологічних рамках. Антиоксиданти містяться в
організмі всюди, де є певна небезпека виникнення окисного вибуху [7, 8].
Компоненти системи цього захисту - антиоксидантні
ферменти мітохондрій і цитозолю клітин (розчинні й мембрано-асоційовані),
ферменти крові, жиро - і водорозчинні антиоксиданти, тіолові сполуки,
металотіонеїни, а також репаративні системи - функціонують координовано.
Основні антиоксидантні ферменти -
супероксиддисмутази (СОД) і каталаза. СОД нейтралізують супероксидний
іон-радикал, перетворюючи його на воду і пероксид водню - активний окисник,
який знешкоджується каталазою. Мідь/цинк-вмісна супероксиддисмутаза (CuZnСОД) є
в цитозолі, а марганець-вмісна (MnСОД) - у мембранах і матриксі мітохондрій.
Каталаза міститься в пероксисомах. Відома також CuZnСОД, яка знаходиться в
крові і захищає від пероксидації ендотелій судин.
Відновлений глутатіон (GSH) є головним фактором
підтримання внутрішньоклітинного редокс-гомеостазу, він безпосередньо інакти -
вує АФК і також функціонує як кофактор і косубстрат GSH-залежних ферментів. Як
і цистеїн, тіоредоксин, ерготіонеїн, він відновлює дисульфідні групи до
тіолових, бере участь у тіол-дисульфідному обміні. Глутатіонпероксидаза
розкладає Н2О2 до води у взаємозв’язку з окисненням глутатіону [1-3].
Пероксидази - група ферментів, які використовують
пероксид водню для окиснення інших субстратів. Це цитохром-С-пероксидаза,
мієлопероксидаза, NADH-пероксидаза, пероксидаза хрому тощо.
У крові людини і тварин міститься церулоплазмін -
головний позаклітинний антиоксидантний фермент, якому притаманна
СОД-активність. Поряд з антиоксидантними ферментами захищають клітини і тканини
від окисного стресу також ферменти і білки, що зв’язують іони металів зі
змінною валентністю і блокують їх здатність каталізувати окиснення і
пероксидацію.
До жиророзчинних антиоксидантів належать: вітамін
Е (токоферол, а також менш активні a-, β - токофероли і
токотрієноли), який захищає ліпідний бішар плазматичних, мітохондріальних,
ядерних мембран, ліпопротеїди крові та лімфи; вітамін А (ретинол, ретиналь,
ретиноєва кислота і провітамін b-каротин) захищає
клітинні й тканинні мембрани, ліпопротеїди, сітківку ока; пігмент білірубін -
продукт метаболізму жовчних кислот; ліпоєва кислота, коензим Q
(убіхінол-убіхінон) - компонент і важливий фактор редокс-стабілізації
електрон-транспортних ланцюгів. Додають свій важливий внесок у редокс-гомеостаз
мікроелементи, зокрема Zn, Fe, Cu, Se, а також гормони, олігопептиди, опіоїдні
пептиди, нейропептид Y та деякі інші нейропептиди, пігмент меланін.
До водорозчинних вітамінів належать С, РР, група
В, до вітаміноподібних речовин - холін, ліпоєва кислота та інші. Деякі вітаміни
синтезуються в організмі людини ендогенно мікрофлорою кишок, більшість не
синтезуються зовсім. Тому потрібно забезпечити їх постійне надходження з
продуктами харчування.
Другу лінію антиоксидантного захисту утворюють
ліполітичні ферменти (ліпази й фосфоліпази), які захоплюють і сприяють
видаленню з ліпідного бішару окиснених жирних кислот,що обриває ланцюгові
реакції ліпідної пероксидації; протеолітичні ферменти, які прискорюють
деградацію окиснених білків. Стресові білки (білки теплового шоку) відновлюють
нормальну конформацію частково окиснених, денатурованих білків і прискорюють
деградацію глибоко змінених білків. Ферменти репаративних систем клітини
ліквідують ушкодження структури ДНК.
Кожен з компонентів антиоксидантного захисту
необхідний для виконання своєї, притаманної тільки йому, функції на різних
стадіях процесу окиснення. Усі ці численні компоненти клітини створюють складну
ієрархічну антиоксидантну систему, вони взаємодіють між собою і в сукупності
забезпечують підтримку і збереження редокс-гомеостазу в умовах дії стресорів
різної природи.
Доведено, що пероксидація ліпідів здійснюється
переважно внаслідок вільнорадикальних реакцій і є ланцюговим процесом, у якому
беруть участь алкільні R, алкоксидні RO, пероксидні RОOрадикали і АФК, зокрема
синглетний кисень і супероксид аніон-радикал [9, 10].
В організмі людини молекулярний кисень є основним
джерелом окиснення. Електронна конфігурація молекули кисню в основному стані
має два неспарені електрони на зовнішній оболонці, даючи триплетний сигнал у
магнітному полі*. Хоча реакції між киснем, який перебуває в основному стані
(3О2), та біологічними молекулами є термодинамічно сприятливими, внаслідок
високого значення енергії активації (146-273 кДж·моль) вони відбуваються
повільно.
Активація триплетного кисню, як окисника в
окисно-відновних реакціях, потребує великих витрат енергії. Одним зі способів
активації є переведення кисню з основного (3О2) у збуджений синглетний стан
(1О2). Синглетний кисень - не радикал, електрофіл, надзвичайно реакційноздатна
і короткоіснуюча ( (50 - 700) 106 с залежно від природи розчинника)
частинка. Він може утворюватися хімічним, ензиматичним і фотохімічним шляхом.
До активних форм кисню, що утворилися внаслідок відновлення його триплетного
стану, відносять супероксид аніон-радикал (О-), його кон’юговану кислоту (НО)
(пергідроксил-радикал), пероксид водню (Н2О2), гідроксильний ради - кал ОН,
гіпохлоритну кислоту НОСl та пероксинітрит ONOOˉ. Найсильнішими
електрофілами і найбільш реакційноздатними фор - мами кисню є 1О2 та ОН[11].
Механізм
дії природних, синтетичних антиоксидантів і ліків
Основним методом захисту біологічних систем
людини від окиснення є використання специфічних харчових добавок або лікарських
засобів, які гальмують цей процес.
Вільні радикали можуть реагувати з багатьма
сполуками, що містяться в клітинах, за різними механізмами - перенос електрона
до чи від радикала з отриманням відповідних іонів; відщеплення атома водню з
утворенням нових радикалів та ймовірністю ланцюгового механізму; утворення хелатних
комплексів з d-металами; протонізація вільних радикалів з накопиченням
іон-радикалів; реакції приєднання, диспропорціонування, самоанігіляції тощо.
Антиоксидантна активність сполук залежить від
багатьох факторів, зокрема від їх концентрації, природи біологічних компонентів
(білки, жири, вуглеводи, амінокислоти, ліпіди та ін.), температури, тиску
кисню, наявності інших антиоксидантів, води, природи каталізаторів тощо.
На рис.2 наведено основні класи антиоксидантів.
Антиоксидантна система організму людини містить дві основні групи
антиоксидантів - ензиматичні й неензиматичні. Первинну ланку ензиматичного
захисту забезпечують супероксиддисмутаза, яка перетворює супероксид
аніон-радикал на H2O2, який каталаза розщеплює до H2O і O2, і глутатіонпероксидаза,
що слугує відновником для пероксидів.
Вторинну ланку становлять глутатіонредуктаза і
глюкозо-6-фосфатдегідрогеназа, які безпосередньо не реагують з радикалами,
протее важливі для діяльності інших ендогенних антиоксидантів.
До неeнзиматичних ендогенних антиоксидантів
належать вітаміни, кофактори ензимів, пептиди, сполуки азоту непротеїнової
природи, фенольні кислоти, органічні сірковмісні сполуки тощо. Коензим Q10,
наприклад, взаємодіє з ліпідними пероксидними радикалами, а також бере участь у
регенерації вітаміну Е. Уринова кислота захищає від надлишку
оксогем-оксидантів, які утворюються в реакції гемоглобіну з пероксидами, а
також реагує з синглетним киснем та гідроксильними радикалами.
Окремий клас становлять синтетичні антиоксиданти
- переважно це просторово екрановані феноли, а також фармпрепарати, які
здебільшого є витяжками з біологічно активних рослин, плодів, овочів [10, 12].
Антиоксиданти захоплюють вільні радикали, надаючи
їм водень, а також продукуючи відносно стабільні антиоксидантні радикали з
низьким відновним потенціалом (менш як 0,5 В) [9]. Підвищена стабільність
антиоксидантних радикалів пов’язана з резонансною делокалізацією структур, які
містять фенольне ядро, чи просторовим екрануванням реакційного центру об’ємними
замісниками [10]. Прикладами похідних фенолу, які слугують вільнорадикальними
пастками, є токофероли, трет-бутилгідрокситолуол, трет-бутилгідроксіанізол,
трет-бутилгідрохінон, лігніни, флавоноїди, фенольні кислоти, наприклад
розмаринова.
Енергія дисоціації зв’язку О-Н фенольних
антиоксидантів загалом визначає стабільність відповідних антиоксидантних
радикалів: чим вона менша, тим стабільніший антиоксидантний радикал.
Потужним інгібітором активних форм кисню є
розмаринова кислота. Вона широко застосовується як терапевтичний препарат при
лікуванні діуретичних, запальних процесів, має антисклеротичні властивості
[13]. Зерна кави містять значну кількість одного з найпотужніших фенольних
антиоксидантів - хлорогенової кислоти. Її споживання знижує ризики виникнення
цукрового діабету ІІ типу.
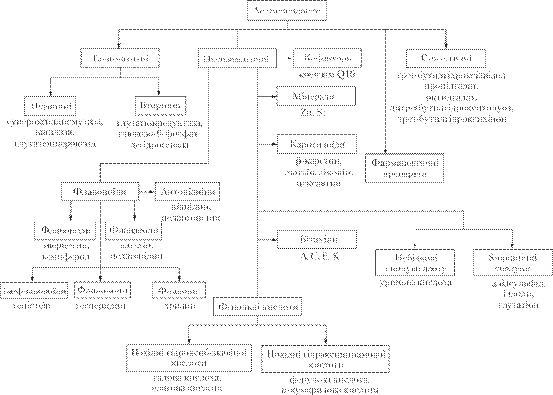
Рис. 2. Основні класи
антиоксидантів [10, 12] логічних і серцево-судинних захворювань [14, 15].
У великих кількостях кава шкідлива для осіб, що
страждають на артеріальну гіпертензію, ішемічну хворобу серця, гастрити, а
також для вагітних. Крім того, вона може викликати залежність, особливо серед
любителів розчинної кави.
Флавоноїди - група антиоксидантних сполук, що
складається з флавонолів, антоціанінів, ізофлавоноїдів, флаванолів і флавонів.
Найефективнішими серед них є катехін, катехінгалат, кверцетин та кемпферол.
Флавоноїди, особливо кверцетин і лутеолін, - потенційні інгібітори
ксантиноксидази, яка долучена до процесів оксидативного ушкодження, переважно
після ішемічної реперфузії, оскільки, реагуючи з молекулярним киснем, продукує
супероксид-радикал [16, 17]. Біофлавоноїди, зокрема корвітин, як розчинну
лікарську форму кверцетину, й таблетки квертину (випускаються київським
Борщагівським хімфармзаводом) ефективно використовують у лікуванні гострого
інфаркту міокарда, ішемічної хвороби серця, інсультів [18]. У комбінаціях з
гіпоглікемічними засобами їх рекомендують для профілактики розвитку нефропатії
у хворих на цукровий діабет І та ІІ типу [19].
Властивість флавоноїдів пригнічувати ріст
злоякісних пухлин також пов’язана з їх функцією вільнорадикальної пастки.
Флавоноїди гальмують розмноження онкоклітин і зумовлюють їх апоптоз
(руйнування).
Одним із найпоширеніших і ефективних
антиоксидантів є каротиноїди [20, 21]. Давно відомо, що ці сполуки втрачають
свій колір, коли потрапляють у середовище, яке містить вільні радикали, або за
наявності окисників, що пояснюється порушенням ланцюга кон’югованих подвійних
зв’язків. Рослина шафран містить каротиноїдний антиоксидант кроцин. Втрату
забарвлення цього каротиноїду використовують як метод визначення
антиоксидантної ємності в плазмі крові, а також природних сполук та екстрактів
рослин. Одним із основних біологічних продуктів окиснення каротиноїдів вважають
ретиноєву кислоту, яка бере участь у процесах синтезу кісток і м’яких тканин
під час розвитку ембріона. Плазма крові містить приблизно 1-2 μМ каротиноїдів. У такій концентрації за фізіологічного
парціального тиску прооксидантна здатність каротиноїдів незначна, тоді як
антиоксидантна доволі велика [22]. Ретинол (вітамін А) - ліпофільний
антиоксидант, який синтезується в організмі людини з β-каротину. Він необхідний для роботи зорової, опорно-рухової,
імунної систем, а також для підтримки здоров’я шкіри та волосся. Вітамін А і β-каротин - потужні антиоксиданти, які використовують як
засоби профілактики онкологічних захворювань, зокрема, вони за - побігають
рецидиву пухлин після операцій. Ретинол та β-каротин захищають мембрани головного мозку від руйнівної дії
вільних радикалів, при цьому β-каротин
нейтралізує найнебезпечніші з них.
Прикладом механізму приєднання радикала є
взаємодія β-каротину й монооксиду
азоту, який міститься в тютюновому димі:
+ NО = NO-CAR.
Отже, каротиноїди є потенційно корисними для
осіб, які палять, зважаючи на зниження токсичного впливу оксидантів, що містяться
у тютюновому димі [10].
Аскорбінова кислота, глутатіон і цистеїн, які
мають властивості вільнорадикальних пасток, виступають донорами атома водню,
надаючи його вільним радикалам і продукуючи більш стабільні радикали глутатіону
та аскорбінової кислоти [9]. Ця кислота енергійно реагує з супероксид
аніон-радикалом, Н2О2, та 1О2
і впливає на синтез в організмі людини NO, який
бере участь у регуляції тонусу судин і багатьох фізіологічних процесах.
Амінокислоти, що містять сульфгідрильні та
гідроксильні групи, такі як цистеїн, фенілаланін і пролін, також інактивують
вільні радикали. При цьому відбувається конкуренція між білковими сполуками та
ліпідами за високореакційноздатні радикали [9]. Взаємні перетворення в системі
цистин - цистеїн визначають активну участь цих амінокислот в окисно-відновних
реакціях біохімічних процесів дихання, обміну речовин, нервової діяльності
живих організмів тощо [10].
оксидативний стрес актиоксидантний фермент
Останнім часом зростає інтерес до антиоксидантних
властивостей ліпоєвої кислоти (6,8 - дитіооктанової), яка існує у двох формах -
окисненій (дисульфід) і відновленій. Ліпоєва кислота може функціонувати як
акцептор вільних радикалів і метаболічний природний антиоксидантний протектор.
Увага дослідників зосереджена на цій кислоті як клітинному редокс-регуляторі,
який бере участь у процесах передачі сигналу. Тому ліпоєва кислота є потенційно
важливим терапевтичним агентом при окисному стресі. Її використання
перспективне в терапії нейродегенеративних хвороб, діабетичної нейропатії,
ішемічної реперфузії, ВІЛ, захворювань печінки (цироз, хвороба Боткіна) тощо
[23].
Деякі антиоксиданти (вітамін С, убіхінон,
глутатіон) можуть рециклювати вітамін Е - головний антиоксидант, що обриває
радикаль - ні ланцюги і захищає біомембрани від ліпідного перокиснення [24,
25]. Глутатіон є головним внутрішньоклітинним антиоксидантом, що діє як
сульфгідрильний буфер, захищаючи зали - шок цистеїну від окиснення в протеїнах,
тобто дію глутатіону можна розглядати в рамках терапевтичної стратегії.
Катіони важких металів - каталізатори окиснення,
які розкладають гідропероксиди, утворені на ранніх стадіях [9, 10] з
накопиченням радикалів, що включаються в ланцюгові реакції аутоокиснення. У
незначних кількостях важкі метали містяться в багатьох ензимах та інших
металовмісних білках. Білки гем (Fe2+) і гемін (Fe3+) часто присутні в харчових
продуктах. Гемоглобін, міоглобін та цитохром С поглиблюють перокиснення ліпідів
у тканинах та сировині тваринного походження.
Хелатні комплекси гальмують процес окиснення
внаслідок утворення нерозчинних комплексів і зниження таким чином
редокс-потенціалів металів або завдяки створенню стеричних перешкод між
металами та компонентами біологічних систем чи їх окиснених інтермедіатів [9,
10]. Лимонна та етилендіамінтетраоцтова (ЕДТА) кислоти є класичними прикладами
сполук, що утворюють з металами хелатні комплекси. Більшість подібних
комплексоутворювачів розчинні у воді, а лимонна кислота обмежено розчинна в
жирах. У ролі сполук, здатних утворювати хелати, можуть виступати фосфоліпіди
[9], флавоноїди, активність яких залежить від їх структурних особливостей [17].
Утворення комплексів хелатного типу з катіонами металів має велике значення в
патогенезі деяких хвороб. Реакції Фентона відбуваються в дофамінових нейронах
нервових тканин, де внаслідок катаболізму утворюється певна кількість пероксиду
водню [14]. Накопичення радикалів у цих нейронах вважається основним
патогенетичним агентом хвороби Паркінсона [26]. Ознакою інших
нейродегенеративних хвороб, таких як хвороба Альцгеймера та синдром
Хантінгтона, вважається накопичення катіонів заліза в деяких ділянках мозку
[27]. У людей, які страждають на хворобу Альцгеймера, підвищується кількість
феритинового заліза базальних ганглій.
Взаємодія антиоксидантів між собою може бути
синергічною, антагоністичною або просто адитивною. Типовим прикладом синергізму
антиоксидантів є дія суміші -токоферолу та аскорбінової кислоти при
аутоокисненні й фотоокисненні ліпідів [9, 10]. Поліфенольні сполуки, такі як
епігалокатехінгалат, кверцетин, епікатехінгалат, епікатехін та ціанідин,
характеризуються адитивним ефектом з
-токоферолом, який слугує
вільнорадикальною пасткою [24].
Надзвичайно важливою функцією антиоксидантів є
регулювання діяльності радикал - генеруючих ензимів, таких як NAD (P) H-оксидаза
і ксантиноксидаза, а також активності експресії антиоксидантних ензимів (су -
пероксиддисмутаза, каталаза, глутатіонпероксидаза). Ці антиоксидантні ензими
виробляються в організмі людини і є важливою ланкою захисту проти дії вільних
радикалів.
Окиснення
ліпідів, білків і вуглеводів
Ліпіди, що містять подвійний С-С зв’язок, а саме
ненасичені жирні кислоти, фосфоліпіди, гліколіпіди, холестерол та його ефіри, є
особливо чутливими до реакцій окиснення. Поліненасичені жирні кислоти, які
містять 1,4 - пентадієнові функціональні фрагменти, також схильні до реакцій
окиснення. Наприклад, окиснення лінолевої кислоти, що входить до складу
багатьох харчових продуктів, відбувається за двома основними механізмами -
відщеплення атома водню та приєднання синглетного кисню.
Утворені під час первинного окиснення
гідроксипероксиди жирних кислот - нестабільні сполуки, які зазнають вторинного
окиснення з утворенням продуктів полімеризації чи низькомолекулярних альдегідів
і кетонів [9, 10].
Малоновий діальдегід - один із найпоширеніших
продуктів окиснення жирів. Його часто використовують як індикатор ступеня
окиснення ліпідів біологічних систем, він ви - никає в організмі внаслідок
розкладання полі - ненасичених жирів високореакційноздатними формами кисню,
слугує маркером оксидативного стресу. Відомо, що він здатен реагувати з ДНК,
утворюючи мутагенні аддукти. У хворих на цукровий діабет, ускладнений
ангіопатією, рівень малонового діальдегіду значно вищий, ніж у таких пацієнтів
без ангіопатій.
При дії вільних радикалів білки, пептиди та
амінокислоти, які містяться в них, можуть за - знавати оксидативних змін [9].
Найбільш чутливими і схильними до окисного розкладання амінокислотами вважають
метіонін, цистеїн (цистин), гістидин і триптофан [9, 10], а за певних умов -
також тирозин, серин і треонін. Окиснення білків та амінокислот може
відбуватися під дією світла, випромінювання, перокиснених ліпідів, іонів
металів, продуктів ензиматичних і неензиматичних реакцій, що супроводжуються
зміною кольору, тощо [9].
Крім перокиснення ліпідів і руйнування ДНК
макромолекул АФК можуть включатися в реакції нітрування і хлорування
амінокислот, модифікуючи відповідні протеїни. Пероксинітрит ONOOˉ та його
протонована форма пероксинітрозна кислота ONOOH є потужними оксидантами і
нітруючими агентами. Гемо-протеїн мієлопероксидаза каталізує утворен ня HOCl
(H2O2 + Clˉ ®HOCl).
Гіпохлоритна кислота реагує з жирними кислотами,
холестеролом, протеїнами, ДНК, РНК, утворюючи відповідні продукти хлорування
[28]. Наявність нітро- чи хлоротирозину слугує біомаркером цих процесів [29].
Протеїни, що містять залишок нітротирозину, було знайдено при різних
патологіях, зокрема діабеті, гіпертензії, атеросклерозі тощо. Інгібітором пероксинітриту,
який відіграє ключову роль у хворобі Альцгеймера, є розмаринова кислота.
Ефективними інгібіторами дії HOCl виступають окиснений і відновлений глутатіон,
метилглутатіон, ліпоєва кислота.
Вуглеводи не настільки чутливі до окиснен - ня,
як білки та ліпіди, а продукти їх окиснення не леткі [30].
Незважаючи на потужну ендогенну антиоксидантну
систему організму людини, для підтримки адекватного антиоксидантного статусу і
концентрації вільних радикалів на низькому рівні потрібно щодня вживати їжу,
багату на антиоксиданти. Проте біологічні антиоксиданти можуть виявляти
прооксидантні властивості, що залежить від їх концентрації та умов середовища.
Прооксиданти розглядають як високореакційні частинки, що індукують оксидативний
стрес або виступають інгібіторами антиоксидантної системи організму людини
[31].
Редокс-потенціал антиоксидантів характеризує їх
активність в окисно-відновних реакціях і пов’язаний з прооксидантними ефектами,
які залежать від їх концентрації. Наприклад, ліпоєва і дигідроліпоєва кислоти інгібують
утворення нітротирозину з пероксинітриту за концентрації 0,01-0,05 мМ, а за
вищих концентрацій - виявляють прооксидантні властивості [29].
Потужний антиоксидант - водорозчинний вітамін С
за наявності солей міді чи заліза ви - являє прооксидантні властивості,
відновлюю - чи іони Fe3+ до Fe2+ і Cu2+ до Cu+ і сприяючи розкладанню пероксиду
водню до гідроксильних радикалів. Збагачення харчових продуктів аскорбіновою
кислотою не рекомендується. позитивний ефект для хворих з низьким його рівнем у
плазмі, що характер - не для багатьох хвороб, у тому числі онкологічних.
Вживання їжі, збагаченої вітаміном С, є корисним при діабеті, атеросклерозі,
гіпертензії, гіпохолестеролемії, що пояснюють його здатністю захищати від
окиснення ліпопротеїди низької густини і збільшувати кількість атерозахисного
оксиду азоту в організмі [12, 25].
Прооксидантний ефект виявляють у високих дозах
каротиноїди, флавоноїди, зумовлюючи розвиток онкозахворювань. Загалом, про -
оксидантний ефект антиоксидантів залежить від: а) їх концентрації; б)
редокс-потенціалу; в) наявності інших антиоксидантів; г) присутності іонів
перехідних металів; д) активності та концентрації ендогенних антиоксидантів.
Шляхи
подолання оксидативного стресу
Надмірний довготривалий оксидативний стрес
супроводжується утворенням високореакцій - них АФК, АФА, АФС, АФХ і призводить
до низки серйозних захворювань, таких як онкологічні, серцево-судинні, інфаркт,
атероскле - роз, нервові, ниркові, печінкові хвороби, гіпертензія, ревматоїдний
артрит, синдром респіраторного дистресу, запалення, дегенеративні зміни,
пов’язані з віком, діабет і його ускладнення, ожиріння, катаракти, аутизм,
хвороби Альцгеймера, Паркінсона, Хантінгтона, васкуліт, гломерулонефрит,
гемохроматоз, виразка шлунку тощо [1]. Оксидативний стрес супроводжується
виснаженням внутрішніх резервів і потребує надійного захисту. В процесі
захисної дії антиоксиданти поступово виводяться з організму, і тому необхідно
постійно відновлювати їх кількість з продуктами харчування чи фармпрепаратами.
Уже в невеликих кількостях (0,01-0,001 %) антиоксиданти помітно гальмують
процеси окиснення біосистем, коли потужний внутрішньоклітинний антиоксидантний
захист доповнюється позаклітинним.
Синтетичні антиоксиданти, такі як іонол,
трет-бутилгідрокситолуол, трет-бутилгідроксихінон, використовують у харчовій
промисловості для захисту продукції від окиснення ліпідів. Однак через
токсикологічні проблеми вони поступаються фармакологічним препаратам. Більшість
натуральних антиоксидантів отримують із фруктів, овочів, екстрактів зернових
культур і трав, до них належать, наприклад, куркума, розмарин, зелений чай,
грейпфрут, часник тощо. Сильну антиоксидантну дію виявляють екстракти гінкго
завдяки наявності флавонових глікозидів, які нейтралізують вільні радикали,
екстракти зеленого чаю і грейпфруту, що містять флавоноїди катехін і епікатехін
[33].
Велику антистресову активність мають мед і
продукти бджільництва, а також речовини, що містять біологічно активні
складові, - женьшень, китайський лимонник, елеутерокок, мумійо тощо. Потужним
джерелом антиоксидантів є чай, кава, шоколад.
Крім вищеназваних антиоксидантів фарм - індустрія
пропонує ще десятки інших, серед яких найбільш уживаними є глікозид МВ (діа -
бетон MR), мексидол, емоксипін та тіотриазолін. Глікозид (сульфанілсечовина II
покоління) належить до гіпоглікемічних засобів лікування діабету ІІ типу,
виявляє антитератогенну і антиоксидантну дію, збільшуючи стійкість бета-клітин
підшлункової залози до оксидативного стресу [19]. Мексидол і емоксипін
(сукцинат і гідрохлорид 3-гідрокси-6-метил-2-етил - піридину) мають
антигіпоксичну, ангіопротекторну і антиагрегаційну дію, застосовуються в
офтальмії для лікування діабетичної ретинопатії і при порушенні мозкового
кровообігу та інших станів, пов’язаних з гіпоксією тканин [34]. Вітчизняний
антиоксидант тіотриазолін (морфоліній 2-метил-1,2,4-триазоліл-5-тіоацетат)
виявляє протиішемічні, мембраностабілізуючі та імуномодулюючі властивості. Він
активує антиоксидантну систему, гальмує процеси перекисного окиснення ліпідів в
ішемічних ділянках міокарда, запобігає загибелі гепатоцитів, нормалізує
білковий, вуглеводний, ліпідний та печінковий обміни, покращує реологічні
властивості крові [35].
У наш час біоантиоксиданти розглядають як
перспективні терапевтичні засоби для лікування багатьох хвороб. Активність
таких антиоксидантів залежить від того, на якій стадії хвороби вводять
препарат, оскільки розвиток захворювання супроводжується зміною антиокисної
активності. Перспективним напрямом є синтез багатофункціональних
антиоксидантів, що поєднують антиоксидантну та інші функціональні властивості.
Тому важливим завданням спеціалістів агропромислового комплексу є розроблення
нових сортів рослин, що мають такі властивості. Новим напрямом у вивченні
біоантиоксидантів є ефект їх дії в над - малих дозах [36]. На прикладі
токоферолу і фенозану К знайдено, що вони діють однотип - но у звичайних (103-105)
і надмалих (109 - 1013 М) концентраціях. Подальше вивчення
цього феномену обіцяє великі перспективи у практичному плані, особливо в
геронтології та профілактиці онкозахворювань. Встановлено важливу роль
антиоксидантів в експресії генів і стабільності геному, оскільки вільні
радикали можуть регулювати активність генів [9].
Мінерали відіграють важливу роль у метаболізмі
антиоксидантів. Дефіцит чи надлишок есенціальних елементів призводить до
непередбачуваних метаболічних змін у здоров’ї людини і потребує адекватного
збагачення ними харчових продуктів, яке слід ретельно контролювати [37].
Зараз велику увагу приділяють вивченню
взаємозв’язку гіпоелементозу (Zn, Fe, Cu, Se, Mo, Mn, Co) і оксидативного
стресу. Дослідження вмісту 25 мікроелементів у плазмі крові за допомогою
плазмової мас-спектроскопії високої роздільної здатності показали, що дефіцит
мікроелементів, особливо селену, цинку і марганцю, зменшує активність
антиоксидантних ензимів, збільшуючи оксидативний стрес, що порушує коронарну
мікроциркуляцію і призводить до серцевої дисфункції [38]. Над - звичайно
важливою в розвитку оксидативного стресу є роль цинку і селену. Селен в
організмі людини міститься як в органічній (селеноцистеїн і селенометіонін),
так і в неорганічній (селеніт і селенат) формах. Хоча селен, як і цинк,
безпосередньо не реагує з вільними радикалами, він активує антиоксидантні
ензими (металоензими, глутатіонпероксидазу, тіоредоксин редуктазу та ін.). Цинк
є інгібітором NAD (Р) Н - оксидази, яка каталізує утворення синглетного кисню,
він входить до складу супероксид - дисмутази, яка перетворює синглетний кисень
на Н2О2, а також до металотіонеїнів, які є пасткою гідроксильних радикалів.
Оксидативний стрес відіграє важливу роль у
патогенезі залізодефіцитної анемії, у розвитку ангіопатії при цукровому
діабеті. Тому дієтотерапія при цукровому діабеті повинна включати
біоантиоксиданти, особливо ті, що містять селен. Наслідком нестачі його є зниження
імунітету, перевантаження серця, передчасне ста - ріння організму людини тощо
[1].
Дослідження останніх років показують, що однією з
причин розвитку оксидативного стресу є нестача цинку в організмі, що в
кінцевому підсумку призводить до ініціювання багатьох хронічних хвороб. Якщо
врахувати, що близько 2 млрд людей на Землі потерпають від нестачі цинку,
проблема забезпечення адекватного рівня його споживання людиною стає нагальною
в усьому світі [39].
Одним із можливих шляхів вирішення проблеми
дефіциту мікроелементів у харчуванні може стати застосування сполук з корисними
властивостями, які отримують шляхом нано-технологій, зокрема солей біогенних
металів харчових кислот [40].
Згідно з визначенням ВООЗ, однією з головних
проблем харчування в XXI ст. стане подолання дефіциту мікронутрієнтів загалом і
мікроелементів зокрема. Зміна харчового статусу пов’язана з усе меншим
споживанням свіжої рослинної їжі й дедалі більшим - продукції промислового
виробництва, в якій у процесах технологічної обробки залишається мало
вітамінів, біологічно активних речовин і мікроелементів, натомість додаються
нехарчові інгредієнти - барвники, емульгатори тощо [39]. Інтенсивні технології
виробництва в землеробстві і тваринництві також зумовлюють істотне зменшення
необхідних інгредієнтів уже в самій природній сировині. Малорухливий спосіб
життя, споживання висококалорійних продуктів промислового виробництва,
психоемоційні навантаження призводять до суттєвого погіршення здоров’я
населення і виникнення різного роду стресів.
Загалом порушення хиткої рівноваги між
антиоксидантами, що містяться в більшій кількості, ніж це потрібно для
виконання біологічних функцій, і високореакційними частинками спричинює
антиоксидант-індукований стрес. Одним із надійних шляхів боротьби з ним є
збільшення ендогенного антиоксидантного захисту завдяки помірним щоденним
фізичним вправам, а також досягненню стійкої психоемоційної рівноваги.
Список
літератури
1. Барабой
В.А., Резніков О.Г. Фізіологія, біохімія і психологія стресу. - К.: Інтерсервіс,
2013. - 314 с.
2. Durackova
Z. Some
current insights into oxidative stress // Physiol. Res. - 2010. - V.59. -
P.459-469.
3. Fisher-Wellman
K., Bell H. K., Bloomer R. J. Oxidative stress and antioxidant defense mechanisms linked to
exercise during cardiopulmonary and metabolic disorders // Oxid. Med. Cell.
Longev. - 2009. - V.2. - P.43-51.
4. Laranjinha
J. Oxidative
stress: from 1980’s to recent update // Oxidative Stress. Inflammation and
Angiogenesis in the Metabolic Syndrome. - N. Y., 2009. - P.21-32.
5. Min
D. B., Doff I. M. Chemistry and Reaction of Singlet Oxygen in Foods // Comp. Rev. Food Sci.
Food Saf. - 2002. - V.1. - P.58-72.
6. Valko
M., Leibfritz D., Moncol J. et al. Free radicals and antioxidants in normal physiological
functions and human disease // Int. J. Biochem. Cell. Biol. - 2007. - V.39. -
P.44-84.
7. Lobo
V., Phatak A., Chandra N. Free radicals and functional foods: impact on human health //
Pharmacol. Rev. - 2010. - V.4. - P.118-126.
8. Diet,
nutrition and the prevention of chronic diseases. Report of a Joint WHO/FAO
Expert Consultation. - Geneva: WHO, 2003. - http://www.whglibdoc. who.
int/trs/WHOTRS916. pdf. <http://www.whglibdoc.who.int/trs/WHOTRS916.pdf>
9. Choe E.,
Min D. B. Mechanisms of
antioxidants in the oxidation of foods // Comp. Rev. Food Sci. Food Saf. -
2009. - V.8. - P.345-358.
10. Polumbryk
M., Ivanov S., Polumbryk O. Antioxidants
in food systems. Mechanism of action // Ukr. J. Food Sci. - 2013. - V.1. -
P.15-40.
11. Durackova
Z. Oxidants, antioxidants and
oxidative stress // Mitochondrial Medicine / ed. A. Gvordjakova. - N. Y.:
Springer, 2008. - Р. 19-54.
12. Carocho M.,
Ferreira I. C. F. R. A review
on antioxidants, prooxidants and related controversy: natural and synthetic
compounds, screening and analysis methodologies and future perspectives // Food
Chem. Toxicol. - 2013. - V.57. - P.15-25.
13. Gao L. P.,
Wei H. L., Zhao H. S. et al. Antiapoptotic
and antioxidant effects of rosmarinic acid in astrocytes // Pharma - cia. -
2005. - V.50. - P.62-65.
14. Leopoldini
M., Russo N., Toscano M. The
molecular basis of working mechanism of natural polyphenolic antioxi - dants //
Food Chem. - 2011. - V.125. - P.288-306.
15. Maurya D.
K., Devasagayam T. P. Antioxidant
and prooxidant nature of hydroxyl cinnamic acid derivatives ferulic and caffeic
acids // J. Appl. Toxicol. - 2005. - V.25. - P.535-548.
16. Pietta P.
G. Flavonoids as antioxidants
// J. Nat. Food. - 2000. - V.63. - P.1035-1042.
17. Prochazkova
D., Bousova I., Wilhelmova N. Antioxidant
and prooxidant properties of flavonoids // Fitoterapia. - 2011. - V.82. -
P.513-523.
18. Максютина
Н.П., Мойбенко А.А., Мохарт Н.А. и др. Биофлавоноиды как органопротекторы (кверцитин,
корвитин, квертин). - К.: Наук. думка, 2012. - 274 с.
19. Аметов
А.С., Соловьева О.Л. Окислительный
стресс при сахарном диабете 2-го типа и пути его коррекции // Проблемы
эндокринологии. - 2011. - Т.57, № 6. - С.52-56.
20. Young A.
J., Lowe G. M. Antioxidant
and prooxidant properties of carotenoids // Arch. Biochem. Biophys. - 2001. -
V.382. - P. 20-27.
21. Krinsky
N.I., Yeum K. J. Carotenoid-radical
interactions // Biochem. Biophys. Res.commun. - 2003. - V.305. - P.754-760.
22. Palozza P. Prooxidant actions of carotenoids in biologic
systems // Nutr. Rev. - 1998. - V.56. - Р.257-265.
23. Moini H.,
Packer L., Saris N. E. Antioxidant
and prooxidant activities of alpha-lipoic acid and dihydrolipoic acid //
Toxicol. Appl. Pharmacol. - 2002. - V.182. - P.84-90.
24. Murakami
M., Yamaguchi T., Takamura H. et al. Effects of ascorbic acid and L-tocopherol on antioxidant activity of
polyphenolic compounds // J. Food Sci. - 2003. - V.68. - P.1622-1625.
25. Lu J. M.,
Lin P. H., Yao Q., Chen C. Chemical
and molecular mechanisms of antioxidants: experimental approaches and model systems
// J. Cell. Mol. Med. - 2010. - V.14. - P.840-860.
26. Hirsch E.
C., Faucheux B. A. Iron
metabolism and Parkinson’s disease // Movem. Disord. - 1998. - V.13. - P.39-45.
27. Cuajungco
M. P., Faget K. Y., Huang X et al. Metal chelation as a potential therapy for Alzheimer’s disease // Ann.
N. Y. Acad. Sci. - 2000. - V.920. - P.292-304.
28. Pacher P.,
Beckman J. S., Liaudet L. Nitric
oxide and peroxynitrite in health and disease // Physiol. Rev. - 2007. - V.87.
- P.315-424.
29. Viappiani
S., Schulz R. Detection of
specific nitrotyrosine - modified proteins as a marker of oxidative stress in
car - diovascular disease // Am. J. Physiol. Heart Circ. Physiol. - 2006. -
V.290. - P.2167-2168
30. Полумбрик
М.О. Вуглеводи в харчових
продуктах і здоров’я людини. - К.: Академперіодика, 2011. - 487 с.
31. Villanueva
C., Kross R. D. Antioxidant-induced
stress // Int. J. Mol. Sci. - 2012. - V.13. - P. 2091-2109.
32. Duarte T.
L., Lunec J. Review: When is
an antioxidant not an antioxidant? A review of novel actions and reaction of
vitamin C // Free Radic. Res. - 2005. - V.39. - P.671-680.
33. Rababah T.
M., Hettiarachchy N. S., Horax R. Total phenolics and antioxidant activities of fenugreek, green tea,
black tea, grape seed, ginger, rosemary, gotu cola and ginkgo extracts, vitamin
E and tret-butylhydroquinone // J. Agric. Food Chem. - 2004. - V.52. -
P.5183-5186.
34. Машковский
М.Д. Лекарственные средства.
- М.: Новая волна, 2005. - 1200 с.
35. Бибик Е.Ю.,
Фомина К.А., Ющак М.В. Тиотриазолин
- потенциальное лекарственное средство с детоксикаци - онной активностью //
Укр. мед. альманах. - 2009. - Т.12, № 1. - С.213-217.
36. Бурлакова
Е.Б. Биоантиоксиданты // Рос.
хим. журн. - 2007. - Т.51, № 1. - С.3-12.
37. Fragg C. G. Relevance, essentiality and toxicity of
trace elements in human health // Mol. Asp. Med. - 2005. - V.26. - P.235-244.
38. Eide D. J. The oxidative stress of Zinc deficiency //
Metallomics. - 2011. - V.3. - P.1124-1129.
39. Тронько
М.Д., Полумбрик О.М., Ковбаса В.М. та ін. Біологічна роль цинку і необхідність забезпечення
адекват - ного рівня його споживання людиною // Вісн. НАН України. - 2013. - №
6. - С.21-31.
40. Сердюк
А.М., Гуліч М.П., Каплуненко В.Г., Косінов М.В. Нанотехнології мікронутрієнтів і проблеми, перспек -
тиви та шляхи ліквідації дефіциту макро - та мікроелементів // Журн. АМН
України. - 2010. - Т.16, № 1. - С.107-114.