Синтез и свойства эфиров алиатических карбоновых кислот
LXXI Московская олимпиада школьников по
химии
МОСКОВСКИЙ ГОРОДСКОЙ ПЕДАГОГИЧЕСКИЙ
УНИВЕРСИТЕТ
РЕФЕРАТ
СИНТЕЗ И СВОЙСТВА ЭФИРОВ
АЛИФАТИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ
Москва - 15.03.2015
Сложными эфирами алифатических карбоновых кислот называются функциональные
производные алифатических карбоновых кислот с общей формулой RC(O)OR/.
Алифатические кислоты могут быть насыщенными, ненасыщенными и
полиненасыщенными. Отличаются они, в основном, по количеству углеродных атомов
и двойных связей между ними. Насыщенные жирные кислоты имеют одинарную связь
между атомами углерода. Ненасыщенные - одну двойную связь, а полиненасыщенные,
соответственно, несколько двойных или даже тройных связей.
К алифатическим относятся и кислоты жиров, связанные с глицерином.
Различают летучие и нелетучие алифатические кислоты.
К летучим относятся только одноосновные кислоты: уксусная, муравьиная,
пропионовая, масляная, валериановая - все они обладают резким запахом.
Нелетучие алифатические кислоты кроме карбоксильных имеют еще и
гидроксильные группы химических соединений и делятся на: одноосновные,
двухосновные и трехосновные. Наиболее широко распространены: яблочная,
лимонная, которые присутствуют почти во всех растениях.
|
Монокарбоновые
|
|
|
|
Метановая (муравьиная)
|
НСООН
|
формиат
|
|
Этановая (уксусная)
|
СН3СООН
|
ацетат
|
|
Пропановая (пропионовая)
|
СН3СН2СООН
|
пропионат
|
|
Бутановая (масляная)
|
СН3(СН2)2СООН
|
бутират
|
|
2-метилпропановая (изомасляная)
|
(СН3)2СНСООН
|
изобутират
|
|
Пропеновая (акриловая)
|
СН2=СНСООН
|
акрилат
|
|
Бутен-3-овая (винилуксусная)
|
СН2=СНСН2СООН
|
винилацетат
|
|
Дикарбоновые
|
|
|
|
Этандиовая (щавелевая)
|
НООС─СООН
|
оксалат
|
|
Пропандиовая (малоновая)
|
НООССН2СООН
|
малонат
|
|
Бутандиовая (янтарная)
|
НООССН2СН2СООН
|
сукцинат
|
|
Пентандиовая (глутаровая)
|
НООС(СН2)3СООН
|
глутарат
|
|
(Z)-Бутендиовая
(малеиновая)
|
(Z)-НООССН=СНСООН
|
малеинат
|
|
(Е)-Бутендиовая (фумаровая)
|
(Е)-НООССН=СНСООН
|
фумарат
|
Физические свойства
Простейшие по составу сложные эфиры карбоновых кислот - бесцветные
легкокипящие жидкости, высшие сложные эфиры - вязкие жидкости или твердые воскообразные
вещества.
Температура кипения сложных эфиров меньше, чем температуры кипения кислот
и спиртов с близкой молярной массой, т.к. сложные эфиры, в отличие от кислот и
спиртов, не способны образовывать водородные связи между молекулами.
С ростом молекулярной массы температура кипения и плавления сложных
эфиров обычно растет.
В отсутствие влаги сложные эфиры относительно стабильны к нагреванию,
термическая устойчивость их существенно зависит от длины углеводородной цепи и
степени разветвления радикалов.
Сложные эфиры низших карбоновых кислот и спиртов - летучие,
малорастворимые или практически нерастворимые в воде жидкости. С увеличением
относительной молекулярной массы растворимость сложных эфиров в воде падает.
Сложные эфиры хорошо растворяются в диэтиловом эфире, многие из них
растворяются в этаноле.
Высшие твердые эфиры запаха не имеют. Многие жидкие эфиры имеют приятный
фруктовый запах.
|
Этилформиат
|
Ром
|
|
Изопентилацетат
|
Груша
|
|
Этилбутират
|
Абрикос
|
|
Изопентилбутират
|
Банан
|
|
Бензилацетат
|
Жасмин
|
|
Изопентилформиат
|
|
Бутилформиат
|
Вишня
|
|
Бутилбутират
|
Ананас
|
|
Пентилпентаноат
|
Апельсин
|
|
Этилизопентаноат
|
Яблоко
|
|
Этилбензоат
|
Мята
|
|
Этилсалицилат
|
Орхидея
|
Низшие алифатические сложные эфиры легче воды и, как правило, хорошие
растворители для многих органических соединений.
Среди сложных эфиров дикарбоновых кислот наибольшим применением обладают
эфиры адипиновой, азелаиновой и себациновой кислот. Эфиры этих кислот обладают
весьма пологой кривой зависимости вязкости от температуры в интервале
+100...-60°С, соответственно низкой температурой застывания, весьма малой
испаряемостью, высокими термическими и термоокислительной стабильностями, не
вызывают коррозию различных металлов и по этим показателям значительно
превосходят минеральные масла.
Получение сложных эфиров
. При взаимодействии карбоновых кислот со спиртами в присутствии
кислотных катализаторов образуются сложные эфиры, а сама реакция называется
реакцией этерификации:
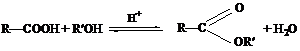
сложный эфир
В качестве катализаторов используют концентрированную серную кислоту,
газообразный хлороводород, сульфоновые кислоты, катионообменные смолы в Н+-
форме. В случае сильных карбоновых кислот, таких, как щавелевая, муравьиная,
трифтороуксусная, отпадает необходимость добавления минеральной кислоты, так
как подобные карбоновые кислоты сами катализируют реакцию:
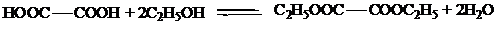
Реакция этерификации, как и многие другие реакции замещения у
тригонального атома углерода, чаще всего протекает по тетраэдрическому
механизму.
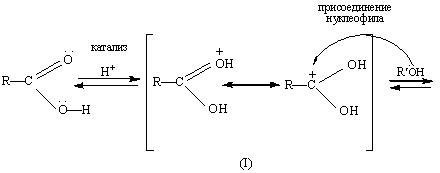
На стадии катализа протонируется карбонильный атом кислорода карбоновой
кислоты; гидроксильная группа не присоединяет протон, потому что неподеленная
пара электронов атома кислорода находится в сопряжении с карбонильной группой.
Возникший карбокатион (I)
обладает значительно более сильными электрофильными свойствами, чем исходная
карбоновая кислота, и поэтому может присоединять даже слабый нуклеофил, каким
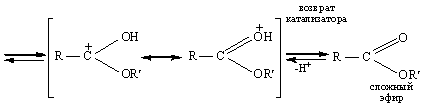
является молекула спирта. В образовавшемся катионе (II) происходит перенос протона к одной из гидроксильных групп,
и при этом формируется хорошо уходящая группа - молекула воды. После отщепления
воды от катиона (III) и возврата
катализатора образуется сложный эфир.

Все стадии реакции этерификации обратимы; обратная реакция представляет
собой катализируемый кислотой гидролиз сложных эфиров. При получении сложных
эфиров смещение равновесия вправо достигается разными способами: удалением воды
азеотропной отгонкой или с помощью осушителей, либо с применением большого
избытка спирта или кислоты, если тот или другой реактив достаточно доступен.
Смещение равновесия достигается также путем отгонки образующегося сложного
эфира.
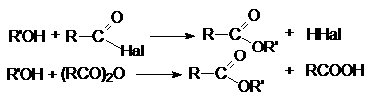
. Ацилирование спиртов галогенангидридами и ангидридами карбоновых
кислот.
. Ацилирование алкоголятов галогенангидридами и ангидридами карбоновых
кислот.
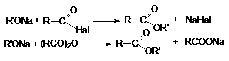
. Алкилирование солей карбоновых кислот.
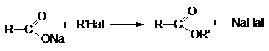
. Этерификация амидов и нитрилов карбоновых кислот.

. Реакция Байера-Виллигера
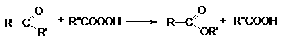
. Сложные эфиры высших дикарбоновых кислот получают из солей кислых
эфиров дикарбоновых кислот в условиях электрохимический реакции Кольбе:
2ROOC(CH2)nCOONa ROOC(CH2)2nCOOR
ROOC(CH2)2nCOOR
8. При присоединении кислот к ацетилену образуются эфиры несуществующего
в свободном состоянии винилового спирта CH2=CH-OH - сложные
виниловые эфиры.
Важнейший в этом ряду винилацетат - эфир винилового спирта и уксусной
кислоты. Его получают при пропускании смеси паров уксусной кислоты и ацетилена
над ацетатами кадмия и цинка при 180-220оС:
СН3-СООН + СН=СН → СН3-СО-О-СН=СН2
Химические свойства
эфир алифатичекий карбоновый кислота
Полярность связей в молекуле сложного эфира подобна полярности связи в
карбоновых кислотах.
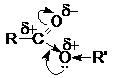
Основное отличие от карбоновых кислот - отсутствие подвижного протона,
вместо него находится углеводородный остаток. Электрофильный центр находится на
карбонильном и алкильном углеродном атоме. В то же время карбонильный кислород
обладает основностью.
Важнейшей из реакций ацилирования является гидролиз сложных эфиров с
образованием спирта и карбоновой кислоты:
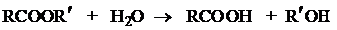
Реакция осуществляется как в кислой, так и в щелочной среде.
. Кислотный гидролиз:
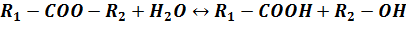
Кислотно-катализируемый гидролиз сложных эфиров - реакция, обратная
этерификации, протекает по тому же самому механизму, что и реакция
этерификации:
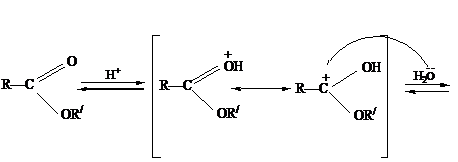

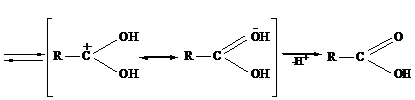
Нуклеофилом в этой реакции является вода. Смещение равновесия в сторону
образования спирта и кислоты обеспечивается добавлением избытка воды.
2. Щелочной гидролиз:
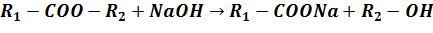
Щелочной гидролиз необратим, в процессе реакции на моль эфира расходуется
моль щелочи, т.е. щелочь в этой реакции выступает в качестве расходуемого
реагента, а не катализатора:
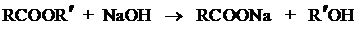
Гидролиз сложных эфиров в щелочной среде протекает по бимолекулярному
ацильному механизму через стадию образования тетраэдрического интермедиата (I).
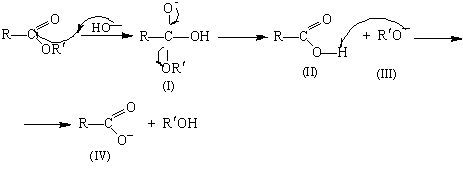
Необратимость щелочного гидролиза обеспечивается практически необратимым
кислотно-основным взаимодействием карбоновой кислоты (II) и алкоксид-иона (III). Образовавшийся анион карбоновой кислоты (IV) сам является довольно сильным нуклеофилом и потому не
подвергается нуклеофильной атаке.
3. Переэтерификация - алкоголиз:
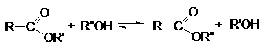
Реакция катализируется кислотами или основаниями.

4. Переэтерификация - ацидолиз:
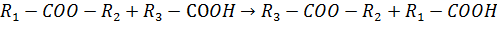
5. Восстановление:
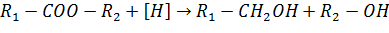
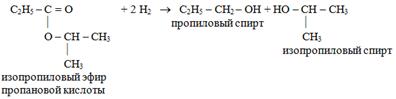
6. Образование амидов (аммонолиз):
При взаимодействии с аммиаком, а также с первичными или вторичными
аминами, сложные эфиры превращаются в амиды кислот и спирты:
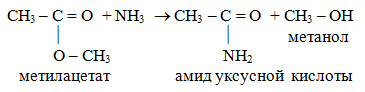
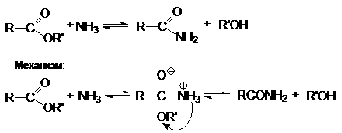
Объектами нуклеофильной атаки могут быть ацильный или алкильный углерод.
В то же время кислотность водородных атомов при a-углеродном атоме радикала кислоты обусловливает
склонность сложность эфиров к реакции конденсации.
7. Сложноэфирная конденсация:
При конденсации двух молекул сложного эфира в присутствии основного
катализатора образуются эфиры β-оксокислот.
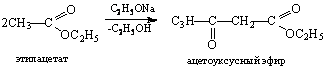
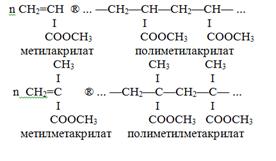
8. Полимеризация эфиров непредельных кислот:
Эфиры непредельных кислот легко полимеризуются с разрывом двойной связи.
Применение
Сложные эфиры используются как растворители, экстрагенты, ацилирующие
средства, инсектициды, гербициды, флотореагенты, пластификаторы, присадки к
маслам, являются промежуточными подуктами в органическим синтезе и т.д.
Полиэфиры используются для производства синтетических смол, пластмасс,
органического стекла, эластомеров, фармацевтических препаратов и медцинских
материалов.
Сложные эфиры дикарбоновых кислот нашли широкое применение в качестве
основ и компонентов авиационных синтетических масел и гидравлических жидкостей.
Сложные эфиры дикарбоновых кислот применяют также в качестве гидротормозных
жидкостей, белых масел для текстильной промышленности, компонентов для
различных ответственных консистентных смазок и приборных масел, работающих в
широком диапазоне температур - от +100...200 до -40...-60 С.
Воски как растительные, так и животные представляют собой в основном
сложные эфиры высших карбононовых кислот и высших одноатомных спиртов. Так,
например, в состав пчелиного воска входит эфир пальмитиновой кислоты и
мирицилового спирта С15Н31-СО-ОС30Н61.
Воски образуют защитную смазку на коже человека и животных и предохраняют
растения от высыхания. Они применяются в фармацевтической и парфюмерной
промышленности при изготовлении кремов и мазей. Примером служит цетиловый эфир
пальмитиновой кислоты (цетин) - главный компонент спермацета. Спермацет
выделяется из жира, содержащегося в полостях черепной коробки кашалотов. Другим
примером является мелиссиловый эфир пальмитиновой кислоты - компонент пчелиного
воска.
В организме человека жиры играют роль структурного компонента клеток или
запасного вещества («жировое депо»). Их энергетическая ценность примерно вдвое
больше, чем белков или углеводов. Однако повышенный уровень триацилглицеринов в
крови является одним из дополнительных факторов риска развития ишемической
болезни сердца.
Твердые триацилглицерины называют жирами, жидкие - маслами.
В промышленности пластических масс большое значение имеют эфиры
непредельных кислот - акриловой и метакриловой. Образующиеся полимеры бесцветны
и прозрачны. Полиметилакрилат используют для производства пленок и листов, в
качестве клея (для изготовления без осколочного стекла триплекс), а также в
производстве искусственной кожи. Из полиметилметакрилата готовят исключительно
ценный синтетический материал - органическое стекло (плексиглас). Последнее превосходит
силикатное стекло по прозрачности и по способность пропускать УФ-лучи. Его
используют в машино- и приборостроении, при изготовлении различных бытовых и
санитарных предметов, посуды, украшений, часовых стекол. Благодаря
физиологической индифферентности полиметилметакрилат нашел применение для
изготовления зубных протезов и т.п.
Токсическое действие
Выраженные наркотические свойства сложных эфиров связывают с действием
целой молекулы. В организме под влиянием ферментов (различных эстераз) сложные
эфиры гидролизуются, поэтому характер их токсического действия в значительной
степени зависит от образующихся в процессе гидролиза кислот, в меньшей степени
от спирта. Характер, место и сила действия зависит от скорости гидролиза.
Эфиры, при гидролизе которых образуются сильные кислоты (они гидролизуются
быстро и освобождают большое количество ионов водорода), раздражают
преимущественно слизистые оболочки дыхательных путей. Типичным примером служат
сложные эфиры галогенозамещенных кислот (хлормуравьиной или хлоругольной,
галогеноуксусных). Некоторые из этих соединений обладают и высокой общей
токсичностью, обусловленной токсичностью продуктов распада. С другой стороны,
сложные эфиры жирных кислот обладают лишь слабыми раздражающими свойствами.
Вследствие высокого коэффициента распределения паров накопление в организме до
высоких концентраций при вдыхании сложных эфиров происходит довольно медленно,
что и обуславливает слабый наркотический эффект. Поэтому опасность внезапных
острых отравлений не так велика как при вдыхании углеводородов. Сложные эфиры
кислот и непредельных спиртов обладают более выраженным раздражающими
свойствами: винилацетат более выраженным, чем этилацетат. Еще сильнее
становится раздражающий эффект при включении в спиртовую часть молекул сложных
эфиров галогенов. Наличие двойной связи в кислотном радикале, по-видимому,
меньше влияет на усиление раздражающих свойств. Особой токсичностью обладают
сложный эфир муравьиной кислоты и метиловые эфиры. Особенностью сложного эфира
этиленгликоля является образование в процессе метаболизма в организме щавелевой
кислоты.
Список литературы
1. И.Л. Кнунянц
<https://ru.wikipedia.org/wiki/%D0%9A%D0%BD%D1%83%D0%BD%D1%8F%D0%BD%D1%86,_%D0%98%D0%B2%D0%B0%D0%BD_%D0%9B%D1%8E%D0%B4%D0%B2%D0%B8%D0%B3%D0%BE%D0%B2%D0%B8%D1%87>,
Н.С. Зефиров
<https://ru.wikipedia.org/wiki/%D0%97%D0%B5%D1%84%D0%B8%D1%80%D0%BE%D0%B2,_%D0%9D%D0%B8%D0%BA%D0%BE%D0%BB%D0%B0%D0%B9_%D0%A1%D0%B5%D1%80%D0%B0%D1%84%D0%B8%D0%BC%D0%BE%D0%B2%D0%B8%D1%87>.
Химическая энциклопедия. М., Советская энциклопедия, 1999
. Фрейдлин Г.Н.
Алифатические дикарбоновые кислоты. М., Химия, 1978
. Томилов А.П.
Электрохимический синтез органических веществ. М., Наука, 1976
. Мельников Н.Н. Химия
пестицидов. М., Химия, 1968.
. Локтев С.М. Высшие
жирые кислоты. М., Наука, 1964
. Болотин И.М.,
Милосердов П.Н., Суржа Е.И. Синтетические жирные кислоты и продукты на их
основе. М., Химия, 1970
. Леенсон И.А.
Занимательная химия. М., Дрофа, 1996