Межмолекулярное взаимодействие полиэлектролитов в разбавленных растворах
Министерство
высшего и среднего специального образования Республики Узбекистан
Национальный
университет Узбекистана имени Мирзо Улугбека
5А
440405-Электрохимия
Диссертация
на соискание
академической степени магистра
Межмолекулярное
взаимодействие полиэлектролитов
в разбавленных растворах
Осербаева Альфия
Курбанбаевна
Научные руководители:
д.х.н. проф. Акбаров Х.И.,
к. х.н. Закирова Н.Т.
Ташкент-2010
оглавление
Введение
. Обзор литературы
.1 Интерполимерные комплексы
натрийкарбоксиметилцеллюлозы с азотсодержащими полиэлектролитами
.2 Взаимодействие в системах
сополимер-металл и полимер-металл-сополимер
. Экспериментальная часть
.1 Объекты исследования
.2 Методы исследования
. Полученные результаты и их
обсуждение
.1 Физико-химическое исследование
интерполимерных комплексов
.2 Термодинамических взаимодействие
в системах сополимер-ион металла и NаКМЦ-ион металла-сополимер
.3 Изучение полимер-металлических
взаимодействий в растворе фотометрическим методом
.4 ИК-спектроскопическое изучение
интерполимерных комплексов
.5 ИК-спектроскопическое изучение
двух и трехкомпонентных соединений на полимерной основе
Выводы
Литература
Введение
Актуальность работы.
Изучение процессов взаимодействия между комплементарными макромолекулами, сопровождающееся
образованием интерполимерных комплексов (ИПК), уже на протяжении нескольких
десятков лет неизменно является одной из наиболее актуальных задач химии
полимеров.
Обусловлено это тем, что ИПК обладают целым
набором уникальных физико-химических, коллоидных и механических свойств,
существенно отличающихся от свойств исходных полимерных реагентов, и
по-существу, представляют собой новый класс полимерных материалов,
перспективных для использования в различных областях медицины, биотехнологии,
мембранной технологии и т.п. С практической точки зрения реакции
комплексообразования широко применяется в гидрометаллургии для селективного
извлечения и концентрирования ионов редких и благородных металлов, для ионного
обмена в почве, создания высокоэффективных полимерных катализоторов, обладающих
высокой селективностью и работающих в мягких условиях. Координационные
соединения полимер-металл, аналогично металлоферментам, катализируют
окислительно-восстановительные реакции, сольволиз сложных эфиров, реакции декарбоксилирования
и разложения.
Реакции комплексообразования макромолекул с
ионами металлов это один из типов реакций внутримолекулярного сшивания. К
настоящему времени накоплен большой материал по изучению процессов между
катиону- анионогенными макромолекулами в водных растворах, приводящих к
образованию интерполимерных комплексов. Последние, избирательно связывающие
ионы переходных металлов, могут служить для создания полупроницаемых мембран и
в качестве сорбентов.
Особый интерес представляет исследование взаимодействия
ионов металлов с полимерами. Это позволяет не только установить закономерности
связывания макромолекула- ион металла, но и получить плёнки на их основе,
которые могут быть использованы в качестве ионоселективных мембран и сорбентов
для разделения и выделения ионов металлов. Эти проблемы непосредственно связаны
с применением таких композиционных материалов в биологии, медицине и в решении
экологических задач. Поэтому разработка интерполимерных, сополимер-
металлических композиционных материалов является весьма актуальной.
Целью магистерской
диссертации является исследование влияния строения полимерной цепи и
положения в ней функциональных групп, способных к комплексообразованию, на
физико-химические свойства интерполимерных комплексов и сополимер-металлических
комплексов. Для достижения поставленной цели были проведены следующие
исследования:
изучение образования интерполимерных комплексов
между Nа-
карбоксиметилцеллюлозой (Nа-КМЦ)
с декстраном и коллаген декстраном методами вискозиметрии, потенциометрии,
оптической плотности и электропроводности;
изучение образования тройных
полимер-металлических комплексов в системе Nа-КМЦ
- металл-сополимер;
установление механизма взаимодействия между
компонентами;
определение констант диссоциации, энергий
конформационного перехода, ионизации, электростатического взаимодействия,
полной энергии Гиббса;
определение степени превращения в зависимости от
рН раствора;
определение состава, константы устойчивости
образующихся комплексов;
Объектами исследования
явились декстран, Nа-КМЦ,
коллаген, сополимер ион металла
Научная новизна. Впервые
исследованы полимер- полимерные, сополимер- металлические и тройные
сополимер-металлические комплексы и рассчитаны константы диссоциации, энергии
конформационного перехода, ионизации, электростатического взаимодействия,
полной энергии Гиббса.
В магистерской диссертации исследован механизм
кооперативного взаимодействия в системах сополимер- металл и полимер-
металл-сополимер и показано образование сополимер-металлического и
интерполимер-металлического комплексов. Определен состав, область его
устойчивости, рассчитаны константы диссоциации и степень превращения в
зависимости от рН раствора.
Практическая значимость. Установлены
фундаментальные закономерности интерполимерного комплексообразования и
изучены системы сополимер-ион металла и полимер-металл-сополимер, что открывает
новые возможности научно- обоснованного подхода к решению проблемы получения
материалов с заранее заданными свойствами.
Полученные интерполимерные комплексы могут быть
применены в медицине в изготовлении гелей и мембран, предназначенных для
очистки и разделения а также полимер-металлических композиционных материалов с
повышенными физико-механическими свойствами.
Публикации. По
теме магистерской диссертации опубликованы 3 статьи и 5 тезисов докладов в
материалах ежегодных традиционных конференций профессорско-преподавательского
состава химического факультета НУУз им. Мирзо Улугбека, проходивших в 2008-2010
годах.
Методы исследования. Оптические
методы исследования, электрохимические методы, вискозиметрия,
потенциометрическое титрование.
1. Обзор литературы
.1 Интерполимерные комплексы
натрийкарбоксиметилцеллюлозы с азотсодержащими полиэлектролитами
Взаимодействия разнородных макромолекул,
приводящие к образованию ИПК, являются объектом интенсивных исследований на
протяжении последних десятилетий. К настоящему времени вышло достаточно большое
количество публикаций, посвященных этой проблеме, что свидетельствует о
важности этих систем для ряда производственных процессов, создания новых
медицинских препаратов, а также для моделирования сложных биохимических
процессов.
Полиэлектролитные комплексы широкого
распространены в живой природе. Поэтому изучение взаимодействия природных
полимеров или синтетических ионогенных полимеров в водных растворах
представляет несомненный интерес как с точки зрения моделирования реакций,
протекающих в живых системах, так и для практического применения их в
гидрометаллургии, медицине и фармакологии.
Авторами в работе [1]
рассмотрены свойства растворов смесей фиброина с Nа-КМЦ.
Полимерные компоненты растворяются в разных растворителях, поэтому следили за
изменением вязкости раствора фиброина в ДМФА при добавлении воды и водного
раствора Nа-КМЦ. Параметры
уравнения Джонса-Дола [2], характеризующие межионные
взаимодействия в растворе и структуроукрепляющее или структуроразрушающее
действие на растворитель, подтверждают наличие взаимодействий между
макромолекулами Nа-КМЦ и
белка разрушающее действие поликомплекса на структуру растворителя. Результаты
свидетельствуют об образовании возможного интерполимерного комплекса в данной
смеси, наряду с этим характерные результаты образования интерполимерного
комплекса получены при измерении вязкости (hотн),
оптической плотности (D)
и рН среды смесей этих растворов. В работе [3]
изучены свойства растворов смесей серицина с Na-карбоксиметилцеллюлозной
(Na-КМЦ). Результаты
исследования вискозиметрии, потенциометрии, спектрофотометрии позволяют судить
о том, что соотношение полимерных компонентов при взаимодействии между
функциональными группами Nа-КМЦ
(карбоксилат анионы, недиссоцированные СООН группы) и серицина (NH2,
СО -группы) возможны как электростатические взаимодействия, так и водородные
связи. Авторы работы делают вывод, что в системе Nа-КМЦ-
серицин возможны интерполимерные взаимодействия между компонентами за счет
образования Н-связей или электростатических взаимодействий проявляющиеся в ходе
кривых вязкости, потенциометрии, оптической плотности, двулучепреломления.
В статье [4,5] показана термодинамика взаимодействия
в разбавленных растворах смесей Nа-КМЦ-коллаген.
Термодинамические параметры свидетельствуют об усилении межмолекулярных
взаимодействий в водных растворах между Nа-КМЦ
и коллагеном и об образовании интерполимерных комплексов. Комплекс в системе Nа-КМЦ-коллаген
образуется в области рН ниже изоэлектрической точки (ИЭТ) коллаген (4,7) когда
его молекулы заряжены положительно, а макромолекулы Nа-КМЦ-
отрицательно, т.е. в области не слишком низких значений рН. Закономерности
интерполимерного комплексообразования Nа-КМЦ
с природными полиэлектролитами в основном, те же, как в случае синтетических
[6,7]. Характер изменения термодинамических параметров комплексообразования Nа-КМЦ
с протеинами и синтетическими полиэлектролитами идентичен и сопровождается отрицательными
изменениями энергии Гиббса, энтропии и экзотермическим эффектом: при
комплексообразовании система переходит в более упорядоченное состояние,
стабилизированное водородными связями, но и интенсивность взаимодействия
макромолекул в этих поликомплексах различна и свойства интерполимерных
комплексов отличаются друг от друга [8].
В работе [9] изучена термодинамика
комплементарного взаимодействия Nа-КМЦ-СПЛ
(гидрохлорид N,N-
(диметиламинометакрилат -акриламид). Термодинамические исследования показали образование
устойчивых ИПК в системе с нарушенной комплементарностью взаимодействующих
макромолекул. Установлено, что чем больше содержание активных групп во
взаимодействующих макромолекулах, тем больше наблюдается образование более
устойчивых комплексов.
В статье А.С. Тураева [10] приведены способы
химической сшивки Nа-КМЦ с
целью получения на ее основе сильнонабухающих гелей. Гели на основе ИПК
перспективны в связи с их способностью к избирательной сорбции ионов металлов и
некоторых других веществ. Так, в работе [11] выявлены особенности
комплексообразования полиэлектролита природного происхождения (Nа-КМЦ)
с олигомерами МФС аммониевым ионеном на основе дихлоргидрина с
гексаметилендиамином и ионогенным олигомером гуанильгидразоном формальдегида.
Установлено влияние структур взаимодействующих компонентов на структуру
конечного продукта. Показана возможность регулирования структуры и свойств
интерполимерных комплексов на основе КМЦ с N-содержащими
олигомерами и полимерами. Исследованы некоторые электрофизические свойства.
Обнаружено разрушение поликомплекса Nа-КМЦ-полиэтиленимин
при высоких концентрациях хлорида натрия [12]. Показано, что высаливающее
действие соли приводит к перераспределению макромолекул полиэтиленамина между
цепями, составляющими привитой сополимер. Как известно, смешение двух растворов
полимеров в общем растворителе приводит либо к образованию гомогенного
однофазного раствора, либо, чаще всего, фазовому разделению. Разделение может
быть обусловлено несовместимостью полимеров. При этом образуются две фазы, в
каждой из которых находятся преимущественно один из полимерных компонентов.
Другой тип разделение фаз - следствие комплексообразования, взаимного
притяжения разнородных макромолекул. В этом случае полимеры осаждаются
совместно, так что соотношение их в фазе осадке часто оказывается
стехиометрическим.
В работах [13,14] авторы изучали влияние
дисперсных наполнителей на свойства интерполимерного композиционного материала
(ИПКМ). В статье приводятся результаты физико-механических, химических исследований
новых полимерных композитов для установления взаимосвязи их со строением и его
свойствами.
В работе [15,16] изучали антикоагулянтные
свойства коллаген-гепаринового комплекса. Целью данной работы было изучение
антикоагулентных свойств этого комплекса. Антикоагулянтные свойства комплекса
были изучены в опытах in
Vitro и in
Vivo методом трамбо
эластографии, который достаточно полно характеризует свертывающую систему
плазмы и крови. В этих опытах было установлено, что гепарин, выделяющийся из
комплекса коллагена при его инкубации в плазме, активно влияет на процесс
свертывания фибрина. Влияние его возрастает с увеличением количества гепарина в
комплексе. Однако известно, что антикоагулентный эффект чистого гепарина
кратковременный.
В работе [17] рассмотрены анафилактогенные
свойства продуктов полного растворения коллагена. Задачей этой работы являлось
изучение анафилактогенных свойств применяемых продуктов полного растворения
коллагена, полученного из дермы крупного рогатого скота. По результатам данной
работы сделаны выводы, что продукты полного щелочно-кислотного растворения
коллагена в виде растворов, осажденных волокон и коллаген-гепаринового
комплекса обладают крайне слабыми анафилактическими свойствами, которые не
препятствуют применению коллагена в клинике.
В работе [18] изучали изменения коллагена в
процессе его полного растворения и реконструкции. Проведенные морфологические и
биохимические исследования показали, что предварительная щелочно- солевая
обработка приводит с разрушению основного цементирующего вещества, в частности
кислых мукополисахаридов, дезорганизации структурных элементов коллагена,
нарушения межмакромолекулярных связей, что делает возможным его полное
растворения в слабой уксусной кислоте.
Несмотря на интенсивную обработку щелочью, трех
спиральная молекула коллагена сохраняется, что позволяет получить из раствора
коллагеновые материалы, обладающие близкими к нативному коллагену свойствами
для использования их в пластической хирургии.
В работе [19] изучены антибактериальные свойства
комплекса коллагена с антибиотиками in
Vitro.
Имеется много работ, посвященных связыванию
некоторых полимеров с лекарственными веществами, в частности с антибиотиками.
Кроме того, известно, что антибиотики в организме связываются с белками плазмы
крови тканей. Такое сочетание антибиотиков с полимерами и белками организма
осуществляется благодаря взаимодействию и активных функциональных групп. В
структуре биополимера- коллагена имеются такие функциональные группы (NH2,
COOH, OH)
которые могут обусловливать прочную связь с лекарственными соединениями.
В статье [20] показана термодинамика
взаимодействия в разбавленных растворах смесей натрий карбоксиметилцеллюлозы и
коллагена. Термодинамические параметры свидетельствуют об усилении
межмакромолекуярных взаимодействий в водных растворах между Nа-КМЦ/коллаген
и об образовании интерполимерных комплексов. Комплекс в системе Nа-КМЦ/коллаген
образуется в области рН ниже
изоэлектрической точки (И.ЭТ) коллагена (4,7), когда его молекулы заряжены
положительно, а макромолекулы Nа-КМЦ
- отрицательно, т.е. в области не слишком низких значений рН.
Закономерности интерполимерного
комплексообразования Nа-КМЦ
с природными полиэлектролитами- протеинами, в основном, те же, как в случае
синтетических [21]. Характер изменения термодинамических параметров
комплексообразования Nа-КМЦ
с протеинами и синтетическими полиэлектролитами идентичен и сопровождается
отрицательными изменениями энергии Гиббса, энтропии и экзотермическими эффектом
при комплексооброзовании система переходит в более упорядоченное состояние,
стабилизированное водородными связями, по интенсивность взаимодействия
макромолекул в этих поликомплексах различна и свойства интерполимерных
комплексов отличаются друг от друга [22- 24].
Методами [25] динамического рассеяния света,
просвечивающей электронной микроскопии, атомно-силовой микроскопии и
флуоресцентной спектроскопии исследован процесс агрегации в водной среде
конъюгатов, представляющих собой образцы гидрофобно модифицированного
пространственно-затрудненными фенолами декстрана. Установлено, что в растворах
декстрана и конъюгатов на его основе присутствуют индивидуальные молекулы и их
агрегаты. Концентрация, размер и форма агрегатов, а также число агрегации
определяются степенью замещения гликозидных групп декстрана. Показано, что при
увеличении степени замещения молекул декстрана критическая концентрация
агрегирования конъюгатов уменьшается
В работах [26,27], для исследования строения
декстрана был применен термогравиметрический метод. На термограммах всех
исследованных препаратов декстрана обнаруживаются эндотермические пики в
области 130 - 310° С. Пик в области 200° характерен для декстранов, в
макромолекулах которых содержатся в основном а- 1, 6- гликозидные связи, пик в
области 245° наблюдался на термограммах декстранов, содержащих значительное
количество а -1,3-гликозидных связей. Строение макромолекул декстрана оказывает
влияние и на характер сорбции полимером паров воды [28,29].
Количество воды, сорбированное образцами
декстрана, содержащими наряду с а-1,6-гликозидными связями значительное число
а-1,3- и а-1,4- связей, монотонно возрастало при увеличении относительной
упругости паров воды. В случае препаратов с высоким содержанием
а-1,6-гликозидных связей, количество сорбированной воды возрастало при
увеличении относительной упругости паров воды до 75- 85%, а затем снижалось.
Авторы этих работ полагают, что описанное явление связано с кристаллизацией
декстрана. Кристаллизоваться могут, по-видимому, препараты декстрана,
макромолекулы которых слабо разветвлены, а ответвления состоят преимущественно
из одного- двух ангидро -D-
глюкопиранозных звеньев. Такой препарат декстрана изучен в работе [30], где с
помощью оригинального метода определения длины боковых цепей было установлено,
что в исследованном препарате декстрана приблизительно 40% боковых ответвлений
содержали один остаток глюкозы, 45% - два остатка и только 15% имели более
длинную цепь. При исследовании 8 различных препаратов декстрана
рентгенографическим методом было установлено [31], что все изученные полимеры
находятся в аморфном состоянии.
Предметом исследования ряда работ, выполненных в
последнее время, явилось взаимодействие макромолекул декстрана с растворителем.
В работе [32] показано, что макромолекулы некоторых препаратов нативных
декстранов образуют структурные ассоциаты с растворителем. Возможность
образования ассоциатов рассмотрена в указанной работе с учетом спиральной
структуры нативного декстрана, стабилизированной внутримолекулярными
водородными связями, и характера водородных связей, образующихся в растворе.
Присутствие в водных растворах декстрана других веществ влияет на форму
макромолекул декстрана и на вязкость растворов. Показано, что в водных
растворах мочевины, глюкозы и в концентрированных растворах солей степень
асимметрии макромолекул нативного декстрана больше, а в водно-метанольном
растворе - меньше, чем в воде [33] .
Характеристическая вязкость водных растворов
гидролизованного декстрана при добавлении в раствор КSCN
и СаСI2 увеличивается, а
при добавлении LiCI
и KCI - уменьшается [34]
В работе [35] показано, что характеристическая вязкость водных растворов
декстрана зависит от pH
раствора. Авторы предполагают, что изменение вязкости в этом случае обусловлено
изменением характера и числа внутримолекулярных водородных связей. Изучению связи
между степенью разветвленности макромолекул декстранов и других природных
полимеров и вязкостью их растворов посвящены работы [36,37]. Работе [38]
исследовано влияние природы растворителя (вода, формамид, метанол - вода,
диметилформамид - вода), молекулярного веса декстрана (Мn
= 4100 - 32 000) и температуры
на характеристическую вязкость растворов. Различные аспекты использования
вискозиметрического метода для определения молекулярного веса декстрана
рассмотрены также в работах [38-41].
Таким образом, обзор литературных данных
показывает актуальность и практическую значимость исследования интерполимерных
комплексов. Работы, посвященные изучению полимер-полимерных взаимодействий в
системах гибкоцепный полимер-жесткоцепный полимер, а также сополимер-металл на
основе Nа-КМЦ недостаточны,
между тем продукты их взаимодействия могут обладать ценными свойствами. Такие
исследования особый интерес представляют и с теоретической точки зрения, так
как закономерности интерполимерного комплексообразования в различных
полимер-полимерных системах могут сильно отличаться.
.2
Взаимодействие
в системах сополимер-металл и полимер-металл-сополимер
Полимер металлические комплексы могут быть
получены различными путями: 1) в результате внутри- или межмолекулярной
"сшивки"; 2) при взаимодействии полимерного лиганда со стабильными
комплексами, в котором центральный ион металла замаскирован низкомолекулярным
лигандом; 3) полимеризацией пар мономер-ионы металлов; 4) путем включения ионов
металлов в сетку полимера и т. д.
Обычно связь между ионом металла и полимерным
лигандом осуществляется посредством донорно-акцепторного взаимодействия с
образованием координационной связи (хелатные комплексы) или замещением протона
лиганда ионом металла с образованием ионной связи. Ионы металлов являются
акцепторами; атомы -O, -N, -S, -F, -Cl полимерной цепи, предоставляющие пару
электронов для образования связи, являются донорами. В низкомолекулярных
комплексных соединениях обычно координационное число металла равно 2; 4 или 6.
В случае макромолекулярных лигандов могут образовываться координационные центры
состава 1:1; 1:2; 1:3 или 1:4. Свободные вакансии координационной сферы ионов
переходных металлов занимают молекулы растворителя или других низкомолекулярных
веществ. Изменение конформации полимерного лиганда в процессе
комплексообразования может значительно влиять на результаты расчетов
координационного числа иона металла и константы устойчивости комплексов.
Характерной особенностью комплексов
полимер-металл в отличие от комплексов низкомолекулярный лиганд-металл является
близость всех последовательных констант комплексообразования. Это связано с
высокой локальной плотностью активных центров взаимодействия в полимерных
цепях, т.е. "полимерный эффект" может играть значительную роль в
образовании комплексов полимер-ион металла.
Комплексы полимер-ион металла в воде имеют
компактную структуру, стабилизированную внутри- или межцепными координационными
"сшивками", которые существенно изменяют размер клубка полилиганда.
Методом потенциометрического титрования
исследован процесс связывания ионов Al3+, Cu2+, Co2+
с макромолекулами карбоксиметилцеллюлозы (КМЦ) [42]. Показано, что в широком
диапазоне рН среды происходит электростатическое связывание ионов металлов.
Методом вискозиметрии установлено, что с увеличением концентрации исходного
раствора КМЦ и в присутствии многоосновных кислот эффективность
межмакромолекулярного сшивания КМЦ возрастает. Таким образом, в широком
диапазоне слабокислых, нейтральных и щелочных сред происходит сшивания КМЦ с
ионами Al3+, Cu2+, Co2+ посредствам ионных
связей.
Будтовым Т.В. и другими [43] было проведено
исследование сверхнабухающего гидрогеля на основе полиакрилата натрия,
подшитого аминовым эфиром КМЦ, в растворе солей 1-валентных металлов и
обнаружен эффект концентрирования солевого раствора вне набухшего образца
гидрогеля.
Обратимые интерполиэлектролитные реакции,
приводящие к образованию нестехиометричных полиэлектролитных комплексов
(Н-ПЭК), могут найти применение для создания самых разнообразных функциональных
макромолекулярных систем [44]. Например, эти полиэлектролитные комплексы
способны прочно связывать ионы переходных металлов, такие как Cu2+,
Fe2+, Fe3+, Ni2+, Co2+ и другие.
Образующиеся при этом тройные полимер-металлические комплексы могут быть как
стехиометричными полиэлектролитными комплексами (С-ПЭК), так и водорастворимыми
нестехиометричными и превращаться друг в друга.
Изучено [45] комплексообразование и исследована
каталазная активность (КА) тройного полимер-металлического комплекса Fe+3-гелеобразующая
полиакриловая кислота (ГПАК)- этилендиамин (ЭДА). Комплексы Fe+3-
ЭДА и Fe+3-ГПАК разлагают пероксид водорода с малыми скоростями. Как
и в предыдущем случае только комбинация металла и обоих лигандов, смешанных в
последовательности Fe+3, ГПАК, ЭДА очень активна. Активность
комплекса FeCl3-ГПАК-ЭДА на порядок выше активности комплекса FeCl3-ПАК-ГПЭИ.
Проявление высокой каталазной активности системы FeCl3-ГПАК-ЭДА
обусловлено образованием смешанного комплекса, включающего координационное
связанную молекулу пероксида водорода. Не исключено, что роль ЭДА заключается
не только в образовании смешанного комплекса, но и в активации молекул
пероксида водорода в зоне реакции путем образования комплекса с пероксидом.
Однако активность комплекса FeCl3-ГПАК-ЭДА при хранении уменьшается.
Стабилизирующие свойства ГПЭИ выше, чем ЭДА. Повышение стабильности нативного
фермента (каталазы) при его иммобилизации на ГПЭИ наблюдалось нами ранее.
В работе [46] изучено взаимодействие гели
интерполимерного комплекса на основе NaКМЦ
с ионами металлов. Тройной полимер -металлический комплекс (ТПМК) может быть
получен путем добавления иона меди в систему полиакриловая кислота
-полиэтиленимин. Введение иона металла может разрушать полуионный комплекс
из-за конкуренции низкомолекулярных ионов с полимерными реагентами. Однако,
неподеленая пара электронов на атоме азота поиэтиленимина способна образовывать
донорную связь с координационно - ненасыщенными металлами. Таким образом,
сложное поведение односолевых растворов привитых сополимеров и их
поликомплексов следствие как реакции поликомплексообразования между
макромолекулярными компонентами, так и высаливающего действия солей.
2. Экспериментальная часть
.1 Объекты исследования
Объектами исследования служили коллаген,
декстран натрийкарбоксиметилцеллюлоза (Nа-КМЦ),
водорастворимые сополимер и диметиламиноэтилметакрилат-акриламид (ДМАЭМА-АА) и
ион металла.
Декстран - групповое название полисахаридов,
получаемых методом микробиологического синтеза, оснавная
молекулярная цепь которых состоит из ангидро- D-
глюкопираноззных звеньев, соединенных преимущественно a-1,-
6 - гликозидными связми.
Структура декстрана:
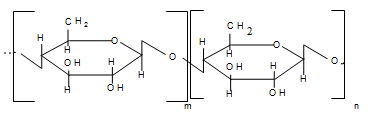
Кроме a-1,6
- гликозидных связей в макромолекулах разных преператов декстрана может
содержаться различное количество а-1,2-, а-1,3- или а-1,4- гликозидных связей,
при помощи которых обычно осуществляется присоединение к основной цепи боковых
цепей. Получены декстраны, молекулы которых являются практически
неразвлетвленными, а элементарные звенья на 95% соединены а-1,6- гликозидными
связами. Декстран получают при культивировании микроорганизмов Leuconostoc
mesenteroides, Leuconostoc
dextranicum, Streptobacterium
dextranicum и др. в среде,
содержащей сахарозу или другие углеводы, в состав которых входят ангидро- D
-глюкопиранозные звенья, в том числе и низкомолекулярный декстран. Продуктом
микробиологического синтеза является так называемый нативный декстран.
Широкую известность полисахарид декстран
приобрел в связи с тем, что водные растворы некоторых препаратов этого полимера
с молекулярным весом 35-70 тыс. и низкой степенью разветвленности являются
эффективными заменителями плазмы крови. Преимущество декстрана перед
карбоцепными полимерами (поливинилпирролидон, поливиниловый спирт), также
применяющимися для этой цели, заключается в том, что декстран в отличие от
карбоцепных полимеров постепенно гидролизуется в организме ферментами. Это
исключает опасность накопления полимера в органах макроорганизма. Очень важным
оказалось использование декстрана в качестве исходного вещества при получении
сефадексов, широко применяющихся в гель-хроматографии. Декстран и его
производные находят все возрастающее применение и для других целей.
Микробиологический синтез, строение,
биологические свойства и применение в медицине этого полисахарида подробно
описаны в обзорах и монографиях. Однако отсутствуют систематические обзоры, в
которых рассматривались бы физико-химические свойства декстрана, синтез и
свойства его производных. Данный обзор посвящен этим проблемам и охватывает
работы, опубликованные в основном в последнее десятилетие.
В качестве второго компонента использовали
коллаген. Коллаген является основным фибриллярным белком соединительной ткани,
выполняющей важнейшие функции организма. Молекулярная масса коллагена имеет
трехспиральную форму. Коллаген растворяется в растворе уксусной кислоты и в
этом растворе имеет рН в интервале 2,5- 3,5.
Nа-КМЦ со степенью
замещения 0,80 и степенью полимеризации 450 Наманганского производства очищали
переосаждением в системе вода-этиловый спирт.
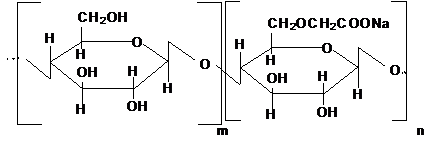
В промышленности Nа-КМЦ
получают взаимодействием щелочной целлюлозы с монохлоруксусной кислотой или ее
натриевой солью в присутствии NaOH.
Она находит широкое применение в нефтяной, текстильной, пищевой,
фармацевтической технологиях, в производстве детергентов и т.д. как
стабилизирующее, загущаюшее, клеящее, пленкообразующее и т.п. вещество. Эта
соль, хорошо растворяется в воде при всех температурах. Nа-КМЦ
является весьма гигроскопичным веществом. По данным, при 293 К в обычных
лабораторных условиях этот продукт содержит около 11,5% влаги. Вязкость 1%-ного
раствора Nа-КМЦ имеет
максимум в пределах рН от 6 до 9 . При рН ниже 6 она быстро падает, что
является следствием постепенного выпадения в осадок свободной КМЦ, полностью
заканчивающееся при рН 2,5. При значениях
рН выше 9 вязкость раствора также начинает уменьшаться: сначала медленно, потом
более быстро, когда величина рН достигает 11,5%. Весьма значительное уменьшение
вязкости в сильно щелочной области не является, однако, следствием осаждения
КМЦ, т.к. даже при рН=13 она полностью остается в растворенном состоянии.
Указанные изменения вязкости обратимы и
начальная вязкость раствора может быть вновь восстановлена до своей
максимальной величины рН в пределах от 6 до 9. Таким образом, здесь имеет место
определенное специфическое влияние щелочи на вязкость.
В настоящее время полагают, что такое влияние,
по-видимому, объясняется изменением конформации молекул КМЦ в растворе под
влиянием электролита. В отсутствии электролита ионизированные группы полимерной
цепи отталкиваются друг от друга, в результате чего макромолекула становится
более выпрямленной. При добавлении электролита вследствие его экранирующего
действия отталкивание между соседними ионизированными группами полимерной цепи
становится меньше и макромолекула приобретает более свернутую конформация.
Температура также оказывает сильное влияние на
вязкость растворов Nа-КМЦ. Если
растворы нагреть, а затем вновь
охладить, то конечная вязкость раствора Nа-КМЦ,
определенная при комнатной температуре составляет менее половины начальной
величины.
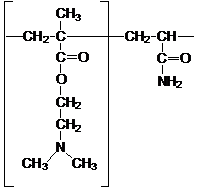
Водорастворимые сополимер и
диметиламиноэтилметакрилат-акриламид (ДМАЭМА·АА), синтезированы на кафедре
физической и коллоидной химии НУУз.
.2 Методы исследования
полимерный комплексообразование
раствор фотометрический
Оптическую плотность
растворов измеряли на приборе ФЭК-56. Экспериментально определяли оптимальную
длину волны и диаметр кюветы, исходя из максимального светопропускания (d=5,085).
Вискозиметрические исследования
проводили при 20оС; 25оС; 30оС на капиллярном
вискозиметре типа Убеллоде (длина капилляра 9,8 см; объем шарика 2см3;
расстояние, соответствующее началу и концу истечения раствора в шарике 1,5 см).
Электропроводность
измеряли на мосту Кольрауша при помощи платинового электрода.
Потенциометрическое титрование
проводили на рН-метре марки "Иономер универсальный ЭВ-74" в
термостатированной ячейке. Предварительно прибор калибровали по буферным
растворам с рН 1,68 и 9,18. Перемешивание осуществляли с помощью магнитной
мешалки. Исходная концентрация растворов 0,01 моль/л. При титровании использовали
0,01н НСl и КОН.
На основании кривых потенциометрического
титрования раствором КОН (HCl)
строили дифференциалную кривую титрования в координатах DрН/DV=¦(V)
и находили степень диссоциации a по максимальной точке
дифференциальной кривой, которую принимали за точку полной диссоциации a=1
и далее распределяя отрезок a=1 на 10 равных частей на
графике рН=¦(V)
находили рН. Используя найденные рН рассчитывали значения рК по формулам
рК=рН-lg 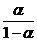
когда рН увеличиваеться (как при
титровании КОН);
рК=рН+lg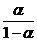
когда рН уменьшается (как при
титровании НСl).
По рассчитанным значениям рК строили
график зависимости
рК=¦(a).
Для нахождения значений pHтеор
строили график зависимости
рН=¦(lg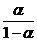 ),
),
откуда находили рНтеор
экстраполяцией экспериментальных данных. По данным рНтеор
рассчитывали рКтеор по формуле
рКтеор= рНтеор
± lg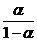
На графике зависимости рК=¦(a) обозначали значение рКтеор,
рассчитанные по найденным значением рНтеор и далее определяли DрКконф., DрКэл и DрКо и по Зимму и
Райсу рассчитывали изменение средней свободной энергии системы при
комплексообразовании.
DG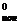 =2,303 ×RT DрКо
=2,303 ×RT DрКо
DG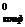 = 2,303×RT DрКконф
= 2,303×RT DрКконф
DG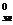 = 2,303×RT DрКэл
= 2,303×RT DрКэл
DG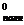 =DG
=DG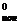 + DG
+ DG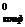 + DG
+ DG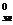
ИК-спектры поглощения
соединений регистрировали в области 400-4000 см-1 на
спектрофотометре Avatаr System 360 FT-IR и Protеgе 460 Magna-IR technology фирмы
"Nicolet Instument Corparation"
(США), используя образцы в виде таблеток с KBr диаметром 7
мм и с разрешением-4 см-1 .
Степень превращения в реакции
между полиэлектролитами q определяли
как долю функциональных групп, связанных солевыми связями, от общей
концентрации функциональных групп любого компонента
q
= Ск / Со
где Ск- концентрация
функциональных групп, образующих солевые связи, моль/л; Со- исходная
концентрация любого полиэлектролита, моль/л.
Из кривой потенциометрического
титрования смеси слабой поликислоты и соли полиоснования рассчитывали q при некоторых значениях рН
раствора по формуле
Ск = qСо = 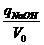 +[H+]-[H+]пк
+[H+]-[H+]пк
где qNаОН- количество
введенной щелочи, моль; Vо- объем
реакционной смеси, л; [H+]-
концентрация протонов в растворе, моль/л; [H+]пк-
концентрация протонов в растворе, создаваемая непрореагировавшей поликислотой,
моль/л.
Поскольку [H+]пк
не поддается экспериментальному определению, он может быть рассчитан по формуле
[H+]пк =
в предположении, что диссоциация
полимерной кислоты описывается характеристической константой диссоциации Кхар.пк; такое
допущение справедливо при рН £
рНпк водного
раствора поликислоты той же концентрации.
Для реакции между слабым
полиоснованием и солью поликислоты, протекающей в щелочной среде, q определяется по формуле
Ск = qСо= 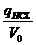 +[OH-]-[OH-]по
+[OH-]-[OH-]по
где qНСl -
количество введенной кислоты, моль; [OH-]-
концентрация гидроксильных ионов в реакционной смеси, моль/л; [OH-]по-
концентрация гидроксильных ионов, создаваемая непрореагировавшим основанием,
моль/л и рассчитываемая по формуле
[OH-]по=
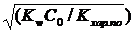
(здесь Кv-ионное
произведение воды); Кхар.по- характеристическая кислотная константа
ионозации полиоснования; такое допущение справедливо при рОН ³ рОНпо. раствора
полиоснования той же концентрации.
3. Полученные результаты и их
обсуждение
.1 Физико-химическое исследование
интерполимерных комплексов
Интерес к полимерным комплексам
связан с тем, что взаимодействие комлементарных структур и продукты их
ассоциации играют исключительно важную роль в живых организмах. Полимер-полимер
комплексы, образующиеся в результате реакции между функциональными группами
макромолекул и можно охарактеризовать в качестве новых полимерных веществ,
обладающих рядом ценных физико-химических свойств и имеющих определенный
химический состав, молекулярную массу и гидродинамические параметры.
В связи с вышесказанным,
представляет большой научный и практический интерес изучение
комплексообразования Nа-КМЦ и коллаген с декстраном. На
рис.1,2. приведена зависимость оптической плотности раствора от соотношения
компонентов Nа-КМЦ/декстран
1,0:3,0 и
коллаген/декстран соотношение 1,0:1,0; кривая оптической плотности проходит
через максимум
[47].
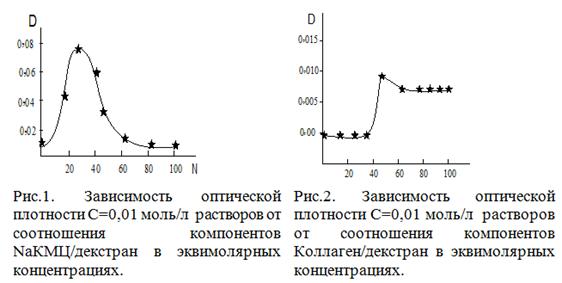
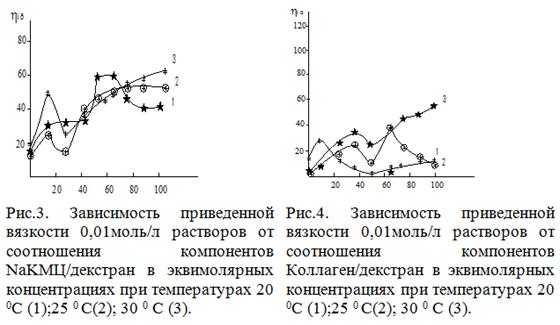
Вискозометрические исследования
растворов смесей Nа-КМЦ/ декстран и коллаген /декстран
показали, что кривые вязкости и электропроводности в
зависимости от состава компонента проходят через минимум при соотношениях Nа-КМЦ
/декстран = 1,0:3,0 коллаген/ декстран = 1,0:1,0 (рис.3,4)
Интенсивность этих связей зависит от
ряда факторов, главным из которых является рН раствора. В процессе
комплексообразования в системе Nа-КМЦ/декстран наблюдается снижение
рН среды при соотношениях Nа-КМЦ/декстран = 1,0: 3,0;
коллаген/декстран =1,0:1,0.
Методом рис.5.
потенциометрического
титрования исследовано влияние рН среды на устойчивость полимер-полимер
комплексов эквимольного соотношения. Кривая титрования имеет плавный ход в
интервалах рН для систем Nа-КМЦ/декстран рН от 3,2 до 8,3,
коллаген/декстран рН от 4,2 до 6,7; где образовавшийся полимер-полимер комплекс
является устойчивым.
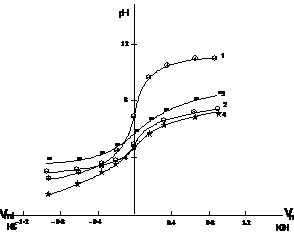
Рис.5. Кривые
потенциометрического титрования: 1. NаКМЦ; 2. коллаген;
3.
NаКМЦ/декстран;
4.
коллаген/декстран (С=0,01 моль/л)
На основе кривых
потенциометрического титрования исходного полимерного компонента и комплекса на
его основе растворами 0,01 н НСI и 0,01 н КОН рассчитаны значения рК
в зависимости от степени ионизации. По методу Зимма и Райса рассчитаны значения
энергии ионизации ∆Gион, электростатической составляющей
энергии Гиббса ∆Gэл, энергии конформационного перехода ∆Gконф
и полной энеогии Гиббса при комплексообразовании.
Из таблиц 1-2 видно, что ∆Gион,
∆Gэл и ∆Gконф для смеси Nа-КМЦ/декстран,
коллаген/декстран принимают большие отрицательные значения, что также является
свидетельством образования полимер-полимер комплекса.
Таблица 1. Значения
констант диссоциации и энергий конформационного
перехода, ионизации, электростатического взаимодействия и полной энергии
Гиббса при ионизации растворов Nа-КМЦ, коллаген и
поликомплекса на их основе раствором 0,01 н НСI)
|
Образец
|
DрКконф.
|
-DGконф., кДж/моль
|
DрКэл.,
кДж/моль
|
-DGэл., кДж/моль
|
рК 0
|
-DG0, кДж/моль
|
-DGпол, кДж/моль
|
|
NaКМЦ
|
0,90
|
0,65
|
0,18
|
0,98
|
7,15
|
40,7
|
42,40
|
|
Коллаген
|
0,03
|
0,22
|
0,15
|
0,89
|
5,25
|
29,94
|
30,05
|
|
NaKMЦ-декстран
|
4,0976
|
23,368
|
0,7612
|
4,3412
|
6,40
|
36,214
|
28,074
|
|
Коллаген-декстран
|
4,55
|
25,983
|
0,5134
|
2,927
|
6,30
|
35,929
|
64,839
|
Таблица 2. Значения
констант диссоциации и энергий конформационного
перехода, ионизации, электростатического взаимодействия и полной энергии Гиббса
при ионизации растворов Nа-КМЦ,
коллаген и поликомплекса на их основе раствором 0,01 н
КОН)
|
Образец
|
DрКконф
|
-DGконф.,
кДж/моль
|
DрКэл., кДж/моль
|
-DGэл.,
кДж/моль
|
рК
0
|
-DG0,
кДж/моль
|
-DGпол.,
кДж/моль
|
|
NaКМЦ
|
0,1
|
0,57
|
0,27
|
1,50
|
7,65
|
43,62
|
51,84
|
|
Коллаген
|
0,03
|
0,48
|
0,14
|
0,82
|
5,9
|
33,64
|
34,74
|
|
NaKMЦ-декстран
|
0,07544
|
0,4300
|
0,6798
|
3,8769
|
6,35
|
36,214
|
40,521
|
|
Коллаген-декстран
|
2,56
|
14,599
|
0,61
|
3,478
|
6,20
|
35,359
|
53,436
|
Характеризирующим важным параметром
полимер-полимер реакции является степень превращения в реакции θ,
которая
представляет собой долю образовавшихся межмолекулярных солевых связей от их
максимально возможного числа. Расчет θ
производили из данных потенциометрического титрования по методике, описанной в
работах [48].
Результаты
потенциометрического титрования смесей Nа-КМЦ/декстран,
коллаген/декстран позволяют определить количеству ионных связей в системе
полимер-полимер по количеству выделившихся при диссоциации ионов, в зависимости
от рН раствора. Установлено, что каждому значению рН соответствует определенное
равновесное значение степени превращения θ:
q = Ск /Со
где Ск - концентрация звеньев ПЭ,
образовавших друг с другом солевые связи, Со - начальная концентрация
звеньев одного из ПЭ:
Ск = qСо= 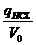 +[OH-]-[OH-]по
+[OH-]-[OH-]по
где qHCl
-
количество (г.экв.) введенной во время титрования кислоты;
Vo-объем
реакционной смеси, л; [ОН-]-исходная концентрация гидроксилионов в
растворе; [ОН-]По-концентрация гидроксильных ионов,
создаваемая непрореагировавшим основанием.
Зависимость
рН среды от степени
превращения q показывает, что интерполимерное комплексо
образование Nа-КМЦ и коллагена с
декстраном протекает в узких интервалах изменения рН растворов. Отсюда следует,
что образование интерполимерных комплексов обусловлено кооперативностью
взаимодействия в изученных системах, которые одновременно включают гидрофобные
взаимодействия [49].
.2 Термодинамических
взаимодействие в системах сополимер-ион металла и NаКМЦ-ион
металла-сополимер
Исследование сополимер-металлические комплексов
содержащих два противоположно заряженных полиэлектролита и ионы металла, новое
направление полимерной химии объединяющее положения, развитые в координационной
химии и химии макромолекулярных реакций. Исследование сополимер-металлических
систем представляет интерес прежде всего для ионов переходных металлов и
высокоэффективных полимерных катализаторов, окислительно-восстановительных
процессов [50-51].
Очевидно, что только использование широкого
круга полимерных лигандов, различающихся по своей комплексообразующей
способности, может позволить выявить роль различных взаимодействий в реакциях
образования сополимер-металлических комплексов, а также глубже понять строение
и свойства этих новых полимер-металл- сополимерных систем. Многочисленные
исследования процессов комплексообразования ионов металлов с макромолекулярными
лигандами показали, что природа лиганда влияет как на процесс формирования
металлокомплексов, так и на их свойства. Так, например, тройные
сополимер-металлические комплексы обладают новыми, существенно отличными от
исходных компонентов физико-химическими свойствами. Реакции
комплексообразования на модельных системах макромолекула-ион металла позволяют
выснить специфические особенности действия металлоэнзимов, биокатализаторов,
приблизиться к проблеме создания искусственных иммуногенов.
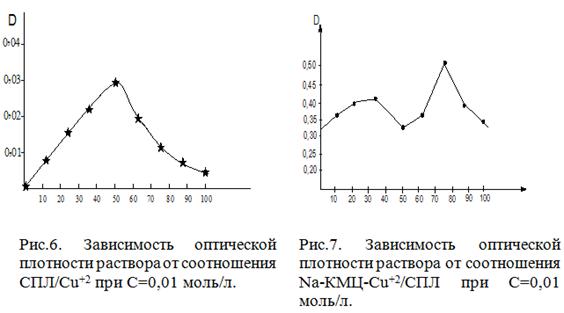
На рис.9,10 приведена зависимость оптической
плотности раствора от соотношения компонентов СПЛ-Сu+2
1,0:1,0 и Nа-КМЦ-Сu+2
/СПЛ 1,0:3,0 кривая оптической плотности проходит через максимум. И наблюдается
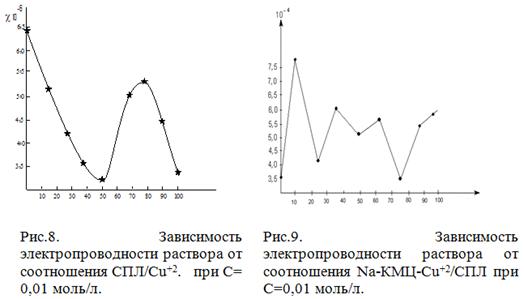
резкое уменьшение электропроводности раствора от соотношения компонентов СПЛ-Сu+2
1,0:1,0 и Nа-КМЦ-Сu+2
/СПЛ 3,0:1,0
(рис.11,12)
и наблюдается резкое уменьшение
электропроводности раствора, (рис.8,
9)
Методом потенциометрического титрования
исследовано влияние рН среды на устойчивость сополимер-металлических комплексов
эквимольного соотношения. Как видно из рис.10,
кривая титрования имеет плавный ход в интервалах рН для систем: СПЛ/Cu+2
pH от
5,0
до 5,20 и NаКМЦ-Cu+2/СПЛ
от 5,0
до
8,0; где образовавшийся сополимер-металлической
комплекс является устойчив. Этот результат указывает на увеличение области
устойчивости тройного комплекса по сравнению с сополимер-металлическим
комплексом.

Рис. 10. Кривые
потенциометрического титрования: 1.
Nа-КМЦ;
2.
ДМАЭМА×АА;
3.
ДМАЭМА×АА/Cu+2
; 4. ИПК (Nа-КМЦ-Cu+2/ДМАЭМА×АА)
(С=0,01 моль/л)
На основе кривых потенциометрического титрования
исходных компонентов и комплекса растворами 0,01 н НСI
и 0,01 н КОН рассчитаны значения рК в зависимости от степени ионизации. По
методу Зимма и Райса рассчитаны значения энергии ионизации ∆Gион,
электростатической составляющей энергии Гиббса ∆Gэл, энергии
конформационного перехода ∆Gконф и полной энергии Гиббса при
комплексообразовании.
Из таблиц.3,4 видно, что ∆Gион,
∆Gэл и ∆Gконф для системы полимер-металл-полимер
принимают большие отрицательные значения, что также является свидетельством
межмолекулярных взаимодействий и образования полимер- металлического комплекса.
Таблица 3. Значения
констант диссоциации и энергий конформационного перехода, ионизации, электростатического
взаимодействия и полной энергии Гиббса при ионизации при растворов ДМАЭМА·АА,
NаКМЦ, ДМАЭМАА/Сu+2,
Nа-КМЦ-Сu+2
/ДМАЭМА
АА и их смесей с ион металла при эквимолярном соотношении (по результатам
титрованиям 0,01 н НСI)
|
Образец
|
∆рК
конф
|
-∆Gконф
кДж/моль
|
∆
рКЭл.
|
-∆Gэл
кДж/моль
|
∆
рК 0
|
-∆G кДж/моль
|
∆Gполн.
кДж/моль
|
|
ДМАЭМА·АА
|
0,027
|
0,142
|
0,450
|
2,560
|
3,91
|
22,696
|
25,398
|
|
NаКМЦ
|
0,90
|
0,65
|
0,18
|
0,98
|
7,15
|
40,7
|
42,40
|
|
ДМАЭМА·АА/Сu+2
|
0,2268
|
1,2934
|
0,1916
|
1,0927
|
5,10
|
29,08
|
31,466
|
|
NаКМЦ-Сu+2/ ДМАЭМА·АА
|
4,176
|
23,81
|
0,688
|
3,894
|
7,20
|
41,06
|
68,76
|
Таблица
4.
Значения
констант диссоциации и энергий конформационного перехода, ионизации,
электростатического взаимодействия и полной энергии Гиббса при ионизации ДМАЭМА·АА,
NаКМЦ, ДМАЭМА·АА/Сu+2,
NаКМЦ-Сu+2/
ДМАЭМА· АА и их смесей с ион металла при эквимолярном соотношении (по
результатам титрованиям 0,01 н КОН)
|
Образец∆рК
конф-∆Gконф
кДж/моль∆ рКЭл.-∆Gэл кДж/моль∆ рК 0-∆G кДж/моль-Gполн.
кДж/моль
|
|
|
|
|
|
|
|
|
ДМАЭМА·АА
|
0,012
|
0,070
|
0,586
|
3,410
|
5,32
|
30,340
|
33,82
|
|
NаКМЦ
|
0,1
|
0,57
|
0,27
|
1,50
|
7,65
|
43,62
|
51,84
|
|
ДМАЭМА·
АА / Сu+2
|
27,38
|
157,29
|
1,0882
|
6,206
|
6,40
|
36,499
|
42,86
|
|
NаКМЦ-Сu+2 /ДМАЭМА·АА
|
3,026
|
17,25
|
0,252
|
1,437
|
6,30
|
35,929
|
54,62
|
Расчет θ производили
из данных потенциометрического титрования. Из кривых зависимости q
от рН можно также заметить (рис.11), то реакции образования
сополимер-металлических комплексов протекают в сравнительно узких интервалах
изменения рН растворов.
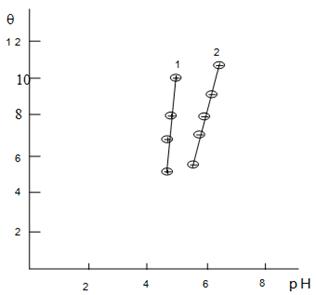
Рис.11.
Зависимость
степени общего связывания
от pH
раствора для систем:
1. ДМАЭМА· АА/ Сu+2
2.
NаКМЦ-Сu+2
/МАЭМА·
АА
Взаимодействие такого характера между ДМАЭМА·АА/Сu+2
и
NаКМЦ-Сu+2
/ДМАЭМА·АА
можно объяснить кооперативностью реакции в системе полимер-металл и
полимер-металл-сополимера. Из рисунки 11 также видно, что системе ДМАЭМА·АА/Сu+2
и
NаКМЦ-Сu+2/ДМАЭМА·АА
комплексообразования практически при определенном постоянном значении рН.
.3 Изучение полимер-металлических
взаимодействий в растворе фотометрическим методом
Наиболее широко применяются фотометрические
методы анализа, которые основаны на избирательном поглощении света
анализируемым веществом. При взаимодействии со световой энергией в атомах
поглощающего вещества происходит переход электронов на более удаленные от ядра
орбиты. Электронные переходы, вызванные поглощением строго определенных квантов
световой энергии, характеризуются наличием строго определенных полос поглощения
в электронных спектрах поглощающих атомов или молекул. Причем поглощение света
происходит только в том случае, когда энергия поглощаемого кванта совпадает с
разностью энергий между квантованными энергетическими уровнями в конечном и
начальном состояниях поглощающего атома [ 52].
Нами были исследованы равновесия в водных
растворах полимер- металлических комплексов в системе ДМАЭМА· АА/Сu+2
и
NаКМЦ-Сu+2
/
ДМАЭМА· АА фотометрическом методом. Записаны спектры поглощения для
изученных систем, определены длины волн максимального поглощения растворов. Из
зависимости светопоглощения растворов комплексов от концентрации
полиэлектролитов получена информация об устойчивости комплексов в водных
растворах. Из зависимости светопоглощения растворов комплексов от концентрации
полиэлектролитов получена информация об устойчивости образующихся в водных
средах комплексов, рассчитанные методам Фостера.
Константы устойчивости комплексов рассчитаны
методом Фостера [53].
Таблица 5
|
№
|
Система
|
Состав
|
Цвет
|
Λмах
|
Ig
Куст по Фостеру
|
|
1.
|
ДМАЭМА
×АА/ Сu+2
|
1:1
|
зеленый
|
490
|
0,34
|
|
2.
|
NаКМЦ/Сu+2 ДМАЭМА АА
|
1:3
|
Светло-зеленый
|
0,87
|
Как видно из экспериментальных данных (табл.5),
значения констант устойчивости образующихся в водных средах комплексов,
рассчитанные методами Фостера, находятся в удовлетворительном согласии и имеют
соответствующие значения.
Таким образом, проведенные исследования
комплексообразования в системе ДМАЭМА· АА/Сu+2
и
NаКМЦ-Сu+2/
ДМАЭМА· АА в растворе показали, что в растворах в исследуемых пределах
концентрации образуются полимер-металлические комплексы.
.4 ИК-спектроскопическое изучение
интерполимерных
комплексов
Для установления строения разработанных нами
соединений полимерной формы, содержащих в своём составе функциональные группы
различной природы и для определения центров связывания в интерполимерных
соединениях записаны ИК-спектры исходных веществ и конечных продуктов реакций.
В ИК-спектре Na-КМЦ
в среднечастотной области при 1615 см-1 наблюдается интенсивная
полоса поглощения, отнесенная к антисимметричным валентным колебаниям С=О связи
карбоксильного иона.
Симметричные валентные колебания этой группы
проявляются при 1310 см-1 в виде широкой полосы со средней
интенсивностью. Валентные колебания С-О-С проявляются при 1064-1137 см-1,
полоса средней интенсивности при 1427 см-1 (табл. 6) согласно [54]
отнесена к характеристическим колебаниям СН2-С-О группы. В
длинноволновой области спектра при 3432 - 3544 см-1 наблюдается
интенсивная полоса ответственная за валентные колебания гидроксильной группы.
Валентные колебания метиленовых групп (С-Н) цикла наблюдаются в виде группы
полос с центрами при 2750, 2852, 2922 см-1 . Деформационные
колебания этих групп проявляются в низкочастотной области при 699-913 см-1
также в виде группы полос со средней интенсивностью.
В ИК- спектре декстрана валетные колебания метиленовых
групп (С-Н) цикла наблюдаются в виде группы полос с центрами при 2720, 2832,
2920 см -1.Деффмационные колебания тэтих групп проявляются в
низкочасстатной области при 690-910 см -1 также в виде группы полос
со средней интенсивностью.
В ИК-спектрах коллаген наблюдаются интенсивные
полосы поглощения в области 3410-3544 см-1 ответственные за
валентные колебания NH2
группы (табл.6). Деформационные колебания d NH2
зафиксированы при 1539-1559 см-1 в виде малоинтенсивной полосы. В
среднечастотной области при 1752-1620 см-1 проявляются интенсивные
полосы, отнесенные согласно [55]
к характеристичным антисимметричным валентным колебаниям С=О связи - СООН
группы. Колебания ОН связи карбоксильной группы наблюдаются в области при
1312-1384 см-1.
Полосы поглощения средней интенсивности при
1619-1600 и 1234-1199 см-1 также согласно [55]
отнесены к антисимметричным и симметричным валентным колебаниям связи C-N
для всех трех соединений соответственно. Группа полос в высокочастотной области
в пределах 2600-2950 см-1 отнесена к валентным, а полосы
распложенные в низкочастотной области спектров соединений при 600-900 см-1
к деформационным колебаниям С-Н связи.
С целью определение центров координации в
интерполимерных комплексах записаны ИК-спектры разработанных ИПК. Сопоставление
ИК спектре комплекса Na-КМЦ/
декстрана с ИК спектрами исходных соединений показало, что в общем,
значительным изменениям подвергается положение полос поглощения СОО-
группы Na-КМЦ
смещаясь в высокочастотную область от 1615см-1 до 1630 см-1 .
Дале также изменениям подвергаются положения полос поглощения ответственные за
симметричные и антисимметричные валентные колебания функциональных групп С-Н на
2-3 см -1 .Другие колебания функциональных групп Na-КМЦ
и декстран значительным изменениям не подвергается. В комплексе Na-КМЦ
/декстран существует межмолекулярная водородная связь, возникающая между
функциональными группами Na-КМЦ
/декстран об этом свидетельствует появление новых полос ИК- спектре комплекса в
области длинных волн при 2670- 3004 см -1 [54]. Ик-
спектра комплекса [коллаген\декстран] отличается от ИК- спектра исходных
соединений. Симметричные и асимметричные колебания NH2
- группы коллагена проявляются для n
as
(NH2)
при 3471 n
as
(NH2)
при 3425 см-1,
соответственно. Деформационные колебания d(NН2)
этой группы зафиксированы при 1550см-1 со смещением в область коротких волн по
сравнению с их положением в ИК- спектре свободного коллагена. И ИК- спектре
комплекса положение полос других функциональных групп значительным изменениям
не подвергаются (табл-6) О существовании межмолекулярных водородных связей
между функциональными группами коллаген и декстрана свидетельствует появление
полос, отсутствующих и ИК- спектре исходных веществ при 2545, 2640, 3110см -1[55].
Таблица 6. Отнесения
полос поглошения в ИК-спектрах соединение (см-1)
|
Соедин.
|
nS(C=О)
|
nAS=(С=О)
|
nS(NН2)
|
nAS(NН2)
|
d(NН2)
|
n(СН)d(СН)
|
n(ОН)(СООН)
|
n(С-N)
|
n (C-O-C)
|
n(CH2CO)
|
|
NaКМЦ
|
1310
|
1615
|
-
|
-
|
-
|
2750 2652
2922 699 728 849 913
|
nS =3432 nAS
=3544
|
-
|
1064
1097
|
1427
|
|
Декстран
|
-
|
-
|
-
|
-
|
-
|
2720 2832
2920
690
720
840, 910
|
nS=3417
|
-
|
-
|
|
|
Коллаген
|
1620
|
1637
|
3416
|
3464
|
1559
|
2854
2925 617 877
|
3464
|
1134
1199
|
-
|
1454
|
|
NаКМЦ/Декстран
|
|
1630
|
|
|
|
3004 2670
616
|
3434
|
|
|
-
|
|
Коллаген/декстран
|
|
-
|
3472
|
3429
|
1555
|
2858 2929
618
890
|
-
|
-
|
-
|
-
|
3.5 ИК-спектроскопическое изучение
двух и трехкомпонентных соединений на полимерной основе
В настоящее время инфракрасная спектроскопия
стала одним из основных физических методов исследования в химии, с помощью
которого можно решать задачи качественного и количественного анализа вещества и
судить о строении молекул.
В ИК-спектре СПЛ (ДМАЭМА-АА)
в области средних частот зафиксированы полосы с центрами при 1728 см-1 соответственно,
отнесенные к антисимметричным валентным колебаниям С=О связи. Симметричные
колебания этой связи в области 1220-1390 см-1 идентифицировать не
удалось, из-за накладывания в этой области полос СН2-С-О группы. В
высокочастотной области при 3967-3429 см-1 наблюдаются полосы с
высокой интенсивностью, отнесенные согласно [54]
к валентным колебаниям NH2
группы. dNH2
наблюдается
для СПЛ (ДМАЭМА-АА)-1555 см-1.
Валентные колебания С-N
связи зафиксированы при 1640 и 1632 см-1 СПЛ (ДМАЭМА-АА)
соответственно. В области коротких волн при 1148 и 1154 см-1наблюдаются
полосы поглощения сложноэфирной группы (С-О-С). В длинноволновой области при
2853, 2923, 2854 и 2925 см-1 проявляются полосы, отнесенные к
валентным колебаниям СН групп.
В ИК-спектре Na-КМЦ
в среднечастотной области при 1615 см-1 наблюдается интенсивная
полоса поглощения, отнесенная к антисимметричным валентным колебаниям С=О связи
карбоксильного иона.
Симметричные валентные колебания этой группы
проявляются при 1310 см-1 в виде широкой полосы со средней
интенсивностью. Валентные колебания С-О-С проявляются при 1064-1137 см-1,
полоса средней интенсивности при 1427 см-1 (табл.7) согласно [55]
отнесена к характеристическим колебаниям СН2-С-О группы. В
длинноволновой области спектра при 3432 - 3544 см-1 наблюдается
интенсивная полоса ответственная за валентные колебания гидроксильной группы.
Валентные колебания метиленовых групп (С-Н) цикла наблюдаются в виде группы
полос с центрами при 2750, 2852, 2922 см-1 . Деформационные
колебания этих групп проявляются в низкочастотной области при 699-913 см-1
также в виде группы полос со средней интенсивностью.
Строение двухкомпонентного комплекса [СПЛ/CuCl2]
устанавливали при помощи ИК-спектроскопии. В ИК-спектре соединения в области
длинных волн при 3410 см-1 зафиксирована полоса поглощения NH2
группы. Характеристичные колебания связи С=О связи зафиксированы при 1696, 1732
см-1 (табл.7).
Полосы поглощения C-N
связи претерпевают изменения, проявляясь при 1650 см-1, смещаясь в
область длинных волн по сравнению с их положением в ИК-спектре свободного
[СПЛ].
Таблица 7. Отнесения
полос поглощения в ИК-спектрах соединение (см-1)
|
Соедин.
|
nCu-N
|
n Cu-O
|
nC=O
|
nCOO-
|
n C-N
|
nNH2
|
nCu-Cl
|
nOH
|
nC-C
|
nas=(С=О)
|
δ=NH2
|
|
NaКМЦ
|
-
|
-
|
-
|
1615
|
-
|
-
|
-
|
3432 3544
n
|
2750 2852
2922
|
-
|
-
|
|
СПЛ
|
-
|
-
|
1728 1732 n
|
1148 1154
|
1632
|
3417
|
-
|
3544
|
-
|
1728
|
1555
|
|
[СПЛ:CuCl2]
|
557
|
-
|
1732 1696
|
1615
|
1650
|
3410
|
664
|
3649 3740
|
2342 2850
2916
|
-
|
-
|
|
[NаКМЦ-СuCl2/СПЛ]
|
415
|
501
|
1732 n
|
1615
|
1676
|
3410
|
664
|
3753
|
2352 2922
|
-
|
-
|
Эти изменения свидетельствуют о возможной
координации электронной пары атома азота NH2
группы СПЛ. В области при 664 см-1 проявляется новая отсутствующая в
ИК спектре СПЛ полоса, отнесенная согласно [54], к колебанием связи Cu-Cl.
При
557 см-1 также проявляется новая полоса, отсутствующая в ИК-спектре
СПЛ, отнесенная согласно [54,55] к валентным колебаниям связи Cu-N.
Эти
результаты свидетельствуют об образовании донорно- акцепторной связи между
неподеленной электронной парой атома азота атомом меди (II).
Сопоставление ИК-спектров свободных компонентов
и комплекса на их основе показало, что значительным изменениям подвергается
положение полос поглощения валентных колебаний связи C-N,
которое проявляется в ИК-спектре комплекса при 1676 см-1. Также
претерпевает смещение полоса поглощения ответственная за колебания NH2
группы проявившаяся в области длинных волн при 3410 см-1 (табл.7).
Деформационные колебания этой группы так же претерпевают изменения со смещением
~10 см-1 в высокочастотную область спектра. Это свидетельствуют о
том, что комплексообразование происходит через аминогруппу. Появление новой
полосы поглощения при 415 см-1 в ИК-спектре комплекса отнесенная к
валентным колебаниям связи N-Cu
так же свидетельствует о происходящей координации через NH2
группу СПЛ. В ИК-спектре комплекса в отличие от ИК-спектра NaКМЦ
в области коротких волн появляется так же новая полоса при 501см-1
отнесенная согласно [55] к колебаниям Cu-O
связи. В ИК-спектре комплекса в области средних волн при 1376-1381 см-1проявляется
полоса поглощения связи при Cu-Cl.
Валентные колебания сложноэфирной группы С-О-С, связей С-О-Н, С-Н, С-С, С=О
зафиксированы при 1050-1096; 1305; 1416; 2352; 2922; 16154 1732; 1772 и 1767 см-1,
соответственно.
По результатам ИК-спектроскопического изучения
строения комплекса [NaКМЦ-Cu2+/СПЛ]
можно сделать вывод, что координация при комплексообразовании к иону металла
осуществляется через атомы NH2
и СОО- групп компонентов, при этом образуется смешаннополилигандный
четырех координационный комплекс, где компоненты монодентатно связаны с
комплексообразователям; третье и четвертое места в координационной сфере
занимают атомы хлора.
Выводы
. Показано образование полимер-полимерного и
сополимер- металлического комплекса в системе Nа-КМЦ/декстран
коллаген/декстран ДМАЭМА×АА-Сu+2,
Nа-КМЦ-Сu+2/ДМАЭМА×АА
методами потенциометрического титрования, оптической плотности,
вискозометрического титрования.
. Установлено, что полимер-полимер,
сополимер-металлический комплекс устойчив в интервалах Nа-КМЦ/декстран
рН от 3,2 до 8,3, коллаген/декстран 4,2 до 6,7, ДМАЭМА×АА
/Сu+2 рН
от 5,0 до 5,20 и Nа-КМЦ- Сu+
2/ДМАЭМА×АА
устойчив в интервалах рН от 5,0 до 8,0 .
. Определены зависимости константы диссоциации
от степени ионизации, рассчитаны значения энергии ионизации ∆Gион, электростатической
составляющей энергии Гиббса ∆Gэл, конформационного перехода ∆Gконф
для исходных полимеров и комплексов при титровании кислотой и щелочью.
. Установлен механизм по типу кооперативного
взаимодействия в системе Nа-КМЦ/декстран,
коллаген/декстран и ДМАЭМА×АА/Сu+2
и
Nа-КМЦ- Сu+2/ДМАЭМА×АА.
Изменение рН в узком интервале свидетельствуют об образовании кооперативной
системы связей, включающей гидробофные взаимодействия.
. Фотометрическим методом изучено
комплексообразование ионов металла с полимерами в растворах. Определены составы
и рассчитаны константы устойчивости изученных сополимер-металлических
комплексов.
Литература
1. Холмуминов
А,А., Нургалиева Ф.Ф., Куринских Л.В., Тиллаев Р.С. Свойства растворов смесей
фиброина с Nа-КМЦ// Узб. хим.
журн. 1996.-№3.-С.49-52.
2. Карапетян
Ю.А., Эйчис В.Н. Физикохимиические свойства электролиты неводны растворов. м.:
Химия, 1989.-С.64-68.
3. Нургалиева.
Ф.Ф., Холмуминов. А.А., Кучкарова. О.Р., Тиллаев Р.С. О свойствах растворов
смесей серицина с Nа-КМЦ// Узб.
хим. журн. 1995.- №5-6.-С.59-62.
4. Каримова
Ю.А., Эйчис В.Н. Физико-химические свойства электролитных неводных растворов.
М. Химия, 1989.С.64-68.
5. Зокирова
Н.Т, Курбанова М.Х., Акбаров Х.И.,
Тиллаев Р.С. Макромолекулярные
взаимодействия
в разбавленных растворах натрийкарбоксиметилцеллюлоза и альбумина
//"Аналитик Киме ва экологиянинг долзарб муаммолари илмий амалий
конф." Самарканд, 2006.-С.
232-233.
6. Зокирова
Н.Т, Курбанова М.Х., Акбаров Х.И.,
Тиллаев Р.С. Термодинамика межмакромолекулярных
взаимодействия в системе натрийкарбоксиметилцеллюлоза-коллаген //"Аналитик
кимё
ва экологиянинг долзарб муаммолари илмий амалий конф." Самарканд, 2006.-С.
234.
7. Зокирова
Н.Т., Тиллаев Р.С., Акбаров Х.И., Умаров Б.У. Термодинамика комплементарного
молекулярного взаимодействия натрийкарбоксиметилцеллюлозы с природными и
синтетическими полиэлектролитами // Тез. Докл. Конф. Современные проблемы науки
о полимерах. Санкт-Петербург. 2005. -С.23.
8. Акбаров
Х.И., Тиллаев Р.С., Умаров Б.У., Зокирова Н.Т. Взаимодействие
натрийкарбоксиметилцеллюлозы с протеинами // "Ўзбекистонда
кимё таълими, фани ва технологияси"
Респ. Илмий- амалий конф. Ташкент. 2002.-С.
69.
9. Тиллаев
Р.С., Акбаров Х.И., Зокирова Н.Т. Термодинамика комплементарного взаимодействия
натрийкарбоксиметилцеллюлозы с сополимером (гидрохлорид N,N-диметиламиноэтилметакрилат-акриламид)
// Вестник ГулГУ. 2003. -№4. -С.88-92.
10. Зокирова
Н.Т., Тиллаев Р.С., Акбаров Х.И., Курбанова М.Х. Термодинамика взаимодействия в
системе натрийкарбоксиметилцеллюлоза-альбумин //Композиционные
материалы.
2005. №3. -С.19-21.
11. Зокирова
Н.Т. Термодинамика взаимодействия натрийкарбоксиметилцеллюлоза с альбумином //Хоразм
Маъмун академиясининг 1000 йиллигига бағишланган ёш олимлар халқаро
илмий конф. Тезислар тўплами. Хива 2006.-С.
127-128.
12. Зокирова
Н.Т, Курбанова М.Х., Акбаров Х.И.,
Тиллаев Р.С. Макромолекулярные
взаимодействия
в разбавленных растворах натрийкарбоксиметилцеллюлоза и альбумина
//"Аналитик Киме ва экологиянинг долзарб муаммолари илмий амалий
конф." Самарканд, 2006.-С.
232-233.
13. Тиллаев Р.С.,
Акбаров Х.И., Зокирова Н.Т,
Курбанова М.Х. Термодинамика взаимодействия
натрийкарбоксиметилцеллюлоза с альбумином //Респ. науч.
технич.
конф.
Ташкент. 2005.-С. 76-77.
14. Будтов
Т.В. Перераспределение концентрации низкомолекулярных солей металлов в
присутствии сильно набухающих полиэлектролитных гидрогелей// Высокомолек.
Соедин. 1992.А.-№5.-С.830.
15. Кованов
В.В. и Сычеников И.А. Комплексообразование коллагена с гепарином.
Коллагенопластика в медицине. М: "Медицина" 1978.С. 71-75.
16. Леменев
В.Л, Хилькин А.М, Шехтер А.Б, Сычеников И.А, Кальмансон Е.А, А.Ф. Дронов,
Аракчеев Д.Т Изучение антикогулентных свойств коллагне- гепаринового комплекса.
Коллаген и его применение в медицине. М: "Медицина" 1976.С.278-287.
17. Шехтер
А.Б, Хилькин А.М, Дронов А.Ф, П.П. Соколов, Изучение анаффилактогенных свойств
продуктов полного растворения коллагена.
"Коллаген и его применение в медицине" . -М.: Медицина,
1976.С.271-277
18. Шехтер
А.Б, Хилькин А.М, Дронов А.Ф,П.П. Соколов, Изучение анаффилактогенных свойств
продуктов полного растворения коллагена.
"Коллаген и его применение в медицине" . -М.: Медицина,
1976.С.271-277
19. Шехтер
А.Б, Хилькин А.М, Дронов А.Ф,П.П. Соколов, Изучение анаффилактогенных свойств
продуктов полного растворения коллагена.
"Коллаген и его применение в медицине" . -М.: Медицина,
1976.С.271-277
20. Зокирова
Н.Т., Тиллаев Р.С., Акбаров Х.И., Курбанова Х.И.. Термодинамика взаимодействия
в системе натрийкарбоксиметилцеллюлоза-коллаген //Композиционные
материалы.
2005. №2. -С.8-10.
21. Акбаров
Х.И. Тиллаев Р.С, Умаров Б.С, Зокирова Н.Т, Взаимодействия
натрийкарбоксиметилцеллюлозы с протеинами //Тез. Докл.конф в УзРФА 2002.С.68-69.
22. Akbarov.Kh.I,
Tillaev R.S., Umarov B.U., Zokirova N.T. Thermodynamics of Intermolecular
interaction of Sodium carboxymethylcellulose with Proteins and Copolumers//
Sceientific materials- 2003.-P.81-82.
23. Tillaev
R.S., Akbarov Kh.I., Umarov B.U., Zokirova N.T. Thermodynamics of complementari
molecular interaction sodium carboxymethylcellulose with natural and
synthetically polyelectrolytes // Bildiri ozetleri. XVIII. Ulusal Kimya
Kongresi, Kars. 2004. -S.1205.
24. Зокирова
Н.Т., Тиллаев Р.С., Акбаров Х.И., Умаров Б.У. Термодинамика комплементарного
молекулярного взаимодействия натрийкарбоксиметилцеллюлозы с природными и
синтетическими полиэлектролитами // Тез. Докл. Конф. Современные проблемы науки
о полимерах. Санкт-Петербург. 2005. -23.С.
25. Филиппов
С.К., Комолов А.С и другие Агрегация декстрана, гидрофобно модифицированного
пространственно- затрудненными фенолами//Высокомолекулярные соединения, Серия.
А 2009 том 51.№2. 209-217.С.
26. Stimuli-
Responsive Water Soluble ahd Amphiphilic Polymers/ Ed/by Charles L/
MeCormick.New York:Am.Chem.Soc., 2001.
27. Akiyoshi K. Deguchi S.,Moriguchi
N. Yavagichi S.// Macromolecules. 1993. V.26.№12
. Akiyoshi K. Deguchi
S.,Nishikawa T. SunamonoJ// Macromolecules. 1997.
V.30.№4.Р.857.
. Akiyoshi K.
SunamonoJ// Supramolec. Sci. 1996. V.3.№ 1-3.157.
. Волков
Е.В. Филиппова О.Е. Смирнов В.А и другие //Сб.докл. Х Всерос. Конф. Структура и
динамика молекулярных систем" Яльчик, Россия. 2003. С.234.
. Esquenet
C/ Buhler E// Macromolecules.2001. V.34.№15.Р.5287.
. Esquenet
C Terech P. Boue F. Buhler . E.// Langmuir. 2004. V. 20№.9.
Р.
3583.
. Nichifor
M ., Stanciua M.C Zhu X.X.// React. Functional Polymers. 2004. V. 108. №
2. Р.
2329.
. Nichifor
M .Lopes S. Bastos M. //Phys.Chem. B. 2001. V. 108 № 42. Р.
2314.
. Nichifor
M .Lopes S. Bastos M. //Macromolecules. 1999.
V.32. № 21 Р.7078.
. Молчанов
И.В., Гольдина ОА., Горбачевский Ю.В. Растворы гидроксиэтилированного крахмала
- современные и эффективные плазмозамещающие средства инфузионной терапии:
Монографический обзор. - М., 1998.Haisch
G. et
al. // Вестник службы
крови России. - 2003. -- № 3. - С. 27 - 33.
. Baron J. F. //
Transition Medicine, -- 2000. - Vol. 2, № 2. - P. 13 - 21.V.
. Буланов
А.Ю.. и др. // Новые лекарства. - 2003, -- № 9 - 10. - С. 27.
. Буланов
А.Ю. и др. // Аестезиология и реаниматология. - 2004. № 2. - С. 25 - 30.
. Neff
T A.
et al.
// Вестник сужбы крови России. - 2 2003. -- № 4. - С.
41. Bepperling F. et al. //
Crit. Care Med. - 1999. - Vol. 3, Suppl. 1. - P. 76.
. Хван
А.М, Маджидова В.Е, Тураев А.С, Ионное сшивание карбоксиметилцеллюлозы// Химия
природ.соедин. 2005.-№2.-71.С.
43. Будтова
Т.В. Перераспределение концентрации низкомолекулярных солей металлов в
присутствии сильно набухающих полиэлектролитных гидрогелей // Высокомолк.соед.
1992. Т.А.-№5.-830.С
44. Зезин
А.Б., Кабанов Н.М., Кокорин А.И. Тройные полимер - металлические комплексы на
основе полиакриловой кислоты, линейного полиэтиленимина и меди //
Высокомолек.соедин. 1977.-№1.Т А 19. -118 С
. Бектенова
Г.А., Чинибаева Н.С., Бектуров Е.А. Каталазная активность тройных полимер -
металлических комплексов // Актуальные проблемы химии и физики полимеров.
Сборник тезисов и докладов. Ташкент. 2006.-166.С.
. Зокирова
Н.Т., Акбаров Х.И., Тиллаев Р.С Взаимодействие геля интерполимерного комплекса
на основе Nа-КМЦ с ионами
металлов. Международная конференция. Актуальные проблемы химии и физики
полимеров. Аккад.наук. Рес. Узбекстан. 2006. 162-163.С.
. ОсербаеваА.К.,
ЗакироваН.Т., АкбаровХ.И., Тиллаев Р.С Термодинамическое исследования в системқ
коллаген/декстран в разбавленнқх растворах Академик А.Ғ. Ғаниевнинг
80 йиллигига бағишланган "Аналитик кимё фанининг долзарб
муаммолари" Термиз 2010 . 53,54.С.
. Маматкулова Н.Ш.,
ОсербаеваА.К.,Абдуллаева Г.А., ЗакироваН.Т., АкбаровХ.И., Тиллаев Р.С Изучение
комплексообразования полимер-металлических комплексов потенциометрического
титрования Нефт ва газ саноати кимёвий технологияларининг долзарб муаммолари
Карши 2009. 185.С.
. Закирова
Н.Т., ОсербаеваА.К.,Абдуллаева
Г.А., АкбаровХ.И., Тиллаев Р.С Физико-химические исследования полимер-
металлических комплексов " Кимёнинг долзарб муаммолари" республика
илмий- амалий конференцияси Самарқанд 2009. 19,20.С.
. Накописи
К. ИК-спектры и строение органических соединений: перев.с англ / -М.: Мир.
1965.-8-34 С.
. Миронов
В.А., Янковский С.А. Спектроскопии в органической химии / М.: Мир. 1985. -229
С.
. Козицина
Л.А., Куплетская Н.Б. Применение УФ-, ИК- и ЯМР спектроскопии в органической
химии / -М.:Высшая школа. 1971.-С.214-234.С.
. Беллами
Л. Новые данные по ИК-спектрам сложных молекул / М.: Мир. 1971.-318 С.
. Больбит
Н.М., Тарабан В.Б., Дуфлот В.Р. Спектроскопическое изучение процессов
гелеобразования в водных растворах полиэлектролитов в присутствии соли хрома
//Высокомолек.соедин. 2004. Т. А 46. -№5.- .857-866.
С.
. Булатов
М.И., Калинкин И.П. Практическое руководство по фотометрическим и
спектрофотометрическим методам анализа/-Л.: Химия. 1968.-364 С.